journal - Tumorzentrum Erfurt eV
journal - Tumorzentrum Erfurt eV
journal - Tumorzentrum Erfurt eV
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
ISSN 1868-291X<br />
JOURNAL<br />
TUMORZENTRUM ERFURT<br />
Darmkrebs 2000 – 2010 bei Patienten<br />
der Stadt <strong>Erfurt</strong> und des Kreises Gotha<br />
Die klinische Tumordokumentation ist ein wesentliches Element der Qualitätssicherung<br />
in der Onkologie und eine der Hauptaufgaben eines <strong>Tumorzentrum</strong>s.<br />
Das Klinische Krebsregister des <strong>Erfurt</strong>er <strong>Tumorzentrum</strong>s ist für die Region<br />
Mittel- und Westthüringen zuständig. Im Mai 1993 begann die Dokumentation<br />
zunächst für einige Kliniken der beiden <strong>Erfurt</strong>er Krankenhäuser. Inzwischen<br />
beteiligen sich alle Krankenhäuser und eine immer größer werdende<br />
Zahl von niedergelassenen Ärzten sowie alle onkologischen Rehabilitationskliniken<br />
des Einzugsgebietes an der Krebsregistrierung.<br />
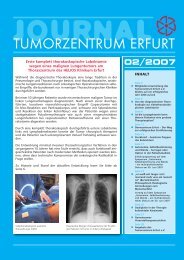
Die Zahl der neu dokumentierten Erkrankungen aller Entitäten konnte Jahr<br />
für Jahr gesteigert werden (siehe Abb.).<br />
Lesen Sie weiter auf Seite 23<br />
Abb. Jährlich neu<br />
erfasste Patienten<br />
und Tumoren aller<br />
Entitäten im KlinischenKrebsregister<br />
des <strong>Tumorzentrum</strong>s<br />
<strong>Erfurt</strong><br />
Derzeit sind mehr als 100.000 Krankheitsverläufe im <strong>Erfurt</strong>er Krebsregister<br />
gespeichert (siehe Tabelle Seite 23).<br />
Die Daten stehen den Ärzten im Rahmen ihres Behandlungsverhältnisses<br />
zur Verfügung und sind eine wertvolle Informationsquelle, wenn beispielsweise<br />
nach lange zurückliegender Primärbehandlung von den Patienten<br />
nur ungenaue anamnestische Angaben zu ihrer Erkrankung gemacht<br />
werden können oder die Beschaffung von Informationen etwa wegen<br />
einer Praxisschließung erschwert wird. Die im Einzugsgebiet bestehenden<br />
Organtumorzentren und das Onkologische Zentrum HELIOS<br />
Klinikum <strong>Erfurt</strong> nutzen das Klinische Krebsregister im Rahmen der jährlichen<br />
Qualitätsberichterstattung für die Zertifizierungen. Darüber hinaus<br />
ist das Krebsregister eine wertvolle Datenbasis für die klinische Versorgungsforschung.<br />
02/2011<br />
INHALT<br />
Seite 3<br />
■ Editorial<br />
Seite 5<br />
■ Supportive Therapie –<br />
Ausgewählte Aspekte in der<br />
Hämatologie und Onkologie<br />
Seite 6<br />
■ Prophylaxe und Therapie<br />
von thromboembolischen<br />
Komplikationen<br />
Seite 6<br />
■ Behandlung von<br />
Zytostatika-Paravasaten<br />
Seite 8<br />
■ Malignes Melanom des Rektums<br />
Seite 10<br />
■ Fallkasuistiken abdomineller<br />
Weichgewebssarkome<br />
Seite 13<br />
■ Chemotherapie-assoziierte<br />
Lebererkrankungen<br />
Seite 14<br />
■ GALLIUM-Studie erfolgreich<br />
gestartet<br />
Seite 16<br />
■ Aktuelle Diagnose-, Therapieund<br />
Nachsorgeleitlinien<br />
Seite 19<br />
■ Auditierung und Zertifizierung<br />
der ersten drei Kopf-Hals-<br />
Tumorzentren in Deutschland<br />
Seite 21<br />
■ Jahreskonferenz der Thüringischen<br />
Gesellschaft für<br />
Chirurgie in Bad Langensalza<br />
Seite 23<br />
■ Erfasste Maligne Neubildungen<br />
und deren Vorstufen im Klinischen<br />
Krebsregister des <strong>Tumorzentrum</strong><br />
<strong>Erfurt</strong><br />
Seite 24<br />
■ Darmkrebs 2000 – 2010 bei<br />
Patienten aus <strong>Erfurt</strong> und dem<br />
Kreis Gotha – Datenauswertungen<br />
des Klinischen Krebsregisters<br />
<strong>Erfurt</strong><br />
Seite 36<br />
■ Gemeinsames<br />
Veranstaltungsverzeichnis<br />
Seite 37<br />
■ Angebote des<br />
<strong>Tumorzentrum</strong> <strong>Erfurt</strong> e.V.
Prof. Dr. Albrecht Stier<br />
Vorsitzender<br />
des Vorstandes<br />
Wir wünschen allen Mitgliedern,<br />
Partnern, Freunden und Förderern<br />
des <strong>Tumorzentrum</strong> <strong>Erfurt</strong> e.V.<br />
ein gesundes neues Jahr.<br />
Wir danken Ihnen herzlich<br />
für Ihr Engagement<br />
und hoffen auf eine<br />
weitere gute Zusammenarbeit.<br />
Dr. Hubert Göbel<br />
Geschäftsführer<br />
Prof. Dr. Hartwig Kosmehl<br />
Vorsitzender<br />
des Wissenschaftlichen Beirates
■ Editorial<br />
Sehr geehrte Damen und Herren,<br />
liebe Kolleginnen und Kollegen,<br />
im Februar 2012 besteht unser <strong>Tumorzentrum</strong> <strong>Erfurt</strong> e.V. 20 Jahre.<br />
Wir werden dieses Jubiläum mit einer Festveranstaltung begehen. Aber nicht der Rückblick soll in dieser Feierstunde<br />
im Vordergrund stehen, sondern das Aufzeigen von aktuellen Perspektiven in der Onkologie.<br />
Für die Festvorträge haben wir deshalb einen Themenkreis ausgewählt, der zum einen das Spektrum der Tätigkeiten<br />
des <strong>Tumorzentrum</strong>s erkennen lässt und zum anderen das Bemühen um ständige Verbesserungen in der Tumortherapie<br />
exemplarisch beleuchtet. Wir freuen uns, dafür anerkannte Experten als Referenten gewonnen zu haben.<br />
Herr Prof. Hölzel aus München, bekannter und streitbarer Wissenschaftler auf dem Gebiet der Krebsregistrierung, wird<br />
uns die Bedeutung klinischer Krebsregister und deren enormes Potenzial für die onkologische Forschung darstellen. Die<br />
Auswertungen seiner über mehr als 30 Jahre akribisch erhobenen Daten mündeten bereits vor Jahren in der Forderung,<br />
die ausgedehnte axilläre Lymphadenektomie bei Brustkrebs aufzugeben. Weitergehende Untersuchungen stellen das<br />
gesamte bisherige Metastasierungsmodell in Frage und führen zu der Hypothese, dass nur der Primärtumor metastasieren<br />
kann. Die Auswirkungen dieses Paradigmawechsels könnten weitreichend sein.<br />
Herr Prof. Meyer aus Solingen wird sich als international renommierter onkologischer Chirurg, exzellenter Redner und<br />
ausgewiesener Experte, insbesondere der Karzinome des oberen Gastrointestinaltraktes, der Diskussion stellen. Er ist<br />
Initiator mehrerer multizentrischer Studien zur Prognosebeeinflussung der systematischen Lymphadenektomie beim<br />
Magenkarzinom, Mitglied der bundesdeutschen Leitlinienkommission zur Therapie des Magenkarzinoms und des<br />
deutschsprachigen TNM-Komitees. Dadurch hat er die Tumorklassifikation der UICC zu den Karzinomen des oberen Gastrointestinaltraktes<br />
maßgeblich mitgestaltet.<br />
Wenn es gelingt, im Rahmen unserer Festveranstaltung neue Sichtweisen zu bekannten Problemen in der Onkologie<br />
zu vermitteln und zum Nachdenken anzuregen, ist das Jubiläum unseres Erachtens richtig begangen worden.<br />
Mit freundlichen Grüßen<br />
Prof. Dr. A. Stier<br />
Vorsitzender<br />
JOURNAL 02/2011<br />
Prof. Dr. med. Albrecht Stier<br />
Vorsitzender des<br />
<strong>Tumorzentrum</strong> <strong>Erfurt</strong> e.V.<br />
■ Seite 3 ■
20 Jahre<br />
FESTVERANSTALTUNG<br />
Samstag, 03. März 2012, 10.00 Uhr<br />
Festsaal des Rathauses der Stadt <strong>Erfurt</strong> · Fischmarkt 1 · 99084 <strong>Erfurt</strong><br />
PROGRAMM<br />
Begrüßung<br />
Prof. Dr. med. Albrecht Stier<br />
Vorsitzender des <strong>Tumorzentrum</strong> <strong>Erfurt</strong> e.V.<br />
Chefarzt der Klinik für Allgemein- und Viszeralchirurgie, HELIOS Klinikum <strong>Erfurt</strong><br />
Grußansprachen<br />
Heike Taubert<br />
Ministerin für Soziales, Familie und Gesundheit des Freistaates Thüringen<br />
Dr. h. c. Fritz Pleitgen<br />
Präsident der Deutschen Krebshilfe e.V.<br />
Prof. Dr. med. Andreas Hochhaus<br />
Vorsitzender der Thüringischen Krebsgesellschaft e.V.<br />
Direktor der Abteilung Hämatologie und Internistische Onkologie der Klinik für Innere Medizin II<br />
des Universitätsklinikum Jena und Direktor des UniversitätsTumorCentrums Jena<br />
Andreas Bausewein<br />
Oberbürgermeister der Landeshauptstadt <strong>Erfurt</strong><br />
FESTVORTRÄGE<br />
Zum Metastasierungsprozess: Erleben wir einen Paradigmawechsel?<br />
Prof. Dr. hum. biol. Dieter Hölzel<br />
Stellvertretender Vorsitzender der Arbeitsgemeinschaft Deutscher Tumorzentren e.V. (ADT),<br />
Em. Leiter des Tumorregisters des <strong>Tumorzentrum</strong>s München, Institut für medizinische Informationsverarbeitung,<br />
Biometrie und Epidemiologie, Klinikum Großhadern der Ludwig-Maximilians-Universität München<br />
Die Bedeutung der Lymphadenektomie bei Karzinomen des oberen Gastrointestinaltraktes<br />
Prof. Dr. med. Dr. h. c. Hans-Joachim Meyer<br />
Past-Präsident der Deutschen Gesellschaft für Allgemein- und Viszeralchirurgie,<br />
Koordinator des European Network of Excellence for Gastric Cancer,<br />
Chefarzt der Klinik für Allgemein- und Viszeralchirurgie des Städtischen Klinikums Solingen<br />
Die Festveranstaltung wird musikalisch umrahmt vom Ärzte-Kammerorchester<br />
des <strong>Tumorzentrum</strong> <strong>Erfurt</strong> e.V.<br />
Nach der Veranstaltung sind alle Teilnehmer zu einem Empfang eingeladen.<br />
Anmeldungen werden erbeten an:<br />
<strong>Tumorzentrum</strong> <strong>Erfurt</strong> e.V. · Geschäftsstelle · HELIOS Klinikum <strong>Erfurt</strong><br />
Nordhäuser Straße 74 · 99089 <strong>Erfurt</strong><br />
Telefon: 0361 781-4802 · Telefax: 0361 781-4803 · e-Mail: tuz@tumorzentrum-erfurt.de<br />
■ Seite 4 ■ JOURNAL 01/2005 02/2011
■ Supportive Therapie –<br />
Ausgewählte Aspekte in der<br />
Hämatologie und Onkologie<br />
Zusammenfassung des Vortrags auf der 24. Onkologischen<br />
Konferenz des <strong>Tumorzentrum</strong> <strong>Erfurt</strong> e.V. am<br />
4. und 5. November 2011 in Eisenach, Tagungsschwerpunkt<br />
„Supportive Therapie“<br />
Cordelia Steinbrecher<br />
4. Medizinische Klinik, Onkologisches Zentrum,<br />
HELIOS Klinikum <strong>Erfurt</strong><br />
Ziel supportiver Therapie ist es, den Patienten vor therapiebedingten<br />
Komplikationen zu schützen, um den bestmöglichen<br />
Therapieerfolg und eine gute Lebensqualität<br />
zu erreichen.<br />
Primärprophylaxe der febrilen Neutropenie durch<br />
G-CSF<br />
Infektionen infolge chemotherapie-induzierter febriler<br />
Neutropenie sind die häufigsten therapiebedingten Todesursachen.<br />
Durch prophylaktische G-CSF-Gabe kann<br />
das Risiko für febrile Neutropenie deutlich reduziert werden.<br />
Die letzte Überarbeitung der internationalen Leitlinien<br />
zum Einsatz von G-CSF (ASCO-Guidelines 2006) trug<br />
dieser Tatsache Rechnung und führte zu einer deutlichen<br />
Indikationserweiterung zum primär prophylaktischen Einsatz<br />
von G-CSF. Folgendes Vorgehen wird empfohlen: Vor<br />
jeder Chemotherapie sollte das chemotherapie-bedingte<br />
febrile Neutropenie-Risiko (FN-Risiko) beurteilt werden.<br />
Bei einem FN-Risiko ≥ 20 % wird die primäre G-CSF-Prophylaxe<br />
empfohlen (Beispiele: R-CHOP bei NHL, FEC bei<br />
Mammakarzinom, Cisplatin/Etoposid bei NSCLC). Bei einem<br />
FN-Risiko von 10-20% (Beispiele: FOLFIRI, Docetaxel,<br />
Topotecan) sollten patienten- und krankheitsbezogene<br />
Risikofaktoren identifiziert werden, die das FN-Risiko erhöhen<br />
können (Alter > 65 Jahre, weibliches Geschlecht,<br />
Begleiterkrankungen, reduzierter AZ und EZ, fortgeschrittene<br />
Tumorerkrankung bei Erstdiagnose u. a.). Bei Vorliegen<br />
dieser Risikofaktoren wird auch in diesem Fall die primär<br />
prophylaktische Gabe von G-CSF empfohlen. Bei einem<br />
FN-Risiko < 10% (Beispiele: FOLFOX, Paclitaxel/Carboplatin,<br />
Cisplatin/Gemcitabine) ist die Primärprophylaxe<br />
mit G-CSF nicht indiziert.<br />
(Literatur: TJ Smith et al.: 2006 Update of Recommendations for the use of<br />
white blood cell growth factors: an evidence-based clinical practice guideline.<br />
JCO 24:3187-3205)<br />
Osteoprotektion bei onkologischen Patienten<br />
Onkologische Patienten sind Risikokandidaten für die Entwicklung<br />
einer frühen Osteoporose (Beispiele: ossäre Metastasen,<br />
Osteolysen beim Multiplen Myelom, Glukokortikoidtherapie<br />
als Bestandteil der Chemotherapie oder<br />
Antiemese, frühe Menopause nach intensiver Chemotherapie,<br />
antiöstrogene und antiandrogene Hormontherapie).<br />
Sie sollten über die Basismaßnahmen zur Osteoporoseprophylaxe<br />
informiert sein (Basismaßnahmen: regel-<br />
JOURNAL 02/2011<br />
mäßige körperliche Aktivität, ausreichende Ernährung,<br />
1000 mg Calcium und 1000 I.E. Vitamin D tägl., Sonnenlicht<br />
30 Min. tägl., Sturzanamnese, Vermeidung sturzfördernder<br />
Medikamente wie Sedativa). Insbesondere bei<br />
wiederholter Glukokortikoideinnahme sollte früh ein<br />
Screening auf Osteoporose durch Knochendichtemessung<br />
(DXA-Verfahren) erfolgen, um bei Indikation eine<br />
spezifische Osteoporosemedikation (Bisphosphonate, Parathormon,<br />
AK gegen RANKL) einzuleiten.<br />
(Literatur: DVO-Leitlinie 2009 unter www.dv-osteologie.org)<br />
Impfungen bei onkologischen Patienten<br />
Für onkologische Patienten unter/nach konventioneller<br />
Chemotherapie gelten die gleichen Impfempfehlungen<br />
der STIKO (Ständige Impfkommission beim Robert-Koch-<br />
Institut) wie für Gesunde. Ab einem Alter >60 Jahre ist die<br />
jährliche saisonale Influenza-Schutzimpfung und alle 4-5<br />
Jahre die Auffrisch-Impfung für Pneumokokken empfohlen.<br />
Die Impfung sollte 3-6 Monate nach der Chemotherapie<br />
erfolgen, wenn genug Zeit besteht, ist eine Impfung<br />
auch 2 Wochen vor Chemotherapiebeginn möglich. Eine<br />
Impfung mit Totimpfstoffen während einer Chemotherapie<br />
ist nicht gefährlich, jedoch oft ineffektiv, daher wird<br />
eine Impfung während laufender Chemotherapie nicht<br />
empfohlen. Lebendimpfstoffe (Masern, Mumps, Röteln,<br />
Varicella-Zoster-Virus) sind während einer Chemotherapie<br />
kontraindiziert und dürfen erst 6-12 Monate nach Therapieende<br />
verabreicht werden.<br />
Spezielle Impfempfehlungen bestehen für splenektomierte<br />
Patienten. Sie sollten gegen Pneumokkoken, Meningokokken<br />
und Hämophilus influenza geimpft sein. Patienten<br />
die im Laufe ihrer Therapie Blutprodukte erhalten, sollten<br />
gegen Hepatitis B geimpft werden.<br />
Die Anti-CD20-Antikörper Rituximab und Ofatumumab<br />
führen zu einer B-Lymphozyten-Depletion von 12 und<br />
mehr Monaten. Durch die seit 2009 bzw. 2010 bestehende<br />
Indikation zu einer 2- jährigen Rituximab-Erhaltungstherapie<br />
nach first-line und second-line Therapie beim<br />
follikulären Lymphom haben diese Patienten eine B-Zellimmunsuppression<br />
über 3-4 Jahre, in denen sie keinen effektiven<br />
Impfschutz aufbauen können. Angesichts dieser<br />
Situation wird deutlich, wie wichtig es ist, dass sich medizinisches<br />
Fachpersonal und familiäre Kontaktpersonen<br />
gegen Influenza impfen lassen. Leider liegt die Impfquote<br />
bei medizinischem Personal derzeit bei nur 20 %.<br />
(Ausführliche aktuelle Impfempfehlungen der STIKO unter:<br />
www.rki.de )<br />
Korrespondenzadresse:<br />
Dr. med. Cordelia Steinbrecher<br />
4. Medizinische Klinik<br />
Onkologisches Zentrum<br />
HELIOS Klinikum <strong>Erfurt</strong><br />
Nordhäuser Straße 74<br />
99089 <strong>Erfurt</strong><br />
Telefon: 0361 781-5297<br />
e-Mail: cordelia.steinbrecher@helios-kliniken.de<br />
■ Seite 5 ■
■ Prophylaxe und Therapie von<br />
thromboembolischen Komplikationen<br />
Zusammenfassung des Vortrags auf der 24. Onkologischen<br />
Konferenz des <strong>Tumorzentrum</strong> <strong>Erfurt</strong> e.V. am<br />
4. und 5. November 2011 in Eisenach, Tagungsschwerpunkt<br />
„Supportive Therapie“<br />
Christine Schubert<br />
4. Medizinische Klinik, Hämatologie, internistische<br />
Onkologie, Hämostaseologie,<br />
HELIOS Klinikum <strong>Erfurt</strong><br />
Empfehlungen zur Thromboembolieprophylaxe bei<br />
Tumorpatienten<br />
1. Jeder hospitalisierte Tumorpatient soll eine medikamentöse<br />
Thromboembolieprophylaxe mit unfraktioniertem<br />
Heparin oder niedermolekularem Heparin erhalten.<br />
2. Für ambulant behandelte Tumorpatienten wird eine<br />
routinemäßige Thromboembolieprophylaxe nicht empfohlen.<br />
Ausnahme: Patienten, die mit Lenalidomid oder Thalidomid<br />
behandelt werden, sowie Patienten mit Pankreaskarzinom,<br />
die eine Chemotherapie erhalten.<br />
3. Alle Patienten sollen bei einer bevorstehenden größeren<br />
Tumoroperation eine medikamentöse Thromboembolieprophylaxe<br />
erhalten.<br />
4. Niedermolekulare Heparine sind die bevorzugten Antikoagulanzien<br />
sowohl zur initialen Therapie als auch<br />
zur Langzeitprophylaxe bei Tumorpatienten mit tiefer<br />
Venenthrombose.<br />
5. Ein Einfluss von niedermolekularen Haparinen auf die<br />
Überlebensrate von Tumorpatienten ist derzeit nicht<br />
abschließend beurteilbar.<br />
Empfehlungen zur Therapie von Thromboembolien<br />
bei Tumorpatienten<br />
1. vital bedrohliche Thromboembolie: Thrombolyse,<br />
Thrombektomie, Cava-Filter<br />
2. stabile Patienten: Einsatz von niedermolekularen Heparinen<br />
oder unfraktionierten Heparinen für ca.<br />
3-6 Monate.<br />
3. bei Hochrisikopatienten längere Sekundärprophylaxe<br />
mit niedermolekularen Heparinen oder Vitamin-K-<br />
Antagonisten<br />
(nach Empfehlungen ASCO 2007, DGHO 2011)<br />
Korrespondenzadresse:<br />
Dr. med. Christine Schubert<br />
4. Medizinische Klinik<br />
Hämatologie, internistische Onkologie, Hämostaseologie<br />
HELIOS Klinikum <strong>Erfurt</strong><br />
Nordhäuser Straße 74<br />
99089 <strong>Erfurt</strong><br />
Telefon: 0361 781-72469<br />
e-Mail: christine.schubert@helios-kliniken.de<br />
■ Behandlung von<br />
Zytostatika-Paravasaten<br />
Zusammenfassung des Vortrags auf der 24. Onkologischen<br />
Konferenz des <strong>Tumorzentrum</strong> <strong>Erfurt</strong> e.V. am<br />
4. und 5. November 2011 in Eisenach, Tagungsschwerpunkt<br />
„Supportive Therapie“<br />
Ulrike Börner<br />
Apotheke, HELIOS Klinikum <strong>Erfurt</strong><br />
Zytostatika können schwere Gewebeschäden verursachen,<br />
wenn die Substanzen an der Vene vorbei ins Gewebe<br />
gelangen. Dafür gibt es zwei Ursachen. Wird die Injektion<br />
oder Infusion nicht korrekt appliziert, kommt es zu einem<br />
Paravasat. Dringt das Zytostatikum durch brüchig gewordene<br />
Venen ins Gewebe über, spricht man von einem<br />
Extravasat.<br />
Die zu ergreifenden speziellen Notfallmaßnahmen lassen<br />
sich oft aus den Pathomechanismen der jeweiligen<br />
Substanz ableiten.<br />
Die Gruppe der Anthracycline (z.B. Doxorubicin, Daunorubicin,<br />
Epirubicin) basiert auf einer Chinon-Struktur, die<br />
leicht Elektronen aufnehmen und wieder abgeben kann.<br />
Dadurch sind diese sehr reaktionsfreudig und es können<br />
toxische Radikale gebildet werden.<br />
Eine Radikalreaktion verläuft temperaturabhängig. Deshalb<br />
ist es sinnvoll, Anthracyclin-Paravasate zu kühlen, damit<br />
diese Reaktion langsamer verläuft. Eingesetzt als Radikalfänger<br />
wird das Dimethylsulfoxid (DMSO), welches<br />
als 99%ige Lösung aufgetragen wird. Es wirkt entzündungshemmend,<br />
analgetisch und antihistaminisch. Die<br />
Vorteile von DMSO liegen in einer einfachen, billigen und<br />
schnellen Handhabung. Paravasate treten oft verzögert<br />
auf, DMSO kann auch nach Ablauf von 6 Stunden noch<br />
angewendet werden.<br />
Ein weiterer Ansatzpunkt ist die Behandlung mit Dexrazoxan.<br />
Dieses Arzneimittel wirkt hier als Komplexbildner<br />
mit Eisen-Ionen (Fe 3 +). Dadurch können Radikalreaktionen<br />
und die daraus folgenden zytotoxischen Reaktionen<br />
verringert werden. Wichtig ist die Anwendung innerhalb<br />
von sechs Stunden nach Auftreten des Paravasates. Die<br />
Wirksamkeit von DMSO und Dexrazoxan ist in Studien<br />
überprüft worden [5, 4], allerdings steht eine klare Entscheidung,<br />
wann DMSO und wann Dexrazoxan angewendet<br />
wird, noch aus.<br />
Dosierung von Dexrazoxan<br />
Tag 1 1000 mg/m 2 KOF<br />
Tag 2 1000 mg/m 2 KOF<br />
Tag 3 500 mg/m 2 KOF<br />
Die Infusionsdauer beträgt 1-2 Stunden. Wichtig ist die<br />
Anwendung innerhalb von sechs Stunden. Während der<br />
Behandlung mit Dexrazoxan darf kein DMSO und keine<br />
Kälte angewendet werden.<br />
■ Seite 6 ■ JOURNAL 01/2005 02/2011
Die Vinca-Alkaloide (Vincristin, Vindesin, Vinflunin etc.)<br />
stellen eine weitere Gruppe von Zytostatika dar, die bei Paravasation<br />
zu schweren Nekrosen führen. Diese besitzen<br />
eine hohe Gewebeaffinität. Um die Substanzen aus dem<br />
Gewebe wieder zu entfernen wird Wärme eingesetzt und<br />
zusätzlich Hyaluronidase als spezifisches Antidot. Dabei<br />
handelt es sich um ein Enzym, das die Struktur von Binde-<br />
und Stützgewebe auflöst und dadurch den Flüssigkeitsaustausch<br />
zwischen Gewebe und Gefäßen erleichtert.<br />
Daraus resultiert ein beschleunigter Abtransport der<br />
Vinca-Alkaloide. Das Paravasat sollte sternförmig subcutan<br />
oder intradermal umspritzt werden. Die maximale Dosierung<br />
hierbei liegt bei 1500 I.E. Achtung! Dies ist mit<br />
starken, brennenden Schmerzen verbunden und sollte in<br />
Verbindung mit einem Lokalanästhetikum gespritzt werden.<br />
Die rekonstituierte Lösung von Hylase ® 150 ist mischbar<br />
mit Mepivacain oder Lidocain [7].<br />
Weitere Zytostatika, die bei Paravasationen schwere Nekrosen<br />
hervorrufen können, sind strukturverwandte Verbindungen<br />
der Anthracycline, wie Mitoxantron, Amsacrin<br />
und Dactinomycin. Diese Paravasate werden deshalb<br />
auch durch DMSO und Kälteanwendungen behandelt.<br />
Nicht bei allen Zytostatika sind die Pathomechanismen bei<br />
Paravasation bekannt, deshalb erfolgt die Behandlung auf<br />
Grund einzelner Fallberichte bzw. der Auswertung einzelner<br />
Paravasatebögen. So wird bei Paclitaxel-Paravasaten<br />
Hyaluronidase zur Umspritzung empfohlen. Bei Mitomycin<br />
wird dagegen mit DMSO und Kälte behandelt.<br />
Die Folgen eines Cisplatin-Paravasates kann man verringern,<br />
in dem Infusionslösungen verwendet werden, bei<br />
denen eine Konzentration von 0,5 mg/ml nicht überschritten<br />
wird. Kommt es zu einem Paravasat, wird die Anwendung<br />
von DMSO und Kälte empfohlen [1].<br />
Klagt der Patient über Schmerzen und Brennen an der Injektionsstelle,<br />
treten Schwellungen und Rötung auf,<br />
nimmt die Infusionsgeschwindigkeit ab, gibt es Widerstände<br />
bei der Injektion, ist nur noch eine geringe oder gar<br />
keine Aspiration von Blut mehr möglich, muss mit der<br />
Möglichkeit eines Paravasates gerechnet werden. Dann<br />
sind umgehend Maßnahmen einzuleiten. Begonnen wird<br />
mit den allgemeinen Maßnahmen, daran schließen sich<br />
die substanzspezifischen Maßnahmen an.<br />
Allgemeine Maßnahmen<br />
1. Injektion / Infusion sofort stoppen<br />
2. i.v.-Zugang belassen, nicht nachspülen<br />
3. Paravasat aspirieren, soviel wie möglich<br />
4. i.v.-Zugang entfernen<br />
5. betroffene Extremität hoch lagern<br />
JOURNAL 02/2011<br />
Stationen und Arztpraxen, die Zytostatika anwenden,<br />
müssen Zugang zu einem Paravasate-Notfallkoffer haben.<br />
In diesem sollte Folgendes enthalten sein:<br />
Zusammensetzung eines Paravasate-Sets<br />
1. Kälte-Wärmepackungen (10 x 26)<br />
2. Sterile Tupfer<br />
3. Einmalspritzen und Kanülen<br />
4. Sterile Handschuhe<br />
5. Dimethylsulfoxid 99% Lösung<br />
6. Hyaluronidase Amp. (insgesamt 1500 I.E.)<br />
7. Dexrazoxane (5000 mg)<br />
auf Abruf in Apotheke vorrätig<br />
8. Kurzübersicht zur Behandlung der Paravasate<br />
9. Paravasate-Dokumentationsbogen<br />
Bei der Versorgung eines Paravasates sollte beachtet werden,<br />
dass der Zugang nicht mehr gespült wird und keine<br />
Umschläge angewendet werden, die die Haut aufquellen<br />
lassen und damit bewirken, dass die Zytostatika noch tiefer<br />
in das umliegende Gewebe eindringen.<br />
Substanzspezifische Maßnahmen<br />
Die Lösung wird zu Beginn 4-6 mal täglich, dann alle<br />
8 Stunden mit einem sterilen Kugeltupfer ohne Druck aufgetragen.<br />
DMSO soll an der Luft trocknen und nicht abgedeckt<br />
werden. Die Behandlungszeit beträgt 7-14 Tage.<br />
Trockene Kälte:<br />
Zu Beginn wird mindestens eine Stunde gekühlt, dann<br />
mehrmals täglich über 15 Minuten. DMSO und Kälte werden<br />
abwechselnd angewendet.<br />
Anwendung von Hyaluronidase:<br />
Das Paravasat wird je nach Größe sternförmig s. c. umspritzt.<br />
1-10 Umspritzungen von je 150 I.E. (insgesamt<br />
maximal 1500 I.E.)<br />
Trockene Wärme:<br />
Die Wärmeanwendungen erfolgen über 4 x 20 Minuten<br />
mindestens 2 Tage lang.<br />
Die Anzahl der Paravasate kann verringert werden,<br />
wenn folgende Dinge bei der Applikation von Zytostatika<br />
beachtet werden:<br />
Es sollten entweder zentrale Zugänge oder starke Venen<br />
möglichst in Unterarmmitte punktiert werden. Zugänge<br />
an Handrücken und in der Nähe von Gelenken sind zu vermeiden,<br />
da hier die Gefahr von Gelenkzerstörungen besteht.<br />
Vor Beginn der Injektion oder Infusion ist der Sitz<br />
der Kanüle durch einen Vorlauf mit 10 ml NaCl 0,9 % bzw.<br />
einer Kurzinfusion zu überprüfen.<br />
Wichtig ist außerdem eine gute Patientenaufklärung, bei<br />
der der Patient ermutigt wird, evtl. auftretende Beschwerden<br />
und Auffälligkeiten im Infusionsverlauf mitzuteilen.<br />
■ Seite 7 ■
Es sollte immer bedacht werden, dass Paravasate mit Infusionsbeginn,<br />
verzögert und auch bei zentralen Zugängen<br />
(z.B. Ports) auftreten können.<br />
Sofortiges Handeln, Durchführung der allgemeinen und<br />
evtl. der spezifischen Maßnahmen sowie schneller Zugriff<br />
auf das Paravasate-Set können die Auswirkungen einer<br />
Paravasation verringern und eine chirurgische Intervention<br />
verhindern.<br />
„Jede Minute, die durch falsch verstandene Zurückhaltung<br />
verloren wird, kann zu bleibenden Schäden führen.“<br />
(Robert Mader)<br />
Literatur<br />
1. Mader et al.: Paravasation von Zytostatika 2006 (www.Paravasate.at)<br />
2. Maike de Wit, Petra Ortner, Hans-Peter Lipp, Jalid Sehouli, Michael<br />
Untch, Markus Ruhnke, Regine Mayer-Steinacker, Carsten Bokemeyer,<br />
Karin Jordan: Zytostatika-induzierte Paravasate – Empfehlungen zu<br />
Diagnose, Prophylaxe und Therapie, Arbeitsversion der ASORS Paravasate-Guidelines<br />
(Stand April 2010), www.onkosupport.de<br />
3. Hans-Peter Lipp: Extra- und Paravasation von Zytostatika, Medizinische<br />
Monatszeitschrift für Pharmazeuten, 33. Jahrgang, Heft 3, März 2010<br />
4. Mouridsen et al.: Treatment of anthracycline extravasation with Savene ® ,<br />
Ann Oncol 2007; 18: 546-550<br />
5. Bertelli M, Gozza A, Forno GB et al.: Tropical dimethyl sulfoxide for the<br />
prevention of soft tissue injury after extravasation of vesicant cytoxic<br />
drugs: a perspective clinical study. J Clin Oncol 1995; 13: 2851-2855<br />
6. Krämer I, Stützle M et al.: Zytostatika-Paravasation – Wie ist vorzugehen?<br />
Eine Konsensusempfehlung des Stammzellqualitätszirkels Rheinland<br />
Pfalz. Krankenhauspharmazie 2002; 23: 261-268<br />
7. Information Hylase® 05/2011, Riemser Arzneimittel AG,<br />
www.pharmazie.com<br />
Korrespondenzadresse:<br />
Ulrike Börner<br />
Krankenhausapotheke<br />
HELIOS Klinikum <strong>Erfurt</strong><br />
Nordhäuser Str. 74<br />
99089 <strong>Erfurt</strong><br />
Telefon: 0361-781 1516<br />
e-Mail: ulrike.boerner@helios-kliniken.de<br />
■ Malignes Melanom des Rektums<br />
Zusammenfassung des Vortrags auf der 24. Onkologischen<br />
Konferenz des <strong>Tumorzentrum</strong> <strong>Erfurt</strong> e.V. am<br />
4. und 5. November 2011 in Eisenach, Tagungsschwerpunkt<br />
„Der interessante Fall“<br />
Stefanie Vischer<br />
Klinik für Allgemein-, Visceral- und Gefäßchirurgie,<br />
Katholisches Krankenhaus „St. Johann Nepomuk“<br />
<strong>Erfurt</strong><br />
Cornelia Steiner<br />
Institut für bildgebende Diagnostik, Katholisches<br />
Krankenhaus „St. Johann Nepomuk“ <strong>Erfurt</strong><br />
Jörg Pertschy<br />
Klinik für Allgemein-, Visceral- und Gefäßchirurgie,<br />
Katholisches Krankenhaus „St. Johann Nepomuk“<br />
<strong>Erfurt</strong><br />
Fallbericht<br />
Es wird der Fall einer 65jährigen Frau geschildert.<br />
Die Einweisung erfolgte zur weiteren Diagnostik einer<br />
Raumforderung des unteren Rektums. Anamnestisch<br />
klagte die Patientin über rezidivierende rektale Blutabgänge.<br />
Bei der rektal/digitalen Untersuchung und in der Rektoskopie<br />
fiel ein kirschkerngroßer Tumor an der Rektumvorderwand<br />
in 2 cm Höhe bei 4 Uhr SSL auf. Zur Histologiegewinnung<br />
wurde eine Koloskopie durchgeführt, die die<br />
Raumforderung bestätigte und zusätzlich eine reizlose<br />
Sigmadivertikulose zeigte.<br />
Histologisch (Abb. 1 und 2) wurde ein malignes Melanom<br />
nachgewiesen.<br />
Abb. 1 Immunhistochemnische Untersuchung mittels HMB45<br />
In der Endosonographie (Abb. 3) stellte sich die Raumforderung<br />
als exophytisch wachsender Tumor, der an der Basis<br />
die Submukosa infiltierte mit zwei pathologisch vergrößerten<br />
Lymphknoten (uT1, N pos.) dar.<br />
■ Seite 8 ■ JOURNAL 01/2005 02/2011
Abb. 2 200fache Vergrößerung in HE-Färbung<br />
(Für die Überlassung der Bilder bedanken wir uns beim Institut für Pathologie,<br />
HELIOS Klinikum <strong>Erfurt</strong>)<br />
Eine Metastasierung wurde mittels thorakoabdomineller<br />
Computertomographie ausgeschlossen. Es bestätigte sich<br />
die tiefsitzende Raumforderung im Rektum, welche bis an<br />
den Sphinkter heran reichte. Kranial und präsakral fielen<br />
pathologisch vergrößerte Lymphknoten auf.<br />
Abb. 3 Endosonographie des Rektums<br />
Im MRT des Beckens (Abb. 4) stellte sich der Tumor als unmittelbar<br />
sphinternahe, exzentrisch das Lumen nach ventral<br />
paramedian links überschreitende, nodulär imponierende<br />
Raumforderung der Rektumwandung ohne Überschreitung<br />
der Muscularis dar. Das umgebende Fettgewebe<br />
wies keine Infiltrationszeichen auf. Wie bereits in der<br />
CT-Voruntersuchung fand sich deutlich vom primären Tumorbefund<br />
entfernt eine ovaläre Lymphknotenvergrößerung<br />
lateral links (uT1, N pos.)<br />
In der augenärztlichen Untersuchung konnten ein Melanom<br />
des Augenhintergrunds und in der dermatologischen<br />
Beurteilung ein malignes Melanom der Haut ausgeschlossen<br />
werden.<br />
Abb. 4 MRT des kleinen Beckens<br />
JOURNAL 02/2011<br />
Zum Ausschluss zerebraler Metastasen wurde ein MRT des<br />
Schädels veranlasst. Nebenbefundlich fiel hierbei ein kleines<br />
Konvexitätsmeningeom links frontal ohne lokal raumfordernde<br />
Wirkung auf.<br />
Zur Festlegung des therapeutischen Vorgehens erfolgte<br />
die Besprechung des Falls im interdisziplinären Tumorkonsil<br />
mit der Empfehlung der primären Resektion.<br />
Aufgrund der sphinkternahen Lage wurde die abdominoperineale<br />
Rektumamputation mit totaler Entfernung des<br />
Mesorektums durchgeführt (Abb. 5). Intraoperativ gab es<br />
keinen Anhalt für eine sekundäre Tumormanifestation.<br />
Abb. 5 OP-Präparat<br />
Der endgültige histologische Befund bestätigte das maligne<br />
Melanom im Anorektum mit oberflächlichen Ulzerationen.<br />
Der Tumor wies eine maximale horizontale Ausdehnung<br />
von 1,1 cm und einer maximalen Tiefenausdehnung<br />
von 0,9 cm auf. Eine eigene TNM-Klassifikation für<br />
diese Tumorentität gibt es nicht, so dass der Tumor entsprechend<br />
der der Haut pT4b pN1a (1/15) V0 L1 R0 klassifiziert<br />
wurde.<br />
Als adjuvantes Behandlungskonzept wurde entsprechend<br />
der Empfehlung des interdisziplinären Tumorkonsils eine<br />
Interferonmonotherapie für 16 Monate festgelegt.<br />
■ Seite 9 ■
Die bis jetzt durchgeführte Tumornachsorge (19 Monate)<br />
zeigt eine Rezidivfreiheit.<br />
Schlussfolgerung<br />
Das anorektale Schleimhautmelanom als Differenzialdiagnose<br />
anorektaler Tumoren ist selten. Das Anorektum<br />
ist die vierthäufigste Lokalisation neben der Haut, dem<br />
Auge und den Schleimhäuten im HNO-Bereich. Weniger<br />
als 2 % der Melanome treten im Anorektum auf. Lediglich<br />
0,5 – 2 % aller Neoplasmen dieser Region gehören dieser<br />
Entität an. Frauen erkranken häufiger als Männer (2,3:1).<br />
Das mediane Erkrankungsalter liegt bei 77 Jahren vs. 57<br />
Jahren.<br />
Der Pigmentierungsgrad ist sehr variabel. Es treten<br />
schwarz, braun, blau bis hin zu blauroten Farbtönen auf.<br />
Bis zu 30 % sind amelanotisch.<br />
Häufig sind hierbei oberflächliche Ulzerationen mit Verschorfungen.<br />
In der Hälfte der Fälle sind die Tumore sehr<br />
vulnerabel, so dass rektale Blutabgänge, wie auch in dem<br />
oben beschriebenen Fall, eines der führenden klinischen<br />
Symptome ist.<br />
Eine eigene TNM-Klassifikation für diese Tumorentität gibt<br />
es nicht. Sie wird an die der Haut angelehnt. Man unterscheidet<br />
3 Stadien:<br />
Stadium I Tumor nur lokal<br />
Stadium II lokoregionäre Metastasen<br />
Stadium III Fernmetastasen<br />
Maligne Melanome im Anorektum haben aufgrund einer<br />
frühzeitigen lymphogenen und auch hämatogenen Metastasierung<br />
eine schlechte Prognose. Die mediane Überlebenszeit<br />
beträgt zwischen 12 und 18,6 Monaten, die<br />
5 Jahres Überlebensrate liegt bei 33 %.<br />
Korrespondenzadresse:<br />
Dr. med. Stefanie Vischer<br />
Klinik für Allgemein-, Visceral- und Gefäßchirurgie<br />
Katholisches Krankenhaus „St. Johann Nepomuk“<br />
Haarbergstraße 72<br />
99097 <strong>Erfurt</strong><br />
Telefon: 0361 654-1201<br />
e-Mail: visceralchirurgie@kkh-erfurt.de<br />
■ Fallkasuistiken abdomineller<br />
Weichgewebssarkome<br />
Zusammenfassung des Vortrags auf der 24. Onkologischen<br />
Konferenz des <strong>Tumorzentrum</strong> <strong>Erfurt</strong> e.V. am<br />
4. und 5. November 2011 in Eisenach, Tagungsschwerpunkt<br />
„Der interessante Fall“<br />
Uta Wichmann<br />
Klinik für Allgemein-, Visceral- und Gefäßchirurgie,<br />
Katholisches Krankenhaus „St. Johann Nepomuk“<br />
<strong>Erfurt</strong><br />
Uta Pertschy<br />
Institut für bildgebende Diagnostik, Katholisches<br />
Krankenhaus „St. Johann Nepomuk“ <strong>Erfurt</strong><br />
Jörg Pertschy<br />
Klinik für Allgemein-, Visceral- und Gefäßchirurgie,<br />
Katholisches Krankenhaus „St. Johann Nepomuk“<br />
<strong>Erfurt</strong><br />
Einleitung<br />
Sarkome sind Tumoren aus Zellen mesenchymalen Ursprungs.<br />
Sie machen nur 1 % aller malignen Tumoren aus.<br />
In 30 % der Fälle eines Sarkoms ist dieses am Körperstamm<br />
lokalisiert. Unter den mehr als 150 histopathologischen<br />
Untergruppen weisen das Liposarkom mit einem<br />
Anteil von 62 % und das Leiomyosarkom mit einem Anteil<br />
von 19 % die größte Häufigkeit auf. Sarkome bilden<br />
eine tumorinfiltrierte Pseudokapsel und zeigen durch ihr<br />
diskontinuierliches Wachstumsverhalten „skip-Läsionen“.<br />
Eine Metastasierung erfolgt zumeist hämatogen hauptsächlich<br />
in die Lunge und Leber.<br />
Diagnostik und Klassifikation<br />
Die Sonographie steht ob der schnellen Verfügbarkeit am<br />
Anfang der Diagnostik. Die Vertifizierung im Sinne der Tumorgrenzen<br />
und Organinfiltration ist mit Hilfe der Magnetresonanztomographie<br />
(MRT) als wichtigstes Verfahren<br />
zu erzielen. Die Computertomographie (CT) zur Komplettierung<br />
des Stagings beantwortet Fragen der Metastasierung.<br />
Die Positronenemissionstomographie (PET)<br />
gewinnt zunehmend im Rahmen der Rezidiv- und Metastasendiagnostik<br />
an Bedeutung. Zur endgültigen Diagnosestellung<br />
bedarf es der Biopsie. Hierbei gilt es zu beachten,<br />
ausreichend vitale Gewebspartikel von mindestens<br />
1,5 cm 3 Größe zu gewinnen und den Zugangsweg im späteren<br />
Operationsgebiet zu planen.<br />
Das histopathologische Grading wird nach dem FNCLCC-<br />
Schema (French Fédération Nationale des Centres de Lutte<br />
Contre le Cancer) anhand eines Punktesystems bezüglich<br />
der Parameter Tumordifferenzierung, Tumornekrosen<br />
und Mitosenanzahl ermittelt.<br />
■ Seite 10 ■ JOURNAL 01/2005 02/2011
Primärtumor (T)<br />
TX Primärtumor nicht identifizierbar<br />
T0 Keine Evidenz des Primärtumors<br />
T1 Tumor 5 cm oder weniger in größter Ausdehnung<br />
T1a Oberflächlicher Tumor<br />
T1b Tiefer Tumor<br />
T2 Tumor mehr als 5 cm in größter Ausdehnung<br />
T2a Oberflächlicher Tumor<br />
T2b Tiefer Tumor<br />
Regionale Lymphknoten (N)<br />
NX Regionale Lymphknoten nicht evaluierbar<br />
N0 Keine regionalen Lymphknotenmetastasen<br />
N1 Regionale Lymphknotenmetastasen<br />
Fernmetastasen (M)<br />
M0 Keine Fernmetastasen<br />
M1 Fernmetastasen<br />
Histopathologisches Grading (G)<br />
Low grade G1/G2<br />
High grade G3/G4<br />
Abb. 1 TNM-Klassifikation<br />
Stadium IA<br />
Stadium IB<br />
Stadium IIA<br />
Stadium IIB<br />
Stadium III<br />
Stadium IV<br />
T1a<br />
T1b<br />
T2a<br />
T2b<br />
T1a<br />
T1b<br />
T2a<br />
T2b<br />
jedes T<br />
jedes T<br />
N0, NX<br />
N0, NX<br />
N0, NX<br />
N0 , NX<br />
N0, NX<br />
N0, NX<br />
N0, NX<br />
N0, NX<br />
N1<br />
jedes N<br />
M0<br />
M0<br />
M0<br />
M0<br />
M0<br />
M0<br />
M0<br />
M0<br />
M0<br />
M1<br />
Abb. 2 Stadieneinteilung nach UICC und AJCC (2010)<br />
Low grade<br />
Low grade<br />
Low grade<br />
Low grade<br />
High grade<br />
High grade<br />
High grade<br />
High grade<br />
jedes G<br />
jedes G<br />
Kasuistik 1<br />
Im April 2009 stellte sich ein 58 Jahre alter Patient mit einer<br />
tastbaren Resistenz im rechten Hemiabdomen vor.<br />
Schnittbildmorphologisch bestätigte sich ein großer retroperitonealer<br />
Tumor mit resultierender Organverlagerung<br />
nach ventral. Das Staging verblieb ohne Hinweis auf<br />
Metastasen.<br />
Abb. 3 Großer retroperitonealer Tumor mit Organverlagerung (CT)<br />
JOURNAL 02/2011<br />
Wir führten die en-bloc-Resektion mit Nephrektomie<br />
rechts, Adrenalektomie rechts und Appendektomie durch.<br />
Abb. 4 En-bloc-Resektat<br />
Histopathologisch ergab sich ein hochdifferenziertes Liposarkom<br />
mit Ausbreitungsklassifikatin T2b N0 M0 low<br />
grade und Nachweis einer R0-Resektion.<br />
Wir konnten den Patienten am 15. postoperativen Tag<br />
nach komplikationslosem Verlauf nach Hause entlassen.<br />
Die Fallvorstellung im interdisziplinären Tumorkonsil ergab<br />
die Empfehlung einer engmaschigen Tumornachsorge.<br />
Diese erfolgte bis dato in unserer Klinik ohne Hinweis<br />
auf Lokalrezidiv oder Metastasierung.<br />
Kasuistik 2<br />
Im Juli 2005 stellte sich ein 58-jähriger Patient wegen Subileussymptomatik<br />
in unserer Notaufnahme vor. Die angefertigte<br />
Computertomographie bestätigte einen mechanischen<br />
Subileus durch einen monströsen Mesenterialtumor.<br />
Abb. 5a Monströser Mesenterialtumor (CT)<br />
■ Seite 11 ■
Abb. 5b Monströser Mesenterialtumor (CT)<br />
Das Staging blieb bezüglich einer Metastasierung unauffällig.<br />
Nach histopathologischem Befund eines undifferenzierten<br />
hochgradig pleomporphen Sarkoms aus der<br />
Stanzbiopsie planten wir die multiviszerale Resektion. Diese<br />
erfolgte als Tumorexstirpation mit Jejunumsegmentresektion<br />
und Ileozökalresektion. Im endgültigen Histologiebefund<br />
bestätigte sich das pleomorphe Sarkom mit der<br />
Ausbreitungsklassifikation T2b N0 M0 high grade und<br />
Nachweis der R0-Resektion.<br />
Abb. 6 Pleomorphes Sarkom (Für die Überlassung der Bilder bedanken wir<br />
uns beim Institut für Pathologie, HELIOS Klinikum <strong>Erfurt</strong>)<br />
Nach unkompliziertem Verlauf konnten wir den Patienten<br />
am 21. postoperativen Tag nach Hause entlassen. Entsprechend<br />
der Empfehlung nach Fallvorstellung im interdisziplinären<br />
Tumorkonsil erfolgte die engmaschige Tumornachsorge<br />
in einer onkologischen Praxis bisher ohne<br />
Nachweis eines Rezidivs oder Metastasierung.<br />
Zusammenfassung<br />
Die einzig kurative Therapie abdomineller Weichgewebssarkome<br />
stellt die primäre Resektion dar. Aufgrund der<br />
häufigen Notwendigkeit eines multiviszeralen Eingriffs<br />
empfiehlt sich die Behandlung in Tumorzentren. Für die<br />
adjuvante Radio-Chemotherapie konnte bisher keine höhere<br />
Überlebensrate aufgezeigt werden, jedoch stellt sich<br />
ein Vorteil im rezidivfreien bzw. metastasenfreien Intervall<br />
dar. In einzelnen Arbeiten wird der intraoperativen Radiatio<br />
ein Vorteil zugesprochen. Eine Empfehlung zur Tumornachsorge<br />
gibt die nachstehende Tabelle.<br />
Tabelle Tumornachsorgeempfehlung<br />
1.-3. Jahr<br />
postoperativ<br />
3.-5. Jahr<br />
postoperativ<br />
5.-10. Jahr<br />
postoperativ<br />
vierteljährlich MRT/CT lokal<br />
+ CT Thorax<br />
halbjährlich MRT/CT lokal<br />
+ CT Thorax<br />
jährlich MRT/CT lokal<br />
+ CT Thorax<br />
Perspektiven<br />
Die Optimierung der Chemotherapie, der Tumornachsorge<br />
in Hinblick auf die Ausweitung der Verwendung des<br />
PET-Verfahrens sowie die Forschung auf dem Feld der molekularen<br />
Marker stellen Pfeiler der Perspektiven für die<br />
Sarkome dar.<br />
Literatur beim Verfasser.<br />
Korrespondenzadresse:<br />
Uta Wichmann<br />
Klinik für Allgemein-, Visceral- und Gefäßchirurgie<br />
Katholisches Krankenhaus „St. Johann Nepomuk“ <strong>Erfurt</strong><br />
Haarbergstraße 72<br />
99097 <strong>Erfurt</strong><br />
Telefon: 0361 654-1201<br />
e-Mail: visceralchirurgie@kkh-erfurt<br />
■ Seite 12 ■ JOURNAL 01/2005 02/2011
■ Chemotherapie-assoziierte<br />
Lebererkrankungen<br />
Jens-Gerd Scharf<br />
2. Medizinische Klinik<br />
Gastroenterologie / Hepatologie, Endokrinologie /<br />
Diabetologie, Rheumatologie,<br />
HELIOS Klinikum <strong>Erfurt</strong><br />
Albrecht Stier<br />
Klinik für Allgemein- und Viszeralchirurgie,<br />
HELIOS Klinikum <strong>Erfurt</strong><br />
Ca. 30-35 % der Patienten mit einem kolorektalen Karzinom<br />
(KRK) entwickeln im Verlauf ihrer Erkrankung Lebermetastasen.<br />
Die überwiegende Anzahl der Lebermetastasen<br />
ist dabei primär nicht resektabel. Heutzutage stehen<br />
jedoch wirksame Chemotherapieregime zur Verfügung,<br />
mit denen primär nicht resektable Metastasen in eine resektable<br />
Form überführt werden können (Konversionschemotherapie).<br />
Ziele einer derartigen präoperativen Chemotherapie<br />
sind neben dem Downsizing der Lebermetastasen,<br />
der Verbesserung der Resektabilität mit einer erhöhten<br />
Rate an R0-Resektionen auch die Einsparung von<br />
gesundem Leperparenchym bei der Operation. Daneben<br />
hat eine präoperative Chemotherapie eine Reduktion der<br />
mikroskopischen Lebermetastasierung zum Ziel. Das 5-<br />
Jahres-Überleben von Patienten mit Lebermetastasen<br />
nach präoperativer Chemotherapie mit sekundärer Resektion<br />
beträgt in einer Untersuchung von Adam et al. [1]<br />
33 % bzw. 27 % nach 10 Jahren. Diese Überlebensdaten<br />
sind insbesondere vor dem Hintergrund, dass bei den Patienten<br />
eine Tumorerkrankung im Stadium der Metastasierung<br />
vorliegt, so bemerkenswert.<br />
Neben der Wirksamkeit der oben genannten Chemotherapien<br />
ist in den letzten Jahren aber auch die Nebenwirkung<br />
dieser Therapien in den Fokus des Interesses von Kliniken<br />
und Pathologen gerückt: die Chemotherapie-induzierte<br />
Lebertoxizität. Auf zellulärer Ebene sind in der Leber<br />
im Wesentlichen die Hepatozyten, die Cholangiozyten<br />
und das Endothel Zielzellen der Medikamentennebenwirkung<br />
[2, 3]. Während die Cholangiozyten als relativ resistent<br />
gelten, sind an Hepatozyten Verfettung und Einzelzellnekrosen<br />
als Folge der zytostatischen Wirkung lichtmikroskopisch<br />
sichtbar. Am hepatischen Eindothel sind<br />
insbesondere Ektasien nachweisbar. In einer Untersuchung<br />
von Vauthey et al. [4] finden sich bei Patienten nach<br />
einer Irinotecan-haltigen Chemotherapie in 10,6 % der<br />
Fälle eine Fettleber (Steatosis >30 %) sowie in 20,2 % eine<br />
Fettleberhepatitis (Steatohepatitis). Histologisch sind<br />
diese Veränderungen denen einer nicht-alkoholischen<br />
Steatohepatitis (NASH) ähnlich und werden daher als<br />
CASH bezeichnet (Chemotherapie-assoziierte Steatohepatitis).<br />
Vergleichbar einer NASH reichen die histologischen<br />
Veränderungen von einer Steatosis hepatis bis zu einer<br />
manifesten Fettleberhepatitis (Steatohepatitis).<br />
Dagegen führen Oxaliplatin-haltige präoperative Chemotherapien<br />
zu Gefäßschäden an der Leber, die als sinusoidales<br />
Obstruktionssyndrom (SOS, „sinusoidal obstruction<br />
syndrome“) bezeichnet werden. Histologisch sind diese<br />
JOURNAL 02/2011<br />
Gefäßläsionen als sinusoidale Dilatationen mit Blutung<br />
und Austritt von Erythrozyten in den Disse’schen Raum<br />
sowie mit Gefäßwandfibrose und umschriebenen Hyperplasien<br />
charakterisiert. Das SOS-Syndrom wird als direkte<br />
Schädigung der Sinusendothelien verstanden, wobei sich<br />
histopathologisch neben Entzündungs- und Fibroseprozessen<br />
lokale Thrombosen mit embolischem Verschluss<br />
nachgeschalteter kleiner und größerer Gefäße nachweisen<br />
lassen. Durch Schädigung des Sinusendothels in den<br />
terminalen hepatischen Venolen und sublobulären Venen<br />
kommt es einerseits zur Aktivierung der Gerinnungskaskade<br />
(Thrombose), andererseits zur Hyperfibrinolyse (Blutungen).<br />
Die Endstrecke der „disseminierten intravasalen<br />
Koagulation“ der Leber ist die Entzündung mit kensekutiver<br />
Fibrose, bis hin zum Gefäßverschluss. In einer Untersuchung<br />
von Morris-Stiff et al. [5] treten diese Veränderungen<br />
in 20-40 % aller Patienten mit präoperativer Chemotherapie<br />
auf. Intraoperativ können diese Veränderungen<br />
als „blue liver“ in Erscheinung treten.<br />
Welche Patienten sind besonders gefährdet, eine Chemotherapie-assoziierte<br />
Lebertoxizität zu entwickeln?<br />
In einer Untersuchung von Nakano und Mitarbeitern [6]<br />
konnte gezeigt werden, dass Frauen und Patienten, die<br />
mehr als 6 Zyklen einer präoperativen Oxaliplatin-haltigen<br />
Chemotherapie und Patienten, die präoperativ AST-Werte<br />
von mehr als 36 U/l hatten, ein höheres Risiko hatten,<br />
eine Chemotherapie-assoziierte Lebertoxizität zu entwickeln.<br />
Insgesamt muss besonderes Augenmerk auf Patienten<br />
gerichtet werden, bei denen bereits eine Lebervorschädigung<br />
wie z.B. eine nicht alkoholische Steatohepatitis<br />
(NASH) bzw. auch eine alkoholische Steatohepatitis<br />
(ASH) besteht.<br />
Gibt es protektive Substanzen gegen das SOS?<br />
Zum jetzigen Zeitpunkt liegen nur kleinere klinische Studien<br />
vor, bei denen durch zusätzliche Gabe von Bevacizumab<br />
zu einer Oxaliplatin-haltigen Chemotherapie die Inzidenz<br />
des sinusoidalen Obstruktionssyndroms reduziert<br />
werden konnte [7, 8]. Bevacizumab ist dabei ein Antikörper<br />
gegen das VEGF, das nicht nur eine Rolle bei der Tumorangiogenese<br />
spielt, sondern auch bei einer Vielzahl<br />
anderer Prozesse wie der Stimulation von anderen Wachstumsfaktoren<br />
(u.a. dem HGF [Hepatocyte Growth Factor])<br />
involviert ist. Als potentieller Wirkmechanismus von Bevacizumab<br />
gegen das SOS wird eine Reduktion des SOS<br />
durch Blockade einer VEGF-induzierten MMP-9-Expression,<br />
eine Reduktion der prothrombogenen Eigenschaften<br />
der VEGF-Mediatoren und insgesamt eine generelle Gefäßprotektion<br />
durch die VEGF-Blockade angenommen.<br />
Einschränkend muss jedoch bemerkt werden, dass es sich<br />
bei den oben genannten Untersuchungen um retrospektive<br />
Analysen von relativ kleinen Patientenzahlen handelt.<br />
Für die Beurteilung des Stellenwertes des protektiven Effektes<br />
von Bevacizumab auf das SOS müssen jedoch prospektiv<br />
randomisierte Studien an größeren Patientenzahlen<br />
abgewartet werden.<br />
Bedeutung der Chemotherapie-induzierten Hepatotoxizität<br />
für Morbidität und Mortalität<br />
Bis zum jetzigen Zeitpunkt liegen nur kleinere Untersuchungen<br />
vor, die allesamt gezeigt haben, dass die Mortalität<br />
bei einer Oxaliplatin-haltigen präoperativen Chemo-<br />
■ Seite 13 ■
therapie nicht erhöht ist (Übersicht in [9]). Hinsichtlich der<br />
Irinotecan-assoziierten Steatohepatitis konnte nur in der<br />
Studie von Vauthey et al. [4] ein signifikante Erhöhung der<br />
90-Tages-Mortalität von 1,6 % auf 14,7 % (p=0,001) gezeigt<br />
werden. In allen anderen Untersuchungen war jedoch<br />
die Mortalität durch eine CASH nicht erhöht. In allen<br />
diesen Untersuchungen zeigte sich jedoch eine Erhöhung<br />
der perioperativen Morbidität (Leberinsuffizienz, Infektion),<br />
die abhängig war von der Anzahl der verabreichten<br />
präoperativen Chemotherapiezyklen [9].<br />
Zusammenfassend kann festgestellt werden, dass umfangreiche<br />
präoperative Chemotherapien (>9 Zyklen) das<br />
Risiko für eine Hepatotoxizität nach Resektion von KRK-<br />
Metastasen erhöhen und gleichzeitig das histologische<br />
Ansprechen der Metastasen nicht weiter verbessern. Dabei<br />
sind Irinotecan-haltige präoperative Chemotherapien<br />
mit dem Auftreten einer Chemotherapie-assoziierten<br />
Steatohepatitis (CASH) sowie Oxaliplatin-haltige Chemotherapien<br />
mit dem Auftreten eines sinusoidalen Obstruktionssyndroms<br />
(SOS) assoziiert. Eine operative Entfernung<br />
von Lebermetastasen sollte daher, sobald eine R0-Resektion<br />
bildgebend möglich erscheint, erfolgen. In der Regel<br />
kann durch eine prolongierte präoperative Therapie das<br />
Therapieansprechen der Lebermetastasen nicht verbessert<br />
werden. Besonderes Augenmerk sollte auf Risikopatienten,<br />
d.h. Patienten mit einer vorbestehenden Lebererkrankung<br />
(NASH, ASH) gelegt werden, die regelmäßigen<br />
Kontrolluntersuchungen unterzogen werden sollten. Bei<br />
unklar erhöhten Leberwerten, die nicht durch eine Lebermetastasierung<br />
erklärbar sind, sollte eine Leberbiopsie<br />
durchgeführt werden.<br />
Zusammenfassung<br />
Chemotherapie-assoziierte Lebertoxizität<br />
Präoperative<br />
Chemotherapie<br />
Histologische<br />
Merkmale<br />
Makroskopischer<br />
Aspekt<br />
Inzidenz 4<br />
Literatur<br />
Chemotherapie<br />
assoziierte<br />
Steatohepatitis<br />
(CASH)<br />
Irinotecan<br />
5-FU<br />
Fettleber<br />
Fettleberhepatitis<br />
Fettleber<br />
~ 50 %<br />
Sinusoidales<br />
Obstruktionssyndrom<br />
(SOS)<br />
Oxaliplatin<br />
Sinusoidale Dilatation,<br />
Entzündung,<br />
Fibrose, lokale<br />
Thrombose mit embolischemVerschluss<br />
kleiner und<br />
größerer Gefäße,<br />
Blutungen<br />
„blue liver“<br />
20 – 40 %<br />
1. Adam R, Wicherts DA, de Haas RJ, et al. Patients with initially unresectable<br />
colorectal liver metastases: is there a possibility of cure? J Clin<br />
Oncol 2009;27:1829-1835<br />
2. Tannapfel A, Reinacher-Schick A. [Chemotherapy associated hepatotoxicity<br />
in the treatment of advanced colorectal cancer (CRC)]. Z Gastroenterol<br />
2008;46:435-440<br />
3. Tannapfel A, Reinacher-Schick A, Flott-Rahmel B. [Steatohepatitis after<br />
chemotherapy for colorectal liver metastases (CASH)]. Pathologe;32:330-335<br />
4. Vauthey JN, Pawlik TM, Ribero D, et al. Chemotherapy regimen predicts<br />
steatohepatitis and an increase in 90-day mortality after surgery for<br />
hepatic colorectal metastases. J Clin Oncol 2006;24:2065-2072<br />
5. Morris-Stiff G, Tan YM, Vauthey JN. Hepatic complications following<br />
preoperative chemotherapy with oxaliplatin or irinotecan for hepatic<br />
colorectal metastases. Eur J Surg Oncol 2008;34:609-614<br />
6. Nakano H, Oussoultzoglou E, Rosso E, et al. Sinusoidal injury increases<br />
morbidity after major hepatectomy in patients with colorectal liver metastases<br />
receiving preoperative chemotherapy.<br />
Ann Surg 2008;247:118-124<br />
7. Kishi Y, Zorzi D, Contreras CM, et al. Extended preoperative chemotherapy<br />
does not improve pathologic response and increases postoperative<br />
liver insufficiency after hepatic resection for colorectal liver metastases.<br />
Ann Surg Oncol;17:2870-2876<br />
8. Ribero D, Wang H, Donadon M, et al. Bevacizumab improves pathologic<br />
response and protects against hepatic injury in patients treated with<br />
oxaliplatin-based chemotherapy for colorectal liver metastases. Cancer<br />
2007;110:2761-2767<br />
9. Zorzi D, Laurent A, Pawlik TM, et al. Chemotherapy-associated hepatotoxicity<br />
and surgery for colorectal liver metastases.<br />
Br J Surg 2007;94:274-286<br />
■ GALLIUM-Studie erfolgreich<br />
gestartet<br />
Michael Herold<br />
4. Medizinische Klinik, Onkologisches Zentrum,<br />
HELIOS Klinikum <strong>Erfurt</strong><br />
Multizentrische und randomisierte Phase III Studie bei<br />
unbehandelten Patienten mit fortgeschrittenem und<br />
behandlungsbedürftigen follikulärem Lymphom vergleicht<br />
den Goldstandard Rituximab plus Chemotherapie<br />
mit dem neuen Anti-CD20-Antikörper Obinutuzomab<br />
(GA101) plus Chemotherapie<br />
In der Behandlung indolenter Lymphome, insbesondere<br />
der des follikulären Lymphoms, wurden in der letzten Dekade<br />
bahnbrechende Fortschritte erzielt. Erstmals seit<br />
Jahrzehnten ist es gelungen, für die betroffenen Patienten<br />
eine signifikante Verlängerung der Zeit bis zum Progress<br />
des Lymphoms und damit der Zeit bis zur nächsten<br />
notwendigen Behandlung zu erzielen. In einigen Studien<br />
konnte erstmals sogar ein Überlebensvorteil gegenüber<br />
alleiniger Chemotherapie gezeigt werden. Die Kombination<br />
des Anti-CD20-Antikörpers Rituximab mit Chemotherapie<br />
ist inzwischen als Goldstandard etabliert und der<br />
zusätzliche Einsatz des Antikörpers in der Erhaltungstherapie<br />
verlängert die Zeit bis zum erneuten Fortschreiten<br />
der Erkrankung zusätzlich.<br />
■ Seite 14 ■ JOURNAL 01/2005 02/2011
Trotz der erzielten großen Erfolge bleiben die fortgeschrittenen<br />
indolenten Lymphome jedoch auch heute noch<br />
chronische Erkrankungen mit einem rezidivierenden Verlauf<br />
und es besteht weiterhin kein kurativer Behandlungsanspruch.<br />
Diese Tatsache ist unverändert eine Herausforderung<br />
für die klinische Forschung auf diesem Gebiet.<br />
Verminderte<br />
CDC Aktivität<br />
Abb. 1 Antikörper GA101 (Obinutuzomab)<br />
Erhöhte Rate von direktem<br />
Zelltod (Apoptose)<br />
(Typ II Bindung + elbow-hinge<br />
Modifikation)<br />
Gesteigerte ADCC<br />
(erhöhte Affinität zum ’ADCC<br />
Rezeptor’ FcgR IIIa) durch<br />
Glycolysierung der FC-Region<br />
Die GALLIUM-Studie ist eine weltweite Studie, die ca.<br />
1.400 Patienten rekrutieren wird. Hauptzielgruppe der<br />
Studie sind die follikulären Lymphome (n=1.200), jedoch<br />
können auch Patienten mit Marginalzonenlymphomen in<br />
die Studie eingeschlossen werden (ca. 200). Dabei wird<br />
GA101 (siehe Abb. 1), ein neuer Anti-CD20-Antikörper der<br />
3. Generation mit potentiell höherer Aktivität als Rituximab,<br />
in Kombination mit Chemotherapie gegen Rituximab<br />
plus Chemotherapie, gefolgt von einer Erhaltungstherapie<br />
mit GA101 bzw. Rituximab verglichen. Es handelt<br />
sich hierbei um eine Zulassungsstudie (FDA/EMA) der Firmen<br />
Hoffmann-La Roche AG (Schweiz) und Genentech,<br />
Inc. (USA). Die führenden Studiengruppen sind dabei die<br />
Deutsche Studiengruppe für niedrigmaligne Lymphome<br />
(GLSG) und die Ostdeutsche Studiengruppe Hämatologie<br />
und Onkologie (OSHO) für Deutschland und das National<br />
Cancer Research Institute (NCRI) für Großbritannien. Die<br />
globalen Studienleiter sind Prof. Hiddemann (GLSG) und<br />
Prof. Marcus (NCRI), der Studienleiter für Deutschland ist<br />
Prof. Herold (OSHO/HELIOS Klinikum <strong>Erfurt</strong>). Seit dem Studienstart<br />
im Juli 2011 wurden bis Ende Oktober über 50<br />
Patienten, davon 5 in Deutschland, rekrutiert. Damit<br />
konnte das gestellte Ziel deutlich übertroffen werden.<br />
Die 4. Medizinische Klinik des HELIOS Klinikum <strong>Erfurt</strong> ist<br />
ein Zentrum der Studie und nimmt Patienten auf. Die randomisierte<br />
Phase III-Studie hat ein zweiarmiges Design.<br />
Die Patienten erhalten eine Induktionschemotherapie, für<br />
die sich das Zentrum primär festlegt (<strong>Erfurt</strong>: Bendamustin).<br />
Diese wird randomisiert mit Rituximab oder GA101<br />
kombiniert und für die Patienten mit einem Ansprechen<br />
(CR oder PR) folgt eine Erhaltungstherapie mit Rituximab<br />
oder GA101 über 2 Jahre in 2-monatigem Abstand (siehe<br />
Abb. 2).<br />
R – CHOP<br />
(6 x CHOP + 8 x R)<br />
vs<br />
G – CHOP<br />
(6 x CHOP + 8 x G<br />
and on days 8+15<br />
of Cycle 1)<br />
JOURNAL 02/2011<br />
CR or PR SD<br />
Maintenance Observation<br />
PD<br />
Rituximab or GA101<br />
monotherapy, every<br />
2 month for 2 years<br />
PD<br />
Abb. 2 Studienablauf BO21223 GALLIUM<br />
Haupteinschlusskriterien:<br />
· Follikuläres Lymphom (FL) Grad 1-3a oder Marginalzonenlymphom<br />
(MZL) (splenisch, nodal oder extranodal)<br />
· fortgeschrittenes Stadium (Ann Arbor III, IV oder Ann<br />
Arbor II mit Bulky-Befall)<br />
· Behandlungsindikation (GELF-Kriterien)<br />
Hauptausschlusskriterien:<br />
· Aggressive oder transformierte Lymphome, FL Grad<br />
3b, ZNS-Befall<br />
· Ann Arbor Stadium I<br />
· vorbehandelte Patienten<br />
Weitere Informationen zu dieser Studie sind über Clinical<br />
Trial Portal (www.clinicaltrials.gov; NCT01332968) oder<br />
über die Studienärzte der 4. Medizinischen Klinik des<br />
HELIOS Klinikum <strong>Erfurt</strong> (Dr. Franziska Walther, OÄ Dr. Elke<br />
Richter, Prof. Dr. M. Herold, Telefon 0361-781 5290 oder<br />
e-Mail michael.herold@helios-kliniken.de) erhältlich.<br />
Korrespondenzadresse:<br />
Induction<br />
R – CVP<br />
(8 x CVP + 8 x R)<br />
vs<br />
G – CVP<br />
(8 x CVP + 8 x G<br />
and on days 8+15<br />
of Cycle 1)<br />
Response evaluation<br />
No further protocol<br />
specified treatment<br />
Follow for next antilymphoma<br />
Tx and<br />
survival until the<br />
official end of the trial<br />
5 years of FU 5 years of FU<br />
Prof. Dr. med. Michael Herold<br />
4. Medizinische Klinik<br />
Onkologisches Zentrum<br />
HELIOS Klinikum <strong>Erfurt</strong><br />
Nordhäuser Str. 74<br />
99089 <strong>Erfurt</strong><br />
Telefon: 0361-781 2473<br />
e-Mail: michael.herold@helios-kliniken.de<br />
R – bendamustine<br />
(6 x benda + 6 x R)<br />
vs<br />
G – bendamustine<br />
(6 x benda + 6 x G<br />
and on days 8+15<br />
of Cycle 1)<br />
PD<br />
■ Seite 15 ■<br />
No further protocol<br />
specified treatment<br />
Follow for<br />
progression every<br />
2 month for 2 years
■ Aktuelle Diagnose-, Therapie- und<br />
Nachsorgeleitlinien<br />
Die Verbreitung aktueller Leitlinien im Versorgungsgebiet<br />
ist eine Hauptaufgabe der Tumorzentren. Wir werden an<br />
dieser Stelle regelmäßig auf die geltenden Leitlinien hinweisen.<br />
In dieser Ausgabe finden Sie die Empfehlungen zur Nachsorge<br />
ausgewählter Tumorentitäten.<br />
In den folgenden Abschnitten werden für die einzelnen<br />
Tumorerkrankungen notwendige und sinnvolle Nachsorgeuntersuchungen<br />
bei primär kurativ behandelten Patienten<br />
angegeben.<br />
Nachsorge Mammakarzinom<br />
Die Heilungschancen beim Mammakarzinom hängen vor<br />
allem von der Tumorgröße, dem Lymphknotenstatus und<br />
der adäquaten Primärtherapie ab. Sie besteht in der chirurgischen<br />
Resektion und je nach Situation ggf. einer adjuvanten<br />
Strahlen- und/oder Chemo- bzw. Hormontherapie.<br />
Vordringliches medizinisches Ziel der Nachsorgeuntersuchungen<br />
ist die frühe Erkennung eines Rezidivs in der<br />
brusterhaltend operierten Brust, des Zweitkarzinoms in<br />
der kontralateralen Brust und des Lokalrezidivs nach<br />
Mastektomie, weil hier noch kurative Therapiemöglichkei-<br />
Nachsorgeempfehlung:<br />
Die Empfehlungen der routinemäßigen Untersuchungen<br />
gelten nur für beschwerdefreie Patienten.<br />
Immer dann, wenn Beschwerden oder Symptome den<br />
Verdacht auf ein Rezidiv oder Metastasen lenken, sind<br />
gezielte Untersuchungen indiziert, um eine entsprechende<br />
Behandlung einleiten zu können.<br />
Bei Patienten, deren Tumorerkrankung nur palliativ behandelt<br />
werden kann, hängen Art und Umfang von Untersuchungen<br />
allein vom palliativen Therapieziel und der<br />
individuellen Situation ab. Dies ist nicht Gegenstand dieser<br />
Leitlinien.<br />
ten bestehen. Deshalb stehen gründliche klinische Untersuchung,<br />
gezielte Anamnese und einige wenige Zusatzuntersuchungen<br />
ganz im Vordergrund. Die Früherkennung<br />
einer Fernmetastasierung bei einer beschwerdefreien Patientin<br />
ändert demgegenüber wenig an der Prognose und<br />
ist deswegen nicht Hauptziel der Nachsorge. Wegen des<br />
erhöhten Risikos für Zweittumoren an Ovarien, Endometrium<br />
und Dickdarm sollten die entsprechenden Früherkennungsuntersuchungen<br />
unbedingt angeboten werden.<br />
nach Mastektomie nach brusterhaltender Therapie<br />
Anamnese und Untersuchung vierteljährlich für 3 Jahre, vierteljährlich für 3 Jahre,<br />
halbjährlich bis 5. Jahr, halbjährlich für noch nicht<br />
dann jährlich definierte Zeit<br />
Tumormarker Tumormarker in der Routine verzichtbar<br />
Selbstuntersuchung monatlich auf Dauer<br />
Mammografie kontralaterale Brust jährlich kontralaterale Brust jährlich,<br />
ipsilaterale Brust in den ersten<br />
3 Jahren halbjährlich, dann jährlich<br />
Sonografie von Mamma, in den ersten 3 Jahren<br />
regionären Lymphabflussgebieten / halbjährlich vierteljährlich,<br />
Thoraxwand dann jährlich<br />
Röntgen-Thorax bei entsprechenden Symptomen oder auf Wunsch der Patientin<br />
Ganzkörperskelettszintigrafie, bei klinischem Verdacht auf Metastasen,<br />
Labor z.B. Knochenschmerzen<br />
Oberbauchsonografie bei entsprechenden Symptomen oder auf Wunsch der Patientin<br />
■ Seite 16 ■ JOURNAL 01/2005 02/2011
Nachsorge Ovarialkarzinom<br />
In den Stadien I, seltener in den Stadien II und nur in Ausnahmefällen<br />
in den Stadien III nach der FIGO-Stadieneinteilung<br />
besteht eine realistische Heilungschance. Die<br />
Nachsorge hat in erster Linie das Ziel, Folgeschäden zu erkennen<br />
und zu behandeln. Die Erkennung eines Rezidivs,<br />
auch eines solitären, bedeutet in der Regel, dass keine kurative<br />
Chance mehr besteht. Je nach Vorbehandlung, Dauer<br />
des rezidivfreien Intervalls und Art des Rezidivs oder der<br />
Metastasierung bestehen aber zum Teil gute Möglichkeiten<br />
einer längerfristigen Palliation, so dass Nachuntersuchungen,<br />
die dazu beitragen, ein Rezidiv in einem Stadium<br />
mit geringerer Ausdehnung zu behandeln, sinnvoll<br />
sind. Als Besonderheit ist zu berücksichtigen, dass Borderline-Karzinome<br />
auch nach vielen Jahren noch rezidivieren<br />
können und oft erneut zu therapieren sind. Gerade diese<br />
Patientinnen sollten dazu motiviert werden, die jährliche<br />
gynäkologische Nachsorge- bzw. Früherkennungsuntersuchung<br />
wahrzunehmen.<br />
Notwendige Untersuchungen:<br />
· Ärztliche Untersuchung<br />
alle 3 Monate, nach 2 Jahren alle 6 Monate<br />
· Sonografie<br />
alle 6 Monate<br />
- vaginal zum Ausschluss eines Lokalrezidivs<br />
- abdominell zum Ausschluss von Aszites, Nierenstau<br />
und abdomineller Metastasierung<br />
Ergänzende Untersuchungen:<br />
· Laboruntersuchungen<br />
(BSG, BB, gGT, Kreatinin, CA-125)<br />
alle 6 Monate, vor allem bei Verdacht auf Rezidiv<br />
· Röntgenuntersuchungen (bei Beschwerden und<br />
Verdacht auf Rezidiv oder Metastasen)<br />
- CT<br />
- Röntgen-Thorax<br />
- MRT<br />
- ggf. PET-CT<br />
Nachsorge Vulva-, Zervix-, Korpuskarzinom<br />
Die Heilungsaussichten richten sich nach der Ausdehnung<br />
des Tumors bei Diagnose und Primärtherapie. Medizinisches<br />
Ziel der Nachsorge ist die Entdeckung des Lokalrezidivs<br />
und die Behandlung von Folgeschäden, insbesondere<br />
wenn adjuvante strahlentherapeutische Maßnahmen<br />
durchgeführt wurden.<br />
Bei Fernmetastasen ist eine Heilung nicht möglich. Die<br />
palliativen systemischen Therapiemöglichkeiten sind<br />
äußerst begrenzt. Die Früherkennung einer Fernmetastasierung<br />
bei symptomlosen Patientinnen hat daher nur geringen<br />
Wert.<br />
Notwendige Untersuchungen:<br />
· Ärztliche Untersuchung<br />
alle 3 Monate, nach 2 Jahren alle 6 Monate<br />
· vaginale Sonographie alle 6 Monate<br />
JOURNAL 02/2011<br />
Ergänzende Untersuchungen<br />
(nur bei Beschwerden oder Metastasenverdacht):<br />
· Laboruntersuchungen (BSG, BB, Kreatinin)<br />
· abdominelle Sonographie<br />
· Röntgenuntersuchungen<br />
- CT des Abdomens<br />
- Röntgen-Thorax<br />
- MRT<br />
- PET-CT<br />
Korrespondenzadresse:<br />
Prof. Dr. med. Udo B. Hoyme<br />
Klinik für Frauenheilkunde und Geburtshilfe<br />
HELIOS Klinikum <strong>Erfurt</strong><br />
Nordhäuser Str. 74<br />
99089 <strong>Erfurt</strong><br />
Telefon: 0361-781 4001<br />
e-Mail: udo.hoyme@helios-kliniken.de<br />
Nachsorge Nierenzellkarzinom<br />
Das Tumorstadium zum Zeitpunkt der Primärtumoroperation<br />
bestimmt die Prognose von Patienten mit Nierenzellkarzinom.<br />
Diese ist ausgesprochen gut bei organbegrenzten<br />
Tumoren niedrigen Tumorvolumens und verschlechtert<br />
sich dramatisch bei lokal fortgeschrittenen Tumoren<br />
mit Invasion in Nachbarorgane (Nebennierenbeteiligung)<br />
bzw. lymphknotenpositiven Befunden. Eine Orientierung<br />
bietet eine 2002 – vor Einführung neuer Therapieoptionen<br />
der Targettherapie beim metastasierten Tumor – publizierte<br />
Übersicht (Tabelle 1).<br />
Tabelle 1<br />
5-Jahres-Überlebensraten in Abhängigkeit vom Tumorstadium<br />
bei Nephrektomie.<br />
Modifiziert nach American Joint Committee on Cancer 2002<br />
Befund TNM Stadium 5-Jahres-<br />
Überlebensrate (%)<br />
Organbegrenzter<br />
Tumor T1-T2 N0 M0 70 – 90<br />
< 4 cm T1a N0 M0 90 – 100<br />
4 – 7 cm T1b N0 M0 80 – 90<br />
> 7 cm T2 N0 M0 70 – 80<br />
Invasion perirenales<br />
Fett T3a N0 M0 60 – 80<br />
venöser<br />
Tumorthrombus T3b-T3c N0 M0 40 – 65<br />
lokal fortgeschritten<br />
(inkl. Nebenniereninvasion)<br />
T4 N0 M0 0 – 20<br />
Lymphknotenbefall<br />
TX N+ M0 0 – 20<br />
■ Seite 17 ■
Insgesamt entwickeln ca. 30 % der Patienten nach primär<br />
kurativer Operation eines Nierenzellkarzinoms im Verlauf<br />
Rezidive oder Metastasen. An Hand der genannten Überlebensdaten<br />
wird klar, dass eine stadien- und damit risikoadaptierte<br />
Nachsorge erfolgen sollte. Dabei gilt die Nierenteilresektion<br />
bei Tumoren der Stadien T1a/b N0 als absolut<br />
gleichwertig mit der radikalen Tumornephrektomie<br />
und erfordert keine intensivierte Nachsorge. Bei lokal fortgeschrittenen<br />
Tumoren bzw. nach ablativen Therapieverfahren<br />
wird eine intensivierte Nachsorge unabhängig von<br />
der Operationstechnik empfohlen.<br />
Folgt man der theoretischen Überlegung, dass allein die<br />
chirurgische Resektion von Metastasen eine potenzielle<br />
Chance auf Heilung erreicht und jegliche medikamentöse<br />
Tumortherapie auch im Zeitalter der Targettherapie rein<br />
palliativen Charakter trägt, so wäre vielleicht eine extrem<br />
engmaschige Nachsorge empfehlenswert. Leider weisen<br />
nur etwa 5 % aller Patienten mit Metastasierung eines<br />
Nierenzellkarzinoms solitäre bzw. oligolokuläre Befunde<br />
auf, die einer Metastasenchirurgie zugänglich wären.<br />
Prognostisch relevant ist dabei ein Zeitintervall von mindestens<br />
einem Jahr zwischen Primärtherapie und Metastasierung.<br />
Patienten mit früher Metastasierung profitieren<br />
äußerst selten vom metastasenchirurgischen Vorgehen.<br />
Verschiedene Autoren propagierten daher bisher,<br />
Nachsorgeuntersuchungen mittels Schnittbilddiagnostik<br />
erst nach einem Zeitintervall von minimal 2 Jahren nach<br />
Tumornephrektomie bzw. Teilresektion zu beginnen.<br />
Bereits 2005 veröffentlichte eine Arbeitsgruppe der University<br />
of California Los Angeles (UCLA) basierend auf<br />
dem dort entwickelten Risikoscore (UISS, vgl. Abb.) eine<br />
detaillierte Nachsorgeempfehlung.<br />
Grade<br />
1-2<br />
ECOG<br />
0<br />
Low<br />
Risk<br />
N<br />
Stage<br />
T Stage<br />
Nodal<br />
Disease<br />
T1 T2 T3 T4<br />
ECOG<br />
>0<br />
Grade<br />
3-4<br />
0<br />
Grade<br />
1-4<br />
ECOG<br />
0-3<br />
Intermediate<br />
Risk<br />
1+<br />
Grade<br />
1<br />
ECOG<br />
0<br />
Grade<br />
>1<br />
ECOG<br />
>0<br />
Grade<br />
1-4<br />
ECOG<br />
0-3<br />
High<br />
Risk<br />
Abb. Definition von Risikogruppen nach Primärtumoroperation nach UCLA<br />
(aus Lam et al. J Urol 174 (2005): 466-472)<br />
Fraglich erscheint, ob die Einbeziehung des ECOG Performancestatus<br />
klinisch sauber umsetzbar ist und die Risikostratifizierung<br />
wirklich verbessert. Aus Sicht des Autors<br />
würde sich eine Einteilung der Risikogruppen nach histologischem<br />
Befund anbieten (Tabelle 2):<br />
Tabelle 2<br />
Definition von Risikogruppen an Hand des histopathologischen<br />
T- und N-Stadiums.<br />
Zeitpunkt<br />
Untersuchung<br />
3 Monate<br />
6 Monate<br />
12 Monate<br />
18 Monate<br />
24 Monate<br />
36 Monate<br />
48 Monate<br />
60 Monate<br />
Zeitpunkt<br />
Untersuchung<br />
3 Monate<br />
6 Monate<br />
12 Monate<br />
18 Monate<br />
24 Monate<br />
36 Monate<br />
48 Monate<br />
60 Monate<br />
84 Monate<br />
108 Monate<br />
Risikogruppe Charakteristika<br />
Low risk<br />
(geringes Risiko) T1a/b N0 M0 G1-2<br />
Intermediate risk T1a/b N0 M0 G3<br />
(mittleres Risiko) T2 N0 M0 G1-2<br />
High risk T2 N0 M0 G3<br />
(hohes Risiko) T3-4 u./o. N+<br />
Für die differenzierte Nachsorge der Patienten wäre folgendes<br />
Schema denkbar (Tabellen 3-5):<br />
Tabelle 3<br />
Nachsorgeempfehlung Niedriges Risiko<br />
Klinische<br />
Untersuchung<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
Klinische<br />
Untersuchung<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
Laborwertkontrolle<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
Laborwertkontrolle<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
Sonografie<br />
Abdomen<br />
Tabelle 4<br />
Nachsorgeempfehlung Mittleres Risiko<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
Sonografie<br />
Abdomen<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
CT<br />
Thorax<br />
x<br />
x<br />
x<br />
x<br />
x<br />
CT<br />
Thorax<br />
■ Seite 18 ■ JOURNAL 01/2005 02/2011<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
CT<br />
Abdomen<br />
x<br />
x<br />
CT<br />
Abdomen<br />
x<br />
x<br />
x<br />
x<br />
x
Tabelle 5<br />
Nachsorgeempfehlung Hohes Risiko<br />
Zeitpunkt<br />
Untersuchung<br />
3 Monate<br />
6 Monate<br />
12 Monate<br />
18 Monate<br />
24 Monate<br />
36 Monate<br />
48 Monate<br />
60 Monate<br />
84 Monate<br />
108 Monate<br />
Klinische<br />
Untersuchung<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
Obwohl die Nierenteilresektion gegenüber der Tumornephrektomie<br />
als onkologisch gleichwertig gilt, bietet sie<br />
doch das Problem der sicheren Abgrenzung operationsbedingter<br />
narbiger Veränderungen von Tumorrezidiven.<br />
Im klinischen Alltag hat es sich daher bewährt, ca. 8 Wochen<br />
postoperativ eine Schnittbildgebung der Niere (CT<br />
oder MRT) als Basisuntersuchung zur Gewährleistung späterer<br />
Vergleichsmöglichkeit zu veranlassen. Abgesehen<br />
von dieser Besonderheit wird insbesondere bei niedrigem<br />
Risiko die Tumornachsorge auch nach partieller Nephrektomie<br />
primär Sonografie-gestützt durchgeführt.<br />
Literatur beim Verfasser<br />
Korrespondenzadresse:<br />
Laborwertkontrolle<br />
Prof. Dr. med. Thomas Steiner<br />
Klinik für Urologie<br />
HELIOS Klinikum <strong>Erfurt</strong><br />
Nordhäuser Straße 74<br />
99089 <strong>Erfurt</strong><br />
Telefon: 0361 781-2201<br />
e-Mail: thomas.steiner@helios-kliniken.de<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
Sonografie<br />
Abdomen<br />
x<br />
x<br />
CT<br />
Thorax<br />
JOURNAL 02/2011<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
CT<br />
Abdomen<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
x<br />
■ Auditierung und Zertifizierung der<br />
ersten drei Kopf-Hals-Tumorzentren in<br />
Deutschland – <strong>Erfurt</strong> ist dabei!<br />
Hans Pistner<br />
Klinik für Mund-, Kiefer- und Gesichtschirurgie,<br />
HELIOS Klinikum <strong>Erfurt</strong><br />
Dirk Eßer<br />
Klinik für Hals-, Nasen- und Ohrenheilkunde,<br />
HELIOS Klinikum <strong>Erfurt</strong><br />
Kerstin Breitenstein<br />
Klinik für Hals-, Nasen- und Ohrenheilkunde,<br />
HELIOS Klinikum <strong>Erfurt</strong><br />
Dirk Vollrath<br />
Klinik für Mund-, Kiefer- und Gesichtschirurgie,<br />
HELIOS Klinikum <strong>Erfurt</strong><br />
Wettbewerb in der Medizin ist heute politisch gewollt. Er<br />
führt im kleinen täglichen Ablauf zur Arbeitsverdichtung<br />
für Ärzte und Pfleger. Eine sinnvolle und notwendige Ausgleichsmaßnahme<br />
ist die Leitlinienentwicklung (möglichst<br />
nach AWMF-Standard) und die Zertifizierung von Zentren,<br />
z.B. in der Onkologie, vorzugsweise nach den Standards<br />
der Deutschen Krebsgesellschaft und ihrer Zertifizierungsgesellschaft<br />
OnkoZert. Seit 2003 gibt es Brustzentren,<br />
seit 2006 Darmkrebs- und seit 2007 Prostatakarzinomzentren.<br />
Seit dem Jahr 2008 gibt es neben den Organzentren<br />
die übergeordneten onkologischen Zentren.<br />
Das erste und bisher einzige in Thüringen wurde 2011 am<br />
HELIOS Klinikum <strong>Erfurt</strong> GmbH auditiert und zertifiziert.<br />
Doch damit nicht genug: Unter dem Dach des onkologischen<br />
Zentrums sind als Modul seit dem 12.03.2010 Kopf-<br />
Hals-Tumorzentren zur Auditierung vorgesehen.<br />
Im gemeinsamen Gespräch fassten wir im Frühjahr 2010<br />
den Entschluss, zur ersten Gruppe der zertifizierten Kliniken<br />
gehören zu wollen. Nach Zustimmung der Geschäftsführung<br />
am 29.05.2010 wurde ein externer Beratervertrag<br />
abgeschlossen und ein Pflichtenheft im August 2010<br />
erarbeitet. In monatlichen Arbeitssitzungen planten wir<br />
das Audit durch OnkoZert für den 30.03.2011. Die Anforderungen<br />
für Kooperationsvereinbarungen, Arbeitsanweisungen,<br />
Standards jeder Art waren nicht geringfügig.<br />
Daher war es nicht nur Enttäuschung, sondern auch ein<br />
Stück Erleichterung, als OnkoZert am 15.03.2011 – zwei<br />
Wochen vor dem geplanten Audit – aufgrund interner<br />
Organisationsprobleme von OnkoZert den Termin<br />
30.03.2011 absagte. Zu diesem Termin im Frühjahr 2011<br />
gab es noch keine ausgebildeten Fachauditoren bei OnkoZert.<br />
Dies ermöglichte uns in der HNO-Heilkunde wie in<br />
der MKG-Chirurgie eine Intensivierung der Vorbereitungen.<br />
Schließlich fand ganztägig am 06.09.2011 das Audit<br />
durch einen OnkoZert-Mitarbeiter und zwei Klinikdirektoren<br />
aus dem Südwesten Deutschland statt.<br />
Wir sind sehr stolz, dass dieses erste Audit gelang:<br />
· OHNE Abweichung<br />
· mit positiven Feststellungen und ohne Einzelbefunde,<br />
die behoben werden müssten,<br />
und nur mit<br />
· wenigen moderaten Hinweisen zur Psychoonkologie,<br />
zur onkologischen Fachpflege und zur Unterscheidung<br />
■ Seite 19 ■
von Haupt- und Kooperationspartnern. (Die Umsetzung<br />
dieser Hinweise wird angeregt, muss aber nicht<br />
bis zur Zertifizierung erfüllt sein.)<br />
Die Anforderungen an die Klinik für Mund-, Kiefer- und<br />
Gesichtschirurgie ebenso wie an die Klinik für Hals-Nasen-<br />
Ohrenheilkunde bezüglich Qualifikation der Mitarbeiter<br />
und der Fallzahlen wurden in beiden Fällen weit übererfüllt.<br />
Zitat aus dem Auditbericht: „Im Audit entstand der<br />
Eindruck eines gut vorbereiteten und offensichtlich durch<br />
andere Zertifizierungen erfahrenen Hauses. Durch Novellierungen<br />
des Erhebungsbogens noch kurz vor dem Audit<br />
aufgrund der Kommentierungen in der zugestellten Bewertung<br />
konnten noch etliche offene Fragen vorab ge-<br />
Die Leiter des Kopf-Hals-<strong>Tumorzentrum</strong>s am HELIOS Klinikum <strong>Erfurt</strong>,<br />
Prof. Dr. Eßer und Prof. Dr. Dr. Pistner, freuen sich, gemeinsam mit einigen<br />
ihrer engagierten Mitarbeiter über den erfolgreichen Abschluss des Zertifizierungsverfahrens.<br />
Im Bild von links: Prof. Dr. Dirk Eßer (Chefarzt der Klinik<br />
für HNO-Heilkunde), OÄ Dr. Kerstin Breitenstein (HNO), Dr. Natalie<br />
Nebel (MKG), Dr. Uta Blockmann (HNO), Dr. Dirk Vollrath (MKG), Dr. Sören<br />
Seeliger (HNO), Prof. Dr. Dr. Hans Pistner (Chefarzt der Klinik für Mund-,<br />
Kiefer- und Gesichtschirurgie)<br />
Foto: HELIOS Klinikum <strong>Erfurt</strong><br />
Korrespondenzadressen:<br />
Prof. Dr. med. Dirk Eßer<br />
Klinik für Hals-, Nasen- und Ohrenheilkunde<br />
HELIOS Kopf-Hals-<strong>Tumorzentrum</strong><br />
HELIOS Klinikum <strong>Erfurt</strong><br />
Nordhäuser Straße 74<br />
99089 <strong>Erfurt</strong><br />
Telefon: 0361 781-2101<br />
e-Mail: dirk.esser@helios-kliniken.de<br />
klärt werden. Die Organisation und Durchführung des<br />
Audits war sehr gut: Die Angebote zur Kontaktaufnahme<br />
und Visitierung der Einrichtung war bereitwillig und vorbereitet<br />
… Der Gesamteindruck im Zertifizierungsaudit ist<br />
gut.“<br />
In der Folge erwarteten wir zum Jahresende 2011 die Erteilung<br />
des Zertifikats als Kopf-Hals-<strong>Tumorzentrum</strong> (Modul<br />
im onkologischen Zentrum) als eines der drei ersten<br />
Kopf-Hals-Tumorzentren in Deutschland und als erstes<br />
und bisher einziges in Thüringen.<br />
Tatsächlich erreichte uns im Dezember die erstrebte Anerkennung<br />
zusammen mit der abgebildeten Urkunde.<br />
Prof. Dr. med. Dr. med. dent. Hans Pistner<br />
Klinik für Mund-, Kiefer- und Gesichtschirurgie<br />
HELIOS Kopf-Hals-<strong>Tumorzentrum</strong><br />
HELIOS Klinikum <strong>Erfurt</strong><br />
Nordhäuser Straße 74<br />
99089 <strong>Erfurt</strong><br />
Telefon: 0361 781-2230<br />
e-Mail: hans.pistner@helios-kliniken.de<br />
■ Seite 20 ■ JOURNAL 01/2005 02/2011
■ Jahreskonferenz der<br />
Thüringischen Gesellschaft<br />
für Chirurgie in<br />
Bad Langensalza<br />
Lutz-Dieter Schreiber<br />
Thüringische Gesellschaft für Chirurgie e.V.<br />
Im zauberhaften Ambiente des im Rokoko-Stil erbauten<br />
und aufwendig sanierten Friederikenschlösschens an der<br />
Kurpromenade in Bad Langensalza fand am 27. und 28.<br />
Mai 2011 die Jahrestagung der Thüringischen Gesellschaft<br />
für Chirurgie statt.<br />
Unter der wissenschaftlichen Leitung des 1. Vorsitzenden<br />
der Gesellschaft und Chefarztes der Abteilung für Allgemein-<br />
und Viszeralchirurgie und Proktologie der Hufeland<br />
Klinikum GmbH Standort Bad Langensalza, Herrn PD Dr.<br />
med. Lutz-Dieter Schreiber, war die Entwicklung der Mininalinvasiven<br />
Chirurgie (MIC) das Thema. Nach gut zwei<br />
Jahrzehnten war es Zeit für eine kritische Bilanz.<br />
Nach der Begrüßung und Eröffnung durch den Tagungspräsidenten<br />
gab es Grußworte vom Bürgermeister der<br />
Stadt Bad Langensalza und Gesellschafter der Hufeland<br />
Klinikum GmbH, Herrn Bernhard Schönau, sowie vom Generalsekretär<br />
der Deutschen Gesellschaft für Chirurgie,<br />
Herrn Prof. Dr. Hartwig Bauer (Berlin). Prof. Bauer war von<br />
der Atmosphäre der Tagung und der Begeisterung der<br />
Thüringer Chirurgen beeindruckt.<br />
Im wissenschaftlichen Programm kamen die einzelnen<br />
Gebiete der Chirurgie in 6 Sitzungsblöcken zur Darstellung.<br />
Neben namhaften Referenten und Pionieren der<br />
MIC wie Prof. I. Gastinger (Cottbus), der die erste Rektumexstirpation<br />
auf endoskopischem Weg durchgeführt hat,<br />
kamen vor allem Kolleginnen und Kollegen aus Thüringen<br />
zu Wort. Wie schon auf dem letzten Kongress gab auch<br />
diesmal das „Junge Forum“ dem chirurgischen Nachwuchs<br />
Gelegenheit, interessante wissenschaftliche Vorträge<br />
zu halten. Die beiden Besten wurden durch die Gesellschaft<br />
prämiert. So erhielt Frau Dr. S. Seidel aus der Bad<br />
Langesalzaer Klinik für ihren Beitrag „NOTES-Chirurgie an<br />
der Hufeland Klinikum GmbH Standort Bad Langensalza:<br />
Wie ist NOTES-Chirurgie in Thüringen etabliert? – Ein<br />
Überblick“ den Preis für den besten Vortrag.<br />
Preisträgerin Dr. med. Susanne Seidel, Bad Langensalza, bei ihrem Vortrag<br />
JOURNAL 02/2011<br />
Bemerkenswert war der Vortrag „Abdominelle MIC – Was<br />
hat’s gebracht? von Herr Prof. J. M. Müller (Berlin). Er zog<br />
nach exakter Analyse der weltweiten wissenschaftlichen<br />
Publikationen den Schluss, dass lediglich eine Erhöhung<br />
der Kosten pro Fall und eine Verlängerung der Operationszeiten<br />
gesichert sei.<br />
Die meisten Teilnehmer zeichneten aber ein deutlich optimistischeres<br />
Bild und verwiesen auf Erfolge und vielversprechende<br />
Entwicklungen. So berichtete Prof. G. Kähler<br />
(Mannheim) in seinem Vortrag: „NOTES: endoskopische<br />
Artistik oder sinnvolle Weiterentwicklung der MIC?“ über<br />
erste eigene Erfahrungen mit der Appendektomie und<br />
Cholezystektomie über einen oralen transgastralen Zu-<br />
■ Seite 21 ■
Tagungsstätte Frederikenschlösschen in Bad Langensalza<br />
Intensive Gespräche in der Pause<br />
Prof. (em.) Dr. med. h.c. Helmut Wolff, Berlin<br />
Prof. Dr. med. Georg Kähler, Leiter der Zentralen Interdisziplinären Endoskopie,<br />
Viszeralchirurgisches Zentrum, Universitätsmedizin Mannheim<br />
gang zur Bauchhöhle mit dem flexiblen Endoskop in<br />
Deutschland.<br />
Bei der Entwicklung und Bewertung neuer Verfahren und<br />
Methoden in der Minimalinvasiven Chirurgie muss vor allem<br />
die Sicherheit unserer Patienten gewährleistet sein. So<br />
wurde für NOTES (chirurgische Eingriffe über natürliche<br />
Körperöffnungen wie Mund, Scheide, Anus oder Harnröhre,<br />
um sichtbare Narben zu vermeiden) von der Deutschen<br />
Gesellschaft für Visceralchirurgie ein spezielles Melderegister<br />
eingerichtet, das über mögliche Komplikationen<br />
unterrichtet.<br />
Eine Industrieausstellung informierte in den Sitzungspausen<br />
über neueste Entwicklungen auf dem Gebiet der Medizintechnik<br />
für minimalinvasive Eingriffe. Gleichzeitig<br />
konnten hier, wie auch beim Gesellschaftsabend in der<br />
„Ratswaage“ vertiefende Gespräche mit den Kolleginnen<br />
und Kollegen geführt werden.<br />
Wie uns zahlreiche Rückinformationen der Teilnehmer bestätigten,<br />
war es insgesamt ein wichtiger rundherum gelungener<br />
Kongress.<br />
Der Jahreskongress 2012 der Thüringischen Gesellschaft<br />
für Chirurgie wird am 18. und 19. Mai 2012 in Mühlhausen<br />
stattfinden.<br />
Korrespondenzadresse:<br />
PD Dr. med. Lutz-Dieter Schreiber<br />
Hufeland Klinikum GmbH<br />
Standort Bad Langensalza<br />
Klinik für Allgemein- und Visceralchirurgie<br />
und Proktologie<br />
Rudolf-Weiss-Straße 1-5<br />
99947 Bad Langensalza<br />
Telefon: 03603 855-673<br />
e-Mail: medizin.lsz@hufeland.de<br />
■ Seite 22 ■ JOURNAL 01/2005 02/2011
■ Erfasste Maligne Neubildungen<br />
und deren Vorstufen im Klinischen<br />
Krebsregister des <strong>Tumorzentrum</strong><br />
<strong>Erfurt</strong><br />
Stand: Dezember 2011<br />
ICD-10 Bezeichnung M % W % Gesamt %<br />
C00 Lippe 74 0.14 31 0.07 105 0.10<br />
C01 Zungengrund 143 0.26 27 0.06 170 0.17<br />
C02 Zunge 209 0.39 99 0.21 308 0.30<br />
C03 Zahnfleisch 102 0.19 59 0.13 161 0.16<br />
C04 Mundboden 244 0.45 48 0.10 292 0.29<br />
C05 Gaumen 94 0.11 24 0.05 118 0.12<br />
C06 Andere Teile<br />
des Mundes 57 0.06 49 0.10 106 0.10<br />
C07 Parotis 94 0.17 75 0.16 169 0.17<br />
C08 Große<br />
Speicheldrüsen 28 0.05 15 0.03 43 0.04<br />
C09 Tonsille 305 0.56 85 0.18 390 0.39<br />
C10 Oropharynx 203 0.38 27 0.06 230 0.23<br />
C11 Nasopharynx 64 0.12 21 0.04 85 0.08<br />
C12 Recessus<br />
piriformis 132 0.24 15 0.03 147 0.15<br />
C13 Hypopharynx 179 0.33 16 0.03 195 0.19<br />
C14 Andere Lokalisationen<br />
im<br />
Mundbereich 2 0.00 1 0.00 3 0.00<br />
C15 Ösophagus 518 0.96 99 0.21 617 0.61<br />
C16 Magen 1.350 2.50 945 2.01 2.295 2.27<br />
C17 Dünndarm 152 0.28 145 0.31 297 0.29<br />
C18 Dickdarm 3.257 6.03 2.974 6.32 6.230 6.17<br />
C19 Rektosigmoid 2 0.00 2 0.00 4 0.00<br />
C20 Rektum 2.448 4.53 1.518 3.23 3.966 3.92<br />
C21 Analkanal 60 0.11 134 0.28 194 0.19<br />
C22 Leber 444 0.82 185 0.39 629 0.62<br />
C23 Gallenblase 60 0.11 302 0.64 363 0.36<br />
C24 Andere Teile<br />
der Gallengänge 182 0.34 177 0.38 359 0.36<br />
C25 Pankreas 930 1.72 863 1.83 1.793 1.77<br />
C26 Verdauungsorgane<br />
o. n. A. 4 0.01 7 0.01 11 0.01<br />
C30 Nasenhöhle u.<br />
Mittelohr 38 0.07 34 0.07 72 0.07<br />
C31 Nasennebenhöhlen<br />
74 0.14 30 0.06 104 0.10<br />
C32 Larynx 756 1.40 57 0.12 818 0.80<br />
C33 Trachea 10 0.02 7 0.01 17 0.02<br />
C34 Lunge 7.541 13.97 2.250 4.78 9.791 9.69<br />
C37 Thymus 41 0.08 29 0.06 70 0.07<br />
C38 Herz, Mediastinum,<br />
Pleura 46 0.09 23 0.05 69 0.07<br />
C39 Sonstige und<br />
ungenau bezeichneteLokalisationen<br />
des<br />
Atmungssytems 1 0.00 0 0.00 1 0.00<br />
C40 Knochen und<br />
Gelenkknorpel<br />
der Extremitäten 37 0.07 34 0.07 71 0.07<br />
JOURNAL 02/2011<br />
ICD-10 Bezeichnung M % W % Gesamt %<br />
C41 Knochen und<br />
Gelenkknorpel<br />
sonstiger<br />
Lokalisationen 49 0.09 42 0.09 91 0.09<br />
C43 Melanom der<br />
Haut 1.640 30.4 1.623 3.45 3.263 3.23<br />
C44 Sonstige<br />
Hauttumoren 6.776 12.55 5.358 11.39 12.134 12.01<br />
C45 Mesotheliom 48 0.09 24 0.05 72 0.07<br />
C46 Kaposi-Sarkom 6 0.01 8 0.02 14 0.01<br />
C47 Periphere Nerven<br />
und autonomes<br />
Nervensystem 12 0.02 14 0.03 26 0.03<br />
C48 Retroperitoneum<br />
und Peritoneum 41 0.08 48 0.10 89 0.09<br />
C49 Sonstiges Bindegewebe<br />
und<br />
andere Weichteile<br />
181 0.34 181 0.38 362 0.36<br />
C50 Brustdrüse 85 0.16 11.862 25.21 11.947 11.82<br />
C51 Vulva 0 0.00 269 0.57 269 0.27<br />
C52 Vagina 0 0.00 87 0.18 87 0.09<br />
C53 Cervix uteri 0 0.00 1799 3.82 1799 1.78<br />
C54 Corpus uteri 0 0.00 2.222 4.72 2.222 2.20<br />
C55 Uterus o. n. A. 0 0.00 122 0.26 122 0.12<br />
C56 Ovar 0 0.00 1.237 2.63 1.237 1.22<br />
C57 Sonstige<br />
weibliche<br />
Genitalorgane 0 0.00 89 0.19 89 0.09<br />
C58 Plazenta 0 0.00 5 0.01 5 0.00<br />
C60 Penis 146 0.17 0 0.00 146 0.14<br />
C61 Prostata 9.584 17.75 0 0.00 9.584 9.48<br />
C62 Hoden 1.072 1.99 0 0.00 1072 1.06<br />
C63 Sonstige<br />
männliche<br />
Genitalorgane 18 0.03 0 0.00 18 0.02<br />
C64 Niere 2.831 5.24 1.713 3.64 4.544 4.50<br />
C65 Nierenbecken 172 0.32 120 0.26 292 0.29<br />
C66 Ureter 114 0.21 71 0.15 185 0.18<br />
C67 Harnblase 3.026 5.60 975 2.07 4.001 3.96<br />
C68 Sonstige<br />
Harnorgane 105 0.19 15 0.03 120 0.12<br />
C69 Auge und<br />
Augenanhangsgebilde<br />
64 0.12 64 0.14 128 0.13<br />
C70 Meningen 4 0.01 8 0.02 12 0.01<br />
C71 Gehirn 681 1.26 528 1.12 1.209 1.20<br />
C72 Rückenmark,<br />
Hirnnerven 13 0.02 5 0.01 18 0.02<br />
C73 Schilddrüse 233 0.43 504 1.07 737 0.73<br />
C74 Nebenniere 23 0.04 25 0.05 48 0.05<br />
C75 Sonstige endokrine<br />
Drüsen 3 0.01 7 0.01 10 0.01<br />
C76 Sonstige und<br />
ungenau bezeichneteLokalisationen<br />
24 0.04 26 0.06 50 0.05<br />
C77 Sekundäre Neubildung<br />
der<br />
Lymphknoten 10 0.02 6 0.01 16 0.02<br />
■ Seite 23 ■
ICD-10 Bezeichnung M % W % Gesamt %<br />
C78 Sekundäre Neubildung<br />
der<br />
Atmungs- und<br />
Verdauungsorgane<br />
10 0.02 2 0.00 12 0.01<br />
C79 Sekundäre<br />
Neubildung<br />
sonstiger<br />
Lokalisationen 0 0.00 1 0.00 1 0.00<br />
C80 Unbekannte<br />
Lokalisation 617 1.14 592 1.26 1.209 1.20<br />
C81 Hodgkin-<br />
Krankheit 291 0.54 252 0.54 543 0.54<br />
C82 Follikuläres<br />
Non-Hodgkin-<br />
Lymphom 181 0.34 216 0.46 397 0.39<br />
C83 Diffuses<br />
Non-Hodgkin-<br />
Lymphom 716 1.33 631 1.34 1.347 1.33<br />
C84 Periphere und<br />
kutane T-Zell-<br />
Lymphome 269 0.50 139 0.30 408 0.40<br />
C85 Sonstige 291 0.54 285 0.61 576 0.57<br />
C88 Immunproliferative<br />
Krankheit 7 0.01 9 0.02 16 0.02<br />
C90 Plasmozytom 470 0.87 436 0.93 906 0.90<br />
C91 Lymphatische<br />
Leukämie 672 1.24 476 1.01 1.148 1.14<br />
C92 Myeloische<br />
Leukämie 429 0.79 383 0.81 812 0.80<br />
C93 Monozytenleukämie<br />
23 0.04 26 0.06 49 0.05<br />
C94 Sonstige<br />
Leukämien 11 0.02 6 0.01 17 0.02<br />
C95 Leukämie<br />
n. n. b. 8 0.01 14 0.03 22 0.02<br />
C96 Sonstige und<br />
n. n. b. Neubildungen<br />
des<br />
lymphatischen<br />
u. blutbildenden<br />
Gewebes 2 0.00 3 0.01 5 0.00<br />
in situ Carcinoma in citu<br />
und u. sonstige Neu-<br />
Sonstige bildungen 3.154 5.84 4.118 8.75 7.272 7.20<br />
Gesamt 53.993 100.00 47.055 100.00 101.048 100.00<br />
■ Darmkrebs 2000 – 2010 bei Patienten<br />
aus <strong>Erfurt</strong> und dem Kreis Gotha –<br />
Datenauswertungen des Klinischen<br />
Krebsregisters <strong>Erfurt</strong><br />
Hubert Göbel<br />
Klinisches Krebsregister, <strong>Tumorzentrum</strong> <strong>Erfurt</strong><br />
Die folgenden Auswertungen zum Darmkrebs wurden mit<br />
dem vom Südwestsächsischen <strong>Tumorzentrum</strong> Zwickau<br />
entwickelten Programmsystem © SWS-GTDS-SPSS-Auswertungssystem<br />
in einer standardisierten Form erstellt,<br />
die auch bevölkerungsbezogene Bezüge und Aussagen<br />
enthält.<br />
Das <strong>Erfurt</strong>er Register dokumentiert im Wesentlichen die in<br />
den Krankenhäusern und Praxen der Region Mittel- und<br />
Westthüringen diagnostizierten und behandelten Tumorerkrankungen.<br />
Die Dokumentation bezieht sich also nicht<br />
auf die in diesem Gebiet wohnenden, sondern auf die von<br />
den Versorgungseinrichtungen im Einzugsgebiet betreuten<br />
Tumorpatienten. Obwohl sich die meisten Patienten<br />
wohnortnah behandeln lassen, kommt es an den Rändern<br />
des Einzugsgebietes zu nicht unerheblichen Wanderungen<br />
(Erreichbarkeit der Einrichtung, Verkehrsverbindungen<br />
etc.).<br />
Die Beschränkung auf die Stadt <strong>Erfurt</strong> und den Kreis Gotha<br />
trägt dem Rechnung, weil beide Kreise vollständig im<br />
Einzugsgebiet liegen und auch fast alle Fälle im <strong>Erfurt</strong>er<br />
Register geführt werden.<br />
■ Seite 24 ■ JOURNAL 01/2005 02/2011
JOURNAL 02/2011<br />
■ Seite 25 ■
■ Seite 26 ■ JOURNAL 01/2005 02/2011
JOURNAL 02/2011<br />
■ Seite 27 ■
■ Seite 28 ■ JOURNAL 01/2005 02/2011
JOURNAL 02/2011<br />
■ Seite 29 ■
■ Seite 30 ■ JOURNAL 01/2005 02/2011
JOURNAL 02/2011<br />
■ Seite 31 ■
■ Seite 32 ■ JOURNAL 01/2005 02/2011
JOURNAL 02/2011<br />
■ Seite 33 ■
■ Seite 34 ■ JOURNAL 01/2005 02/2011
Korrespondenzadresse:<br />
Dr. rer. nat. Hubert Göbel<br />
Klinisches Krebsregister<br />
<strong>Tumorzentrum</strong> <strong>Erfurt</strong><br />
Nordhäuser Straße 74<br />
99089 <strong>Erfurt</strong><br />
Telefon: 0361 781-14806<br />
e-Mail: hubert.goebel@helios-kliniken.de<br />
JOURNAL 02/2011<br />
■ Seite 35 ■
■ Gemeinsames Veranstaltungsverzeichnis<br />
von Medizinisch-wissenschaftlicher Gesellschaft <strong>Erfurt</strong> e.V.<br />
HELIOS Klinikum <strong>Erfurt</strong> GmbH und <strong>Tumorzentrum</strong> <strong>Erfurt</strong> e.V.<br />
Liebe Kolleginnen und Kollegen,<br />
wir möchten Ihre gezielten und konzentrierten Fortbildungsaktivitäten<br />
mit einem gemeinsamen Veranstaltungsverzeichnis unterstützen und Ihnen<br />
ein breites Spektrum zertifizierter und hoffentlich für Sie interessanter<br />
Fort- und Weiterbildungen anbieten.<br />
Die nachstehende Kurzfassung kann weder vollständig sein, noch umfassend<br />
informieren. Sie soll als Orientierungshilfe dienen und Sie animieren,<br />
alle weiteren Informationen und die laufenden Aktualisierungen<br />
auf der Internetseite www.mwg-erfurt.de nachzulesen und / oder<br />
direkt bei den Organisatoren zu erfragen.<br />
Über eine zahlreiche Teilnahme an den Veranstaltungen, rege Diskussionen<br />
sowie die Vertiefung und Ausweitung persönlicher Kontakte freuen<br />
wir uns besonders.<br />
Prof. Dr. med. Prof. Dr. med. Prof. Dr. med.<br />
R. Erkwoh A. Stier D. Eßer<br />
Vorsitzender Vorsitzender Ärztlicher Direktor<br />
MWG e.V. <strong>Tumorzentrum</strong> <strong>Erfurt</strong> e.V. HELIOS Klinikum <strong>Erfurt</strong><br />
Januar 2012<br />
18.01.2012, 16.00 Uhr<br />
HELIOS Klinikum <strong>Erfurt</strong>, Auditorium<br />
1. Fortbildung Neuromedizin<br />
Thema: Management und Standards bei Tumoren und Metastasen der<br />
Wirbelsäule<br />
HELIOS Klinikum <strong>Erfurt</strong>, Klinik für Neurochirurgie<br />
20.01.2012, 8.45 bis 15.30 Uhr<br />
HELIOS Klinikum <strong>Erfurt</strong>, Auditorium<br />
Workshop Trachealkanülenmanagement für Logopäden, Stimmund<br />
Sprachtherapeuten, Krankenschwestern und Pflegekräfte<br />
HELIOS Klinikum <strong>Erfurt</strong>, Klinik für Hals-, Nasen- und Ohrenheilkunde,<br />
Plastische Operationen, Abteilung für Phoniatrie und Pädaudiologie<br />
25.01.2012, 17.00 bis 20.00 Uhr<br />
HELIOS Klinikum <strong>Erfurt</strong>, Auditorium<br />
10 Jahre Kardiale Resynchronisationstherapie – Etabliertes,<br />
Konkretes und Künftiges<br />
HELIOS Klinikum <strong>Erfurt</strong>, 3. Medizinische Klinik, Kardiologie,<br />
Internistische Intensivmedizin<br />
27. bis 28.01.2012<br />
Besprechungsraum der Klinik für Allgemein- und Viszeralchirurgie,<br />
HELIOS Klinkum <strong>Erfurt</strong><br />
Grundkurs Ultraschalldiagnostik im Kopf- und Halsbereich<br />
(A-Bild- und B-Bild-Verfahren)<br />
HELIOS Klinikum <strong>Erfurt</strong>, Klinik für Hals-, Nasen- und Ohrenheilkunde,<br />
Plastische Operationen<br />
Februar 2012<br />
15.02.2012, 17.00 bis 20.00 Uhr<br />
Evangelisches Augustinerkloster<br />
Neuroendokrine Tumore<br />
<strong>Tumorzentrum</strong> <strong>Erfurt</strong> e.V.<br />
22. bis 26.02.2012<br />
Seminarraum, Hotel „Weißer Schwan“ <strong>Erfurt</strong>-Kerspleben,<br />
<strong>Erfurt</strong>er Straße 179, 99198 <strong>Erfurt</strong>-Kerspleben<br />
14. <strong>Erfurt</strong>er Seminar „Endokrinologie aktiv“<br />
HELIOS Klinikum <strong>Erfurt</strong>, 2. Medizinische Klinik, Endokrinologie<br />
25.02.2012, 10.00 bis 13.00 Uhr<br />
HELIOS Klinikum <strong>Erfurt</strong>, Auditorium<br />
46. <strong>Erfurt</strong>er Ophtalmologengespräch<br />
HELIOS Klinikum <strong>Erfurt</strong>, Klinik für Augenheilkunde<br />
25.02.2012, 9.00 bis 15.00 Uhr<br />
HELIOS Klinikum <strong>Erfurt</strong>, Mensa<br />
Polytraumatag<br />
HELIOS Klinikum <strong>Erfurt</strong>, Klinik für Unfall-, Hand- und Wiederherstellungschirurgie<br />
März 2012<br />
03.03.2012, 10.00 bis 13.00 Uhr<br />
Festsaal des <strong>Erfurt</strong>er Rathauses<br />
Festveranstaltung „20 Jahre <strong>Tumorzentrum</strong> <strong>Erfurt</strong> e.V.“<br />
<strong>Tumorzentrum</strong> <strong>Erfurt</strong> e.V.<br />
28.03.2012, 10.00 bis 13.00 Uhr<br />
HELIOS Klinikum <strong>Erfurt</strong>, Auditorium<br />
4. <strong>Erfurt</strong>er Dermatologische Frühjahrstagung<br />
Klinik für Hautkrankheiten und Allergologie, HELIOS Hauttumorzentrum<br />
<strong>Erfurt</strong>, HELIOS Klinikum <strong>Erfurt</strong> in Zusammenarbeit mit dem<br />
<strong>Tumorzentrum</strong> <strong>Erfurt</strong> e.V.<br />
April 2012<br />
21.04.2012, 9.00 bis 15.00 Uhr<br />
Zentralklinik Bad Berka, Station 33, Robert-Koch-Allee 9,<br />
99437 Bad Berka<br />
Berkaer Symposium Palliativmedizin<br />
Thema: Ich mache jetzt Schluss – Suizidalität in der Palliativmedizin<br />
Klinik für Palliativmedizin, Zentralklinik Bad Berka in Zusammenarbeit<br />
mit dem <strong>Tumorzentrum</strong> <strong>Erfurt</strong> e.V.<br />
Mai 2012<br />
09.05.2012, 17.00 bis 20.00 Uhr<br />
Evangelisches Augustinerkloster <strong>Erfurt</strong><br />
Symposium „Aktuelle Diagnostik und Therapie des Magenkarzinoms“<br />
<strong>Tumorzentrum</strong> <strong>Erfurt</strong> e.V.<br />
Juni 2012<br />
13.06.2012, 17.00 bis 20.00 Uhr<br />
Evangelisches Augustinerkloster <strong>Erfurt</strong><br />
22. <strong>Erfurt</strong>er Fortbildung Hämatologie und Onkologie<br />
<strong>Tumorzentrum</strong> <strong>Erfurt</strong> e.V.<br />
08. bis 09.06.2012<br />
Besprechungsraum der Klinik für Allgemein- und Viszeralchirurgie,<br />
HELIOS Klinikum <strong>Erfurt</strong><br />
Aufbaukurs Ultraschalldiagnostik im Kopf- und Halsbereich<br />
(A-Bild- und B-Bild-Verfahren)<br />
HELIOS Klinikum <strong>Erfurt</strong>, Klinik für Hals-, Nasen- und Ohrenheilkunde,<br />
Plastische Operationen<br />
September 2012<br />
26.09.2012, 17.00 bis 20.00 Uhr<br />
Evangelisches Augustinerkloster <strong>Erfurt</strong><br />
Symposium „Gynäkologische Onkologie“<br />
<strong>Tumorzentrum</strong> <strong>Erfurt</strong> e.V. in Zusammenarbeit mit der Klinik für<br />
Frauenheilkunde und Geburtshilfe, HELIOS Klinikum <strong>Erfurt</strong><br />
■ Seite 36 ■ JOURNAL 01/2005 02/2011
Oktober 2012<br />
13.10.2012, 9.00 bis 14.00 Uhr<br />
HELIOS Klinikum <strong>Erfurt</strong>, Auditorium<br />
4. <strong>Erfurt</strong>er Dermatologische Herbsttagung<br />
Klinik für Hautkrankheiten und Allergologie, HELIOS Hauttumorzentrum<br />
<strong>Erfurt</strong>, HELIOS Klinikum <strong>Erfurt</strong> in Zusammenarbeit mit dem<br />
<strong>Tumorzentrum</strong> <strong>Erfurt</strong> e.V.<br />
November 2012<br />
02. bis 03.11.2012<br />
Haus Hainstein Eisenach<br />
25. Onkologische Konferenz<br />
<strong>Tumorzentrum</strong> <strong>Erfurt</strong> e.V. in Kooperation mit der Medizinisch-<br />
Wissenschaftlichen Gesellschaft <strong>Erfurt</strong> e.V.<br />
09. bis 10.11.2012<br />
Besprechungsraum der Klinik für Allgemein- und Viszeralchirurgie,<br />
HELIOS Klinikum <strong>Erfurt</strong><br />
Abschlusskurs Ultraschalldiagnostik im Kopf- und Halsbereich<br />
(A-Bild- und B-Bild-Verfahren)<br />
HELIOS Klinikum <strong>Erfurt</strong>, Klinik für Hals-, Nasen- und Ohrenheilkunde,<br />
Plastische Operationen<br />
22. bis 25.11.2012<br />
Frau-Mutter-Kindzentrum, HELIOS Klinikum <strong>Erfurt</strong><br />
Aufbaukurs Pädiatrische Ultraschalldiagnostik Abdomen,<br />
Harntrakt, Genitale<br />
HELIOS Klinikum <strong>Erfurt</strong>, Klinik für Kinder- und Jugendmedizin<br />
KONTAKTADRESSEN:<br />
Medizinisch-wissenschaftliche Gesellschaft <strong>Erfurt</strong> e.V.<br />
Sekretär Priv.-Doz. Dr. med. Klaus Hamm<br />
Nordhäuser Straße 74 · 99089 <strong>Erfurt</strong><br />
Telefon: 03 61 / 7 81-67 18<br />
Telefax: 03 61 / 7 81-67 19<br />
e-Mail: klaus.hamm@helios-kliniken.de<br />
www.mwg-erfurt.de<br />
HELIOS Klinikum <strong>Erfurt</strong><br />
Pressesprecherin Sylvia Kreyßel-Minar<br />
Nordhäuser Straße 74 · 99089 <strong>Erfurt</strong><br />
Telefon: 03 61 / 7 81-10 36<br />
Telefax: 03 61 / 7 81-10 32<br />
e-Mail: sylvia.kreyssel-minar@helios-kliniken.de<br />
www.helios-kliniken/erfurt<br />
<strong>Tumorzentrum</strong> <strong>Erfurt</strong> e.V.<br />
Geschäftsführer Dr. Hubert Göbel<br />
Nordhäuser Straße 74 · 99089 <strong>Erfurt</strong><br />
Telefon: 03 61 / 7 81-48 06<br />
Telefax: 03 61 / 7 81-48 03<br />
e-Mail: hubert.goebel@helios-kliniken.de<br />
www.tumorzentrum-erfurt.de<br />
JOURNAL 02/2011<br />
■ ANGEBOTE DES<br />
TUMORZENTRUM ERFURT e.V.<br />
KONSILARDIENSTE<br />
• Interdisziplinäres onkologisches Konsil<br />
Jeden Mittwoch, 7.30 Uhr, Demo-Raum C 1.400 des Instituts<br />
für bildgebende Diagnostik, Hauptgebäude 1. OG,<br />
HELIOS Klinikum <strong>Erfurt</strong>, Nordhäuser Straße 74<br />
Anmeldungen über Telefon 03 61 / 7 81-48 02<br />
Leitung: Prof. Dr. Herold / Prof. Dr. Scharf<br />
Jeder Arzt kann seine onkologischen Fälle persönlich einem<br />
Gremium von Experten aller Fachdisziplinen vorstellen.<br />
Am Ende der (kostenfreien) Beratung erhält er eine<br />
konkrete Therapieempfehlung. Zu jeder Fallbesprechung<br />
wird ein Protokoll angefertigt, das dem vorstellenden Arzt<br />
und eventuellen mitbehandelnden Ärzten zugeht.<br />
• Telefonischer Konsilardienst<br />
Unkompliziertes Vermitteln von Kontakten zu den<br />
speziellen onkologischen Ansprechpartnern aller Fachgebiete<br />
f www.tumorzentrum.de<br />
ONKOLOGISCHE LEITLINIEN<br />
Hilfestellung bei der Umsetzung der aktuellen Diagnose-,<br />
Therapie- und Nachsorgeleitlinien der Deutschen<br />
Krebsgesellschaft und der medizinischen Fachgesellschaften.<br />
In Ergänzung und zur praktischen Durchführung werden<br />
diese bei Bedarf für die speziellen regionalen Bedingungen<br />
adaptiert.<br />
KONTAKTE ZU SELBSTHILFEGRUPPEN UND<br />
HOSPIZDIENSTEN IN DER REGION<br />
PSYCHOLOGISCHE BETREUUNG<br />
Betreuungsangebote für stationäre Patienten des HELIOS<br />
Klinikum <strong>Erfurt</strong> sowie für Ärzte und Pflegepersonal.<br />
FORT- UND WEITERBILDUNG<br />
• Ärzte<br />
• Krankenschwestern und -pfleger<br />
• Sozialdienste<br />
DOKUMENTATION<br />
• Klinische Tumordokumentation<br />
In Erfüllung des Qualitätssicherungsauftrages des Sozialgesetzbuches<br />
(SGB V) wird für jeden Patienten der gesamte<br />
Krankheitsverlauf nach anerkannten Regeln (Tumorbasisdokumentation)<br />
dokumentiert. Die Unterlagen stehen<br />
dem Patienten und ihren behandelnden Ärzten zur Verfügung.<br />
Im Einzelfall (bei Umzug, Arztwechsel, Verlust von<br />
Originalunterlagen) sind sie für den Arzt eine unschätzbare<br />
Hilfe.<br />
■ Seite 37 ■
• Gemeinsames Krebsregister der neuen<br />
Bundesländer<br />
Epidemiologisch relevante Daten werden entsprechend<br />
geltender Gesetze an das Gemeinsame Krebsregister der<br />
neuen Bundesländer weitergegeben.<br />
Mehr als 95 % der Meldungen des Einzugsgebietes kommen<br />
vom <strong>Tumorzentrum</strong>. Diese Daten werden regelmäßig<br />
mit den amtlichen Sterbedaten abgeglichen und stehen<br />
dem meldenden Einrichtungen zur Verfügung.<br />
SERVICE<br />
• Unterstützung der Nachbetreuung,<br />
Erinnerungsfunktion<br />
Auf persönlichen Wunsch werden Patienten (und ihre betreuenden<br />
Ärzte) an vereinbarte bzw. vergessene Nachsorgetermine<br />
erinnert.<br />
• Statistiken für Krankenhäuser und Praxen<br />
Erstellung von Übersichten, Leistungsstatistiken und<br />
Überlebenszeitanalysen für die von der jeweiligen Einrichtung<br />
betreuten Patienten.<br />
• Informationen<br />
Kostenlose Bereitstellung von Tumor-Nachsorgepässen<br />
und Informationsmaterialien für Patienten, Ärzte, Pflegepersonal<br />
und Sozialdienste<br />
■ HIER ERREICHEN SIE UNS<br />
HELIOS Klinikum <strong>Erfurt</strong> GmbH<br />
Haus 8, Nordhäuser Straße 74, 99089 <strong>Erfurt</strong><br />
Telefon: 03 61 / 7 81-48 02<br />
Telefax: 03 61 / 7 81-48 03<br />
E-Mail: tuz@tumorzentrum-erfurt.de<br />
Homepage: http://www.tumorzentrum-erfurt.de<br />
Geschäftsführer: Dr. rer. nat. Hubert Göbel<br />
■ WISSENSCHAFTLICHER BEIRAT<br />
Prof. Dr. med. Hartwig Kosmehl (Vorsitzender)<br />
Chefarzt, Institut für Pathologie, HELIOS Klinikum <strong>Erfurt</strong><br />
Telefon: 03 61 / 7 81-27 50<br />
Adjunct Professor Dr. med. Rainer Bonnet M.D.<br />
Dpt. of Medicine, Loma Linda Univ., California<br />
Chefarzt, Klinik für Pneumologie, Zentralklinik Bad Berka<br />
Telefon: 03 64 58 / 5 15 00<br />
Dr. med. Karl-Matthias Deppermann<br />
Chefarzt, 1. Medizinische Klinik, Thoraxzentrum,<br />
HELIOS Klinikum <strong>Erfurt</strong>,<br />
Telefon: 03 61 / 7 81-25 80<br />
Michael Domrös<br />
Leiter der Landesvertretung Thüringen<br />
Verband der Ersatzkassen e.V. (vdek)<br />
Lucas-Cranach-Platz 2, 99099 <strong>Erfurt</strong><br />
Telefon: 03 61 / 4 42 52 11<br />
Dr. med. Alexander Fichte<br />
Urologe, Geschwister-Scholl-Straße 6, 99085 <strong>Erfurt</strong><br />
Telefon: 03 61 / 6 43 73 03<br />
Dr. med. Michael Glatzel<br />
Designierter Chefarzt, Klinik für Strahlentherapie und<br />
Radioonkologie, HELIOS Klinikum <strong>Erfurt</strong>,<br />
Telefon: 03 61 / 7 81-24 00<br />
Priv.-Doz. Dr. med. Klaus Hamm<br />
Leiter der Abteilung Stereotaktische Neurochirurgie und<br />
Radiochirurgie, HELIOS Klinikum <strong>Erfurt</strong><br />
Telefon: 03 61 / 7 81-67 18<br />
Prof. Dr. med. Udo B. Hoyme<br />
Direktor, Klinik für Frauenheilkunde und Geburtshilfe,<br />
HELIOS Klinikum <strong>Erfurt</strong><br />
Telefon: 03 61 / 7 81-40 00<br />
Markus Klaus<br />
Leiter des Fachbereichs Verhandlungsstrategie KH/Reha,<br />
AOK PLUS – Die Gesundheitskasse für Sachsen und Thüringen,<br />
Samuel-Beck-Weg 4, 99097 <strong>Erfurt</strong>,<br />
Telefon: 03 61 / 65 32 38 12 41<br />
Dipl.-Med. Susanne Köhler<br />
Oberärztin, 1. Medizinische Klinik, Hämatologie und<br />
internistische Onkologie, HELIOS Kreiskrankenhaus<br />
Gotha-Ohrdruf,<br />
Telefon: 0 36 21 / 2 20-1 30<br />
Prof. Dr. med. Steffen Rosahl<br />
Chefarzt, Klinik für Neurochirurgie, HELIOS Klinikum <strong>Erfurt</strong><br />
Telefon: 03 61 / 7 81-22 60<br />
Prof. Dr. med. Axel Sauerbrey<br />
Chefarzt, Klinik für Kinder- und Jugendmedizin,<br />
HELIOS Klinikum <strong>Erfurt</strong><br />
Telefon: 03 61 / 7 81-45 00<br />
Priv.-Doz. Dr. med. Lutz-Dieter Schreiber<br />
Chefarzt, Chriurgische Abteilung, Hufeland Klinikum,<br />
Standort Bad Langensalza<br />
Telefon: 0 36 03 / 8 55-0<br />
Prof. Dr. med. Thomas Steiner<br />
Chefarzt, Klinik für Urologie,<br />
HELIOS Klinikum <strong>Erfurt</strong>,<br />
Telefon: 03 61 / 7 81-22 00<br />
Sie können die Arbeit<br />
des <strong>Tumorzentrum</strong> <strong>Erfurt</strong> e.V.<br />
durch Ihre Spende unterstützen!<br />
Sparkasse Mittelthüringen<br />
BLZ 820 510 00 · Konto-Nr. 130 123 609<br />
(Spenden sind steuerlich begünstigt!<br />
■ Seite 38 ■ JOURNAL 01/2005 02/2011
■ VORSTAND<br />
Prof. Dr. med. Albrecht Stier (Vorsitzender)<br />
Chefarzt, Klinik für Allgemein- und Viszeralchirurgie,<br />
HELIOS Klinikum <strong>Erfurt</strong>,<br />
Telefon: 03 61 / 7 81-23 30<br />
Prof. Dr. med. Michael Herold (Stellvertr. Vorsitzender)<br />
Chefarzt, 4. Medizinische Klinik, HELIOS Klinikum <strong>Erfurt</strong><br />
Telefon: 03 61 / 7 81-25 66<br />
Prof. Dr. med. Dirk Eßer<br />
Chefarzt, Klinik für Hals-, Nasen- und Ohrenheilkunde,<br />
HELIOS Klinikum <strong>Erfurt</strong><br />
Telefon: 03 61 / 7 81-21 00<br />
Prof. Dr. med. Rudolf A. Herbst<br />
Chefarzt, Klinik für Hautkrankheiten und Allergologie,<br />
HELIOS Klinikum <strong>Erfurt</strong>,<br />
Telefon: 03 61 / 7 81-43 00<br />
Prof. Dr. med. Hartwig Kosmehl<br />
Chefarzt, Institut für Pathologie, HELIOS Klinikum <strong>Erfurt</strong>,<br />
Telefon: 03 61 / 7 81-27 50<br />
Dr. med. Jörg Pertschy<br />
Chefarzt, Klinik für Allgemein- und Viszeralchirurgie,<br />
Katholisches Krankenhaus St. Nepomuk <strong>Erfurt</strong>,<br />
Telefon: 03 61 / 6 54-12 00<br />
Dr. med. Jörg Weniger<br />
Hämatologe und internistischer Onkologe,<br />
Geschwister-Scholl-Straße 6, 99085 <strong>Erfurt</strong><br />
Telefon: 03 61 / 5 66 78 19<br />
IMPRESSUM<br />
ISSN 1868-291X (Print-Ausgabe)<br />
ISSN 1868-2928 (Internet)<br />
■ Herausgeber:<br />
<strong>Tumorzentrum</strong> <strong>Erfurt</strong> e.V.<br />
■ Redaktion:<br />
Prof. Dr. med. Hartwig Kosmehl · Dr. rer. nat. Hubert Göbel<br />
■ Redaktionsbüro und Versand:<br />
<strong>Tumorzentrum</strong> <strong>Erfurt</strong> e.V.<br />
Nordhäuser Straße 74 · 99089 <strong>Erfurt</strong><br />
Telefon: 03 61 / 7 81-48 02 · Telefax: 03 61 / 7 81-48 03<br />
E-Mail: tuz@tumorzentrum-erfurt.de<br />
■ Layout, Satz und Druck:<br />
Handmann Werbung GmbH <strong>Erfurt</strong><br />
■ Hinweis:<br />
Das <strong>Tumorzentrum</strong> <strong>Erfurt</strong> erstellt die Artikel nach bestem<br />
Wissen und Gewissen. Die Verantwortung für den Inhalt der<br />
medizinischen und wissenschaftlichen Beiträge obliegt den<br />
Autoren. Sie stellen keine Handlungsempfehlungen für den<br />
individuellen Fall dar.
<strong>Tumorzentrum</strong> <strong>Erfurt</strong> e.V.<br />
Nordhäuser Straße 74<br />
99089 <strong>Erfurt</strong><br />
Telefon: 03 61 / 7 81-48 02<br />
Telefax: 03 61 / 7 81-48 03<br />
E-Mail: tuz@tumorzentrum-erfurt.de<br />
www.tumorzentrum-erfurt.de