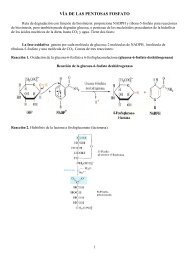
Estructura general de un aminoácido. Esta estructura es común a ...
Estructura general de un aminoácido. Esta estructura es común a ...
Estructura general de un aminoácido. Esta estructura es común a ...
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
Formación <strong>de</strong> <strong>un</strong> enlace<br />
peptídico por con<strong>de</strong>nsación. El<br />
grupo alfa-amino <strong>de</strong> <strong>un</strong><br />
<strong>aminoácido</strong> (el que tiene el R2),<br />
actúa como nucleófilo<br />
<strong>de</strong>splazando el grupo hidroxilo<br />
<strong>de</strong> otro <strong>aminoácido</strong> (el que tiene<br />
el R1) para formar <strong>un</strong> enlace<br />
covalente <strong>de</strong>nominado enlace<br />
peptídico (sombreado en gris).<br />
Al ser <strong>es</strong>ta reacción<br />
energéticamente <strong>de</strong>sfavorable<br />
los <strong>aminoácido</strong>s <strong>de</strong>ben ser<br />
activados previamente.<br />
<strong>Estructura</strong> <strong>de</strong>l pentapéptido seril-glicil-tirosinil-alanil-leucina o Ser-Gly-Tyr-Ala-Leu.<br />
Los péptidos se nombran empezando por el r<strong>es</strong>iduo amino-terminal que, por convención,<br />
se sitúa a la izquierda y terminan con el r<strong>es</strong>iduo carboxilo-terminal, a la <strong>de</strong>recha. Los<br />
enlac<strong>es</strong> peptídicos se mu<strong>es</strong>tran sombreados en gris y las ca<strong>de</strong>nas lateral<strong>es</strong> en rojo.