Acidos carboxílicos y derivados - Grupo de Sintesis Organica ...
Acidos carboxílicos y derivados - Grupo de Sintesis Organica ...
Acidos carboxílicos y derivados - Grupo de Sintesis Organica ...
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
Química Orgánica Tema 11. <strong>Acidos</strong> <strong>carboxílicos</strong> y <strong><strong>de</strong>rivados</strong><br />
www.sinorg.uji.es<br />
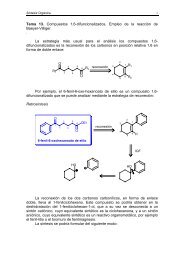
Alquilación <strong>de</strong> b-cetoesteres. Síntesis acetilacética.<br />
En la tabla que se da a continuación se compara la aci<strong>de</strong>z <strong>de</strong> algunos<br />
compuestos carbonílicos con la <strong>de</strong> los alcoholes y el agua. Como se acaba <strong>de</strong> explicar,<br />
el metileno central <strong>de</strong> los compuestos β-dicarbonílicos contiene hidrógenos mucho<br />
más ácidos que los hidrógenos <strong>de</strong>l agua y <strong>de</strong> los alcoholes. Esta mayor aci<strong>de</strong>z es el<br />
resultado <strong>de</strong> la mayor estabilidad <strong>de</strong>l correspondiente anión enolato, puesto que la base<br />
conjugada <strong>de</strong> los compuestos β-dicarbonílicos <strong>de</strong>slocaliza la carga negativa sobre dos<br />
grupos carbonilo en lugar <strong>de</strong> uno sólo.<br />
acido conjugado base conjugada pKa<br />
H O H<br />
agua<br />
OH<br />
15.7<br />
CH 3 O H<br />
metanol<br />
CH 3 CH 2 O H<br />
etanol<br />
O<br />
CH 3 C CH 3<br />
acetona<br />
O<br />
CH3 C OCH2CH3 acetato <strong>de</strong> etilo<br />
CH3CH2O C CH2 C OCH2CH3 malonato <strong>de</strong> dietilo<br />
O<br />
O<br />
CH 3 C CH 2<br />
O<br />
C<br />
O<br />
acetilacetato <strong>de</strong> etilo<br />
OCH 2CH 3<br />
CH 3O<br />
CH 3 CH 2 O<br />
O<br />
CH 2 C CH 3<br />
O<br />
CH 2 C OCH 2 CH 3<br />
O<br />
CH 3CH 2O C CH<br />
CH 3<br />
O<br />
C<br />
O<br />
C<br />
OCH 2CH 3<br />
OCH 2 CH 3<br />
El acetilacetato <strong>de</strong> etilo es semejante a la acetona pero con un grupo éster<br />
adicional, lo que explica su mayor aci<strong>de</strong>z. De hecho, el acetilacetato <strong>de</strong> etilo se pue<strong>de</strong><br />
convertir completamente en su base conjugada empleando el anión etóxido en el<br />
proceso <strong>de</strong> enolización. El enolato que se forma en este proceso es un buen nucleófilo<br />
y pue<strong>de</strong> reaccionar con un reactivo electrofílico, por ejemplo un haluro o tosilato <strong>de</strong><br />
alquilo estéricamente no impedido, mediante una reacción <strong>de</strong> tipo SN2.<br />
O<br />
C<br />
CH<br />
15.5<br />
15.9<br />
20<br />
25<br />
13<br />
11<br />
24