Algunas aplicaciones de las reacciones redox ... - DePa - UNAM
Algunas aplicaciones de las reacciones redox ... - DePa - UNAM
Algunas aplicaciones de las reacciones redox ... - DePa - UNAM
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
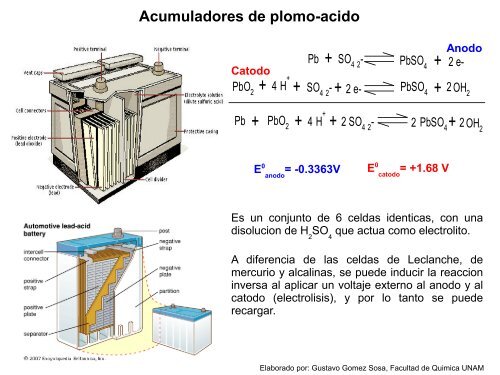
Acumuladores <strong>de</strong> plomo-acido<br />
Catodo<br />
PbO 2<br />
Pb SO 4 2 - PbSO 4<br />
H +<br />
+ 4 + SO -<br />
PbSO 4 2 + 2 e- 4 + 2 OH2 Pb PbO 2 H +<br />
+ + 2 e-<br />
+ + 4 + 2 2 + 2<br />
E 0<br />
= -0.3363V E<br />
anodo<br />
Anodo<br />
SO 4 2 - PbSO 4 OH 2<br />
0<br />
= +1.68 V<br />
catodo<br />
Es un conjunto <strong>de</strong> 6 celdas i<strong>de</strong>nticas, con una<br />
disolucion <strong>de</strong> H 2 SO 4 que actua como electrolito.<br />
A diferencia <strong>de</strong> <strong>las</strong> celdas <strong>de</strong> Leclanche, <strong>de</strong><br />
mercurio y alcalinas, se pue<strong>de</strong> inducir la reaccion<br />
inversa al aplicar un voltaje externo al anodo y al<br />
catodo (electrolisis), y por lo tanto se pue<strong>de</strong><br />
recargar.<br />
Elaborado por: Gustavo Gomez Sosa, Facultad <strong>de</strong> Quimica <strong>UNAM</strong>












![Síntesis de los isómeros de enlace [Co(NH3)5(ONO)]Cl2 y - DePa](https://img.yumpu.com/16368707/1/190x245/sintesis-de-los-isomeros-de-enlace-conh35onocl2-y-depa.jpg?quality=85)


