Algunas aplicaciones de las reacciones redox ... - DePa - UNAM
Algunas aplicaciones de las reacciones redox ... - DePa - UNAM
Algunas aplicaciones de las reacciones redox ... - DePa - UNAM
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
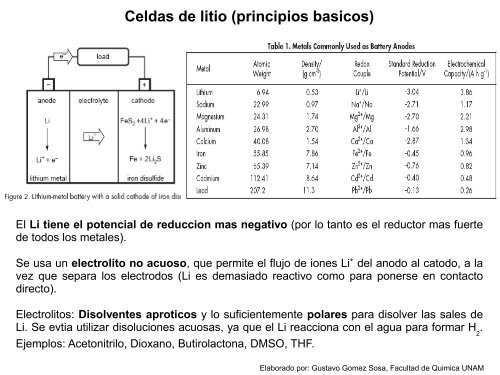
Celdas <strong>de</strong> litio (principios basicos)<br />
El Li tiene el potencial <strong>de</strong> reduccion mas negativo (por lo tanto es el reductor mas fuerte<br />
<strong>de</strong> todos los metales).<br />
Se usa un electrolito no acuoso, que permite el flujo <strong>de</strong> iones Li + <strong>de</strong>l anodo al catodo, a la<br />
vez que separa los electrodos (Li es <strong>de</strong>masiado reactivo como para ponerse en contacto<br />
directo).<br />
Electrolitos: Disolventes aproticos y lo suficientemente polares para disolver <strong>las</strong> sales <strong>de</strong><br />
Li. Se evtia utilizar disoluciones acuosas, ya que el Li reacciona con el agua para formar H 2 .<br />
Ejemplos: Acetonitrilo, Dioxano, Butirolactona, DMSO, THF.<br />
Elaborado por: Gustavo Gomez Sosa, Facultad <strong>de</strong> Quimica <strong>UNAM</strong>












![Síntesis de los isómeros de enlace [Co(NH3)5(ONO)]Cl2 y - DePa](https://img.yumpu.com/16368707/1/190x245/sintesis-de-los-isomeros-de-enlace-conh35onocl2-y-depa.jpg?quality=85)


