correction chapitre O8 : acidité des H en alpha
correction chapitre O8 : acidité des H en alpha
correction chapitre O8 : acidité des H en alpha
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
Exercice 1 : fait <strong>en</strong> TD<br />
Exercice 2 :<br />
Exercices MathSpé PC 2012-2013<br />
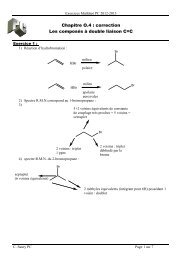
Chapitre O7 <strong>correction</strong><br />
Les composés carbonylés-partie 1<br />
1) A= CH3PPh3 + , Cl - ion phosphonium<br />
Ph3P CH2 2) Ylure correspondant :<br />
O<br />
O<br />
CH2 + + P<br />
Ph<br />
PPh3 Ph<br />
3)<br />
Ph<br />
La réaction est déplacée vers la droite du fait de la grande stabilité de la liaisonP=O.<br />
O<br />
O<br />
4)<br />
Exercice 3 :<br />
O<br />
CH<br />
+ + P<br />
PPh 3<br />
H 2O, H 2SO 4<br />
HBr<br />
Markovnikov<br />
+<br />
MgBr<br />
1)O 3<br />
C. Saury Page 1 sur 5<br />
Ph<br />
OH O<br />
Br<br />
2) Me 2S<br />
CrO 3<br />
Mg<br />
Et 2O<br />
Et 2O<br />
O<br />
MgBr<br />
Ph<br />
OH<br />
Ph<br />
O
O<br />
1)BH 3<br />
2)H 2O 2,OH -<br />
O<br />
+<br />
NaBH 4, EtOH<br />
MgBr<br />
HBr<br />
+<br />
1) BH3<br />
Exercices MathSpé PC 2012-2013<br />
H 2O, H 2SO 4<br />
HBr<br />
peroxy<strong>des</strong><br />
HBr<br />
Markovnikov<br />
HO<br />
2) H 2O 2, OH -<br />
Br<br />
MgBr<br />
OH<br />
CrO 3, H 2SO 4<br />
COOH<br />
OH O<br />
C. Saury Page 2 sur 5<br />
Et 2O<br />
CrO 3<br />
Br MgBr<br />
Mg<br />
OH<br />
O<br />
Br<br />
1) PPh 3<br />
2) NaH<br />
H 2SO 4<br />
PBr 3<br />
O<br />
Et 2O<br />
NaCN<br />
SN2<br />
PPh 3<br />
Br<br />
OH<br />
OH<br />
MCPBA<br />
Mg, Et 2O<br />
CN<br />
B 1<br />
MgBr<br />
O
Exercice 4 : fait <strong>en</strong> TD<br />
Exercice 5 : fait <strong>en</strong> TD<br />
Exercice 6 : fait <strong>en</strong> TD<br />
Exercice 7 :<br />
1) a/ D =<br />
b/on réduirait la fonction cétone pour obt<strong>en</strong>ir :<br />
O<br />
O<br />
Exercices MathSpé PC 2012-2013<br />
O<br />
O<br />
OH<br />
O<br />
C. Saury Page 3 sur 5<br />
OH<br />
2) a/ F =<br />
« oxydation douce » signifie que l’on obti<strong>en</strong>t l’aldéhyde et non l’acide carboxylique.<br />
b/ Réactif de Collins : CrO3 + pyridine <strong>en</strong> solvant CH2Cl2<br />
Réactif de Sarett : CrO3 dans pyridine<br />
Réactif de Corey : CrO3 dans pyridine + HCl : chromate de pyridinium<br />
c/En spectroscopique infrarouge, on voit l’apparition d’une bande int<strong>en</strong>se vers 1700cm -1 et la disparition<br />
de la bande large à 3300 cm -1 . En spectroscopie RMN du proton, on caractérise le proton de l’aldéhyde<br />
très déblindé : au <strong>des</strong>sus de 10 ppm.<br />
3) a/<br />
b/L’hydrolyse est effectuée <strong>en</strong> :<br />
-milieu acide pour éviter la précipitation <strong>des</strong> sels ROMgBr<br />
-milieu faiblem<strong>en</strong>t acide sinon on risque l’hydratation de l’alcène.<br />
4) a/<br />
H=<br />
O<br />
O<br />
O<br />
O<br />
O<br />
+<br />
O<br />
MbBr<br />
G=<br />
O<br />
OEt<br />
O<br />
O<br />
O<br />
O<br />
O<br />
hydrolyse<br />
b/ Les liaisons C=C et C=O sont conjuguées. Cela se traduit dans le spectre infrarouge de H par un<br />
vibration à un nombre d’onde plus faible.<br />
OH<br />
MgBr
5) a-b/<br />
H 3C I<br />
Exercices MathSpé PC 2012-2013<br />
SN2<br />
+ PPh 3 H3C PPh 3<br />
NaH<br />
H 2C PPh 3<br />
H 2C PPh 3<br />
c/ addition : attaque sur une double liaison avec rupture de la liaison double qui devi<strong>en</strong>t simple.<br />
Nucléophile : espèce riche <strong>en</strong> électron.<br />
d/<br />
b/<br />
6)<br />
O<br />
O<br />
+<br />
O H2C PPh3 O<br />
O<br />
J=<br />
O<br />
7) a/ mécanisme de la réaction de réduction :<br />
H 3C<br />
ipsénol<br />
Li<br />
O<br />
CH 3<br />
+<br />
H<br />
H<br />
H<br />
Al<br />
Me2HCO Me2HCO H<br />
OCHMe 2<br />
Al<br />
OH<br />
OCHMe 2<br />
Li<br />
C. Saury Page 4 sur 5<br />
I=<br />
2-Methyl-6-methyl<strong>en</strong>e-oct-7-<strong>en</strong>-4-ol<br />
c/L’ipsénol n’est pas optiquem<strong>en</strong>t actif car la réduction par les hydrures n’est pas stéréosélective.<br />
8) la réaction B → C est une réaction de protection.<br />
H 3C<br />
Exercice 8 :<br />
1) La bande à 1685 cm -1 correspond à la vibration de la liaison C=O. Elle est plus faible que dans la<br />
cyclop<strong>en</strong>tanone car la liaison est affaiblie par la conjugaison (avec C=C).<br />
H<br />
H<br />
O<br />
CH 3<br />
hydrolyse<br />
H<br />
Al<br />
H<br />
4<br />
OH<br />
Me Me<br />
H<br />
Al(OH) 4 -
Exercices MathSpé PC 2012-2013<br />
2) a)On a 10 électrons à placer dans le système . La BV est : et la HO : <br />
O<br />
b) Pour l’attaque d’un nucléophile, on étudie la BV de l’életcrophile (: on regarde le<br />
plus gros coeffici<strong>en</strong>t <strong>en</strong> valeur absolue : C4.<br />
c) Sous contrôle de charge, on regarde la plus grande charge positive : C2.<br />
d) L’addition nucléophile se fait sur la molécule plane de manière équiprobable sur les deux<br />
faces de la molécule. L’énol est <strong>en</strong>suite <strong>en</strong> équilibre avec les deux configurations du carbone <strong>en</strong><br />
<strong>alpha</strong> : on obti<strong>en</strong>t donc les 4 stéréoisomères.<br />
O (14)<br />
il y a trois hydrogènes aci<strong>des</strong> (<strong>en</strong> <strong>alpha</strong> du C=O)<br />
C. Saury Page 5 sur 5