Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
Devoir Surveillé MathSpé PC 2012-<strong>2013</strong><br />
DS 5<br />
<strong>samedi</strong> <strong>19</strong> <strong>janvier</strong> <strong>2013</strong>, <strong>4h</strong><br />
La calculatrice est autorisée pour cette épreuve. Toute classification périodique est interdite.<br />
La forme : veuillez à la propreté de votre copie, soignez votre écriture et encadrez les résultats<br />
importants.<br />
Le fond : repérez pour commencer les problèmes courts qui vous semblent les plus faciles. Les<br />
problèmes ont souvent des questions progressives, donc ne pas rester bloquer longtemps sur une<br />
question. Il faut absolument avoir lu l’ensemble de chaque problème avant la fin de l’épreuve. Soyez<br />
efficace dans vos réponses : ne répondez qu’aux questions posées (même si vous savez beaucoup plus de<br />
choses que ce qui est demandé) et ayez une rédaction claire.<br />
Un résultat sans unité ne verra l’attribution d’aucun point<br />
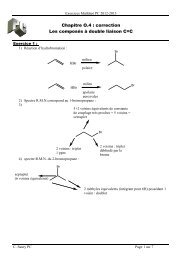
Problème 1 : Les terpènes<br />
Ce problème traite des terpènes qui représentent une famille de molécules naturelles de formule<br />
générale (C5H8)n et de leurs dérivés fonctionnalisés.<br />
Numéros atomiques : Z(H) = 1 ; Z(C) = 6 ; Z(N) = 7 ; Z(O) = 8<br />
Masses molaires (g.mol -1 ) : H : 1 ; C : 12 ; O : 16<br />
Domaines de déplacements chimiques de quelques espèces de protons (δ est exprimé en ppm par rapport<br />
au tétraméthylsilane (CH3)4Si pris comme référence).<br />
R désigne un radical aliphatique saturé.<br />
Types d’atomes d’hydrogène (en gras) Domaine de déplacements<br />
chimiques (δ/ppm)<br />
RCH3 (alkyle primaire) 0,8 à 1,0<br />
CH3-CR2-OH 1,1 à 1,3<br />
R2CH2 (alkyle secondaire) 1,2 à 1,4<br />
R3CH (alkyle tertiaire) 1,4 à 1,7<br />
R2C=CR-CH3 (H en position allylique) 1,6 à 1,9<br />
RCH2OH 3,3 à 3,9<br />
R2C=CH2 (alcène terminal) 4,6 à 5,0<br />
R2C=CHR 5,2 à 5,7<br />
ROH<br />
Table de nombres d’onde de quelques groupes fonctionnels<br />
0,5 à 5,0<br />
Liaison Type de composé Nombre d’onde (cm -1 ) Intensité<br />
C-H alcane 2800 – 3000 Forte<br />
=C-H alcène 3000 – 3100 Moyenne<br />
≡C-H alcyne 3300 Moyenne<br />
C-C alcane 1000 – 1250 Forte<br />
C=C alcène 1625 – 1685 Moyenne<br />
C≡C alcyne 2100 – 2250 Faible<br />
C-O alcool, éther, acide 1050 – 1450 forte<br />
C=O carbonyle 1700 – 1750 forte<br />
O-H alcool libre 3580 – 3670 fine et forte<br />
O-H alcool lié 3200 – 3400 large et forte<br />
C. Saury PC Page 1 sur 14
Devoir Surveillé MathSpé PC 2012-<strong>2013</strong><br />
A) Synthèse de l’alcool monoterpénique I :<br />
On fait réagir le bromoacétynylmagnésium sur la propanone. Après réaction et hydrolyse acide, on isole<br />
A.<br />
La structure du bromoacétynylmagnésium est la suivante :<br />
1. Proposer une méthode de synthèse du bromoacétynylmagnésium à partir de composés organiques et<br />
minéraux de votre choix. On donnera la structure des réactifs et du solvant des différentes étapes de cette<br />
préparation.<br />
2. Donner la structure de A et le mécanisme de sa formation.<br />
Par hydrogénation partielle A conduit à B. Sous action d’un rayonnement UV, le bromure d’hydrogène<br />
(en présence de peroxydes) agit sur B pour conduire à C de formule C5H11OBr dont le spectre RMN est<br />
donné ci-après.<br />
3. Quel catalyseur utiliser pour l’obtention de B ?<br />
4. Donner la structure de C et interpréter le spectre RMN 1 H.<br />
5. Donner le mécanisme du passage de B à C.<br />
6. La déshydratation intramoléculaire de C en milieu acide conduit à un mélange de deux isomères de<br />
position D et E. donner la structure de ces deux isomères et expliquer pourquoi l’un des deux (D) est<br />
obtenu majoritairement.<br />
On forme un composé organomagnésien dérivé de D. Celui-ci est opposé au méthanal. Après réaction,<br />
hydrolyse et purification on obtient F. On transforme ensuite la fonction alcool de F en dérivé<br />
monochloré G.<br />
7. Donner les formules semi-développées de F et G.<br />
8. Donner un réactif permettant de passer de F à G. écrire l’équation bilan de la réaction. Expliquer<br />
notamment pourquoi le chlorure d’hydrogène ne permet pas de réaliser efficacement cette<br />
transformation.<br />
9. En justifiant la réponse, représenter le stéréoisomère de I de configuration (R).<br />
L’action de l’organomagnésien issu de G sur la butènone (composé H) conduit après hydrolyse et<br />
purification au composé I recherché.sous forme de racémique et d’un isomère J.<br />
10. Dans cette réaction, l’organomagnésien joue-t-il le rôle de nucléophile ou d’électrophile ? Justifier.<br />
11. Montrer à partir du modèle de la mésomérie que la butènone présente deux sites électrophiles (l’atome<br />
de carbone de la fonction carbonyle noté 1 et un autre atome noté 2).<br />
Question 5/2 uniquement : Quel est l’isomère J qui accompagne la formation de I ?<br />
MgBr<br />
C. Saury PC Page 2 sur 14<br />
OH
Devoir Surveillé MathSpé PC 2012-<strong>2013</strong><br />
On donne pour H les énergies des orbitales frontières (plus haute occupée HO et plus basse vacante BV)<br />
ainsi que les coefficients des orbitales moléculaires correspondant aux atomes de carbone numérotés 1<br />
et 2 .<br />
HO BV<br />
Energies <br />
Coefficient atome 1 0,01 -0,55<br />
Coefficient atome 2 -0,58 0,67<br />
12. Une analyse orbitalaire permet-elle de justifier l’obtention préférentielle de I ? Justifier<br />
soigneusement la réponse.<br />
B) Réactivité du nérol<br />
Le nérol est un monoterpène naturel, de formule topologique :<br />
On réalise le mode opératoire suivant :<br />
Dans un ballon de 50 mL, on introduit 200 mg de nérol, 10 mL de dichlorométhane (CH2Cl2) et 45 mg<br />
d’acide paratoluènesulfonique monohydraté (noté TsOH,H2O). On agite le milieu à température<br />
ambiante pendant une heure.<br />
On introduit alors 25 mL d’une solution saturée d’hydrogénocarbonate de sodium (NaHCO3).<br />
On place le mélange réactionnel dans une ampoule à décanter et on extrait la phase organique avec 2<br />
fois 20 mL de diéthyléther (C2H5-O-C2H5).<br />
Les phases éthérées sont rassemblées, lavées à l’eau, puis séchées et enfin le mélange de produits est<br />
séparé du solvant.<br />
On recueille un mélange de trois produits qui sont ensuite séparés.<br />
nérol<br />
OH<br />
Ts-OH<br />
C. Saury PC Page 3 sur 14<br />
OH<br />
C H 2C l 2 OH<br />
1<br />
-terpinéol<br />
+ +<br />
2<br />
limonène<br />
3<br />
terpinolène<br />
20 % 35 % 45 %<br />
Formation de 1, 2 et 3 :<br />
12. Donner la formule topologique du carbocation non cyclique A qui se forme par action de Ts-OH<br />
(acide soluble en milieu organique) sur le nérol.<br />
13. Proposer un mécanisme pour cette étape.<br />
14. Expliquer pourquoi le carbocation A évolue vers la formation d’un carbocation cyclique B.<br />
15. Proposer un mécanisme pour le passage de A à B.<br />
16. À partir de B, proposer des mécanismes de formation des composés 1, 2 et 3.<br />
17. À quelles familles de réactions appartiennent respectivement ces trois réactions.<br />
18. Justifier que l’on obtienne plus de terpinolène que de limonène.
Devoir Surveillé MathSpé PC 2012-<strong>2013</strong><br />
Analyse du mode opératoire<br />
<strong>19</strong>. Quel est le rôle de l’ajout de la solution d’hydrogénocarbonate de sodium saturée ?<br />
20. Pourquoi faut-il extraire deux fois avec 20 mL d’éther plutôt qu’une seule fois avec 40 mL ?<br />
21. Quel est le rôle du lavage de la phase éthérée à l’eau ?<br />
22. En quoi consiste le séchage de la phase éthérée ?<br />
23. Quel appareil utilise-t-on pour séparer le mélange final du solvant ?<br />
Amélioration de la sélectivité<br />
La synthèse précédente est très peu sélective.<br />
On reprend le même protocole expérimental en remplaçant le dichlorométhane (CH2Cl2) par le<br />
nitrométhane (CH3-NO2). On isole alors 175 mg d’un unique produit, noté D.<br />
Le spectre R.M.N. de D montre, entre autres, les signaux suivants :<br />
δ = 1,15 ppm (singulet, 6 H) ; δ = 1,65 ppm (singulet, 3 H) ; δ = 5,40 ppm (signal mal résolu, 1 H).<br />
Le spectre infra-rouge de D est donné ci-après :<br />
Spectre infra-rouge de D (transmittance (%) en fonction du nombre d’onde (cm -1 ))<br />
24. Donner une formule de Lewis du nitrométhane et au besoin indiquer les différentes formules<br />
mésomères.<br />
25. Proposer une structure tridimensionnelle de cette molécule à l’aide de la théorie V.S.E.P.R.<br />
26. Identifier D parmi les composés 1, 2 ou 3, à l’aide des spectres infrarouge et R.M.N. et des tableaux<br />
fournis dans les données. En particulier, attribuer les trois signaux R.M.N.<br />
27. Définir la notion de sélectivité pour une réaction chimique. Donner des exemples de sélectivité.<br />
L’eau et le nitrométhane sont miscibles ce qui n’est pas le cas pour l’eau et le dichlorométhane.<br />
28. Le justifier.<br />
29. À l’aide de cette information, justifier l’obtention du seul produit D avec le nitrométhane comme<br />
solvant alors qu’avec le dichlorométhane comme solvant, on obtient un mélange des composés 1, 2 et 3.<br />
C. Saury PC Page 4 sur 14
Devoir Surveillé MathSpé PC 2012-<strong>2013</strong><br />
C) Etude de la molécule de limonène<br />
limonène<br />
Le limonène est un monoterpène, c'est-à-dire qu’il possède un squelette carboné provenant de la<br />
condensation de deux molécules d’isoprène.<br />
isoprène<br />
squelette carboné<br />
de l'isoprène<br />
30. Déterminer la formule brute du limonène et montrer qu’elle est en accord avec la formule brute<br />
générale des terpènes (C5H8)n en précisant la valeur de n.<br />
31. Montrer que la molécule de limonène possède un squelette carboné en accord avec la condensation<br />
des n molécules d’isoprène.<br />
32. Quel est le nom officiel de l’isoprène ?<br />
33. Combien de stéréoisomères présente la molécule de limonène. Les représenter en plaçant le cycle<br />
carboné dans le plan de la feuille et les nommer.<br />
Le limonène se trouve dans la peau des oranges et des citrons. On réalise deux solutions de limonène à<br />
0,5 g dans 100 mL de méthanol. Pour la première, le limonène est extrait de peaux d’oranges et pour la<br />
seconde, le limonène est extrait de peaux de citrons. On mesure le pouvoir rotatoire des deux solutions<br />
avec une cuve de longueur l = 1 dm, pour la raie D du sodium. On obtient pour la première solution α1 =<br />
+ 53° et pour la seconde α2 = + 34°.<br />
34. Avec quel appareil mesure-t-on le pouvoir rotatoire d’une solution ?<br />
35. Rappeler la loi de Biot.<br />
36. Le pouvoir rotatoire spécifique du (+)-limonène à 20 °C, pour la raie D du sodium vaut 20 = + D<br />
10,60 °.dm -1 .L.g -1 . Combien vaut le pouvoir rotatoire spécifique du (-)-limonène ?<br />
37. Calculer la composition (exprimée en pourcentage) en (+) et (-)-limonène de chacune des deux<br />
solutions précédentes.<br />
38. Peut-on prévoir qui de l’énantiomère R ou S du limonène est le (+)-limonène ?<br />
Problème 2 : synthèse de médicaments<br />
De nombreux médicaments ont été découverts par l’étude des propriétés biologiques des plantes.<br />
Un des exemples les plus connus est l’aspirine (extrait de l’écorce de saule). D’autres exemples célèbres<br />
sont la morphine ou le taxol, issus respectivement du pavot ou de l’écorce de l’if. L’apparition de<br />
cancers ou de bactéries résistantes aux médicaments courants a obligé les chimistes à trouver de<br />
nouvelles substances actives. Les chercheurs se sont alors davantage intéressés à la flore mais aussi à la<br />
faune et en particulier aux espèces marines.<br />
C. Saury PC Page 5 sur 14
A) synthèse de la dolastatine<br />
Devoir Surveillé MathSpé PC 2012-<strong>2013</strong><br />
L’étude du lièvre de mer Dolabella Auricularia a permis d’isoler plusieurs<br />
composés possédant une activité anticancéreuse très puissante : les<br />
dolastatines. Parmi l’ensemble de ces substances, deux produits sont<br />
maintenant en essai clinique pour le traitement de plusieurs types de<br />
cancer.L’objet de ce problème est la synthèse d’un fragment de ce produit<br />
nommé acide dolatriénoïque [figure 1(b)].<br />
O<br />
N H<br />
O<br />
N<br />
O<br />
N<br />
O<br />
N<br />
O<br />
N<br />
O<br />
O<br />
N<br />
N<br />
OMe O<br />
(a) Dolastatine 14<br />
O<br />
O<br />
N H 2<br />
C. Saury PC Page 6 sur 14<br />
O<br />
OH<br />
OMe OH<br />
*<br />
(b) Acide Dolatriénoïque<br />
1. Combien de stéréoisomères de configuration possède l’acide dolatriénoïque ? Justifier la réponse.<br />
La synthèse est réalisée à partir du lactate de méthyle protégé sous forme d’éther silylé [le groupe<br />
OtBDPS représente le groupe OSi(Ph) 2( t Bu)<br />
et n’intervient pas dans la synthèse].<br />
O<br />
OtBDPS<br />
O<br />
1) LiAlH 4, THF<br />
2) hydrolyse<br />
OH<br />
OtBDPS<br />
OtBDPS = O Si<br />
Au cours de la réaction, on voit sur le spectre infrarouge du mélange réactionnel disparaître une bande à<br />
1780 cm -1 et apparaître une bande très large vers 3500 cm -1 .<br />
2. Attribuez les bandes de vibration.<br />
Le composé A est alors traité par le chlorure de tosyle (Ts-Cl) dans le dichlorométhane. Après<br />
traitement, le produit obtenu est mis à réagir avec le chlorure d’allylmagnésium pour former après<br />
hydrolyse le produit B dont la formule brute est donnée ci-après.<br />
1) Tos TsCl<br />
-C l / C H2Cl2 A B (C22H30OSi)<br />
2) MgCl<br />
3) hydrolys e<br />
A<br />
*<br />
Ph<br />
Ph<br />
tBu
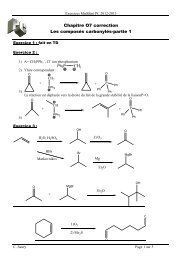
Devoir Surveillé MathSpé PC 2012-<strong>2013</strong><br />
Le spectre RMN H<br />
1<br />
du produit B montre la présence de 2 massifs situés l’un à 5,80 ppm et l’autre vers<br />
5,05 ppm, dont l’intégration donne respectivement 1 et 2 protons. On sait de plus que le composé B<br />
décolore l’eau de brome.<br />
3. Le chlorure de tosyle est le chlorure de l’acide 4-méthylbenzènesulfonique H3C C6H<br />
4 SO<br />
2Cl<br />
.<br />
Donner sa structure de Lewis.<br />
4. Par analogie avec la réaction d’acylation d’un alcool par un chlorure d’acyle, donner la structure<br />
du composé obtenu par réaction de A et de Ts-Cl.<br />
5. Le groupe OTs est un excellent groupe partant. Comment est-il possible de rendre compte<br />
simplement de cette propriété ?<br />
6. Donner la structure de B. Quelle est la réaction qui a eu lieu ? Avec quelle transformation connue<br />
peut-on faire l’analogie ?<br />
7. Interpréter les données RMN fournies, ainsi que la décoloration de l’eau de brome.<br />
Le composé B est alors traité par HBr en présence d’amorceurs radicalaires. Après traitement du<br />
mélange réactionnel, on isole un produit C qui ne décolore plus l’eau de brome.<br />
B<br />
C. Saury PC Page 7 sur 14<br />
HB r<br />
amorceur<br />
radicalaire<br />
8. Donner la structure de C. Justifier la régiosélectivité de la réaction.<br />
C est ensuite traité par la triphénylphosphine. Le composé D est alors obtenu.<br />
C<br />
PPh 3<br />
D :<br />
OtBDPS<br />
C<br />
PPh 3 , Br<br />
9. Sachant que le phosphore est situé dans la même colonne de la classification périodique que<br />
l’azote, indiquer quelle propriété de la triphénylphosphine est sollicitée dans la réaction de<br />
formation de D. Quel est le mécanisme de la réaction ? Justifier la réponse.<br />
10. Sur le spectre RMN proton de D, on peut remarquer un triplet dédoublé d’intégration égale à 2H.<br />
À quels protons correspond ce massif ? Comment pouvez-vous expliquer l’allure de ce massif ?<br />
D<br />
O<br />
F<br />
H<br />
Ph-Li<br />
?<br />
E<br />
O<br />
O<br />
OtBDPS<br />
OtBDPS<br />
G<br />
F<br />
H<br />
C<br />
O<br />
O<br />
O
G<br />
Devoir Surveillé MathSpé PC 2012-<strong>2013</strong><br />
OtBDPS OH O<br />
I<br />
NaH, CH3I, DMF<br />
J<br />
I est alors traité par l’hydrure de sodium et l’iodométhane, en solution dans le DMF (N,Ndiméthylméthanamide,<br />
solvant polaire non protogène). Le spectre IR de J ne présente plus de bande<br />
large à 3500 cm -1 .<br />
11. Proposer un mécanisme pour la réaction de formation de J à partir de I. L’hydrure de sodium est<br />
une base très forte. De plus, le DMF ne joue qu’un rôle de solvant dans la réaction. Donner la<br />
structure de J.<br />
12. Comment peut-on rendre compte de la très forte valeur du moment dipolaire du DMF ? Pourquoi<br />
a-t-on choisi le DMF comme solvant pour réaliser cette transformation ?<br />
L’ester J est alors réduit en alcool puis immédiatement oxydé en aldéhyde pour conduire à l’aldéhyde K.<br />
K<br />
J<br />
M<br />
1) réduction<br />
2) oxydation<br />
O<br />
?<br />
OCH 3<br />
L<br />
OtBDPS<br />
C. Saury PC Page 8 sur 14<br />
K<br />
OCH 3<br />
OtBDPS OCH3 OH<br />
OtBDPS OCH 3<br />
13. La synthèse proposée permet-elle l’obtention d’un seul stéréoisomère de N ?<br />
Malheureusement, lors de la réaction entre G et H, le composé I n’est obtenu qu’avec un rendement de<br />
seulement 30%. Il faut donc envisager une autre stratégie pour obtenir l’acide dolatriénoïque.<br />
Pas de données RMN /IR<br />
N<br />
M<br />
O<br />
I<br />
O<br />
OCH 3<br />
OMe<br />
H<br />
O<br />
OCH 3
Devoir Surveillé MathSpé PC 2012-<strong>2013</strong><br />
B) Synthèse d’un antibiotique<br />
La sarcomycine est un antibiotique dont la synthèse est proposée ci-dessous.<br />
Dans une première étape, le cyclopenta-1,3-diène réagit avec le prop-2-ènoate de méthyle selon une<br />
réaction de Diels-Alder pour donner le produit A.<br />
+<br />
O<br />
OMe<br />
14. Ecrire la structure plane du composé A sans s’intéresser ici à sa stéréochimie.<br />
15. Sous combien de stéréoisomères de configuration peut exister ce composé A,<br />
indépendamment de la façon dont il est obtenu dans cette synthèse ?<br />
16. Préciser, sur cet exemple, la notion de réaction stéréoselective.<br />
Le cyclopenta-1,3-diène est modélisé par le buta-1,3-diène dont les orbitales moléculaires, calculées par<br />
la méthode de Hückel, sont indiquées ci-après :<br />
E1 = + 1,618 1 = 0,37 1 + 0,60 2 + 0,60 3 + 0,37 4<br />
E2 = + 0,618 2 = 0,60 1 + 0,37 2 – 0,37 3 – 0,60 4<br />
E3 = - 0,618 3 = 0,60 1 – 0,37 2 – 0,37 3 + 0,60 4<br />
E4 = - 1,618 4 = 0,37 1 – 0,60 2 + 0,60 3 – 0,37 4<br />
Pour le prop-2-ènoate de méthyle, dont la numérotation est indiquée ci-dessous et pour lequel le méthyle<br />
est considéré comme un hétéroatome à 2 électrons, les orbitales moléculaires selon Hückel sont les<br />
suivantes :<br />
4<br />
C. Saury PC Page 9 sur 14<br />
1<br />
O<br />
3<br />
2<br />
5<br />
O<br />
6<br />
CH3 E1 = + 2,77 1 = 0,<strong>19</strong> 1 + 0,33 2 + 0,14 3 + 0,05 4 + 0,74 5 + 0,54 6<br />
E2 = + 1,93 2 = 0,48 1 + 0,45 2 + 0,32 3 + 0,17 4 + 0,08 5 – 0,65 6<br />
E3 = + 1,34 3 = 0,45 1 + 0,15 2 + 0,26 3 + 0,<strong>19</strong> 4 – 0,63 5 + 0,53 6<br />
E4 = + 1,00 4 = 0,58 1 + 0,00 2 – 0,58 3 – 0,58 4 + 0,00 5 + 0,00 6<br />
E5 = – 0,44 5 = 0,38 1 – 0,54 2 – 0,29 3 + 0,67 4 + 0,<strong>19</strong> 5 – 0,04 6<br />
E6 = – 1,60 6 = 0,24 1 – 0,61 2 + 0,63 3 – 0,39 4 + 0,14 5 – 0,02 6<br />
17. Pour chaque molécule mise en jeu, indiquer quelles sont les orbitales moléculaires la plus haute<br />
occupée HO et la plus basse vacante BV.<br />
18. Quelle est l’interaction HO-BV la plus importante ? Cette interaction sera la seule prise en<br />
compte dans la suite.<br />
A
Devoir Surveillé MathSpé PC 2012-<strong>2013</strong><br />
<strong>19</strong>. En admettant que le diène et le diènophile se rapprochent dans des plans parallèles, il y a deux<br />
modes d’approche possibles selon que le groupe –CO2CH3 du diènophile se place en vis-à-vis<br />
du cycle du diène ou à l’extérieur de celui-ci. Représenter les interactions orbitalaires<br />
principales dans les deux cas et montrer que l’une des deux approches est plus favorable que<br />
l’autre.<br />
20. En déduire le couple d’énantiomères majoritairement obtenu et le dessiner.<br />
Un certain nombre d’étape de synthèse permet d’obtenir le composé E :<br />
O<br />
La réaction de Diels-Alder est une réaction inversable.<br />
COOEt<br />
21. Indiquer le signe de l’entropie standard de réaction rS° pour une réaction de Diels-Alder.<br />
22. Cette réaction est généralement exothermique ; montrer qu’il existe une température au-delà<br />
de laquelle la variation d’enthalpie libre standard est positive.<br />
23. La rétro-Diels-Alder, effectuée sur le composé E donne deux produits : le composé F et du<br />
cyclopenta-1,3-diène. Donner la structure du composé F.<br />
Le produit F subit une saponification, puis après un passage en milieu acide, la sarcomycine est obtenue.<br />
C. Saury PC Page 10 sur 14<br />
E
Devoir Surveillé MathSpé PC 2012-<strong>2013</strong><br />
Problème 3 : Diagramme d’orbitales moléculaires pour une molécule<br />
diatomique<br />
Numéros atomiques :<br />
C (Z = 6) ; N (Z = 7) ; O (Z = 8) ; Mg (Z = 12) ; V (Z = 23) ; Cr (Z = 24) ; Cu (Z = 29)<br />
Masses atomiques :<br />
M(Mg) = 24,3 g.mol -1 ; M(Cu) = 63,5 g.mol -1<br />
Constante d’Avogadro : NA = 6,02.10 23 mol -1<br />
Coefficients de Slater :<br />
Groupe Contribution des autres électrons<br />
de l’électron niveaux niveau autress électrons du niveau n niveaux<br />
étudié n-2, n-3,.. n-1 s et p d f supérieurs<br />
ns et np 1,00 0,85 0,35 0 0 0<br />
nd 1,00 1,00 1,00 0,35 0 0<br />
nf 1,00 1,00 1,00 1,00 0,35 0<br />
1.- Rappeler la configuration électronique des atomes de carbone et d’oxygène.<br />
2.- Calculer l’énergie d’ionisation du carbone selon le modèle de Slater ; il est rappelé que l’énergie<br />
associée à une orbitale atomique caractérisée par le nombre quantique n se met sous la forme : E = -<br />
13,6. Z * ² en eV, Z* étant le numéro atomique effectif.<br />
n²<br />
3.- Construire le diagramme d’orbitales moléculaires pour la molécule O2 ; seules seront prises en<br />
compte les orbitales atomiques de valence.<br />
Remarque : dans le cas de la molécule de dioxygène, les orbitales atomiques se combinent deux à<br />
deux avec une bonne approximation ; en particulier, il n’y a pas lieu d’envisager d’interaction entre<br />
l’orbitale 2s de l’un des atomes et l’une des orbitales 2p de l’autre.<br />
4.- Cette molécule est-elle paramagnétique ou diamagnétique ?<br />
5.- Calculer les indices de liaison pour la molécule O2 et pour les ions moléculaires O2 - , O2 2- et O2 + ,<br />
sachant que l’indice de liaison, dans le cas d’une molécule homonucléaire diatomique, peut être<br />
défini simplement par<br />
2 antiliant<br />
liant N N où N l i ant et N antiliant sont respectivement les nombres<br />
d’électrons peuplant les orbitales moléculaires liantes et antiliantes.<br />
Justifier les valeurs expérimentales des longueurs de liaisons données ci-après :<br />
Espèce<br />
chimique<br />
O2 2- O2 - O2 O2 + ,<br />
d (en pm) 149 126 121 112<br />
Si les niveaux d’énergie des orbitales 2s et 2p sont trop proches, le type de diagramme, établi<br />
précédemment pour le dioxygène, n’est plus valable ; il faut envisager la construction d’un diagramme<br />
avec interaction s-p.<br />
C. Saury PC Page 11 sur 14
Devoir Surveillé MathSpé PC 2012-<strong>2013</strong><br />
Pour cela deux types de diagrammes doivent être envisagés : d’une part, celui sans interactions s-p<br />
construit précédemment (cas du dioxygène) et d’autre part, un diagramme limite où les orbitales<br />
atomiques 2s et 2p seraient dégénérées.<br />
6. Démontrer que si deux orbitales atomiques 2s et 2p sont dégénérées avec l’énergie E, toute<br />
combinaison linéaire de ces deux orbitales atomiques est encore solution de l’équation de<br />
Schrödinger avec la même énergie E.<br />
Remarque : l’équation de Schrödinger pour un système quelconque et une fonction le<br />
décrivant, sera simplement écrite HE ˆ , où Hˆ , opérateur hamiltonien correspondant, est<br />
linéaire.<br />
Dans le cas hypothétique d’un atome dont les orbitales atomiques 2s et 2p seraient dégénérées et en<br />
prenant l’axe x’Ox pou l’axe de liaison des deux atomes de la molécule, il est possible de remplacer,<br />
pour chaque atome, les orbitales atomiques 2s et 2px par :<br />
<br />
1 ( 2s2px)<br />
2<br />
' 1 ( 2s2px)<br />
2<br />
L’allure de ces nouvelles fonctions est la suivante :<br />
Le diagramme d’orbitales moléculaires, OM, donné ci-dessous, est construit sur la base des fonctions<br />
2py1, 2pz1, 1, ’1 pour l’atome A1 de gauche et 2py2, 2pz2, 2, ’2 pour l’atome A2 de droite. Un très<br />
faible recouvrement, pratiquement nul, est envisagé entre ’1 et ’2 : deux OM de symétrie ,<br />
pratiquement dégénérées, sont obtenues.<br />
7. Préciser pour chaque orbitale moléculaire i, les orbitales atomiques qui ont servi à la construire<br />
ainsi que sa symétrie ou .<br />
C. Saury PC Page 12 sur 14
Devoir Surveillé MathSpé PC 2012-<strong>2013</strong><br />
8.- Dans le « Document-Réponse » les deux diagrammes, celui sans interaction s-p (cas du dioxygène<br />
entre autres) (diagramme de gauche) et celui avec interaction s-p totale (cas étudié ci-dessus)<br />
(diagramme de droite), sont représentés.<br />
Il est admis qu’il y a une continuité entre ce deux diagrammes ; les niveaux moléculaires de<br />
correspondent de l’un à l’autre, ils sont corrélés.<br />
Les règles de correspondance sont les suivantes : l’orbitales moléculaire liante, de plus basse énergie,<br />
du diagramme de gauche, est corrélée avec l’orbitale moléculaire liante, de plus basse énergie, du<br />
diagramme de droite. Puis l’orbitale moléculaire liante immédiatement supérieure du diagramme de<br />
gauche est corrélée avec l’orbitale moléculaire liante immédiatement supérieure du diagramme de<br />
droite et ainsi de suite. Il en va de même pour les antiliantes, les liantes et les antiliantes.<br />
Compléter le schéma 1 du « Document-Réponse » en reliant par des traits les niveaux corrélés.<br />
9.- Mettre alors en évidence deux points de croisement des lignes de corrélation. En déduire qu’il y a a<br />
priori trois types de diagrammes d’orbitales moléculaire pour des molécules A2. Dans la réalité,<br />
seuls deux cas existent ; le cas avec interaction totale n’existe pas.<br />
10.- La molécule de diazote appartient au type intermédiaire. Donner son diagramme d’orbitales<br />
moléculaires et calculer l’indice de liaison.<br />
11.- Le diagramme d’orbitales moléculaires de la molécule de monoxyde de carbone CO, est le même<br />
que celui de la molécule de diazote (les niveaux des orbitales atomiques sont différents mais l’ordre<br />
des énergies des orbitales moléculaires est le même).<br />
a) Proposer un schéma de Lewis pour cette molécule en accord avec l’indice de liaison, et en<br />
faisant apparaître les éventuelles charges formelles.<br />
b) La molécule de monoxyde de carbone a des propriétés de ligand (ou coordinat). Se fixe-telle<br />
préférentiellement par le carbone ou par l’oxygène ?<br />
12.- Le monoxyde de carbone réagit avec les métaux de transition pour conduire à des complexes<br />
carbonyle. Ainsi, il est possible de préparer V(CO)6 et Cr(CO)6.<br />
a) Faire le décompte des électrons de valence intervenant dans ces deux espèces c’est-à-dire la<br />
somme des électrons de valence de l’élément de transition et des électrons apportés par les<br />
molécules de monoxyde de carbone.<br />
b) Quel est probablement le plus stable des deux complexes ? Pourquoi ?<br />
C. Saury PC Page 13 sur 14
Devoir Surveillé MathSpé PC 2012-<strong>2013</strong><br />
DOCUMENT – REPONSE<br />
C. Saury PC Page 14 sur 14