CHIMIE et COULEUR
CHIMIE et COULEUR
CHIMIE et COULEUR
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
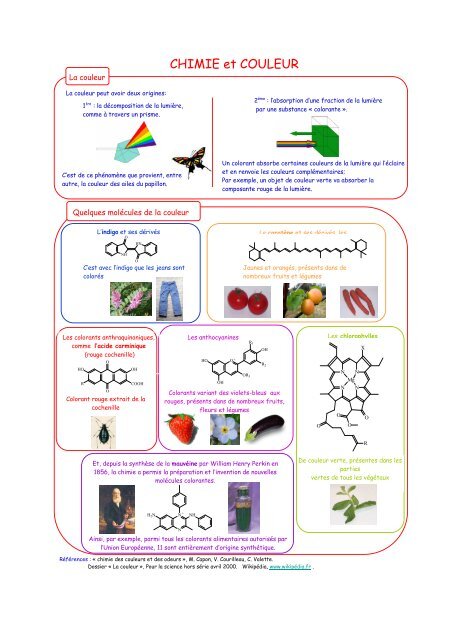
La couleur<br />
<strong>CHIMIE</strong> <strong>et</strong> <strong>COULEUR</strong><br />
La couleur peut avoir deux origines:<br />
1 ère : la décomposition de la lumière,<br />
comme à travers un prisme.<br />
2 ème : l’absorption d’une fraction de la lumière<br />
par une substance « colorante ».<br />
C’est de ce phénomène que provient, entre<br />
autre, la couleur des ailes du papillon.<br />
Un colorant absorbe certaines couleurs de la lumière qui l’éclaire<br />
<strong>et</strong> en renvoie les couleurs complémentaires;<br />
Par exemple, un obj<strong>et</strong> de couleur verte va absorber la<br />
composante rouge de la lumière.<br />
Quelques molécules de la couleur<br />
L’indigo <strong>et</strong> ses dérivés<br />
O<br />
NH<br />
HN<br />
C’est Et avec bien l’indigo d’autres que les encore!!! jeans sont<br />
colorés<br />
O<br />
Le carotène <strong>et</strong> ses dérivés, les<br />
Jaunes <strong>et</strong> orangés, présents dans de<br />
nombreux fruits <strong>et</strong> légumes<br />
Les colorants anthraquinoniques,<br />
comme l’acide carminique<br />
(rouge cochenille)<br />
HO<br />
R<br />
O<br />
O<br />
OH<br />
COOH<br />
Colorant rouge extrait de la<br />
cochenille<br />
Les anthocyanines<br />
HO<br />
OH<br />
O +<br />
OR 3<br />
R 1<br />
OH<br />
Colorants variant des viol<strong>et</strong>s-bleus aux<br />
rouges, présents dans de nombreux fruits,<br />
fleurs <strong>et</strong> légumes<br />
R 2<br />
O<br />
Les chlorophylles<br />
X<br />
N N<br />
Mg<br />
N N<br />
O<br />
O<br />
O<br />
R<br />
Et, depuis la synthèse de la mauvéine par William Henry Perkin en<br />
1856, la chimie a permis la préparation <strong>et</strong> l’invention de nouvelles<br />
molécules colorantes.<br />
De couleur verte, présentes dans les<br />
parties<br />
vertes de tous les végétaux<br />
H 2 N<br />
+<br />
N<br />
NH<br />
N<br />
Ainsi, par exemple, parmi tous les colorants alimentaires autorisés par<br />
l’Union Européenne, 11 sont entièrement d’origine synthétique.<br />
Références : « chimie des couleurs <strong>et</strong> des odeurs », M. Capon, V. Courilleau, C. Val<strong>et</strong>te.<br />
Dossier « La couleur », Pour la science hors série avril 2000. Wikipédia, www.wikipédia.fr .
<strong>CHIMIE</strong> <strong>et</strong> SAVEUR<br />
Épices <strong>et</strong> herbes aromatiques : aux sources du piquant<br />
Le piquant<br />
des piments<br />
Le piquant des<br />
aulx<br />
ail, oignon, échalote,<br />
ciboul<strong>et</strong>te<br />
Et d’autres<br />
poivre de tasmani, le poivre<br />
d’eau ou les zingibéracées<br />
comme le gingembre<br />
O<br />
O<br />
NH 2<br />
O<br />
O<br />
O<br />
O<br />
N<br />
H<br />
S<br />
OH<br />
alliinase<br />
S<br />
H<br />
O<br />
O<br />
HO<br />
Capsaicine : 16 000 000 scoville<br />
• Obtenus par les piments en effectuant<br />
la condensation enzymatique de<br />
vanillylamine <strong>et</strong> d’un acide gras ramifié<br />
<strong>et</strong> insaturé.<br />
• Sur l’échelle de Scoville, le piment le<br />
plus fort est mesuré à environ 600 000<br />
scoville, <strong>et</strong> la capsaicine pure à 16 000<br />
000 !<br />
S-alcèncystéine sulfoxide<br />
Sulfoxydes<br />
O<br />
• Libéré lorsque nous éminçons ces épices. Le<br />
mélange de la S-alk(en)ylcystéine sulfoxyde<br />
avec l’enzyme alliinase libère les sulfoxydes.<br />
• Au contact de l’air, l’allicine se dégrade<br />
rapidement. Il faut donc émincer l’ail au<br />
dernier moment pour en profiter pleinement !<br />
Les tanins du thé<br />
alliine<br />
O<br />
• Formation d’esters volatiles<br />
participant de façon très importante à<br />
l’arôme du vin :<br />
CH 3 -COOH + C 2 H 5 -OH => CH 3 -COO-<br />
C 2 H 5 + H 2 O<br />
• Tanin cédé par le bois au vin lors du<br />
vieillissement en fût de chêne.<br />
Aframodial<br />
(+E)-E-labda-8(17),12-<br />
dien-15,16-dial<br />
• Nous r<strong>et</strong>rouvons ces principes<br />
piquants dans de nombreuses espèces<br />
comme la cardamome.<br />
OH<br />
• Composition du thé :<br />
HO<br />
OH<br />
HO<br />
O<br />
OH<br />
TANINS 20 à 35%<br />
PROTEINES 20 à 30%<br />
CARBOHYDRATES 20 à 25%<br />
CAFFEINE 3 à 5%<br />
HO<br />
O<br />
HO<br />
O<br />
O<br />
HO<br />
HO<br />
O<br />
HO<br />
HO<br />
• Tanin : substance d’origine organique que l’on r<strong>et</strong>rouve dans<br />
pratiquement tous les végétaux, <strong>et</strong> dans toutes leurs parties<br />
(écorces, racines, feuilles, <strong>et</strong>c.), caractérisée par leur<br />
astringence (sensation de dessèchement en bouche)<br />
• Chimiquement parlant, ce sont des composés phénoliques<br />
précipitant les protéines.<br />
OH<br />
OH<br />
OH<br />
OH<br />
O<br />
OH<br />
OH<br />
OH<br />
O<br />
O<br />
HO<br />
O<br />
O<br />
n<br />
OH<br />
OH<br />
O<br />
OH<br />
OH<br />
OH<br />
OH<br />
OH<br />
Le vin : la fermentation du raisin<br />
• III ème millénaire avant Jésus-Christ : l’Égypte cultivait déjà des vignes <strong>et</strong> les chinois connaissait<br />
l’art de faire du vin.<br />
• 19 ème siècle : travaux de Pasteur pour percer les mystères de la fermentation alcoolique<br />
HO<br />
O<br />
OH<br />
OH<br />
Proanthocyanidines<br />
Les anthocyanidines<br />
• responsables des couleurs rose, rouge, mauve, viol<strong>et</strong> <strong>et</strong> bleu<br />
dans les fleurs, fruits, jus de fruits <strong>et</strong> vins<br />
• responsables aussi du taux d’astringence des fruits <strong>et</strong> des vins.<br />
• Aujourd’hui, les scientifiques ont identifié quelques 200 substances représentant environ 97 à 98%<br />
du vin.<br />
Processus de la fermentation<br />
alcoolique<br />
Gallotanin<br />
Plusieurs étapes de vinification<br />
• la limpidité, élimination des précipités du vin<br />
• le sulfitage, addition d’un antiseptique (SO 2 )<br />
• l’action de microorganismes : fermentations (bactéries pour la<br />
fermentation malolactique, levures pour la fermentation alcoolique,<br />
champignons lors du vieillissement)<br />
Vieillissement<br />
du vin<br />
Références : www.toildepices.com ; www.futura-sciences.com ; www.ansci.cornell.edu/plants/toxicagents/tannin ; www.wikipedia.org<br />
chauffage en milieu acide<br />
des proanthocyanidines
<strong>CHIMIE</strong> <strong>et</strong> AROME<br />
Pourquoi la chimie au service des arômes <br />
Odeur (nom féminin) : Impression que produisent certaines émanations sur l’odorat.<br />
REPRESENTATION SCHEMATIQUE<br />
DE LA CAVITE NASALE<br />
Arôme : désigne un parfum, une odeur agréable provenant d’essences d’origine<br />
végétale, animale ou chimique (Nom formé à partir d’un mot grec " arôma " qui<br />
signifie parfum).<br />
Essence ou huile essentielle : produits huileux, volatils <strong>et</strong> inflammables, d’origine<br />
végétale.<br />
Parmi elles, 2 familles principales : les terpènes <strong>et</strong> les<br />
esters.<br />
terpènes<br />
(obtenus par distillation d’une partie de la plante ou par synthèse chimique)<br />
http://www.frein<strong>et</strong>.org/creactif/blain/cm/2001/exposes/5sens2.jpg<br />
Furfural<br />
Citral<br />
Vanilline<br />
Eucalyptol<br />
α-pinène<br />
O<br />
O<br />
O<br />
OH<br />
OCH3<br />
H<br />
H<br />
O<br />
Graine torréfiée<br />
de café<br />
Écorce du citron<br />
C<br />
H O<br />
Gousse de vanille<br />
Eucalyptus, Laurier, Menthe<br />
Laurier, Citron, Menthe<br />
(+)-limonène<br />
CH 3<br />
H<br />
H 3 C CH 2<br />
Écorce d'orange, Citron<br />
(-)-limonène<br />
CH 3<br />
H<br />
H 3 C CH 2<br />
Menthe verte, Citron<br />
La vanilline<br />
d'origine naturelle<br />
coûte environ 250<br />
fois plus cher que<br />
la même molécule<br />
obtenue par<br />
synthèse !!!!!!!<br />
esters<br />
(présents dans la plante mais obtenus par<br />
synthèse chimique : l’estérification)<br />
2-éthyl-butyrate de<br />
méthyle<br />
O<br />
O<br />
CH3<br />
Ethanoate de 3-méthylbutyle<br />
O<br />
O<br />
Banane<br />
Exemple : Le LIMONÈNE<br />
Pomme<br />
•MACÉRATION des écorces d'orange dans de l'eau chaude pour faire<br />
éclater les cellules végétales pour libérer les composés organiques.<br />
•DISTILLATION : La phase gazeuse qui se dégage<br />
par chauffage contient de l'eau <strong>et</strong> des produits<br />
organiques dont le limonène. C<strong>et</strong>te phase est<br />
ensuite récupérée par condensation grâce au<br />
réfrigérant.<br />
•DÉCANTATION : le distillat<br />
récupéré précédemment<br />
contient 2 phases que l’on<br />
sépare grâce à une ampoule à<br />
décanter :<br />
•la phase organique<br />
(Le limonène)<br />
•la phase aqueuse.<br />
Huile essentielle , utilisée dans la parfumerie <strong>et</strong><br />
comme agent de saveur : saveur "spearmint"<br />
(dentifrice <strong>et</strong> chewing-gum)<br />
Eau aromatique, utilisée dans la<br />
cosmétique, dans l’alimentaire<br />
Estérification :<br />
Alcool + acide<br />
ester + H2O<br />
Parce que la chimie perm<strong>et</strong> de<br />
comprendre les arômes, <strong>et</strong> perm<strong>et</strong> de les<br />
reproduire pour que la vie soit plus<br />
aromatisée, odorante, parfumée !!!<br />
Références : http://lesaromes.free.fr/Pages/chimie.htm ; http://www.snv.jussieu.fr/vie/dossiers/aromes/nature-arome/aromes.htm ;<br />
http://www.educ.usherbrooke.ca/proj<strong>et</strong>s/fpt223-06/proj613/contenus.htm#odorat ; http://www.ac-orleans-tours.fr/physique/phyel/term/parf/ext.htm ;