Notice scientifique - Guerbet
Notice scientifique - Guerbet
Notice scientifique - Guerbet
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
R C P<br />
Xenetix 1/5<br />
RCP V 9 –08/2005<br />
Dénomination :<br />
XENETIX (Iobitridol)<br />
Titulaire d’enregistrement :<br />
s.a. CODALI - Avenue H. Dunant, 31 - 1140 Bruxelles<br />
Fabricant :<br />
<strong>Guerbet</strong> - BP 57400 – F-95943 Roissy CdG Cedex Situé 16, rue J. Chaptal / F-93600 Aulnay<br />
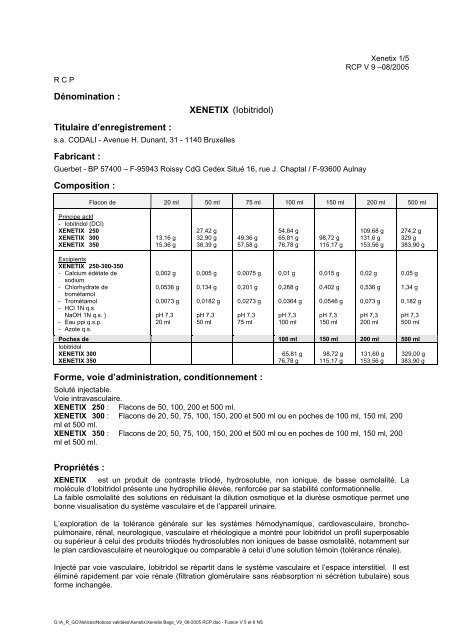
Composition :<br />
Flacon de 20 ml 50 ml 75 ml 100 ml 150 ml 200 ml 500 ml<br />
Principe actif<br />
- Iobitridol (DCI)<br />
XENETIX 250<br />
XENETIX 300<br />
XENETIX 350<br />
13,16 g<br />
15,36 g<br />
27,42 g<br />
32,90 g<br />
38,39 g<br />
49,36 g<br />
57,58 g<br />
54,84 g<br />
65,81 g<br />
76,78 g<br />
98,72 g<br />
115,17 g<br />
109,68 g<br />
131,6 g<br />
153,56 g<br />
274,2 g<br />
329 g<br />
383,90 g<br />
Excipients<br />
XENETIX 250-300-350<br />
- Calcium édétate de<br />
sodium<br />
- Chlorhydrate de<br />
trométamol<br />
- Trométamol<br />
- HCl 1N q.s.<br />
NaOH 1N q.s. }<br />
- Eau ppi q.s.p.<br />
- Azote q.s.<br />
0,002 g<br />
0,0536 g<br />
0,0073 g<br />
pH 7,3<br />
20 ml<br />
0,005 g<br />
0,134 g<br />
0,0182 g<br />
pH 7,3<br />
50 ml<br />
0,0075 g<br />
0,201 g<br />
0,0273 g<br />
pH 7,3<br />
75 ml<br />
0,01 g<br />
0,268 g<br />
0,0364 g<br />
pH 7,3<br />
100 ml<br />
0,015 g<br />
0,402 g<br />
0,0546 g<br />
pH 7,3<br />
150 ml<br />
0,02 g<br />
0,536 g<br />
0,073 g<br />
pH 7,3<br />
200 ml<br />
0,05 g<br />
1,34 g<br />
0,182 g<br />
pH 7,3<br />
500 ml<br />
Poches de 100 ml 150 ml 200 ml 500 ml<br />
Iobitridol<br />
XENETIX 300<br />
XENETIX 350<br />
65,81 g<br />
76,78 g<br />
98,72 g<br />
115,17 g<br />
131,60 g<br />
153,56 g<br />
329,00 g<br />
383,90 g<br />
Forme, voie d’administration, conditionnement :<br />
Soluté injectable.<br />
Voie intravasculaire.<br />
XENETIX 250 : Flacons de 50, 100, 200 et 500 ml.<br />
XENETIX 300 : Flacons de 20, 50, 75, 100, 150, 200 et 500 ml ou en poches de 100 ml, 150 ml, 200<br />
ml et 500 ml.<br />
XENETIX 350 : Flacons de 20, 50, 75, 100, 150, 200 et 500 ml ou en poches de 100 ml, 150 ml, 200<br />
ml et 500 ml.<br />
Propriétés :<br />
XENETIX est un produit de contraste triiodé, hydrosoluble, non ionique, de basse osmolalité. La<br />
molécule d’Iobitridol présente une hydrophilie élevée, renforcée par sa stabilité conformationnelle.<br />
La faible osmolalité des solutions en réduisant la dilution osmotique et la diurèse osmotique permet une<br />
bonne visualisation du système vasculaire et de l’appareil urinaire.<br />
L’exploration de la tolérance générale sur les systèmes hémodynamique, cardiovasculaire, bronchopulmonaire,<br />
rénal, neurologique, vasculaire et rhéologique a montré pour Iobitridol un profil superposable<br />
ou supérieur à celui des produits triiodés hydrosolubles non ioniques de basse osmolalité, notamment sur<br />
le plan cardiovasculaire et neurologique ou comparable à celui d’une solution témoin (tolérance rénale).<br />
Injecté par voie vasculaire, Iobitridol se répartit dans le système vasculaire et l’espace interstitiel. Il est<br />
éliminé rapidement par voie rénale (filtration glomérulaire sans réabsorption ni sécrétion tubulaire) sous<br />
forme inchangée.<br />
G:\A_R_GC\<strong>Notice</strong>s\<strong>Notice</strong>s validées\Xenetix\Xenetix Bags_V9_08-2005 RCP.doc - Fusion V 5 et 6 NS
Xenetix 2/5<br />
RCP V 9 –08/2005<br />
En cas d’insuffisance rénale, l’élimination se produit par voie biliaire et est ralentie. Iobitridol est<br />
dialysable.<br />
Indications :<br />
Chez l’adulte et chez l’enfant :<br />
XENETIX 250 :<br />
• phlébographie<br />
• tomodensitométrie du corps entier<br />
• angiographie numérisée par voie intra-artérielle<br />
XENETIX 300 - XENETIX 350 :<br />
• urographie intraveineuse<br />
• tomodensitométrie crânienne et corps entier<br />
• angiographie numérisée par voie intraveineuse<br />
• artériographie<br />
• angiocardiographie<br />
Posologie et mode d’emploi :<br />
Les doses doivent être adaptées à l’examen et aux territoires à opacifier ainsi qu’au poids et à la fonction<br />
rénale du sujet notamment chez l’enfant.<br />
Posologie moyenne recommandée :<br />
XENETIX 250 :<br />
Indications Dose moyenne ml/kg Volume total (mini.-maxi.) ml<br />
Phlébographie 2.6 150-220<br />
Tomodensitométrie du thorax 2.0 95-170<br />
Angiographie numérisée par voie<br />
intra-artérielle<br />
3.1 75-360<br />
XENETIX 300 :<br />
Indications Dose moyenne ml/kg Volume total (mini.-maxi.) ml<br />
Urographie en injection<br />
intraveineuse rapide :<br />
intraveineuse lente :<br />
Tomodensitométrie<br />
- crâne<br />
- corps entier<br />
1.2<br />
1.6<br />
1.4<br />
1.9<br />
50-100<br />
100<br />
20-100<br />
20-150<br />
Angiographie numérisée<br />
par voie intraveineuse 1.7 40-270<br />
Artériographie<br />
- cérébrale<br />
- membres inférieurs<br />
1.8<br />
2.8<br />
45-210<br />
85-300<br />
Angiocardiographie 1.1 70-125<br />
G:\A_R_GC\<strong>Notice</strong>s\<strong>Notice</strong>s validées\Xenetix\Xenetix Bags_V9_08-2005 RCP.doc - Fusion V 5 et 6 NS
Xenetix 3/5<br />
RCP V 9 –08/2005<br />
XENETIX 350 :<br />
Indications Dose moyenne ml/kg Volume total (mini.-maxi.) ml<br />
Urographie intraveineuse 1 50-100<br />
Tomodensitométrie<br />
- crâne<br />
- corps entier<br />
1<br />
1.8<br />
40-100<br />
90-180<br />
Angiographie numérisée par<br />
voie intraveineuse 2.1 95-250<br />
Artériographie<br />
- périphérique<br />
- membres inférieurs<br />
- abdominale<br />
Angiocardiographie<br />
- adultes<br />
- enfants<br />
2.2<br />
1.8<br />
3.6<br />
1.9<br />
4.6<br />
105-205<br />
80-190<br />
155-330<br />
65-270<br />
10-130<br />
Contre-indications :<br />
• Hyperthyroïdie manifeste<br />
• En l’absence d’études spécifiques, la myélographie n’est pas une indication de XENETIX.<br />
• Hypersensibilité à l'un des composants de la préparation.<br />
Effets indésirables :<br />
Chez certains patients prédisposés atteints de goitre, surtout polynodulaire ou présentant une<br />
hyperthyroïdie asymptomatique, l’injection de produit de contraste peut entraîner une hyperthyroïdie,<br />
exceptionnellement une thyrotoxicose (attention aux personnes âgées). Les manifestations cliniques<br />
peuvent apparaître plusieurs semaines après l’injection du produit de contraste.<br />
De façon générale, l’absorption d’iode par la glande thyroïde sera réduite pendant au moins 4 semaines.<br />
Pendant cette période, les tests thyroïdiens peuvent être perturbés.<br />
Chez le nouveau-né on peut observer une hypothyroïdie transitoire.<br />
Des manifestations bénignes d’intolérance peuvent survenir précocement ou tardivement.<br />
Elles peuvent être isolées ou associées et de type :<br />
- neurosensoriel : sensation de chaleur, angoisse, agitation, céphalées, tremblement, sensation<br />
vertigineuse.<br />
- respiratoire : toux, sensation d’oppression respiratoire.<br />
- digestif : nausées, vomissements.<br />
- cutané : flush, prurit, urticaire localisée ou généralisée, rash cutané, œdème palpébral.<br />
Des accidents plus graves peuvent suivre ces signes mineurs ou survenir d'emblée :<br />
- troubles neurologiques : tétanie, crise convulsive, coma.<br />
- troubles cardiovasculaires : trouble du rythme, pâleur, cyanose pouvant conduire exceptionnellement<br />
à une défaillance cardiaque et à un collapsus cardiovasculaire.<br />
- réactions allergoïdes : dyspnée, hypotension : plus rarement choc anaphylactique, bronchospasme,<br />
œdème du larynx, œdème pulmonaire et exceptionnellement, œdème de Quincke.<br />
Des réactions d’hypersensibilité retardées peuvent survenir dans les 48 heures suivant l’administration de<br />
produits de contraste iodés. Ces réactions se manifestent surtout par des effets indésirables cutanés<br />
(rougeur de la peau, démangeaison, urticaire), mais quelques cas d’œdème respiratoire, d’œdème de<br />
Quincke, de bronchospasme et d’hypotension ont également été rapportés.<br />
G:\A_R_GC\<strong>Notice</strong>s\<strong>Notice</strong>s validées\Xenetix\Xenetix Bags_V9_08-2005 RCP.doc - Fusion V 5 et 6 NS
Précautions particulières :<br />
Xenetix 4/5<br />
RCP V 9 –08/2005<br />
Comme tous les produits de contraste iodés, les produits triiodés hydrosolubles, non ioniques, peuvent<br />
entraîner des réactions légères, graves ou fatales d’intolérance, souvent précoces, parfois tardives. Elles<br />
sont imprévisibles mais plus fréquentes chez les patients présentant des antécédents allergiques<br />
(urticaire, asthme, rhume des foins, eczéma, allergies diverses alimentaires ou médicamenteuses) ou qui<br />
ont présenté une sensibilité particulière lors d’un examen antérieur, à l’aide d’un produit iodé.<br />
Elles ne peuvent être dépistées par la pratique de tests à l’iode, ni à l’heure actuelle par aucun test.<br />
Pendant la durée de l’examen, il convient d’assurer :<br />
- la surveillance par un médecin<br />
- le maintien de la voie d’abord veineuse, pour traiter sans délai un éventuel accident.<br />
La prudence est conseillée en cas d'hypersensibilité aux produits de contraste iodés.<br />
La prudence est conseillée dans les cas d’insuffisances hépatiques et rénales simultanées.<br />
La prudence est conseillée dans les cas de maladies cardiovasculaires comme l'insuffisance<br />
coronarienne décompensée, les arythmies sévères, l'angine de poitrine instable, un antécédent<br />
d'infarctus du myocarde et l'hypertension pulmonaire.<br />
La prudence est conseillée dans les cas d'antécédents de crises d'épilepsie.<br />
La prudence est conseillée dans les cas d'artériosclérose cérébrale progressive, d'infarctus cérébral aigu<br />
et d'hémorragie intracrânienne aiguë ou d'affections caractérisées par une barrière hémato-encéphalique<br />
endommagée.<br />
La prudence est conseillée en cas d'utilisation chez des nouveau-nés, des patients âgés et des patients<br />
avec une condition générale fortement détériorée.<br />
La restriction hydrique est inutile : il est prudent de maintenir une diurèse abondante chez les sujets<br />
insuffisants rénaux, diabétiques, myélomateux, hyperuricémiques ainsi que chez les enfants très jeunes<br />
et les sujets athéromateux. Une prémédication semble souhaitable chez les sujets présentant le plus<br />
grand risque de réaction (allergiques, intolérants aux produits iodés) soit 50 mg de prednisone per os ou<br />
100 mg d’hydrocortisone par voie i.v. toutes les 6 heures avec un total de 3 doses, la dernière étant<br />
administrée une heure avant l’injection du produit de contraste, soit 50 mg de diphenhydramine par voie<br />
i.m., i.v. ou orale et 300 mg de cimétidine par voie i.v. ou orale une heure avant l’examen.<br />
Le risque implique la disposition des moyens nécessaires à une réanimation d’urgence. Ceci plus<br />
particulièrement lorsque le patient est en même temps sous bêta-bloquants : l’adrénaline et le<br />
remplissage vasculaire sont alors peu efficaces.<br />
Pour les patients atteints de drépanocytose, il est conseillé, afin d’éviter une crise drépanocytaire, qu’ils<br />
soient suffisamment hydratés et d’utiliser un volume minimal d’un produit de contraste faiblement<br />
concentré et de basse osmolalité.<br />
Le patient doit être prévenu du fait que des réactions d’hypersensibilité peuvent survenir jusqu’à 48<br />
heures après l’administration d’un produit de contraste iodé.<br />
Un médecin doit être consulté en cas d’apparition d’une éruption cutanée, de difficultés respiratoires,<br />
d’œdème ou d’hypotension.<br />
Incompatibilité :<br />
Aucune n’est connue à ce jour. Cependant pour éviter tout risque d’incompatibilité aucune autre<br />
médication ne doit être injectée dans la même seringue.<br />
Grossesse et lactation :<br />
Grossesse :<br />
L’innocuité de la prescription de XENETIX chez la femme enceinte n’a pas été établie.<br />
Les résultats des études réalisées chez l’animal n’ont pas mis en évidence d’effet<br />
tératogène. Cependant, toute exposition aux rayons-X devant être évitée durant la<br />
G:\A_R_GC\<strong>Notice</strong>s\<strong>Notice</strong>s validées\Xenetix\Xenetix Bags_V9_08-2005 RCP.doc - Fusion V 5 et 6 NS
Xenetix 5/5<br />
RCP V 9 –08/2005<br />
grossesse, la décision de réaliser un examen devra mettre en balance le bénéfice qu’on<br />
pense en tirer avec le risque encouru.<br />
Allaitement :<br />
Aucune étude n’a été menée concernant le passage de Iobitridol dans le lait maternel.<br />
Les résultats des études animales ont montré que l’excrétion dans le lait est faible (<<br />
3%).<br />
Il est conseillé d’interrompre l’allaitement maternel pendant les 24 heures suivant<br />
l’administration de XENETIX.<br />
Interactions :<br />
Le traitement par biguanides (metformine) doit être suspendu 48 heures avant l'exploration pour n'être<br />
restauré que 2 jours après l'examen radiologique. Ceci permet d'écarter la possibilité d'une acidose<br />
lactique qui serait déclenchée par l'insuffisance rénale fonctionnelle induite par l'exploration radiologique<br />
chez le diabétique.<br />
En cas de déshydratation provoquée par les diurétiques, il existe un risque majoré d’insuffisance rénale<br />
aiguë en particulier lors de l’utilisation de doses importantes de produit de contraste iodé.<br />
Dans ce cas, une réhydratation est nécessaire avant l’administration du produit iodé.<br />
Certains tests thyroïdiens (P.B.I., iode marqué) ne reflètent pas de façon précise la fonction thyroïdienne<br />
pendant plusieurs semaines après l’administration de produits de contraste iodés. Le dosage direct des<br />
hormones thyroïdiennes (thyroxine, triiodothyronine) permet d’éviter toute confusion.<br />
Conservation :<br />
Flacon :<br />
A conserver à l’abri de la lumière et à une température inférieure ou égale à 30° C.<br />
Poche :<br />
A conserver à l’abri de la lumière.<br />
Ne pas dépasser la date de péremption figurant sur l'emballage en regard du sigle Exp., signifiant périmé<br />
(mois/année) le dernier jour du mois indiqué.<br />
A la fin de la journée la solution de produit de contraste non utilisée au cours de la session d'examens<br />
ainsi que son dispositif de prélèvement associé devront être détruits.<br />
Délivrance :<br />
Sur prescription médicale.<br />
Dernière mise à jour de la notice :<br />
08/2005<br />
G:\A_R_GC\<strong>Notice</strong>s\<strong>Notice</strong>s validées\Xenetix\Xenetix Bags_V9_08-2005 RCP.doc - Fusion V 5 et 6 NS