1 Termodinamikai állapothatározók
1 Termodinamikai állapothatározók
1 Termodinamikai állapothatározók
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
<strong>Termodinamikai</strong> alapfogalmak<br />
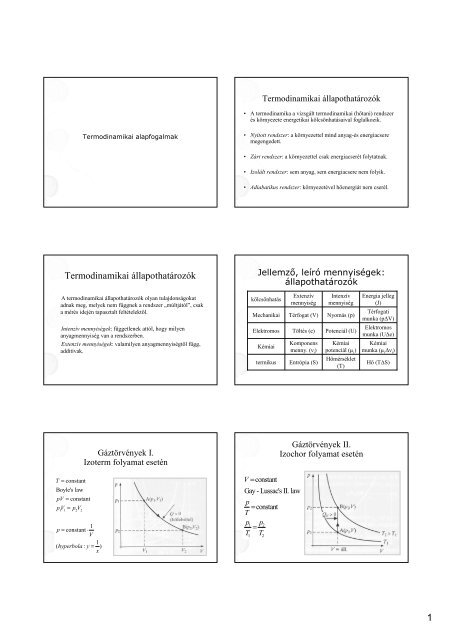
<strong>Termodinamikai</strong> <strong>állapothatározók</strong><br />
A termodinamikai <strong>állapothatározók</strong> olyan tulajdonságokat<br />
adnak meg, melyek nem függnek a rendszer „múltjától”, csak<br />
a mérés idején tapasztalt feltételektıl.<br />
Intenzív mennyiségek: függetlenek attól, hogy milyen<br />
anyagmennyiség van a rendszerben.<br />
Extenzív mennyiségek: valamilyen anyagmennyiségtıl függ,<br />
additívak.<br />
T = constant<br />
Boyle's law<br />
pV = constant<br />
p V = p V<br />
1 1 2 2<br />
1<br />
p = constant ⋅<br />
V<br />
1<br />
( hyperbola : y = )<br />
x<br />
Gáztörvények I.<br />
Izoterm folyamat esetén<br />
<strong>Termodinamikai</strong> <strong>állapothatározók</strong><br />
• A termodinamika a vizsgált termodinamikai (hıtani) rendszer<br />
és környezete energetikai kölcsönhatásaival foglalkozik.<br />
• Nyitott rendszer: a környezettel mind anyag-és energiacsere<br />
megengedett.<br />
• Zárt rendszer: a környezettel csak energiacserét folytatnak.<br />
• Izolált rendszer: sem anyag, sem energiacsere nem folyik.<br />
• Adiabatikus rendszer: környezetével hıenergiát nem cserél.<br />
Jellemzı, leíró mennyiségek:<br />
<strong>állapothatározók</strong><br />
kölcsönhatás<br />
Mechanikai<br />
Elektromos<br />
Kémiai<br />
termikus<br />
V = constant<br />
Gay - Lussac's II. law<br />
p<br />
= constant<br />
T<br />
p1 p2<br />
=<br />
T T<br />
1 2<br />
Extenzív<br />
mennyiség<br />
Térfogat (V)<br />
Töltés (e)<br />
Komponens<br />
menny. (ν i)<br />
Entrópia (S)<br />
Intenzív<br />
mennyiség<br />
Nyomás (p)<br />
Potenciál (U)<br />
Kémiai<br />
potenciál (µ i)<br />
Hımérséklet<br />
(T)<br />
Gáztörvények II.<br />
Izochor folyamat esetén<br />
Energia jelleg<br />
(J)<br />
Térfogati<br />
munka (p∆V)<br />
Elektromos<br />
munka (U∆e)<br />
Kémiai<br />
munka (µ i∆ν i)<br />
Hı (T∆S)<br />
1
p=<br />
constant<br />
Gay - Lussac's I. law<br />
V<br />
= constant<br />
T<br />
V1 V2<br />
=<br />
T T<br />
1 2<br />
Gáztörvények III.<br />
Izobár folyamat esetén<br />
Termodinamika fıtételei:<br />
o. fıtétel<br />
• Ha két (A;B)termodinamikai rendszer hımérsékleti<br />
enyensúlyban van, és B egyensúlyban van C term. Rendszerrel<br />
akkor A is egyensúlyban van C-vel.<br />
Termodinamika fıtételei:<br />
II. fıtétel<br />
Hı nem alakítható át maradéktalanul semmilyen más<br />
energiává.<br />
Az át nem alakítható hıenergia-hányad a végállapot<br />
molekuláinak a hıenergiája. 0K-tıl különbözı hımérsékleten<br />
minden anyagi rendszer molekulái mozgásban vannak.<br />
Nem valósítható meg olyan reverzibilis lépésekbıl álló<br />
folyamat, amelynek egyedüli végeredmény az, hogy egy<br />
hıtartályból hıt von el és azt munkává alakítja.<br />
Belsı energia<br />
• A termikus és a szerkezetbıl következı, alapállapothoz tartozó<br />
energia összegét belsı energiának (U) nevezzük. A belsı<br />
energia állapotfüggvény.<br />
• Állapotfüggvény: olyan, a rendszert jellemzı mennyiség,<br />
amelynek értéke adott rendszer esetén kizárólag a rendszer<br />
állapotától függ. Független az úttól, melyen a rendszer az adott<br />
állapotba került.<br />
• U= E el +E vibr +E rot +E kin +E egyéb<br />
Termodinamika fıtételei:<br />
I. fıtétel<br />
∆U=Q−W<br />
∆U=Q−p∆V<br />
Ha a rendszer végez munkát,(tágul) akkor −W;<br />
Ha a rendszeren végzünk munkát,(összenyomjuk) akkor +W.<br />
Hess tétele:Ha a termodinamikai rendszert a állapotból b<br />
állapotba visszük, az összes energiája megváltozik, de ez csak<br />
az a és b állapot függvénye és nem függ az úttól.<br />
A biológiai folyamatok a termodinamika adatainak<br />
felhasználásával tárgyalhatók.!!!<br />
Termodinamika fıtételei:<br />
II. fıtétel statisztikus megfogalmazása<br />
Entrópia<br />
Onsager lineáris törvénye: J=L i*X i<br />
L : extenzív; X: intenzív mennyiség<br />
A J helyébe hıáramot , X helyébe Hımérséklete írva:<br />
Q=LT;<br />
L változása állandó hımérsékleten: dL=dQ/T.<br />
L voltaképpen az entrópia (S).<br />
∆S=∆Q/T<br />
Az entrópia állapotfüggvény, amely a spontán lejátszódó<br />
folyamatok irányának meghatározásában játszik jelentıs<br />
szerepet.<br />
2
Termodinamika fıtételei:<br />
II. fıtétel statisztikus megfogalmazása<br />
makroállapot<br />
A<br />
B<br />
C<br />
D<br />
E<br />
Az I-es cella részecskéi<br />
szám jelölés<br />
4<br />
3<br />
2<br />
1<br />
0<br />
abcd<br />
abc; abd; acd; bcd<br />
ab, ac; ad; bc; bd; cd<br />
a; b; c; d<br />
Entalpia, szabadenergia<br />
H=U+pV; állapotfüggvény<br />
Szabadentalpia vagy Gibbs-féle szabadenergia:<br />
a) p=áll. és T=áll. végbemenı folyamatok esetén<br />
G= H−TS; G, F: állapotfüggvény<br />
b) V=áll. és T=áll. végbemenı folyamatok esetén<br />
F=H−TS;<br />
F.:Helmholtz-féle szabadenergia<br />
−<br />
mikroállapot<br />
<strong>Termodinamikai</strong> állapotváltozások I.<br />
Izotermikus állapotváltozás:<br />
T=<br />
constant →ΔT=0<br />
f<br />
Δ U= NkΔT →Δ U=<br />
0<br />
2<br />
Δ U= Q+ W<br />
Q+ W=<br />
0<br />
Q=−W 1<br />
4<br />
6<br />
4<br />
1<br />
Termodinamika fıtételei:<br />
II. fıtétel statisztikus megfogalmazása<br />
Entrópia: a termodinamikai valószínőség természetes alapú<br />
lg-jével arányos. Arányossági tényezı a k.<br />
S=klnP<br />
<strong>Termodinamikai</strong> valószínőség: az egy makroállapothoz tartozó<br />
mikroállapotok száma.<br />
Entalpia, szabadenergia<br />
Spontán folyamatok iránya:<br />
∆G (∆F)
<strong>Termodinamikai</strong> állapotváltozások III.<br />
Izobár állapotváltozás:<br />
p = constant<br />
W = p( V −V<br />
)<br />
2 1<br />
f<br />
Qp = cpmΔ T = ( + 1) mΔT 2<br />
Δ U = Q+ W<br />
4













![Microsoft PowerPoint - Intermedier filamentumok [Kompatibilis m\363d]](https://img.yumpu.com/17119137/1/190x135/microsoft-powerpoint-intermedier-filamentumok-kompatibilis-m363d.jpg?quality=85)


