Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
78<br />
Contoh:<br />
Nitrogen dan oksigen dapat membentuk senyawa-senyawa N 2 O, NO,<br />
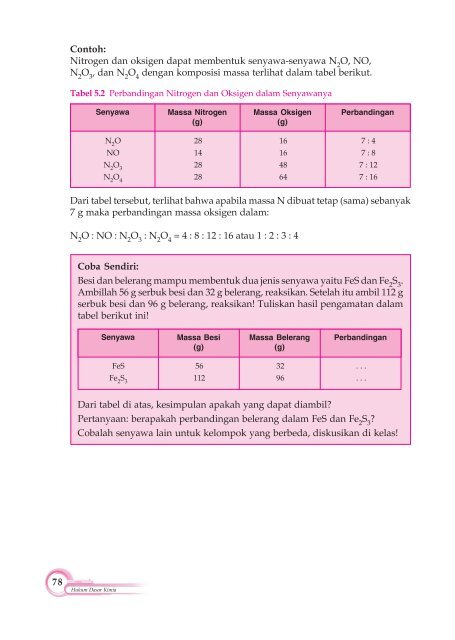
N 2 O 3 , dan N 2 O 4 dengan komposisi massa terlihat dalam tabel berikut.<br />
Tabel 5.2 Perbandingan Nitrogen dan Oksigen dalam Senyawanya<br />
Dari tabel tersebut, terlihat bahwa apabila massa N dibuat tetap (sama) sebanyak<br />
7 g maka perbandingan massa oksigen dalam:<br />
N 2 O : NO : N 2 O 3 : N 2 O 4 = 4 : 8 : 12 : 16 atau 1 : 2 : 3 : 4<br />
Coba Sendiri:<br />
Besi dan belerang mampu membentuk dua jenis senyawa yaitu FeS dan Fe2S3 .<br />
Ambillah 56 g serbuk besi dan 32 g belerang, reaksikan. Setelah itu ambil 112 g<br />
serbuk besi dan 96 g belerang, reaksikan! Tuliskan hasil pengamatan dalam<br />
tabel berikut ini!<br />
Dari tabel di atas, kesimpulan apakah yang dapat diambil?<br />
Pertanyaan: berapakah perbandingan belerang dalam FeS dan Fe2S3 ?<br />
Cobalah senyawa lain untuk kelompok yang berbeda, diskusikan di kelas!<br />
Hukum Dasar <strong>Kimia</strong><br />
Senyawa Massa Nitrogen<br />
(g)<br />
N2O NO<br />
N2O3 N2O4 28<br />
14<br />
28<br />
28<br />
Senyawa Massa Besi<br />
(g)<br />
FeS<br />
Fe2S3 56<br />
112<br />
Massa Oksigen<br />
(g)<br />
16<br />
16<br />
48<br />
64<br />
Massa Belerang<br />
(g)<br />
32<br />
96<br />
Perbandingan<br />
7 : 4<br />
7 : 8<br />
7 : 12<br />
7 : 16<br />
Perbandingan<br />
. . .<br />
. . .