You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
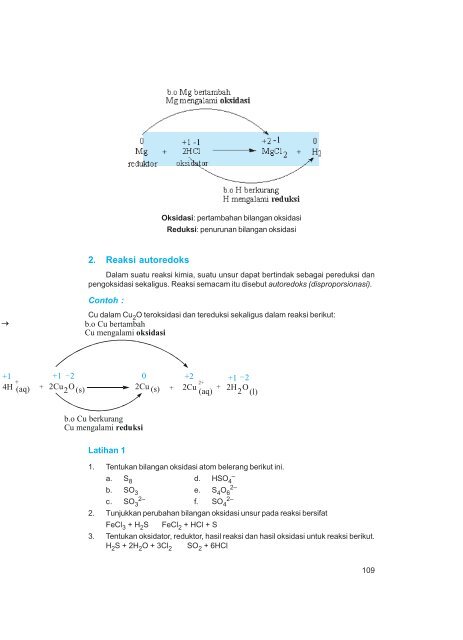
2. Reaksi autoredoks<br />
Oksidasi: pertambahan bilangan oksidasi<br />
Reduksi: penurunan bilangan oksidasi<br />
Dalam suatu reaksi kimia, suatu unsur dapat bertindak sebagai pereduksi dan<br />
pengoksidasi sekaligus. Reaksi semacam itu disebut autoredoks (disproporsionasi).<br />
Contoh :<br />
Cu dalam Cu2O teroksidasi dan tereduksi sekaligus dalam reaksi berikut:<br />
b.o Cu bertambah<br />
Cu mengalami oksidasi<br />
4H +<br />
2+<br />
(aq) + 2Cu<br />
2<br />
O (s) 2Cu (s) + 2Cu<br />
(aq)<br />
2H<br />
(l)<br />
+<br />
2 O<br />
_<br />
+1 +1 2 0 +2<br />
_<br />
+1 2<br />
b.o Cu berkurang<br />
Cu mengalami reduksi<br />
Latihan 1<br />
1. Tentukan bilangan oksidasi atom belerang berikut ini.<br />
a. S 8 d. HSO 4 –<br />
b. SO 3 e. S 4 O 6 2–<br />
c. SO 3 2– f. SO 4 2–<br />
2. Tunjukkan perubahan bilangan oksidasi unsur pada reaksi bersifat<br />
FeCl3 + H2S FeCl2 + HCl + S<br />
3. Tentukan oksidator, reduktor, hasil reaksi dan hasil oksidasi untuk reaksi berikut.<br />
H2S + 2H2O + 3Cl2 SO2 + 6HCl<br />
109