fasit
fasit
fasit
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
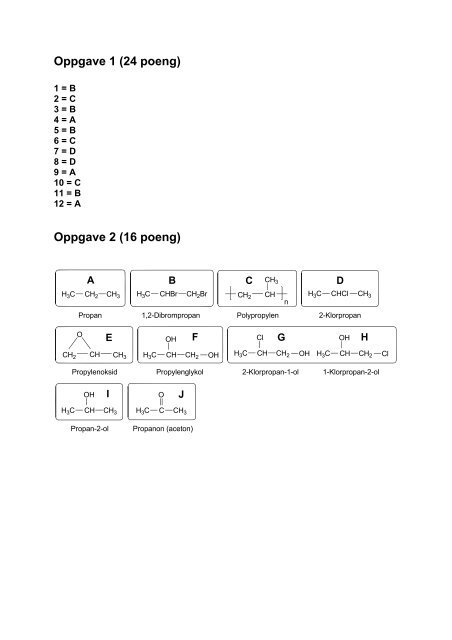
Oppgave 1 (24 poeng)1 = B2 = C3 = B4 = A5 = B6 = C7 = D8 = D9 = A10 = C11 = B12 = AOppgave 2 (16 poeng)AB C CH 3DCH 2 H 3 CH 3 C CH 3 H 3 C CHBr CH 2 Br CH 2 CHPropan 1,2-Dibrompropan Polypropylen 2-KlorpropannCHCl CH 3OE F Cl G OH HOHCH 2 CH CH 3 H 3 C CH CH 2 OH H 3 C CH CH 2 OH H 3 C CH CH 2ClPropylenoksid Propylenglykol 2-Klorpropan-1-ol 1-Klorpropan-2-olOHIOJH 3 CCH CH 3H 3 CC CH 3Propan-2-olPropanon (aceton)
Oppgave 3 (20 poeng)6 M HCl 6 M HNO 3 6 M NaOHBaCO 3 Ba 2+ (aq), CO 2 (g) Ba 2+ (aq), CO 2 (g) (---)Ag (X) Ag + (aq), NO(g) (X)BaSO 4 (X) (X) (X)Fe(OH) 3 Fe 3+ (aq), H 2 O Fe 3+ (aq), H 2 O (X)FeS Fe 2+ (aq), H 2 S(g) Fe 3+ (aq), H 2 S(g), NO(g) (---)Zn Zn 2+ (aq), H 2 (g) Zn 2+ (aq), NO(g) (---)Zn(OH) 2 Zn 2+ (aq), H 2 O Zn 2+ (aq), H 2 O Zn(OH) 2- 4 (aq)Oppgave 4 (12 poeng)a) 2 S 2 O 2- 3 + I 2 S 4 O 2- 6 + 2 I -b) IO - 3 + 5 I - + 6 H 3 O + 3 I 2 + 9 H 2 Oc) Stoffmengde I 2 fra KIO 3 /KI : 1,19410 -3 mol I 2Konsentrasjonen av S 2 O 2- 3 -løsningen er: 0,1063 Md) 2 Cu 2+ + 4 I - 2 CuI(s) + I 2e) 2 mol Cu 2+ gir 1 mol I 2[Cu 2+ ] = 0,1507 MOppgave 5 (14 poeng)a) Cl 2 + H 2 O Cl - + HClO + H +b) i) Reaksjon mot høyre, (nøytralisering av H + ), Cl 2 mindre stabilii) Reaksjon mot høyre, (fortynningseffekt). Cl 2 mindre stabil.iii) Reaksjon mot høyre, (Cl - fjernes som AgCl (s)). Cl 2 mindre stabiliv) Reaksjon mot venstre, (Økning i [Cl - ]). Cl 2 mer stabil.c) 3HClO 2Cl - +3H + -+ ClO 3
Oppgave 6 (16 poeng)a) Masseprosent Li i LiH = 12,64% Hb) LiH(s) + H 2 O(l) → LiOH(aq) + H 2 (g)c) 2,45 L gass er 0,100 mol ved standard betingelser, det er altså dannet 0,100mol H 2 (g). Et 1:1-forhold mellom H 2 (g) og LiH(s) tyder på at 0,100 mol LiH(s)ble tilsatt vannet, noe som tilsvarer 0,795g LiH(s).d) 12,8 g/100 mL gir at maksimal konsentrasjon av LiOH(aq) er 0,534mol/100 mL, som tilsvarer 4,26 g/100 mL.pH i løsningen er 14,7(I realiteten må man også ta volumendringen av vann med i betraktningen,volumet vil minke med 9 mL ved tilsetting av en slik mengde LiH. Detteforventes likevel ikke i denne oppgaven. - Svaret dersom dette tas ibetraktning er 4,12 g.)e) 3LiH(s) + N 2 (g) → Li 3 N(s) + NH 3 (g). Nitrogen reduseres fra elementærtnitrogen til nitrid med ladning –III. Hydrogen har negativ formell ladning i LiH,og får oksidasjonstall +I i NH 3 . Totalt 6 elektroner overføres i reaksjonen.