Português - Curso Objetivo
Português - Curso Objetivo
Português - Curso Objetivo
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
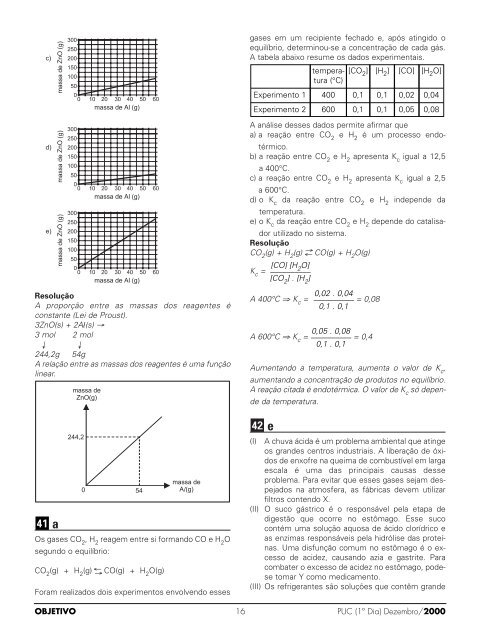
Resolução<br />
A proporção entre as massas dos reagentes é<br />
constante (Lei de Proust).<br />
3ZnO(s) + 2Al(s) →<br />
3 mol 2 mol<br />
↓ ↓<br />
244,2g 54g<br />
A relação entre as massas dos reagentes é uma função<br />
linear.<br />
41<br />
a<br />
massa de<br />
ZnO(g)<br />
244,2<br />
0 54<br />
Os gases CO2 , H2 reagem entre si formando CO e H2O segundo o equilíbrio:<br />
CO 2 (g) + H 2 (g) → ← CO(g) + H 2 O(g)<br />
massa de<br />
A l(g)<br />
Foram realizados dois experimentos envolvendo esses<br />
gases em um recipiente fechado e, após atingido o<br />
equilíbrio, determinou-se a concentração de cada gás.<br />
A tabela abaixo resume os dados experimentais.<br />
Experimento 1<br />
Experimento 2<br />
A análise desses dados permite afirmar que<br />
a) a reação entre CO2 e H2 é um processo endotérmico.<br />
b) a reação entre CO2 e H2 apresenta Kc igual a 12,5<br />
a 400°C.<br />
c) a reação entre CO2 e H2 apresenta Kc igual a 2,5<br />
a 600°C.<br />
d) o Kc da reação entre CO2 e H2 independe da<br />
temperatura.<br />
e) o Kc da reação entre CO2 e H2 depende do catalisador<br />
utilizado no sistema.<br />
Resolução<br />
CO2 (g) + H2 (g) → ← CO(g) + H2O(g) K c =<br />
A 400°C ⇒ K c = = 0,08<br />
A 600°C ⇒ K c = = 0,4<br />
Aumentando a temperatura, aumenta o valor de Kc ,<br />
aumentando a concentração de produtos no equilíbrio.<br />
A reação citada é endotérmica. O valor de Kc só depende<br />
da temperatura.<br />
42<br />
[CO] [H 2 O]<br />
––––––––––<br />
[CO 2 ] . [H 2 ]<br />
e<br />
tempera-<br />
tura (°C)<br />
400<br />
600<br />
0,02 . 0,04<br />
––––––––––<br />
0,1 . 0,1<br />
0,05 . 0,08<br />
––––––––––<br />
0,1 . 0,1<br />
[CO 2 ]<br />
0,1<br />
0,1<br />
[H 2 ]<br />
0,1<br />
0,1<br />
[CO]<br />
0,02<br />
0,05<br />
[H 2 O]<br />
0,04<br />
0,08<br />
(I) A chuva ácida é um problema ambiental que atinge<br />
os grandes centros industriais. A liberação de óxidos<br />
de enxofre na queima de combustível em larga<br />
escala é uma das principais causas desse<br />
problema. Para evitar que esses gases sejam despejados<br />
na atmosfera, as fábricas devem utilizar<br />
filtros contendo X.<br />
(II) O suco gástrico é o responsável pela etapa de<br />
digestão que ocorre no estômago. Esse suco<br />
contém uma solução aquosa de ácido clorídrico e<br />
as enzimas responsáveis pela hidrólise das proteínas.<br />
Uma disfunção comum no estômago é o excesso<br />
de acidez, causando azia e gastrite. Para<br />
combater o excesso de acidez no estômago, podese<br />
tomar Y como medicamento.<br />
(III) Os refrigerantes são soluções que contêm grande<br />
OBJETIVO 16<br />
PUC (1º Dia) Dezembro/2000