Pré-tratamento dos dados Modelos PLS - lqta
Pré-tratamento dos dados Modelos PLS - lqta
Pré-tratamento dos dados Modelos PLS - lqta
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
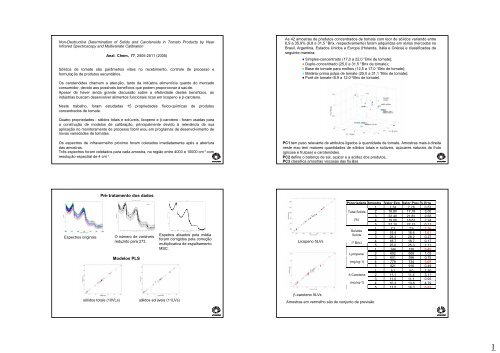
Non-Destructive Determination of Solids and Carotenoids in Tomato Products by Near<br />
Infrared Spectroscopy and Multivariate Calibration<br />
Anal. Chem., 77, 2505-2511 (2005)<br />
Sóli<strong>dos</strong> de tomate são parâmetros vitais no recebimento, controle de processo e<br />
formulação de produtos secundários.<br />
Os carotenóides chamam a atenção, tanto da indústria alimentícia quanto do mercado<br />
consumidor, devido aos possíveis benefícios que podem proporcionar à saúde.<br />
Apesar de haver ainda grande discussão sobre a efetividade destes benefícios, as<br />
indústrias buscam desenvolver alimentos funcionais ricos em licopeno e -caroteno.<br />
Neste trabalho, foram estudadas 15 propriedades físico-químicas de produtos<br />
concentra<strong>dos</strong> de tomate.<br />
Quatro propriedades - sóli<strong>dos</strong> totais e solúveis, licopeno e -caroteno - foram usadas para<br />
a construção de modelos de calibração, principalmente devido à relevância de sua<br />
aplicação no monitoramento de processo fabril e/ou em programas de desenvolvimento de<br />
novas variedades de tomates.<br />
Os espectros de infravermelho próximo foram coleta<strong>dos</strong> imediatamente após a abertura<br />
das amostras.<br />
Três espectros foram coleta<strong>dos</strong> para cada amostra, na região entre 4000 e 10000 cm -1 com<br />
resolução espectral de 4 cm -1 .<br />
Espectros originais<br />
<strong>Pré</strong>-<strong>tratamento</strong> <strong>dos</strong> da<strong>dos</strong><br />
O número de variáveis<br />
reduzido para 273.<br />
<strong>Modelos</strong> <strong>PLS</strong><br />
sóli<strong>dos</strong> totais (10VLs) sóli<strong>dos</strong> solúveis (11LVs)<br />
Espetros alisa<strong>dos</strong> pela média<br />
foram corrigi<strong>dos</strong> pela correção<br />
multiplicativa de espalhamento<br />
MSC.<br />
As 42 amostras de produtos concentra<strong>dos</strong> de tomate com teor de sóli<strong>dos</strong> variando entre<br />
6,9 a 35,9% (6,8 a 31,5 °Brix, respectivamente) foram adquiridas em vários merca<strong>dos</strong> no<br />
Brasil, Argentina, Esta<strong>dos</strong> Uni<strong>dos</strong> e Europa (Holanda, Itália e Grécia) e classificadas da<br />
seguinte maneira:<br />
♦Simples-concentrado (17,0 a 22,0 °Brix de tomate);<br />
♦Duplo-concentrado (25,0 a 31,5 °Brix de tomate);<br />
♦Base de tomate para molhos (12,5 a 17,0 °Brix de tomate);<br />
♦Matéria-prima polpa de tomate (25,0 a 31,1 °Brix de tomate);<br />
♦Purê de tomate (6,9 a 12,0 ºBrix de tomate).<br />
PC1 tem peso relevante de atributos liga<strong>dos</strong> à quantidade de tomate. Amostras mais à direita<br />
neste eixo tem maiores quantidades de sóli<strong>dos</strong> totais e solúveis, açúcares naturais do fruto<br />
(glicose e frutose) e carotenóides.<br />
PC2 define o balanço de sal, açúcar e a acidez <strong>dos</strong> produtos,<br />
PC3 classifica amostras viscosas das fluídas<br />
Licopeno 5LVs<br />
-caroteno 5LVs<br />
Amostras em vermelho são do conjunto de previsão<br />
Propriedade Amostra Valor Exp. Valor Prev. % Erro<br />
1 7,74 7,78 0,57<br />
Total Solids 2 16,80 17,18 3,00<br />
3 22,40 21,81 2,63<br />
(%) 4 19,06 18,63 2,24<br />
Soluble<br />
Solids<br />
(º Brix)<br />
Lycopene<br />
(mg kg-1)<br />
-Carotene<br />
(mg kg-1)<br />
5 27,10 27,13 0,11<br />
1 7,3 7,9 7,76<br />
2 15,4 16,6 7,61<br />
3 28,3 28,2 0,27<br />
4 18,7 18,7 0,17<br />
5 25,0 25,3 1,11<br />
1 144 135 6,45<br />
2 602 608 1,03<br />
3 601 596 0,75<br />
4 779 734 5,69<br />
5 921 916 0,49<br />
1 5,1 5,0 1,50<br />
2 11,1 11,4 3,11<br />
3 11,0 11,1 0,93<br />
4 10,3 10,8 4,79<br />
5 17,5 16,3 6,83<br />
1
Atividade do Omeprazol e compostos análogos com atividade anti- Helicobacter<br />
pylori<br />
Bruni, A. T.; Ferreira, M. M. C, J. Chemom. 2002, 16, 510.<br />
Kühler, T. C.; Fryklund, J.; Bergaman, N. A.; Weiliotz, J.; Lee, A.; Larsson, H.; . Med. Chem.,<br />
1995, 38, 4906.<br />
Estudo da atividade do omeprazol e de alguns de seus deriva<strong>dos</strong> na inibição da<br />
urease H. pylori.A bactéria H. pylori vive no estomago e necessita da enzima urease<br />
para colonizar a mucosa.<br />
Esta enzima metaboliza rapidamente a uréia no suco gástrico gerando os íons<br />
bicarbonato e amônio em torno da bactéria. Isto permite que ela passe de forma segura<br />
através da barreira ácido-gástrica e chegue até à mucosa causando inflamações.<br />
R1<br />
R2<br />
R3<br />
O<br />
S<br />
(a)<br />
N<br />
N<br />
(b)<br />
N<br />
H<br />
R4<br />
R5<br />
R6<br />
Compostos %cont R1 R2 R3 R4 R5 R6<br />
1 32,0 H OCH 3 CH 3 H CH 2O H<br />
2 8,0 H OCH 2CH 3 CH 3 H H H<br />
3 1,0 H OCH3 CH3 H C(CH 3 H<br />
4 58,0 H OCH 3 H F H H<br />
5 80,0 H OCH 3 H F H F<br />
6 84,0 H OC H 2 OCH 3 H F H<br />
7 - H OCH(CH 3) 2 CH3 H OCH3 H<br />
8 b<br />
O<br />
- H OCH3 CH3 H<br />
Lansoprazol 29,0 H OCH 2CF 3 CH 3 H H H<br />
Omeprazol 28,0 CH3 OCH3 CH3 H OCH3 H<br />
Este conjunto de da<strong>dos</strong> pode ser usado para construir vários modelos e extrair<br />
diferentes informações.<br />
Os compostos 7 e 8 foram removi<strong>dos</strong> da análise<br />
8 compostos no conjunto de treinamento;<br />
Modelo QSAR com todas as estruturas de mínima energia do conjunto de<br />
treinamento X = (2627).<br />
Para entender melhor o sistema em<br />
estudo, deve-se proceder a uma seleção<br />
de variáveis.<br />
Cálcula-se o coeficiente de correlação de cada um <strong>dos</strong> descritores com a atividade<br />
biológica e exclue to<strong>dos</strong> aqueles com coeficiente de correlação menor que 0,6.<br />
Dos 27 descritores originais, 18 foram elimina<strong>dos</strong> restando apenas 9.<br />
N<br />
O<br />
S<br />
N<br />
N<br />
H<br />
A produção de amônia na presença da urease H. pylori foi comparada com a<br />
produção de amônia na sua ausência. O fármaco foi então adicionado e a<br />
resposta biológica in vitro foi medida em termos da porcentagem de controle<br />
(%cont) definida como a % de amônia restante após a adição de 100mM do<br />
mesmo.<br />
O omeprazol e os respectivos congêneres são opticamente ativos tendo o<br />
enxofre como centro quiral.<br />
Eles são anfóteros, i. e., os valores de pKa são dependentes das propriedades<br />
eletrônicas <strong>dos</strong> substituintes nos anéis benzimidazol e piridina.<br />
O omeprazol é um pro-fármaco que facilmente se converte na respectiva<br />
sulfenamida em meio ácido.<br />
Descritores: 4 EXPERIMENTAIS E O RESTANTE TEÓRICOS<br />
tempo de meia vida, t1/2, (relacionado com a rapidez de decomposição do omeprazol<br />
na sulfenamida)<br />
lipofilia, logk0, (obtida tomando o omeprazol como referência)<br />
pKa de cada um <strong>dos</strong> anéis benzimidazol e piridina (pKapy e pKabz).<br />
Foi feita a análise conformacional <strong>dos</strong> 10 compostos estuda<strong>dos</strong> e foram<br />
encontradas conformações significativamente diferentes para cada composto,<br />
embora com diferenças de energia menores que 1,0 kcal mol -1.<br />
Inicialmente, cada uma destas estruturas de mínima energia (26 n o total) foi<br />
considerada como uma amostra na matriz de da<strong>dos</strong> X.<br />
23 descritores teóricos foram calcula<strong>dos</strong> para cada conformação.<br />
energia do orbital de fronteira HOMO (HOMO, –0,65),<br />
energia do orbital de fronteira LUMO (LUMO, –0,71),<br />
eletronegatividade (Eletroneg, 0,73),<br />
coordenada z do momento dipolar (Dip_z, 0,59),<br />
carga do átomo de carbono do anel piridínico ligado a R2 (R2, 0,63),<br />
carga de um <strong>dos</strong> átomos de nitrogênio do anel benzimidazol (N(a), 0,58)<br />
três das propriedades experimentais (t1/2, 0,92; pKapy, –0,78; e p Kabz, –0,65).<br />
Propriedades eletrônicas foram selecionadas indicando que elas devem ter uma<br />
maior importância na atividade biológica destes compostos.<br />
As propriedades estéreas e hidrofóbicas foram todas eliminadas.<br />
T1/2<br />
Eletronegatividade<br />
Dip_z<br />
pKapy<br />
LUMO<br />
2
Composto<br />
1<br />
2<br />
3<br />
4<br />
5<br />
6<br />
Lanso<br />
Ome<br />
%cont<br />
Medida<br />
32,0<br />
8,0<br />
1,0<br />
58,0<br />
80,0<br />
84,0<br />
29,0<br />
28,0<br />
%cont<br />
Estimada<br />
26,2<br />
13,3<br />
1,4<br />
55,8<br />
81,9<br />
84,6<br />
27,9<br />
28,9<br />
Previsão para os compostos 7 e 8:<br />
Res íduo<br />
Ambos os compostos foram aponta<strong>dos</strong> como potentes inibidores da<br />
urease H. pylori, sendo o composto 7 mais potente.<br />
H<br />
O<br />
O<br />
CH H C<br />
3<br />
3<br />
O<br />
O<br />
H<br />
O<br />
H 3C<br />
C H<br />
3<br />
H<br />
O<br />
O<br />
O<br />
H<br />
O<br />
HOO H<br />
H<br />
O<br />
O N<br />
N<br />
C H H<br />
O<br />
O<br />
H C<br />
3<br />
3<br />
O<br />
O<br />
H<br />
O<br />
C H 14<br />
3<br />
4<br />
5<br />
15<br />
6<br />
3<br />
H C<br />
O<br />
2<br />
7<br />
5a<br />
3<br />
1 O 8a<br />
8<br />
13<br />
12a<br />
12<br />
H<br />
11<br />
H<br />
10<br />
9<br />
C H 3<br />
1 O<br />
2 3 4<br />
H C H 3<br />
H C H 3<br />
C H 3<br />
H<br />
H C H 3<br />
H C<br />
3<br />
O<br />
O<br />
O<br />
H C<br />
3<br />
O<br />
O<br />
O<br />
H C<br />
3<br />
O<br />
O<br />
O<br />
H C<br />
3<br />
O<br />
O<br />
O<br />
O<br />
H<br />
H<br />
O<br />
H<br />
O<br />
H<br />
O<br />
O<br />
H<br />
H<br />
OH<br />
5 O<br />
CH<br />
3 6 O<br />
7 O<br />
8 H OH<br />
H C<br />
3<br />
O<br />
H C H 3<br />
O<br />
O<br />
H<br />
O<br />
N<br />
H<br />
S N<br />
H C<br />
3<br />
S<br />
9 C H<br />
3<br />
10<br />
H C H 3<br />
O<br />
O<br />
O<br />
O<br />
H S<br />
H CH 3<br />
S<br />
H CH 3<br />
H<br />
N<br />
N<br />
CH 3<br />
H C H 3<br />
H C H 3<br />
H C<br />
3<br />
O<br />
O<br />
O<br />
H C<br />
3<br />
O<br />
O<br />
O<br />
H<br />
H<br />
O<br />
O<br />
O<br />
O<br />
11<br />
HOO H<br />
12<br />
HO<br />
H<br />
H C H 3<br />
H C<br />
3<br />
O<br />
O<br />
O<br />
H<br />
H C<br />
3<br />
O<br />
O<br />
O<br />
H C<br />
3<br />
O<br />
O<br />
O<br />
H<br />
H C<br />
3<br />
O<br />
O<br />
O<br />
13<br />
O<br />
O<br />
C H<br />
3<br />
H<br />
14<br />
O<br />
O<br />
CH<br />
3<br />
15<br />
O<br />
O<br />
CH 3<br />
C H<br />
3<br />
16<br />
O<br />
O<br />
C H<br />
3<br />
H<br />
C H 3<br />
H<br />
CH<br />
3<br />
H<br />
H C<br />
3<br />
O<br />
O<br />
O<br />
H C<br />
3<br />
O<br />
O<br />
O<br />
H 3C<br />
O<br />
O<br />
O<br />
O<br />
H<br />
H<br />
O<br />
H<br />
H<br />
O<br />
CH 3<br />
17 O<br />
C H<br />
3 18 O<br />
C H<br />
3<br />
19 O<br />
H<br />
H O<br />
OH<br />
C H<br />
3<br />
H<br />
H<br />
H<br />
C H 3<br />
5,8<br />
-5,3<br />
-0,4<br />
2,2<br />
-1,9<br />
-0,6<br />
1,1<br />
-0,9<br />
DESCRITORES<br />
*Energia do orbital LUMO+1,<br />
*cargas nos átomos C9 e O11,<br />
*um descritor topológico<br />
*número máximo de átomos de<br />
hidrogênio que podem interagir<br />
com a heme.<br />
H C<br />
3<br />
H3 C<br />
Estudo quimiométrico/QSAR de artemisininas como agentes contra as<br />
cepas de P. falciparum resistentes à mefloquina<br />
CH 3<br />
O<br />
C H3<br />
H<br />
O<br />
O<br />
H<br />
O<br />
R<br />
2<br />
R<br />
1<br />
O<br />
O<br />
O<br />
O<br />
H C H 3<br />
H<br />
O R<br />
H<br />
O<br />
14<br />
CH 3<br />
4 5<br />
H<br />
1<br />
3 2 O<br />
6<br />
5a<br />
O<br />
O 12 8a<br />
13 12a<br />
7<br />
8<br />
O<br />
11<br />
9<br />
10<br />
H<br />
QHS<br />
CH 3<br />
Molecule R 1 R 2 R<br />
__________________________________________<br />
20 C=NH C(H)CH 3<br />
21 C=S C(H)CH 3<br />
22 C=O C 4 H 6 O 2<br />
23 C=O C 9 H 8 O 2<br />
24 C=O C(H)CHO<br />
25 C=O C 6 H 6 O 2<br />
26 C 3 H 4 O 2<br />
27 C 9 H 10 O 2<br />
28 C 5 H 6 O 2<br />
29 C=O C(H)C 3 H 5 O 2<br />
________________________________________________________________<br />
3
Composto log IC 50<br />
20 -0,025<br />
21 0,103<br />
22 0,752<br />
23 0,801<br />
24 0,437<br />
25 0,749<br />
26 -0,382<br />
27 0,234<br />
28 -0,228<br />
29 -0,040<br />
Os orbitais LUMO+1 de compostos mais ativos são concentra<strong>dos</strong> no centro do<br />
esqueleto de artemisinina, enquanto nos compostos menos ativos ficam nos<br />
grupos terminais.<br />
Standards Known Predicted Residual<br />
ST0 0.00 0.01 -0.01<br />
ST1 0.08 0.07 0.01<br />
ST2 0.45 0.44 0.01<br />
ST3 0.80 0.80 0.00<br />
ST4 1.18 1.19 -0.01<br />
ST5 1.65 1.63 0.02<br />
SEP 0.01 R 2 0.9999*<br />
Comparison between the results of caramel calculated by two<br />
methods (<strong>PLS</strong> and rate A210/A282)*. (BC) Brazilian cachaça.<br />
Sample <strong>PLS</strong> A 210/A 210 Sample <strong>PLS</strong> A 210/A 210 Sample <strong>PLS</strong> A 210/A 210 Sample <strong>PLS</strong> A 210/A 210<br />
BC1a 0.16 0.21 BC12 0.06 0.01 BC29 0.02 - 0.05 BC48 0.04 0.5<br />
BC1b 0.05 0.03 BC13a 0.05 0.00 BC30 0.03 0.08 BC49 0.04 -0.02<br />
BC1c 0.05 0.02 BC13b 0.05 0.00 BC31 0.04 0.03 BC50 0.06 -0.02<br />
BC1d 0.05 0.03 BC14a 0.09 0.04 BC32 -0.03 0.11 BC51 0.07 0.28<br />
BC1e 0.05 0.04 BC14b 0.09 0.05 BC33a 0.14 0.1 BC52 0.05 -1.04<br />
BC2a 0.09 0.12 BC14c 0.09 0.11 BC33b 0.12 0.11 BC53 0.05 0.05<br />
BC2b 0.08 0.05 BC15 0.14 0.11 BC33c 0.12 0.14 BC54 0.05 0.13<br />
BC2c 0.08 0.03 BC16a 0.11 0.09 BC34a 1.04 1.19 BC55 -0.22 -0.04<br />
BC3a 0.05 0.11 BC16b 0.12 0.07 BC34b 1.11 1.26 BC56 0.03 0.03<br />
Spectrophotometric Determination of Caramel Content in Spirits Aged in Oak<br />
Casks<br />
J. AOAC Int., 85, 744-750 (2002).<br />
Differences in the UV-visible spectra of oak aqueous-alcoholic extracts and<br />
caramel solutions in the same solvent are used for caramel analysis in spirits<br />
aged in oak casks.<br />
Absorbance<br />
2.5<br />
2<br />
1.5<br />
1<br />
0.5<br />
0<br />
240<br />
300<br />
360<br />
420<br />
Wavelength, nm<br />
480<br />
Caramel<br />
The data treatment has been carried out by two different approaches:<br />
♦based on the plot of caramel concentration versus the ratio of absorbance values<br />
at 210 and 282 nm.<br />
♦based on partial least squares (<strong>PLS</strong>) calibration model using the first derivative<br />
of the spectral data.<br />
(USW) US whisky;<br />
(SW) Scottish whisky;<br />
(CW) Canadian whisky;<br />
(IW) Irish whisky<br />
PC1 (74%)<br />
25<br />
15<br />
-15<br />
5<br />
-25 -15 -5 5 15 25<br />
-5<br />
P C2 (16 %)<br />
USW CW<br />
SW IW<br />
Standard Oaks<br />
Oak<br />
Mix<br />
540<br />
600<br />
PC1 (66%)<br />
20<br />
10<br />
0<br />
-35 -20 -5 10 25 40 55<br />
-10<br />
-20<br />
PC2 (21 %)<br />
NE SE<br />
CW S<br />
Standard Oaks<br />
4
Classificação de filmes de fécula de mandioca quanto às suas<br />
propriedades físico-químicas e a quantificação da gramatura por<br />
espectroscopia no infravermelho<br />
Henrique, C.M.; Ferreira, M.M.C; Cereda, M.P., Sabino, L.<br />
A matéria-prima para a formação <strong>dos</strong> filmes são féculas modificadas comerciais:<br />
mandioca cross link - fécula pré gelatinizada modificada<br />
carboximetilamido de baixa e alta viscosidade<br />
esterificada<br />
As concentrações avaliadas foram as suspensões filmogênicas em água de 3 e 5%.<br />
Essas soluções filmogênicas foram secas por 24 hs/40ºC.<br />
Os filmes foram caracteriza<strong>dos</strong> para: a gramatura, permeabilidade ao vapor d'água,<br />
atividade de água, tração (força na deformação), solubilidade, perfuração (força na<br />
deformação) e a espessura <strong>dos</strong> filmes.<br />
Os espectros foram registra<strong>dos</strong> na região do infravermelho médio empregando-se um<br />
espectrofotômetro provido com acessório de reflectância atenuada, na região de 4000 a<br />
650 cm -1 com resolução de 2 cm -1<br />
Modelo de calibração para a determinação da gramatura<br />
Gramatura Gramatura Resíduo Erro<br />
Pred. Exp.<br />
(%)<br />
Éster 03 347.151 370.973 23.821 6.421<br />
Alta 13 386.347 423.856 37.508 8.849<br />
Amido05 354.643 335.272 19.371 5.778<br />
Classificação <strong>dos</strong> filmes em relação à<br />
modificação química sofrida pela fécula<br />
PC1 PC2 PC3<br />
Espessura 0,510 -0,555 0,146<br />
Gramatura 0,149 0,799 0,287<br />
Solubilidade -0,549 -0,224 0,803<br />
Permeabilidade 0,646 0,063 0,501<br />
Quantitative Determination of Epoxidized Soybean Oil Using Near-Infrared<br />
Spectroscopy and Multivariate Calibration<br />
Appl. Spectrosc., 56, 1607-1614 (2002)<br />
Soybean oil is a triglyceride which typically contains 14% stearic, 23% oleic, 55% linoleic<br />
and 8% linolenic acid. Three of them are unsaturated acids: oleic (18:1), linoleic (18:2) and<br />
linolenic (18:3).<br />
Chemical modification on commercial available soybean oil such as epoxidation can<br />
enhance its properties (reactivity) for industrial applications.<br />
PVC degradation caused by sunlight eliminating HCl<br />
5
The epoxidized soybean oil (ESO) is used in plastic industry as plasticizer (at levels ranging<br />
from 0.1 to 27%), to increase flexibility and as stabilizer to minimize decomposition in<br />
polyvinyl chloride (PVC) products.<br />
Reaction of oxirane ring with HCl inhibits the degradation process.<br />
Epoxidation process is followed by quantification of some analytes related to<br />
the product’s quality:<br />
♣The epoxide index (E.I.) is directly related to the stabilizer feature of the product. The<br />
higher the epoxide content, the more efficient the additive as thermal stabilizer.<br />
♣The iodine content (I.I.) is an indicator to the amount of unsaturations present in the<br />
epoxidized soybean oil.<br />
♣The percentage of water (% Water), results from washing of the final product. Its<br />
concentration must be minimal since water can cause degradation of the epoxide group.<br />
DETERMINAÇÃO DA PORCENTAGEM DE ÁGUA<br />
(A) 7050-7290, 5190-5310 cm -1 (B) 7110-7230, 5130-5310 cm -1 C) 6930-7350, 4500-5910 cm -1<br />
(A) Espectros de Maior e Menor concentração<br />
(B) Correlograma.<br />
(C) Pesos e vetor de regressão.<br />
Tabela I. Resulta<strong>dos</strong> <strong>dos</strong> modelos <strong>PLS</strong> para a água.<br />
Método # Variables Latent Var. SECV PRESS R<br />
Boxcar<br />
averaging<br />
160 3 0,011 0,006 0,992<br />
Seleção A 14 3 0,012 0,007 0,992<br />
Seleção B a<br />
12 3 0,013 0,008 0,990<br />
Seleção C 63 3 0,011 0,006 0,993<br />
Prev. externa b<br />
14 3 0,013 c 0,002<br />
a Seleção de variáveis feita pelo correlograma para cutoff = 0,80. b Previsão com<br />
um conjunto de da<strong>dos</strong> externo. Modelo <strong>PLS</strong> com variáveis selecionadas em A.<br />
c SEP (standard error of prediction).<br />
C) 6930-7350, 4500-5910 cm -1<br />
METODOLOGIA<br />
NIR absorbance spectra were recorded from<br />
9300 cm-1 to 4500 cm-1 with a 2 cm-1<br />
increment, using a BOMEM – MB160 – FTIR<br />
spectrophotometer.<br />
DADOS ORIGINAIS (2400 VARIÁVEIS)<br />
DADOS REDUZIDOS (160 VARIÁVEIS)<br />
SELEÇÃO A<br />
(Diferença espectral)<br />
SELEÇÃO C<br />
(Pesos e vetor de regressão)<br />
VALIDAÇÃO EXTERNA<br />
(usando o melhor modelo)<br />
Média móvel (Box car)<br />
SELEÇÃO B<br />
(Correlograma)<br />
Porcentagem de água. Valores experimentais, estima<strong>dos</strong>* e os resíduos<br />
Sample Exp. Values Pred. Values Residuals<br />
9 0,06 0,048 -0,012<br />
15 0,07 0,060 -0,010<br />
19 0,05 0,048 -0,002<br />
27 0,08 0,083 0,003<br />
44 0,19 0,219 0,029<br />
48 0,13 0,144 0,014<br />
50 0,13 0,121 -0,009<br />
53 0,16 0,149 -0,011<br />
56 0,06 0,047 -0,013<br />
60 0,008 0,006 -0,002<br />
Mean 0,094 0,093 -0,001<br />
Std. 0,056 0,064 0,014<br />
Range 0,182<br />
RPDa 4,00 RERb 13,00<br />
*(<strong>PLS</strong> 3VLs). aRPD =std(exp.)/std(residuals). bRER = range(exp.)/std(residuals).<br />
6
FATOR DE BIOCONCENTRAÇÃO (BCF) DE HIDROCARBONETOS POLICÍCLICOS<br />
AROMÁTICOS (PAHS).<br />
Ferreira, M. M. C.;Chemosphere 2001, 44, 125.<br />
Estudo da relação entre as características estruturais de alguns PAHs e a sua<br />
bioacumulação em invertebra<strong>dos</strong> aquáticos (Daphnia Magna). O fator de<br />
bioconcentração foi obtido de medidas experimentais da concentração de uma<br />
substância presente num organismo aquático e no ambiente que o cerca, de acordo com<br />
a expressão<br />
Corg<br />
BCF Cw<br />
Corg é a concentração do poluente no<br />
organismo (mg/kg) e Cw é a sua concentração em água pura (mg/l).<br />
1<br />
9<br />
2<br />
5 6<br />
10<br />
3<br />
7<br />
11<br />
8<br />
4<br />
Quatro descritores foram utiliza<strong>dos</strong> para modelar o<br />
fator de bioconcentração dado por logBCF,<br />
dois experimentais: logS e logP<br />
dois calcula<strong>dos</strong> teoricamente: volume molecular,<br />
Vol, e o índice de conectividade, Xv.<br />
Variância percentual e acumulada da<br />
análise PCA e SEP <strong>dos</strong> modelos de regressão.<br />
val<br />
LV %Var %Varacumulada SEPval* 1 95,09 95,09 0,295<br />
2 3,50 98,59 0,323<br />
3 1,30 99,89 0,406<br />
4 0,11 100,00 0,478<br />
*Erro padrão de predição da validação cruzada.<br />
Uma variável latente descrevendo 95,09% da informação original <strong>dos</strong> da<strong>dos</strong> é o número<br />
ótimo de fatores para a construção do modelo <strong>PLS</strong>: o que produz o menor erro padrão<br />
de validação (0,295).<br />
Apenas o logBCF do fenantreno e do trifenileno, foram estima<strong>dos</strong> com erro maior que<br />
10%.<br />
Valores experimentais e estima<strong>dos</strong> de logBCF<br />
para PAHs no invertebrado aquático Daphnia-<br />
Magna.<br />
Valores experimentais e estima<strong>dos</strong> a do fator de bioconcentração<br />
de PAHs no invertebrado aquático Daphnia-Magna.<br />
Exp.<br />
Est.<br />
Res.<br />
1-Naftaleno<br />
logBCF<br />
2,12<br />
logBCF<br />
b<br />
2,167 -0,047<br />
2-Antraceno 2,95 2,948 0,002<br />
3-Fenantreno 2,51 2,887 -0,377<br />
4-Benzo[a]antraceno 4,00 3,744 0,256<br />
5-Criseno 3,79 3,738 0,047<br />
6-Trifenileno 3,96 3,478 0,482<br />
7-Pireno 3,43 3,295 0,135<br />
8-Perileno 3,86 3,965 -0,105<br />
9-Benzo[a]pireno 3,82 4,019 -0,199<br />
10-<br />
Dibenzo[a,h]antraceno<br />
4,00 4,355 -0,355<br />
11-Benzo[ghi]perileno 4,45 4,288 0,162<br />
SEPval Q<br />
0,295 SEPval 0,272<br />
2<br />
0,81 R 2<br />
0,87<br />
Coef. de regressão: Xv = 0,246<br />
c<br />
F = 60.018 p < 0.0001<br />
Vol = 0,225 logP = 0,246 logS = -0,238<br />
log(BCF) = 0,694 + 0,0959 Xv + 0,0022 Vol + 0,163 logP 0,109 log S<br />
aModelo <strong>PLS</strong> com da<strong>dos</strong> autoescala<strong>dos</strong>, 1 variável latente (LV)<br />
e validação cruzada removendo uma amostra de cada vez.<br />
b Para Daphnia-Pulex. c F é o teste de significância estatística<br />
de Fischer e p o nível de confiabilidade da equação.<br />
Matriz de correlação <strong>dos</strong> descritores.<br />
Xv Vol logp logS<br />
Xv 1,000 0,924 0,994 0,954<br />
Vol 1,000 0,935 0,834<br />
logP 1,000 0,964<br />
logS 1,000<br />
Como to<strong>dos</strong> eles são muito<br />
eleva<strong>dos</strong>, é impossível construir<br />
um modelo MLR, mas isto não se<br />
constitui num problema quando se<br />
usa os méto<strong>dos</strong> PCR ou <strong>PLS</strong>.<br />
LIPOFILIA DE ALGUNS ÁCIDOS INDOL-3-ACÉTICOS MONOSSUBSTITUIDOS<br />
Os áci<strong>dos</strong> indol-3-acéticos são importantes hormônios de crescimento de plantas da<br />
classe auxina. Vários substituintes pequenos em diferentes posições do anel indol (2, 4,<br />
5, 6 e 7) são os responsáveis pelas mudanças nas propriedades físico-químicas e na<br />
atividade biológica das auxinas.<br />
A estrutura de áci<strong>dos</strong> indol-3-acéticos.<br />
5<br />
6<br />
4<br />
7<br />
3a<br />
8 9<br />
CH CO H 2 2<br />
3<br />
7a N1<br />
H<br />
O parâmetro de lipofilia de 14 auxinas, dado pelo logaritmo da razão entre P<br />
(coeficiente de partição entre as fases orgânica/aquosa) do ácido indol-3-acético<br />
substituído e o do ácido não substituído (IAA) foi medido experimentalmente por RP-<br />
HPLC e usado como variavel dependente no estudo QSAR.<br />
2<br />
7
Descritores:<br />
a polarizabilidade molecular média (E),<br />
os momentos da inércia em relação aos eixos principais de inércia Y (I 2 ) e Z (I 3 ),<br />
a massa molar relativa (M r )<br />
o raio de van der Waals (r) do substituinte,<br />
O tamanho e propriedades eletrônicas do substituinte, bem como a posição de substituição,<br />
são em princípio importantes no estudo da lipofilia das auxinas.<br />
O composto 2Me-IAA se mostrou anômalo (outlier),<br />
pois tem uma leverage e um resíduo de Student<br />
acima do desejável em ambos os modelos e<br />
portanto será removido do conjunto de treinamento.<br />
Exp. a Est. b (PCR) Res (PCR) Est. c (MLR) Res (MLR)<br />
IAA 0,00 -0,03 0,03 -0,12 0,12<br />
4F-IAA 0,12 0,12 0,00 0,11 0,01<br />
5F-IAA 0,17 0,17 0,00 0,19 -0,02<br />
6F-IAA 0,19 0,21 -0,02 0,21 -0,02<br />
7F-IAA 0,18 0,18 0,00 0,16 0,02<br />
4Me-IAA 0,23 0,26 -0,03 0,25 -0,02<br />
5Me-IAA 0,32 0,29 0,03 0,31 0,01<br />
6Me-IAA 0,33 0,34 -0,01 0,34 -0,01<br />
7Me-IAA 0,30 0,30 0,00 0,29 0,01<br />
4Cl-IAA 0,31 0,36 -0,05 0,36 -0,05<br />
5Cl-IAA 0,49 0,43 0,06 0,43 0,06<br />
6Cl-IAA 0,50 0,55 -0,05 0,56 -0,06<br />
7Cl-IAA 0,45 0,44 0,01 0,41 0,04<br />
SEPval 0,031 0,046<br />
R 2<br />
Q<br />
0,98 0,99<br />
2<br />
0,96 0,93<br />
Coeficientes de Regressão E<br />
I2<br />
I 3<br />
M r<br />
r<br />
0,351<br />
0,231<br />
0,203<br />
0,064<br />
0,289<br />
0,370<br />
-0,114<br />
0,691<br />
-0,095<br />
0,235<br />
Foram então construí<strong>dos</strong> modelos PCR e MLR (modelo PCR com todas as componentes<br />
principais A=J=5).<br />
PCR <strong>dos</strong> da<strong>dos</strong> autoescala<strong>dos</strong> e validação cruzada, removendo uma amostra por vez,<br />
mostrou que três PCs contendo 98,73% da informação original <strong>dos</strong> da<strong>dos</strong> é o número<br />
ótimo de PCs pois foi o modelo que apresentou o menor erro padrão de validação:<br />
SEP val = 0,031.<br />
Variâncias percentual e total acumulada, e SEP do modelo de<br />
regressão PCR.<br />
PCs %Var %Varacumulada SEPval a<br />
SEPcal b<br />
1 75,13 75,13 0,036 0,033<br />
2 17,05 92,18 0,033 0,029<br />
3 6,55 98,73 0,031 0,024<br />
4 0,96 99,69 0,035 0,024<br />
5 0,31 100,00 0,046 0,021<br />
8