Apostila QBQ 230N - Instituto de QuÃmica - USP
Apostila QBQ 230N - Instituto de QuÃmica - USP
Apostila QBQ 230N - Instituto de QuÃmica - USP
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
UNIVERSIDADE DE SÃO PAULOINSTITUTO DE QUÍMICABIOQUÍMICA <strong>QBQ</strong><strong>230N</strong>Biologia NoturnoProfessores :Alexan<strong>de</strong>r Henning Ulrich, Bloco 8 sup., sala 853.Mario Jose Politi, Bloco 12 sup., sala 1258.Monitores:Ariane Ferreira Nunes Alves email:anunesalves@usp.brArquime<strong>de</strong>s Cheffer email: arquiqbq@iq.usp.brErika <strong>de</strong> S. Molina email: molina.kk@gmail.comTalita Glaser email:talita.glaser@usp.br2013
ÍNDICEBIOQUÍMICA <strong>QBQ</strong><strong>230N</strong>.INTRODUÇÃO E NORMAS GERAIS..........................................................................................................................3NORMAS E RECOMEDAÇÕES NO LABORATÓRIO...............................................................................................3AVALIAÇÃO..................................................................................................................................................................4BIBLIOGRAFIA RECOMENDADA..............................................................................................................................4CALENDÁRIO DE MÓDULOS E ATIVIDADES 2013...............................................................................................5MÓDULO 1: ÁGUA; REAÇÃO ÁCIDO-BASE, PH E SISTEMA TAMPÃO..............................................................6MÓDULO 2: AMINOÁCIDOS: ESTRUTURA, PROPRIEDADES QUIMICAS.........................................................7MICROPIPETADORES.................................................................................................................................................10MÓDULO 3: PROTEINAS: ESTRUTURA PRIMARIA..............................................................................................12Laboratório 1 FRACIONAMENTO DE PROTEÍNAS:................................................................................................13MÓDULO 4: INTRODUÇÃO À CINÉTICA E TERMODINÂMICA QUIMICA.................................................... 21Laboratório 2 COLORIMETRIA E ESPECTROMETRIA:..........................................................................................26MÓDULO 5: PROTEINAS: ESTRUTURA 3D E CONFORMAÇÃO.........................................................................30MÓDULO 6: CINÉTICA ENZIMÁTICA.....................................................................................................................33Laboratório 3: CINÉTICA DA INVERTASE ...............................................................................................................37Laboratório 4: REAÇÃO DE TRANSAMINAÇÃO.....................................................................................................41MÓDULO 7: AÇÚCARES; ESTRUTURA E FUNÇÃO..............................................................................................47MÓDULO 8: GLICÓLISE.............................................................................................................................................51MÓDULO 9: ACETIL-COA e CICLO DE KREBS......................................................................................................54MÓDULO 10: CADEIA RESPIRATÓRIA E FOSFORILAÇÃO OXIDATIVA.........................................................55MÓDULO 11: GLICONEOGÊNESE............................................................................................................................57MÓDULO 12. ÁCIDOS GRAXOS: ESTRUTURA, FUNÇÃO E METABOLISMO..................................................58MÓDULO 13: LÍPIDEOS, MEMBRANA & TRANSPORTE......................................................................................60MÓDULO 14: CICLO DAS PENTOSES......................................................................................................................63MÓDULO 15. FOTOSSÍNTESE...................................................................................................................................64MÓDULO 16: METABOLISMO DO GLICOGÊNIO E CONTROLE HORMONAL DO METABOLISMO .........66MÓDULO 17: METABOLISMO DE AMINOÁCIDOS...............................................................................................71MÓDULO 18: CICLO DO NITROGÊNIO...................................................................................................................722
INTRODUÇÃO E NORMAS GERAISA disciplina <strong>de</strong> Bioquímica (<strong>QBQ</strong>230-noturno) compreen<strong>de</strong> o programa <strong>de</strong> 18 módulosapresentado no calendário abaixo. Cada módulo focaliza um tópico a ser <strong>de</strong>senvolvidoem um dia <strong>de</strong> aula, envolvendo 2 ativida<strong>de</strong>s:a) Aula expositiva pelo professor, eventualmente complementada por umdos monitores;b) Grupos <strong>de</strong> discussão centrada em questões objetivas, coor<strong>de</strong>nadospelos monitores.Além <strong>de</strong>stes módulos, <strong>de</strong>senvolvidos em sala <strong>de</strong> aula, haverá também um conjunto <strong>de</strong>5 módulos <strong>de</strong> laboratório, consistindo na execução <strong>de</strong> tarefas <strong>de</strong> bancada comprotocolos antecipadamente preparados.No primeiro dia <strong>de</strong> aula serão organizados conjuntos <strong>de</strong> no máximo 5 estudantes quepermanecerão fixos por todo o curso tanto para os grupos <strong>de</strong> discussão como para aspráticas <strong>de</strong> laboratório..NORMAS E INSTRUÇÕES PARA O LABORATÓRIOUSO DE AVENTAL NAS AULAS PRÁTICAS É OBRIGATÓRIO. COMER, BEBER EFUMAR NO RECINTO DO LABORATÓRIO NÃO É PERMITIDO.- Leia cuidadosamente os protocolos experimentais e atente para as instruçõesdos monitores antes <strong>de</strong> iniciar o experimento.- Familiarize-se com o ambiente do laboratório, particularmente, com osreagentes, vidraria e equipamentos disponíveis, procurando utiliza-los comproprieda<strong>de</strong> para evitar erros experimentais, <strong>de</strong>sperdícios <strong>de</strong> material eaci<strong>de</strong>ntes.- Mantenha sua bancada <strong>de</strong> trabalho organizada e livre <strong>de</strong> objetos e usopessoal. Ao terminar o experimento passe água na vidraria utilizada e acoloque no local indicado.- Qualquer dúvida ou aci<strong>de</strong>nte peça auxílio aos monitores, ao professor ou àtécnica do laboratório.- Registre seus resultados em ca<strong>de</strong>rno, pois serão indispensáveis nas PROVASLAB (veja no calendário).3
AVALIAÇÃOA avaliação <strong>de</strong> <strong>de</strong>sempenho será composta dos seguintes itens:a) Provas em grupo (PROVAS LAB e PG), envolvendo trabalho emgrupo para resolução <strong>de</strong> questões objetivas por um período <strong>de</strong> 4 h,com consultas a livros, apostilas e anotações <strong>de</strong> ca<strong>de</strong>rno. Notem queos registros das observações qualitativas e resultados quantitativosdas práticas <strong>de</strong> laboratório serão necessários e obrigatórios nasPROVAS LAB.b) Provas escritas individuais <strong>de</strong> avaliação (Av1, Av2 e Av3).O cálculo da média final consistirá na soma das seguintes parcelas: [(média dasPROVAS LAB) X 2 ] + [(média dos GDs) X 0,5] + [ Av1 X 2] + [Av2 X 2,5] + [Av3 X 3,0]dividida por 10.Haverá uma única prova substitutiva para substituir uma das avaliações individuais.Reposições das PROVAS LAB E PG não serão possíveis. A presença em todas asativida<strong>de</strong>s é obrigatória e será registrada em lista diária <strong>de</strong> presença. É importante<strong>de</strong>stacar que faltas a laboratório incorrerão em redução <strong>de</strong> nota na PROVA LABcorrespon<strong>de</strong>nte. Alunos que alcançarem a média final 5,0 e mostrarem freqüência 70% estarão aprovados. Aqueles cuja média for no mínimo igual a 3,0 eapresentarem freqüência 70% po<strong>de</strong>rão fazer a prova <strong>de</strong> recuperação.BIBLIOGRAFIA RECOMENDADADois bons livros texto em português:TORRES, B. B. & MARZZOCCO, A. Bioquímica Básica;VOET, D. ; VOET, J. & PRATT, C. W. Fundamentos <strong>de</strong> Bioquímica;e mais 3 outros, também excelentes, em inglês:VOET, D. & VOET, J. Biochemistry;BERG, J. M., TYMOCZKO, J. L. & STRYER, L. Biochemistry;LEHNINGER, A. L. Principles of Biochemistry;estarão disponíveis para consulta na sala <strong>de</strong> aula durante as discussões em grupo.4
DEZ.NOVEMBROOUTUBROSETEMBROAGOSTOCALENDÁRIO DE MÓDULOS E ATIVIDADES 2013DATA PROF ATIVIDADE TÍTULO AVALIAÇÃOHENNINGÁgua; Reação ácido-base, pH e Sistema tampão. Equilíbrio1Tquímico2 HENNING T Aminoácidos: Estrutura, proprieda<strong>de</strong>s químicas provinhaPOLITIProteínas: análise <strong>de</strong> sequências e métodos <strong>de</strong> separação e8T+MManálise9 POLITI MM+ED Proteínas: Estrutura (software) Provinha15 HENNING P Prática: Fracionamento <strong>de</strong> proteínas Relatório16 HENNING T Introdução à Cinética e Termodinâmica Química22 POLITI P Prática: Colorimetria e espectrofotometria Relatório23 POLITI T Cinética enzimática Provinha29 HENNING T+MM cont. Cinética enzimática30 HENNING AVALIAÇÃO 1 AVALIAÇÂO5-6 Feriado SEMANA DA PÁTRIA12 HENNING T+MM Lipí<strong>de</strong>os, membranas e transporte13 HENNING T Açúcares: estrutura e função Provinha19 POLITI ED+MM Introdução ao metabolismo20 POLITI P Prática: Cinética da invertase Relatório26 HENNING ED+T Glicólise Provinha27 HENNING T Ciclo <strong>de</strong> Krebs Provinha3-4 Feriado Semana Temática da Biologia – não haverá aula10 HENNING T+MM Ca<strong>de</strong>ia respiratória e fosforilação oxidativa11 HENNING T+MM Ca<strong>de</strong>ia respiratória e fosforilação oxidativa Provinha18 HENNING AVALIAÇÃO 2 AVALIAÇÃOHENNINGOxidação <strong>de</strong> ácidos graxos, metabolismo do etanol e <strong>de</strong> corpos24Tcetônicos25 HENNING T Via das pentoses e síntese <strong>de</strong> ácidos graxos Provinha31 HENNING T Metabolismo do glicogênio e controle hormonal Provinha7 HENNING T Metabolismo <strong>de</strong> aminoácidos e ciclo da uréia8 POLITI P Prática: Reação <strong>de</strong> transaminação Relatório14 POLITI ED+T Integração do Metabolismo Provinha15 Feriado NÃO HAVERÁ AULA21 HENNING T Fotossíntese22 HENNING T Ciclo do Nitrogênio Provinha28 HENNING Plantão <strong>de</strong> Dúvidas29 HENNING AVALIAÇÃO 3 AVALIAÇÃO6 HENNING Plantão <strong>de</strong> Dúvidas7 POLITI AVALIAÇÃO SUBSTITUTIVA AVALIAÇÃO5
MÓDULO 1: ÁGUA; REAÇÃO ÁCIDO-BASE, pH E SISTEMA TAMPÃO1. A molécula <strong>de</strong> água, H 2 O, apresenta um ângulo <strong>de</strong> 104,5 graus entre as duasligações O–H, dando-lhe um caráter altamente polar. Além disso, o átomo <strong>de</strong> O possui2 pares <strong>de</strong> elétrons livres, permitindo a formação <strong>de</strong> ligações (ou pontes) <strong>de</strong> H entremoléculas vizinhas. Esta estrutura dá à água proprieda<strong>de</strong>s físicas e químicas <strong>de</strong>enorme importância biológica.2. A água se ioniza através <strong>de</strong> uma reação ácido-base:H 2 O + H 2 O H 3 O + + OH -A reação ácido-base se caracteriza pela troca <strong>de</strong> prótons entre pares conjugados <strong>de</strong>ácidos e bases. A água po<strong>de</strong> se comportar como ácido e como base:AH + H 2 O H 3 O + + A -B + H 2 O BH + OH -Estas são reações <strong>de</strong> equilíbrio, às quais correspon<strong>de</strong>m constantes <strong>de</strong> equilíbrio<strong>de</strong>finidas. Por exemplo: K = [H 3 O + ] [A - ][AH] [H 2 O]K me<strong>de</strong> a afinida<strong>de</strong> relativa das bases, <strong>de</strong> cada par ácido-base conjugados (AH/ A - eH 3 O + / H 2 O), por prótons. Fala-se comumente em constante <strong>de</strong> dissociação <strong>de</strong> umácido (K a ), significando:K a = K [H 2 O] = [H + ] [A - ], on<strong>de</strong> [H 2 O] é essencialmente constante (55 M).[AH]3. [H + ] é a concentração hidrogeniônica e os valores <strong>de</strong> [H + ] para a maioria dassoluções são muito baixos e difíceis <strong>de</strong> serem comparados. Um valor mais prático éconhecido como pH: pH = - log [H + ] como 1/[H + ] = 1/K x [A - ]/[AH] po<strong>de</strong>-se obterpH = - logK + log [A - ]/[AH] por analogia - log K = pK e pH = pK + log [A - ]/[AH]Conclui-se que pK é numericamente igual a pH da solução na qual as concentraçõesmolares do ácido e sua base conjugada são iguais (ie log [A - ]/[AH] = 0).A igualda<strong>de</strong> pH = pK + log [A - ]/[AH] é conhecida como Equação <strong>de</strong> Hen<strong>de</strong>rson-Hasselbach.4. Ácidos são classificados <strong>de</strong> acordo com sua força relativa, ou seja, <strong>de</strong> acordo comsua capacida<strong>de</strong> <strong>de</strong> transferir um próton para a água. Ácidos com constantes <strong>de</strong>dissociação menores do que aquela <strong>de</strong> H 3 O + (que, por <strong>de</strong>finição, é igual a 1 emsoluções aquosas (vê se consegue confirmar por que!)) são só parcialmente ionizadosem soluções aquosas e são conhecidos como ácidos fracos (K 1). Já os ácidosfortes têm constantes <strong>de</strong> dissociação maiores que a <strong>de</strong> H 3 O + , sendo quasecompletamente ionizados em soluções aquosas (K1).5. Tampões são sistemas aquosos que ten<strong>de</strong>m a resistir a variações no seu pHquando pequenas quantida<strong>de</strong>s <strong>de</strong> ácido (H + ) ou base (OH - ) são adicionadas. Umsistema tampão consiste <strong>de</strong> um ácido fraco (o doador <strong>de</strong> prótons) e sua base6
conjugada (o aceptor <strong>de</strong> prótons). É comum encontrar os seguintes símbolos pararepresentar um ácido (AH ou BH + ) e sua base conjugada (A - ou B:)6. A adição <strong>de</strong> ácido forte (H + ) ou base forte (OH - ) a uma solução aquosa <strong>de</strong> umácido fraco, por exemplo, ácido acético (pK a = 4,76), causa pequenas variações <strong>de</strong> pH,se a solução estiver a um pH próximo do pK do ácido. Este comportamento <strong>de</strong>fine umtampão ácido-base.MÓDULO 2: AMINOÁCIDOS: ESTRUTURA, PROPRIEDADES QUIMICAS1. Aminoácidos, bases purínicas e pirimidínicas, nucleosí<strong>de</strong>os e nucleotí<strong>de</strong>os,hexoses (como glicose), são componentes monoméricos dos principais polímerosbiológicos, ou seja, proteínas, ácidos nucléicos (DNA e RNA) e polissacarí<strong>de</strong>os(glicogênio, amido e celulose). Aminoácidos, bases, nucleosí<strong>de</strong>os e nucleotí<strong>de</strong>os sãomuito solúveis em água e possuem grupos funcionais que participam em reaçõesácido-base. Glicose também é altamente solúvel em água, mas não participa emreações ácido-base.i. Há 20 aminoácidos que compõem proteínas (Tabela 1, p.10), todos mostrando afórmula geral:R+ H 3 N C COO - íon dipolar ou zwitterion encontrado em água pH 7H2. Aminoácidos po<strong>de</strong>m ser agrupados em classes com base nas proprieda<strong>de</strong>s dosseus grupos radicais (R), em particular sua polarida<strong>de</strong> ou tendência <strong>de</strong> interagir comágua em pH biológico ( 7,0).3. Todos os aminoácidos livres comportam como ácidos polipróticos. Quando umaminoácido cristalino é dissolvido em água, ele po<strong>de</strong> agir como um ácido ou comouma base. O grupo carboxílico mostra um pK em torno <strong>de</strong> 2,0, enquanto o grupoamino tem um pK entre 9,0 e 10,0. Portanto, no pH fisiológico (pH 7,0), a maioria dasmoléculas <strong>de</strong> todos os aminoácidos está na forma <strong>de</strong> íons dipolares (zwitterions).Chama-se pI <strong>de</strong> um aminoácido o pH da solução na qual suas moléculaspossuem carga líquida nula. Na ca<strong>de</strong>ia lateral (-R) os aminoácidos apresentamgrupos funcionais, entre os quais existem grupos ácido-base.4. Titulação <strong>de</strong> aminoácidos: A curva <strong>de</strong> titulação mostra como varia o pH em função<strong>de</strong> equivalentes do titulante (ácido ou base forte) adicionados. Para um aminoácido,<strong>de</strong>ve-se observar no mínimo dois patamares nessa curva correspon<strong>de</strong>ndo à titulaçãodos grupos carboxilato e -amino, respectivamente. No meio <strong>de</strong> cada um <strong>de</strong>ssespatamares há um ponto <strong>de</strong> inflexão, cujo valor <strong>de</strong> pH é numericamente igual ao pKa7
do grupo correspon<strong>de</strong>nte. Essa relação numérica entre pH e pKa é facilmentecompreensível da análise da equação <strong>de</strong> Hen<strong>de</strong>rson-Hasselbalch.5. O carbono dos aminoácidos, excetuando-se a glicina, é assimétrico, fazendocom que estas substâncias tenham ativida<strong>de</strong> óptica e, portanto, apresentem pares <strong>de</strong>isômeros ópticos.8
MICROPIPETADORES10
Fonte: http://www.analiticaweb.com.br/11
MÓDULO 3: PROTEINAS: ESTRUTURA PRIMARIA1. A <strong>de</strong>scrição da estrutura das proteínas é dividida em quatro níveis <strong>de</strong> organização:estrutura primária, secundária, terciária e quartenária.2. A estrutura primária se refere à seqüência <strong>de</strong> aminoácidos que compõem aproteína. Trata-se, portanto, da estrutura <strong>de</strong> ligações covalentes. A principal ligaçãocovalente entre aminoácios é a ligação peptídica. Os aminoácidos po<strong>de</strong>m formarpolímeros através da ligação do grupo carboxila <strong>de</strong> um aminoácido com o grupo amino<strong>de</strong> outro. Esta ligação carbono-nitrogênio chamada ligação peptídica, é obtida porexclusão <strong>de</strong> uma molécula <strong>de</strong> água. Quimicamente, a formação da ligação peptídicapo<strong>de</strong> ser representada pela seguinte equação:Esta reação, como está escrita, jamais ocorre nos seres vivos. A união dosaminoácidos por ligação peptídica não é feita por reação direta entre eles, mas através<strong>de</strong> um complexo aparato <strong>de</strong> síntese protéica, que inclui ribossomos, ácidosribonucléicos, várias proteínas e enzimas num processo chamado “tradução”. Aequação mostra apenas o resultado liquido do processo.3. As proprieda<strong>de</strong>s da ligação peptídica impõem restrições ao dobramento dopolímero formado. A ligação peptídica apesar <strong>de</strong> ser representada por um único traço<strong>de</strong> ligação, tem características intermediarias entre uma ligação simples e uma duplaligação, <strong>de</strong>vido às interações entre duas formas <strong>de</strong> ressonância.A conseqüência <strong>de</strong>sse caráter parcial <strong>de</strong> dupla ligação é que não há possibilida<strong>de</strong> <strong>de</strong>rotação em torno da ligação peptídica. Assim sendo, os quatro átomos dosgrupamentos que participam da ligação peptídica ficam dispostos em um plano rígido,constituindo o que se costuma chamar <strong>de</strong> grupo peptídico ou unida<strong>de</strong> peptídica (vi<strong>de</strong>retângulos) Notar também que os dois carbonos alpha (C ) vizinhos <strong>de</strong> cada ligaçàopeptídica também se encontram o plano.12
Marzzocco & Torres, Bioquímica Básica.O polímero formado po<strong>de</strong>, portanto, ser visualizado como uma ca<strong>de</strong>ia constituída porunida<strong>de</strong>s planares (unida<strong>de</strong>s peptídicas), unidas entre si com uma articulação flexível:o carbono α. Esta ca<strong>de</strong>ia chama-se ca<strong>de</strong>ia polipeptídica. As proteínas po<strong>de</strong>m serformadas por uma ou mais ca<strong>de</strong>ias polipeptídicas.4. Todavia, existem pontos <strong>de</strong> dobramento entre as unida<strong>de</strong>s peptídicas rígidas,graças a possibilida<strong>de</strong> <strong>de</strong> rotação em torno das ligações com o carbono alfa (N-Cα eCα-C), que são ligações efetivamente simples (vi<strong>de</strong> figura acima). Estas ligações sãochamadas phi () e psi () respectivamente.5. A ca<strong>de</strong>ia polipeptídica po<strong>de</strong> ser dividida entre a ca<strong>de</strong>ia principal e as ca<strong>de</strong>iaslaterais (grupos R) ligados aos carbonos alfa.LABORATÓRIO 1: FRACIONAMENTO DE PROTEÍNASI. FUNDAMENTOSMétodos <strong>de</strong> Purificação <strong>de</strong> ProteínasÉ possível purificar e isolar proteínas utilizando-se princípios físico-químicos, quelevam em conta as proprieda<strong>de</strong>s características <strong>de</strong>ssas biomoléculas. Uma <strong>de</strong>ssas13
características está baseada na solubilida<strong>de</strong> das diferentes ca<strong>de</strong>ias laterais dosaminoácidos, que <strong>de</strong>pen<strong>de</strong>m da concentração <strong>de</strong> sais dissolvidos no solvente (forçaiônica da solução), da polarida<strong>de</strong> do solvente (constante dielétrica <strong>de</strong>sse solvente), dopH do meio (ponto isoelétrico da proteína) e da temperatura.Em uma solução aquosa <strong>de</strong> baixa força iônica, a solubilida<strong>de</strong> <strong>de</strong> uma proteína, emgeral, aumenta com a concentração salina. Esse fenômeno é conhecido como“salting in”. Em soluções com alta força iônica, entretanto, a solubilida<strong>de</strong> <strong>de</strong> umaproteína em geral <strong>de</strong>cresce, fenômeno que resulta da competição entre os íons salinosadicionados e o soluto (proteína), diminuindo a capacida<strong>de</strong> <strong>de</strong> solvatação do solventeaquoso. Esse fenômeno é conhecido como “salting out”, constituindo uma dastécnicas mais utilizadas para a purificação <strong>de</strong> proteínas. Sulfato <strong>de</strong> Amônio[(NH4) 2 SO 4 ] é o sal mais utilizado para “salting out”, uma vez que sua solubilida<strong>de</strong> éalta (3,9 M a 0C), permitindo gerar soluções aquosas <strong>de</strong> alta força iônica.Proteínas em geral possuem uma gran<strong>de</strong> varieda<strong>de</strong> <strong>de</strong> aminoácidos comgrupamentos ionizáveis com diferentes pKs. A um pH característico para cadaproteína, as cargas positivas da molécula são balanceadas pelas cargas negativas,conferindo à proteína carga total zero. Neste pH, <strong>de</strong>nominado ponto isoelétrico (pI),a molécula torna-se imóvel em presença <strong>de</strong> um campo elétrico. Como po<strong>de</strong> ser vistona Figura 1, a solubilida<strong>de</strong> da lactoglobulina po<strong>de</strong> variar com a concentração salina(NaCl). No entanto, em qualquer caso, ao se ajustar o pH para valores próximos ao pIda proteína, ocorre uma solubilização mínima e a maior fração <strong>de</strong> proteínas ficaráinsolúvel.Em muitas situações, po<strong>de</strong>-se utilizar os conceitos <strong>de</strong> “salting out” e <strong>de</strong>precipitação no pI para purificar uma proteína específica.Solubilida<strong>de</strong>mg/mLpHFigura 1 – Solubilida<strong>de</strong> da lactoglobulina em função do pH em diferentes concentrações <strong>de</strong>NaCl.14
Eletroforese e Separação <strong>de</strong> Proteínas Totais (SDS-PAGE)A separação <strong>de</strong> macromoléculas (proteínas, DNA e RNA) po<strong>de</strong> ser feitaaplicando-se um campo elétrico numa matriz sólida, como um gel ou papel, quecontem a mistura <strong>de</strong> interesse. Esse método, amplamente utilizado, <strong>de</strong>nomina-seeletroforese e baseia-se na migração das moléculas em relação a um campo elétrico,<strong>de</strong>vido à sua carga.Normalmente se utiliza um gel, <strong>de</strong>vido a supressão das correntes <strong>de</strong>convenção produzidas por pequenos gradientes <strong>de</strong> temperatura e também porque ogel funciona como uma peneira molecular, permitindo a separação dasmacromoléculas por peso molecular.O gel <strong>de</strong> eletroforese é constituído <strong>de</strong> um polímero <strong>de</strong> acrilamida cuja estruturaestá <strong>de</strong>monstrada na Figura 2. Esta polimerização ocorre na presença <strong>de</strong> radicaislivres, os quais são gerados por persulfato <strong>de</strong> amônio e estabilizados por TEMED(N,N,N’,N’-tetrametilenenodiamino). A polimerização também <strong>de</strong>pen<strong>de</strong> da presença <strong>de</strong>um agente, o N’N’metileno-bis-acrilamida, que facilita a ligação das ca<strong>de</strong>iras entre si,formando um gel cuja porosida<strong>de</strong> é <strong>de</strong>terminada pelo comprimento das ca<strong>de</strong>ias e pelograu <strong>de</strong> interligação entre estas.Figura 2 – Esquerda: ação <strong>de</strong> peneiramento <strong>de</strong> um gel poroso <strong>de</strong> acrilamida. Direita: formação<strong>de</strong> um gel <strong>de</strong> poliacrilamida. O tamanho do poro po<strong>de</strong> ser controlado pelo ajuste daconcentração do monômero ativado (acrilamida, em azul) e do interligante (bis-acrilamida, emvermelho).A separação <strong>de</strong> proteínas ocorre em condições <strong>de</strong>snaturantes. A mistura <strong>de</strong>proteínas e dissolvida em tampão <strong>de</strong> amostra. Este tampão <strong>de</strong> amostra contém SDS(do<strong>de</strong>cil sulfato <strong>de</strong> sódio), que é um <strong>de</strong>tergente aniônico que acaba rompendo as15
ligações não covalentes existentes na proteína nativa resultando na sua <strong>de</strong>snaturação.Neste tampão também temos -mercaptoetanol que reduz as pontes <strong>de</strong> dissulfetoexistentes na proteína.II. OBJETIVOS1) Precipitar as proteínas totais <strong>de</strong> uma solução <strong>de</strong> leite em pó, utilizando osconceitos <strong>de</strong> precipitação no pI.2) Utilizar eletroforese em gel <strong>de</strong> poliacrilamida/SDS (SDS-PAGE) para separar asproteínas <strong>de</strong> diferentes amostras e estimar sua concentração.III. PROCEDIMENTO EXPERIMENTAL1) Precipitação no pI- Preparar uma série <strong>de</strong> tubos <strong>de</strong> ensaio <strong>de</strong> acordo com a tabela 1Tabela 1 – Preparação dos tubos em diferentes pH’s.Tubo 1 2 3 4 5Ácido Acético 0,1 mM1,0 mLÁcido Acético 1,0 mM1,0 mLÁcido Acético 50 mM1,0 mLÁcido Acético 1,0 M1,0 mLÁcido Acético 2,0 M1,0 mLpH 6,7 5,7 4,7 3,7 2,7Turvação (sim / não)- Adicionar, a cada um dos tubos, uma alíquota (5,0 mL) <strong>de</strong> solução <strong>de</strong> leite em pó<strong>de</strong>snatado (5%, previamente centrifugado).- Agitar os tubos e aguardar 5 minutos- Separar alíquotas <strong>de</strong> 1,0 mL, distribuir em tubos plásticos pequenos e centrifugar(5000 rpm, 5 minutos, temperatura ambiente). Descartar a fase sobrenadante eressuspen<strong>de</strong>r o precipitado em NaOH 0,1M (1,0 mL) (Observação: utilizar o mesmoprocedimento mesmo para os tubos que aparentemente não apresentam precipitado)- Após a dissolução total do precipitado, separar uma alíquota da solução obtida (10,0L) para SDS-PAGE.2) Eletroforese em gel <strong>de</strong> poliacrilamida/SDS (SDS-PAGE)Para este experimento, serão utilizadas como amostras: alíquotas <strong>de</strong> proteínas purificadas anteriormente, a partir <strong>de</strong> uma solução <strong>de</strong>leite em pó (5%) (amostras 1 a 5) a solução contendo o extrato bruto <strong>de</strong> proteínas totais <strong>de</strong> leite em pó (5,0 L)para comparação (amostra 6) Soro bovino diluído a 10% (10,0 L) para comparação (amostra 7)16
Albumina bovina a 4,0 mg/mL (5,0 L) (padrão <strong>de</strong> peso molecular: 66,0 KDa)Montar o aparato para eletroforese conforme figura 3 (o gel <strong>de</strong> eletroforese serápreparado previamente <strong>de</strong> acordo com o apêndice 1), adicionar na cuba o tampão <strong>de</strong>corrida até cobrir os poços do gel para eletroforese.Adicionar tampão <strong>de</strong> amostra (10 L) a cada uma das amostras, e aquecer (2minutos, 100C) para <strong>de</strong>snaturar as proteínas. Resfriar (gelo) e aplicar 15 L nospoços do gel para eletroforese seguindo a or<strong>de</strong>m da tabela 2.TABELA 2 – ADIÇÃO DAS AMOSTRAS AO SDS-PAGEpoço n° 1 2 3 4 5 6 7 8Amostra padrão amostra 1 amostra 2 amostra 3 amostra 4 amostra 5 amostra 6 amostra 7Aplicar a tensão nos eletrodos do aparato <strong>de</strong> eletroforese (150 V) e aguardar (30minutos) até que o corante marcador (Azul <strong>de</strong> Bromofenol) se aproxime da base do gelInterromper a eletroforese e mergulhar o gel em uma solução <strong>de</strong> coloração:Coomassie Blue R (0,25g) em metanol : ácido acético : água (45% : 10% : 45%).Aguardar (5-10 minutos)Substituir a solução <strong>de</strong> coloração pela solução <strong>de</strong> <strong>de</strong>scoloração: metanol : ácidoacético : água (45% : 10%: 45%) (15 minutos)Verificar as proteínas coradas, e estimar por comparação, a purificação da amostra.V. APÊNDICEPreparação do gel <strong>de</strong> acrilamida / SDSInicialmente montam-se as placas <strong>de</strong> vidro com os espaçadores posicionados. Vedaro espaço entre as placas com agarose (1% aquecida em ebulição). Aguardarresfriamento.PRECAUÇÕES: Acrilamida é neurotóxica quando não polimerizada. Utilize sempreluvas <strong>de</strong>scartáveis para manipular soluções contendo acrilamida. Evite inalar TEMED(mesmo diluído, po<strong>de</strong> ser tóxico) e butanol.Preparar a solução para o gel <strong>de</strong> resolução (<strong>de</strong> “corrida”): água <strong>de</strong>stilada (3,7 mL) solução A (1,8 mL) solução B (1,9 mL) APS (Persulfato <strong>de</strong> Amônio) (0,12 mL) (solução a 10%) TEMED (0,45 mL) (diluído 40 vezes)OBS: Adicionar o TEMED por último, pois ele o agente polimerizante <strong>de</strong>ste gel.Utilizar a solução imediatamente após o preparo (aplicando-a no espaço entre asplacas <strong>de</strong> vidro com uma pipeta. Serão necessários aproximadamente 4,0 mL <strong>de</strong>17
solução. Aguardar a polimerização do gel (5 minutos). Será necessário <strong>de</strong>ixaraproximadamente 1,0 cm <strong>de</strong> espaço para aplicar o gel <strong>de</strong> empilhamentoOBS: A solução começa a polimerizar muito rapidamente, é necessário atenção erapi<strong>de</strong>z para aplicar a solução no aparato <strong>de</strong> eletroforese.Preparar a solução para o gel <strong>de</strong> empilhamento: Água <strong>de</strong>stilada (1,66 mL) Solução A (0,3 mL) Solução C (0,75 mL) APS (Persulfato <strong>de</strong> Amônio) (0,05 mL) (solução a 10%) TEMED (0,24 mL) (diluído 40 vezes)OBS: Adicionar o TEMED por último, pois ele o agente polimerizante <strong>de</strong>ste gel.Utilizar a solução imediatamente após o preparo, aplicando-a sobre o gel <strong>de</strong>resolução (<strong>de</strong>ve preencher um espaço <strong>de</strong> cerca <strong>de</strong> 1 cm <strong>de</strong> altura). Colocar um penteplástico para formar os poços on<strong>de</strong> as amostras serão aplicadas (<strong>de</strong> acordo com a<strong>de</strong>monstração). Serão necessários aproximadamente 1,60 mL <strong>de</strong> solução. Aguardar apolimerização do gel (15 minutos)OBS: A solução começa a polimerizar muito rapidamente, é necessário atenção erapi<strong>de</strong>z para aplicar a solução no aparato <strong>de</strong> eletroforese.Soluções utilizadasSolução A: Acrilamida e bis-acrilamida45 g acrilamida1,2 g bis-acrilamidaágua <strong>de</strong>stilada (até 100 mL)Solução B: Tris-HCl pH 8,818,17 g Tris (em 50 mL <strong>de</strong> água <strong>de</strong>stilada)Ajustar o pH para 8,8 (com HCl)Adicionar SDS (4,0 mL, solução a 10%)Completar o volume com água <strong>de</strong>stilada (até 100 mL)Solução C: Tris-HCl pH 6,86,06 g Tris (em 50 mL <strong>de</strong> água <strong>de</strong>stilada)Ajustar o pH para 6,8 (com HCl)Completar o volume com água <strong>de</strong>stilada (até 100 mL)Tampão <strong>de</strong> corrida:3,0 g <strong>de</strong> Tris, 14,4 g <strong>de</strong> Glicina e 10, 0mL <strong>de</strong> SDS (10%)Ajustar o volume <strong>de</strong> água <strong>de</strong>stilada para 1000 mL18
Tampão <strong>de</strong> amostra:SDS 10% (5,0 mL), 2-mercaptoetanol (0,5 mL), Glicerol (2,0 mL), EDTA 0,1M(0,1 mL), Azul <strong>de</strong> Bromofenol 1% (1,0 mL), Solução C (2,5 mL) e água<strong>de</strong>stilada (até 20,0 mL).19
Figura 3 – Esquema do aparato para eletroforese.20
MÓDULO 4: INTRODUÇÃO À CINÉTICA E TERMODINÂMICA QUIMICA1. A variação <strong>de</strong> energia livre padrão é diretamente relacionada à constante <strong>de</strong>equilíbrio:G o = -2.3RT log K eq2. A composição <strong>de</strong> um sistema <strong>de</strong> reação (uma mistura <strong>de</strong> reagentes e produtos)ten<strong>de</strong> a uma variação contínua até que o equilíbrio é alcançado. No equilíbrio, as taxas<strong>de</strong> reação para um lado e para outro são exatamente iguais. As concentrações <strong>de</strong>reagentes e produtos no equilíbrio <strong>de</strong>finem a constante <strong>de</strong> equilíbrio. Na reação:A + BC + D, a constante <strong>de</strong> equilíbrio é dada por:K eq = [C][D] / [A][B]3. Quando um sistema não está em equilíbrio, ele ten<strong>de</strong> ao equilíbrio, e a magnitu<strong>de</strong><strong>de</strong>sta tendência po<strong>de</strong> ser medida como a variação <strong>de</strong> energia livre da reação, G. Aenergia livre <strong>de</strong> Gibbs (G), uma proprieda<strong>de</strong> termodinâmica, é <strong>de</strong>finida pela equação:G = H – TS, on<strong>de</strong> H, T e S são respectivamente entalpia, temperatura absoluta eentropia, todas também proprieda<strong>de</strong>s termodinâmicas.4. Numa transição <strong>de</strong> estado a temperatura (T) e pressão constantes (condiçõescomuns às reações bioquímicas) a variação <strong>de</strong> G (G) é: G = H - TS.Se se trata <strong>de</strong> uma reação bioquímica, H é o calor <strong>de</strong> reação. Quando H é positivoa reação é endotérmica, se H for negativo a reação é exotérmica. Nestas condições,a espontaneida<strong>de</strong> da reação é <strong>de</strong>finida pelo valor <strong>de</strong> G: se G é negativo, a reação éespontânea, sendo <strong>de</strong>nominada exergônica. Se, ao contrário, G for positivo, a reaçãonão ocorre espontaneamente e é <strong>de</strong>nominada en<strong>de</strong>rgônica. Portanto, a reação ocorreno sentido em que a energia livre total diminui.4. No equilíbrio, G = 0. Logo, é possível <strong>de</strong>monstrar a valida<strong>de</strong> das seguintesigualda<strong>de</strong>s:G = G + 2,3 RT logB/A B/A = K G = - 2,3 RT logK5. Em condições padrão, à 25C (298K), com concentrações <strong>de</strong> reagentes e produtosiguais a 1M, pH = 0, a variação <strong>de</strong> energia livre é consi<strong>de</strong>rada padrão, ou G.Entretanto, a maioria das reações bioquímicas ocorrem em pH 7,0, para as quaisutiliza-se G´.6. A Figura 4 (p.35) mostra esquematicamente como varia G com o <strong>de</strong>senvolvimentoda reação, indicado no eixo das abcissas como coor<strong>de</strong>nada <strong>de</strong> reação.Para que a reação ocorra, necessariamente tem-se G final G inicial , isto é, G é negativo.Um ponto importante a ser <strong>de</strong>stacado é que o valor <strong>de</strong> G permite prever se a reaçãopo<strong>de</strong> ocorrer, mas não a velocida<strong>de</strong> com que a reação atinge o equilíbrio. Avelocida<strong>de</strong> <strong>de</strong> reação <strong>de</strong>pen<strong>de</strong> da energia livre do Estado <strong>de</strong> Transição que é maior21
que do que o dos reagentes no Estado Inicial, isto é, G* é positivo. Quanto maior ovalor <strong>de</strong> G*, menor será a velocida<strong>de</strong> <strong>de</strong> reação.7. Na reação genérica A B a velocida<strong>de</strong> (v) é proporcional a [A], isto é, v 1 =k 1 [A]. Avelocida<strong>de</strong> da reação inversa será, consequentemente, v -1 =k -1 [B]. k 1 e k -1 sãoconstantes <strong>de</strong> velocida<strong>de</strong> e reações como AB e BA são ditas <strong>de</strong> primeira or<strong>de</strong>m,porque as suas respectivas velocida<strong>de</strong>s <strong>de</strong>pen<strong>de</strong>m <strong>de</strong> concentração molar <strong>de</strong> umúnico reagente elevado à potência 1. As constantes <strong>de</strong> velocida<strong>de</strong> k 1 e k -1 sãodiferentes da constante <strong>de</strong> equilíbrio da reação, K=[B]/[A]. No estado <strong>de</strong> equilíbrio, por<strong>de</strong>finição, v 1 =v -1 e, portanto, formalmente, K=k 1 /k -1 . As reações representadas pelasequações seguintes: 2AB e A+BC são <strong>de</strong> segunda or<strong>de</strong>m, cujas velocida<strong>de</strong>s são,respectivamente, v=k A [A] 2 e v=k AB [A][B]. Notar que a or<strong>de</strong>m da reação não coinci<strong>de</strong>necessariamente com a estequiometria da equação química.8.EnergiaLivre(G)Estado <strong>de</strong> Transição(T)G*Estado Inicial (S)G°'Estado Final (P)Coor<strong>de</strong>nada <strong>de</strong> ReaçãoVariação <strong>de</strong> energia livre (G) no <strong>de</strong>correr <strong>de</strong> uma reação genérica.9. As quinases formam uma classe muito importante e abundante <strong>de</strong> enzimas, que secaracterizam por catalisar a transferência <strong>de</strong> um grupo fosfato <strong>de</strong> alta energia parauma outra substância receptora.10. São chamados compostos <strong>de</strong> alta energia substâncias orgânicas com o grupofosfato em ligações anidrido ou fosfoenol, cuja hidrólise libera fostato inorgânico (Pi)com um G 0’ negativo e em valor absoluto superior a 8kcal/mol. Outros compostosfosforilados com o fosfato em ligações ester ou tioester também mostram um G 0’ <strong>de</strong>hidrólise negativo, mas <strong>de</strong> valor absoluto da or<strong>de</strong>m <strong>de</strong> 3kcal/mol. Estas classes <strong>de</strong>compostos estão ilustradas na Tabela 2. O principal composto fosforilado da célula é oATP; cuja fórmula estrutural está na Figura 5. O ATP possui fosfato em ligaçõesanidrido e ester, aos quais correspon<strong>de</strong>m G 0’ <strong>de</strong> hidrólise <strong>de</strong>, respectivamente, -22
8kcal/mol e -3,5kcal/mol. Todas estas reações são, portanto, muito voltadas para osprodutos <strong>de</strong> hidrólise, sendo praticamente irreversíveis. No entanto, nenhuma <strong>de</strong>stasreações ocorre na célula a velocida<strong>de</strong> significante se não houver catálise por umaenzima específica, da classe das fosfatases.11. No metabolismo é muito importante a transferência <strong>de</strong> fosfatos <strong>de</strong> um compostofosforilado <strong>de</strong> alta energia para outro. Uma das reações chave <strong>de</strong>ste tipo é:fosfoenolpiruvato + ADP ATP + piruvatoG 0’ =-5kcal/molComo esta reação não ocorre sem catálise, seu controle pela célula é feito através<strong>de</strong> uma enzima quinase específica.NH 2HCNCCNA d e n i n aO -O -O -NCNCH- O - P - O - P - O - P - O - C H 2OOOOHHHHR i b o s eHOOHA MPADPA T PATP = A<strong>de</strong>nosina 5’-trifosfatoNa célula:[ATP] + [ADP] + [AMP] = ConstanteFIGURA 2Fórmula estrutural do ATP.23
12. Além das quinases que catalisam a transferência <strong>de</strong> grupo fosfato do ATP parametabólitos, existem as quinases que tem como substratos proteínas, genericamentereferidas como quinases <strong>de</strong> proteína ou, simplesmente, proteína-quinases.Há alguns milhares <strong>de</strong> proteína-quinases diferentes em um organismo, que catalisama transferência <strong>de</strong> fosfato <strong>de</strong> ATP para o grupo OH da ca<strong>de</strong>ia lateral <strong>de</strong> resíduosespecíficos <strong>de</strong> serina e treonina formando um éster <strong>de</strong> fosfato. As reações <strong>de</strong>ste tiposão genericamente chamadas <strong>de</strong> fosforilações e são modificações covalentes quecausam mudança <strong>de</strong> conformação das proteínas, alterando sua ativida<strong>de</strong> biológica.Por exemplo, um gran<strong>de</strong> número <strong>de</strong> enzimas são fosforiladas para sofrer umatransição do estado inativo ao ativo ou vice-versa. Mais raramente as proteínas sãofosforiladas no grupo enólico <strong>de</strong> resíduos <strong>de</strong> tirosina.24
Compostos fosforilados.RRC OCH 2P+ H 2OC O + P i G o ' = - 13.000 cal/molCH 3FosfoenolcetonaácidoRRC O P+ H 2OC O H + P iG o ' = - 8.000 cal/molOAnidrido fosfóricoOácidoácidoR O P + H 2 O R OH+ P iÉster fosfóricoálcool ácidoG o ' = - 3.000 cal/molR C S CoA+ H 2O R C OH +HS-CoAG o ' = - 3.000 cal/molOTioésterOácidotioálcoolATPA<strong>de</strong>nosina trifosfatoADPA<strong>de</strong>nosina difosfatoAMPA<strong>de</strong>nosina monofosfato+ H 2O ADP + P iácidoácido+ H 2O AMP + P iácido ácido+ H 2O A OH + P iálcool ácido(A<strong>de</strong>nosina)G o ' = - 8.000 cal/molG o ' = - 8.000 cal/molGo ' = - 3.500 cal/molP i = fosfato inorgânico = HPO 42-= PO 32-P(pH=7,4)Na célula:[ATP] + [ADP] + [AMP] = constante25
LABORATÓRIO 2: COLORIMETRIA E ESPECTROFOTOMETRIAI. FUNDAMENTOSA Colorimetria e a Espectrofotometria po<strong>de</strong>m ser conceituadas como um procedimentoanalítico através do qual se <strong>de</strong>termina a concentração <strong>de</strong> espécies químicas mediantea absorção <strong>de</strong> energia radiante (luz).Fotometria é uma técnica <strong>de</strong> análise quantitativa que envolve a medida <strong>de</strong>intensida<strong>de</strong> <strong>de</strong> absorção <strong>de</strong> luz monocromática <strong>de</strong> um composto químico em solução.Serve para i<strong>de</strong>ntificar o comprimento <strong>de</strong> onda característico para cada composto epara quantificação do composto através <strong>de</strong> 1) absorção direta e 2) através <strong>de</strong> métodocolorimétrico. Essa intensida<strong>de</strong> <strong>de</strong> absorção <strong>de</strong>pen<strong>de</strong>:1) do comprimento <strong>de</strong> onda escolhido (normalmente usa o máx - on<strong>de</strong> ocomposto absorve mais luz),2) do percurso que o feixe <strong>de</strong> luz percorrerá na solução e3) da concentração do composto nessa solução.A lei <strong>de</strong> Lambert-Beer estabelece que a absorbância é diretamente proporcional áconcentração da espécie absorvente. A fração <strong>de</strong> luz que passa por uma amostra (atransmitância = I t /I 0 ) está relacionada logaritmicamente, e não linearmente, com aconcentração da amostra (figura 1).A lei <strong>de</strong> Lambert-Beer relaciona esses três fatores e estabelece que:A = .l.cOn<strong>de</strong>:A = absorbância é <strong>de</strong>finida pela reação seguinte: A = - log I t /I 0 , que por seruma razão, não possui unida<strong>de</strong> (I o é intensida<strong>de</strong> <strong>de</strong> luz inci<strong>de</strong>nte; I t éintensida<strong>de</strong> <strong>de</strong> luz transmitida); = absortivida<strong>de</strong> molar (característico <strong>de</strong> cada substância), em L.(mol.cm) -1 ;l = caminho óptico (percurso da luz monocromática na solução), em cm;c = concentração da substância em mol/L.lI 0I t26
Figura 1 – I o é intensida<strong>de</strong> <strong>de</strong> luz inci<strong>de</strong>nte; I t é intensida<strong>de</strong> <strong>de</strong> luz transmitida apóspercorrer o caminho óptico (l) pela solução da amostra.Desta forma, mantendo-se o caminho óptico constante, a absorbância torna-sediretamente proporcional à concentração da substância no respectivo máx .Nestas condições, po<strong>de</strong>mos utilizar uma solução <strong>de</strong> concentração conhecida docomposto a ser analisado (ou outra substância <strong>de</strong> características químicassemelhantes) para construir um diagrama <strong>de</strong> absorbância em função da concentraçãoda substância em questão. Com este diagrama, <strong>de</strong>nominada curva padrão, po<strong>de</strong>mosmedir a quantida<strong>de</strong> do composto em amostras <strong>de</strong> concentração <strong>de</strong>sconhecida, pelasimples medida <strong>de</strong> suas absorbâncias <strong>de</strong>s<strong>de</strong> que, estas estejam nas mesmascondições utilizadas para a construção da curva padrão (mesmos reagentes, mesmatemperatura, etc).Um exemplo <strong>de</strong> uma curva padrão:Absorbância***Concentração (mol/L)**Um dos métodos utilizados para dosagem <strong>de</strong> proteína é chamado <strong>de</strong> métododo Biureto. Esse método faz uso da proprieda<strong>de</strong> <strong>de</strong> íons Cu 2+ em meio alcalino <strong>de</strong>formar ligações com o nitrogênio das ligações peptídicas. Desta reação (reação <strong>de</strong>biureto) resulta uma coloração púrpura intensa. Este fato po<strong>de</strong> ser explorado para se<strong>de</strong>terminar por colorimetria a quantida<strong>de</strong> <strong>de</strong> proteína <strong>de</strong> uma solução. A cor<strong>de</strong>senvolvida numa reação <strong>de</strong> íons <strong>de</strong> Cu 2+ em meio alcalino com estas proteínas<strong>de</strong>ve-se exclusivamente às ligações peptídicas e a sua intensida<strong>de</strong> é proporcional aquantida<strong>de</strong> <strong>de</strong> tais ligações. A absorbância é <strong>de</strong>tectada no espectrofotômetro (figura2).Um outro método para <strong>de</strong>terminar a quantida<strong>de</strong> <strong>de</strong> proteína é baseado no fatoque certos aminoácidos possuem anéis aromáticos o que os leva a absorver emcomprimentos <strong>de</strong> onda específicos na região <strong>de</strong> UV. Bases purínicas e pirimidínicastambém possuem estas proprieda<strong>de</strong>s.27
II. OBJETIVOSFigura 2 – Mo<strong>de</strong>lo <strong>de</strong> um espectrofotômetro.1) Determinação da concentração <strong>de</strong> uma proteína em solução aquosa porfotometria.2) Determinação do espectro <strong>de</strong> absorção <strong>de</strong> luz <strong>de</strong> aminoácidos e bases purínicas epirimidínicas.III. PROCEDIMENTO EXPERIMENTAL1) Determinação da concentração <strong>de</strong> uma proteína em solução aquosa porfotometria1a) Determinação do máx do produto da reação <strong>de</strong> biuretoAdicionar no tubo 1:- 1,0 mL <strong>de</strong> padrão <strong>de</strong> albumina (8 mg/mL),- 0,5 mL <strong>de</strong> água,- 2,5 mL <strong>de</strong> reagente <strong>de</strong> biureto.Adicionar no tubo 2:- 1,5 mL <strong>de</strong> água,- 2,5 mL <strong>de</strong> reagente <strong>de</strong> biureto.Após adição dos reagentes, agitar e incubar os tubos por 15 min a 37 o C.Transferir conteúdo dos tubos para cubetas do espectrofotômetro e ler asabsorbâncias nos comprimentos <strong>de</strong> onda 400, 420, 450, 470, 500, 520, 550, 580, 600,630, 650, 680 e 700 nm. Usar a solução <strong>de</strong> biureto como branco (tubo 2).Com isso, você estará construindo a curva <strong>de</strong> absorbância em função docomprimento <strong>de</strong> onda. Estabelecer qual é o máx do produto da reação <strong>de</strong> biureto.1b) Determinação da concentração <strong>de</strong> proteínaPreparar os tubos como <strong>de</strong>scrito na tabela 1 utilizando uma solução <strong>de</strong> 8 mg/mL <strong>de</strong>albumina (proteína padrão) e a solução <strong>de</strong> proteína <strong>de</strong>sconhecida. No tubo branco não28
<strong>de</strong>verá ser adicionada solução <strong>de</strong> proteína. A or<strong>de</strong>m <strong>de</strong> adição dos componentes dareação <strong>de</strong>ve ser:- primeiro solução <strong>de</strong> proteína,- água,- por último o regente biureto.Após adição do reagente, agitar e incubar os tubos por 15 min a 37 o C.Transferir o conteúdo dos tubos para cubetas do espectrofotômetro e ler asabsorbâncias a 540nm.Utilizando a curva padrão (tubos <strong>de</strong> 1 a 5) e o valor medido <strong>de</strong> absorção a 540nm daamostra <strong>de</strong>sconhecida, calcular a concentração <strong>de</strong> proteína nesta amostra.Tabela 1 – Dados para a construção da curva padrão para <strong>de</strong>terminação <strong>de</strong> concentração <strong>de</strong>proteínas.Padrão <strong>de</strong>proteína água reagente concentraçãotubos albumina<strong>de</strong>sconhecida <strong>de</strong>stilada biureto(mg/mL)(8mg/mL)absorbância(540 nm)branco - - 1,5 mL 2,5 mL1 0,1mL - 1,4 mL 2,5 mL2 0,2mL - 1,3 mL 2,5 mL3 0,4mL - 1,1 mL 2,5 mL4 0,7mL - 0,8 mL 2,5 mL5 1,0mL - 0,5 mL 2,5 mLamostra<strong>de</strong>sconhecida- 1,0 mL 0,5 mL 2,5 mL2) Determinação do espectro <strong>de</strong> absorção <strong>de</strong> luz <strong>de</strong> aminoácidos e bases purínicas epirimidínicas2a) Determinação do máxPipetar 1 mL <strong>de</strong> cada solução em uma cubeta <strong>de</strong> quartzo <strong>de</strong> espectrofotômetro:- Leucina (0,2 mg/mL)- Triptofano (0,004 mg/mL)- Tirosina (0,1 mg/mL)- A<strong>de</strong>nina (0,004 mg/mL)- Timina (0,01 mg/mL)Determinar nas diferentes soluções fornecidas:a) máx ,b) absorbância obtida em máx ,c) calcular <strong>de</strong> cada substância.2b) Determinação da curva <strong>de</strong> absorbância x concentraçãoPara construção da curva <strong>de</strong> absorbância em diferentes concentrações <strong>de</strong> triptofano,pipetar os seguintes volumes e medir a absorbância em máx . (tabela 2).Tabela 2 – Absorbância em máx . em diferentes concentrações <strong>de</strong> triptofano.29
tubosTriptofano(0,01 mg/mL)água <strong>de</strong>stiladabranco - 2,0 mL1 0,1 mL 1,9 mL2 0,2 mL 1,8 mL3 0,4 mL 1,6 mL4 0,7 mL 1,3 mLconcentração(mg/mL)absorbânciaobtidaFazer curva <strong>de</strong> absorbância x concentração e verificar se a mesma obe<strong>de</strong>ce a lei <strong>de</strong>Lambert-Beer.MÓDULO 5: PROTEINAS: ESTRUTURA 3D E CONFORMAÇÃO1. A estrutura secundária é <strong>de</strong>finida pela conformação local do esqueleto <strong>de</strong> ligaçõespeptídicas que compõe o eixo da proteína. Esta conformação local po<strong>de</strong> serexplicitamente expressa através dos ângulos phi () e psi () (vi<strong>de</strong> Módulo 3). Emgeral, certas combinações <strong>de</strong> ângulos phi () e psi () são permitidas enquanto outrasnão são permitidas <strong>de</strong>vido a impedimentos estéricos entre âtomos <strong>de</strong> grupos vizinhos.Este princípio po<strong>de</strong> ser resumido numa diagrama <strong>de</strong> Ramachandran (Figura 1).Diagramas <strong>de</strong> Ramachandran. Esquerda: Estruturas secundáriascorrepon<strong>de</strong>ntes às combinações estericamente permitidas para angulos phi epsi. Direta: ângulos observados para todas as ligações em 12 proteínas comestruturas <strong>de</strong> alta resolução <strong>de</strong>terminadas por cristalografia.2. Há duas estruturas secundárias principais: -hélice (Figura 2) e folha pregueada(Figura 3), que são estruturas organizacionais regulares e repetitivas. Estas duasestruturas po<strong>de</strong>m ser caracterizadas por combinações <strong>de</strong> ângulos phi e psi (Figura 1)30
adotadas pela ca<strong>de</strong>ia principal. Além <strong>de</strong> -hélice e folha , as proteínas globularesmostram também alças <strong>de</strong> formas <strong>de</strong>finidas, mas irregulares e não repetitivas.-hélice.Folha pregueada.3. A estrutura terciária <strong>de</strong>screve o arranjo tridimensional da ca<strong>de</strong>ia principal daproteína, incluindo a disposição espacial das ca<strong>de</strong>ias laterais dos aminoácidos. Hámuitas possibilida<strong>de</strong>s <strong>de</strong> arranjos tridimensionais para a estrutura terciária dasproteínas.a. As proprieda<strong>de</strong>s bioquímicas e biológicas <strong>de</strong> uma proteína são <strong>de</strong>terminadaspelo arranjo tridimensional <strong>de</strong> sua ca<strong>de</strong>ia, isto é, pela sua estrutura terciária. Logo, nascondições fisiológicas a proteína adquire uma estrutura terciária bem <strong>de</strong>finida enecessária à sua função, que é conhecida como estrutura nativa. O <strong>de</strong>sarranjo daestrutura terciária leva à perda <strong>de</strong> função da proteína, processo que é genericamentechamado <strong>de</strong> <strong>de</strong>snaturação.b. Em proteínas pequenas da estrutura primária <strong>de</strong>fine a estrutura terciária nativada proteína. Nestes casos os processos <strong>de</strong> <strong>de</strong>snaturação e renaturação da estruturada proteína são reversíveis. A estrutura nativa é a conformação da proteína <strong>de</strong> menornível <strong>de</strong> energia livre (G) e é alcançada espontaneamente (processo exergônico). Oexemplo clássico <strong>de</strong>sse comportamento é dado pela proteína Rnase A, uma enzimaque no seu estado nativo catalisa a hidrólise <strong>de</strong> RNA. Para proteínas gran<strong>de</strong>s oprocesso <strong>de</strong> <strong>de</strong>snaturação é irreversível e o fenômeno <strong>de</strong> alcance da conformaçãonativa é complexo e ainda mal entendido.c. A estrutura tridimensional das proteínas é mantida por ligações fracas comopontes <strong>de</strong> H, ligações iônicas e interações hidrofóbicas. A exceção é a ponte <strong>de</strong>dissulfeto (-S-S-) que, apesar <strong>de</strong> covalente, é importante na manutenção daconformação nativa <strong>de</strong> proteínas.31
d. Proteínas possuem muitos grupos ionizáveis através <strong>de</strong> reação ácido-base,cujos pKs variam enormemente. O pI <strong>de</strong> uma proteína é <strong>de</strong>finido como pH da soluçãona qual a carga líquida da molécula <strong>de</strong> proteína é nula.4. Existem muitas maneiras diferentes para apresentar estruturas tridimensionais <strong>de</strong>proteínas.Estrutura <strong>de</strong> mioglobina <strong>de</strong> baleia, uma proteína globular típicaTopografia<strong>de</strong> superfícieFita (azul = H)mo<strong>de</strong>lo “space-filling”32
MÓDULO 6: CINÉTICA ENZIMÁTICA1. Enzimas são catalisadores biológicos cuja natureza química é proteica. A naturezaproteica das enzimas lhes proporciona alto grau <strong>de</strong> especificida<strong>de</strong>.2. A gran<strong>de</strong> maioria das reações biológicas não ocorre, ou ocorrem a velocida<strong>de</strong>sbaixíssimas nas condições fisiológicas <strong>de</strong> pH e temperatura. Logo, as reaçõesbiológicas, em geral, necessitam <strong>de</strong> catálise para ocorrer, isto é, necessitam <strong>de</strong>enzimas. Para cada reação há uma enzima específica.3. Na reação genérica A B a direção espontânea da reação é dada pela variação<strong>de</strong> energia livre, .G 0 , conforme esquematizado no gráfico da Figura 5.G 0 é uma constante que se relaciona com a constante <strong>de</strong> equilíbrio da reação pelaexpressão -G 0 =2.3 RTlogK. Por outro lado, as velocida<strong>de</strong>s das reações AB e BAou, respectivamente, as constantes <strong>de</strong> velocida<strong>de</strong> k 1 e k -1 não <strong>de</strong>pen<strong>de</strong>m do G 0 dareação, mas dos, respectivos, G 0 0,1 e G -1 que por sua vez só <strong>de</strong>pen<strong>de</strong>m daenergia livre (G) do estado <strong>de</strong> transição (energias <strong>de</strong> ativação). A enzima(catalisador) não muda o G 0 da reação, pois catalisadores não interferem comos estados inicial e final das reações, mas mudam o “caminho” da reação e, porconseqüência diminuem a energia do Estado <strong>de</strong> Transição.EnergiaLivre (G)G 10#*G 0# -1Estado <strong>de</strong> transição dareação não catalisada*Estado <strong>de</strong> transição dareação catalisadaEstado Inicial(S)(Reagentes)G 0# 1catG 0G 0# -1catEstado Final(P)(Produtos)Coor<strong>de</strong>nada <strong>de</strong> ReaçãoVariação <strong>de</strong> energia livre (G) na reação genérica A B.33
4. Uréia é uma substância muito estável em água, mas que po<strong>de</strong> ser rapidamente<strong>de</strong>compostas por hidrólise se a reação for catalisada pela enzima urease:H 2 NUREASEH 2 NC=O + H 2 O CO 2 + 2 NH 3Trata-se <strong>de</strong> reação <strong>de</strong> primeira or<strong>de</strong>m, on<strong>de</strong> v=k 1 [uréia], apesar <strong>de</strong> a equaçãoestequiométrica indicar a existência <strong>de</strong> 2 reagentes. Esta reação po<strong>de</strong> seracompanhada em tubo <strong>de</strong> ensaio no laboratório.As Tabelas 3 e 4 mostram resultados obtidos na prática.Cinética da enzima urease.Tubo n o Tempo (minuto) NH 3 (moles)1 0 02 2 0.0843 4 0.1684 6 0.2525 8 0.3366 10 0.420Concentração da uréia: 5 mM; Concentração da urease: 0,1 g/mL;Volume <strong>de</strong> reação: 1 mL; Temperatura: 30 o C.Os dados da Tabela anterior mostram que a velocida<strong>de</strong> da reação é constante aolongo do tempo estudado. Já os dados da Tabela seguinte mostram variaçõesrelativamente complexas da velocida<strong>de</strong> <strong>de</strong> reação em função da concentração dauréia para um período <strong>de</strong> 10 minutos <strong>de</strong> reação. Os dados da Tabela seguintepermitem medir experimentalmente duas constantes importantes das reaçõesenzimáticas V max (velocida<strong>de</strong> máxima) e K m (constante <strong>de</strong> Michaelis) através daequação v = V max [S] / (K m + [S]).Cinética da enzima urease.Tubo n Uréia (mM) Urease (g) NH 3 (moles)1 2,5 0,1 0,212 5,0 0,1 0,423 10 0,1 0,594 15 0,1 0,675 25 0,1 0,736 50 0,1 0,787 100 0,1 0,798 200 0,1 0,789 200 - 0,0034
Os significados <strong>de</strong> V max e K m são <strong>de</strong>finidos no mo<strong>de</strong>lo <strong>de</strong> cinética enzimática propostopor Michaelis e Menten no início do século passado on<strong>de</strong> ES é um complexo enzima– substrato formado antes <strong>de</strong> conversão do substrato em produtos.E + S ES E + Pk catk 1k -1A <strong>de</strong>rivação da equação Michaelis – Menten:/ (K m + [S]) é apresentada a seguir.Velocida<strong>de</strong>naquela [S]v = V max [S] / (K m + [S]) = k cat [E t ][S]Velocida<strong>de</strong> máximaConcentraçãodo substratoK diss aparente doComplexo enzima-substratoFração <strong>de</strong> E tot na forma <strong>de</strong> ES =[S]/(K diss + [S])35
5. Substâncias que reduzem a ativida<strong>de</strong> <strong>de</strong> uma enzima são chamadas inibidores.Em termos gerais, inibidores po<strong>de</strong>m atuar em várias maneiras. Aqui vamos focalizarem inibidores que ligam reversivelmente com a enzima com constantes <strong>de</strong>dissociação K I . Estes tipos <strong>de</strong> inibidores po<strong>de</strong>m atuar em duas maneiras diferentes:a) Eles po<strong>de</strong>m competir com o substrato para o mesmo sítio <strong>de</strong> ligação na superfícieda enzima livre. Neste caso são chamados inibidores competitivos ou b) Elespo<strong>de</strong>m ligar em outro sítio na enzima livre (E) e/ou no complexo enzima-substrato(ES). Estes inibidores são chamados inibidores mistos/não-competitivos se po<strong>de</strong>mligar a E e ES e são chamados acompetitivos se ligam somente ao complexo ES.6. A presença <strong>de</strong> um inibidor competitivo se manifesta em uma mudança no valor doK m :K m obs = K m (1+[I]/K I ) = K m on<strong>de</strong> (1+[I]/K I )36
7. A presença <strong>de</strong> um inibidor misto/não-competitivo se manifesta em uma mudançanos valores do K m e no valor do V max : K m obs = K m (1+[I]/K I )/(1+[I]/K I’ ) = K m ’V max obs = V max /’8. A presença <strong>de</strong> um inibidor acompetitivo se manifesta em uma mudança nosvalores do K m e no valor do V max :K m obs = K m / (1+[I]/K I’ ) = K m ’V max obs = V max /’LABORATÓRIO 3: CINÉTICA DA INVERTASEI. FUNDAMENTOSA Cinética Enzimática estuda os mecanismos <strong>de</strong> reações químicas catalisadas porenzimas. Há na estrutura da enzima, uma <strong>de</strong>terminada região diretamenteresponsável pela ação catalítica. Essa região é <strong>de</strong>nominada sítio ativo e a suaconformação correta é fundamental para a ativida<strong>de</strong> enzimática. Ali se localizamdiversos resíduos <strong>de</strong> aminoácidos que po<strong>de</strong>m <strong>de</strong>sempenhar funções <strong>de</strong> orientação dosubstrato e <strong>de</strong> direta interação com este, permitindo que a reação ocorra.Em 1913, L. Michaelis e M. L. Menten, <strong>de</strong>senvolveram estudos consi<strong>de</strong>rando asprincipais proprieda<strong>de</strong>s das enzimas e aplicando as teorias conhecidas <strong>de</strong> CinéticaQuímica para um mo<strong>de</strong>lo simplificado, o qual envolvia a enzima livre (E), o substrato(S), o complexo enzima-substrato (ES) e o produto (P). Esse mo<strong>de</strong>lo po<strong>de</strong> serexpresso pela equação química:k 1k2E + S ES E + Pk-1Michaelis e Menten, com essas consi<strong>de</strong>rações, <strong>de</strong>senvolveram a expressão <strong>de</strong>velocida<strong>de</strong> para uma reação catalisada enzimaticamente, on<strong>de</strong> V é função <strong>de</strong> [S] eV max e K m são constantes:V máx . [S]v =K m + [S]Na figura 1 está apresentada a curva <strong>de</strong> velocida<strong>de</strong> inicial <strong>de</strong> reação em função daconcentração <strong>de</strong> substrato para uma enzima que siga o mo<strong>de</strong>lo proposto por Michaelise Menten. Essa enzima é dita <strong>de</strong> características michaelianas e obe<strong>de</strong>ce à expressão<strong>de</strong> velocida<strong>de</strong> apresentada acima.37
Vel. Inicial Reação mol ( / min.l)VmáxVmáx / 2KmConcentração <strong>de</strong> Substrato (M)Figura 1 – Velocida<strong>de</strong> <strong>de</strong> reação em função da concentração <strong>de</strong> substrato para uma enzimamichaeliana.Nesta curva po<strong>de</strong>-se facilmente i<strong>de</strong>ntificar o efeito <strong>de</strong> saturação do substrato. Nestascircunstâncias, o sistema ten<strong>de</strong> a adquirir velocida<strong>de</strong> <strong>de</strong> reação máxima (V máx ),gran<strong>de</strong>za que é função da concentração inicial da enzima livre (E). Po<strong>de</strong>mos também<strong>de</strong>finir uma concentração <strong>de</strong> substrato na qual se obtém meta<strong>de</strong> <strong>de</strong> V máx . Esse valor<strong>de</strong> [S] é numericamente igual ao K m , parâmetro que <strong>de</strong>ntro <strong>de</strong> certos limites me<strong>de</strong> aafinida<strong>de</strong> da enzima pelo substrato.O método mais preciso para <strong>de</strong>terminação gráfica <strong>de</strong>ssas gran<strong>de</strong>zas numexperimento <strong>de</strong> Cinética Enzimática é através do gráfico <strong>de</strong> duplo-recíproco ou <strong>de</strong>Lineweaver-Burk. Para tanto se <strong>de</strong>ve plotar 1/V em função <strong>de</strong> 1/[S].A enzima escolhida para este estudo é a invertase <strong>de</strong> levedura que catalisa ahidrólise da sacarose para produzir glicose e frutose:C 12 H 22 O 11 + H 2 O C 6 H 12 O 6 + C 6 H 12 O 6Sacarose Glicose FrutoseA <strong>de</strong>terminação da velocida<strong>de</strong> da reação (ou da ativida<strong>de</strong> enzimática) po<strong>de</strong> ser feitaatravés da dosagem dos açúcares redutores formados (frutose e glicose). A dosagembaseia-se na reação entre o ácido 3,5-dinitro-salicílico (DNS) e os açúcares redutores.Estes monossacarí<strong>de</strong>os reduzem o DNS fornecendo um produto <strong>de</strong> cor característica,cuja formação po<strong>de</strong> ser acompanhada a 540 nm.Conhecendo-se por colorimetria a quantida<strong>de</strong> (mols) <strong>de</strong> açúcares redutoresformada, por um cálculo estequiométrico simples, po<strong>de</strong>-se <strong>de</strong>terminar a quantida<strong>de</strong>correspon<strong>de</strong>nte (mols) <strong>de</strong> sacarose hidrolisada. Nestas experiências as velocida<strong>de</strong>sda reação serão expressas em mols <strong>de</strong> sacarose hidrolisada por minuto.Para estudos <strong>de</strong> velocida<strong>de</strong>, o tempo <strong>de</strong> reação <strong>de</strong>ve ser medido com a maiorexatidão possível. Para isso, o grupo <strong>de</strong>verá organizar-se <strong>de</strong> maneira a não permitirque a reação se inicie em tempos diferentes nos vários tubos. Para tal, é importantemanter os tubos em gelo durante a adição dos reagentes. Esses <strong>de</strong>vem seradicionados na or<strong>de</strong>m em que aparecem nos protocolos, com a enzima sendo38
adicionada por último. Levam-se então os tubos, todos juntos, ao banho a 37°C parareagir. Transcorrido o tempo <strong>de</strong>terminado, os tubos <strong>de</strong>vem voltar, todos juntos esimultaneamente, para o gelo. Neste ponto a reação pára.A ativida<strong>de</strong> enzimática é medida em unida<strong>de</strong> (U), sendo que 1 U é a quantida<strong>de</strong> <strong>de</strong>enzima necessária para a formação <strong>de</strong> 1 mol <strong>de</strong> produto por minuto.II. OBJETIVOSEstudar as influências das concentrações <strong>de</strong> enzima e substrato nas velocida<strong>de</strong>s <strong>de</strong>uma reação enzimática, examinar as curvas obtidas experimentalmente, calcular osparâmetros cinéticos e discutir seus valores e importância.III. PROCEDIMENTO EXPERIMENTAL1) Construção da curva padrãoAdicionar a seis tubos (180 X 20 mm) com volumes crescentes <strong>de</strong> solução padrãoredutora (glicose 6 mM + frutose 6 mM), conforme indicado na tabela 1. Complete ovolume em cada tubo para 2,0 mL com tampão. Adicionar em seguida 2 mL doreagente DNS. As quantida<strong>de</strong>s estão indicadas na tabela 1.Tabela 1 – Curva padrão da solução redutora.tubossolução padrãoredutora (mL)soluçãotampão (mL)reagenteDNS(mL)absorbância(540 nm)sacarosehidrolisada(mols)branco - 2,0 2,0 0,000 0,001 0,2 1,8 2,02 0,4 1,6 2,03 0,6 1,4 2,04 0,8 1,2 2,05 1,0 1,0 2,0Anotar aqui a concentração da solução padrão: ________Após a adição do DNS (ácido 3,5-dinitro-salicílico), colocar os tubos em banho-mariafervente por 10 min. Após este tempo, esfriar em água corrente e adicionar 16 mL <strong>de</strong>água <strong>de</strong>stilada. Agitar com inversão da posição na vertical (3x). Ler as absorbâncias a540 nm contra o branco.39
Construir o gráfico absorbância versus concentração <strong>de</strong> sacarose hidrolisada. Estegráfico será a curva padrão.2. Efeito da concentração da enzimaNumerar sete tubos <strong>de</strong> ensaio (180 X 20 mm) e adicionar os reagentes conformetabela 2.Manter todos os tubos no gelo.tubosTabela 2 – Estudo da concentração <strong>de</strong> enzima x velocida<strong>de</strong> <strong>de</strong> reação.sacarose 5%em tampão(mL)tampãopH 4,77(mL)soluçãoenzima(mL)Concentraçãoenzima (M)Abs. 540nmsacarosehidrolisada pormin. (mol/min)branco 1,0 1,0 - 0,00 0,000 0,001 1,0 0,9 0,12 1,0 0,7 0,33 1,0 0,5 0,54 1,0 0,3 0,75 1,0 0,1 0,96 1,0 - 1,0Após a adição da enzima, agitar suavemente. Retirar os tubos do gelo e colocá-losimediatamente (e simultaneamente) em banho-maria a 37C por 5 min. Transcorridoeste tempo, os tubos <strong>de</strong>vem retornar imediatamente para o gelo. Assume-se quenesse instante a reação para. Ainda no gelo, adicionar a cada tubo 2 mL <strong>de</strong> DNS. Napresença <strong>de</strong> DNS, <strong>de</strong>vido à alcalinida<strong>de</strong> do reagente, a enzima para <strong>de</strong> funcionar.Transferir os tubos para banho-maria fervente e esperar 10 min. Findo este tempo,esfriar em água corrente e adicionar 16 mL <strong>de</strong> água <strong>de</strong>stilada em cada tubo. Agitarcom inversão da posição na vertical (3x). Ler as absorbâncias a 540 nm.Fazer o gráfico colocando a concentração da enzima (M) nas abscissas e avelocida<strong>de</strong> <strong>de</strong> hidrólise expressa em mols <strong>de</strong> sacarose hidrolisada por minuto nasor<strong>de</strong>nadas. Durante a aula <strong>de</strong> laboratório será fornecido o valor da concentração daenzima na solução estoque.3. Efeito da concentração <strong>de</strong> substratoNumerar sete tubos <strong>de</strong> ensaio (180 X 20 mm) e adicionar os reagentes segundo atabela 3.Manter todos os tubos no gelo.Tabela 3 – Estudo da concentração <strong>de</strong> substrato x velocida<strong>de</strong> <strong>de</strong> reação.tubossacarose5% emtampão(mL)tampãopH 4,77(mL)soluçãoenzima(mL)concentraçãosacarose (M)Abs. 540nmsacarosehidrolisada pormin. (mol/min)40
anco 1,0 1,0 - 0,000 0,001 0,05 1,45 0,52 0,1 1,4 0,53 0,3 1,2 0,54 0,5 1,0 0,55 0,7 0,8 0,56 1,0 0,5 0,5Proce<strong>de</strong>r exatamente como no caso do estudo da concentração da enzima (itemanterior).Após a adição da enzima, agitar suavemente. Retirar os tubos do gelo e colocá-losimediatamente (e simultaneamente) em banho-maria a 37C por 5 min. Transcorridoeste tempo, os tubos <strong>de</strong>vem retornar imediatamente para o gelo. Assume-se quenesse instante a reação para. Ainda no gelo, adicionar a cada tubo 2 mL <strong>de</strong> DNS. Napresença <strong>de</strong> DNS, <strong>de</strong>vido à alcalinida<strong>de</strong> do reagente, a enzima (valor elevado <strong>de</strong> pH)pára <strong>de</strong> funcionar.Transferir os tubos para banho-maria fervente e esperar 10 min. Findo este tempo,esfriar em água corrente e adicionar 16 mL <strong>de</strong> água <strong>de</strong>stilada em cada tubo. Agitarcom inversão da posição na vertical (3x). Ler as absorbâncias a 540nm.Fazer um gráfico da velocida<strong>de</strong> “versus” concentração inicial do substrato.Estimar os valores <strong>de</strong> V máx e K m .Fazer o gráfico <strong>de</strong> Lineweaver-Burk e calcular os valores <strong>de</strong> V máx e K m .Comparar o valor <strong>de</strong> K m com o encontrado na literatura científica.LABORATÓRIO 5: REAÇÃO DE TRANSAMINAÇÃOI. FUNDAMENTOSEnzimas transaminases ou aminotransferases são importantes no metabolismo <strong>de</strong>aminoácidos, pois transferem o grupo –NH3 + <strong>de</strong> um aminoácido para um –cetoácido. Foram i<strong>de</strong>ntificadas mais <strong>de</strong> 50 tipos <strong>de</strong> transaminases, presentes em todosos tipos <strong>de</strong> células e sendo encontradas tanto no citossol como em mitocôndrias <strong>de</strong>células eucarióticas. O grupo –NH + 3 <strong>de</strong> todos os aminoácidos (com exceção <strong>de</strong> Lys,Arg e Thr) po<strong>de</strong>m ser removidos por transaminases em diferentes organismos. Astransaminases possuem especificida<strong>de</strong> diferenciada: relativamente específica para o–cetoácido aceptor do grupo –NH + 3 e, numa menor intensida<strong>de</strong>, para o aminoácidodoador. A coenzima PLP (piridoxal-fosfato) é essencial para as transaminações evárias outras enzimas envolvidas no catabolismo <strong>de</strong> aminoácidos (figura 1). PLP é<strong>de</strong>rivada da vitamina B6, hidrossolúvel, o piridoxal. A figura 2 mostra como os41
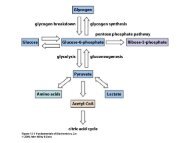
processos catabólicos dos diversos aminoácidos colaboram com o eficientefuncionamento do ciclo <strong>de</strong> Krebs pelo fornecimento <strong>de</strong> intermediários <strong>de</strong>sse ciclo.O ácido glutâmico (Glu), produzido em diversas transaminações, po<strong>de</strong> tanto sofrer<strong>de</strong>saminação oxidativa, produzindo o - cetoglutarato e o íon NH4+, que será utilizadono ciclo da uréia, como doar o grupo –NH + 3 para a biossíntese <strong>de</strong> outros aminoácidos.O Glu é o principal doador <strong>de</strong> grupos –NH + 3 nesta função. A figura 3 ilustra essesprocessos metabólicos.NH 3+OR C COO-HAMINOÁCIDOR CCOO- -CETOÁCIDOOCHNH3HOH 3C+NHCH 2OPHOH 3CCH 2+NHCH 2OPPiridoxal-fosfatoPiridoxamino-fosfatoNH 3+-OOC CH 2CH 2 C-OOC CH 2CH 2OCCOO-COO-GLUTAMATOH -CETOGLUTARATOFigura 1 - Reação <strong>de</strong> transaminação, mostrando a <strong>de</strong>pendência pela coenzima PLP noprocesso <strong>de</strong> transferência dos grupos amino entre aminoácidos e cetoácidos.42
Figura 2 - Os processos catabólicos dos diversos aminoácidos colaboram com oeficiente funcionamento do ciclo <strong>de</strong> Krebs pelo fornecimento <strong>de</strong> intermediários <strong>de</strong>sseciclo.Figura 3 – Formação <strong>de</strong> -cetoglutarato e uréia a partir <strong>de</strong> glutamato.Cromatografia - Separação <strong>de</strong> aminoácidosUm dos problemas que continuamente <strong>de</strong>safiam os bioquímicos é a separação e apurificação <strong>de</strong> um ou mais compostos <strong>de</strong> uma mistura complexa. Uma gran<strong>de</strong>varieda<strong>de</strong> <strong>de</strong> técnicas mo<strong>de</strong>rnas, tanto analíticas quanto preparativas, é <strong>de</strong>nominada<strong>de</strong> cromatografia. O que elas possuem em comum é a proprieda<strong>de</strong> <strong>de</strong> fracionar umamistura complexa <strong>de</strong> substâncias usando diferentes características químicas entre oscomponentes da mistura, o que faz com que eles interajam diferencialmente com afase estacionária e com uma fase móvel.Existem quatro tipos principais <strong>de</strong> cromatografia: cromatografia líquida,cromatografia gasosa, cromatografia <strong>de</strong> camada fina e cromatografia em papel. Aseleção do tipo <strong>de</strong> cromatografia para realizar uma <strong>de</strong>terminada etapa <strong>de</strong> separação é<strong>de</strong>pen<strong>de</strong>nte do material a ser isolado. Freqüentemente, diversos métodoscromatográficos po<strong>de</strong>m ser usados seqüencialmente para que seja obtido umcomposto na forma pura.Um leito cromatográfico po<strong>de</strong> ser construído <strong>de</strong> várias formas, mas ele sempreconsistirá, basicamente, <strong>de</strong> duas fases: a fase estacionária e a fase móvel. A faseestacionária po<strong>de</strong> ser sólida, líquida ou po<strong>de</strong> consistir <strong>de</strong> uma mistura <strong>de</strong> um sólido43
com um líquido. A fase móvel, que po<strong>de</strong> ser líquida ou gasosa, preenche osinterstícios da fase estacionária e <strong>de</strong>ve ser capaz <strong>de</strong> fluir através <strong>de</strong>sta. As fasesmóvel e estacionária <strong>de</strong>vem ser escolhidas <strong>de</strong> forma que os compostos que serãoseparados durante o processo cromatográfico possuam um coeficiente <strong>de</strong> partição<strong>de</strong>finido entre as duas fases. Neste processo, vários mecanismos <strong>de</strong> distribuiçãopo<strong>de</strong>m ser empregados: a distribuição po<strong>de</strong> ser uma simples partição entre doislíquidos imiscíveis; um equilíbrio <strong>de</strong> adsorção entre uma fase estacionária adsorventee uma fase líquida móvel; ou um equilíbrio <strong>de</strong> troca iônica entre uma fase estacionáriatrocadora <strong>de</strong> íon e uma fase móvel constituída por uma solução <strong>de</strong> um eletrólito.Cromatografia <strong>de</strong> aminoácidos em papelNeste protocolo emprega-se uma mistura <strong>de</strong> solventes que interagem com as fibras<strong>de</strong> celulose no papel <strong>de</strong> formas diferentes. O <strong>de</strong>slocamento do soluto po<strong>de</strong> serexplicado da seguinte forma: as fibras <strong>de</strong> celulose do papel possuem uma forteafinida<strong>de</strong> pela água presente na mistura <strong>de</strong> solvente, mas muito pouca afinida<strong>de</strong> pelafase orgânica. O papel, assim, po<strong>de</strong> ser visto como um suporte inerte contendo umafase estacionária aquosa (polar). Na medida em que o solvente flui através <strong>de</strong> umaseção do papel contendo o soluto, uma partição <strong>de</strong>ste composto ocorre entre a fasemóvel orgânica (pouco polar) e a fase estacionária aquosa (polar). Desta forma, partedo soluto <strong>de</strong>ixa o papel e entra na fase móvel. Com o fluxo contínuo <strong>de</strong> solvente, oefeito <strong>de</strong>sta partição entre a fase móvel e a fase estacionária é a transferência dosoluto do seu ponto <strong>de</strong> aplicação ao papel para um outro ponto localizado a algumadistância do local <strong>de</strong> aplicação, no sentido do fluxo <strong>de</strong> solvente. Após o equilíbrio dopapel com o vapor <strong>de</strong> um solvente saturado com água, o <strong>de</strong>senvolvimento do solventeproduz a separação (figura 2).Figura 1 – Cromatografia em papel ascen<strong>de</strong>nte.Quanto mais apolar for o grupo R, maior a mobilida<strong>de</strong> do aminoácido com a fasemóvel. Conseqüentemente a relação (R F ) entre a distância percorrida pelo aminoácido44
no papel e a distância percorrida pela fase móvel será também maior. A Tabela Iapresenta valores <strong>de</strong> R F <strong>de</strong> alguns aminoácidos nas condições <strong>de</strong>scritas.R F = distância percorrida pelo aminoácido no papeldistância percorrida pela fase móvelAtravés da cromatografia em papel i<strong>de</strong>ntificaremos um aminoácido <strong>de</strong>sconhecido emcomparação com quatro outros conhecidos (<strong>de</strong>nominados <strong>de</strong> aminoácidos-padrão).Com ajuda da Tabela II e dos valores <strong>de</strong> pKa obtidos na titulação, confirmaremos ai<strong>de</strong>ntida<strong>de</strong> do aminoácido.A solubilida<strong>de</strong> relativa dos aminoácidos nestas duas fases po<strong>de</strong> ser mudada poralterações na polarida<strong>de</strong> do solvente, ou no pH da solução, o qual irá alterar o estadoiônico dos aminoácidos. Sob um conjunto a<strong>de</strong>quado <strong>de</strong> condições, então, cadamolécula <strong>de</strong> uma mistura irá se <strong>de</strong>slocar a uma diferente velocida<strong>de</strong> sobre a faseestacionária e estará a uma distância específica <strong>de</strong> um do ponto <strong>de</strong> origem, quandocessar o fluxo <strong>de</strong> solvente.Devido ao fato dos aminoácidos não absorverem luz no comprimento <strong>de</strong> ondavisível, eles não po<strong>de</strong>m ser vistos. Assim, algum método <strong>de</strong>ve ser usado após acromatografia para localizá-los. A reação <strong>de</strong> ninhidrina é usada para este propósito porque reage com grupamentos amino livres produzindo um composto colorido(usualmente púrpura) (figura3). Diversos aminoácidos,contudo, produzem diversastonalida<strong>de</strong>s <strong>de</strong> cores com aninhidrina, o que po<strong>de</strong>ajudar em sua i<strong>de</strong>ntificação.A reação da ninhidrina comprolina, por exemplo, geraum composto amarelo e areação da ninhidrina com atirosina produz umacoloração azul metálica.Figura 2 – Reação da ninhidrina com aminoácidos.II. OBJETIVOSEstudar as reações <strong>de</strong> transaminases e i<strong>de</strong>ntificar os produtos e reagentes através dacromatografia em papel.III. PROCEDIMENTO EXPERIMENTAL1) Preparação do homogeneizado <strong>de</strong> fígado45
Essa etapa será realizada previamente. Fígados <strong>de</strong> camundongos (5 a 7 animais) ou<strong>de</strong> galinha foram extraídos e lavados com PBS (tampão fosfato: 0,05M, pH 7,4),picados e macerados para homogeneização com PBS (até 10,0 mL <strong>de</strong> volume final).O homogeneizado foi centrifugado (800 g, 15 minutos) para eliminar célulasremanescentes, núcleos e <strong>de</strong>bris celulares. O sobrenadante foi aliquotado parautilização em sala <strong>de</strong> aula, mantido em gelo e em seguida mantido congelado (-20C)até sua utilização.2) Preparação da mistura reacionalO sistema completo da reação é composto por um aminoácido, um cetoácido, opreparado enzimático, arsenito <strong>de</strong> sódio e o tampão. O arsenito <strong>de</strong> sódio é empregadocom a finalida<strong>de</strong> <strong>de</strong> evitar a oxidação dos cetoácidos pelo sistema enzimático.Montar a seguinte reação:- 0,3 mL <strong>de</strong> solução <strong>de</strong> –cetoglutarato 0,2M pH 7,4- 0,3 mL <strong>de</strong> solução <strong>de</strong> Alanina a 0,2M pH 7,4- 0,3 mL <strong>de</strong> preparação enzimática- 0,5 mL <strong>de</strong> tampão fosfato 0,05M pH7,4- 0,4 mL <strong>de</strong> solução <strong>de</strong> arsenito <strong>de</strong> sódio 0,2ME também um controle negativo (branco) contendo todos os componentes exceto apreparação enzimática, que é substituída por tampão:- 0,3 mL <strong>de</strong> solução <strong>de</strong> –cetoglutarato 0,2M pH 7,4- 0,3 mL <strong>de</strong> solução <strong>de</strong> Alanina a 0,2M pH 7,4- 0,8 mL <strong>de</strong> tampão fosfato 0,05M pH7,4- 0,4 mL <strong>de</strong> solução <strong>de</strong> arsenito <strong>de</strong> sódio 0,2MIncubar os dois tubos (reação e controle negativo) a 37C por 30 minutos. Emseguida, inativar a reação em banho-maria fervente por 3 minutos. Centrifugar a 5000rpm, 10 minutos (centrífuga Eppendorf). Decantar o sobrenadante transferindo paraum segundo tubo Eppendorf e fazer a cromatografia com os padrões a<strong>de</strong>quados.3. CromatografiaEm um papel <strong>de</strong> filtro Whatman número 1 (10 cm X 20 cm) traçar com um lápis umalinha horizontal <strong>de</strong> 2,5 cm <strong>de</strong> altura a partir da origem (ponto <strong>de</strong> contato do papel coma solução na cuba <strong>de</strong> cromatografia). Marcar 7 pontos com 2,5 cm <strong>de</strong> distância entresi.Aplicar, com um capilar <strong>de</strong> vidro fino, sobre os pontos marcados, uma pequenaalíquota dos padrões <strong>de</strong> alanina, glutamato, piruvato, e -cetoglutarato, a mistura <strong>de</strong>reação, o branco (controle negativo) e 2,4-dinitrofenil-hidrazina. Sobre os pontos on<strong>de</strong>foram aplicados os padrões e as amostras, adicionar 3 uL <strong>de</strong> 2,4-dinitrofenil-hidrazina.O solvente utilizado para a cromatografia será uma mistura <strong>de</strong> butanol/etanol/NH 4 OH0,5 M na proporção 70:20:30 (v/v).Após o solvente alcançar 1 cm do final do papel, secar o papel a 80C em estufa emarcar os produtos coloridos formados. Revelar os aminoácidos do cromatograma46
com a solução <strong>de</strong> ninhidrina, secando em seguida o papel. Marcar a posição dasmanchas que aparecerem.MÓDULO 7: AÇÚCARES; ESTRUTURA E FUNÇÃO1. Os carboidratos são compostos que apresentam a fórmula empírica (CH 2 O) n(n> ou = 3), sendo funcionalmente poliidroxial<strong>de</strong>ídos ou poliidroxicetonas. Oscarboidratos mais simples são os monossacarí<strong>de</strong>os, que se apresentam na formas <strong>de</strong>aldoses ou cetoses, conforme o grupo funcional carbonílico que possuem, isto é,respectivamente, al<strong>de</strong>ído ou cetona. Há duas trioses: o gliceral<strong>de</strong>ído, uma aldotriose, ea diidroxiacetona, uma cetotriose (Figura 8). O gliceral<strong>de</strong>ído apresenta um carbono(C2) assimétrico, dando origem a dois isômeros opticos, as formas D e L (Figura 9). Jáa diidroxiacetona não possui C assimétrico e, por isso, não mostra esse tipo <strong>de</strong>isomeria. Os outros monossacarí<strong>de</strong>os po<strong>de</strong>m ser <strong>de</strong>rivados pelo crescimento daca<strong>de</strong>ia <strong>de</strong>stas duas trioses. A Figura 10 mostra a família D <strong>de</strong>rivada do D-gliceral<strong>de</strong>ido, cujas fórmulas estruturais planares obe<strong>de</strong>cem as regras <strong>de</strong> Fisher.Gliceral<strong>de</strong>ído e diidroxiacetona.Carbono quiral ou carbono assimétrico.47
Família D <strong>de</strong>rivada do D-gliceral<strong>de</strong>ído.Ciclização da D-glicose48
O aumento da ca<strong>de</strong>ia do monossacarí<strong>de</strong>o leva ao aparecimento <strong>de</strong> novos Csassimétricos e, portanto mais isômeros estruturais, também chamadosestereoisômeros. O número <strong>de</strong> isômeros é dado pela expressão 2 n on<strong>de</strong> n é o número<strong>de</strong> carbonos assimétricos. Por exemplo, em aldoexoses há 4 Cs assimétricos, logo onúmero <strong>de</strong> isômeros é 2 4 =16, sendo 8 da forma D e 8 da forma L. Mas, as estruturaslineares como representadas na Figura 10 tanto para pentoses como para hexosessão poucos estáveis em solução, formando estruturas cíclicas segundo a reaçãomostrada na Figura 11. Esta é uma reação bem conhecida da química orgânica, pelaqual um álcool (OH) faz uma adição nucleofílica a carbonila <strong>de</strong> um al<strong>de</strong>ído, formandoum composto <strong>de</strong> con<strong>de</strong>nsação da conhecido como semiacetal. No caso do exemploda Figura 11 a hexose é a D-glicose e, como a figura mostra, a ciclização leva aoaparecimento <strong>de</strong> uma outra isomeria estrutural <strong>de</strong>vido às duas posições possíveis doOH do C1 em relação ao plano do anel, gerando os isômeros e . É importanteenfatizar que o OH do C1 não é quimicamente equivalente aos <strong>de</strong>mais OHs que sãoalcoólicos, sendo por isso chamado <strong>de</strong> OH glicosídico. A existência do OH glicosídicopermite que todos os monossarí<strong>de</strong>os sejam oxidados em condições brandas peloreagente <strong>de</strong> Fehling, uma reação <strong>de</strong> oxido-reação na qual os OHs alcoólicos nãoparticipam.Nomenclatura para estereoisômeros.49
2. Conforme exemplificado na Figura 12 há uma nomenclatura especificamente<strong>de</strong>signada para distinguir pares <strong>de</strong> estereoisômeros. Enantiômeros possuemestruturas isoméricas que são uma imagem especular da outra, por exemplo, cadamembro da família D <strong>de</strong> hexoses mostrada na Figura 10 tem um, e, somente um,enantiômero na família L. São epímeros pares <strong>de</strong> estereoisômeros que diferemapenas pela configuração <strong>de</strong> um C assimétrico. São anômeros os dois isômerosresultantes da posição do OH glicosídico do C1 na estrutura cíclica da hexose. E,finalmente, são <strong>de</strong>nominados diastereoisômeros pares <strong>de</strong> isômeros que não caem emnenhuma das categorias anteriores.3. Ligação glicosídica: os monossacarí<strong>de</strong>os po<strong>de</strong>m se apresentar na forma <strong>de</strong>oligo ou polissacarí<strong>de</strong>os, on<strong>de</strong> os monômeros são ligados através <strong>de</strong> ligaçõesglicosídicas. Oligossacarí<strong>de</strong>os são formados por um pequeno número <strong>de</strong>monossacarí<strong>de</strong>os, resultantes da con<strong>de</strong>nsação <strong>de</strong> um OH glicosídico com um OHalcoólico, como exemplificado abaixo pela dimerização <strong>de</strong> duas moléculas <strong>de</strong> α-glicosepor ligação 1-4, originando o dissacarí<strong>de</strong>o maltose:Caso a ligação glicosídica envolva a con<strong>de</strong>nsação dos dois OHs glicosídicos como éo caso da trealose, uma α1-1-diglicose, o dissacarí<strong>de</strong>o não po<strong>de</strong> ser oxidado peloreagente <strong>de</strong> Fehling (dissacarí<strong>de</strong>o não redutor). Já a maltose, que possue um OHglicosídico livre é um dissacarí<strong>de</strong>o redutor, sendo oxidado pelo reagente <strong>de</strong> Fehling.4. Polissacarí<strong>de</strong>os são polímeros constituídos <strong>de</strong> centenas ou milhares <strong>de</strong>resíduos <strong>de</strong> monossacarí<strong>de</strong>os, geralmente glicose, formando ca<strong>de</strong>ias lineares, como acelulose (β1-4-poliglicose), ou ca<strong>de</strong>ias ramificadas, como o glicogênio e o amido.O glicogênio é altamente ramificado, as suas ca<strong>de</strong>ias lineares são formadas porligações α1-4-glicosídicas e suas ramificações <strong>de</strong>correm <strong>de</strong> ligações α1-6-glicosídicas(Figura 13). O glicogênio apresenta uma única extremida<strong>de</strong> redutora livre (C1 noresíduo final na última molécula <strong>de</strong> glicose da ca<strong>de</strong>ia) e inúmeras extremida<strong>de</strong>s nãoredutoras. A partir das extremida<strong>de</strong>s não redutoras há acréscimo ou retirada <strong>de</strong>resíduos do polímero. Portanto, as moléculas <strong>de</strong> glicogênio não têm tamanhos<strong>de</strong>finidos.50
Glicogênio Poli (α1-4) (α1-6) glicose.MÓDULO 8: GLICÓLISE1. A glicólise é a principal via catabólica da glicose compreen<strong>de</strong>ndo as 10 reaçõesenzimaticamente catalisadas que são mostradas na figura abaixo e cujaestequiometria total po<strong>de</strong> ser observada na equação química seguinte:Glicose + 2 NAD + + 2 ADP + 2 P i 2 Piruvato + 2 NADH + 2 ATP + 2 H 2 O + 2 H +A glicólise, como todas as vias catabólicas, é exergônica e a equação acimacorrespon<strong>de</strong> a G o ’ = -43,4 kJ/mol. Mas o dado da variação <strong>de</strong> energia livre maisinteressante é em termos <strong>de</strong> G, cujo valor exato <strong>de</strong>pen<strong>de</strong> <strong>de</strong> cada célula específica,por exemplo, em músculo cardíaco estima-se que seja igual a –74,0 kJ/mol.2. A finalida<strong>de</strong> da glicólise é obtenção <strong>de</strong> energia, como a equação estequiométricaindica, cada molécula <strong>de</strong> glicose é <strong>de</strong>gradada a duas <strong>de</strong> piruvato e parte da energialivre liberada nesta <strong>de</strong>gradação é retida nos produtos na forma <strong>de</strong> 2 NADH e 2 ATP.3. A reação que permite a obtenção <strong>de</strong> NADH é a única <strong>de</strong> oxido-redução da glicólise,pela qual gliceral<strong>de</strong>ído-3-P é oxidado a glicerato-1,3-bisP, através da ação oxidante <strong>de</strong>NAD + catalisada pela enzima gliceral<strong>de</strong>ído <strong>de</strong>sidrogenase. A manutenção dacapacida<strong>de</strong> oxidante da glicólise exige que NADH seja re-oxidada a NAD + , umaalternativa para isso é apresentada na figura, através da reação pela qual NADH reduzpiruvato a lactato, recuperando NAD + . Esta alternativa ocorre no músculo esqueléticocom baixos níveis <strong>de</strong> O 2.4. Já ATP é produzido em duas reações distintas pelas quais um radical fosforil étransferido <strong>de</strong>, respectivamente, glicerato-1,3-P e P-enolpiruvato para ADP, emtransferências catalisadas por glicerato-1,3-P-quinase e P-enolpiruvato-quinase. Estamaneira <strong>de</strong> fosforilação <strong>de</strong> ADP é conhecida como fosforilação a nível do substrato,para distingui-la da fosforilação oxidativa da mitocôndria que será vista mais adiante.51
5. Na glicólise, há 3 reações <strong>de</strong> fosforilação irreversíveis catalisadas, respectivamente,pela hexoquinase, fosfofrutoquinase e piruvato-quinase, que funcionam como marcapassosda via, cuja regulação se dá por um elaborado sistema <strong>de</strong> controle alostéricodas enzimas.6. Diversas outras hexoses, como frutose, galactose e manose, também sãometabolisadas pela via glicolítica.7. A glicólise em condições anaeróbicas tem energética e funções variadas, conforme oorganismo. Cabe fazer dois <strong>de</strong>staques importantes.8. Em vertebrados, encontram-se músculos esqueléticos muito pobres em mitocôndria,que são especializados para produzir ATP a partir <strong>de</strong> glicólise anaeróbica, cujaenergética obe<strong>de</strong>ce a seguinte reação geral: Glicose → 2Lactato + 2H + ; ΔG o ’ = -196kJ/mol. Mas, parte <strong>de</strong>ssa energia livre liberada que seria dissipada (61kJ/mol) éretida na forma <strong>de</strong> 2ATP produzidos por mol <strong>de</strong> glicose <strong>de</strong>gradada. Deve-se aindaenfatizar que o lactato não é <strong>de</strong>scartado, pois vai ser aproveitado no fígado, aon<strong>de</strong> éreoxidado a piruvato, alternativa metabólica importante a ser examinada mais à frente.9. Leveduras mostram um exemplo <strong>de</strong> glicólise anaeróbica na forma da fermentaçãoalcoólica, segundo a reação geral: Glicose → 2Etanol + CO 2 ; ΔG o ’ = -235kJ/mol. Aquitambém parte da energia livre, +61kJ/mol, é mantida com a produção <strong>de</strong> 2ATP. Aparte final da fermentação alcoólica compreen<strong>de</strong> duas reações: a primeira envolve a<strong>de</strong>scarboxilação <strong>de</strong> piruvato e liberação <strong>de</strong> acetal<strong>de</strong>ído, catalisada pela enzimapiruvato-carboxilase, que não existe em animais. Na segunda reação a <strong>de</strong>sidrogenasealcoólica catalisa a redução do acetal<strong>de</strong>ído por NADH.52
HOCH 2OHHOOOHOHATPADPGLICÓLISEGlicoseATPADPP -OCH 2OHOOHOHOHGlicose 6-fosfatoOP -O-CH 2HOCH 2 OHHOOHATPFrutose 6-fosfatoATPP -O-CH O 2ADPCH 2 O- PADPHOOHFrutose 1,6 bisfosfatoHOH 2 C-O- PC=OH 2 C-OHHC=OHC-OHH 2 C-O- PDiidroxiacetonafosfatoGliceral<strong>de</strong>ído3-fosfatoP iNAD +NADHO=C-O- PNAD +NADHHC-OHH 2 C-O- P1,3 BisfosfogliceratoADPATPO=C-O -ADPATPHC-OHH 2 C-O- P3-FosfogliceratoCOO -HC-O- PH 2 C-OH2-FosfogliceratoCOO -H 2 OCOO -C-O- PCH 2ADPATPCOO -P iATPFosfoenolpiruvatoADPHC-OHCH 3NAD + NADHC=OCH 3LactatoNAD +NADHPiruvato53
MÓDULO 9: ACETIL-COA E CICLO DE KREBS1. Em condições aeróbicas, o <strong>de</strong>stino do piruvato produzido na glicólise é sofrer uma<strong>de</strong>scarboxilação oxidativa catalisada pela piruvato <strong>de</strong>sidrogenase, que é um complexomultienzimático existente no interior da mitocôndria <strong>de</strong> eucariotos. Portanto, o piruvatoprecisa entrar na mitocôndria para ser <strong>de</strong>gradado por essa via. A reação geral é aseguinte:Piruvato + CoA + NAD + Acetil-CoA + NADH + CO 22. O acetilCoA resultante da metabolização do piruvato é totalmente oxidado no ciclodo ácido cítrico, também chamado ciclo <strong>de</strong> Krebs, conforme a seguinte reação geral:Acetil-CoA + 3 NAD + + FAD + GDP + P i + 2 H 2 O→ 2 CO 2 + 3 NADH + FADH 2 + GTP+ CoA + 2 H +3. O ciclo <strong>de</strong> Krebs, esquematizado na figura, compreen<strong>de</strong> 8 reações, envolvendo 8enzimas e 8 ácidos carboxílicos, di e tri-ácidos, todos dispersos na matriz damitocondria. Portanto, começando no piruvato e passando pelo acetilCoA, ocorreoxidação completa <strong>de</strong>sses metabolitos liberando 3CO 2 sem participação <strong>de</strong> O 2molecular. Os agentes oxidantes em todas as reações são NAD + ou FAD e as formasreduzidas <strong>de</strong>stas co-enzimas (NADH + FADH 2 ), resultantes do processo, só sãoreoxidadas na ca<strong>de</strong>ia respiratória, uma via especializada que se localiza na membranamitocondrial interna e será consi<strong>de</strong>rada mais adiante.4. O ciclo <strong>de</strong> Krebs, conforme sua reação geral indica, é essencialmente catabólico,pois promove a oxidação do radical acetil a 2CO 2 e retém parte da energia livre <strong>de</strong>stareação na forma <strong>de</strong> coenzimas reduzidos que, posteriormente, servirão à produção <strong>de</strong>ATP através da fosforilação oxidativa. Para cumprir esta função basta que os 8intermediários do ciclo ocorram em concentrações catalíticas. Mas, o ciclo possui outrafunção, além da catabólica, diversos <strong>de</strong> seus intermediários alimentam as vias <strong>de</strong>síntese <strong>de</strong> aminoácidos, lipí<strong>de</strong>os e glicose, isto é, o ciclo tem também funçãoanabólica e, portanto, <strong>de</strong>ve ser classificado como anfibólico. Para que o ciclo<strong>de</strong>sempenhe concomitantemente ambas as funções, catabólica e anabólica, asconcentrações dos intermediários são mantidas e controladas através <strong>de</strong> um complexosistema <strong>de</strong> reações auxiliares, conhecidas como reações anapleróticas. Um exemplo<strong>de</strong> reação anaplerótica é a carboxilação <strong>de</strong> piruvato para obter oxalacetato, catalisadapela enzima piruvato carboxilase.5. A transformação <strong>de</strong> piruvato em acetil-CoA, é uma reação para a qual convergemdiversas vias catabólicas e anabólicas, além da glicólise. Por esse motivo a piruvato<strong>de</strong>sidrogenase está sujeita a um controle altamente elaborado, compreen<strong>de</strong>ndo doisníveis <strong>de</strong> regulação: a) controle alostérico através da inibição pelo produto, exercidopor NADH e acetil-CoA; b) modificação covalente reversível da subunida<strong>de</strong> E 1 daenzima, por fosforilação/<strong>de</strong>sfosforilação.54
6. As enzimas citrato sintase, isocitrato <strong>de</strong>sidrogenase e -cetoglutarato<strong>de</strong>sidrogenase são as reguladoras do fluxo metabólico através do ciclo <strong>de</strong> Krebs eestão sujeitas a controle alostérico, envolvendo NADH como inibidor e Ca + e ADPcomo ativadores.Piruvato CoASH + NAD+CO2 + NADHAcetil-CoAH2OCoASHOxaloacetatoCitratoNADH + H+H2ONAD+L-Malatocis-AconitatoH2OH2OFumaratoCiclo <strong>de</strong> KrebsIsocitratoFADH2NAD+FADNADH + H+SuccinatoGTPOxalosuccinatoCO2 CoASHCO2GDP + PiSuccinil-CoAa-CetoglutaratoNADH+ H+NAD+MÓDULO 10: CADEIA RESPIRATÓRIA E FOSFORILAÇÃO OXIDATIVA1. Fosforilação oxidativa é o processo bioquímico pelo qual a oxidação <strong>de</strong> NADH eFADH 2 , produzidos na glicólise e ciclo <strong>de</strong> Krebs, ocorre acoplada à produção <strong>de</strong> ATP,a partir <strong>de</strong> ADP + Pi. Este processo se dá na ca<strong>de</strong>ia respiratória ou ca<strong>de</strong>ia <strong>de</strong>transporte <strong>de</strong> elétrons, que compreen<strong>de</strong> um conjunto or<strong>de</strong>nado <strong>de</strong> enzimas etransportadores <strong>de</strong> elétrons inseridos na membrana interna da mitocôndria.2. A ca<strong>de</strong>ia respiratória contem 4 complexos, I,II, III e IV, or<strong>de</strong>nados por or<strong>de</strong>mcrescente <strong>de</strong> potencial redox, indo do potencial padrão <strong>de</strong> NAD + /NADH (E 0 ’= -0,315V)ao do O 2 /H 2 O (E 0 ’= +0,815V). Os elétrons são transferidos do complexo I ou II para ocomplexo III pela coenzima Q (ou ubiquinona), e do complexo III para o complexoIV pelo citocromo C para chegar ao O 2 . NADH e FADH 2 , ce<strong>de</strong>m elétrons,respectivamente, aos complexo I e II. A transferência exergônica <strong>de</strong> elétrons do nívelredox <strong>de</strong> NADH para o <strong>de</strong> O 2 (ΔE 0 ’= 1,130V) envolve uma diferença <strong>de</strong> energia livre55
liberada (ΔG 0 ’= -218kJ/mol) que é em parte retida pelo transporte <strong>de</strong> H + do ladointerno para o externo da membrana, criando o gradiente eletroquímico <strong>de</strong> prótons quepermitirá “empurrar” o processo en<strong>de</strong>rgônico <strong>de</strong> fosforilação <strong>de</strong> ADP por Pi para gerarATP, através da bomba <strong>de</strong> prótons que constitui a ATP sintase (também conhecidacom F 1 F 0 - ATPase).EspaçoIntermembranar2 H+4 H+Cit C2 H+Complexo I Q Complexo III Complexo IVMatrixMitocondrialNAD+NADH + H+1/2 O2 + 2H+H2OComplexo IIFADH23. A ATP sintase é distinta e fisicamente separada da ca<strong>de</strong>ia <strong>de</strong> transporte <strong>de</strong>elétrons. A transferência <strong>de</strong> 2e <strong>de</strong> NADH até O 2 envolve um ΔG 0 ’= -218kJ/mol, quegera um incremento no gradiente <strong>de</strong> prótons suficiente para mover a ATP sintase,permitindo a produção <strong>de</strong> 3 moles <strong>de</strong> ATP (ΔG 0 ’= +30,5kJ/mol). Nestas condições, aATP sintase trabalha com uma eficiência termodinâmica igual a 42%. É, no entanto,necessário <strong>de</strong>stacar que quando os 2e saem do nível redox <strong>de</strong> FADH 2 , formam-seapenas 2ATP. Naturalmente, para uma melhor medida da real eficiênciatermodinâmica da fosforilação oxidativa seria preciso estimar o ΔG da transferência <strong>de</strong>elétrons em vez do ΔG 0 ’.4. A gran<strong>de</strong> quantida<strong>de</strong> <strong>de</strong> energia livre que seria dissipada na oxidação completa daglicose a CO 2 e H 2 O [C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O; G 0 ’= -2823 kJ/mol] éaproveitada para produção <strong>de</strong> ATP, graças quase exclusivamente ao processo <strong>de</strong>fosforilação oxidativa, ren<strong>de</strong>ndo 38ATP por mol <strong>de</strong> glicose (incluindo neste total 2ATPda glicólise e 2 do ciclo <strong>de</strong> Krebs).5. Vários mecanismos da ca<strong>de</strong>ia <strong>de</strong> transporte <strong>de</strong> elétrons e <strong>de</strong> seu acoplamento àsíntese <strong>de</strong> ATP foram elucidados através da utilização <strong>de</strong> inibidores e <strong>de</strong>sacopladores,entre os quais estão: rotenona, amital, antimicina A, cianeto e DNP. Rotenona e amital inibem a redução dos complexo I e III por NADH. Antimicina A inibe o transporte <strong>de</strong> elétrons no complexo II. Cianeto inibe o transporte no complexo IV.56
DNP é <strong>de</strong>sacoplador, pois promove o “vazamento“ <strong>de</strong> H + ,levando à dissipação dogradiente <strong>de</strong> prótons e contínuo transporte <strong>de</strong> elétrons, <strong>de</strong>sacoplado da síntese <strong>de</strong>ATP.6. A síntese <strong>de</strong> ATP a partir <strong>de</strong> ADP e P i na mitocôndria, que é catalisada pela ATPsintase, é dirigida pelo processo <strong>de</strong> transporte <strong>de</strong> elétrons. Mas como a ATP sintase éfisicamente separada das proteínas do transporte <strong>de</strong> elétrons, a energia livre liberadano transporte <strong>de</strong> elétrons <strong>de</strong>ve ser conservada em uma forma que possa ser utilizadapela ATP sintase. A energia livre do transporte <strong>de</strong> elétrons é conservada pelobombeamento <strong>de</strong> H + da matriz mitocondrial para o espaço intermembranar, criandoum gradiente <strong>de</strong> H + . A volta dos prótons ao interior da mitocôndria étermodinamicamente favorável. A membrana interna da mitocôndria é impermeável aprótons em toda sua extensão, exceto na ATP sintase; e é então por este canal que osprótons atravessam a membrana, <strong>de</strong> volta à matriz mitocondrial. A variação <strong>de</strong> energialivre associada ao transporte <strong>de</strong> um próton através da membrana interna damitocôndria po<strong>de</strong> ser <strong>de</strong>terminada através <strong>de</strong> medidas da diferença <strong>de</strong> pH e dopotencial <strong>de</strong> membrana estabelecidos em mitocôndrias consumindo oxigênio.MÓDULO 11: GLICONEOGÊNESE1. O fígado humano precisa manter níveis mínimos da glicose circulante, porquecérebro e hemácias <strong>de</strong>pen<strong>de</strong>m quase exclusivamente <strong>de</strong> glicose para produção <strong>de</strong>energia. No entanto, a reserva <strong>de</strong> glicogênio hepático não é suficiente para essafinalida<strong>de</strong>. Por isso, o fígado sintetiza glicose <strong>de</strong> novo a partir <strong>de</strong> lactato, piruvato,glicerol, intermediários do ciclo <strong>de</strong> Krebs e aminoácidos, através <strong>de</strong> uma via anabólicachamada <strong>de</strong> gliconeogênese. No jejum, mesmo o jejum <strong>de</strong> poucas horas, agliconeogênese é a principal fonte da glicose liberada pelo fígado na circulação.2. A glicólise, como já foi visto, é um a via catabólica com a finalida<strong>de</strong> <strong>de</strong> produzirenergia na forma <strong>de</strong> 2 NADH + 2 ATP a partir da <strong>de</strong>gradação <strong>de</strong> glicose a piruvato <strong>de</strong>acordo com a equação química seguinte:Glicose + 2 NAD + + 2 ADP + 2 Pi 2 Piruvato + 2 NADH + 2 ATP + 2 H 2 O + 2 H +A gliconeogênese tem a finalida<strong>de</strong> <strong>de</strong> sintetizar glicose a partir <strong>de</strong> piruvato, isto é, fazo caminho metabólico inverso ao da glicólise. Mas, a gliconeogênese, contrariamenteà glicólise, é muito en<strong>de</strong>rgônica. Para produzir glicose a partir <strong>de</strong> piruvato necessitamse2 NADH + 4 ATP +2 GTP, conforme a estequiometria indicada na equação abaixo:2 Piruvato + 2 NADH + 4 ATP + 2 GTP + 2 H 2 O Glicose + 2 NAD + + 4 ADP + 2 GDP + 6 P i+ 2 H +3. A gliconeogênese utiliza enzimas glicolíticas reversivelmente, mas três <strong>de</strong>ssasenzimas, a hexoquinase, a fosfofrutoquinase e a piruvato quinase, catalisam reaçõescom G -muito negativo, sendo essencialmente irreversíveis. Estas reações sãosubstituídas na gliconeogênese por reações exergônicas, tornando57
termodinamicamente favorável a síntese <strong>de</strong> glicose a partir <strong>de</strong> piruvato. Destasreações, as duas primeiras correspon<strong>de</strong>ntes às enzimas hexoquinase efosfofrutoquinase, são substituídas por reações simples <strong>de</strong> hidrólise <strong>de</strong> ligação fosfoester,catalisadas, respectivamente, pelas enzimas glicose-6-P-fosfatase e frutose-1,6-bis-fosfatase. Já a terceira reação, que permite a volta <strong>de</strong> piruvato para P-enolpiruvatoé mais complexa e se dá em duas etapas catalisadas, respectivamente, por piruvatocarboxilasee P-enolpiruvato-carboxiquinase.4. O balanceamento entre glicólise e gliconeogênese é coor<strong>de</strong>nadamente controladopor um complexo sistema <strong>de</strong> regulação enzimática, envolvendo interações alostéricase modificações covalentes. Todo esse controle está concentrado nas 3 reações nasquais glicólise e gliconeogênese seguem reações in<strong>de</strong>pen<strong>de</strong>ntes, irreversíveis eopostas, que são: 1) glicose / glicose-6-P; 2) frutose-6-P / frutose-1,6-bisP; 3) P-enolpiruvato / piruvato.MÓDULO 12. ÁCIDOS GRAXOS: ESTRUTURA, FUNÇÃO E METABOLISMO1. Lípi<strong>de</strong>s ou lipí<strong>de</strong>os são substâncias biológicas solúveis em solventes orgânicos,como clorofórmio e metanol e, praticamente, insolúveis em água. Os lípi<strong>de</strong>scompreen<strong>de</strong>m: a) ácidos graxos, em geral na forma <strong>de</strong> triacilglicerois; b)glicerofosfolípi<strong>de</strong>s; c) esfingolípi<strong>de</strong>s; d) colesterol e <strong>de</strong>rivados. Este módulo serestringe a ácidos graxos e triacilglicerois.2. Ácidos graxos são ácidos carboxílicos com longas ca<strong>de</strong>ias hidrocarbonadas,encontrados na forma <strong>de</strong> tri-esteres <strong>de</strong> glicerol. A maioria possui um número par <strong>de</strong> C,predominando os <strong>de</strong> 16 C (ácido palmítico) e os <strong>de</strong> 18 C (ácido oléico). Gran<strong>de</strong> parteapresenta dupla ligação (insaturado) e muitos são poli-insaturados.3. As proprieda<strong>de</strong>s físicas dos ácidos graxos <strong>de</strong>pen<strong>de</strong>m do grau <strong>de</strong> insaturação daca<strong>de</strong>ia hidrocarbonada. As moléculas dos ácidos graxos saturados são muito flexíveis,facilitando a atração e coesão entre si. Duplas ligações entre C impõe rigi<strong>de</strong>z à ca<strong>de</strong>ia,tornando-a menos flexível e limitando a coesivida<strong>de</strong> entre as moléculas do ácidograxo. Em conseqüência disso, a temperatura <strong>de</strong> fusão (transição <strong>de</strong> fasesólido/líquido) diminui com o grau <strong>de</strong> insaturação dos ácidos graxos.4. Os triacilglicerí<strong>de</strong>os <strong>de</strong>sempenham um papel <strong>de</strong> reserva <strong>de</strong> energia metabólica.Algumas <strong>de</strong> suas proprieda<strong>de</strong>s físico-quimicas são i<strong>de</strong>ais para essa função: a) elevadograu <strong>de</strong> redução <strong>de</strong> seus C, maximizando a quantida<strong>de</strong> <strong>de</strong> energia livre liberada naoxidação e b) alta hidrofobicida<strong>de</strong>, permitindo estocagem livre <strong>de</strong> água (estoquesanidros). Não é por acaso que os triglicerí<strong>de</strong>os compõe cerca <strong>de</strong> 90% da reserva <strong>de</strong>energia metabólica e também da dieta lipídica dos humanos.5. A reserva <strong>de</strong> triacilglicerí<strong>de</strong>os do tecido adiposo é mobilizada através da hidrólise aglicerol e ácidos graxos livres, catalisada por lípase específica. Os ácidos graxos livres58
são carregados pela corrente sanguínea na forma <strong>de</strong> complexos com albumina, querepresenta 50% da proteína do plasma. Ácidos graxos livres são muito insolúveis, a~1microM formam micelas, que são altamente tóxicas.6. A via catabólica <strong>de</strong> <strong>de</strong>gradação <strong>de</strong> ácidos graxos para produção <strong>de</strong> ATP ocorre namatriz mitocondrial e se chama beta-oxidação. Esta via leva à clivagem sequencial daca<strong>de</strong>ia do ácido graxo em pares <strong>de</strong> C, liberando a cada ciclo: 1 acetilCoA, 1 NADH e 1FADH 2 (ver reações abaixo), que alimentarão, respectivamente, o ciclo <strong>de</strong> Krebs e aca<strong>de</strong>ia respiratória. Mas, a beta-oxidação exige previamente uma ativação inicial queconsome 1 ATP e libera o ácido graxo na forma <strong>de</strong> acilCoA. Esta etapa preliminar <strong>de</strong>ativação se dá associada à membrana externa da mitocôndria e, a transferência daacilCoa para <strong>de</strong>ntro da mitocôndria, é mediada pela carnitina.7. A oxidação completa <strong>de</strong> uma molécula <strong>de</strong> palmitato (16 C) a CO 2 e H 2 O, através dabeta-oxidação, ciclo <strong>de</strong> Krebs e ca<strong>de</strong>ia respiratória, ren<strong>de</strong> 129 ATP. É importante<strong>de</strong>stacar que este rendimento, medido em ATP/mol-oxidado, é muito superior ao daoxidação completa <strong>de</strong> açucares e proteínas, pois a oxidação <strong>de</strong> um ácido graxo leva áliberação <strong>de</strong> 37,6 kJ/g <strong>de</strong> energia livre, enquanto oxidação <strong>de</strong> açucares ou proteínaslibera apenas 16,7 kJ/g.8. Os ácidos graxos são sintetizados no citosol por via anabólica própria que adicionaseqüencialmente unida<strong>de</strong>s <strong>de</strong> 2 C á ca<strong>de</strong>ia em crescimento. Esta via é alimentada poracetilCoA, mas só a primeira unida<strong>de</strong> <strong>de</strong> 2 C entra como acetilCoA, as subseqüentessão na forma <strong>de</strong> malonilCoA. Portanto, o acetilCoA precisa ser previamente ativado amalonilCoA, por carboxilação e consumo <strong>de</strong> 1 ATP, para permitir a reação <strong>de</strong>con<strong>de</strong>nsação, levando ao crescimento da ca<strong>de</strong>ia do ácido graxo <strong>de</strong> uma unida<strong>de</strong> <strong>de</strong> 2C, por ciclo <strong>de</strong> síntese. A ativação <strong>de</strong> acetilCoA é catalisada pela acetilCoAcarboxilase,uma enzima sujeita a controle complexo, envolvendo regulação alostéricae ativação / <strong>de</strong>sativação por modificação covalente (fosforilação / <strong>de</strong>sfosforilação).9. A síntese <strong>de</strong> palmitato (16 C) é altamente en<strong>de</strong>rgônica, obe<strong>de</strong>cendo a sequinteestequiometria:AcetilCoA + 7 malonilCoA + 14 NADPH + 7H + palmitato + 7 CO 2 + 14 NADP + + 8CoA + 6H 2 OA elongação da ca<strong>de</strong>ia além <strong>de</strong> 16 C e a inserção <strong>de</strong> duplas ligações é feita por outrossistemas enzimáticos especializados, que se localizam na membrana do retículoendoplasmático. Mas, mamíferos não possuem enzimas para introduzir duplasligações em ca<strong>de</strong>ias <strong>de</strong> ácidos graxos acima do C9. Por isso, linoleato (18:2) elinolenato (18:3), são ácidos graxos essenciais que precisam ser adquiridos pela dieta.59
Reações <strong>de</strong> um ciclo <strong>de</strong> beta-oxidação:OR – CH 2 – CH 2 – CH 2 – C – S-CoA(acil-CoA)oxidaçãoFADFADH 2HOR – CH 2 – C = C – C – S-CoA(enoil-CoA)HhidrataçãoH 2 OHO HOR – CH 2 – C – C – C – S-CoA(L-hidroxiacil-CoA)H Hoxidação NAD +NADHOOR – CH 2 – C – CH 2 –C –S-CoA(ceto acil-CoA)tióliseCoAOR – CH 2 – C – S-CoA + H 3 C – C –S-CoA (acetil-CoA)O10. É importante <strong>de</strong>stacar que animais <strong>de</strong>gradam eficientemente glicose até acetilCoApela glicólise e assim po<strong>de</strong>m converter C <strong>de</strong> açúcar em ca<strong>de</strong>ias <strong>de</strong> lipí<strong>de</strong>o <strong>de</strong> reserva.Mas, estes organismos não po<strong>de</strong>m fazer o caminho <strong>de</strong> volta <strong>de</strong> ca<strong>de</strong>ias <strong>de</strong> ácidograxo para glicose, pois não possuem reações que convertam acetilCoA em piruvatoou oxalacetato.MÓDULO 13: LÍPIDEOS, MEMBRANA & TRANSPORTE1. Moléculas anfifílicas, como lipí<strong>de</strong>os com uma única cauda hidrofóbica, ácidosgraxos livres e <strong>de</strong>tergentes, quando em solução aquosa e acima <strong>de</strong> um limiar <strong>de</strong>concentração (concentração micelar crítica ou cmc) formam agregados globulareschamados micelas.60
2. Por outro lado, lipí<strong>de</strong>os com duas caudas hidrofóbicas, como glicerofosfolipí<strong>de</strong>os eesfingolipí<strong>de</strong>os, ten<strong>de</strong>m a formar bicamadas lipídicas, que são a base estrutural dasmembranas biológicas.MicelaBicamada3. As membranas biológicas são compostas por proteínas associadas a uma matriz <strong>de</strong>bicamada lipídica. As proteínas que compõe as membranas pertencem a duascategorias: a) integrais ou intrínsecas e b) periféricas ou extrínsecas. Este arranjoestrutural foi originalmente proposto em 1972 por Singer e Nicholson como o mo<strong>de</strong>lo<strong>de</strong> mosaico fluído para as membranas biológicas, que foi plenamente confirmado porresultados experimentais estruturais e funcionais.Mo<strong>de</strong>lo <strong>de</strong> mosaico fluído para membranas biológicas61
4. As membranas são barreiras hidrofóbicas que oferecem gran<strong>de</strong> resistência àpassagem <strong>de</strong> solutos hidrofílicos, cuja permeação exige proteínas transportadorasespecíficas, conforme esquematizado na figura abaixo. Desta maneira a membrana,através <strong>de</strong> transportadores específicos, regula o transporte <strong>de</strong> metabolitos entrecompartimentos celulares.5. Um exemplo clássico <strong>de</strong> transporte é a tomada <strong>de</strong> glicose pela hemácia mediadapor um transportador específico, cuja velocida<strong>de</strong> <strong>de</strong>pen<strong>de</strong> da concentração externa <strong>de</strong>62
glicose e obe<strong>de</strong>ce a uma curva hiperbólica <strong>de</strong> saturação já bem conhecida da cinéticaenzimática, sendo K t análogo a K m : Esta forma <strong>de</strong> transporte é conhecida comotransporte passivamente mediado ou difusão facilitada. Trata-se <strong>de</strong> um processoexergônico, pelo qual o soluto, no caso a glicose, atravessa espontaneamente amembrana indo do compartimento <strong>de</strong> maior para o <strong>de</strong> menor concentração.6. Existem 5 transportadores conhecidos que mediam a difusão facilitada <strong>de</strong> glicoseem humanos: GLUT1 a 5, cujos K t s são diferentes para aten<strong>de</strong>r as necessida<strong>de</strong>sfuncionais dos tecidos nos quais são expressos. GLUT1 é o transportador emhemácias, já GLUT2 é expresso no fígado e células beta do pâncreas, enquantoGLUT4 aparece no músculo esquelético, tecido adiposo etc.7. Mas, no epitélio do intestino a glicose obtida da dieta é transportada para <strong>de</strong>ntro dacélula contra o gradiente <strong>de</strong> concentração, portanto através <strong>de</strong> um processoen<strong>de</strong>rgônico que exige consumo <strong>de</strong> energia metabólica para ocorrer e é referido comotransporte ativo. Neste caso o transportador é chamado simport, pelo qual a glicose étransportada junto com Na + e é termodinamicamente possível porque existe umgradiente eletroquímico <strong>de</strong> Na + <strong>de</strong> fora para <strong>de</strong>ntro da célula. Há múltiplas formas <strong>de</strong>transporte ativo, das quais este exemplo da glicose é apenas uma <strong>de</strong>las. Gran<strong>de</strong> parteda energia metabólica consumida pelas células se <strong>de</strong>ve á manutenção da enormediversida<strong>de</strong> <strong>de</strong> transportadores que promovem a transferência <strong>de</strong> metabolitos e íonscontra gradientes <strong>de</strong> concentração.MÓDULO 14: CICLO DAS PENTOSES1. Muitas funções celulares que envolvem reações en<strong>de</strong>rgônicas são efetuadasgraças à hidrólise exergônica <strong>de</strong> ATP. Outras reações en<strong>de</strong>rgônicas, como a síntese<strong>de</strong> ácidos graxos e colesterol e a fotossíntese, requerem NADPH, que tem um gran<strong>de</strong>po<strong>de</strong>r redutor.2. O grupo fosforila no carbono 2 <strong>de</strong> uma das unida<strong>de</strong>s <strong>de</strong> ribose do NADPH odiferencia <strong>de</strong> NADH. NADH é oxidado pela ca<strong>de</strong>ia respiratória para gerar ATP,enquanto que NADPH serve como um doador <strong>de</strong> elétrons em reações biossintéticasredutoras.3. Na via das pentoses, NADPH é gerado quando a glicose-6-fosfato é oxidada aribose-5-fosfato, que é um açúcar <strong>de</strong> 5 carbonos, componente <strong>de</strong> vários compostosimportantes, como ATP, CoA, NAD + , FAD, RNA e DNA.4. A via das pentoses também catalisa a interconversão <strong>de</strong> açúcares <strong>de</strong> 3, 4, 5, 6 e 7carbonos, em uma série <strong>de</strong> reações não oxidativas que ocorrem no citosol.5. As reações da via das pentoses são as seguintes: glicose-6-fosfato é <strong>de</strong>sidrogenado e convertido a ribulose-5-fosfato, em trêsreações, produzindo 2 NADPH + H + . ribulose-5-fosfato é isomerizada a ribose-5-fosfato.63
Nestas reações, 2 NADPH + H + e uma ribose-5-fosfato são gerados para cada glicose-6-fosfato oxidada. ribose-5-fosfato é convertida a gliceral<strong>de</strong>ído-3-fosfato e frutose-6-fosfato pelatranscetolase e transaldolase. A transcetolase catalisa a transferência <strong>de</strong> unida<strong>de</strong>s <strong>de</strong>C2 <strong>de</strong> uma cetose para uma aldose. A transaldolase transfere unida<strong>de</strong>s <strong>de</strong> C3 <strong>de</strong> umaaldose para uma cetose.As reações <strong>de</strong> transcetolase e transaldolase criam uma ligação reversível entre a viadas pentoses e a via glicolítica. O resultado <strong>de</strong>ssas reações é a formação <strong>de</strong> 2hexoses e 1 triose a partir <strong>de</strong> 3 pentoses:C 5 + C 5 C 3 + C 7 TranscetolaseC 7 + C 3 C 4 + C 6 TransaldolaseC 5 + C 4 C 3 + C 6 Transcetolase6. O excesso <strong>de</strong> ribose-5-fosfato formado pela vias das pentoses po<strong>de</strong> sercompletamente convertido em intermediários da via glicolítica.7. A primeira reação da via das pentoses, a <strong>de</strong>sidrogenação da glicose-6-fosfato, épraticamente irreversível. E é essa a reação em que a via das pentoses é controlada.O fator regulatório mais importante é o nível <strong>de</strong> NADP + , o receptor <strong>de</strong> elétrons naoxidação da glicose-6-fosfato a 6-fosfogluconolactona. Além disso, NADPH competecom NADP + pela ligação à enzima. A parte não oxidativa da via das pentoses écontrolada principalmente pela disponibilida<strong>de</strong> <strong>de</strong> substratos.8. A via percorrida pela glicose-6-fosfato <strong>de</strong>pen<strong>de</strong> da necessida<strong>de</strong> celular <strong>de</strong> NADPH+ H + , ribose-5-fosfato e ATP: Quando muito mais ribose-5-fosfato é requerida que NADPH + H + , a maior parte <strong>de</strong>glicose-6-fosfato é convertida a frutose-6-fostato e gliceral<strong>de</strong>ído-3-fosfato pela viaglicolítica, a transaldolase e a transcetolase convertem esses em ribose-3-fosfato. Quando a necessida<strong>de</strong> <strong>de</strong> NADPH + H + e ribose-5-fosfato estão balanceadas, areação predominante é a formação <strong>de</strong> 2 NADPH e uma ribose-5-fosfato <strong>de</strong> glicose-6-fosfato pela fase oxidativa da via das pentoses. Quando muito mais NADPH + H + é requerido que ribose-5-fosfato, a glicose-6-fosfato é completamente oxidada a CO 2 , ou convertida a piruvato.MÓDULO 15. FOTOSSÍNTESE1. A fotossíntese é o processo pelo qual a energia luminosa é transformada emenergia química e po<strong>de</strong>r redutor, armazenada nas moléculas <strong>de</strong> ATP e NADH +H + .Num segundo passo fase escura (na verda<strong>de</strong>, fase in<strong>de</strong>pen<strong>de</strong>nte <strong>de</strong> luz) a energiaarmazenada é utilizada para síntese <strong>de</strong> glicose a partir <strong>de</strong> CO 2 +H 2 O. A fotossínteseocorre nos cloroplastos, uma organela que, como a mitocôndria, possui umamembrana externa altamente permeável e uma membrana interna praticamenteimpermeável, separadas por um espaço intermembranar.64
A equação geral da fotossíntese é:6 CO 2 + 6 H 2 O C 6 H 12 O 6 + 6 O 2 G o´= +2.870 KJ x mol -12. As reações <strong>de</strong>pen<strong>de</strong>ntes <strong>de</strong> luz ocorrem na membrana tilacói<strong>de</strong> e envolvemprocessos semelhantes ao transporte <strong>de</strong> elétrons e fosforilação oxidativa damitocôndria. As reações in<strong>de</strong>pen<strong>de</strong>ntes <strong>de</strong> luz ocorrem no estroma.3. Os primeiros estudos <strong>de</strong> fotossíntese realizados levaram à conclusão <strong>de</strong> que CO 2era a fonte do O 2 gerado na fotossíntese. Em 1931, entretanto, <strong>de</strong>monstrou-se quebactérias fotossintetizantes anaeróbicas, sintetizam glicose a partir <strong>de</strong> CO 2 , sem gerarO 2 :CO 2 + 2 H 2 S luz (CH 2 O) + 2 S + H 2 O4. A reação geral da fotossíntese po<strong>de</strong> ser <strong>de</strong>monstrada como segue:CO 2 + 2 H 2 A luz (CH 2 O) + 2 A + H 2 OEm cianobactérias, H 2 A é H 2 S, e em plantas, H 2 O. Isso sugere que a fotossíntese sejaum processo <strong>de</strong> duas fases, nos quais a energia solar é utilizada para oxidar H 2 A (faseclara):2 H 2 A luz 2 A + 4[H]e o agente redutor resultante [H] subsequentemente reduz CO 2 (fase escura):4[H] + CO 2 luz (CH 2 O) + H 2 O5. O principal fotorreceptor na fotossíntese é a clorofila. A luz absorvida pelas clorofilasantena e pigmentos acessórios é transferida para centros <strong>de</strong> reação fotossintéticos,on<strong>de</strong> ocorrem as principais reações da fotossíntese.6. Plantas e cianobactérias utilizam o po<strong>de</strong>r redutor gerado pela oxidação <strong>de</strong> H 2 Odirigida pela luz para produzir NADPH.7. A produção <strong>de</strong> O 2 na fotossíntese requer 2 fotossistemas: Fotossistema I (P700)gera um forte agente redutor, capaz <strong>de</strong> reduzir NADP + , e concomitantemente, umoxidante fraco; Fotossistema II (P680) gera um forte agente oxidante, capaz <strong>de</strong> oxidarH 2 O, e concomitantemente, um redutor fraco. O redutor fraco reduz o oxidante fraco.Assim, fotossistemas I e II precisam funcionar em série para acoplar a oxidação daH 2 O com a redução <strong>de</strong> NADP+ (transferência <strong>de</strong> elétrons <strong>de</strong> H 2 O para NADP + ,formando O 2 e NADPH + H + ).8. Quando iluminado, o FS II passa para uma forma excitada e per<strong>de</strong> elétrons, osquais são transportados por reações <strong>de</strong> óxido-redução para o fotossistema I. O PS Iiluminado fornece elétrons para a redução <strong>de</strong> NADP+. Como resultado temos aoxidação do FS II e a redução do FS I. A reposição <strong>de</strong> elétrons em PS II é feita porelétrons provenientes da oxidação <strong>de</strong> água e, em PSI, por elétrons emitidos por PSII.9. Os componentes envolvidos no transporte <strong>de</strong> elétrons <strong>de</strong> H 2 O para NADP+ comprodução <strong>de</strong> NAPDPH + H+ estão organizados em três partículas, que estão ligadas amembrana tilacói<strong>de</strong>: (1) fotossistema II; (2) complexo do citocromo b 6 f; (3)fotossistema I (fotofosforilação não-ciclica).65
10. Os cloroplastos geram ATP <strong>de</strong> maneira muito semelhante à da mitocôndria, ouseja, através do acoplamento da dissipação <strong>de</strong> um gradiente <strong>de</strong> prótons à síntese <strong>de</strong>ATP.11. Na fotofosforilação cíclica, os elétrons emitidos por P700 (PSI) são transferidos aocomplexo citocromo b 6 f, retornando finalmente a P700. Não há síntese <strong>de</strong> NADPH +H + , nem liberação <strong>de</strong> oxigênio.12. Na fase clara da fotossíntese, ATP e NADPH + H + são sintetizados, e esses sãoutilizados na fase escura para a síntese <strong>de</strong> carboidratos. A via pela qual as plantasincorporam CO 2 em carboidratos é <strong>de</strong>nominada <strong>de</strong> Ciclo <strong>de</strong> Calvin.13. O ciclo <strong>de</strong> Calvin engloba duas fases: (1) a fase <strong>de</strong> produção, na qual 3 moléculas<strong>de</strong> ribulose-5-fosfato reagem com 3 moléculas <strong>de</strong> CO 2 , gerando 6 moléculas <strong>de</strong>gliceral<strong>de</strong>ído-3-fosfato, com o gasto <strong>de</strong> 9 ATPs e 6 NADPH + H + ; (2) a fase <strong>de</strong>recuperação, na qual os átomos <strong>de</strong> carbono <strong>de</strong> 5 gliceral<strong>de</strong>ído-3-fosfato entram emuma série <strong>de</strong> reações para dar origem a 3 ribulose-5-fosfato, com as quais o ciclorecomeça.MÓDULO 16: METABOLISMO DO GLICOGÊNIO E CONTROLE HORMONAL1. O glicogênio é um polissacarí<strong>de</strong>o que funciona como forma <strong>de</strong> reserva <strong>de</strong> energiaem animais e microrganismos. Em animais, o glicogênio está <strong>de</strong>positado no fígado,um órgão central <strong>de</strong> reserva <strong>de</strong> energia, e, também, nos músculos, on<strong>de</strong> é <strong>de</strong>gradadolocalmente. O glicogênio hepático é exportado para manter a glicemia.2. A natureza polimérica e semi-solúvel do glicogênio constitui-se numa maneiraperfeita <strong>de</strong> armazenar energia na forma <strong>de</strong> glicose. O estoque <strong>de</strong> glicogênio do fígadona forma <strong>de</strong> glicose causaria tamanha pressão osmótica, que a viabilida<strong>de</strong> dohepatócito seria impossível.3. O glicogênio é um polímero <strong>de</strong> -D-glico-piranose altamente ramificado. Na ca<strong>de</strong>iaos monômeros são interligados por ligações glicosídicas (14); nos pontos <strong>de</strong>ramificação a ligação também é glicosídica, mas (16).4. A glicose, na forma <strong>de</strong> glicose-1-P, é liberada da reserva <strong>de</strong> glicogênio pelafosforólise da ligação (14) da extremida<strong>de</strong> não redutora do polímero. Esta reaçãoé catalisada pela glicogênio fosforilase.5. A glicogênio fosforilase <strong>de</strong>grada até restarem 4 resíduos antes <strong>de</strong> uma ramificaçãoaté que a enzima <strong>de</strong>sramificadora transfere 3 dos 4 resíduos para outra extremida<strong>de</strong>da ca<strong>de</strong>ia <strong>de</strong> glicogênio formando uma nova ligação (14). O resíduo restante estáligado a ca<strong>de</strong>ia pela ligação (16) que é hidrolisada pela enzima <strong>de</strong>sramificadoraatravés <strong>de</strong> sua ativida<strong>de</strong> (16) glicosidase.66
6. Glicose-1-fosfato é convertida a glicose-6-fosfato pela fosfoglicomutase, esta po<strong>de</strong>ser liberada pela circulação no fígado pela ação da glicose-6-fosfatase ou <strong>de</strong>gradadapelo músculo.7. A síntese do glicogênio se dá através <strong>de</strong> via uma diferente da <strong>de</strong> <strong>de</strong>gradação. Aglicose-1-P é primeiro ativada à uridinadifosfato-glicose, ou simplesmente UDP-G.UDP-G é o substrato da glicogênio sintase que catalisa a adição <strong>de</strong> um resíduo <strong>de</strong>glicose ao carbono 4 da glicose <strong>de</strong> uma extremida<strong>de</strong> não redutora do glicogênio,liberando ainda como produto UDP. Esta reação necessita <strong>de</strong> ca<strong>de</strong>ias glicogênicaspré-existentes que funcionam como PRIMER da reação, oferecendo extremida<strong>de</strong>s nãoredutoras para reagir com UDP-G.Gli 6-P Gli 1-PGli 1-P + UTP UDP-Gli + PP I (1-fosfato uridil transferase)UDP-Gli + glicogênio (n) UDP + glicogênio (n + 1)O UDP é convertido a a UTP as custas da utilização <strong>de</strong> ATP:PP I + H 2 O 2 P I (pirofosfatase)UDP + ATP UTP + ATP (nucleosí<strong>de</strong>o difosfato quinase)8. A glicogênio fosforilase e glicogênio sintase formam um ciclo que,respectivamente, libera e <strong>de</strong>posita glicose-1-P no estoque da glicogênio:Glicose-1PUTP + H 2 OUDPG2 P iGlicogênio nFosforilaseSintaseIP i Glicogênio n+1 UDPÉ fácil notar que se estas enzimas funcionarem concomitantemente o ciclo seráFÚTIL, cujo único resultado líquido será dissipação <strong>de</strong> energia através da reação:UTP + H 2 O UDP + P iConclui-se que, necessariamente, no hepatócito estas enzimas são coor<strong>de</strong>nadamentereguladas, isto é, quando a fosforilase é ativada para mobilizar glicose-1-P, a sintase é<strong>de</strong>sativada, e vice-versa, conforme a necessida<strong>de</strong> celular.9. Ambas fosforilase e sintase são reguladas por fosforilação (modificação covalente)em resíduos específicos <strong>de</strong> serina, reações catalisadas pela mesma proteína-quinaseque possui dupla especificida<strong>de</strong>, sendo por isso chamada <strong>de</strong> sintase-fosforilasequinase. A fosforilase e a sintase são espécies fosforiladas, portanto a fosforilação,catalisada pela sintase-fosforilase quinase, causa ativação da fosforilase e inativaçãoda sintase.67
10. A fosforilase a e a sintase I (formas ativas), por um lado, e a fosforilase b e asintase D (formas não ativas), por outro, são, respectivamente interconversíveis. Paratanto é necessário que fosforilase a e a sintase I sejam <strong>de</strong>sfosforiladas, através <strong>de</strong>uma reação que requer catálise. A principal enzima, catalisadora comum <strong>de</strong>stas<strong>de</strong>sfosforilações, é a fosfoproteína fosfatase 1.11. A integração metabólica requerida pelo bom funcionamento do organismo faz comque as interconversões coor<strong>de</strong>nadas da fosforilase e sintase do glicogênio no fígado,por fosforilação, sejam controladas extracelularmente por hormônios específicos,principalmente: adrenalina, glucagon e insulina.12. As formas inativas fosforilase b e sintase D são intracelularmente estimuladas porfatores alostéricos positivos, por razões <strong>de</strong> economia interna do metabolismo celular,in<strong>de</strong>pen<strong>de</strong>ntemente <strong>de</strong> controle hormonal. São estimuladores alostéricos da fosforilaseb e sintase D, respectivamente, 5’-AMP e glicose-6P.13. A regulação metabólica é feita <strong>de</strong> interferência direta <strong>de</strong> <strong>de</strong>terminadas reaçõesquímicas que compõem o metabolismo, aumentando ou reduzindo sua velocida<strong>de</strong>. Oresultado direto <strong>de</strong>ste processo é a maior oferta <strong>de</strong> substratos ou acúmulo <strong>de</strong>metabólitos que acabará por influenciar outras vidas <strong>de</strong>pen<strong>de</strong>ntes <strong>de</strong>stes compostos ea forma mais eficiente <strong>de</strong> regulação <strong>de</strong>sta re<strong>de</strong> é aumentar a concentração ou alterar aeficiência da enzima.14. Po<strong>de</strong> se controlar a síntese ou <strong>de</strong>gradação enzimática; também se po<strong>de</strong> modular aativida<strong>de</strong> enzimática através <strong>de</strong> mudanças conformacionais da própria enzimaprovocada através da ligação <strong>de</strong> compostos ou grupos na ca<strong>de</strong>ia peptídica: regulaçãoalostérica e regulação por modificação covalente. A concentração enzimática tambémpo<strong>de</strong> variar conforme a oferta do substrato; alteração mediada através <strong>de</strong> hormônios.15. Hormônios são sinais químicos que permitem a comunicação entre células. Sãosintetizados em células glandulares para atingir células alvo através da circulaçãosanguínea. As células alvo respon<strong>de</strong>m a hormônios específicos por possuírem osrespectivos receptores hormonais. A ligação do hormônio ao receptor segue umareação <strong>de</strong> equilíbrio semelhante à interação enzima-substrato: H + R [RH]: aconstante <strong>de</strong> dissociação <strong>de</strong> RH (K D ), correspon<strong>de</strong>nte à reação inversa é muito baixa -(10 -12 a 10 -9 M) - <strong>de</strong>vido à alta afinida<strong>de</strong> entre hormônio e receptor.16. Uma parte importante dos receptores hormonais são proteínas integrais <strong>de</strong>membrana, muitas da quais tem, atualmente, sua estrutura primária conhecida e suaestrutura tridimensional mo<strong>de</strong>lada, em conseqüência da clonagem e seqüenciamentodos seus respectivos genes. Por exemplo, o receptor -adrenérgico do hormônioadrenalina, encontrado em hepatócito e outros tipos celulares, possui um pesomolecular <strong>de</strong> 64 kD, compreen<strong>de</strong>ndo uma única ca<strong>de</strong>ia peptídica que, <strong>de</strong> maneiraserpentiforme, atravessa a membrana 7 vezes, <strong>de</strong>ixando do lado extracelular, aextremida<strong>de</strong> N-terminal e 3 alças, e do lado intracelular, outras 3 alças mais a68
extremida<strong>de</strong> C-terminal. A porção extracelular do receptor contém o sítio <strong>de</strong> ligação daadrenalina, enquanto a porção intracelular se associa a um trímero <strong>de</strong> proteínasconhecidas como proteína-G, por ter um sítio específico para ligação do nucleotí<strong>de</strong>oGTP. São hoje conhecidos mais <strong>de</strong> 1000 receptores, <strong>de</strong> múltiplos hormônios, com estaestrutura básica formando a superfamília chamada dos receptores associados aproteína-G. A função <strong>de</strong>ste receptor é transduzir o sinal “adrenalina” <strong>de</strong> fora para<strong>de</strong>ntro da célula, processo que é mediado pelas proteínas-G. Há também receptorespresentes no citoplasma nuclear e citoplasmático e neste caso, o hormônio precisa teralta solubilida<strong>de</strong> a lipí<strong>de</strong>os, atravessando a membrana plasmática como os hormôniosesterói<strong>de</strong>s para encontrar o seu receptor <strong>de</strong>ntro da célula.17. Os hormônios estão envolvidos no metabolismo em dois níveis: indução ourepressão gênica <strong>de</strong> <strong>de</strong>terminadas enzimas ou através da modificação covalente: Afosforilação é mediada pelas proteínas quinases que transferem o grupo fosfato doATP para resíduos específicos <strong>de</strong> serina, treonina e tirosina, formando uma ligaçãoéster fosfórico ou a retirada do grupo fosfato é catalisada pela ação <strong>de</strong> fosfoproteínasfosfatases através da hidrólise.18. ligação <strong>de</strong> adrenalina ao receptor -adrenérgico acoplado a proteína G ativa aenzima a<strong>de</strong>nilato ciclase através da ativação da subunida<strong>de</strong> (por ligação <strong>de</strong> GTP),presente na face interna da membrana citoplasmática, qual ativa a a<strong>de</strong>nilato ciclase,catalisando a formação <strong>de</strong> cAMP a partir <strong>de</strong> ATP e <strong>de</strong>senca<strong>de</strong>ando a transdução <strong>de</strong>sinal. A <strong>de</strong>scoberta <strong>de</strong> cAMP, por Sutherland e colaboradores há cerca <strong>de</strong> 40 anos,levou à criação do conceito do segundo mensageiro da ação hormonal, sendo cAMP oprimeiro a ser <strong>de</strong>scrito, e permitiu dar início à progressiva compreensão dosmecanismos <strong>de</strong> ação do receptor <strong>de</strong> adrenalina. Devemos lembrar que os primeirosmensageiros químicos extracelulares são os hormônios. cAMP tem efeito transiente eé hidrolisada pela ação da fosfodiesterase. Na célula, o balanço entre as reações <strong>de</strong>síntese (a) e <strong>de</strong>gradação (b) regula a concentração intracelular do cAMP.a) ATP + H 2 O cAMP + 2 P i ; catalisada pela a<strong>de</strong>nilato ciclaseb) cAMP + H 2 O AMP; catalisada pela fosfodiesterase.19. A base da ação metabólica do cAMP é a ativação alostérica <strong>de</strong> uma quinase cujossubstratos são proteínas, sendo conhecida como proteína quinase <strong>de</strong>pen<strong>de</strong>nte <strong>de</strong>cAMP, ou simplesmente PKA (Protein Kinase <strong>de</strong>pen<strong>de</strong>nt on cAMP). A PKA, uma vezativada, catalisa a fosforilação ativadora (modificação covalente) <strong>de</strong> uma cascata <strong>de</strong>proteínas quinases que terminam na fosforilação da fosforilase a e da sintase doglicogênio, causando, respectivamente, a ativação e a inativação <strong>de</strong>ssas enzimas. Oresultado final <strong>de</strong>ssa seqüência <strong>de</strong> ativações enzimáticas, com alternância <strong>de</strong>regulação alostérica e modificação covalente, é a fosforólise do glicogênio liberandoglicose-1P, comandada por sinais hormonais extracelulares.20. Os efeitos <strong>de</strong> ativação ou não da via <strong>de</strong>pen<strong>de</strong>m do receptor ativado, no caso dosreceptores adrenérgicos, os efeitos <strong>de</strong> 1 são mediados através dos íons cálcio e e69
a ativação <strong>de</strong> 2 leva a inibição da via <strong>de</strong> a<strong>de</strong>nilato ciclase. Há casos aon<strong>de</strong> a proteínaG é do tipo G s sendo ativadora <strong>de</strong> a<strong>de</strong>nilato ciclase e do tipo G R inibindo a a<strong>de</strong>nilatociclase. Algumas toxinas po<strong>de</strong>m ativar ou bloquear a via <strong>de</strong> transdução <strong>de</strong> sinal: toxinada cólera e a toxina da coqueluche.21. Dois hormônios são os principais responsáveis pelo equilíbrio da concentração daglicose circulante: glucagon e insulina.22. O glucagon é um hormônio que tem efeitos equivalentes aos da adrenalina nocontrole do metabolismo do glicogênio: possui um receptor da família dos receptoresacoplados a proteína-G e ativa a cascata que se inicia com cAMP/PKA. Este éliberado em condições <strong>de</strong> hipoglicemia ativando processos <strong>de</strong>gradativos paramanutenção da glicemia sanguínea. A PKA (proteína quinase ativada por cAMP)fosforila a fosforilase quinase tornando-a ativa. A fosforilase quinase fosforila agoraglicogênio fosforilase. A glicogênio fosforilase ativada (quando fosforilada, glicogêniofosforilase b a) catalisa a hidrólise <strong>de</strong> resíduos <strong>de</strong> glicose do glicogênio liberandogrupos <strong>de</strong> glicose-1-fosfato. No mesmo tempo, a fosforilase quinase, ativada pelacascata do receptor <strong>de</strong> glucagon-proteína-G, cAMP/PKA, fosforila a glicogêniosintase, a qual se torna inativa quando fosforilada (síntase I sintase D).23. A insulina tem efeito oposto, promove a absorção <strong>de</strong> glicose pelo fígado emúsculos e usa <strong>de</strong>posição nas reservas <strong>de</strong> glicogênio. Mas é importante notar que ainsulina tem mecanismos <strong>de</strong> ação totalmente diferentes da adrenalina e do glucagon.Os receptores <strong>de</strong> insulina não pertencem à família dos receptores acoplados aproteína-G e não têm ação sobre a a<strong>de</strong>nilato ciclase. Seus receptores são do grupo <strong>de</strong>receptores cujo domínio intracelular apresenta ativida<strong>de</strong> intrínseca <strong>de</strong> proteína-quinase<strong>de</strong> tirosina. A insulina estimula fosfoproteínas fosfatases. Para reverter a ação doglucagon, a insulina promove a ativação da fosfoproteína fosfatase que catalisa a<strong>de</strong>sfosforilação da glicogênio fosforilase e da glicogênio sintase, levando a inativaçãoda primeira (fosforilase a b) e ativação da segunda (síntase D sintase I). Destaforma o fluxo glicoseglicogênio é favorecido. O transporte da glicose no interior dascélulas com a atuação da insulina é um processo passivo mediado por uma família <strong>de</strong>permeases <strong>de</strong>nominadas GLUT (glucose transporter).24. Respostas celulares rápidas <strong>de</strong>senca<strong>de</strong>adas por hormônios só po<strong>de</strong>m ser obtidasatravés da ativação, ou da inibição, <strong>de</strong> enzimas pré-existentes. Hormônios esterói<strong>de</strong>s(por exemplo cortisol) quando secretados difun<strong>de</strong>m-se pela membrana citoplasmáticae ligam-se ao seus receptores intracelulares os quais, quando ativados, promovem nonúcleo a regulação do metabolismo pela indução da transcrição <strong>de</strong> genes quecodificam enzimas específicas, levando à síntese <strong>de</strong> novo das proteínascorrespon<strong>de</strong>ntes, fenômeno conhecido como indução enzimática. Mas o mecanismo<strong>de</strong> indução enzimática <strong>de</strong>senca<strong>de</strong>ado por hormônios resulta necessariamente numaresposta celular lenta, uma vez que os RNAs mensageiros (mRNAs) precisam sertranscritos, processados, transportados para o citoplasma e finalmente traduzidospara produzir as proteínas enzimáticas exigidas.70
25. A adrenalina estimula uma resposta local no músculo. A liberação <strong>de</strong> adrenalina éinduzida por estímulo nervoso autônomo em situações <strong>de</strong> perigo, exercício físico, ehipoglicemia e induz a <strong>de</strong>gradação do glicogênio com os fins <strong>de</strong> fornecer glicose-1-fosfato como fonte <strong>de</strong> energia para ativida<strong>de</strong>s musculares que permitem ao animalreagir a estas situações.26. Regulação da glicólise e gliconeogênese. A glicólise é uma das vias metabólicasprincipais para o fornecimento <strong>de</strong> energia. No fígado, encontra-se também agliconeogênese, a qual é, <strong>de</strong> forma geral, uma via antagônica da glicólise. A regulaçãodas duas vias é feita <strong>de</strong> forma reciproca, isto é, quando uma <strong>de</strong>las está ativa, a outraestá inibida. Há três vias sob controle metabólico: as conversões reversíveis <strong>de</strong>: (i)glicose para glicose-6-fosfato (hexoquinase e glicose-6-fosfatase); (ii) frutose-6-fosfatoe frutose-1,6-bisfosfato (fosfofrutoquinase e frutose-1,6-bisfosfatase; e (iii)fosfoenolpiruvato e piruvato (piruvato quinase e fosfoenolpiruvato carboxiquinase,piruvato carboxilase). A fosfofrutoquinase é o principal ponto <strong>de</strong> regulação da glicólise.AMP e frutose-2,6-bisfosfato agem como efetuadores alostéricos positivos. A formação<strong>de</strong> frutose-2,6-bisfosfato está sob controle hormonal. Em condições <strong>de</strong> hipoglicemia, oglucagon estimula a produção <strong>de</strong> cAMP no fígado. Isso ativa a PKA a fosforilar einativar a fosfofrutoquinase e ativar a frutose-bisfosfatase-2, diminuindo aconcentração <strong>de</strong> frutose-2,6-bisfosfatase. Como resultado, o equilíbrio entre asreações <strong>de</strong> fosfofrutoquinase é alterado, em favor da síntese <strong>de</strong> frutose-6-fosfato,aumentado o fluxo gliconeogênico e a síntese <strong>de</strong> glicose-6-fosfato. Ao contrário, emcondições <strong>de</strong> hiperglicemia, as concentrações <strong>de</strong> cAMP diminuíram, e o conseqüenteaumento <strong>de</strong> frutose-2,6-bisfosfato ativa a fosfofrutoquinase e promove a glicólise.MÓDULO 17: METABOLISMO DE AMINOÁCIDOS1. Em animais, o N do grupo amino dos aminoácidos são eficientemente obtidos apartir <strong>de</strong> NH + 4 pelas reações catalisadas pelas enzimas <strong>de</strong>sidrogenase glutâmica eglutamina sintetase, fornecendo, respectivamente, glutamato e glutamina.2. Ainda em animais <strong>de</strong> forma geral, os aminoácidos alanina e aspartato po<strong>de</strong>m serobtidos a partir <strong>de</strong>, respectivamente, piruvato e oxalacetato, através da reação <strong>de</strong>transaminação tendo glutamato como doador <strong>de</strong> grupo amino. Outros aminoácidosexigem reações adicionais, além da transaminação para sua síntese final. Mas, comoregra, os esqueletos <strong>de</strong> C dos aminoácidos são obtidos a partir dos intermediários daglicólise, do ciclo <strong>de</strong> Krebs e do ciclo das pentoses.3. Há, no entanto, aminoácidos que não po<strong>de</strong>m ser sintetizados por animais <strong>de</strong>vido afalta do precursor que fornece o esqueleto <strong>de</strong> C. Estes são ditos aminoácidosessenciais e tem que ser obtidos na dieta. Por exemplo, humanos tem que conseguirda dieta 9 aminoácidos essenciais.71
4. Triglicerí<strong>de</strong>os e glicogênio são compostos <strong>de</strong> reserva, mobilizados quando hánecessida<strong>de</strong> <strong>de</strong> energia. Em animais, não existem espécies <strong>de</strong> proteína com funções<strong>de</strong> reserva energética, mas no jejum prolongado proteínas são hidrolisadas paraliberar aminoácidos que serão catabolisados para produção <strong>de</strong> energia. O fígado é ocentro <strong>de</strong> catabolisação <strong>de</strong> aminoácidos.5. O catabolismo <strong>de</strong> aminoácidos envolve a eliminação <strong>de</strong> N na forma <strong>de</strong> NH + 4 e atransformação dos esqueletos <strong>de</strong> C em intermediários da glicólise e do ciclo <strong>de</strong> Krebs.6. Duas reações principais permitem a eliminação do amino grupo. Diversosaminoácidos po<strong>de</strong>m transferir o grupo amino para o alfa-cetoglutarato numa reaçãocatalisada por transaminases:aspartato + alfa-cetoglutarato oxalacetato + glutamatoPor outro lado, glutamina e glutamato po<strong>de</strong>m ser <strong>de</strong>saminados em reaçõescatalisadas pela glutaminase e <strong>de</strong>sidrogenase glutâmica, respectivamente:+glutamina + H 2 O glutamato + NH 4glutamato + NAD + (ou NADP + ) + H 2 O NH + 4 + alfa-cetoglutarato + NADH (ouNADPH) + H +O cátion amônio é tóxico, sendo utilizado para a síntese <strong>de</strong> glutamina ou convertidoem uréia no ciclo correspon<strong>de</strong>nte, para fins <strong>de</strong> excreção.7. Aminoácidos como alanina, aspartato e glutamato são ditos glicogênicos porquepo<strong>de</strong>m ser convertidos em, respectivamente, piruvato, oxalacetato e alfa-cetoglutarato,que, por sua vez, po<strong>de</strong>m ser transformados em fosfoenolpiruvato para síntese <strong>de</strong>glicose. Já os aminoácidos leucina e lisina são chamados cetogênicos por produziremexclusivamente acetilCoA como produto <strong>de</strong> <strong>de</strong>gradação, portanto servindo à síntese<strong>de</strong> corpos cetônicos, mas não <strong>de</strong> glicose.MÓDULO 18: CICLO DO NITROGÊNIO1. Os gases mais abundantes no ar atmosférico, O 2 e N 2 , são essenciais para aexistência da vida biológica no planeta Terra, mas divergem quanto à reativida<strong>de</strong>química. O O 2 tem proprieda<strong>de</strong>s <strong>de</strong> radical livre reagindo com relativa facilida<strong>de</strong>, daíservir muito bem como oxidante final na respiração <strong>de</strong> todos os organismos. Já o N 2possui uma tripla ligação altamente estável que lhe confere baixíssima reativida<strong>de</strong>química. Apesar disso, o N 2 gasoso da atmosfera é a fonte do elemento N que garantea vida na Terra. Por essas razões físico-químicas a redução do N 2 atmosférico pelossistemas biológicos tem características muito peculiares.2. A redução química do N 2 a NH 3 exige condições drásticas, 500 graus Celsius <strong>de</strong>temperatura e 300 atm <strong>de</strong> pressão, certamente incompatíveis com a vida biológica.Mas bactérias especializadas do gênero Rhyzobium, que são simbiontes <strong>de</strong> plantas72
leguminosas, reduzem eficientemente N 2 a NH + 4 , uma espécie química totalmentecompatível com o metabolismo <strong>de</strong> todos os organismos. Portanto, o N 2 fixado por essasimbiose entre planta e bactéria garante a disponibilida<strong>de</strong> do elemento N para todasas formas <strong>de</strong> vida terrestre. As bactérias fixadoras <strong>de</strong> N 2 possuem um complexoenzimático singular, a nitrogenase. A reação <strong>de</strong> redução do N 2 a NH + 4 (fixação <strong>de</strong>nitrogênio), qual envolve um redutor po<strong>de</strong>roso a gran<strong>de</strong> investimento <strong>de</strong> energia naforma <strong>de</strong> ATP, é catalisado pela nitrogenase, qual usa NADPH + H + como doador <strong>de</strong>elétrons:N 2 + 8 H + + 8 e- + 16 ATP + 16 H 2 O 2 NH 3 + H 2 + 16 ADP +16 P i3.A volatilida<strong>de</strong> do NH + 4 (NH 3 + H + ) não favorece sua permanência no solo, masexistem bactérias autotróficas <strong>de</strong> vida livre, muito abundantes e largamentedisseminadas, que são especializadas na oxidação do cátion amônio a nitrito e nitratopara fins <strong>de</strong> obtenção <strong>de</strong> energia metabólica. Desta maneira o elemento N éestavelmente <strong>de</strong>positado no solo na forma <strong>de</strong> espécies químicas, sais <strong>de</strong> nitrito enitrato, que são eficientemente absorvidas pelas raízes das plantas e prontamentereduzidas a NH + 4 no interior da célula vegetal.As etapas sumariamente mencionadas compreen<strong>de</strong>m o ciclo do nitrogênio nanatureza: a) redução do N 2 a NH + 4 ; b) oxidação <strong>de</strong> NH + 4 a nitrito e nitrato; c) redução<strong>de</strong> nitrito e nitrato a NH +4 e d) transformação do elemento N <strong>de</strong> inorgânico paraorgânico com a síntese <strong>de</strong> aminoácidos a partir <strong>de</strong> NH + 4 , reação possível em todas aformas <strong>de</strong> organismos biológicos.73






![PE]+ + N. Fragmentação por clivagem sigma](https://img.yumpu.com/50134385/1/180x260/pe-n-fragmentaaao-por-clivagem-sigma.jpg?quality=85)