Redo för omvärdering - Redeye
Redo för omvärdering - Redeye
Redo för omvärdering - Redeye
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
BOLAGSANALYS 17 juni 2010<br />
Sammanfattning<br />
Orexo (ORX.ST)<br />
<strong>Redo</strong> <strong>för</strong> <strong>omvärdering</strong><br />
• Orexo är ett specialty pharma-bolag med fokus på<br />
inflammation och smärta. Huvudprodukten är<br />
Abstral <strong>för</strong> indikationen genombrottssmärta vid<br />
cancer <strong>för</strong> vilken den är godkänd i Europa.<br />
Registreringen pågår i Japan, Kanada och USA.<br />
• Abstral har potential att bli marknadsledande<br />
inom indikationen med en <strong>för</strong>säljningspotential<br />
på upp mot 300 miljoner dollar årligen.<br />
• Orexo står in<strong>för</strong> en period med stark tillväxt, vilket<br />
tar bolaget till lönsamhet redan nästa år.<br />
Värderingen på börsen är låg och vi ser en stor<br />
uppvärderingspotential. Motiverat fundamentalt<br />
värde anser vi är 103 kronor.<br />
Lista:<br />
Börsvärde:<br />
Bransch:<br />
VD:<br />
Styrelseordf:<br />
Small cap<br />
1 025 MSEK<br />
Läkemedel<br />
Torbjörn Bjerke<br />
Håkan Åström<br />
50.0<br />
45.0<br />
40.0<br />
35.0<br />
30.0<br />
25.0<br />
20.0<br />
15.0<br />
10.0<br />
5.0<br />
0.0<br />
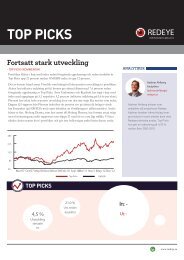
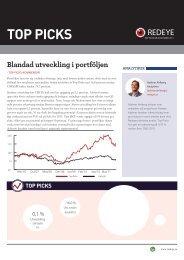
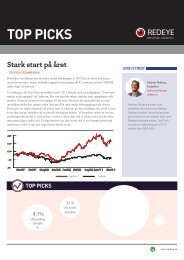
Jun Jul Aug Sep Oct Nov Dec Jan Feb Mar Apr May Jun<br />
OMXS30 Rebased<br />
Orexo<br />
<strong>Redeye</strong> Rating (0-10 poäng)<br />
Ledning<br />
Tillväxtpotential<br />
Lönsamhet<br />
Trygg Placering<br />
Avkastningspotential<br />
8,0 poäng<br />
8,0 poäng<br />
1,0 poäng<br />
7,0 poäng<br />
9,0 poäng<br />
Nyckeltal<br />
2008 2009 2010e 2011e 2012e<br />
Omsättning, MSEK 233 236 201 472 570<br />
Tillväxt 204% 1% -15% 134% 21%<br />
EBITDA -102 -78 -34 168 226<br />
EBITDA-marginal -44% -33% -17% 36% 40%<br />
EBIT -112 -99 -53 148 206<br />
EBIT-marginal -48% -42% -26% 31% 36%<br />
Resultat <strong>för</strong>e skatt -103 -97 -61 140 202<br />
Nettoresultat -103 -98 -61 140 202<br />
Nettomarginal -44% -42% -31% 30% 36%<br />
VPA -4,77 -4,19 -2,46 5,12 7,41<br />
VPA just -4,94 -4,19 -2,46 5,12 7,41<br />
P/E just -8,3 -9,8 -16,7 8,0 5,5<br />
P/S 4,4 4,3 5,1 2,2 1,8<br />
EV/S 3,6 4,0 4,4 1,9 1,6<br />
EV/EBITDA just -8,0 -12,2 -26,4 5,3 4,0<br />
Fakta<br />
Aktiekurs (SEK) 41,0<br />
Antal aktier (milj) 23,4<br />
Börsvärde (MSEK) 1 025<br />
Nettoskuld (MSEK) -107<br />
Free float (%) 55,0<br />
Dagl oms. (’000) 60<br />
Analytiker:<br />
Klas Palin<br />
klas.palin@redeye.se<br />
Björn Fahlén<br />
bjorn.fahlen@redeye.se<br />
Peter Östling<br />
peter.ostling@redeye.se<br />
Viktig information: All information kring ansvarsbegränsningar och potentiella intressekonflikter finns att läsa i slutet av rapporten.<br />
<strong>Redeye</strong>, Mäster Samuelsgatan 42, 10tr, Box 7141, 103 87 Stockholm. Tel +46 8-545 013 30. E-post: info@redeye.se
Orexo<br />
<strong>Redeye</strong> Rating: Bakgrund och definition<br />
Avsikten med <strong>Redeye</strong>s Rating är att den ska ge en bra bild av potential i <strong>för</strong>hållande till risk i<br />
aktien. <strong>Redeye</strong>s Rating utgörs av fem värderingsnycklar. Varje värderingsnyckel består av en<br />
sammanvägning av ett antal faktorer som värderas på en betygskala från 0 till 2 poäng (2 poäng:<br />
Bra/Utmärkt, 1 poäng: Godkänd/Tillfredsställande, 0 poäng: Dålig/Bristfällig).<br />
I <strong>Redeye</strong>s interna handbok specificeras på ett standardiserat sätt vad som krävs <strong>för</strong> varje enskilt<br />
faktorbetyg. I vissa fall kan en faktor viktas mer/mindre om den anses extra viktig/oviktig.<br />
Maxpoängen <strong>för</strong> en värderingsnyckel är 10 poäng (full cirkel=röd cirkel). Minpoängen är 0 poäng<br />
(tom cirkel=grå cirkel). Det är alltså det sammanlagda betyget som ligger till grund <strong>för</strong> <strong>Redeye</strong>s<br />
Rating av aktien, inte de individuella faktorbetygen.<br />
Ledning<br />
De faktorerna som utgör bedömning av ledningen är 1) historik, 2) branscherfarenhet, 3)<br />
marknadskommunikation och 4) motivation. Faktorn historik viktas dubbelt då denna faktor anses<br />
extra viktig.<br />
Tillväxtpotential<br />
De faktorerna som utgör bedömning av tillväxtpotential är 1) marknadsstorlek, 2) marknadstillväxt,<br />
3) samarbeten, 4) produkt differentiering och 5) konkurrenssituation. Kriterierna väger lika tungt i<br />
den sammantagna bedömningen av värderingsnyckeln tillväxtpotential.<br />
Lönsamhet<br />
De faktorerna som utgör bedömning av lönsamhet är 1) stabil vinstutveckling, 2) bruttomarginal,<br />
3) EBIT-marginal och 4) avkastning på eget kapital. Faktorn stabil vinstutveckling viktas dubbelt då<br />
denna faktor anses extra viktig.<br />
Trygg placering<br />
De faktorerna som utgör bedömning av trygg placering är 1) oberoende av enstaka händelser, 2)<br />
finansiell situation, 3) ägarstruktur, 4) konjunkturkänslighet och 5) aktiens likviditet. Faktorn<br />
oberoende av enstaka händelser viktas dubbelt då denna faktor anses extra viktig. Faktorerna<br />
konjunkturkänslighet och aktiens likviditet viktas med 0,5x.<br />
Avkastningspotential<br />
De faktorerna som utgör bedömning av avkastningspotential är 1) fundamental värdering, 2)<br />
relativvärdering, 3) marknads<strong>för</strong>väntningar, 4) nyhetsflöde/triggers, 5) oupptäckt aktie och 6)<br />
insynshandel. Faktorn fundamental värdering viktas dubbelt då denna faktor anses extra viktig.<br />
Faktorerna nyhetsflöde/triggers, marknads<strong>för</strong>väntningar, oupptäckt aktie och insynshandel viktas<br />
med 0,5x.<br />
Bolagsanalys<br />
2
Orexo<br />
Innehåll<br />
Investeringssammanfattning ................................................................ 5<br />
Ledningen får höjt betyg ........................................................................................................... 6<br />
Stor värderingsuppsida ............................................................................................................. 7<br />
Finansiella prognoser ........................................................................... 8<br />
Stark finansiell situation ........................................................................................................... 8<br />
Försäljning och milstolpsintäkter ............................................................................................. 9<br />
Kostnader ................................................................................................................................. 11<br />
Resultat .................................................................................................................................... 11<br />
Risker i prognoser ................................................................................................................... 12<br />
Värdering ............................................................................................ 13<br />
Tyngdpunkt på Abstral ........................................................................................................... 14<br />
Relativvärdering ...................................................................................................................... 16<br />
Scenarioanalys ......................................................................................................................... 17<br />
Stor värderingsrabatt jäm<strong>för</strong>t med branschen ....................................................................... 18<br />
Bolagsbeskrivning .............................................................................. 20<br />
Egna produkter till marknaden .............................................................................................. 20<br />
Bolagets projektportfölj .......................................................................................................... 21<br />
Nya produkter mot marknad .................................................................................................. 21<br />
Abstral - Tillväxtmotor ....................................................................... 22<br />
Cancersmärta utbrett vid cancer ............................................................................................ 23<br />
Utbrett med genombrottssmärta ............................................................................................ 23<br />
Behandlingsriktlinjer saknas .................................................................................................. 24<br />
Behandling av genombrottssmärta ........................................................................................ 25<br />
Fentanyl en lämplig substans ................................................................................................. 26<br />
Actiq <strong>för</strong>sta produkten på marknaden ................................................................................... 27<br />
Nya produkter utmanar .......................................................................................................... 28<br />
Intranasala produkter är snabba ............................................................................................ 28<br />
Oral administration <strong>för</strong>edras .................................................................................................. 29<br />
Hälsoekonomisk påverkan ..................................................................................................... 29<br />
Narkotikaklassning ett visst hinder ........................................................................................ 30<br />
Onkologer viktigast att bearbeta ............................................................................................ 30<br />
Patientunderlaget visar på stor potential ............................................................................... 31<br />
Liten marknad inom ett stort område .................................................................................... 32<br />
Genombrottssmärta – En marknad med potential ................................................................ 33<br />
Den amerikanska marknaden viktigast .................................................................................. 33<br />
Cephalon behåller greppet om USA…. ................................................................................... 33<br />
…men Abstral är en god utmanare till tronen ........................................................................ 33<br />
Europa har haft låg prioriterat av Cephalon .......................................................................... 34<br />
Bra tillväxt i Europa efter lansering ....................................................................................... 34<br />
Prostrakan kopplar grepp om Europa .................................................................................... 36<br />
Okrattad mark i Japan ............................................................................................................ 37<br />
Ensamma på tronen i Japan ................................................................................................... 37<br />
Stor potential men svårigheter tornar upp sig ....................................................................... 37<br />
REMS ett potentiellt hinder .................................................................................................... 38<br />
Speciellt <strong>för</strong> Onsolis ................................................................................................................ 38<br />
Bolagsanalys<br />
3
Orexo<br />
OX17 - Rätt partner men när? ............................................................. 40<br />
Partner på plats ....................................................................................................................... 40<br />
Marknaden .............................................................................................................................. 41<br />
Den receptfria marknaden är målet ....................................................................................... 41<br />
Avtalsvillkoren ett osäkerhetsmoment ................................................................................... 42<br />
Utbredd sjukdom .................................................................................................................... 42<br />
Kliniska resultat ...................................................................................................................... 42<br />
Utvecklingsplan ...................................................................................................................... 43<br />
Patentsituation ännu oklar i USA ........................................................................................... 43<br />
Försäljningsprognoser ............................................................................................................ 43<br />
Edluar - dåligt differentierad .............................................................. 45<br />
Sömnbesvär ett växande problem .......................................................................................... 45<br />
Läkemedel på marknaden ...................................................................................................... 45<br />
Marknaden .............................................................................................................................. 46<br />
Få nya produkter under utveckling ........................................................................................ 47<br />
Silenor godkänt av FDA .......................................................................................................... 47<br />
Bakslag från FDA .................................................................................................................... 47<br />
Försäljningsprognoser ............................................................................................................ 48<br />
Appendix 1 - Övriga projekt ................................................................ 49<br />
Appendix 2 - Kibion AB ....................................................................... 56<br />
Appendix 3 - Konkurrenter Abstral ..................................................... 58<br />
Appendix 4 - Partners Abstral ............................................................. 62<br />
Appendix 5 - Drug delivery ................................................................. 65<br />
Appendix 6 - Vetenskaplig plattform ................................................... 69<br />
Appendix 7 - Ägare ............................................................................... 71<br />
Appendix 8 - Ledning ........................................................................... 73<br />
Appendix 9 - Historik .......................................................................... 76<br />
Sammanfattning <strong>Redeye</strong> Rating .......................................................... 78<br />
Bolagsanalys<br />
4
Orexo<br />
Investeringssammanfattning<br />
Orexo är ett specialty pharma-bolag med i dagsläget tre olika verksamhetsgrenar;<br />
diagnostik, drug delivery och forskning och utveckling inom smärta<br />
och inflammation. Bolaget har fyra produkter i marknaden. Därtill har bolaget<br />
en lovande projektportfölj med produkter både i tidig och sen utvecklingsfas,<br />
se bild nedan.<br />
Produkt och projektportfölj Orexo<br />
Produkt Indikation Preklinik Klinisk fas I Klinisk fas II Klinisk fas III Marknad<br />
Diabact UBT<br />
Heliprobe System<br />
Abstral<br />
Edluar<br />
OX-NLA<br />
OX17<br />
OX914<br />
OX219<br />
OX-AAF<br />
OX-MPI<br />
Helicobacter pylori<br />
Helicobacter pylori<br />
Genombrottssmärta vid cancer<br />
Tillfälliga sömnbesvär<br />
Rinit<br />
GERD<br />
KOL/Astma<br />
Opioidberoende<br />
KOL/Astma<br />
Inflammatorisk smärta<br />
Källa: <strong>Redeye</strong> Research<br />
Fokus på Abstral som är<br />
godkänd <strong>för</strong> genombrottssmärta<br />
vid cancer<br />
I denna analys är fokus fram<strong>för</strong>allt på Abstral en produkt godkänd i Europa<br />
<strong>för</strong> indikationen genombrottssmärta vid cancer. Orexo har ett globalt partnernätverk<br />
men licenstagare och distributörer kring Abstral. Genombrottssmärta<br />
vid cancer är visserligen marknadsmässigt begränsat i sin storlek,<br />
Abstral har potential att bli ledande inom området med en potential på upp<br />
mot 300 miljoner dollar i årlig <strong>för</strong>säljning. Vår värdering av Orexo inkluderar<br />
även prognoser <strong>för</strong> ovanstående projekt i bilden, utom projekten<br />
OX914 och OX-NLA, vilka vi i nuläget av <strong>för</strong>siktighetsskäl exkluderat.<br />
Abstral har potential att<br />
bli marknadsledande<br />
Orexo står in<strong>för</strong> en stark tillväxtperiod drivet av intäkter från lanserade<br />
produkter, främst Abstral som är lanserat i Europa och under registrering i<br />
Japan, Kanada, Ryssland och USA. Marknaden <strong>för</strong> genombrottssmärta<br />
räknar vi med kommer visa stark tillväxt närmaste åren drivet av fler<br />
aktörer och nya produkter som lanseras. Senaste tidens <strong>för</strong>säljningssiffror<br />
som presenterats <strong>för</strong> den europeiska marknaden bekräftar att Abstral har<br />
en marknadsledande position i en marknad under kraftig tillväxt.<br />
Orexo visar vinst år 2011<br />
<strong>Redeye</strong> räknar med att tillväxten <strong>för</strong> Abstral ska ta Orexo till positiva<br />
kassaflöden från den löpande verksamheten under det andra halvåret år<br />
2011. Bolaget har ett fortsatt beroende av engångsposter, vilka tillsammans<br />
med de ökade rörelseintäkterna lyfter bolaget till svarta siffror nästa år.<br />
Bolagsanalys<br />
5
Orexo<br />
Stark finansiell ställning<br />
Bolagets finanser är starka och tillräckliga utan något nära <strong>för</strong>estående<br />
behov av ytterligare kapital med likvida medel på över 200 miljoner kronor.<br />
Det är vårens riktade konvertibelemission till Novo Growth Equity (NGE)<br />
och kontantersättningen på nästan 80 miljoner kronor som bolaget fick vid<br />
tecknandet av avtalet med Johnson & Johnson som snabbt <strong>för</strong>bättrat läget.<br />
Detta ger Orexo resurser <strong>för</strong> mer offensiva satsningar, vilket bland annat<br />
innebär ökat fokus på att bygga bolaget vidare mot egen <strong>för</strong>säljningsorganisation<br />
med egna produkter. Målet riktas mot specialistindikationer<br />
där bolaget med en mindre <strong>för</strong>säljningsorganisation effektivt kan bearbeta<br />
marknaden. Produktutvecklingen kommer ske inom bolagets kärnområde<br />
drug delivery, vilket begränsar kostnaderna och utvecklingstiden.<br />
Bolaget går mot egen<br />
<strong>för</strong>säljningsorganisation<br />
En <strong>för</strong>sta produkt är OX219, ett patentskyddat läkemedel <strong>för</strong> behandling av<br />
missbruk av opioider. Läkemedlet har chans att snabbt nå marknaden<br />
redan 18-24 månader efter att studier påbörjats, vilket vi räknar med sker i<br />
det tredje kvartalet i år. OX219 är en omformulering av det redan godkända<br />
läkemedlet Suboxone vars <strong>för</strong>säljning i USA uppgick till drygt 700 miljoner<br />
dollar i fjol. Produkten är enklare att administrera, har en snabbt insättande<br />
effekt och utan den bittra smaken från ursprungsmolekylen. Vi räknar med<br />
att Orexo tar fler drug delivery-produkter till klinisk prövning kommande<br />
året, <strong>för</strong> att bygga ett bolag inom specialistområden.<br />
Ny ägare rätt medicin<br />
Den riktade emissionen till NGE var inte bara ett välbehövligt kapitaltillskott<br />
<strong>för</strong> Orexo. Dessutom köpte NGE aktier från tidigare ägarna Apax<br />
Partners och SLS Ventures och blev därigenom bolagets näst störste<br />
aktieägare med en ägarandel på 10,7 procent av kapitalet. Därmed <strong>för</strong>svann<br />
två säljare, vilket har minskat det överhäng som funnits i aktien. NGE är en<br />
ägare med industriell bakgrund som vill vara aktiv och har tagit plats i<br />
styrelsen. Vid konvertering kan ägarandelen öka till 18,8 procent.<br />
Avtal med J&J validerar<br />
värdet från Biolipox<br />
Starkt avtal i tufft klimat<br />
ger plus åt ledningen<br />
Orexo har nyligen tecknat ett bra licensavtal med Johnson & Johnson <strong>för</strong> de<br />
prekliniska projekten inom luftvägssjukdomar, OX-CLI och OX-ESI. Avtalet<br />
innebär att J&J betalar forskningsstöd till Orexo <strong>för</strong> den prekliniska<br />
utveckling. En viktig <strong>för</strong>utsättning <strong>för</strong> att framgångsrikt lyckas utveckla<br />
Orexo till ett ledande och lönsamt specialty pharama-bolag där de breda<br />
primärvårdsindikationerna licensieras till resursstarka partners. Avtalet<br />
kan ge Orexo över 500 miljoner dollar samt en royalty från <strong>för</strong>säljning.<br />
Därtill har Orexo rätten att tillsammans med partners marknads<strong>för</strong>a<br />
produkter från samarbetet <strong>för</strong> de nordiska och baltiska länderna. Avtalet är<br />
inte bara viktigt från ett finansiellt perspektiv utan synliggör även värden<br />
från det tidigare ifrågasatta köpet av Biolipox.<br />
Ledningen får höjt betyg<br />
Ledningen har gjort ett bra jobb, inte minst med att knyta värdeskapande<br />
partneravtal senaste åren. Det är under en period med ett tufft klimat <strong>för</strong><br />
licensavtal, speciellt <strong>för</strong> tidiga prekliniska projekt. Vi ger där<strong>för</strong> speciellt<br />
tummen upp till bolagets senaste affär med Johnson & Johnson. Mot<br />
bakgrund av vad ledningen levererat <strong>för</strong>ändrar vi vårt betyg <strong>för</strong> Ledningen<br />
Bolagsanalys<br />
6
Orexo<br />
med två steg från tidigare 6 poäng till 8 poäng (<strong>för</strong> <strong>för</strong>klaring se sid 2,<br />
<strong>Redeye</strong> Rating: Bakgrund och definition). Nästa stora utmaning <strong>för</strong><br />
ledningen är att framgångsrikt utveckla Orexo till ett lönsamt bolag med<br />
egen <strong>för</strong>säljningsorganisation.<br />
Enbart värdet <strong>för</strong> Abstral<br />
motiverar dagens aktiekurs<br />
Stor värderingsuppsida<br />
Efter en trög start på året har aktien utvecklats bättre än index under det<br />
andra kvartalet. Bakom en bra aktieutveckling finns bolagets lösta finansiering,<br />
rapporterade framgångarna i <strong>för</strong>säljning <strong>för</strong> Abstral och senaste<br />
avtalet med Johnson & Johnson. Börsvärdet uppgår idag till cirka 950<br />
miljoner kronor, vilket vi anser långt ifrån återspeglar de värden som finns i<br />
bolaget. Dagens börsvärde motiveras mer än väl enbart av Abstral. Den låga<br />
aktiekursen speglar en grundmurad misstro mot bolagets <strong>för</strong>måga att<br />
kapitalisera på sina tillgångar, vilket är o<strong>för</strong>tjänt.<br />
O<strong>för</strong>tjänt hög värderingsrabatt<br />
Värderingsrabatten <strong>för</strong> Orexo ligger i topp i en jäm<strong>för</strong>else med branschkollegor,<br />
detta trots att bolaget har produkter i marknaden, närmar sig<br />
lönsamhet och har starka finanser. Bästa <strong>för</strong>klaringen bakom detta är<br />
bolagets historik som ännu spökar hos investerare sedan <strong>för</strong>värvet av<br />
Biolipox under år 2007. Ett <strong>för</strong>värv drivet från huvudägaren HealthCap.<br />
Risken <strong>för</strong> liknande affärer framöver har <strong>för</strong>svunnit sedan Novo A/S trätt in<br />
på ägaresidan anser vi.<br />
Tillväxt bakom en<br />
<strong>omvärdering</strong><br />
Låg värderingen och starka finanser, drivet av en stark intäktsökning från<br />
<strong>för</strong>säljning av Abstral talar <strong>för</strong> en <strong>omvärdering</strong> av aktien.<br />
Tabell Orexo - <strong>för</strong>väntat nyhetsflöde 2010<br />
Händelse<br />
Tidpunkt<br />
Stärka finanserna Q1 2010 √<br />
Avtal OX-AAF Q2 2010 √<br />
Abstral godkänt i Kanda Q3 2010<br />
Abstral godkänt i USA Q3 2010<br />
Abstral godkänt i Ryssland Q3 2010<br />
Bioekvivalensstudie inleds, OX219 Q3 2010<br />
Fas III inleds, OX17 Q4 2010<br />
Val läkemedelskandidat OX-MPI Q4 2010<br />
Abstral lanseras i USA Q4 2010<br />
Källa: <strong>Redeye</strong> Research<br />
Bolagsanalys<br />
7
Orexo<br />
Finansiella prognoser<br />
Royaltybaserad affärsmodell<br />
Verksamheten i Orexo är idag <strong>för</strong>lustbringande. Vi räknar dock med att<br />
bolagets läkemedel i lanseringsfas står in<strong>för</strong> en stark tillväxtfas som tar<br />
bolaget till svarta siffror. Redan från och med nästa år bedömer vi att Orexo<br />
ska kunna redovisa vinst från sin verksamhet. Orexos affärsstrategi är en<br />
royaltybaserad modell där partners står <strong>för</strong> kommersialisering av bolagets<br />
produkter.<br />
Stark tillväxt i löpande<br />
intäkter<br />
Stark finansiell situation<br />
För årets <strong>för</strong>sta kvartal redovisade Orexo en nettoomsättning på 36,4<br />
miljoner kronor. Löpande intäkter från lanserade produkter uppgick till<br />
21,3 miljoner kronor. Royaltyintäkterna <strong>för</strong> Abstral har kraftigt <strong>för</strong>bättrats<br />
samtidigt som kvartalet innehöll en mindre del engångsposter jäm<strong>för</strong>t med<br />
fjolåret. Licensintäkterna under kvartalet uppgick till 6,3 miljoner kronor<br />
och är en milstolpsbetalning från Prostrakan i samband med klartecken <strong>för</strong><br />
lansering på den Italienska marknaden, se tabell nedan.<br />
Nettoomsättning under det <strong>för</strong>sta kvartalet, (MSEK)<br />
Period Jan-mars 2010 Jan-mars 2009<br />
Royalty Abstral 8,5 1,3<br />
Royalty Edluar 0 0<br />
Kibion AB 9,9 10,3<br />
Prostrakan AB J/V 2,9 2,6<br />
Löpande intäkter 21,3 14,2<br />
Vidarefakt. FoU 8,8 12,4<br />
Licensintäkter 6,3 88,5<br />
Totalt 36,4 115,1<br />
Källa: Orexo<br />
Kostnaderna sjunker till<br />
följd av fjolårets omstrukturering<br />
Bolagets kostnader <strong>för</strong> det <strong>för</strong>sta kvartalet uppgick till sammanlagt 64,5<br />
miljoner kronor, där den mest framträdande posten är forsknings- och<br />
utvecklingskostnader. Samtliga kostnader under kvartalet har minskat,<br />
dock har inte kostnad sålda varor minskat då dessa samvarierar med<br />
bolagets <strong>för</strong>säljning. Att merparten av kostnaderna sjunker är en följd av att<br />
Orexo genom<strong>för</strong>t en omstrukturering av verksamheten och minskat<br />
organisationen. Dessutom har bolagets verksamhet i Sverige koncentrerats<br />
till huvudkontoret i Uppsala, vilket ger lägre lokalkostnader framåt. En<br />
annan viktig faktor bakom de lägre kostnaderna är att inga kliniska studier<br />
pågår <strong>för</strong> närvarande, se tabell nästa sida.<br />
Bolagsanalys<br />
8
Orexo<br />
Kostnader under det <strong>för</strong>sta kvartalet, (MSEK)<br />
Period jan-mars 2010 jan-mars 2009<br />
Kostnad sålda varor 6,4 5,7<br />
Försäljningskostander 7,4 9,3<br />
Administrationskostnader 8,8 10,8<br />
Forsknings- och<br />
utvecklingskostnader<br />
41,9 66,1<br />
Totalt 64,5 91,9<br />
Källa: Orexo<br />
Likvida medel på omkring<br />
220 miljoner kronor<br />
Trots framsteg i att reducera kostnaderna redovisades ett negativt resultat<br />
<strong>för</strong> det <strong>för</strong>sta kvartalet i år på -27,6 miljoner kronor. Kassaflödet från den<br />
löpande verksamheten under kvartalet uppgick till -19,7 miljoner kronor.<br />
Det negativa kassaflödet under det <strong>för</strong>sta kvartalet till trots är den<br />
finansiella situationen <strong>för</strong> Orexo i ett mycket gott skick efter vårens riktad<br />
konvertibelemission och det nyligen tecknade licensavtalet med Johnson &<br />
Johnson. Per den sista maj beräknar vi att Orexo har likvida medel på<br />
sammanlagt omkring 220 miljoner kronor och därtill en outnyttjad<br />
checkräckningskredit på 35 miljoner kronor.<br />
Finansiella prognoser <strong>för</strong> Orexo 2006-2012<br />
Tabell 2. Prognoser Orexo 2006 2007 2008 2009 Kv1:10 Kv2:10P Kv3:10P Kv4:10P 2010P 2011P 2012P<br />
Intäkter<br />
Royaltyintäkter 0,0 0,0 0,7 18,5 8,5 11,6 14,0 23,5 57,6 179,2 352,4<br />
Abstral® royalties 0,0 0,7 16,2 8,5 11,0 13,0 22,0 54,5 167,6 290,7<br />
Edluar royalties - 0,0 0,0 2,3 0,0 0,6 1,0 1,5 3,1 11,5 28,9<br />
OX219 0,0 0,0 0,0 0,0 22,2<br />
OX17 royalties 0,0 0,0 0,0 0,0 10,7<br />
Licensintäkter (1) 106,2 34,0 123,2 119,6 6,3 2,2 6,5 27,1 42,1 166,0 98,6<br />
Prostrakan AB J/V 50% 9,0 10,8 2,9 3,0 3,0 3,5 12,4 16,7 21,8<br />
Kibion 17,3 24,9 28,6 40,7 9,9 10,0 10,4 12,0 42,3 46,5 51,2<br />
Vidare fakt. FoU 8,4 15,2 71,9 46,6 8,8 10,5 12,4 15,4 47,1 63,7 45,7<br />
Totala rörelseintäkter 131,9 74,1 233,3 236,2 36,4 37,2 46,3 81,5 201,5 472,1 569,6<br />
Kostnader<br />
Kostnad sålda varor -11,2 -14,4 -17,4 -23,6 -6,4 -6,5 -5,4 -7,0 -25,3 -30,0 -32,0<br />
Försäljningskostnader -7,8 -11,6 -38,8 -39,2 -7,4 -7,5 -7,0 -8,5 -30,4 -46,0 -72,2<br />
Administrationskostnader -57,4 -74,2 -55,4 -46,3 -8,8 -9,0 -8,0 -9,0 -34,8 -38,3 -44,0<br />
Forskning och utveckling -95 -156 -238 -224,2 -41,8 -39,0 -38,7 -46,7 -166,2 -210,0 -215,0<br />
Totala rörelsekostnader -170,9 -241,8 -349,8 -333,4 -64,5 -62,0 -59,1 -71,2 -256,7 -324,3 -363,2<br />
Övriga intäkter/kostnader -1,8 -1 4,0 -1,7 1,3 0,0 1,0 0,0 2,3 0,0 0,0<br />
EBIT (Rörelseresultat) -40,8 -167,7 -112,5 -98,9 -26,7 -24,8 -11,8 10,3 -52,9 147,9 206,4<br />
Finansnetto 7,5 7,8 9,0 2,2 -0,9 -2,3 -2,4 -3,0 -8,6 -8,0 -4,0<br />
Skatt 0,0 0,0 0,4 -1,3 0,0 0,0 0,0 0,0 0,0 0,0 0,0<br />
Nettoresultat -33 -160 -103 -98,0 -27,6 -27,1 -14,2 7,3 -61,5 139,9 202,4<br />
Vinst per aktie (VPA) -2,4 -7,4 -4,6 -4,2 -1,1 -1,1 -0,6 0,3 -2,5 5,6 8,1<br />
VPA, full skatt (2) -2,4 -7,4 -3,3 -3,0 -0,8 -0,8 -0,4 0,2 -1,8 4,0 5,8<br />
VPA, justerat (3) -10,0 -9,0 -8,8 -8,1 -1,0 -0,9 -0,7 -0,9 -3,5 -2,6 1,9<br />
Antal aktier, <strong>för</strong>e utspädning 13,9 21,6 22,5 23,4 25,0 25,0 25,0 25,0 25,0 25,0 25,0<br />
(1) Inkluderar milstolpsbetalningar från licensavtal med Boehringer Ingelheim, Johnson & Johnson, Meda, Novartis och ProStrakan<br />
(2) Exklusive skatteeffekter från underskottsavdrag<br />
(3) Exklusive poster av engångskaraktär, licensintäkter, skatteffekter och goodwillavskrivningar<br />
Källa: <strong>Redeye</strong> Research<br />
Bolagsanalys<br />
9
Orexo<br />
Beroendet av engångsersättningar<br />
minskar<br />
kommande år<br />
Försäljning och milstolpsintäkter<br />
Det är royalty och milstolpsbetalningar som är de dominerande intäkterna<br />
<strong>för</strong> Orexo närmaste åren. Under innevarande år och <strong>för</strong> nästa år beräknas<br />
engångsposter så som milstolpsbetalningar fortsatt utgöra en viktig del och<br />
kommer tillsammans med royaltyintäkter balansera kostnaderna med<br />
intäkter, se grafen nedan.<br />
Prognos sammanlagda intäkter år 2008-15<br />
1600,0<br />
1400,0<br />
Miljoner kronr<br />
1200,0<br />
1000,0<br />
800,0<br />
600,0<br />
400,0<br />
200,0<br />
0,0<br />
2008 2009 2010P 2011P 2012P 2013P 2014P 2015P<br />
Försäljnings intäkter Milstolpsbetalningar Vidare fakt. FoU<br />
Källa: Orexo och <strong>Redeye</strong> Research<br />
Den starka tillväxten <strong>för</strong> fram<strong>för</strong>allt Abstral kommer dock leda till att<br />
engångsposter minskar i betydelse, där vi räknar med att positiva kassaflöden<br />
uppnås med löpande intäkter från och med det andra halvåret nästa<br />
år, se graf nedan.<br />
Löpande intäkter står<br />
in<strong>för</strong> en stark tillväxt<br />
Prognos löpande intäkter mot totala kostnader år 2008-15<br />
1200<br />
1000<br />
Miljoner kronor<br />
800<br />
600<br />
400<br />
200<br />
0<br />
2008 2009 2010P 2011P 2012P 2013P 2014P 2015P<br />
Löpande intäkter<br />
Kostnader<br />
Källa: Orexo och <strong>Redeye</strong> Research<br />
Bolagsanalys<br />
10
Orexo<br />
I prognosen fram till år 2015 ingår intäkter från joint venture bolaget<br />
Prostrakan AB, Kibion AB, Abstral, Edluar och riskjusterade intäkter från<br />
projekten OX17 och OX219. Därefter utgår vi ifrån antagande om going<br />
concern <strong>för</strong> verksamheten.<br />
Kostnaderna <strong>för</strong>väntas<br />
stiga men i långsammare<br />
takt än intäkterna<br />
Kostnader<br />
Fjolårets omstrukturering har sänkt kostnaderna betydligt. Med stärkta<br />
finanser och nya samarbetsavtal tror vi att kostnaderna successivt kommer<br />
stiga när det nu finns kapital <strong>för</strong> tillväxt. Därtill räknar vi med att nya<br />
kliniska studier inleds redan i år och därefter får vi en löpande klinisk<br />
aktivitet, vilket ger stigande kostnader. Eftersom det dock handlar om<br />
projekt inom drug delivery där inte lika omfattande kliniska studier<br />
efterfrågas från myndigheter blir effekten inte dramatisk. Vi har i tabellen<br />
nedan sammanställt våra kostnadsprognoser uppdelat på olika<br />
kostnadsslag.<br />
Prognos kostnader år 2008-15 uppdelat på olika kostnadsslag<br />
800,0<br />
700,0<br />
600,0<br />
Miljoner kronor<br />
500,0<br />
400,0<br />
300,0<br />
200,0<br />
100,0<br />
0,0<br />
2008 2009 2010P 2011P 2012P 2013P 2014P 2015P<br />
Kostnad sålda varor<br />
Administrationskostnader<br />
Försäljningskostnader<br />
Forskning och utveckling<br />
Källa: Orexo och <strong>Redeye</strong> Research<br />
Svarta siffror nästa år<br />
Resultat<br />
Orexo står in<strong>för</strong> en stark tillväxtperiod <strong>för</strong> intäkterna samtidigt som<br />
kostnaderna inte ökar i samma takt. Vi räknar där<strong>för</strong> med att resultatet<br />
närmaste åren kommer vända från att vara negativt till positiva siffror<br />
redan från och med nästa år. För nästa års resultat ingår periodiserade<br />
poster av engångskaraktär som milstolpsbetalningar från Johnson &<br />
Johnson, Kyowa Hakko Kirin, Novartis och Prostrakan om cirka 180<br />
miljoner kronor. För enbart intäkter från den löpande verksamheten dröjer<br />
det till år 2012 tills dessa överstiger kostnaderna. I figuren nedan visas vår<br />
prognos <strong>för</strong> nettoresultatet <strong>för</strong> Orexo perioden år 2008-15.<br />
Bolagsanalys<br />
11
Orexo<br />
Prognos rörelseresultatet, 2008-15<br />
800<br />
700<br />
600<br />
Miljoner kronor<br />
500<br />
400<br />
300<br />
200<br />
100<br />
0<br />
-100<br />
2008 2009 2010P 2011P 2012P 2013P 2014P 2015P<br />
-200<br />
Källa: Orexo och <strong>Redeye</strong> research<br />
Ingen skattebetalning<br />
<strong>för</strong>rän år 2014<br />
Bolaget har stora <strong>för</strong>lustavdrag som kan utnyttjas när nu resultatet vänder<br />
till svarta siffror. Vid årsskiftet uppgick de sammanlagda <strong>för</strong>lustavdragen<br />
till 990,7 miljoner kronor, var<strong>för</strong> vi i våra prognoser inte räknar med att<br />
Orexo kommer behöva betala bolagsskatt <strong>för</strong>rän år 2014. Bolagets starka<br />
vinsttillväxt anser vi utgör ett starkt skäl <strong>för</strong> en <strong>omvärdering</strong> av Orexoaktien.<br />
Risker i prognoser<br />
Som alltid vid prognoser <strong>för</strong> produkter i tidig lansering eller under utveckling<br />
finns många osäkra parametrar. Främsta riskerna är kopplade till<br />
konkurrenter, regulatoriska frågor och att nå acceptans i marknaden <strong>för</strong><br />
bolagets godkända produkter. Vad gäller Abstral finns det kvar en betydande<br />
regulatorisk risk, speciellt <strong>för</strong> den amerikanska marknaden, där ett väl<br />
fungerande REMS-program är nyckel till framgång.<br />
För bolagets prekliniska och kliniska projekt finns det en risker kopplade<br />
till utvecklingen. Dock är riskerna betydligt lägre <strong>för</strong> Orexos drug deliveryprojekt<br />
(OX17, OX219, OX-NLA) än <strong>för</strong> den innovativa forskningen (OX-<br />
AAF och OX-MPI).<br />
Bolagsanalys<br />
12
Orexo<br />
Värdering<br />
Värderas med diskonterad<br />
kassaflödesmodell<br />
Orexo står in<strong>för</strong> en mycket viktig period i bolagets historia med godkända<br />
läkemedel på marknaden. Närmaste åren <strong>för</strong>väntas bolagets produkter<br />
godkännas <strong>för</strong> <strong>för</strong>säljning på fler viktiga marknader, vilket kommer ligga<br />
bakom en stark tillväxtfas som tar bolaget till lönsamhet. För att värdera<br />
Orexo tillämpar <strong>Redeye</strong> en traditionell diskonterad kassaflödesmodell. De<br />
framtida kassaflödena utgörs inledningsvis huvudsakligen av <strong>för</strong>säljningsintäkter<br />
från Kibion AB och Prostrakan AB, engångsposter i form av milstolpsbetalningar<br />
från partners och royaltyintäkter från lanserade läkemedel.<br />
De senare kommer bli mer betydelsefulla under prognosperioden.<br />
Orexo går snabbt mot lönsamhet med en trovärdig långsiktig strategi,<br />
var<strong>för</strong> denna modell är att <strong>för</strong>edra fram<strong>för</strong> en projektuppdelad modell.<br />
Fundamentalt motiverat<br />
värde 2.565 miljoner kronor<br />
eller 103 kronor per aktie<br />
Vår värderingsmodell utgår ifrån prognoser <strong>för</strong> varje enskild produkt. För<br />
de projekt som är i klinisk utveckling har vi tagit hänsyn till utvecklingsrisken<br />
och riskjusterat de framtida kassaflödena. För att nuvärdeberäkna de<br />
framtida kassaflödena använder vi bolagets genomsnittliga kapitalkostnad<br />
(WACC) som uppgår till 12,1 procent, när vi har ett betavärde på 1,40.<br />
Baserat på ovanstående antaganden uppgår vårt motiverade fundamentala<br />
värde till 2.565 miljoner kronor eller 103 kronor per aktie. I tabellen nedan<br />
har vi sammanställt en känslighetsanalys mellan avkastningskrav och<br />
rörelsemarginal (EBIT-marginal).<br />
Känslighetsanalys av fundamentalt motiverat värde (DCF)<br />
EBITmarginal<br />
WACC<br />
9,0% 10,0% 11,0% 12,1% 13,0% 14,0% 15,0%<br />
30% 121 109 99 90 84 77 72<br />
35% 133 119 107 97 90 83 77<br />
40% 144 128 115 104 96 88 82<br />
45% 155 138 124 111 102 94 86<br />
50% 166 147 132 118 108 99 91<br />
Källa: <strong>Redeye</strong> Research<br />
Vi räknar med att Orexo från år 2017 når en rörelsemarginal på knappt 40<br />
procent. Från ett branschperspektiv en hög marginal, då den genomsnittliga<br />
rörelsemarginalen <strong>för</strong> läkemedelsbolag inom recept<strong>för</strong>eskrivna<br />
läkemedel mellan år 2005-08 uppgick till 28 procent. Det som gör att<br />
Orexo kommer ligga över detta snitt är dels fortsatt fokus på royaltydrivna<br />
intäkter och dels en inriktning med egen verksamhet till nischade<br />
specialistområden.<br />
Bolagsanalys<br />
13
Tyngdpunkt på Abstral<br />
Orexo<br />
När vi istället tillämpar en projektuppdelad värderingsmodell av Orexo får<br />
vi ett fundamentalt motiverat värde på 2.537 miljoner kronor, eller 101<br />
kronor per aktie, se tabell nedan.<br />
Orexo - Kassaflödesvärdering<br />
Sum-of-the-parts Orexo<br />
Projekt Indikation Chans <strong>för</strong> Royaltysats Topp<strong>för</strong>säljn. Lansering Nuvärde<br />
lansering (MUSD) (MSEK)*<br />
Abstral<br />
Genombrottssmärta<br />
vid cancer<br />
100% 8-30% 300 Lanserad 1 576<br />
Edluar Sömnbesvär 100% 12-15% 80 Lanserad 220<br />
OX17 GERD 50% 12-15% 400 2012 547<br />
OX219 Opioidberoende 50% Egen <strong>för</strong>säljning 100 2012 121<br />
OX-AAF Astma och KOL 5% 8-12% 2 000 2020 445<br />
OX-MPI<br />
Smärta och<br />
inflammation<br />
5% 10% 2 500 2018 100<br />
Motiverat teknologivärde (MSEK) 3 010<br />
Kibion AB 100<br />
Nettokassa (MSEK) 107<br />
Ackumulerade kostnader (MSEK) -680<br />
Motiverat börsvärde (MSEK) 2 537<br />
Antal aktier, full utspädning (milj.) 25,0 #<br />
Motiverad aktiekurs (SEK) 101<br />
Aktuell aktiekurs (SEK) 40<br />
Kurspotential 154%<br />
* Nuvärdesberäkningen baseras på ett avkastningskrav på 12,1 % och en SEK/USD-kurs på 7,4<br />
#<br />
Inklusive full utspädning<br />
Källa: <strong>Redeye</strong> Research<br />
Stor tyngdpunkt på<br />
Abstral<br />
Ovanstående tabell visar värde<strong>för</strong>delningen mellan de olika projekten vi<br />
inkluderat i värderingen av Orexo. I värderingsmodellen har vi inte tagit<br />
med projekten OX-NLA och OX914, vilka vi i nuläget känner osäkra kring<br />
om den fortsatta utvecklingen. För projektet OX219 har vi räknat med att<br />
Orexo står <strong>för</strong> kommersialisering själva, var<strong>för</strong> ingen royalty tillfaller<br />
bolaget. Den projektuppdelade modellen visar tydligt att enbart Abstral mer<br />
än väl motiverar dagens börsvärde <strong>för</strong> Orexo som uppgår till omkring 950<br />
miljoner kronor. På nästa sida presenteras värde<strong>för</strong>delningen mellan de<br />
olika projekten i ett cirkeldiagram.<br />
Bolagsanalys<br />
14
Orexo<br />
Värde<strong>för</strong>delning mellan Orexos olika projekt<br />
OX-MPI<br />
3%<br />
Kibion AB<br />
3%<br />
OX-AAF<br />
14%<br />
OX219<br />
4%<br />
Abstral<br />
51%<br />
OX-17<br />
18%<br />
Edluar<br />
7%<br />
Källa: <strong>Redeye</strong> Research<br />
Cirkeldiagrammet <strong>för</strong>tydligar den stora värde<strong>för</strong>delningen kopplat till<br />
Abstral i dagsläget, vilken uppgår till drygt halva värdet i bolaget. Vi tror att<br />
<strong>för</strong> ett bolag som Orexo skulle det vara gynnsamt med en jämnare <strong>för</strong>delning<br />
av värdet, <strong>för</strong> att attrahera långsiktigt kapital och minska riskerna i<br />
investeringen. Strategin att bygga ett bolag med egen <strong>för</strong>säljningsorganisation<br />
med egna produkter är ett steg i rätt riktning. I tabellen nedan visas<br />
en känslighetsanalys <strong>för</strong> ett antal nyckelvariabler i vår värdering av Orexo.<br />
Abstral är den viktigaste<br />
värdedrivaren<br />
Orexo - Känslighetsanalys<br />
Scenario<br />
Nuvärde<br />
(MSEK)<br />
Per aktie % <strong>för</strong>ändring<br />
Huvudalternativ 2 564 103<br />
Valutakurs (SEK/USD)<br />
+10% 2999 120 16,9%<br />
-10% 2130 85 -16,9%<br />
Avkastningskrav<br />
+5% 1726 69 -32,7%<br />
+2% 2156 86 -15,9%<br />
-2% 3138 126 22,4%<br />
-5% 4614 185 79,9%<br />
Marknadsandel Abstral<br />
+10% 4276 171 66,7%<br />
+5% 3420 137 33,4%<br />
-5% 1709 68 -33,4%<br />
-10% 852 34 -66,8%<br />
Projektrisk OX17<br />
Når marknad 3461 138 35,0%<br />
Läggs ned 1668 67 -35,0%<br />
Projektrisk OX219<br />
Når marknad 2692 108 5,0%<br />
Läggs ned 2443 98 -4,7%<br />
Källa: <strong>Redeye</strong> Research<br />
Bolagsanalys<br />
15
Orexo<br />
Attraktiv värdering jäm<strong>för</strong>t<br />
med branschkollegor<br />
Relativvärdering<br />
Både <strong>för</strong>säljning och resultat <strong>för</strong> Orexo räknar vi med <strong>för</strong>bättras närmaste<br />
åren. I tabellen nedan har vi sammanställt nyckeltal <strong>för</strong> utvalda amerikanska<br />
och europeiska specialty pharma-bolag och drug delivery-bolag<br />
perioden 2010-12. För år 2012 handlas aktien under branschsnittet enligt<br />
marknadens prognoser. Applicerar vi median p/e-talet <strong>för</strong> år 2012 handlas<br />
Orexo med en rabatt jäm<strong>för</strong>t med gruppen på 24 procent. Applicerar vi våra<br />
prognoser är bolagets låga värdering jäm<strong>för</strong>t med jäm<strong>för</strong>bara bolag än mer<br />
framträdande, där p/e-talet indikerar en relativrabatt på 57 procent.<br />
Relativvärdering, utvalda specialty pharma och drug delivery-bolag<br />
P/E EV/EBITDA EV/S<br />
Bolag 2010E 2011E 2012E 2010E 2011E 2012E 2010E 2011E 2012E<br />
ALKERMES INC neg. neg. 32,5 neg. neg. 10,6 4,6 3,7 2,9<br />
AUXILIUM PHARMACEUTICALS INC neg. 41,1 16,6 neg. 26,8 7,8 4,8 3,0 2,3<br />
AVANIR PHARMACEUTICALS INC-A neg. neg. 14,8 n.a. n.a. n.a. n.a. 4,2 1,3<br />
BIODELIVERY SCIENCES INTL 17,5 neg. 14,1 neg. 5,9 5,6 4,6 2,5 1,4<br />
BIOVAIL CORP 9,7 9,1 8,7 7,1 6,9 6,6 2,9 2,8 2,7<br />
CLAVIS PHARMA neg. neg. 22,0 neg. neg. 17,6 16,4 10,7 5,4<br />
DELCATH SYSTEMS INC neg. neg. 33,2 neg. neg. n.a. n.a. 19,1 4,0<br />
DEPOMED INC neg. 31,0 6,5 neg. 13,4 n.a. 1,5 1,1 0,8<br />
DUSA PHARMACEUTICALS INC 42,0 14,0 5,7 n.a. n.a. n.a. 0,9 0,8 0,7<br />
ELAN CORP PLC neg. neg. 49,0 21,6 15,4 11,8 2,9 2,7 2,7<br />
ENDO PHARMACEUT HLDGS INC 6,9 6,6 6,1 3,4 3,3 3,0 1,3 1,2 1,2<br />
ENZON PHARMACEUTICALS INC neg. neg. neg. 12,6 30,9 n.a. 4,1 5,5 4,9<br />
FLAMEL TECHNOLOGIES-SP ADR neg. neg. neg. n.a. n.a. n.a. 3,4 3,7 2,6<br />
HOSPIRA INC 16,2 14,4 12,2 9,7 8,9 8,0 2,6 2,4 2,2<br />
INTERMUNE INC neg. neg. neg. neg. neg. neg. 16,4 7,3 4,0<br />
ISTA PHARMACEUTICALS INC. 90,0 8,1 n.a. 5,1 2,4 1,7 0,4 0,3 0,3<br />
KING PHARMACEUTICALS INC 11,6 10,8 9,3 4,9 4,6 3,6 1,3 1,2 1,1<br />
MEDA AB-A SHS 10,1 9,2 8,0 6,8 6,6 6,3 2,4 2,4 2,3<br />
MEDICINES COMPANY 11,4 71,5 14,2 5,3 neg. n.a. 0,6 0,8 1,0<br />
MEDICIS PHARMACEUTICAL-CL A 11,1 10,4 11,2 4,0 3,8 4,1 1,4 1,3 1,3<br />
NEKTAR THERAPEUTICS neg. neg. neg. neg. neg. n.a. 7,4 8,8 5,2<br />
NOVAVAX INC neg. neg. 51,1 n.a. n.a. n.a. n.a. 28,1 3,2<br />
PENWEST PHARMACEUTICALS CO n.a. n.a. n.a. n.a. n.a. n.a. 2,3 1,9 1,6<br />
PERRIGO CO 21,6 18,5 17,1 13,3 10,4 10,7 2,7 2,3 2,1<br />
PROSTRAKAN GROUP PLC neg. 12,0 5,7 22,3 8,3 4,8 1,6 1,2 1,0<br />
QUESTCOR PHARMACEUTICALS 17,5 13,6 11,5 n.a. n.a. n.a. 4,9 4,2 3,7<br />
SALIX PHARMACEUTICALS LTD n.a. 24,9 12,1 110,5 16,2 7,0 6,0 3,7 2,5<br />
SANTARUS INC 15,9 28,6 7,3 6,1 14,5 neg. 0,6 0,8 0,7<br />
SAVIENT PHARMACEUTICALS INC neg. neg. 60,6 neg. 13,5 n.a. 87,5 7,6 4,9<br />
SHIRE PLC-ADR 17,5 14,4 12,9 n.a. n.a. n.a. n.a. n.a. n.a.<br />
SKYEPHARMA PLC 58,3 2,2 1,4 7,0 5,6 5,7 2,1 2,0 2,1<br />
VALEANT PHARMACEUTICALS INTE 17,2 15,0 12,2 9,7 8,7 n.a. 4,0 3,4 2,8<br />
VIVUS INC neg. neg. 55,0 neg. neg. n, 32,0 8,1 5,3<br />
WARNER CHILCOTT PLC-CLASS A 7,4 6,7 6,2 6,8 6,5 n.a. 2,9 2,9 2,9<br />
Mean 22,5 18,1 18,5 15,1 10,6 7,2 7,5 4,6 2,5<br />
Median 16,2 13,8 12,2 7,0 8,5 6,3 2,9 2,8 2,3<br />
OREXO AB neg. 30,9 9,3 906,2 34,8 7,7 3,9 2,9 2,2<br />
PROGNOSER ( REDEYE) neg. 7,6 5,3 neg. 5,0 3,7 4,2 1,8 1,5<br />
Källa: Bloomberg och <strong>Redeye</strong> Research<br />
Bolagsanalys<br />
16
Orexo<br />
Scenarioanalys<br />
Orexo står in<strong>för</strong> en period med ett flertal olika betydelsefulla besked, vilka<br />
kommer ligga tillgrund <strong>för</strong> vårt tillväxtscenario. Fram<strong>för</strong>allt är det fokus på<br />
besked kring Abstral som är bolagets huvudsakliga värderivare. I tabellen<br />
nedan presenteras en scenarioanalys över tänkbara utfall.<br />
Nuläget: vårt huvudscenario där Abstral blir godkänt i USA i år och Japan<br />
nästa år.<br />
Restriktivt REMS-program,<br />
motiverar lägre värde med<br />
15 procent<br />
Scenario 1, REMS-programmet i USA harmoniseras med det program<br />
som finns <strong>för</strong> Onsolis (se sid 38), vilket ger sämre marknadsutsikter <strong>för</strong> de<br />
snabbverkande fentanylbaserade läkemedlen i USA. Vi bedömer effekter <strong>för</strong><br />
den amerikanska marknaden blir 25 procent lägre i omfattningen än vårt<br />
huvudscenario.<br />
Scenario 2, Abstral blir inte godkänt på den japanska marknaden och<br />
partnern Kyowa Hakko Kirin lägger ned sina ambitioner att få produkten<br />
godkänd.<br />
Scenario 3, De nya snabbverkande fentanylbaserad läkemedlen som lanseras<br />
går bra och den ökade marknadsnärvaron av flera aktörer ger en snabb<br />
<strong>för</strong>bättring i kunskapen inom behandlingsområdet och ger en snabbare<br />
marknadstillväxt än vårt huvudscenario med 20 procent.<br />
Resultat scenarioanalys<br />
120<br />
110<br />
100<br />
90<br />
80<br />
70<br />
60<br />
Nuläge Scenario 1 Scenario 2 Scenario 3<br />
Källa: <strong>Redeye</strong> Research<br />
Bolagsanalys<br />
17
Stor värderingsrabatt jäm<strong>för</strong>t med branschen<br />
Orexo<br />
Orexo handlas idag till en mycket hög rabatt på drygt 60 procent i <strong>för</strong>hållande<br />
till vårt fundamentalt motiverade värde. Det är klart högre än snittet<br />
<strong>för</strong> sektorkollegor noterade på Stockholmsbörsen, se tabell nedan.<br />
Över 60 procents värderingsrabatt<br />
Fundamental värderingsrabatt bolag inom läkemedelsutveckling<br />
80%<br />
Aktiekursrabatt<br />
70%<br />
60%<br />
50%<br />
40%<br />
30%<br />
20%<br />
10%<br />
Genomsnittlig rabatt 42%<br />
0%<br />
Active<br />
Biotech<br />
Bioinvent<br />
Diamyd<br />
Medical<br />
Karo Bio Medivir Orexo<br />
Källa: <strong>Redeye</strong> Research<br />
Det senaste året har flera bolag inom sektorn fått se sina kurser återhämta<br />
sig efter att ha varit mycket låga under finanskrisen. En <strong>för</strong>klaring till det är<br />
att investerare successivt justerat ner sin riskpremie allteftersom finanskrisen<br />
klingat av. Dessutom har flera bolags projekt fortskridit utan<br />
problem, vilket brukar vara goda nyheter <strong>för</strong> investerare i sektorn. Den<br />
genomsnittliga rabattnivån bland svenska bioteknikbolag ligger idag på<br />
drygt 40 procent, vilket är över den historiska nivån <strong>för</strong> de svenska bolagen<br />
som vi följer. Senaste månaderna har vi sett en stigande branschrabatt i takt<br />
med den finansiella krisen i Europa har tilltagit. I spåret av den har osäkerheten<br />
ökat, vilket <strong>för</strong>sämrat riskviljan. När riskviljan snabbt sjunker<br />
drabbas speciellt icke lönsamma bolag.<br />
Rabatten i Orexo bland de<br />
högsta i sektorn<br />
Börserna har dock senaste tiden stabiliserats och återhämtat delar av nedgången<br />
i maj. Det är där<strong>för</strong> rimligt att vi under de närmaste månaderna får<br />
se flera investerare komma tillbaka till denna typ av aktier. Därtill väntas<br />
flera betydelsefulla nyheter från ovanstående bolag, inklusive <strong>för</strong> Orexo,<br />
som kan verka katalysator <strong>för</strong> hela sektorn. Orexo är ett av de bolag där<br />
värderingsrabatten är som allra högst och detta trots att bolaget har en mer<br />
utvecklad produktportfölj än ovanstående bolag och en stabil finansiell<br />
situation. Bästa <strong>för</strong>klaringen bakom detta är bolagets historik som ännu<br />
spökar hos investerare. Det finns fortsatt en utbredd skepsis sedan <strong>för</strong>värvet<br />
av Biolipox under år 2007. Många ansåg att det påtvingades av huvudägaren<br />
HealthCap. Vi anser att det inte finns risk <strong>för</strong> liknande affärer<br />
framöver sedan Novo A/S trätt in på ägaresidan. Dessutom visar senaste<br />
licensavtalet med Johnson & Johnson på värdet av tillgångarna inom astma<br />
och KOL-området, vilka följd med från Biolipox.<br />
Bolagsanalys<br />
18
Orexo<br />
En annan faktor som vägt in var<strong>för</strong> investerare inte varit villiga att ta<br />
position i aktien har varit det överhäng med många riskkapitalbolag bland<br />
ägarna. Även här var affären med Novo viktig där aktier från två<br />
riskkapitalaktörer köptes ut. Det finns kvar ett par till och fram<strong>för</strong>allt har<br />
HealthCap fortsatt en agenda att träda ur sin investering senast år 2012.<br />
Bolagsanalys<br />
19
Orexo<br />
Bolagsbeskrivning<br />
Orexo har fyra produkter<br />
i marknaden<br />
Orexo är ett specialty pharma-bolag med i dagsläget tre olika verksamhetsgrenar;<br />
diagnostik, drug delivery och forskning och utveckling inom smärta<br />
och inflammation. Bolaget har fyra produkter i marknaden. Två läkemedel<br />
och två diagnostiska produkter. Att Orexo lyckats ta egna produkter till<br />
marknaden är en viktig validering av den interna kompetens som finns i att<br />
ta produkt från idé till marknaden. En betydelsefull pusselbit då målet är ta<br />
ett större eget ansvar <strong>för</strong> nya projekt vad gäller klinisk utveckling och<br />
kommersialisering på utvalda marknader. För att uppnå detta är fokus på<br />
specialistsegment där ingen gigantisk <strong>för</strong>säljningsorganisation krävs. Ett<br />
<strong>för</strong>sta steg i att bygga egen <strong>för</strong>säljningsorganisation togs redan under år<br />
2007 när ett <strong>för</strong>säljningsbolag <strong>för</strong> de nordiska marknaderna upprättades,<br />
hälftenägt tillsammans med Prostrakan.<br />
Grundat i Uppsala <strong>för</strong> 15<br />
år sedan<br />
Bolaget satsar på drug<br />
delivery <strong>för</strong> utveckling av<br />
nya läkemedel<br />
Huvudfokus <strong>för</strong> verksamheten är läkemedelsutveckling inom smärta och<br />
inflammation. Affärsmodellen har byggt på en klassisk royaltydriven modell<br />
där partners ansvarar <strong>för</strong> <strong>för</strong>säljning och marknads<strong>för</strong>ing av läkemedlen.<br />
En mycket kostnadseffektiv modell <strong>för</strong> ett litet bolag med begränsade resurser.<br />
Bolaget grundades år 1995 av Thomas Lundqvist, Anders Petterson och<br />
Christer Nyström med målet att utveckla läkemedel med betydande<br />
marknadspotential genom att kombinera egenutvecklad patenterad drug<br />
delivery-teknologi med redan kända och väldokumenterade aktiva läkemedelssubstanser.<br />
Detta var bolagets strategi fram till år 2007 då Biolipox<br />
<strong>för</strong>värvades, då tillträdde nuvarande verkställande direktör Torbjörn Bjerke<br />
sin post. Genom <strong>för</strong>värvet av Biolipox till<strong>för</strong>des ny innovativ forskning inom<br />
inflammationsområdet. Projekten är kostsamma att driva och dessutom<br />
krävs omfattande <strong>för</strong>säljningsresurser vid en kommersialisering, var<strong>för</strong><br />
målet varit att finna partners. Bolaget har framgångsrikt funnit partners<br />
villiga att teckna lukrativa globala licensavtal, senast Johnson & Johnson.<br />
Avtal som ger en validering av bolagets spetskompetens som finns inom<br />
arakidonsyra-området.<br />
Egna produkter till marknaden<br />
Den fortsatta produktutvecklingen av egna produkter ska ske inom bolagets<br />
grundläggande kunskapsområde, drug delivery. Fördelarna med drug<br />
delivery är att kostnaderna och tiden till marknaden kan hållas på låga<br />
nivåer. En stark tillväxt från lanserade produkter kommer bära kostnaderna<br />
och ta bolaget till lönsamhet. Det är positivt <strong>för</strong> med en egen <strong>för</strong>säljningsorganisation<br />
<strong>för</strong> Orexo som ger bättre kontroll över verksamheten.<br />
Orexos huvudkontor ligger i Uppsala och är där bolaget har sina rötter och<br />
är grundat. Utöver sin verksamhet i Uppsala har Orexo även en mindre<br />
enhet i Bath, Storbritannien, vilken följde med vid fjolårets <strong>för</strong>värv av det<br />
brittiska drug delivery-bolaget Pharmakodex. Orexo har idag 103 antal<br />
anställda med kompetens från preklinisk forskning och utveckling hela<br />
vägen fram till en registrering av ett nytt läkemedel. Orexo har även en egen<br />
Bolagsanalys<br />
20
Orexo<br />
GMP-anläggning, vilken används <strong>för</strong> tillverkning av läkemedel till kliniska<br />
prövningar. Anläggningen är dock inte tillräcklig <strong>för</strong> bolagets kommersiella<br />
produkter där produktion sker hos kontraktstillverkare eller hos<br />
samarbetspartners.<br />
En bred projektportfölj<br />
Bolagets projektportfölj<br />
Bolaget har idag en omfattande projektportfölj både med produkter inom<br />
drug delivery och inom arakidonsyra-området. Samtliga projekt inom<br />
arakidonsyra är i dagsläget licensierade till partners som bekostar<br />
utvecklingen och kommer stå <strong>för</strong> kommersialiseringen. Vi har valt att<br />
fokusera vår analys på Abstral som är en lovande produkt godkänd <strong>för</strong> den<br />
Europeiska marknaden och under registrering <strong>för</strong> den amerikanska,<br />
japanska och kanadensiska marknaden. Utifrån den utveckling vi sett på<br />
<strong>för</strong>säljningen <strong>för</strong> den europeiska marknaden finns tydliga signaler att<br />
produkten står sig väl i konkurrensen med möjlighet att bli ledande i<br />
Europa och Japan inom behandlingsområdet genombrottssmärta vid<br />
cancer.<br />
I analysen har vi även inkluderat läkemedlet Edluar mot tillfälliga sömnbesvär.<br />
För Edluar har framgångarna uteblivit, då marknadsgodkännandet<br />
inte inkluderade dess snabbt insättande effekt i produktetikett. Utan en<br />
tydlig differentiering, enbart med dess sublinguala administrationsform,<br />
mot generika inom sömnläkemedel anser vi att produkten har en begränsad<br />
<strong>för</strong>säljningspotential.<br />
Kliniska studier väntas<br />
starta <strong>för</strong> OX219 och<br />
OX17<br />
Nya produkter mot marknad<br />
Produktkandidaten OX17 har i fas II-studier visat lovande resultat <strong>för</strong><br />
patienter med gatroesofageal refluxsjukdom och ett globalt licensavtal<br />
tecknades i fjol med Novartis Consumer Health. Målet är att positionera<br />
OX17som efterträdare till Prevacid 24HR, som säljs receptfritt på den<br />
amerikanska marknaden.<br />
Produkten OX219 följd med i <strong>för</strong>värvet av Pharmakodex och är en ny<br />
formulering av det redan godkända läkemedlet Suboxone. Vi räknar med<br />
att detta blir bolagets <strong>för</strong>sta produkt att bygga en egen organisation kring<br />
<strong>för</strong> den amerikanska marknaden. Detta är en specialistprodukt som kan<br />
säljas med en begränsad organisation.<br />
Projekten OX-NLA och OX-MPI är inte inkluderade i våra prognoser då vi i<br />
nuläget är osäkra på den fortsatta utvecklingen. Även projektet OX-914 är<br />
exkluderat i värderingen av Orexo, då vi anser att möjligheterna <strong>för</strong> att<br />
finna en partner som är villig att vidareutveckla produkten är liten.<br />
Bolagsanalys<br />
21
Orexo<br />
Abstral - Tillväxtmotor<br />
Abstral är ett läkemedel<br />
<strong>för</strong> patienter med genombrottssmärta<br />
Abstral är ett läkemedel utvecklat av Orexo <strong>för</strong> behandling av patienter som<br />
drabbas av akut smärta, vilket uppstår vid exempelvis cancer, operation<br />
eller ryggskott. Första indikationen är genombrottssmärta vid cancer, där<br />
ett godkännande <strong>för</strong> den Europeiska marknaden blev klart under år 2008.<br />
Lanseringen av Abstral går enligt plan och produkten är sedan maj lanserad<br />
på alla de stora europeiska marknaderna. Den europeiska marknaden <strong>för</strong><br />
läkemedel mot genombrottssmärta vid cancer är liten i dagsläget på<br />
omkring 100 miljoner dollar men uppvisar en hög tillväxttakt.<br />
Globalt partner och distributörsnätverk<br />
på plats <strong>för</strong><br />
Abstral<br />
Orexo har varit mycket framgångsrika i att finna partner och distributörer<br />
<strong>för</strong> Abstral på alla viktiga marknader, vilka ansvarar <strong>för</strong> marknads<strong>för</strong>ing<br />
och <strong>för</strong>säljning av Abstral (se appendix sid 62). Bolaget har inte bara varit<br />
framgångsrikt i att teckna avtal <strong>för</strong> Abstral, utan även fått bra villkor vad<br />
gäller milstolpsersättning och royalty från <strong>för</strong>säljning. Jäm<strong>för</strong>t med<br />
konkurrenterna är avtalen <strong>för</strong> Abstral de med bäst villkor, något som visar<br />
på attraktionskraften hos produkten och Orexos partners tro på dess<br />
potential. Till Abstral finns ett etablerat globalt partnernätverk på plats och<br />
läkemedlet är i registreringsprocess på den amerikanska, japanska,<br />
kanadensiska och ryska marknaden, se tabell nedan.<br />
Partners <strong>för</strong> Abstral och utvecklingsstatus<br />
Partner Status Royalty (%) Milstolpsersättning<br />
Europa Prostrakan Marknad 25-30 19,9 MEUR<br />
USA Prostrakan Registrering 23-28 25 MUSD<br />
Japan Kyowa Hakko Kirin Registrering 7-9* 2,25 MUSD<br />
Kanada Prostrakan Registrering 15-20* -<br />
Kina NovaMed Okänt ** 4,75 MUSD<br />
Israel Neopharm Förbereder registrering ** Okänt<br />
Delar av Östeuropa,<br />
ej EU Gedeon Richter Marknad ** -<br />
Källa: <strong>Redeye</strong> Research<br />
* <strong>Redeye</strong>s bedömning, **Distributionsavtal<br />
Abstral ger en snabbt<br />
insättande effekt<br />
Abstral är en tablett innehållande den aktiva substansen fentayl, som är en<br />
syntetisk opioid ofta använd <strong>för</strong> smärtlindring. Det är dess kraftiga smärtlindrande<br />
effekt (1000 gångar starkare än morfin) kombinerat med en kort<br />
varaktighet som gör substansen lämplig vid behandling av akut smärta. När<br />
dessa egenskaper kombineras med Orexos patenterade sublinguala<br />
tabletteknologi ger det en snabbt insättande effekt med en kort varaktighet,<br />
vilket kännetecknar genombrottssmärta vid cancer.<br />
Bolagsanalys<br />
22
Cancersmärta utbrett vid cancer<br />
Orexo<br />
Globalt uppskattar världshälsoorganisationen (WHO) att 12 miljoner<br />
personer under år 2007 fick diagnosen cancer och i Sverige omkring<br />
50.000 personer. Den globala <strong>för</strong>ekomsten <strong>för</strong>väntas öka till följd av en<br />
åldrande befolkning och stiga till 17 miljoner per år från år 2030, en årlig<br />
ökningstakt på drygt 1,5 procent. Behandlingen av cancer har <strong>för</strong>bättrats<br />
med tidigare diagnos och nya behandlingsmetoder, vilket minskat risken<br />
<strong>för</strong> att dö i cancer. Tillsammans med de demografiska <strong>för</strong>ändringarna<br />
innebär det att fler kommer leva med sjukdomen. Vid cancer är smärta<br />
vanligt <strong>för</strong>ekommande och dessutom uppfattas smärta som ett av de mest<br />
fruktade symptomen av sjukdomen.<br />
Många personer kommer<br />
få diagnosen cancer<br />
Det finns flera orsaker till att smärta uppk0mmer i samband med cancer,<br />
där huvudorsakerna är själva tumören eller behandlingen. Smärtsymptomen<br />
varierar givetvis mellan patienter och beroende på tumörtyp, var<br />
tumören är lokaliserad och hur avancerad cancern utvecklats. En mer<br />
framskriden cancer ökar <strong>för</strong>ekomsten av smärta och dess intensitet. Smärta<br />
påverkar bland annat sömnen och kan leda till sömnlöshet, <strong>för</strong>sämrad<br />
rörlighet och social isolering. Där<strong>för</strong> är god behandling av smärta i samband<br />
med cancer viktigt <strong>för</strong> att uppnå bra livskvalité. För att understryka<br />
vikten av en god smärtbehandling av cancerpatienter har WHO klassificerat<br />
den som ett av de viktigaste områdena inom cancervården. Under år 1986<br />
introducerade WHO de <strong>för</strong>sta behandlingsriktlinjerna, som ligger bakom<br />
framgångar i att behandla den kroniska cancersmärtan. Undersökningar<br />
visar att mellan 70-90 procent av cancerpatienterna med kronisk smärta<br />
uppnår en god smärtlindring.<br />
Utbrett med genombrottssmärta<br />
Genombrottssmärta är ett akut smärtillstånd som bryter igenom en i övrigt<br />
god smärtlindrande behandling, med akut smärtökning som följd, se bild<br />
nedan.<br />
Smärtan bryter igenom underhållsbehandlingen<br />
Snabbt <strong>för</strong>lopp <strong>för</strong> vid<br />
genombrottssmärta<br />
Källa: Medscape<br />
En genombrottsattack är mycket smärtsam och härstammar från antingen<br />
sjukdomen, behandlingen eller kopplad till fysisk aktivitet. Studier inom<br />
området visar på ett mycket snabbt <strong>för</strong>lopp där smärttoppen nås redan<br />
inom 3–5 minuter och pågår i 15–60 minuter. Det finns inga exakta siffror<br />
Bolagsanalys<br />
23
Orexo<br />
på hur utbrett det är med genombrottssmärta hos cancerpatienter. Det har<br />
dock genom<strong>för</strong>ts ett antal studier inom området <strong>för</strong> att kartlägga<br />
<strong>för</strong>ekomsten, vars resultat vi sammanställt i tabellen nedan.<br />
Vanligt med genombrottssmärta<br />
Andel patienter med genombrottssmärta vid cancer<br />
Förekomst Population Land Studie referens<br />
47% 180 Sju största marknaderna Datamonitor (2009)<br />
63% 573 Europa och Israel Breivik m.fl. (2009)<br />
65% 1095 Internationell Caraceni (2004)<br />
23% 144 USA Fortner (2003)<br />
70% 74 USA Hwang (2003)<br />
63% 256 USA Fortner (2002)<br />
41% 397 Spanien Gomez-Batiste (2002)<br />
89% 245 Storbritannien Zeppetella (2000)<br />
39% 613 Tyskland Petkze (1999)<br />
51% 178 USA Portenoy (1999)<br />
86% 22 USA Fine (1998)<br />
64% 63 USA Portenoy (1990)<br />
Källa: Datamonitor och Breakthroughcancerpain.org<br />
I tabellen ovan framgår stora skillnader mellan studier där <strong>för</strong>ekomsten<br />
varierar mellan 23-89 procent hos cancerpatienter. Förklaringar till detta är<br />
exempelvis att det saknas en global definition samt olikheter i diagnos och<br />
behandling. Andra anledningar är variationerna i smärtan under sjukdomen,<br />
cancerpatienter upplever flera typer av smärta och skillnader i hur<br />
framskriden cancern är <strong>för</strong> de patienter som inkluderats. De allra högsta<br />
siffrorna i tabellen är <strong>för</strong> patienter med framskriden cancer i livets<br />
slutskede, Fine och Zepptella.<br />
Förekomsten av genombrottssmärta<br />
kan vara<br />
ännu högre<br />
Trots höga siffror är det tänkbart att ovanstående siffror ändå är en<br />
underskattning, då patienter tenderar att inte vilja rapportera sin smärta.<br />
Orsak är dels rädsla <strong>för</strong> ändrad behandling samt dels rädsla <strong>för</strong> att smärta<br />
är ett tecken på <strong>för</strong>värrad sjukdom.<br />
Behandlingsriktlinjer saknas<br />
Trots att vetskapen om genombrottssmärta funnits i över tjugo år saknas<br />
ännu tydliga internationella behandlingsriktlinjer. En del av problemet är<br />
att det fortfarande saknas en global definition, vilket <strong>för</strong>svårat jäm<strong>för</strong>elser<br />
av studier och därmed i att utfärda behandlingsriktlinjer. Organisationen<br />
International Association for the Study of Pain (IASP) gjorde en undersökning<br />
under år 2004 som visade på stora skillnader mellan länder i<br />
diagnos och behandling av genombrottssmärta. Det finns exempelvis en<br />
tydlig skillnad i rapportering av genombrottssmärta i engelskspråkiga<br />
länder där <strong>för</strong>ekomst är vanligare mot icke engelskspråkiga länder.<br />
Bolagsanalys<br />
24
Orexo<br />
Vikten av god smärtkontroll kan inte nog understrykas <strong>för</strong> cancerpatienter.<br />
Det är inte alls ovanligt att genombrottssmärta ofta är kopplat till själva<br />
behandlingen, vilket påverkar patientens följsamhet. En dåligt kontrollerad<br />
smärta kan leda till att patienten väljer att gå ned i dos, uppehåll i behandling<br />
eller till och med att patienten helt och hållet avbryter behandlingen.<br />
Det är där<strong>för</strong> viktigt att uppnå hög tillfredsställelse hos patienter med<br />
behandlingen.<br />
Dagens läkemedel ger dålig<br />
följsamhet till smärt<strong>för</strong>loppet<br />
Behandling av genombrottssmärta<br />
En genombrottsattack kan i vissa lägen <strong>för</strong>utsägas, exempelvis vid fysisk<br />
aktivitet. Då kan patienten välja att i <strong>för</strong>väg öka dosen <strong>för</strong> att <strong>för</strong>ebygga<br />
attacken genom att öka medicineringen av underhållsbehandlingen. Något<br />
som dock leder till ökade biverkningar som exempelvis andningsdepression<br />
och <strong>för</strong>stoppning. Det ger även en hög bestående läkemedelskoncentration<br />
efter att den själva akuta smärtfasen är över. Merparten av attackerna anses<br />
dock inte vara <strong>för</strong>utsägbara, vilket <strong>för</strong>svårar <strong>för</strong>ebyggande behandling.<br />
American Pain Foundation genom<strong>för</strong>de i fjol en undersökning som visade<br />
att 74 procent av attackerna uppstod spontant. Den vanligaste behandlingen<br />
av genombrottssmärta är att addera starka opioider till underhållsbehandlingen,<br />
som exempelvis morfin och oxykodon. Ett problem med<br />
dessa läkemedel är att även när dessa administreras i tablett med<br />
omedelbar frissättning tar det cirka 30-40 minuter till dess att<br />
smärtlindrande effekt uppnås. Det ger en dålig följsamhet till själva<br />
<strong>för</strong>loppet, se illustration nedan.<br />
Dålig följsamhet med etablerad behandling<br />
Källa: Pain.com<br />
Undersökningar som Datamonitor låtit gör visar att många patienter med<br />
genombrottssmärta anser att behandling med morfin och oxykodon är<br />
otillräcklig <strong>för</strong> att få kontroll på sin genombrottssmärta, se nästa sida.<br />
Bolagsanalys<br />
25
Orexo<br />
Andel smärtpatienter där <strong>för</strong>stavalsbehandling är otillräcklig<br />
40<br />
35<br />
30<br />
25<br />
20<br />
15<br />
10<br />
5<br />
0<br />
Totalt USA Japan Frankrike Tyskland Italien Spanien UK<br />
Källa: Datamonitor, Cancer Pain, 2009<br />
Många patienter i behov<br />
av effektivare läkemedel<br />
Morfin och oxykodon inte<br />
lämpligt vid genombrottssmärta<br />
American Pain Foundation har gjort en liknande undersökning på cancerpatienter,<br />
där 44 procent av patienter med genombrottssmärta uppgav att<br />
de inte hade god smärtkontroll med hjälp av nuvarande läkemedel.<br />
European Pain in Cancerstudien uppgav 72 procent av de cancerpatienter<br />
som upplevde genombrottssmärta att deras läkemedel inte gav en god<br />
smärtlindring. Endast 25 procent uppgav att de var nöjda med nuvarande<br />
smärtbehandling, vilket kan jäm<strong>för</strong>as med 78 procent av de som inte<br />
upplevde genombrottssmärta.<br />
Fentanyl en lämplig substans<br />
För att härma det mycket snabba smärt<strong>för</strong>loppet vid genombrottssmärta<br />
krävs läkemedel som kan ge en snabbare insättande effekt. Ett sätt är att<br />
exempelvis ge opioider intravenöst. Det ger en snabbt insättande effekt,<br />
men problemet med en bestående högre läkemedelskoncentration finns<br />
kvar när morfin och oxykodon används, då effekten varar i upp till fyra<br />
timmar. En mer lämpad substans är fentanyl. Den är kraftigt smärtstillande<br />
och ger en snabb smärtstillande effekt med kort varaktighet. I sjukhusmiljö<br />
är intravenösadministrering en möjlighet <strong>för</strong> att substansen snabbt ska<br />
upptas i blodbana och därmed ge god smärtlindring. Utan<strong>för</strong> sjukhuset<br />
behövs dock en enklare administrering som patienten själv kan sköta.<br />
Önskvärd läkemedelsprofil vid genombrottssmärta<br />
Källa: Pain.com<br />
Bolagsanalys<br />
26
Orexo<br />
En <strong>för</strong>utsättning <strong>för</strong> att uppnå en snabbt insättande effekt är att substansen<br />
administreras på ett sätt så att den snabbt upptas i blodbana. I tabellen<br />
nedan har vi sammanställt ett par olika tillgängliga metoder.<br />
Olika administrationsformer av starka opioider<br />
Administration Intravenös Oralt Bukalt/Sublingulat Intranasalt<br />
Insättande effekt Direkt Långsam Snabb Snabb<br />
Fördelar<br />
Nackdelar<br />
Källa: <strong>Redeye</strong> Research<br />
Snabbt och kontrollerbar<br />
dosering. Enkelt att<br />
identifiera en dos som<br />
ger god smärtlindring<br />
Ökad risk <strong>för</strong> infektioner,<br />
kräver övervakning och<br />
är besvärlig i hemmiljö<br />
Enkelt och väl tolererat,<br />
patientvänligt utan behov<br />
av övervakning<br />
Långsamt upptag, därmed<br />
risk <strong>för</strong> dålig följsamhet till<br />
smärt<strong>för</strong>loppet<br />
Enkelt och väl tolererat,<br />
patientvänligt utan behov av<br />
övervakning<br />
Risk <strong>för</strong> dålig predikterbarhet av<br />
dosen, när delar av substansen<br />
sväljs (Actiq/Fentora)<br />
Enkel att administrera<br />
Kan inte användas av<br />
patienter med nedsatt<br />
andnings<strong>för</strong>måga<br />
Bara 25 procent av dosen<br />
<strong>för</strong> Actiq tas snabbt upp<br />
via munslemhinnan<br />
Actiq <strong>för</strong>sta produkten på marknaden<br />
Fentanylbaserade läkemedel är idag det mest utbredda andrahandsalternativ<br />
vid genombrottssmärta efter morfin och oxykodon. Under år 1998<br />
blev Actiq som <strong>för</strong>sta fentanylbaserade läkemedel godkänt <strong>för</strong> behandling<br />
av genombrottssmärta vid cancer. Actiq är en klubba med fentanyl som<br />
gnuggas mot kindens insida <strong>för</strong> upptag av den aktiva substansen genom<br />
munslemhinnan, så kallad bukal till<strong>för</strong>sel. Studier med produkten visar på<br />
att smärtlindring uppnås inom 15 minuter. Upptag via munslemhinnan är<br />
en attraktiv väg <strong>för</strong> att snabbt få substansen till blodbanan. Nackdelen med<br />
Actiq är att bara omkring 25 procent av dosen tas upp via munslemhinnan,<br />
resten sväljs och tas långsamt upp i mag-tarmkanalen. Det ger en <strong>för</strong>dröjd<br />
och <strong>för</strong>längd smärtlindring. Det är även svårt att <strong>för</strong>utsäga dosen, vilket ger<br />
svårigheter i att titrera rätt dos till patienten. Produkter där en högre andel<br />
av aktiv substans tas upp i munslemhinnan kan där<strong>för</strong> ge snabbare smärtlindring,<br />
bättre <strong>för</strong>utsägbarhet och <strong>för</strong>enkla titrering <strong>för</strong> optimal dos. Actiq<br />
har rönt framgångar i marknaden med en topp<strong>för</strong>säljning nära 600 miljoner<br />
dollar under år 2006, vilket ökat intresset <strong>för</strong> området. Värt att poängtera<br />
var att merparten av <strong>för</strong>säljning var utan<strong>för</strong> indikationen genombrottssmärta.<br />
Nya produkter har lanserats och är under utveckling, vilket<br />
presenteras i tabell nedan.<br />
Produkter genombrottssmärta vid cancer<br />
Produkt Abstral Actiq Fentora Instanyl INS-05-001 Onsolis Pecfent<br />
Bolag Orexo Cephalon Cephalon Nycomed<br />
Insys<br />
Therapeutics<br />
Biodelivery<br />
Sciences<br />
Archimedes<br />
Pharma<br />
Partner Prostrakan Eget Eget Eget Saknar Meda Saknar<br />
Insättande effekt 10min 15min 15min 10min 5min 15min 5min<br />
Administration Sublingual Bukal Bukal Intranasal Intranasal Bukal Intranasal<br />
Status: EU Marknad Marknad Marknad Marknad Inga planer Reg. Reg.<br />
USA Reg. Marknad Marknad Inga planer Fas III Marknad Reg.<br />
Japan Reg. Reg. Inga planer Inga planer Inga planer Inga planer Inga planer<br />
Källa: <strong>Redeye</strong> Research, se även appendix sid 58<br />
Bolagsanalys<br />
27
Orexo<br />
I tabellen sidan innan har vi sammanställt de snabbverkande fentanylbaserade<br />
läkemedel vi känner till är i sen utveckling eller redan finns på<br />
marknaden. Det handlar främst om produkter med bättre biotillgänglighet<br />
och som ger ett snabbare insättande effekt än Actiq.<br />
Fentora är en efterföljare<br />
till Actiq<br />
Nya produkter utmanar<br />
Fentora lanserades år 2006 och är en brustablett som fästs på insidan av<br />
den övre delen av kindhålan. Studier visar på att smärtlindring uppnås<br />
inom 15 minuter. För Fentora tas omkring 50 procent av substansen upp<br />
via munslemhinnan och därmed en bättre kontroll över doseringen. Dock<br />
kräver även Fentora likt Actiq rikligt med saliv <strong>för</strong> att tablett ska lösas upp,<br />
vilket är ett problem <strong>för</strong> patienter med muntorrhet där vätska behövs <strong>för</strong> att<br />
fukta munslemhinnan innan intag. Muntorrhet är vanligt <strong>för</strong>ekommande<br />
<strong>för</strong> patienter med cancer med en <strong>för</strong>ekomst på cirka 75 procent, en biverkning<br />
som exempelvis är <strong>för</strong>knippad med morfinbehandling. Onsolis är en<br />
tunn självupplösande disk som sätts mot kinden, även den med upptag via<br />
munslemhinnan. Till skillnad mot Fentora krävs bara lite saliv <strong>för</strong> upplösning<br />
som sker inom 15-30 minuter. Studier med Onsolis visar på en smärtlindrande<br />
effekt uppnås inom 15 minuter. Även Abstral tas upp via munslemhinnan<br />
men tillskillnad mot ovanstående placeras tabletten under<br />
tungan där den snabbt sönderfaller och tas upp via de ytliga blodkärlen<br />
utan behov av så mycket saliv.<br />
Smärtlindring <strong>för</strong> Abstral jäm<strong>för</strong>t med placebo<br />
Källa: Rauck, R., Current Medical Research & Opinion, 2009<br />
Abstral snabbast av lakemedel<br />
som tas upp via<br />
munslemhinnan<br />
Bilden ovan visar på den snabbt insättande smärtlindrande effekt på<br />
omkring 10 minuter som Orexo tillsammans med partners visat i studie. De<br />
främsta <strong>för</strong>delarna med Abstral jäm<strong>för</strong>t med konkurrerande produkter med<br />
bukal administrering är dess snabbt insättande effekt. Abstrals snabba<br />
sönderfall ger även en mindre risk <strong>för</strong> slemhinneirritation, vilket är vanligt<br />
vid användning av Actiq och Fentora. Därtill krävs mindre saliv.<br />
Intranasala produkter är snabba<br />
Administrering av fentanyl intranasalt ger en snabbt insättande effekt.<br />
Studier som genom<strong>för</strong>ts med produkter under utveckling visar på att smärtlindring<br />
med intranasla produkter kan uppnås efter 5-10 minuter. Den<br />
Bolagsanalys<br />
28
Orexo<br />
Intranasala produkter, en<br />
ökad risk <strong>för</strong> andningsdepression<br />
snabba insättande effekten som kan uppnås med intranasala fentanylbaserade<br />
läkemedel har lockat ett antal bolag att utveckla produkter inom<br />
området. I Europa är Instanyl godkänt som i studier visat ge smärtlindring<br />
efter 10 minuter och en andra produkt, Pecfent, är under registrering både<br />
i Europa och USA. Användning av opioider som tas via luftvägarna är dock<br />
<strong>för</strong>enat med en ökad risk <strong>för</strong> andningsdepression. Det betyder att den<br />
avslappnande effekt som opioider har påverkar andningsfunktionen till den<br />
grad att patienten slutar att andas och kan dö. Dessutom är det svårt att<br />
administrera en <strong>för</strong>utsägbar dos, då stora mängder av läkemedlet kan<br />
fastna i munnen och svalget. Där<strong>för</strong> finns en skepsis till intranasala<br />
opioider, vilket bland annat yttrat sig i att flera projekt lämnats tillbaka från<br />
tidigare <strong>för</strong>hoppningsfulla partners eller lagts ned på grund av ovan<br />
nämnda problem.<br />
Oral administration <strong>för</strong>edras<br />
I en europeisk studie på 400 patienter med genombrottssmärta undersöktes<br />
bland annat patienters preferenser mellan olika administrationssätt.<br />
Resultatet visar att oraladministration <strong>för</strong>edrogs fram<strong>för</strong> produkter administrerade<br />
subkutan, intranasal eller inhalerat, se tabell nedan.<br />
Patienters vilja <strong>för</strong> användning av olika administrationssätt<br />
160<br />
Endast 5 procent negativa<br />
till oraladministration<br />
140<br />
147<br />
130<br />
120<br />
112 112<br />
Number of patients (n = 200)<br />
100<br />
80<br />
60<br />
50<br />
57<br />
40<br />
42<br />
38<br />
31<br />
43<br />
27<br />
20<br />
11<br />
0<br />
Oraltransmucosal route Intranasal route Intrapulmonary route Subcutaneous route<br />
Yes Possibly No<br />
Källa: European Survey of Breakthrough Cancer Pain<br />
Hälsoekonomisk påverkan<br />
Smärta i samband med cancer ger patienten en extra börda som påverkar<br />
personens livskvalité. Patienten påverkas fysiskt, psykiskt och socialt av<br />
cancersmärta och det finns tydliga samband till exempelvis depression,<br />
sömnproblem och ångest. I samband med genombrottssmärta <strong>för</strong>värras<br />
situationen ytterligare givet de sämre <strong>för</strong>utsättningarna att lyckas nå bra<br />
kontroll av smärtan med de läkemedel som idag erbjuds. Undersökningar<br />
som genom<strong>för</strong>ts på patienter med genombrottssmärta visar att inte bara<br />
livskvalitén blir lidande utan även att dessa patienter med<strong>för</strong> betydligt<br />
Bolagsanalys<br />
29
Orexo<br />
högre kostnader <strong>för</strong> samhället och individen. Fler och längre sjukhusbesök,<br />
jäm<strong>för</strong>t med patienter med god smärtkontroll. För att öka betalningsviljan i<br />
sjukvårdssystem krävs där<strong>för</strong> fler studier på denna patientgrupp genom<strong>för</strong>s<br />
och att underlagt <strong>för</strong>stärks. Bästa sättet att öka acceptansen <strong>för</strong> att gå ifrån<br />
dagens billiga morfin till de något dyrare läkemedlen är att visa att dessa<br />
inte bara ger effektiv smärtlindring utan även är kostnadseffektiva.<br />
DEA lättade på regelverket<br />
under år 2007<br />
Narkotikaklassning ett visst hinder<br />
Opioider är beroendeframkallande och klassas som narkotika, vilket<br />
innebär att <strong>för</strong>skrivningen är restriktivare drivet av rädsla <strong>för</strong> missbruk och<br />
<strong>för</strong> att motverka illegal handel. I och med klassning som narkotika hanteras<br />
registrering av recept av Drug Enforcement Agency (DEA) och användare<br />
kan inte återanvända recept <strong>för</strong> påfyllnad. En viss attityd<strong>för</strong>ändring har<br />
dock skett under de senaste åren när det gäller rädslan <strong>för</strong> beroende vid<br />
behandling av smärta, vilket lett till ett ökat användande av opioider. Som<br />
ett led i detta antog DEA i december 2007 en ny reglering som gör det<br />
möjligt <strong>för</strong> läkare att skriva ut recept på narkotikaklassade smärtstillande<br />
preparat <strong>för</strong> 90 dagars behandling mot tidigare 30 dagar.<br />
Utbildning krävs <strong>för</strong><br />
bättre vård av patienter<br />
med genombrottssmärta<br />
Det är inte bara hos myndigheter det finns osäkerhet. Det är även vanligt<br />
<strong>för</strong>ekommande att cancerpatienter känner oro <strong>för</strong> att använda starka<br />
opioider, då en utbredd skepsis finns att risken är stor att utveckla tolerans<br />
och beroende. Dessutom är biverkningsprofilen <strong>för</strong> opioider något som<br />
oroar och hämmar användningen. Vad gäller toleransutveckling och<br />
beroende har studier inte visat att detta är ett signifikant problem vid<br />
smärtbehandling vid cancer. Det finns där<strong>för</strong> ett stort behov av att utbilda<br />
patienter om smärtbehandling med opioider <strong>för</strong> att <strong>för</strong>bättra vården av<br />
dessa patienter.<br />
Onkologer viktigast att bearbeta<br />
Datamonitors undersökning och den europeiska EPIC-studien indikerar att<br />
det fram<strong>för</strong>allt är onkologen som beslutar om att inleda smärtbehandling,<br />
se figur nedan.<br />
Ansvariga att inleda smärtmedicinering<br />
Onkolog<br />
Onkolog<br />
Primärvårdsläkare<br />
Neurolog<br />
Narkosläkare<br />
Sjuksköterska<br />
Hematolog<br />
Invärtesmedicin<br />
Primärvårdsläkare<br />
Doktor<br />
Kirurg<br />
Hematolog<br />
Smärtspecialist<br />
Övriga<br />
Källa: Datamonitor och European Pain in Cancer Survey<br />
Bolagsanalys<br />
30
Orexo<br />
Första patientkontakt är<br />
onkologen<br />
Att det är onkologen som inleder den smärtlindrande behandlingen är<br />
logiskt mot bakgrund av deras roll i att behandla den grundläggande<br />
sjukdomen. Onkologers specialistkunskaper är dock främst relaterad till<br />
behandling av tumören och inte smärtlindring. Dessutom är inledningsvis<br />
fokus riktat på att få kontroll av den kroniska smärtan. Det är dock viktigt<br />
att kunskapen där smärtbehandling inleds även är god om läkemedel mot<br />
genombrottssmärta, inte minst <strong>för</strong> att utbilda patienten. Denna grupp utgör<br />
där<strong>för</strong> en av de viktigaste att initialt bearbeta och utbilda om nya behandlingsalternativ<br />
<strong>för</strong> aktörer inom området.<br />
Undersökningar visar att den japanska marknaden skiljer sig något i detta<br />
avseende där det är vanligare med att smärtbehandling inleds och hanteras<br />
av en specialist inom smärta. Detta kan <strong>för</strong>enkla att etablera ett nytt läkemedel<br />
vid en lansering på denna marknad, då denna grupp får anses mer<br />
tillgänglig <strong>för</strong> nya smärtprodukter.<br />
Marknaden <strong>för</strong> genombrottssmärta<br />
är potentiellt<br />
mycket stor<br />
Patientunderlaget visar på stor potential<br />
Genombrottssmärta är visserligen bara en nischindikation inom det stora<br />
behandlingsområdet smärta, där prognoser från exempelvis Datamonitor<br />
indikerar en relativt begränsad affärspotential. Dagens marknad är dock<br />
kraftigt underutvecklad med nuvarande läkemedel. Det finns flera faktorer<br />
som samverkar till det, däribland priset <strong>för</strong> nya läkemedel men även anses<br />
det finnas brister i den grundläggande läkarutbildningen inom smärta. För<br />
att tydliggöra den potentiella marknadsstorleken har vi i tabellen nedan<br />
sammanställt en beräkning utifrån epidemiologiska undersökningar inom<br />
området.<br />
Tabell genombrottssmärta<br />
USA EU Japan<br />
Patienter med cancer 5 214 277 6 630 000 1 561 233<br />
varav med smärta 3 587 423 3 712 800 889 903<br />
andel (%) 69% 56% 57%<br />
varav med genombrottssmärta 1 973 080 2 339 060 462 750<br />
andel (%) 55% 63% 52%<br />
Patienter som får behandling mot<br />
genombrottssmärta 1 617 930 1 660 730 421 100<br />
andel (%) 82% 71% 91%<br />
Patienter som får behandling men<br />
når inte smärtkontroll 582 450 531 430 117 900<br />
andel (%) 36% 32% 28%<br />
Antal genombrottsepisoder per år *<br />
totalt 532 731 600 631 546 200 124 942 500<br />
varav behandlade 436 841 100 448 397 100 113 697 000<br />
varav patienter i behov av bättre<br />
läkemedel 157 261 500 143 486 100 31 833 000<br />
Källa: <strong>Redeye</strong> Research, Globocan 2002, Datamonitor, European Pain in Cancer<br />
Survey och diverse artiklar<br />
* baserat på 3 episoder per dag och en genomsnittlig period på 90 dagar<br />
Bolagsanalys<br />
31
Orexo<br />
Baserat på ovanstående beräkningar sker det totalt 1.290 miljoner genombrottsattacker<br />
årligen på utvalda marknader. En approximativ beräkning av<br />
marknaden baserat på det genomsnittliga priset i Europa indikeras en<br />
marknadspotential på totalt 10 miljarder dollar årligen. Patienter med<br />
genombrottssmärta som inte uppnår god kontroll av sina smärtepisoder<br />
med dagens standardbehandling beräknas till 330 miljoner episoder per år.<br />
Bara denna del av marknaden beräknas enligt ovanstående metod en potential<br />
som uppgår 2,5 miljarder dollar årligen. Beräkningen bygger på generella<br />
antaganden om pris och en dos per attack.<br />
Genombrottssmärta är en<br />
nischindikation och<br />
uppgår till cirka 700<br />
miljoner dollar<br />
Liten marknad inom ett stort område<br />
Den totala <strong>för</strong>säljningen av läkemedel inriktade mot smärta uppgick under<br />
år 2008 till 25,4 miljarder dollar på de sju största marknaderna enligt<br />
Datamonitor (Frankrike, Italien, Japan, Spanien, Storbritannien, Tyskland<br />
och USA). Inom det stora smärtområdet är dock genombrottssmärta enbart<br />
en nischindikation, där <strong>för</strong>säljning av snabb- och kortverkande opioider<br />
dominerar. Försäljningen av snabb- och kortverkande opioider uppgick<br />
enligt samma analys<strong>för</strong>etag till 771 miljoner dollar under år 2007 på de sju<br />
största marknaderna. Inom indikationen finns viss generika <strong>för</strong>säljning<br />
som håller tillbaka <strong>för</strong>säljningen, men nya produkter och aktörer <strong>för</strong>väntas<br />
ligga till grund <strong>för</strong> en stadig tillväxt där marknaden dubblas till år 2018 då<br />
<strong>för</strong>säljningen <strong>för</strong>väntas uppgå till 1,7 miljarder dollar, se graf nedan.<br />
Försäljningsprognoser <strong>för</strong> snabbverkande opioider 2008-18<br />
1 800 000<br />
1 600 000<br />
1 400 000<br />
1 200 000<br />
1 000 000<br />
800 000<br />
600 000<br />
400 000<br />
200 000<br />
0<br />
2008 2009p 2010p 2011p 2012p 2013p 2014p 2015p 2016p 2017p 2018p<br />
USA Japan 5EU<br />
Källa: Datamonitor, Opioids, 2009<br />
Cephalon är det bolag<br />
som idag dominerar<br />
Marknaden <strong>för</strong> snabbverkande opioider är visserligen begränsad till storlek,<br />
men det är en marknad med få och relativt små- till medelstora aktörer som<br />
är aktiva. Fram till årsskiftet dominerades området i princip helt av en<br />
aktör, Cephalon och bolagets två produkter Actiq och Fentora. Sedan<br />
patentet <strong>för</strong> Actiq i USA löpte ut finns viss konkurrens från generikatillverkarna<br />
Watson och Teva (tidigare Barr). Det råder dock i princip ingen<br />
prisskillnad i dagsläget mellan Actiq generika och Fentora.<br />
Bolagsanalys<br />
32
Orexo<br />
Nya aktörer kommer leda<br />
till tillväxt<br />
Två tredjedelar av<br />
marknaden finns i USA<br />
Patentet <strong>för</strong> Fentora<br />
gäller till år 2019<br />
Genombrottssmärta – En marknad med potential<br />
Marknadsområdet <strong>för</strong> genombrottssmärta står in<strong>för</strong> tillväxt under de<br />
närmaste åren drivet av nya produktformuleringar av snabbverkande<br />
fentanyl läkemedel av flera nya aktörer som träder in på marknaden. Vi<br />
räknar med att detta kommer leda till en högre marknadspenetration <strong>för</strong><br />
snabbverkande fentanylbaserade läkemedel framöver tillsammans med en<br />
fortsatt tillväxt av patienter till följd av en åldrande befolkning. Marknaden<br />
<strong>för</strong>väntas fortsätta domineras av små och medelstora aktörer med varierande<br />
konkurrens mellan olika marknader beroende på styrka hos lokala<br />
aktörer. En dålig kännedom och kunskap av genombrottssmärta vid cancer<br />
är ett av huvudproblemen till den låga marknadspenetrationen idag <strong>för</strong><br />
snabbverkande fentanyl läkemedel. Fler aktiva bolag inom <strong>för</strong>säljning och<br />
marknads<strong>för</strong>ing kommer vara gynnsamt <strong>för</strong> att utveckla marknaden.<br />
Abstral anser vi är globalt välpositionerat med dedikerade partners på alla<br />
de stora marknaderna.<br />
Den amerikanska marknaden viktigast<br />
För opioider är den amerikanska marknaden den i särklass mest utvecklade<br />
och står <strong>för</strong> drygt två tredjedelar av den globala <strong>för</strong>säljningen (se bild sidan<br />
innan). Den europeiska marknaden utgör i nuläget ungefär 20 procent av<br />
världsmarknaden. Till skillnad från andra läkemedelsområden är den<br />
amerikanska marknaden inte premium prissatt utan dess dominans<br />
kommer från att <strong>för</strong>säljningsvolymerna även är högst. Under år 2007<br />
utgjorde den amerikanska marknaden 78 procent av de globala volymerna,<br />
enligt IMS Health. Andra marknader där Abstral är i registreringsprocess är<br />
den japanska och kanadensiska marknaden där fast-track <strong>för</strong> ansökan<br />
erållits. På den japanska marknaden saknas godkända läkemedel, vilket är<br />
en <strong>för</strong>klaring till att den i nuläget bara utgör 3 procent av världsmarknaden.<br />
I Kanada är ännu bara Onsolis den produkt som blivit godkänd <strong>för</strong><br />
behandling av genombrottssmärta vid cancer.<br />
Cephalon behåller greppet om USA….<br />
Sedan lanseringen av Actiq har Cephalon byggt upp sin position inom<br />
genombrottssmärta på den amerikanska marknaden, vilket har varit<br />
huvudmarknaden <strong>för</strong> bolaget. Även efter att patentet löpte ut <strong>för</strong> Actiq<br />
bolaget lyckats behålla sin ledande position, även om <strong>för</strong>säljningen av<br />
generika vunnit mark. Cephalon har lyckats behålla greppet genom<br />
lanseringen av Fentora som vi bedömer har <strong>för</strong>utsättningar att fortsätta<br />
vara den ledande produkten på den amerikanska marknaden under sin<br />
livslängd, patentet löper ut år 2019. Vi baserar det på att Fentora är ett<br />
etablerat varumärke och att Cephalon har en väl fungerande <strong>för</strong>säljningsorganisation.<br />
Lutar vi oss på den <strong>för</strong>säljningsutveckling vi sett i Europa är<br />
det <strong>för</strong>st och främst <strong>för</strong>säljning av Actiq som tappar marknadsandelar till<br />
Abstral.<br />
…men Abstral är en god utmanare till tronen<br />
Vi <strong>för</strong>väntar oss att Meda kommer göra ett bra jobb med Onsolis på den<br />
amerikanska marknaden, men <strong>för</strong>säljningen hämmas i nuläget av ett<br />
Bolagsanalys<br />
33
Orexo<br />
Vi räknar med att Abstral<br />
och Onsolis tar kamp om<br />
andra platsen i USA<br />
trasligt REMS-progam (se sidan 38). I vår värderingsmodell utgår vi ifrån<br />
att Abstral och Onsolis når en marknadsandel på vardera 15 procent. Meda<br />
uppfattar vi ännu är något starkare än Prostrakan på den amerikanska<br />
marknaden samtidigt som Prostrakan är mer beroende av framgångar<br />
Abstral, vilket talar <strong>för</strong> en kraftfull satsning. Baserat på 15 procents<br />
marknadsandel räknar vi med att en <strong>för</strong>säljningstopp på 160 miljoner dollar<br />
uppnås år 2016 på den amerikanska marknaden, se figur nedan.<br />
Försäljningsprognoser Abstral i USA, 2010-17<br />
180<br />
160<br />
140<br />
120<br />
Försäljning (MUSD)<br />
100<br />
80<br />
60<br />
40<br />
20<br />
0<br />
2010p 2011p 2012p 2013p 2014p 2015p 2016p 2017p<br />
Källa: <strong>Redeye</strong> Research<br />
Den europeiska marknaden<br />
är liten och underutvecklad<br />
Europa har haft låg prioriterat av Cephalon<br />
Det är viktigt att ha klart <strong>för</strong> sig att marknaden <strong>för</strong> snabbverkande opioider<br />
till och med år 2008 i Europa i princip enbart byggts av Cephalon och<br />
<strong>för</strong>säljning av produkten Actiq. Cephalon har dessutom haft huvudfokus på<br />
den amerikanska hemmamarknaden och prisat ut Actiq, vilket är en av<br />
anledningarna till att den Europeiska marknaden är underutvecklad.<br />
Många nya bolag står in<strong>för</strong> lansering i Europa, med ökad marknads<strong>för</strong>ing<br />
räknar vi med ökad kännedom och en hög tillväxt närmaste åren.<br />
Bra tillväxt i Europa efter lansering<br />
Nyligen presenterade Prostrakan <strong>för</strong>säljningssiffror <strong>för</strong> Abstral <strong>för</strong> årets<br />
fyra <strong>för</strong>sta månader. Försäljningen uppvisar stark tillväxt och uppgick till<br />
5,0 miljoner pund, cirka 56 miljoner kronor. Motorn <strong>för</strong> tillväxten finns i att<br />
Abstral lanserats på nya marknader, en ökad underliggande tillväxt <strong>för</strong><br />
snabbverkande fentanylbaserad produkter och bra marknadsandelar.<br />
Försäljningssiffrorna <strong>för</strong> jan-april <strong>för</strong> i år visar att Abstral hade marknadsandel<br />
i Frankrike på 27 procent, Spanien på 10 procent, Storbritannien på<br />
21 procent, Sverige på 69 procent och i Tyskland på 20 procent.<br />
Bolagsanalys<br />
34
Orexo<br />
Marknadsandel Abstral på sjukhus i Storbritannien<br />
Källa: IMS Health<br />
Utvecklingen i Storbritannien och <strong>för</strong>säljningen till sjukhus visas i grafen<br />
ovan och baseras på siffror från IMS Health, där det tydligt visas att Abstral<br />
tar marknad från Actiq sedan lansering. Samtidigt har <strong>för</strong>säljningen av<br />
exempelvis Effentora och Instanyl inte på samma sätt dragit <strong>för</strong>del av en<br />
sjunkande andel <strong>för</strong> Actiq. Försäljningsunderlaget gäller en kort period och<br />
en liten del av marknaden, var<strong>för</strong> det kan ifrågasättas om några långtgående<br />
slutsatser om preferenser kan dras utifrån detta. Underlaget styrks<br />
dock av liknande trender från fler europeiska marknader, som exempelvis<br />
den svenska där Abstral har en stark position, se graf nedan.<br />
Starka siffror i Sverige<br />
Marknadsandel Abstral på den svenska marknaden<br />
Källa: IMS Health<br />
Precis som i Storbrittanninen har Abstral vunnit marknad från Actiq, vilket<br />
även Instanyl uppvisat i Sverige. I mars hade Abstral en mycket stark<br />
position med en marknadsandel på nästa 70 procent.<br />
Hög tillväxt <strong>för</strong> läkemedel<br />
mot genombrottssmärta<br />
Försäljningen av Abstral på den europeiska marknaden har inte bara<br />
gynnats av att produkten tar marknadsandelar. I den <strong>för</strong>säljningsstatisk<br />
som nyligen presenterades av Prostrakan redovisades även en hög tillväxt<br />
generellt <strong>för</strong> fentanylbaserade produkter mot genombrottssmärta vid<br />
cancer. På kvartalsbasis har den europeiska marknaden vuxit med 45<br />
Bolagsanalys<br />
35
Orexo<br />
procent jäm<strong>för</strong>t med samma period i fjol. Under denna period har Abstral<br />
haft en tillväxt med 61 procent. I grafen nedan kan vi se exempel på ökad<br />
efterfrågan på den svenska marknaden.<br />
Antal sålda tabletter i Sverige (veckovis)<br />
Källa: IMS Health<br />
Potential <strong>för</strong> Abstral att<br />
bli marknadsledande i<br />
Europa<br />
Prostrakan kopplar grepp om Europa<br />
Vi anser att det finns mycket som talar <strong>för</strong> en stark marknadsposition på<br />
den europeiska marknaden <strong>för</strong> Abstral. Det är Prostrakans huvudmarknad<br />
där bolaget har en utbyggd och fungerande marknadsorganisation.<br />
Cephalon har visserligen en längre historik i Europa, men är bara aktiva i<br />
ett fåtal länder och fokus på andra produkter. Den <strong>för</strong>säljningsstatistik som<br />
publicerats senaste året visar tydligt att Abstral har etablerats med en stark<br />
position på flera marknader. När väl Onsolis når marknaden räknar vi med<br />
tuff konkurrens från Meda som satsar stort på att växa i Europa inom<br />
cancervård och har även med andra produkter som exempelvis Ceplene<br />
(akut myeloisk leukemi). Vi räknar med att Onsolis blir godkänt i Europa<br />
under det andra halvåret i år och lansering sker kring årsskiftet 2010/11.<br />
Prostrakan och Cephalon har ett <strong>för</strong>språng med längre tid på marknaden<br />
som talar till deras <strong>för</strong>del. I vår modell räknar vi med att Abstral har en<br />
marknadsandel i Europa på 20 procent och når en <strong>för</strong>säljningstopp på 85<br />
miljoner dollar år 2015 i Europa, se figur nedan.<br />
Försäljningsprognoser Abstral i Europa, 2010-17<br />
90<br />
80<br />
Försäljning (MUSD)<br />
70<br />
60<br />
50<br />
40<br />
30<br />
20<br />
10<br />
0<br />
2010p 2011p 2012p 2013p 2014p 2015p 2016p 2017p<br />
Källa: <strong>Redeye</strong> Research<br />
Bolagsanalys<br />
36
Orexo<br />
Abstral (KW-2246) kan bli<br />
<strong>för</strong>sta produkten på den<br />
japanska marknaden<br />
Vi räknar med en hög<br />
marknadsandel i Japan<br />
Okrattad mark i Japan<br />
Den japanska marknaden saknar i dagsläget godkända snabbverkande<br />
fentanybaseradel läkemedel. Actiq är i registreringsprocess sedan år 2008<br />
då partnern Mitsubishi Tanabe lämnade in en registreringsansökan, vad<br />
som hänt därefter känner vi inte till och inga besked har tillkännagetts. I<br />
början av året lämnade Orexos partner Kyowa Hakko Kirin in en ansökan<br />
till myndigheterna <strong>för</strong> ett marknadsgodkännande, vi räknar med besked<br />
<strong>för</strong>sta halvåret 2011. Konkurrenssituationen talar <strong>för</strong> att KW-2246 (Abstral)<br />
blir den <strong>för</strong>sta produkten att bli godkänt mot genombrottssmärta på den<br />
japanska marknaden. För att dra <strong>för</strong>delar från denna möjlighet tecknades<br />
ett distributionsavtal med det japanska läkemedelsbolaget Hisamitsu<br />
Pharmaceutical Co. i samband med att den regulatoriska ansökan lämnades<br />
in. Hisamitsu är ett läkemedelsbolag med rötter inom smärtområdet och<br />
<strong>för</strong>stärker Kyowas <strong>för</strong>säljningskanaler vid en lansering.<br />
Ensamma på tronen i Japan<br />
I vår modell räknar vi med att KW-2246 (Abstral) blir godkänt nästa år och<br />
lanseras under det andra halvåret. Trots att denna typ av produkter tidigare<br />
inte marknads<strong>för</strong>ts i Japan visar undersökningar att det finns en utbredd<br />
kännedom om snabbverkande opioider, vilket kan underlätta vid lansering.<br />
Det är rimligt att konkurrenter gör entré och då fram<strong>för</strong>allt Actiq. Då vi inte<br />
känner till några andra aktörer som är på väg mot den japanska marknaden<br />
räknar vi med en begränsad konkurrenssituation. Starka marknadspartners<br />
och <strong>för</strong>del att vara tidig på marknaden talar <strong>för</strong> att en hög marknadsandel<br />
kommer kunna uppnås. I vår värderingsmodell utgår vi ifrån att KW-2246<br />
blir marknadsledande med en marknadsandel på 40 procent, vilket ger en<br />
<strong>för</strong>säljningstopp på 60 miljoner dollar år 2016.<br />
Försäljningsprognoser Abstral i Japan, 2010-17<br />
70<br />
60<br />
Försäljning (MUSD)<br />
50<br />
40<br />
30<br />
20<br />
10<br />
0<br />
2010p 2011p 2012p 2013p 2014p 2015p 2016p 2017p<br />
Källa: <strong>Redeye</strong> Research<br />
Stor potential men svårigheter tornar upp sig<br />
Något som haft en negativ inverkan på <strong>för</strong>säljningen på den amerikanska<br />
marknaden har varit de skärpta myndighetskraven <strong>för</strong> kraftigt smärtstillande<br />
läkemedel, vilket begränsat <strong>för</strong>eskrivningen av dessa läkemedel<br />
Bolagsanalys<br />
37
Orexo<br />
Tuffare regelverk och<br />
dödsfall med Fentora har<br />
pressat <strong>för</strong>säljningen<br />
utan<strong>för</strong> godkänd indikation. Något som tidigare utgjort en betydande del av<br />
<strong>för</strong>säljningen <strong>för</strong> Actiq. Även det faktum att det <strong>för</strong>ekommit dödsfall med<br />
Fentora <strong>för</strong> patienter som använt produkten <strong>för</strong> andra indikationer har haft<br />
en negativ påverkan på <strong>för</strong>säljningen, se figur nedan. Cephalon blev i samband<br />
händelserna under år 2007 tvungna att publicera varningsinformation<br />
som <strong>för</strong>tydligade att Actiq inte var utbytbar med Fentora och vikten av<br />
<strong>för</strong>eskrivning till rätt patienter och med rätt dosering av läkemedlet.<br />
Kvartals<strong>för</strong>säljning Actiq, Fentora och Actiq generika (MUSD)<br />
70<br />
60<br />
50<br />
40<br />
30<br />
20<br />
10<br />
0<br />
Q1 07Q2 07Q3 07Q4 07Q1 08Q2 08Q3 08Q4 08Q1 09Q2 09Q3 09Q4 09Q1 10<br />
Actiq Fentora Generic OTFC<br />
Källa: Cephalon<br />
Skärpta regler i USA <strong>för</strong><br />
snabbverkande fentanylbaserade<br />
produkter<br />
REMS ett potentiellt hinder<br />
Under de senaste decennierna visar statistik på ett ökat användande av<br />
narkotikaklassade preparat, däribland starkt smärtstillande läkemedel.<br />
Detta har lett fram till ett skärpt regelverket kring kraftigt smärtstillande<br />
läkemedel, där en registreringsansökan <strong>för</strong> nya produkter numera inte bara<br />
innehåller omfattande klinisk dokumentation utan även ett så kallat REMSprogram<br />
(Risk Evaluation and Mitigation Strategy). Regelverket gäller<br />
kraftigt smärtstillande läkemedel baserat på substanser som fentanyl,<br />
hydromorfon, metadon, morfin, oxykodon och oxymorfon. Avsikten är att<br />
undvika att dessa läkemedel hamnar i orätta händer, där myndigheten<br />
menar att felaktig hantering, missbruk och överdosering ökat senaste<br />
decenniet trots ett antal steg <strong>för</strong> att hantera problemen. För att komma åt<br />
problemet kräver FDA att REMS ska inkludera omfattande processer kring<br />
hantering och utbildning rörande läkemedlet efter ett godkännande. Exakt<br />
hur ett REMS-program ska vara utformat finns inga klara riktlinjer kring i<br />
nuläget.<br />
Speciellt <strong>för</strong> Onsolis<br />
Av de hittills godkända snabbverkande fentanyl läkemedlen på den<br />
amerikanska marknaden är det bara Onsolis som godkänts med ett REMSprogram<br />
kallat FOCUS (Full Ongoing Commitment to User Safety), vilket<br />
skapat en ojämnlik marknadssituation. Både Actiq och Fentora godkändes<br />
innan <strong>för</strong>ändringen och har ännu inget program som blivit godkänt. Process<br />
Bolagsanalys<br />
38
Orexo<br />
pågår dock och besked väntas under sommaren i år <strong>för</strong> Fentora. För<br />
Fentora är processen i mångt och mycket även kopplad till Cephalons<br />
ambitioner att bredda indikationen utan<strong>för</strong> cancer, vilket ännu varit<br />
fruktlöst. Actiq och Fentora är godkända efter det tidigare regelverket, så<br />
kallade RiskMAP, vilket inte är lika restriktivt kring patienthantering.<br />
Nedan följer de viktigaste punkterna <strong>för</strong> Onsolis FOCUS-program.<br />
Svårt att nå patienten med<br />
Medas FOCUS-program<br />
• Varje patient, recept<strong>för</strong>eskrivare, distributör och apotek måste<br />
inkluderas i FOCUS-programmet<br />
• Recept<strong>för</strong>eskrivare faxar receptet <strong>för</strong> Onsolis till FOCUSprogrammet<br />
<strong>för</strong> att påbörja verifieringsprocessen<br />
• Recept<strong>för</strong>eskrivare sänder originalreceptet <strong>för</strong> Onsolis till FOCUSinkluderat<br />
apotek via bud/post som även är godkänt<br />
• Under processen att receptet skickas till apoteket konfirmerar det<br />
att patienten är inkluderad i programmet och <strong>för</strong>bereder det<br />
<strong>för</strong>eskrivna receptet<br />
• När originalreceptet når apoteket kan läkemedlet översändas till<br />
patienten direkt eller via ett godkänt bud<br />
Hanteringen är tidskrävande speciellt eftersom det enbart får hanteras av<br />
utvalda apotek, var<strong>för</strong> mycket tid går åt att skicka recept och produkter<br />
mellan läkare, apotek och patient. Det är faktorer som <strong>för</strong>svårat <strong>för</strong>säljning,<br />
vilket är den främsta <strong>för</strong>klaringen bakom besvikelsen i <strong>för</strong>säljningen så här<br />
långt på den amerikanska marknaden <strong>för</strong> Onsolis. Det är vår uppfattning att<br />
de REMS-program som Cephalon och Prostrakan vill få godkända blir mer<br />
lättillgängliga <strong>för</strong> patienten. De indikationer vi fått är att programmen<br />
sannolikt kommer bli snarlika i dess utformning. En harmonisering är<br />
nödvändig <strong>för</strong> att marknadskonkurrensen inte ska bli snedvriden och det är<br />
där<strong>för</strong> rimligt att även programmet <strong>för</strong> Onsolis <strong>för</strong>ändras om dessa<br />
program blir accepterade.<br />
REMS hämmar<br />
utvecklingen i USA<br />
Vi räknar med att REMS hämmar marknadstillväxten på den amerikanska<br />
marknaden och att <strong>för</strong>säljningstillväxten vid lanseringen av Abstral där<strong>för</strong><br />
blir flackare än vad tidigare produkter som Actiq och Fentora uppvisat.<br />
Osäkerheten kring effekterna från REMS är sannolikt även en <strong>för</strong>klaring till<br />
att få nya produkter är under utveckling. Det finns dock ett positivt inslag<br />
<strong>för</strong> aktörer inom området och det är att <strong>för</strong>säljningen av generika <strong>för</strong>svåras<br />
av regelverket, då det innebär kostsamma eftermarknadsaktiviteter.<br />
Bolagsanalys<br />
39
Orexo<br />
OX17 - Rätt partner men när?<br />
Licensavtal med Novartis<br />
tecknat i fjol<br />
OX17 är ett kombinationsläkemedel som utvecklats av Orexo <strong>för</strong> att snabbt<br />
och varaktigt hämma magsyra produktionen <strong>för</strong> patienter med gastroesofageal<br />
refluxsjukdom (GERD). Under fjolåret tecknades ett licensavtal<br />
med Novartis Consumer Health <strong>för</strong> produkten, vars ambitioner är att<br />
<strong>för</strong>länga produktlivscykel <strong>för</strong> bolagets receptfria läkemedel Prevacid 24HR<br />
(lanzoprazole). Ett läkemedel som sedan i fjol finns tillgängligt som receptfritt<br />
läkemedel på den amerikanska marknaden. Unikt <strong>för</strong> Prevacid 24HR<br />
är att detta är <strong>för</strong>sta receptfria syrahämmaren som får säljas i full terapeutisk<br />
dos. Under fjolåret löpte patent ut <strong>för</strong> det recept<strong>för</strong>eskrivna Prevacid,<br />
<strong>för</strong> den receptfria versionen har Novartis ytterligare tre års patentexklusivitet<br />
till november år 2012. OX17 är en kombinationstablett med H2-<br />
receptorblockerare och protonpumpshämmare (PPI). Det är två välkända<br />
substanser som används vid GERD. Fördelen med en kombinationstablett<br />
av substanserna är att läkemedlet får en snabbt insättande effekt likt H2-<br />
receptor blockerare samt en varaktig effekt resten av dygnet från PPI, se<br />
illustration nedan.<br />
Terapeutisk effekt OX17, H2-receptorblockerare och PPI<br />
Källa: Orexo<br />
OX17 en potentiell efterföljare<br />
till Prevacid 24HR<br />
Partner på plats<br />
Efter flera års <strong>för</strong>handlingar kring projektet tecknade Orexo i fjol ett globalt<br />
exklusivt licensavtal <strong>för</strong> OX17-programmet med läkemedelsbolaget<br />
Novartis, sannolikt Novartis Consumer Health. Novartis är i många<br />
avseenden en perfekt partner <strong>för</strong> OX17-programmet med sin styrka inom<br />
receptfria läkemedel. Bolaget har även en produkt i marknaden <strong>för</strong> GERD<br />
då de år 2005 licensierade de receptfria rättigheterna till Tap Pharmaceuticals<br />
(numera Takeda) storsäljande PPI, Prevacid. En produkt OX17 kan<br />
komma ersätta när patentet löper ut år 2012. Utöver det har Novartis<br />
poängterat att bolaget har som ambition att växa inom konsumentläkemedel,<br />
vilket <strong>för</strong>stärktes när Joe Jimenez utsågs till ny verkställande<br />
direktör. Joe Jimenez har en bakgrund från konsumentmarknaden och är<br />
känd <strong>för</strong> sin <strong>för</strong>måga att bygga varumärken i konkurrensutsatta<br />
verksamheter.<br />
Bolagsanalys<br />
40
Orexo<br />
Stor marknad som kommer<br />
pressas av generika<br />
Marknaden<br />
Den globala marknaden <strong>för</strong> syrahämmande läkemedel uppgick under år<br />
2009 till 17,4 miljarder dollar, enligt Evaluate Pharma. Det är en nedgång<br />
med 10 procent från året innan då <strong>för</strong>säljningen uppgick till 19,3 miljarder<br />
dollar. Marknadsledande inom området är Astrazeneca med läkemedlet<br />
Nexium (esomeprazole), vars <strong>för</strong>säljning under år 2009 uppgick till 5,0<br />
miljarder dollar. Protonpumpshämmare (PPI) är de mest effektiva läkemedlen<br />
<strong>för</strong> behandling av syrarelaterade sjukdomar och dominerar<br />
marknadsområdet. Försäljningen av syrahämmande läkemedel har redan<br />
påverkats av patentutgångar och konkurrens från billiga kopior. Närmaste<br />
åren <strong>för</strong>väntas fram<strong>för</strong>allt <strong>för</strong>säljningen av PPI fortsätta pressas med ökad<br />
<strong>för</strong>säljning av generika och receptfria varumärkesprodukter. I fjol löpte<br />
patent ut <strong>för</strong> Prevacid och ytterligare patentutgångar väntar <strong>för</strong> produkter<br />
som Aciphex (rabeprazole) år 2013 och Protonix i början av år 2011 (här<br />
finns redan generika på marknaden sedan år 2007). Den stora generika<br />
konkurrens räknar vi med sätter in när det amerikanska patentet <strong>för</strong><br />
Nexium löper ut under år 2014.<br />
Marknaden sjunker till<br />
11,7 miljarder dollar år<br />
2016<br />
Prevacid 24HR har en<br />
marknadsandel på 30<br />
procent<br />
Fram till år 2016 räknar analys<strong>för</strong>etaget Globaldata att marknaden sjunker<br />
till 11,7 miljarder dollar till en följd av få nya produkter som gör entré på<br />
marknaden och en hög press från generika. Vi har identifierat 45 molekyler<br />
i klinisk fas, där knappt hälften utgörs av efterföljare till redan godkända<br />
läkemedel. Den produkt som tillskrivs de största <strong>för</strong>väntningarna är<br />
Takedas, Dexilant(dexlansoprazole), <strong>för</strong>st lanserad som Kapidex men<br />
namnändrad <strong>för</strong> att inte <strong>för</strong>växlas med Casodex. Ett dyrt misstag <strong>för</strong> Takeda<br />
som fått se <strong>för</strong>säljningen av Dexilant rasa. Besvärande då lanseringen av<br />
produkten dess<strong>för</strong>innan gått helt enligt regelboken <strong>för</strong> att bygga vidare på<br />
styrkan från <strong>för</strong>säljningen av Prevacid och få patienter att övergå till den<br />
nya produkten. Dexilant är enantiom av lansoprazole, likt Nexium som är<br />
det till Losec.<br />
Den receptfria marknaden är målet<br />
För samhället finns stora ekonomiska <strong>för</strong>delar med ökad användning av<br />
receptfria läkemedel, vilka reducerar kostnader <strong>för</strong> läkemedel. Dessutom<br />
det faktum att patienter inte behöver recept och därmed minskar läkartid<br />
ger betydande besparingar. För Novartis är målet <strong>för</strong> OX17 den konkurrensutsatta<br />
receptfria marknaden. Främsta konkurrent är Prilosec (omeprazole)<br />
som marknads<strong>för</strong> som varumärke av Procter & Gamble, men vi räknar med<br />
att alla varumärken där patenten löper ut kommer växlas till receptfri<br />
<strong>för</strong>säljning. Prilosec <strong>för</strong>säljningen under år 2008 uppgick till cirka 290<br />
miljoner dollar, en nedgång med 25 procent på årsbasis. Den receptfria<br />
<strong>för</strong>säljningen av Prilosec utgör ett bra jäm<strong>för</strong>elseobjekt som visar på<br />
potentialen inom konsumentmarknaden.<br />
Novartis rapporterar att Prevacid 24HR tagit cirka 30 procent av marknaden<br />
sedan lansering i november i fjol, cirka 300 miljoner dollar. Novartis<br />
har kommunicerat att målet med Prevacid 24HR är att nå en <strong>för</strong>säljning på<br />
500 miljoner dollar årligen. Priset <strong>för</strong> 14-dagar Prevacid är satt till 11,99<br />
Bolagsanalys<br />
41
Orexo<br />
dollar, Prilosec receptfritt kostar 10,40 dollar <strong>för</strong> 14-dagar och generika<br />
kostar 8,39 dollar. Vi räknar med att OX17 kommer prissättas något högre<br />
vid en lansering eftersom det handlar om en kombinationsprodukt.<br />
Avtalsvillkoren ett osäkerhetsmoment<br />
När avtalet tecknades under fjolåret var Orexo <strong>för</strong>hindrade att kommentera<br />
de finansiella villkoren. Klart är att Orexo inte fått någon kontantersättning<br />
i samband med att avtalet tecknandes. Det skapar frågor om hur pass<br />
dedikerade Novartis är att utveckla projektet hela vägen till marknaden.<br />
Givetvis finns logiken <strong>för</strong> Novartis med att utveckla ett läkemedel som ska<br />
ersätta Prevacid 24HR vid patentutgång, men marknaden är skeptisk och<br />
vill se start av studier.<br />
Milstolpsbetalning utgår<br />
när OX17 går in i fas III<br />
60 miljoner individer i<br />
USA leder av sura<br />
uppstötningar<br />
Novartis ska finansiera vidareutvecklingen och kommersialiseringen av<br />
OX17, där Orexo får ersättningar vid <strong>för</strong>bestämda utvecklings- och<br />
kommersiella mål samt royalty på <strong>för</strong>säljning. För att få en uppfattning om<br />
storleken på avtalet med Novartis, trots den bristfälliga informationen<br />
tillgänglig, använder vi avtalet mellan Santarus och Schering-Plough som<br />
referens. Det tecknades i slutet av 2006 och avsåg de receptfria<br />
rättigheterna till Zegerid <strong>för</strong> USA och Kanada. Zegerid är en snabbverkande<br />
PPI med natriumkarbonat. Avtalet innehöll en kontantersättning på 15<br />
miljoner dollar och 65 miljoner dollar i milstolpsbetalningar baserat på<br />
utvecklings- och <strong>för</strong>säljningsmål. Det är dock ett globalt avtal som Orexo<br />
tecknat med Novartis, var<strong>för</strong> det kan handla om bättre villkor. Vad gäller<br />
royalty gör vi bedömningen att Orexo kommer få en stigande royalty som<br />
spänner mellan 12-15 procent. Det bolaget har kommunicerat är att en<br />
milstolpsbetalning utfaller när <strong>för</strong>sta patient doseras i fas III, vi uppskattar<br />
storleken till 15 miljoner dollar.<br />
Utbredd sjukdom<br />
Diagnosen GERD innebär att maginnehållet stöts upp i matstrupen, med<br />
åtföljande besvärliga symtom och/eller komplikationer. Hörnsten <strong>för</strong><br />
behandling av GERD är PPI, men det är åtskilliga patienter som trots PPIbehandling<br />
fortsätter att besväras av ihållande symtom. Forskning och<br />
utveckling <strong>för</strong> att komma tillrätta med orsakerna bakom GERD är<br />
nödvändig <strong>för</strong> att hitta nya behandlingsalternativ, så att även denna grupp<br />
kan få sina medicinska behov tillgodosedda. I USA beräknas 44 procent av<br />
den vuxna populationen minst en gång i månaden drabbas av sura<br />
uppstötningar, cirka 60 miljoner individer.<br />
Kliniska resultat<br />
I slutet av mars 2008 presenterade Orexo resultat från en klinisk studie<br />
med OX17 där 59 GERD-patienter behandlades under 14 dagar. Den<br />
kontrollerade studien jäm<strong>för</strong>de den syrahämmande effekten av OX17 med<br />
de aktiva substanserna omeprazol och famotidin separat. Studiens primära<br />
målsättning uppfylldes där OX17 reducerade syrasekretionen mer jäm<strong>för</strong>t<br />
med omeprazol dag 1. Tiden med ett pH-värde över pH 4 under de <strong>för</strong>sta 12<br />
timmarna efter dosering var i medeltal 60 procent längre med OX17 jäm<strong>för</strong>t<br />
Bolagsanalys<br />
42
Orexo<br />
med omeprazol (p
Orexo<br />
Försäljningsprognoser OX17, 2010-17<br />
450<br />
400<br />
Försäljning (MUSD)<br />
350<br />
300<br />
250<br />
200<br />
150<br />
100<br />
50<br />
0<br />
2010p 2011p 2012p 2013p 2014p 2015p 2016p 2017p<br />
Källa: <strong>Redeye</strong> Research<br />
Bolagsanalys<br />
44
Orexo<br />
Edluar - dåligt differentierad<br />
Edluar ger en snabbt<br />
insättande effekt<br />
Mer än 70 miljoner lider<br />
av sömnbesvär i västsvärlden<br />
Läkemedlet Edluar (tidigare Sublinox) är egenutvecklat av Orexo <strong>för</strong><br />
behandling av tillfälliga sömnbesvär. Edluar är en sublingual tablett som<br />
innehåller den redan godkända substansen zolpidem, vilket är den aktiva<br />
substansen i tidigare storsäljande Ambien där patent löpte ut under år<br />
2007. Genom att kombinera Orexos sublinguala tabletteknologi med<br />
zolpidem kan en snabbt insättande effekt uppnås. I kliniska studier har<br />
Orexo visat på mer än ett 30 procent snabbare tillslag utan <strong>för</strong>ändra<br />
sömntiden under natten och en likvärdig biverkningsprofil med Ambien.<br />
Sömnbesvär ett växande problem<br />
Sömnbesvär är ett växande folkhälsoproblem, där omkring en tredjedel av<br />
befolkningen i hela västvärlden uppger att de tillfälligt drabbas av lättare<br />
sömnbesvär. Förekomsten ökar med åldern och är vanligare bland kvinnor.<br />
En annan utveckling som konstaterats är att sömnbesvär kryper allt längre<br />
och längre ned i åldrarna. Dålig sömn orsakar mycket arbetsfrånvaro och<br />
ökar risken <strong>för</strong> hjärt- kärlsjukdomar. Sömnbesvär är ett stort samhällsproblem<br />
med stora sociala och ekonomiska effekter anses behandling av<br />
denna grupp bristfällig och ofta felbehandlad. Mer än 70 miljoner av den<br />
vuxna befolkningen lider av tillfälliga sömnbesvär i västvärlden, varav 25<br />
miljoner lider av svåra eller varaktiga (kroniska) sömnbesvär. Utav dessa<br />
använder endast omkring 20 procent receptbelagda läkemedel <strong>för</strong><br />
sömnbesvär enligt IMS Health, vilket visar på att det finns en stor<br />
marknadspotential <strong>för</strong> nya sömnmedel.<br />
Den främsta <strong>för</strong>klaringen till ett utbrett användande av alternativa sömnmedel<br />
är rädslan <strong>för</strong> beroende som konventionella sömnmedel <strong>för</strong>knippats<br />
med historiskt. Äldre generationers sömnmedel som bensodiazepiner är<br />
starkt beroendeframkallande och ger upphov till toleransutveckling med<br />
avtagande effekt som följd. Därutöver har de visat sig att sömnproblemen<br />
återkommer när man slutar med att ta sömnmedlet, så kallad reboundeffekt.<br />
Till nackdelarna <strong>för</strong> bensodiazepinerna hör också en störd dröm- och<br />
djupsömn, vilket tar sig i utryck i mardrömmar och att patienten vaknar<br />
utan att känna sig utvilad. Dessutom är effekten <strong>för</strong> långvarig i likhet med<br />
alla lugnande medel, vilket ger biverkningar av baksmälletyp; dåsighet,<br />
minnes<strong>för</strong>luster och nedsatt funktions<strong>för</strong>måga dagen efter.<br />
Dagens läkemedel bättre<br />
än sitt rykte<br />
Läkemedel på marknaden<br />
Effekten av nyare sömnmedel, så kallade bensodiazepinliknande sömnmedel,<br />
sitter inte i lika länge som de äldre bensodiazepinerna och ger där<strong>för</strong><br />
en betydligt lindrigare baksmälla. I jäm<strong>för</strong>else med bensodiazepinerna så<br />
stimulerar dessa nya sömnmedel mer specifikt GABA A-receptorerna i<br />
hjärnan (BZ1-receptorn), som gör att de har mindre negativ påverkan på<br />
sömnmönstret, lägre risk <strong>för</strong> toleransutveckling och beroende än<br />
bensodiazepiner. GABA är ett signalämne som finns naturligt i kroppen och<br />
som har en lugnande, ångestdämpande och sömngivande verkan.<br />
Bolagsanalys<br />
45
Orexo<br />
Bensodiazepinliknande sömnmedel <strong>för</strong>stärker GABA:s sömngivande och<br />
ångestdämpande effekt.<br />
De bensodiazepinliknande sömnmedlen utgör idag omkring 80 procent av<br />
den totala receptbelagda sömnmedelsanvändningen. Nyckelprodukter är<br />
Ambien (Stilnoct i Europa), den <strong>för</strong>sta bensodiazepinliknande substansen<br />
som lanserades (1988 i Europa och 1993 i USA) som numera säljs som<br />
generika sedan patenten löpt ut <strong>för</strong> originalformuleringen från Sanofi-<br />
Aventis under 2006; Sanofi-Aventis nya långtidsverkande formulering<br />
Ambien CR (controled release); Lunesta från Sepracor. Därutöver<br />
lanserades Rozarem av japanska Takeda under 2005, ett nytt sömnmedel<br />
som till skillnad från de bensodiazepinliknande sömnmedel inte påverkar<br />
GABA A-receptorkomplexet.<br />
Läkemedel <strong>för</strong> sömnbesvär<br />
uppgick år 2008 till 3,9<br />
miljarder dollar<br />
Marknaden<br />
Marknaden <strong>för</strong> läkemedel <strong>för</strong> sömnbesvär har påverkats negativt de senaste<br />
åren av patentutgången <strong>för</strong> den dess<strong>för</strong>innan storsäljande produkten<br />
Ambien. När patenten löpte ut under år 2007 introducerades billiga<br />
generikakopior som haft ett stort genomslag. Läkemedel <strong>för</strong> behandling av<br />
sömnbesvär uppgick enligt Datamonitor under år 2008 till 3,9 miljarder<br />
dollar på de sju största marknaderna i världen, se graf nedan.<br />
Försäljning läkemedel sömnbesvär 2008-18<br />
8 000 000<br />
7 000 000<br />
6 000 000<br />
5 000 000<br />
4 000 000<br />
3 000 000<br />
2 000 000<br />
1 000 000<br />
0<br />
2008 2009p 2010p 2011p 2012p 2013p 2014p 2015p 2016p 2017p<br />
Källa: Datamonitor, Insomnia, 2008<br />
70 procent av <strong>för</strong>säljningen<br />
sker i USA<br />
USA är den i särklass största enskilda marknaden och representerar drygt<br />
70 procent av den globala <strong>för</strong>säljningen. Anledningen till detta är en mer<br />
utbredd acceptans <strong>för</strong> att ta läkemedel mot sömnbesvär. Fram<strong>för</strong>allt i<br />
Europa finns ett stort motstånd där <strong>för</strong>skrivningen av rogivande naturmedel<br />
och lugnande läkemedel är mest populära. Detta trots att dessa har<br />
bristfälligt dokumenterad effekt på sömnen och ofta ger upphov till biverkningar.<br />
Marknadsledande bolag inom området är Sanofi-Aventis med sin<br />
produkt Ambien CR och Sepracor (numera Dainippon Sumitomo Pharma<br />
America) med sin produkt Lunesta. Under år 2009 uppgick <strong>för</strong>säljningen<br />
<strong>för</strong> Ambien CR-produkter till 873 miljoner dollar. För Lunesta uppgick<br />
<strong>för</strong>säljningen under år 2009 till 736 miljoner dollar.<br />
Bolagsanalys<br />
46
Få nya produkter under utveckling<br />
Orexo<br />
Marknadsundersökningar visar på att endast 20 till 30 procent av alla<br />
patienter som använder bensodiazepinliknande sömnmedel är helt nöjda<br />
med sitt nuvarande sömnmedel. Det största missnöjet är att inte kunna<br />
vakna pigg och utvilad och den dåsighet som sömnpillret kan ge på<br />
morgonen dagen efter. Det finns där<strong>för</strong> intresse i att utveckla nya bättre<br />
läkemedel som kan <strong>för</strong>bättra sömnkvalité och biverkningsprofilen.<br />
Svåra bakslag <strong>för</strong> marknadsledande<br />
Sanofi-Aventis<br />
Produkter i sen utveckling har haft det mottigt och under det senaste året<br />
har det duggat tätt med bakslag, speciellt hårt drabbat är Sanofi-Aventis<br />
som fått lägga ned två projekt i sen utvecklingsfas, eplivanserin och<br />
volinanserin. Det är två projekt där det funnits stora <strong>för</strong>väntningar i<br />
marknaden, speciellt kring eplivanserin som pekats ut som bolagets tillväxtmotor<br />
inom CNS. Bägge projekten är så kallade selektiva serotonin<br />
5HT-2A-receptorhämmare som verkar lugnande och visat på en bra biverkningsprofil<br />
i kliniska studier. FDA har dock begärt ytterligare information<br />
om läkemedlets <strong>för</strong>delar, där det sannolikt uppkommit osäkerhet kring dess<br />
säkerhetsprofil, vilket bedöms ligga bakom Sanofi-Aventis beslut.<br />
Silenor godkänt av FDA<br />
Ett annat läkemedel under utveckling är almorexant, utvecklat av Actelion<br />
och licensierat av GlaxoSmithKline, där under pågående fas III-studier<br />
vissa säkerhetsaspekter uppdagats. Almorexant är en orexin-receptorantagonist<br />
som i tidigare studier visat lovande resultat. Senfasprojekt som<br />
blivit godkänd är Somaxons Silenor, en lågdostablett av den antidepressiva<br />
substansen doxepin. Fördelen med Silenor är att den utgår ifrån en välkänd<br />
substans och är inte heller narkotikaklassat då det inte anses leda till<br />
beroende. Läkemedlet blockerar histamin H1-receptorn och erbjuder en ny<br />
behandlingsprincip <strong>för</strong> patienter med kroniska sömnbesvär. Målet är att<br />
finna en partner som tillsammans ska marknads<strong>för</strong>a produkten <strong>för</strong> den<br />
amerikanska marknaden.<br />
Låg innovationsgrad i<br />
nya produkter<br />
NovaDel har även haft framgång hos FDA med sitt läkemedel ZolpiMist,<br />
baserat på zolpidem likt Edluar. Konkurrens<strong>för</strong>delen med ZolpiMist är<br />
precis som <strong>för</strong> Edluar den snabbt insättande effekten, något som<br />
genom<strong>för</strong>da studier visat på. Användning av tabletter är mer utbrett med<br />
fler patienter välbekanta med administreringen och det är sannolikt att fler<br />
känner sig bekväma med en tablett som Edluar än en spray. Intermezzo<br />
utvecklat av Transcept Pharma, är en lågdosvariant (3,5 och 1,75 mg<br />
zolpidem) av zolpidem i registrering, positionerad mot patienter som<br />
vaknar upp mitt i natten. För att få ett godkännande med denna<br />
produktprofil kräver dock FDA att ytterligare studier genom<strong>för</strong>s som visar<br />
säkerhetsdata <strong>för</strong> eventuella dagenefter effekter.<br />
Bakslag från FDA<br />
Edluar har blivit godkänt av FDA mot tillfälliga sömnbesvär. Det är dock ett<br />
godkännande där inte dess snabbt insättande effekt inkluderats i bipacksedeln.<br />
Därmed är enda differentiering styrkt av FDA mot zolpidem<br />
Bolagsanalys<br />
47
Orexo<br />
generika dess sublinguala upptag. Beskedet var inte enbart en besvikelse i<br />
form av differentiering utan innebar även en lägre milstolpsbetalning från<br />
partnern Meda på 5 miljoner dollar. För att få inkludera den snabba<br />
insättande effekten kräver FDA att ytterligare studier genom<strong>för</strong>s som<br />
styrker tidigare resultat. En kompletterande studie skulle relativt snabbt<br />
kunna genom<strong>för</strong>as till en begränsad kostnad. Huruvida Meda avser att<br />
genom<strong>för</strong>a en sådan är dock i dagsläget oklart.<br />
Risk <strong>för</strong> trög <strong>för</strong>säljning<br />
<strong>för</strong> Edluar<br />
Försäljningsprognoser<br />
Läkemedel <strong>för</strong> sömnbesvär är en konkurrensutsatt konsument marknad.<br />
För att tjäna pengar krävs hög <strong>för</strong>säljning som byggs via ett starkt varumärke.<br />
Det krävs stora direkta marknads<strong>för</strong>ingsinsatser <strong>för</strong> att etablera nya<br />
produkter som <strong>för</strong>stahandsval. Utan volym är det svårt att tjäna pengar i<br />
denna marknad. Med ett pris i nivå med marknadsledande produkter som<br />
Ambien CR och Lunesta utan en tydlig differentiering mot generisk<br />
zolpidem anser vi att Edluar riskerar att leva en tynande tillvaro. Tillsammans<br />
med de hittills begränsade marknads<strong>för</strong>ingsinsatser är Edluar<br />
positionerad som en nischprodukt inom sömnläkemedel och vi räknar med<br />
låg marknadspenetration. Den amerikanska hälsovårdsreformen bedöms<br />
därtill missgynna en produkt som Edluar, med en ökad prispress <strong>för</strong> <strong>för</strong>säkringsbolag,<br />
med ökad press på sin lönsamhet riktas fokus till ökad<br />
användning av generika.<br />
Våra prognoser bygger på en penetration på knappt 1 procent med en<br />
<strong>för</strong>säljningstopp på 80 miljoner dollar, vilket uppnås år 2016 efter långsam<br />
tillväxt. Från <strong>för</strong>säljningen av Edluar får Orexo en stigande royalty. Räknat<br />
bakifrån av rapporterad <strong>för</strong>säljning inleds denna på 12 procent. Vi räknar<br />
med att den under gynnsamma <strong>för</strong>utsättningar kan stiga till 15 procent. Vår<br />
uppfattning är dock att det krävs att <strong>för</strong>säljningen överstiger 100 miljoner<br />
dollar <strong>för</strong> detta, något vi inte räknar med kommer inträffa. Vårt scenario ger<br />
heller inte utrymme <strong>för</strong> att några <strong>för</strong>säljningsrelaterade milstolpar kommer<br />
utbetalas, där den <strong>för</strong>sta aktiveras när <strong>för</strong>säljningen når 150 miljoner dollar.<br />
På nästa sida visas vår prognos på <strong>för</strong>säljning av Edluar till år 2015.<br />
Försäljningsprognoser Edluar, 2010-17<br />
90<br />
80<br />
Försäljning (MUSD)<br />
70<br />
60<br />
50<br />
40<br />
30<br />
20<br />
10<br />
0<br />
2010p 2011p 2012p 2013p 2014p 2015p 2016p 2017p<br />
Källa: <strong>Redeye</strong> Research<br />
Bolagsanalys<br />
48
Orexo<br />
Appendix 1 - Övriga projekt<br />
Orexo har en omfattande projektportfölj men där den kliniska aktiviteten<br />
senaste året varit låg. En orsak är att bolaget satsat befintliga resurser på de<br />
godkända produkterna Abstral och Edluar, samt att få till avtal. Därtill har<br />
bolaget omorganiserat och slimmat verksamheten <strong>för</strong> att återgå till ökat<br />
fokus på drug delivery. Kapitalanskaffningen genom konvertibeln till Novo<br />
Growth Equity och nyligen presenterat avtal med Johnson & Johnson har<br />
skapat utrymme <strong>för</strong> Orexo att lägga en grund <strong>för</strong> att utveckla verksamheten,<br />
där målet är att bli ett ledande specialty pharma-bolag med egna produkter.<br />
OX219 är bolagets nästa<br />
kliniska projekt<br />
Målet är att OX219 ska bli<br />
ett bättre läkemedel än<br />
etablerade Suboxone<br />
OX219 mot opioidberoende<br />
Vid köpet av Pharmakodex följde projektet OX219, som utvecklas <strong>för</strong> att<br />
skapa ett nytt, patentskyddat läkemedel <strong>för</strong> substitutionsbehandling vid<br />
opioidberoende, till exempel heroinmissbruk. Projektet är inriktat på att<br />
vara en uppföljare till det etablerade läkemedlet Suboxone, som marknads<strong>för</strong>s<br />
av Reckitt-Benckiser i USA och av Merck (tidigare Schering-Plough) i<br />
Europa. Försäljningen har utvecklats mycket bra och enbart den amerikanska<br />
marknaden uppgick <strong>för</strong>säljning till drygt 700 miljoner dollar i fjol.<br />
Produktskyddet med marknadsexklusivitet löpte under fjolåret ut <strong>för</strong> den<br />
amerikanska marknaden, men ännu har ingen generika produkt introducerats.<br />
I Europa finns patentskydd fram till år 2016.<br />
OX219 är en bättre produkt<br />
OX219 är en kombinationstablett baserat på de två aktiva substanserna<br />
buprenorfin och naloxon. Storheten i kombinationen ligger i buprenorfins<br />
effekt att reducera symptomen från opioid beroende och Naloxon motverkar<br />
ruseffekten som kan uppnås vid intravenöst intag av buprenorfin,<br />
vilket gör kombinationen oattraktiv att missbruka. OX219 är en sublingual<br />
tablett med en snabbt insättande effekt, enklare att administrera och där<br />
den bittra smaken <strong>för</strong>enat till ursprungsmolekylen maskerats. Orexos<br />
målsättning är att utveckla och marknads<strong>för</strong>a OX219 på egen hand, det är<br />
dock sannolikt att vissa marknader kommer licensieras efter att<br />
bioekvivalensstudier genom<strong>för</strong>ts.<br />
Framgångarna kommer från nya lag<br />
De stora <strong>för</strong>säljningsframgångarna <strong>för</strong> Suboxone på den amerikanska<br />
marknaden har delvis sitt ursprung i den nya lagstiftning inom området<br />
som president Bill Clinton lade fram år 2000, Drug Abuse Treatment Act<br />
2000. Lagen innebar att läkare gavs möjlighet att behandla patienter <strong>för</strong><br />
deras drogmissbruk på privata mindre center. Detta gällde läkemedel<br />
klassade under Controlled Substances Act, schedule III-V. Metadon som<br />
tidigare varit huvudalternativet <strong>för</strong> behandling av missbruk klassades som<br />
en schedule II-substans, med begränsning att enbart användas på större<br />
kliniker <strong>för</strong> missbrukare. Andra faktorer som haft en positiv påverkan finns<br />
i en ökad behandlingsvård av missbrukare där samhället blivit mer <strong>för</strong>stående<br />
att missbruk är ett medicinskt och inte ett resultat av social- och<br />
Bolagsanalys<br />
49
Orexo<br />
kriminellmissanpassning. Suboxone är ett effektivt läkemedel <strong>för</strong><br />
behandling av missbruk, som exempelvis heroin. Läkemedlet är svårt att<br />
missbruka och överdosera, då det gör patient sjuk och mår dåligt. Andra<br />
<strong>för</strong>delar med Suboxone är att metadonbehandling kan pågå i flera år,<br />
jäm<strong>för</strong>t med behandling med Suboxone begränsas till två år.<br />
Svårt <strong>för</strong> Orexo att få<br />
särläkemedelsstatus <strong>för</strong><br />
OX219<br />
Lansering möjlig redan<br />
under år 2012<br />
Ännu ingen generika på<br />
marknaden trots patentet<br />
löpt ut<br />
Särläkemedelsstatus gav acceptans <strong>för</strong> högt pris<br />
Reckitt-Benckiser har varit mycket framgångsrika i sin strategi med<br />
Suboxone och lyckats få läkemedlet särläkemedelsklassad trots skilda<br />
uppfattningar med FDA angående storleken på patientpopulation. Anledningen<br />
till att Suboxone de skilda fick särläkemedelsstatus var att FDA<br />
ansåg att produkten hade en begränsad marknadspotential. Med särläkemedelsklassning<br />
har det funnits en hög acceptans till ett högt pris, där en<br />
månads behandling kostar omkring 400-500 dollar. Vi tror dock att det blir<br />
svårt <strong>för</strong> Orexo att få särläkemedelsstatus <strong>för</strong> OX219, givet framgångarna<br />
med Suboxone och den skillnad i uppfattning som finns hos FDA angående<br />
patientpopulationen, vilka menar att storleken egentligen ligger på mellan<br />
1,0-1,5 miljoner individer. Globalt uppskattas att omkring 6 miljoner<br />
människor missbruka opioider, varav cirka 3 miljoner i Europa och USA.<br />
Ungefär hälften av dessa utgörs av illegala droger, som exempelvis heroin.<br />
Av dessa behandlas omkring 750.000 personer globalt <strong>för</strong> deras missbruk.<br />
Utvecklingsplan<br />
För att nå ett marknadsgodkännande på den amerikanska marknaden <strong>för</strong><br />
OX219 räknar vi inte med att några omfattande studier behöver genom<strong>för</strong>as.<br />
Orexo ska kunna registrera OX219 som ett 505(b)(2)-läkemedel,<br />
vilket möjliggör mindre studier <strong>för</strong> att visa att OX219 har en jäm<strong>för</strong>bar<br />
biotillgänglighet med Suboxone, vilket enbart kräver en bioekvivalensstudie.<br />
Vid en 505(b)(2) registrering kan bolaget tillgodogöra sig resultat<br />
från andras studier <strong>för</strong> den aktiva substansen. Trots det är en 505(b)(2)<br />
registrering inte samma sak som generika registrering, utan exempelvis<br />
produkter utvecklade med en annan formulering. Vi räknar med att Orexo<br />
påbörjar studier under det andra halvåret och att dessa kan slut<strong>för</strong>as inom<br />
loppet av 6-9 månader, vilket möjliggör att produkten når marknaden slutet<br />
av år 2012.<br />
Ingen generika trots patentutgång<br />
Patentet <strong>för</strong> Suboxone har gått ut <strong>för</strong> den amerikanska marknaden, dock<br />
har ännu ingen generika dykt upp. Eftersom marknaden får betraktas som<br />
relativt stor är det trots allt sannolikt att generika kommer introduceras på<br />
den amerikanska marknaden. När så sker <strong>för</strong>väntas en kraftig nedgång i<br />
marknaden med den prispress som följer. Vi räknar med att Orexo kommer<br />
bygga en egen <strong>för</strong>säljningsorganisation <strong>för</strong> den amerikanska marknaden <strong>för</strong><br />
OX219. För den europeiska marknaden är det oklart hur Orexo ska positionera<br />
OX219, men en möjlighet även här är att bygga en egen organisation.<br />
Alternativet är att söka ett partnerskap, där aktörer inom området som<br />
exempelvis Lundbeck och Merck kan tänkas utgöra bra partners.<br />
Bolagsanalys<br />
50
Orexo<br />
Viktigt avtal äntligen i<br />
hamn<br />
Bra avtalsvillkor med<br />
otippad partner<br />
OX-AAF (Arachidonic Acid Franchise)<br />
Vid <strong>för</strong>värvet av Biolipox följde ett antal projekt och däribland två prekliniska<br />
projekt inom astma och KOL (Kronisk Obstruktiv Lungsjukdom), OX-<br />
CLI och OX-ESI. Efter flera år av partnerdiskussioner har Orexo nyligen<br />
tecknat ett av sina största samarbets- och licensavtal någonsin. Det är ett<br />
globalt licensavtal med Ortho-McNeil-Jansen Pharmaceuticals och Jansen<br />
Pharmaceutica NV (bolag inom Johnson & Johnson koncernen). Utöver de<br />
två egna innovativa projekten ingår ett tredje projekt från licenstagarna<br />
riktat mot ett icke tillkännagett målprotein. Målet med samarbetet är att<br />
upptäcka och utveckla nya småmolekylära läkemedel mot luftvägssjukdomar<br />
och andra inflammatoriska sjukdomar. Den prekliniska utvecklingen<br />
kommer ske hos Orexo men är fullt finansierade genom forskningsstöd<br />
under tre år framåt av J&J som totalt uppgår till 11,5 miljoner dollar<br />
(89 miljoner kronor), dessutom betalades 10 miljoner dollar i kontantersättning<br />
vid tecknandet. Når samtliga tre projekt marknaden kan Orexo få<br />
sammanlagt 564 miljoner dollar i forskningsstöd och utvecklingsrelaterade<br />
milstolpsersättningar. Därtill finns potential till ytterligare <strong>för</strong>säljningsrelaterade<br />
milstolpsbetalningar på uppemot 500 miljoner dollar samt<br />
royalty från <strong>för</strong>säljning, vilken vi bedömer är en stegrande royalty på 8-12<br />
procent. Orexo har även rätten att tillsammans med partners marknads<strong>för</strong>a<br />
produkter från samarbetet <strong>för</strong> de nordiska och baltiska marknaderna.<br />
Johnson & Johnson var inte vår huvudmisstänkte partner till projekten, då<br />
bolagets närvaro inom behandlingsområdet i nuläget är begränsat. Däremot<br />
noterar vi att de har en tydlig ambition att växa inom området, vilket<br />
tydliggörs av bolagets projekt i preklinisk och klinisk utvecklingsfas.<br />
Bolag Indikations- Utvecklingsfas Avtalsvärde Ingångs- Tidpunkt<br />
område<br />
betalning<br />
Galapagos / Roche KOL Upptäcksfas 573 MUSD 9 MUSD Jan 2010<br />
Synta / Roche Astma / KOL Upptäcktsfas 415 MUSD 25 MUSD Jan 2009<br />
Actimis / Boehringer Ingelheim Astma Fas I 515 MUSD Okänt Juni 2008<br />
Amira / GlaxoSmithKline Astma / KOL Fas I 425 MUSD Okänt Feb 2008<br />
Kyowa Hakko Kirin / Amgen Astma Fas I 520 MUSD 100 MUSD Mars 2008<br />
Argenta / Astrazeneca Astma / KOL Preklinisk fas 500 MUSD 21 MUSD Jan 2007<br />
Dynavax / Astrazeneca Astma / KOL Upptäcktsfas 136 MUSD 10 MUSD Sept 2006<br />
Källa: <strong>Redeye</strong> Research<br />
Tabellen ovan är en sammanställning av licensavtal som vi anser utgör bra<br />
jäm<strong>för</strong>elseobjekt till avtalet. Det som gör avtalet särskilt starkt mot ovanstående<br />
är att det enbart inkluderade milstolpsbetalningar fram till en<br />
kommersialisering, men innehåller inga <strong>för</strong>säljningsrelaterade ersättningar,<br />
som tillkommer med royalty. Dessutom behålls projekten internt under den<br />
prekliniska fasen, men finansierade via forskningsstöd. Det ger Orexo god<br />
kontroll på utvecklingen och innebär att kompetens kan behållas, dessutom<br />
är avtalet en validering på forskning och synliggör värden från Biolipox.<br />
Bolagsanalys<br />
51
Orexo<br />
OX-CLI utmanar Singulair<br />
OX-CLI är ett projekt där målet är att utveckla ett oralt administrerat<br />
läkemedel <strong>för</strong> behandling av astma och KOL. Läkemedlet är icke-steroidbaserat<br />
med både luftrörsvidgande och antiinflammatoriska egenskaper.<br />
OX-CLI riktar sig mot målproteinet Leukotrien C4-syntas, vilket har en<br />
central roll i den inflammatoriska processen och katalyserar i slutsteget i<br />
bildningen av leukotriener och eoxiner, två grupper proinflammatoriska<br />
mediatorer. En patentportfölj har byggts upp baserat på flera molekylserier<br />
med potentiella läkemedelskandidater. Projektet är i preklinisk fas och har i<br />
djurmodeller visat på lovande resultat <strong>för</strong> luftvägssjukdomar. OX-CLI har<br />
potential att visa en bättre terapeutisk effekt än leukotrienhämmare som<br />
exempelvis det etablerade läkemedlet Singulair, med en <strong>för</strong>säljning under<br />
fjolåret på 4,7 miljarder dollar, se tabell nästa sida.<br />
Verkningssätt <strong>för</strong> OX-CLI<br />
Källa: Orexo<br />
OX-ESI är grunden till<br />
Biolipox<br />
OX-ESI utgjorde en av hörnstenarna kring Biolipox som Orexo <strong>för</strong>värvade<br />
hösten år 2007. Det var upptäckten av en ny grupp mediatorer, eoxiner,<br />
som bildas från arakidonsyra fram<strong>för</strong>allt i luftvägarnas celler, vanligt hos<br />
rökare, patienter med kronisk bronkit eller med astma. Vid allergi eller<br />
astma frigörs inflammatoriska mediatorer som producerar eoxiner som<br />
med sina kraftfulla proinflammatoriska egenskaper kan utgöra ett viktigt<br />
bidrag till inflammationen som uppkommer vid astma och KOL. För<br />
programmet OX-ESI hoppas bolaget kunna utveckla helt nya oralt<br />
administrerbara läkemedel mot astma, KOL och andra inflammatoriska<br />
sjukdomar. Bolaget har utvecklat molekylserier och byggt en patentportfölj<br />
med läkemedelskandidater. För att få fram ett effektivt och säkert<br />
läkemedel pågår utvärdering kring biologisk effekt och andra egenskaper.<br />
Bolagsanalys<br />
52
Orexo<br />
Stor marknad som vätas<br />
växa<br />
En marknad på drygt 20 miljarder dollar<br />
Försäljningen av läkemedel inriktade mot luftvägssjukdomar är ett av de<br />
allra största läkemedelsområdena med <strong>för</strong>säljning på omkring 30 miljarder<br />
dollar under 2009 (Källa: Evaluate Pharma). Området domineras av de två<br />
indikationerna astma och KOL, som noterade en <strong>för</strong>säljning under år 2008<br />
(Källa: Datamonitor) uppgick till cirka 24 miljarder dollar. Den största<br />
marknaden är den amerikanska som står <strong>för</strong> drygt 60 procent av den<br />
globala <strong>för</strong>säljningen följt av Europa med en andel på omkring 30 procent<br />
av <strong>för</strong>säljningen. Området domineras av ett antal stora läkemedelsbolag där<br />
de fem största representerar omkring 75 procent av marknaden. Det största<br />
läkemedelsbolaget inom området är GlaxoSmithKline följt av Merck,<br />
Astrazeneca och Boehringer Ingelheim.<br />
Astma och KOL är två utbredda folksjukdomar med miljoner patienter som<br />
regelbundet är i behov av läkemedel <strong>för</strong> att kunna leva ett drägligt liv. Trots<br />
vissa skillnader i den underliggande sjukdomen mellan astma och KOL<br />
behandlas patienterna med samma läkemedel. Behandlingen utgår från<br />
luftrörsvidgande läkemedel och inhalerade steroider. Luftrörsvidgande<br />
läkemedel gör att musklerna i luftrören slappnar av och det blir lättare att<br />
andas. Inhalerade steroider används <strong>för</strong> att minska inflammationen som<br />
uppkommer och minskar irritation och slembildning. Försäljningsmässigt<br />
är det kombinationsläkemedel av bägge dessa läkemedelsklasser som säljer<br />
bäst, med storsäljare som Advair och Symbicort. I tabellen nedan listas de<br />
<strong>för</strong>säljningsmässigt fem främsta läkemedlen inom området under år 2009.<br />
Ledande läkemedel inom astma och KOL<br />
Läkemedel Tillverkare Läkemedels- Försäljning Patentklass<br />
2009 (MUSD) utgång<br />
Advair/Seretide GlaxoSimthKline LABA/ICS 8,0 2011*<br />
Singulair Merck Leukotrienblockerare 4,7 2012<br />
Boehringer Antikolinergika<br />
Spiriva<br />
Ingelheim (LAMA) 3,4 >2012<br />
Symbicort Astrazeneca LABA/ICS 2,3 2012<br />
Pulmicort Astrazeneca Steroid 1,3 2009<br />
Källa: Bolagsinformation och Evaluate Pharma<br />
*Patent inhalationsutrustning<br />
Kol allt viktigare del av<br />
marknaden <strong>för</strong> luftvägssjukdomar<br />
Marknaden växer till 29 miljarder dollar år 2018<br />
Under den kommande tioårsperioden <strong>för</strong>väntas marknaden <strong>för</strong> läkemedel<br />
mot astma och KOL växa till 29 miljarder dollar år 2018 (Källa:<br />
Datamonitor). Bakom detta finns många nya produkter under utvecklig<br />
som väntas täppa bortfallet då flera av dagens mest sålda läkemedel inom<br />
kategorin under perioden år 2012 till 2015 kommer tappa patentskydd och<br />
utsättas <strong>för</strong> konkurrens från generika. Huvudspåret <strong>för</strong> läkemedelsbolagen<br />
Bolagsanalys<br />
53
Orexo<br />
när det gäller framtida behandlingar mot luftvägssjukdomar är läkemedel<br />
mot KOL, där det finns ett stort behov av nya och effektivare läkemedel. Det<br />
finns flera faktorer som talar <strong>för</strong> en högre tillväxt inom KOL-området än<br />
andra luftvägssjukdomar såsom <strong>för</strong>bättrad <strong>för</strong>ståelse <strong>för</strong> sjukdomen, en<br />
åldrande befolkning och ökad användning av läkemedel. Vi ser stor<br />
potential i projekten men inkluderar ännu bara kontantersättningen och<br />
forskningsstödet i våra prognoser i vår DCF-modell.<br />
Lovande projekt utan<br />
framsteg under flera år<br />
OX-MPI mot smärta och inflammation<br />
Projektets avsikt är att ta fram en selektiv prostaglandin-hämmare <strong>för</strong><br />
smärta, inflammation och ledgångsreumatism. Målet är att utveckla ett nytt<br />
effektivt läkemedel mot smärta, inflammation och feber med färre<br />
biverkningar än existerande läkemedel som de klassiska NSAIDs (t.ex.<br />
diklofenak) och de senare utvecklade COX-2 hämmarna (t.ex. Vioxx och<br />
Celebrex). Försäljningen av NSAIDs och COX-2 hämmare uppgick 2007 till<br />
cirka 5 miljarder dollar på de sju största marknaderna, enligt Datamonitor.<br />
Mekanismen bygger på upptäckten av ett specifikt enzym, membranbundet<br />
prostaglandin (PG) E2 syntas (mPGES), en kroppsegen substans som spelar<br />
en central roll i många inflammatoriska processer. Detta enzym ansvarar<br />
<strong>för</strong> det andra steget i bildningen av PGE2 ur arakidonsyra och bildas i stora<br />
mängder i inflammerad vävnad. Förhoppningen är att läkemedel som riktar<br />
in sig på detta specifika enzym skulle kunna leda till en mer selektiv<br />
antiinflammatorisk behandling, som är minst lika effektivt som existerande<br />
läkemedel fast med färre biverkningar.<br />
Projektet drivs sedan år 2005 i samarbete med Boehringer Ingelheim<br />
GmbH, Tyskland som <strong>för</strong>värvat de globala licensrättigheterna. Orexo har<br />
behållit rättigheterna <strong>för</strong> marknaderna i de nordiska länderna och<br />
Baltikum. Avtalsvärdet uppgick till totalt 250 miljoner euro exklusive<br />
royalty, vilket vi uppskattar till 10 procent. Projektet uppges ha gjort goda<br />
framsteg och en patentportfölj av potentiella läkemedelskandidater har<br />
byggts upp och Orexo <strong>för</strong>väntar sig att projektet når en uppsatt milstolpe<br />
under innevarande år, då Boehringer Ingelheim väljer en läkemedelskandidat.<br />
Vid val av läkemedelskandidat bedömer vi att en<br />
milstolpsbetalning på 10 miljoner euro faller ut.<br />
OX-MPI har länge varit lovande, men mot bakgrund av att projektet pågått<br />
sedan år 2005 utan att en läkemedelskandidat ännu valts gör att vi känner<br />
oss mycket osäkra om dess framtid. Vi har där<strong>för</strong> valt att exkludera eventuella<br />
milstolpsbetalningar och eventuell royalty av <strong>för</strong>siktighetsskäl.<br />
Inget nytt på rinit fronten<br />
OX-NLA<br />
OX-NLA är en nässpray <strong>för</strong> behandling av allergisk och icke-allergisk rinit<br />
innehåller den aktiva beståndsdelen cetirizin som är ett av världens mest<br />
sålda läkemedel mot hösnuva. Läkemedlet är emellertid <strong>för</strong>knippat med<br />
biverkningar som till exempel dåsighet. För att undvika denna bieffekt har<br />
cetirizin i nässpray tidigare prövats av forskare, men metoden har visat sig<br />
ge andra bieffekter i form av sveda och smärta i näsan. Orexo har utvecklat<br />
Bolagsanalys<br />
54
Orexo<br />
en unik formulering med cetirizin i liposomer som administreras som en<br />
nässpray. Liposomberedningen har i genom<strong>för</strong>da kliniska studier visat sig<br />
kunna maskera de irriterande effekterna av cetirizin i näsan. Under år 2008<br />
tecknade Orexo licensavtal med läkemedelsbolaget Meda, som idag<br />
ansvarar <strong>för</strong> vidareutvecklingen av produkten.<br />
Meda är en utmärkt partner - men inget händer<br />
Meda är marknadsledande inom nasala anti-histaminer med den<br />
väletablerade produkten Astelin och numera Astepro. Samtidigt är rinit ett<br />
av Medas viktigaste terapiområden, vilket gör Meda till en utmärkt<br />
marknadspartner <strong>för</strong> OX-NLA. OX-NLA är ett av de projekt som följde med<br />
<strong>för</strong>värvet av Biolipox. Sedan avtalet med Meda skrevs <strong>för</strong> över två år sedan<br />
har ingen ny klinisk aktivitet påbörjats. Vi uppfattar att Meda har haft som<br />
mål att vidareutveckla OX-NLA till en kombinationsprodukt med steroid.<br />
En kombinationsprodukt innebär en stor potential, men vi känner oss<br />
mycket osäkra kring Medas planer <strong>för</strong> framtiden och projektet <strong>för</strong>efaller ha<br />
en låg prioritet. Givet den obefintliga kommunikationen kring projektet och<br />
osäkerheten kring den fortsatta utvecklingen har vi valt att tills vidare<br />
exkludera det i vår värderingsmodell.<br />
Bolagsanalys<br />
55
Orexo<br />
Appendix 2 - Kibion AB<br />
Stark tillväxt <strong>för</strong> Kibion<br />
Dotterbolaget Kibion bildades så sent som år 2005 med målsättningen att<br />
bli ledande inom UBT (Urea Breath Test), ett utandningstest <strong>för</strong> diagnos av<br />
bakterien Helicobacter pylori. Bakterien infekterar magsäckens slemhinna<br />
och är en avgörande faktor vid uppkomsten av magsår. Bolaget har haft en<br />
stark tillväxt och uppnådde under år 2009 omsatte Kibion 40,7 miljoner<br />
kronor, en tillväxt med hela 42 procent jäm<strong>för</strong>t med 2008 års <strong>för</strong>säljning.<br />
Sedan starten har bolaget uppvisat en snabb och stark tillväxt. Den kraftiga<br />
omsättningsökningen har dels skett organiskt samt dels genom <strong>för</strong>värv av<br />
Noster System AB under år 2006, se tabell nedan.<br />
Kvartals<strong>för</strong>säljning Kibion, 2006-10<br />
12<br />
10<br />
8<br />
Miljoner kronor<br />
6<br />
4<br />
2<br />
0<br />
Kv1<br />
2006<br />
Kv2 Kv3 Kv4 Kv1<br />
2007<br />
Kv2 Kv3 Kv4 Kv1<br />
2008<br />
Kv2 Kv3 Kv4 Kv1<br />
2009<br />
Kv2 Kv3 Kv4 Kv1<br />
2010<br />
Källa: Orexo<br />
Kibion utgör inte Orexos<br />
kärnverksamhet<br />
I och med <strong>för</strong>värvet av Noster System AB breddade Kibion bolagets geografiska<br />
positionering så väl som produktportfölj inom diagnostik genom<br />
Noster Systems utandningstest Heliprobe System. Noster System har en<br />
marknadsnärvaro i Mellanöstern, Asien och Östeuropa, medan Kibion<br />
fram<strong>för</strong> allt fanns i England och Nordeuropa. Förvärvet var viktigt <strong>för</strong> att<br />
bygga ett starkare bolag av Kibion, vilket <strong>för</strong>stärkt <strong>för</strong>utsättningarna <strong>för</strong> en<br />
framtida avknoppning eller <strong>för</strong> en industriell lösning. Försäljningen från<br />
Kibion är ännu ett viktigt tillskott <strong>för</strong> Orexo i vägen till lönsamhet. I ett<br />
längre perspektiv är det dock rimligt att bolaget avknoppas.<br />
Gastroskopi är den dominerande diagnosmetoden<br />
Cirka hälften av jordens befolkning uppskattas vara infekterade med<br />
bakterien Heliobacter pylori. Det är dock endast ett fåtal av alla infekterade<br />
som drabbas av besvär eller får magsår och söker läkarvård. Dessutom leder<br />
en infektion till en något <strong>för</strong>höjd risk <strong>för</strong> vissa former av magcancer, men<br />
inte så stor att den motiverar att behandling sätts in. Genom att<br />
diagnostisera infektionen kan magsårssjukdomen effektivt botas med hjälp<br />
Bolagsanalys<br />
56
Orexo<br />
av antibiotika. I majoriteten (>50 procent) av alla fall med dyspepsi kan<br />
ingen orsak påvisas till besvären. Patienten sägs då lida av funktionell<br />
dyspepsi, vars symptom beror på störningar i nerv- (överkänslighet) eller<br />
motorikfunktionen i matsmältningen. I de fall orsak går att fastställa<br />
handlar det om organiska <strong>för</strong>ändringar så som sår i magsäck, inflammation<br />
i matstrupen samt cancer i matstrupe eller magsäck. För att ställa rätt<br />
diagnos vid ihållande smärta i övre buken (dyspepsi) finns flera olika<br />
metoder, exempelvis gastroskopi, blodtester, av<strong>för</strong>ingstester, där gastroskopi<br />
är den dominerande diagnosmetoden . Diagnos kan även göras på<br />
vårdcentralen genom säkra och smärtfria utandningstester <strong>för</strong> en pågående<br />
Helicobacter-infektion.<br />
Utandningstester är enkla<br />
och billiga<br />
Två utandningstest av Heliobacter -infektion<br />
Utandningstest rekommenderas av Helicobacter pylori-expertgrupper i<br />
Europa som <strong>för</strong>stahandsval och det mest till<strong>för</strong>litliga icke-invasiva testet <strong>för</strong><br />
att påvisa – eller utesluta – en aktiv infektion. Till samhällsnyttan hör bland<br />
annat att utandningstest är snabbt, enkelt och dessutom betydligt billigare<br />
än gastroskopi.<br />
Diabact UBT är Orexos <strong>för</strong>sta kommersiella produkt och är ett utandningstest<br />
<strong>för</strong> att diagnostisera bakterien Heliobacter pylori. Testet baseras<br />
på Orexos patenterade teknologi <strong>för</strong> snabblösliga tabletter, vilket ger <strong>för</strong>delaktiga<br />
produktegenskaper jäm<strong>för</strong>t andra liknande utandningstest som finns<br />
på marknaden. Till dessa egenskaper hör lägre dos, <strong>för</strong>bättrad till<strong>för</strong>litlighet,<br />
<strong>för</strong>kortad testtid samt lägre kostnad. Även utandningstestet Heliprobe<br />
System är användarvänligt <strong>för</strong> såväl patienter som sjukvårdspersonal.<br />
Testresultatet är tillgängligt redan inom 15 till 20 minuter efter det att<br />
patienten svalt en ureakapsel som innehåller en ett mycket svagt radioaktivt<br />
märkt ämne (urea som innehåller kolisotopen C14) som möjliggör analys<br />
direkt i samband med själva mottagningsbesöket, till skillnad från Diabact<br />
UBT som vanligtvis måste skickas iväg <strong>för</strong> analys (2-3 dagar). Dock finns<br />
det viss rädsla eller skepticism mot användandet av ett radioaktivt ämne. Av<br />
den anledningen anser vi att de båda utandningstesten Diabact UBT och<br />
Heliprobe System kompletterar varandra.<br />
Fortsatt tillväxt, med ett<br />
hack i kurvan i år<br />
Prognoser<br />
Vi ser endast en begränsad <strong>för</strong>säljningspotential (< 10-20 miljoner dollar<br />
per år) <strong>för</strong> Kibions båda utandningstest. För att nå detta krävs dock att<br />
bolagets produkter även etableras i Nordamerika, vilket kräver att<br />
kostsamma kliniska studier genom<strong>för</strong>s <strong>för</strong> att nå ett marknadsgodkännande<br />
av FDA. Vi räknar inte med att bolaget på egen hand kommer gör det, utan<br />
är beroende av en partner som kan stå <strong>för</strong> denna kostnad. Terrängen <strong>för</strong> ett<br />
sådant partneravtal har sonderats utan framgång, var<strong>för</strong> det i nuläget framstår<br />
som ytterst osäkert och där<strong>för</strong> har <strong>för</strong>säljning <strong>för</strong> den amerikanska<br />
marknaden exkluderas i våra prognoser. Det finns en betydande potential<br />
på befintliga marknader, med ökad användning och högre penetration. Vi<br />
räknar med att Kibion kan fortsätta växa över kommande femårsperiod<br />
med omkring 10 procent årligen, <strong>för</strong> att därefter nå mognadsfas.<br />
Bolagsanalys<br />
57
Orexo<br />
Appendix 3 - Konkurrenter Abstral<br />
Marknaden <strong>för</strong> läkemedel mot genombrottssmärta har under en längre tid<br />
varit begränsad till enbart Actiq, vilket var den <strong>för</strong>sta produkten i att bli<br />
godkänd <strong>för</strong> indikationen. Vi står dock i ett läge där nya produkter lanserats<br />
och fler är på väg. I detta appendix har vi sammanställt godkända läkemedel<br />
och lovande projekt i sen utvecklingsfas inom behandlingsområdet.<br />
Patentet löpte ut under år<br />
2006<br />
Actiq (Cephalon)<br />
Redan år 1998 godkände FDA Actiq och en marknadslansering påbörjades i<br />
mars år 1999. Första lanseringen i Europa skedde i Storbritannien av Elan<br />
under år 2001, men där rättigheterna återgick till Cephalon under år 2002.<br />
Läkemedlet marknads<strong>för</strong>s idag av Cephalon i USA och Europa. Actiq är en<br />
klubba med fentanyl som gnuggas mot kindens insida <strong>för</strong> upptag av den<br />
aktiva substansen genom munslemhinnan, så kallad bukal till<strong>för</strong>sel.<br />
Produkten är godkänd <strong>för</strong> behandling av genombrottssmärta vid cancer hos<br />
patienter som redan får opioider <strong>för</strong> deras underliggande cancersmärta.<br />
Under år 2008 inlämnades en ansökan <strong>för</strong> registrering <strong>för</strong> den japanska<br />
marknaden av dess partner Mitsubishi Tanabe Pharma. Till dags dato har<br />
inget besked avseende ansökan lämnats och vi har ingen kännedom om vad<br />
som <strong>för</strong>dröjt processen <strong>för</strong> ett godkännande.<br />
Genrika finns på<br />
marknaden<br />
Patentet <strong>för</strong> den amerikanska marknaden löpte under år 2006, varefter<br />
generika versioner av produkten introducerats på den amerikanska<br />
marknaden av främst Barr Pharmaceuticals (numer Teva) och Watson. I<br />
realiteten har Watson agerat som <strong>för</strong>säljningsagent <strong>för</strong> Cephalon och Barr<br />
har tidigare saknat en egen godkänd produkt av FDA, utan sålt Actiq<br />
generika producerad av Cephalon. Denna monopolsituation som kunnat<br />
behållas tillsammans med den kraftiga prishöjningen på produkten under<br />
år 2006 av Cephalon har lett fram till att det råder liten prisskillnad mellan<br />
generika och bolagets efterföljande produkt Fentora (se nedan). Mycket<br />
talar <strong>för</strong> att situationen <strong>för</strong>ändras under innevarande år då Barr och<br />
Covidien under slutet av fjolåret fick klartecken från FDA att lansera egna<br />
generika versioner av Actiq. Även på den europeiska marknaden har<br />
patentet <strong>för</strong> Actiq löpt ut och generika introduceras.<br />
Actiq har visat vägen <strong>för</strong> nya behandlingsmöjligheter <strong>för</strong> patienter med<br />
genombrottssmärta, vilket ligger bakom att antal efterföljare som nu gör<br />
entré på marknaden. Produkten är väletablerad inom området med ett<br />
välkänt varumärke. Det finns dock goda <strong>för</strong>utsättningar <strong>för</strong> konkurrenter<br />
att överta rollen som ledandebehandlingsalternativ, då Actiq är en ganska<br />
besvärlig produkt att administrera <strong>för</strong> patienten och svårigheter i att titrera<br />
rätt dos. Omkring 25 procent av dosen tas upp via munslemhinnan men<br />
resten sväljs och tas långsamt upp i mag-tarmkanalen, vilket ger en<br />
<strong>för</strong>dröjning och <strong>för</strong>längd smärtlindring.<br />
Bolagsanalys<br />
58
Orexo<br />
Muntorrhet ett problem<br />
vid användning av<br />
Fentora<br />
Fentora (Cephalon)<br />
Under år 2006 lanserade Cephalon Fentora i ett <strong>för</strong>söka att behålla sin<br />
ledande position inom området genombrottssmärta. Produkten är sedan<br />
april 2008 även godkänd <strong>för</strong> den europeiska marknaden där Cephalon<br />
marknads<strong>för</strong> läkemedlet under namnet Effentora. Fentora är en brustablett<br />
som fästs på insidan av den övre delen av kinden. För att tablett ska lösas<br />
upp krävs saliv och <strong>för</strong> patienter med muntorrhet behöver vätska <strong>för</strong> att<br />
fukta munslemhinnan. Muntorrhet är vanligt <strong>för</strong>ekommande <strong>för</strong> patienter<br />
med cancer med en <strong>för</strong>ekomst på cirka 75 procent, en biverkning som<br />
exempelvis är <strong>för</strong>knippad med morfinbehandling. Eftersom det tar mellan<br />
14-25 minuter <strong>för</strong> tabletten att lösas upp finns risk <strong>för</strong> att ytterligare vätska<br />
behöver till<strong>för</strong>as, vilket ska ske efter 30 minuter då resterna sväljs ned med<br />
vätska. Det som är kvar av tabletten tas då istället tas upp i tarmmagkanalen.<br />
Farmakokinetiska studier där Fentora och Actiq jäm<strong>för</strong>ts visar<br />
att hastighet och graden av absorption är 30-50 procent högre <strong>för</strong> Fentora.<br />
Lansering av Fentora som ersättare till Actiq har till en viss del varit en<br />
besvikelse <strong>för</strong> Cephalon och <strong>för</strong>säljningen har inte lyckats nå de nivåer som<br />
<strong>för</strong> Actiq. Något som negativt påverkat <strong>för</strong>säljningen är den kompletterande<br />
<strong>för</strong>stärkta dos och recept<strong>för</strong>skrivningsinformation som FDA krävde under<br />
år 2007, vilket var till följd av biverkningar och dödsfall kopplade till<br />
felaktig användning. Dessutom har myndighetens generellt mer restriktiva<br />
hållning mot kraftigtsmärtstillande läkemedel senaste åren haft en negativ<br />
påverkan, med en ökad till<strong>för</strong>sikt bland läkare. Kopplat till ett tuffare<br />
regulatoriskt regelverk har möjligheterna <strong>för</strong> <strong>för</strong>säljning <strong>för</strong> andra akuta<br />
smärttillstånd <strong>för</strong>svårats, vilket utgjorde en betydande del av <strong>för</strong>säljningen<br />
<strong>för</strong> Actiq. Cephalon har mot bakgrund av det genom<strong>för</strong>t kliniska studier och<br />
därefter ansökt hos FDA <strong>för</strong> godkännande <strong>för</strong> indikationer utan<strong>för</strong> cancer.<br />
Beslut om ett REMS-program<br />
väntar under sommaren<br />
Under år 2008 efterfrågade FDA kompletterande uppgifter kring implementering<br />
av ett effektivt program <strong>för</strong> att säkerställa korrekt användning.<br />
Det nya regelverket med REMS program (se sidan 38) har satt käppar i<br />
hjulet <strong>för</strong> breddning till nya indikationer. Uppgifter från Cephalon indikerar<br />
att ett besked från FDA från de kompletteringar som skickats in till myndigheten<br />
kommer under sommaren i år. Beslut om ett REMS-program som<br />
visar sig fungera är nyckeln <strong>för</strong> att utöka till nya indikationer utan<strong>för</strong><br />
cancer.<br />
Onsolis (Meda, Biodelivery Sciences)<br />
Det amerikanska bolaget Biodelivery Sciences ligger bakom utvecklingen av<br />
Onsolis, där Meda licensierat de globala rättigheterna till produkten.<br />
Onsolis (tidigare BEMA fentanyl) är en tunn självupplösande disk som<br />
placeras på insidan av kinden. Till skillnad från Fentora krävs lite saliv <strong>för</strong><br />
upplösning, vilket sker på några minuter och disken är helt upplöst inom<br />
15-30 minuter. Läkemedlet blev i fjol godkänt på den amerikanska marknaden<br />
och lanserades i det fjärde kvartalet i fjol. Onsolis är den <strong>för</strong>sta<br />
snabbverkande fentanylbaserade produkten som säljs med ett godkänt<br />
REMS-program, vilket så här långt hämmat <strong>för</strong>säljningen. Orsak till det är<br />
Bolagsanalys<br />
59
Orexo<br />
dels en ojämn konkurrenssituation där produkter som Actiq och Fentora<br />
fortsatt kan säljas utan ett REMS-program, vilket legat bakom en som vi<br />
uppfattar det låg aktivitet från Medas sida. I mars i år godkändes Onsolis<br />
även <strong>för</strong> den kanadensiska marknaden och blev därmed <strong>för</strong>sta fentanylbaserade<br />
läkemedlet godkänt <strong>för</strong> behandling av patienter med genombrottssmärta<br />
vid cancer. På den kanadensiska marknaden har Meda ett<br />
joint venture med Valeant Pharma, vilket kommer ansvara <strong>för</strong> <strong>för</strong>säljningen<br />
och marknads<strong>för</strong>ingen. Onsolis är även under registrering i Europa, där<br />
dock processen blivit <strong>för</strong>dröjd. Vi räknar med att Onsolis godkänns i<br />
Europa under andra halvåret i år och lanseras kring årsskiftet 2010/11.<br />
Inga planer på lansering i<br />
USA <strong>för</strong> Instanyl<br />
Instanyl (Nycomed)<br />
Nycomed har utvecklat Instanyl som är en nässpray med fentanyl. Produkten<br />
blev i fjol godkänd <strong>för</strong> den europeiska marknaden. Bolaget saknar i<br />
nuläget <strong>för</strong>säljningsresurser på den amerikanska marknaden och vi har inte<br />
funnit något som tyder på att Nycomed avser att lansera Instanyl på den<br />
amerikanska marknaden. Produkten är tydligt differentierad mot Abstral,<br />
Actiq, Fentora och Onsolis med att administrera fentanyl som nässpray och<br />
upptag via luftvägarna. Fördelen med att ta upp aktiv substans i luftvägarna<br />
är att det ger en snabbare smärtlindring än upptag via munslemhinnan och<br />
snabbare ger en hög koncentration av substansen. Egenskaper som ger en<br />
bättre följsamhet till själva smärt<strong>för</strong>loppet. Andra <strong>för</strong>delar med nässpray är<br />
att produkten kan användas av illamående patienter, de med kräkning eller<br />
inflammerad munslemhinna. I studier som Nycomed genom<strong>för</strong>t med<br />
Instanyl har statistisk smärtlindring identifierats efter 10 minuter.<br />
Det är en stor utmaning <strong>för</strong> Nycomed och andra bolag med nässprayer att<br />
övertyga att produkterna erbjuder en god säkerhet <strong>för</strong> patienter och inte<br />
ökar risken <strong>för</strong> beroende och missbruk. Det senare kan vara en av anledningarna<br />
till att Nycomed inte funnit någon partner <strong>för</strong> den amerikanska<br />
marknaden där oron är som högst. Instanyl är den <strong>för</strong>sta nässpray med<br />
fentanyl som når marknaden i Europa och har där<strong>för</strong> en <strong>för</strong>del mot<br />
konkurrenter. Nycomed har varit aktiv i den inledande lanseringen och på<br />
vissa marknader fått en bra marknadsandel.<br />
Snabbaste intranasla<br />
produkten<br />
PecFent (Arvhimedes Pharma)<br />
Archimedes Pharma har likt Nycomed utvecklat en nässpray med fentanyl.<br />
Produkten är utvecklad med bolagets drug delivery-teknologi PecSys<br />
Technology. Kliniska studier har framgångsrikt genom<strong>för</strong>ts och bolaget har<br />
lämnat in registreringsansökan <strong>för</strong> produkten både i Europa och USA.<br />
Besked väntas från EMA och FDA under sommaren i år. Genom<strong>för</strong>da<br />
studier med PecFent har visat på smärtlindring redan efter 5 minuter, vilket<br />
ger en mycket god följsamhet till smärt<strong>för</strong>loppet. Archimedes har även gjort<br />
jäm<strong>för</strong>ande studier med snabbverkande morfin som visat på produktens<br />
<strong>för</strong>delar i tid till smärtlindring. Vi tror att det finns tydliga konkurrens<strong>för</strong>delar<br />
mot exempelvis Instanyl. Trots det bedömer vi att potentialen <strong>för</strong><br />
Archimedes fram<strong>för</strong>allt finns på den amerikanska marknaden där<br />
produkten har chans att vara <strong>för</strong>sta av fentanylbaserade nässprayer.<br />
Bolagsanalys<br />
60
Orexo<br />
Archimedes är ett specialty pharma-bolag med verksamhet i ett par<br />
europeiska länder. Under inledningen av året har bolagets finanser stärkts<br />
genom en nyemission som till<strong>för</strong>t bolaget 65 miljoner pund. Kapitaltillskottet<br />
ska fram<strong>för</strong>allt användas till kommersialisering av PecFent både i<br />
Europa och bygga upp en egen organisation i USA. I samband med<br />
emission blev Novo Growth Equity storägare genom att investera 40<br />
miljoner pund, även nytillkomna ägare till Orexo. Bolaget <strong>för</strong>svarar sin<br />
investering i två drug delivery-bolag inom samma behandlingsområde med<br />
att Abstral och PecFent är bästa läkemedlen i sin klass och ser dessa inte<br />
som direkta konkurrenter till varandra.<br />
Utmanare utan<br />
kommersiella resurser<br />
INS-05-001 (Insys Therapeutics)<br />
Insys Therapeutics har rapporterat lovande fas III-resultat <strong>för</strong> bolagets<br />
sublinguala sprayformulering. I nuläget saknas dock en partner och enbart<br />
en studie är rapporterad i USA. Studien visade statistsikt säkerställd<br />
smärtlindringseffekt redan efter 5 minuter, vilket är i nivå med det som<br />
uppnåtts med andra nässprayer. Innan en lansering blir aktuell räknar vi<br />
med att fler studier behöver genom<strong>för</strong>as, var<strong>för</strong> produkten är ett par år från<br />
marknaden. En registreringsansökan <strong>för</strong> den amerikanska marknaden<br />
bedömer vi tidigast kan lämnas in under nästa år. INS-05-001 är en<br />
lovande produkt men avsaknad av partners är en klar svaghet. I nuläget<br />
känner vi inte till att bolaget genom<strong>för</strong> några studier i Europa, var<strong>för</strong> vi<br />
bedömer det som osannolikt att produkten kommer att lanseras på den<br />
europeiska marknaden.<br />
Bolagsanalys<br />
61
Orexo<br />
Appendix 4 - Partners Abstral<br />
Orexo har varit mycket framgångsrika i att finna partners till Abstral och<br />
det finns idag ett kommersiellt nätverk på plats på alla de stora och<br />
betydelsefulla marknaderna. I denna del av appendix har vi sammanställt<br />
samtliga partneravtalen kring Abstral.<br />
Stark partner i Europa<br />
Abstral viktig produkt <strong>för</strong><br />
Prostrakan<br />
Prostrakan har ansvaret i EU och USA<br />
ProStrakan Group är ett Europeiskt specialty pharma-bolag noterat på<br />
Londonbörsen. Bolaget utvecklar och kommersialiserar receptbelagda<br />
läkemedel, bland annat inom onkologiområdet. Under fjolåret omsatte<br />
bolaget 79 miljoner pund, en ökning från 56 miljoner pund under år 2008.<br />
Bolaget redovisar dock fortsatt <strong>för</strong>lust som under år 2009 uppgick till -16<br />
miljoner pund. Konsensus i marknaden är att bolaget mot slutet av året når<br />
break-even <strong>för</strong> att under år 2011 uppnå ett positivt resultat. En betydande<br />
del <strong>för</strong> att uppnå ett positivt resultat är att Abstral uppvisar stark tillväxt,<br />
vilket kommer innebära att det blir bolagets främsta produkt. Huvudkontoret<br />
ligger i Skottland och vid årsskiftet anställde Prostrakan 260<br />
personer, merparten inom <strong>för</strong>säljning. Verksamheten i USA är under uppbyggnad<br />
och omsatte under fjolåret drygt 7 miljoner pund från <strong>för</strong>säljning<br />
av Sancuso (minska biverkningar vid cellgiftsbehandling). Det är en<br />
produkt med <strong>för</strong>säljningsmässiga synergier till Abstral som adresserar<br />
samma kundgrupp. På den amerikanska marknaden har Prostrakan ett<br />
samarbete med Novaquest <strong>för</strong> <strong>för</strong>säljning, vilka tillsammans i nuläget har<br />
en säljkåren på cirka 50 personer. Strategiskt riktas primärt fokus mot<br />
större sjukhus i tätorter på den amerikanska marknaden, <strong>för</strong> att fort nå så<br />
stora patientgrupper som möjligt. Vi räknar med att personalstyrkan<br />
successivt utökas när väl Abstral blir godkänt.<br />
Fördelen med en partner som Prostrakan är deras engagemang <strong>för</strong> Abstral,<br />
som är den mest betydelsefulla produkten <strong>för</strong> bolagets tillväxt. Bolagets<br />
styrka finns fram<strong>för</strong>allt på de stora europeiska marknaderna där <strong>för</strong>säljning<br />
av flera produkter har pågått i flera år. I USA är bolaget ett mer osäkert kort<br />
med en mindre säljstyrka än konkurrenten Cephalon som har omkring 100<br />
<strong>för</strong>säljare inriktade på <strong>för</strong>säljning av Actiq och Fentora. Bolagets finansiella<br />
resurser är dessutom betydligt mer svagare än <strong>för</strong> flera konkurrenter, vilket<br />
kan utgöra en begränsning.<br />
Orexo har ett bra licensavtal med Prostrakan som innebär möjlighet till<br />
ytterligare milstolpsbetalningar på 19,9 miljoner euro i Europa och 25<br />
miljoner dollar i USA. Dessa milstolpsbetalningar är kopplade till<br />
<strong>för</strong>säljningen, dels ackumulerad <strong>för</strong>säljning och dels <strong>för</strong>säljningsnivåer.<br />
Royalty från <strong>för</strong>säljning <strong>för</strong> den Europeiska marknaden spänner mellan 25-<br />
30 procent och <strong>för</strong> den amerikanska marknaden mellan 23-28 procent. Det<br />
är vår uppfattning att det inom ramen <strong>för</strong> våra prognoser är möjligt <strong>för</strong><br />
Orexo att tillgodogöra sig samtliga milstolpsbetalningar och nå upp till<br />
högsta nivån i royaltyavtalen.<br />
Bolagsanalys<br />
62
Orexo<br />
Besked inom kort <strong>för</strong> den<br />
kanadensiska marknaden<br />
Ansökan <strong>för</strong> marknadsgodkännande<br />
inlämnat<br />
<strong>för</strong> den japanska<br />
marknaden<br />
Paladin i samarbete med Prostrakan i Kanada<br />
För den kanadensiska marknaden innehar Prostrakan rättigheterna, men<br />
bolaget avser inte att bygga en egen <strong>för</strong>säljningsorganisation. Istället har<br />
Prostrakan ingått partnerskap med den lokala smärtspecialisten Paladin<br />
Labs Inc. <strong>för</strong> Abstral, vilka kommer bära ansvaret <strong>för</strong> <strong>för</strong>säljning och<br />
marknads<strong>för</strong>ing. Paladin är ett bolag med en befintlig organisation inom<br />
området som möjliggör en snabb lansering vid ett godkännande. En<br />
ansökan är inlämnad i början av året som tilldelats hög prioritet, vilket<br />
innebär att myndighetsbesked ska lämnas inom 180 dagar. Förutsättningarna<br />
<strong>för</strong> ett godkännande är goda. Vi räknar med en lansering på den<br />
kan ske i det fjärde kvartalet i år. Den kanadensiska marknaden är relativt<br />
stor, i nivå med den brittiska marknaden. Vi räknar med att Abstral har en<br />
<strong>för</strong>säljningspotential på mellan 10-20 miljoner dollar årligen med en<br />
royalty som <strong>Redeye</strong> uppskattar ligger mellan 15-20 procent. Försäljningen<br />
från den kanadensiska marknaden är inkluderade i estimaten <strong>för</strong> USA.<br />
Tidigt avtal med Kyowa Hakko Kirin<br />
På den japanska marknaden samarbetar Orexo med det japanska bolaget<br />
Kyowa Hakko Kirin, ett bolag med bland annat tillverkning och marknads<strong>för</strong>ing<br />
av medicinska produkter och läkemedel. Bolaget har särskilt<br />
kunnande inom antikroppsteknologier och inriktar sig främst mot onkologi,<br />
invärtesmedicin och immunologi. Produktportföljen innehåller över 50<br />
läkemedel. Kyowa Hakko Kirin har ca 8 000 anställda och omsatte under<br />
2008 392 miljarder YEN (cirka 34 miljarder kronor). Efter sex års utveckling<br />
har de kliniska studierna med KW-2246 (Abstral) framgångsrikt<br />
slut<strong>för</strong>ts och en ansökan om registrering av läkemedlet <strong>för</strong> den japanska<br />
marknaden har lämnats in i början av året. Vi räknar med ett myndighetsbesked<br />
under det <strong>för</strong>sta halvåret 2011, som ska ligga till grund <strong>för</strong> en<br />
lansering under det andra halvåret. För att stärka positionen på den japanska<br />
marknaden in<strong>för</strong> lansering har Kyowa Hakko Kirin nyligen tecknat<br />
ett samarbetsavtal med ett annat japanskt läkemedelsbolag, Hisamitsu<br />
Pharmaceuticals <strong>för</strong> KW-2246. Bolaget har sina rötter inom smärtområdet<br />
som är betydelsefull kunskap att addera.<br />
Avtalet med Kyowa Hakko Kirin <strong>för</strong> KW-2246 slöts i ett tidigt utvecklingsskede<br />
var<strong>för</strong> milstolpsersättningar och royalty ligger betydligt lägre än de<br />
<strong>för</strong> Prostrakan. <strong>Redeye</strong> uppskattar att royaltynivån uppgår till mellan 7-9<br />
procent. Vid regulatorisk framgång och läkemedlet blir godkänt utfaller en<br />
milstolpsersättning på 2,25 miljoner dollar.<br />
Gedeon Richter partner i Östeuropa<br />
Orexo har tecknat distributionsavtal med Gedeon Richter <strong>för</strong> den Ryska<br />
marknaden, övriga länder i det forna Sovjetunionen (CIS), Bulgarien och<br />
Rumänien. Gedeon Richter är ett ungerskt bolag grundat år 1901 och är ett<br />
av de ledande läkemedels<strong>för</strong>etagen i östra Europa. Bolaget har sedan<br />
många år en egen <strong>för</strong>säljningsstyrka i östra Europa, Ryssland och CIS.<br />
Bolagets <strong>för</strong>säljning under år 2009 uppgick till 952 miljoner euro, varav<br />
cirka 300 miljoner euro i CIS och cirka 350 miljoner euro i Polen,<br />
Bolagsanalys<br />
63
Orexo<br />
Rumänien och Ungern. Gedeon Richter är en stark partner i Östeuropa och<br />
en partner med bra resurser <strong>för</strong> att introducera Abstral <strong>för</strong> dessa relativt<br />
outvecklade marknader <strong>för</strong> genombrottssmärta vid cancer.<br />
Gedeon Richter stark<br />
partner/distributör i<br />
Östeuropa<br />
Gedeon Richter har utöver det direkta avtalet med Orexo även ett distributionsavtal<br />
<strong>för</strong> Abstral med Prostrakan <strong>för</strong> marknader som exempelvis<br />
Polen och Ungern. För Orexo är avtalet bara en del med det som tecknats<br />
med Prostrakan och ingår i deras <strong>för</strong>säljning. Gedeon Richter har påbörjat<br />
<strong>för</strong>säljning på flera marknader, däribland bolagets den ungerska hemmamarknaden.<br />
Närmaste står en lansering på den Ryska marknaden, som är<br />
störst i regionen.<br />
Avtal i Kina med Novamed Pharmaceuticals<br />
För den kinesiska marknaden finns avtal med läkemedelsbolaget Novamed<br />
Pharmaceuticals, en distributör <strong>för</strong> internationella läkemedelsbolag på den<br />
kinesiska marknaden. Bolaget bildades i augusti år 2005 och har på kort tid<br />
lyckats teckna ett antal viktiga distributions- och licensavtal <strong>för</strong> den kinesiska<br />
marknaden, med aktörer som bland annat Baxter, Pfizer och Sanofi-<br />
Aventis. Försäljning sker med en egen organisation på cirka 400 personer<br />
0och marknads<strong>för</strong> bland annat ett tiotal produkter inom onkologiområdet.<br />
Novamed uppskattar att det finns omkring 4,5 miljoner cancerpatienter i<br />
Kina, vilket gör det till det näst största indikationsområdet efter<br />
infektionssjukdomar.<br />
Den kinesiska marknaden<br />
kan överraska<br />
Novamed ansvarar <strong>för</strong> att genom<strong>för</strong>a kliniska studier med Abstral <strong>för</strong> att få<br />
produkten godkänd på den kinesiska marknaden. Orexo är berättigade till<br />
milstolpsbetalningar på 4,75 miljoner dollar, vilka utgörs av ersättning från<br />
kliniska och regulatoriska uppnådda mål. I nuläget känner vi inte till status<br />
och har svårt att bedöma potentialen <strong>för</strong> den kinesiska marknaden. Vi har<br />
där<strong>för</strong> valt att exkludera intäkter i vår värderingsmodell.<br />
Neopharm Ltd partner i Israel<br />
För den israeliska marknaden har Orexo ett distributionsavtal med<br />
Neopharm, som tecknat de exklusiva rättigheterna. Orexo kommer leverera<br />
Abstral till bolaget och få en hög marginal av <strong>för</strong>säljningsintäkterna,<br />
uppskattat till 30 procent. Dessutom är Orexo berättigade till milstolpsbetalningar.<br />
Neopharm ansvarar <strong>för</strong> processen att få Abstral godkänt på<br />
den israeliska marknaden. Bolaget är en lokal partner till flera etablerade<br />
läkemedelsbolag och är ett av Israels ledande <strong>för</strong>etag inom marknads<strong>för</strong>ing<br />
av receptbelagda läkemedel och hälso- och sjukvårdsprodukter. Neopharm<br />
ingår i Neopharm-koncernen, Israels näst största koncern inom marknads<strong>för</strong>ing<br />
på hälso- och sjukvårdsmarknaden, med en omsättning på mer än<br />
300 MUSD per år. Försäljningsintäkterna från den Israeliska marknaden är<br />
inkluderade i våra prognoser <strong>för</strong> Europa.<br />
Bolagsanalys<br />
64
Orexo<br />
Appendix 5 - Drug delivery<br />
Drug delivery viktig<br />
kugge på läkemedelsmarknaden<br />
Orexo har sitt ursprung inom drug delivery och bolaget har i dag tillgång till<br />
ett antal olika teknologier som används i utvecklingen av redan godkända<br />
läkemedelssubstanser med <strong>för</strong>bättrade egenskaper. I den konkurrensutsatta<br />
läkemedelsindustrin utgör drug delivery en viktig kugge <strong>för</strong> att<br />
skapa konkurrens<strong>för</strong>delar och utforska terapeutiska möjligheter inom den<br />
globala hälsovårdsmarknaden. Det är tre primära mål som vill uppnås<br />
genom att använda innovativa drug delivery-metoder.<br />
• <strong>för</strong>längning av patenttiden <strong>för</strong> en substans genom aktiv life cycle<br />
management och en patenterad omformulering<br />
• <strong>för</strong>bättra profilen från en molekyl <strong>för</strong> att öka <strong>för</strong>säljning genom<br />
ökad differentiering gentemot konkurrenter<br />
• utöka en substans terapeutiska egenskaper genom omformulering<br />
Det finns ett stort antal olika patenterade drug delivery-teknologier hos<br />
bolag inom området. För att Orexo ska vara en attraktiv partner till<br />
läkemedelsbolag krävs en kontinuerlig vidareutveckling och <strong>för</strong>bättringar.<br />
Vidareutveckla godkända<br />
substanser inte så<br />
kostsamt<br />
Drug Delivery kortar utvecklingstiden<br />
Att utveckla ett nytt läkemedel kostar stora summor, tar tid och är <strong>för</strong>enat<br />
med stora risker. Genom att använda redan tidigare godkända läkemedelssubstanser<br />
i utvecklingen av nya patenterbara läkemedel kan kostnader<br />
hållas nere samtidigt som studier snabbare kan genom<strong>för</strong>as, detta då de<br />
regulatoriska kraven är lägre då säkerhet och effekt från substansen är mer<br />
väl dokumenterad och resultat från tidigare studier kan utnyttjas. Drug<br />
delivery innebär inte bara bättre chanser <strong>för</strong> att nå marknaden och kortare<br />
utvecklingstider, utan den främsta <strong>för</strong>delen är att kostnaderna är betydligt<br />
lägre. I en undersökning från Bionumbers genom<strong>för</strong>t uppgår den genomsnittliga<br />
kostnaden <strong>för</strong> att ta en drug delivery-produkt till marknaden<br />
uppgår till i genomsnitt 90 miljoner dollar. Det kan jäm<strong>för</strong>as med 1,3<br />
miljarder dollar som den genomsnittliga kostnaden är <strong>för</strong> att ta ett helt nytt<br />
läkemedel till marknaden, enligt J.A. DiMasi and H.G. Grabowski,<br />
Managerial and Decision Economics 28 (2007).<br />
Många storsäljare tappar patent de närmaste åren<br />
Läkemedelsbolagen har haft ett par gyllene decennier där fantastiska<br />
framsteg har gjorts inom en lång rad terapiområden. Industrin har dock fått<br />
det allt svårare att komma fram med nya, innovativa läkemedel och den<br />
närmaste femårsperioden kommer att innebära ett riktigt stålbad <strong>för</strong><br />
läkemedelsindustrin, där flera riktiga storsäljare tappar sina patent.<br />
Processen med patentutgångar <strong>för</strong> storsäljare har pågått några år och<br />
drabbat bolagen vid olika perioder, men den närmaste femårsperioden kan<br />
ses som en klimax när det gäller patentutgångar, se tabell nedan.<br />
Bolagsanalys<br />
65
Orexo<br />
Försäljning året <strong>för</strong>e <strong>för</strong> läkemedel som <strong>för</strong>lorar sitt patent<br />
70<br />
r<br />
la 60<br />
o<br />
ḏ<br />
S 50<br />
U<br />
r<br />
e<br />
rd 40<br />
ilja<br />
i<br />
m 30<br />
g<br />
in<br />
ljn 20<br />
rsä<br />
F<br />
ö 10<br />
0<br />
2005 2006 2007 2008 2009 2010 2011 2012 2013 2014<br />
Källa: McKinsey & company<br />
Utvecklingen med stora patentutgångar har pressat flera stora läkemedelsbolag<br />
till att dels licensiera produkter och dels att överväga närliggande<br />
tillväxtområden inom läkemedelsindustrin som exempelvis konsumentmarknaden.<br />
Två <strong>för</strong>ändringar Orexo kan dra <strong>för</strong>del av, vilket vi fått exempel<br />
på från det nyligen tecknade avtalet med Johnson & Johnson. Bolaget har<br />
därutöver möjlighet att teckna rena drug delivery-avtal. Dessa avtal<br />
kommer dock vara betydligt mindre i sin omfattning än det vi sett med J&J.<br />
Orexo har tillgång till ett<br />
antal patenterade<br />
teknologier<br />
Stark plattform inom tablettformulering<br />
Inom drug delivery ligger Orexos styrka främst i tablettformuleringar som<br />
exempelvis ger <strong>för</strong>bättrad biotillgänglihet, <strong>för</strong>bättrad patientbekvämlighet,<br />
<strong>för</strong>bättrad effekt med till<strong>för</strong>litligare dosering. Nedan följer en genomgång<br />
av bolagets olika patenterade teknologier <strong>för</strong> drug delivery.<br />
Sublingual mukoadhesiv tablettformulering<br />
Den sublinguala teknologin är validerad med två godkända produkter i<br />
marknaden (Abstral och Edluar). Flera andra projekt som baseras på denna<br />
teknologi har initierats där inledande kliniska studier genom<strong>för</strong>ts <strong>för</strong> OX19,<br />
vilka var framgångsrika.<br />
Den sublinguala teknologin kan användas <strong>för</strong> att fram<strong>för</strong>allt uppnå en<br />
snabbt insättande effekt av läkemedlet, vilket uppnås genom att den<br />
verksam substans snabbt sönderfaller tillsammans bärarpartiklar som<br />
fäster på munslemhinnan där den absorberas och går då rakt in i<br />
blodbanan. Andra <strong>för</strong>delar med sublingual administrering av verksam<br />
substans är en till<strong>för</strong>litlig dosering och repeterbar effekt.<br />
Bolagsanalys<br />
66
Orexo<br />
Oral snabblöslig tablett<br />
Orexos andra validerade teknologi är den patenterade teknologin <strong>för</strong> snabb<br />
upplösning av läkemedelssubstanser. Teknologin används i Orexos <strong>för</strong>sta<br />
godkända diagnostiska produkt Diabact UBT samt i det terapeutiska<br />
projektet OX17. Teknologin <strong>för</strong>bättrar den biologiska tillgängligheten<br />
genom att <strong>för</strong>bättra upplösningen av den verksamma substansen i magen.<br />
Det ger en snabbare insättande effekt och kan därmed öka till<strong>för</strong>litligheten i<br />
effekten. Vi känner i nuläget inte till några andra projekt som bolaget driver<br />
baserat på denna teknologi.<br />
Xersol<br />
Ett nytt tillskott som följde med i samband med <strong>för</strong>värvet av PharmaKodex<br />
under år 2009. Detta är en sublingual teknologi som kompletterar bolagets<br />
andra teknologi inom detta område och kan <strong>för</strong>bättra genomträngningen av<br />
munslemhinnan. Teknologin används exempelvis i utvecklingsprojektet<br />
OX219 som även ingick i <strong>för</strong>värvet av PharmaKodex.<br />
Solid Syrup<br />
En teknologi som lämpar sig både <strong>för</strong> läkemedel som sväljs eller tas upp via<br />
munslemhinnan. Solid Syrup är en teknologi som snabbt omvandlar små<br />
läkemedelspartiklar till en flytande vätska vid kontakt med saliv i munnen.<br />
Med teknologin <strong>för</strong>bättras snabbhet till effekt och <strong>för</strong>bättrar precision vid<br />
dosering. Dessutom ger teknologin en maskering av substansens smak och<br />
kan ges med ett brett dosspektra. I <strong>för</strong>hållande till liknande teknologier<br />
uppges produktkostnaden vara låg, vilket alltid är attraktivt från ett<br />
industriellt perspektiv.<br />
Smak<strong>för</strong>bättring av läkemedel med dålig smak<br />
Det finns många etablerade läkemedel på marknaden där smak utgör ett<br />
problem. Något som exempelvis kan leda till dålig följsamhet av recept och<br />
därmed sämre behandlingsresultat. Vid <strong>för</strong>värvet av PharmaKodex fick<br />
Orexo tillgång till flera olika teknologier som utvecklats <strong>för</strong> att maskera eller<br />
<strong>för</strong>bättra ett läkemedels smak.<br />
Lipsomal nässpray<br />
Drug-delivery teknologi som följde vid <strong>för</strong>värvet av Biolipox AB och<br />
används i läkemedelsprojektet OX-NLA. Teknologin möjliggör att lokal<br />
effekt kan uppnås med antihistaminer och steroider vid behandling av<br />
hösnuva. Kan även användas då en snabbt insättande effekt önskas vid<br />
behandling av exempelvis smärta, migrän och astma. Den lipsomala<br />
teknologin begränsas inte bara till användning i nässpray utan kan även<br />
användas <strong>för</strong> administrering på slemhinnor där irritation kan vara ett<br />
problem som exempelvis i ögonen.<br />
Bolagsanalys<br />
67
Orexo<br />
Pandermal<br />
Med hjälp av denna teknologi kan läkemedel tas upp via huden i<br />
kontrollerade doser. Främsta <strong>för</strong>delarna med detta är att läkemedel kan ges<br />
i bestämd dos med ett kontrollerbart upptag samt att substansen kan<br />
frisläppas över en tid. Teknologin bygger på en tablett med aktiv substans<br />
som stryks mot huden. Att ge aktiv substans med tablett mot som kräm är<br />
kontrollen av dosering. En annan <strong>för</strong>del är att teknologin inte är<br />
allergiframkallande, vilket öppnar <strong>för</strong> användning hos patienter med<br />
hudsjukdomar.<br />
Bolagsanalys<br />
68
Orexo<br />
Appendix 6 - Vetenskaplig plattform<br />
I samband med <strong>för</strong>värvet av Biolipox under år 2007 fick Orexo tillgång till<br />
innovativ spetskompetens med forskning inom inflammationsområdet<br />
kring den kroppsegna substansen arakidonsyra. Forskningen härstammar<br />
från Karolinska Institutet som har en stark historik inom området, vilket<br />
underströks då Bengt Samuelsson och Sune Bergström fick Nobelpriset i<br />
medicin.<br />
Avtal med J&J styrker<br />
bolagets spetskompetens<br />
inom området<br />
Arakidonsyra<br />
Arakidonsyra är en essentiell fettsyra som lagras i cellmembranen och är<br />
viktig <strong>för</strong> flera olika processer i kroppen. När cellerna aktiveras frigörs<br />
arakidonsyra som omvandlas till familjer av biologiskt aktiva ämnen<br />
(mediatorer), i synnerhet prostaglandiner och leukotriener. Dessa<br />
mediatorer är nödvändiga <strong>för</strong> normala kroppsfunktioner, men de återfinns<br />
även bakom olika typer av sjukdomsprocesser – i synnerhet<br />
inflammatoriska sjukdomar. Orexo har identifierat en ny familj av<br />
arakidonsyra relaterade mediatorer, eoxiner, som har visat sig ha kraftfulla<br />
proinflammatoriska effekter.<br />
Arakidonsyrafamiljen<br />
Prostaglandiner har många olika funktioner i kroppen. De spelar en<br />
betydelsefull roll <strong>för</strong> fertilitet, blodtrycksreglering och blodkoagulering,<br />
men de kan även orsaka inflammation, smärta och feber. Leukotriener är<br />
ämnen som orsakar astmatiska symtom såsom bronksammandragning,<br />
svullnad och slembildning, vilka i sin tur kan leda till andningssvårigheter.<br />
Eoxinerna har visat sig vara involverade i olika inflammatoriska processer<br />
och Orexo bedriver idag intensiv forskning <strong>för</strong> att öka <strong>för</strong>ståelsen <strong>för</strong> hur<br />
eoxinerna bildas och fungerar i kroppen.<br />
Vanliga läkemedel blockerar bildningen av<br />
arakidonsyramediatorer<br />
Flera av de allra vanligaste läkemedlen som används <strong>för</strong> att behandla<br />
inflammatoriska sjukdomar påverkar bildningen eller effekten av<br />
prostaglandiner och leukotriener. Sådana läkemedel innefattar de<br />
vanligaste smärtlindrande och antiinflammatoriska medlen, de så kallade<br />
NSAI Ds (Non-Steroidal Anti-Inflammatory Drugs), till exempel Voltaren<br />
och Naproxen, men även leukotrienblockeraren Singulair, som används<br />
mot astma. Dagens icke-steroida anti-inflammatoriska läkemedel är<br />
cyklooxygenashämmare (COX -hämmare), som blockerar det <strong>för</strong>sta steget i<br />
bildningen av prostaglandiner. Det finns två typer av cyklooxygenaser, COX<br />
-1 och COX -2, där COX -1-enzymet normalt återfinns i de flesta celler i<br />
kroppen medan COX -2-enzymet i huvudsak nybildas i inflammerad<br />
vävnad. Ökade mängder av COX -2 leder till ökad bildning av<br />
inflammatoriska prostaglandiner, främst prostaglandin E2 (PGE2).<br />
Bolagsanalys<br />
69
Orexo utvecklar nya läkemedel <strong>för</strong> astma, KOL och<br />
inflammatorisk smärta<br />
Orexo<br />
Orexo har idag tre läkemedelsutvecklingsprojekt, som baserar sig på<br />
mekanismer inom arakidonsyrakaskaden. Avsikten är att påverka bildning<br />
och/eller funktion av de mediatorer som leder till sjukdom och/eller<br />
symtom utan att <strong>för</strong> den skull orsaka biverkningar. Ett exempel är OX -<br />
MPI. För några år sedan upptäcktes ett nytt proinflammatoriskt enzym,<br />
membranbundet PGE-syntas (mPGES ). Detta enzym ansvarar <strong>för</strong> det<br />
andra steget i bildningen av PGE2 ur arakidonsyra och bildas i stora<br />
mängder i inflammerad vävnad. Detta skulle kunna vara nyckeln till en mer<br />
selektiv antiinflammatorisk behandling, som skulle vara effektivt mot<br />
smärta, inflammation och feber men tack vare sin selektivitet ha färre<br />
biverkningar än vad som är fallet <strong>för</strong> existerande läkemedel. Ett annat<br />
exempel är OX 2477, där avsikten är att hämma bildningen av eoxiner och<br />
därigenom åstadkomma en minskad inflammation i luftvägarna hos<br />
patienter med inflammatorisk luftvägssjukdom t ex astma eller KOL.<br />
Bolagsanalys<br />
70
Orexo<br />
Appendix 7 - Ägare<br />
HealthCap och Novo<br />
huvudägare<br />
Orexo är sedan år 2005 noterat på Stockholmsbörsen och finns listade på<br />
SmallCap. Totalt finns det per den sista maj 23,4 miljoner aktier <strong>för</strong>delat på<br />
3 924 aktieägare. Största ägarna är HealthCap som äger 5,6 miljoner aktier<br />
med 24,1 procent av kapital. Värt att nämna att HealthCap är ett riskkapitalbolag<br />
vars innehav i Orexo ingår i en privat fond (HC Fond III) som<br />
stänger 2010 och som därefter har en tvåårig avvecklingsperiod. Det<br />
innebär att Health Cap behöver avyttra sitt innehav i Orexo senast 2012.<br />
HealthCap är med andra ord en ägare med en hög motivation att få Orexo<br />
så intressant som möjligt under denna period <strong>för</strong> att underlätta en<br />
avyttring, men givetvis även <strong>för</strong> att få till så bra villkor som möjligt.<br />
HealCap har stundom varit ifrågasatt som ägare, då de ansågs driva på<br />
köpet av Biolipox.<br />
Tabell aktieägare Orexo per den sista maj 2010<br />
Aktieägare aktier Andel röster %<br />
HealthCap 5 632 971 24,1%<br />
Novo Nordisk Fonden 2 496 042 10,7%<br />
Sofinnova Partners 1 397 142 6,0%<br />
Tredje AP-fonden 1 261 592 5,4%<br />
Läns<strong>för</strong>säkringar fonder 1 053 279 4,5%<br />
Staffan Rasjö 987 426 4,2%<br />
Fjärde AP-fonden 907 898 3,9%<br />
Credit Agricole Private Equity 593 397 2,5%<br />
Thomas Lundqvist 495 250 2,1%<br />
Avanza Pension Försäkringar AB 325 448 1,4%<br />
Christer Nyström 301 000 1,3%<br />
HSBC Private Bank 300 000 1,3%<br />
JP Morgan Bank 260 550 1,1%<br />
Pyrinox AB 234 149 1,0%<br />
Nordnet Pensions<strong>för</strong>säkring AB 220 197 0,9%<br />
Gamla liv<strong>för</strong>säkringsaktiebolaget 215 600 0,9%<br />
Totalt 23 401 252 100,0%<br />
Källa: Orexo<br />
Bolagsanalys<br />
71
Orexo<br />
I början av året <strong>för</strong>stärkte Orexo sin kapitalbas genom en riktad konvertibelemission<br />
på 111 miljoner kronor till Novo Growth Equity (NGE). I samband<br />
med emissionen köpte NGE även aktier från riskkapitalbolagen Apax<br />
Partners och SLS Venture och blev därigenom bolagets näst störste aktieägare<br />
med en ägarandel på 10,7 procent av kapitalet, som kan komma att<br />
öka till 18,8 procent vid konvertering.<br />
Novos ägarandel kan<br />
komma stiga till 19<br />
procent<br />
Konvertibelemissionen innebar flera <strong>för</strong>delar utöver kapitaltillskottet, vilket<br />
skapat <strong>för</strong>utsättningar <strong>för</strong> Orexo att öka sina aktiviteter i att bygga ett<br />
rörelsedrivandebolag och addera nya egna projekt. Det minskade även<br />
överhänget i aktien från två aktörer som ville sälja sina innehav. En tredje<br />
<strong>för</strong>del är att Orexo fått en ägare med industriell bakgrund och kunskap<br />
inom området med nätverk inom branschen. NGE har som ambition att<br />
vara en aktiv ägare och har tagit plats i bolagets styrelse. En fjärde positiv<br />
faktor var att HealthCaps dominans bland ägarna minskar, vilket ger en<br />
lägre risk <strong>för</strong> nya arrangerade äktenskap med andra HealthCap-bolag likt<br />
köpet av Bioliopx. Sist men inte minst är intåget från NGE en bekräftelse på<br />
Orexo som en intressant investering från en aktör med stor kunskap inom<br />
branschen.<br />
Bolagsanalys<br />
72
Orexo<br />
Appendix 8 - Ledning<br />
Orexo har en ledningsgrupp som består av sex personer. Den ledas av<br />
verkställande direktör Torbjörn Bjerke som tillträdde posten år 2007 och<br />
kom till bolaget från det <strong>för</strong>värvade Biolipox. Bolagets ledning har en lång<br />
erfarenhet av branschen och har gedigna kunskaper i att ta läkemedel från<br />
idé till marknaden. På den kommersiella sidan finns vissa brister som<br />
kommer behöva <strong>för</strong>stärkas när Orexo utvecklas till ett bolag med egen<br />
<strong>för</strong>säljning, distribution och marknads<strong>för</strong>ing av läkemedel. Ledningen har<br />
genom åren levererat en rad olika licens-, distributions- och partneravtal,<br />
vilket varit bra <strong>för</strong> att på ett kostnadseffektivt driva verksamheten.<br />
Nackdelen med detta har dock varit att vissa partners inte prioriterat<br />
projekt <strong>för</strong> vidare utveckling. Problemet med att kommunicera vad som<br />
sker hos partners har slagit tillbaka mot ledningen. Nedan följer en<br />
kortfattad beskrivning av respektive person inom ledningen:<br />
Torbjörn Bjerke, verkställande direktör och koncernchef<br />
• Har varit anställd som verkställande direktör <strong>för</strong> Orexo sedan<br />
november 2007 och kom till bolaget i samband med <strong>för</strong>värvet av<br />
Biolipox AB där han hade samma position från januari 2004<br />
• Har cirka 15 års erfarenhet från läkemedelsbranschen från bolag<br />
som bland annat Astra Zeneca och innan Biolipox som chef <strong>för</strong><br />
forskning och utveckling på ALK-Abello<br />
• Är styrelseledamot i NeuroSearch AS och DBV Technologies<br />
• Aktie- och optionsinnehav i Orexo: 121.108 aktier och<br />
personaloptioner berättigande till täckning av 84.586 aktier<br />
Claes Wenthzel, <strong>för</strong>ste vice verkställande direktör och<br />
finansdirektör<br />
• Har varit anställd sedan september 2005<br />
• Han har tidigare bland annat varit vice verkställande direktör och<br />
finansdirektör i det på Stockholmsbörsen noterade Perbio Science<br />
AB (1999-04) och finansdirektör i det på Stockholmsbörsen<br />
noterade bolaget Louis Gibeck AB (1997-99) och Sandblom &<br />
Stohne AB (1995-97)<br />
• Är styrelseord<strong>för</strong>ande i Stille AB<br />
• Aktie- och optionsinnehav i Orexo: 10.000 aktier och<br />
personaloptioner berättigande till täckning av 86.250 aktier<br />
Bolagsanalys<br />
73
Orexo<br />
Thomas Lundqvist, andre vice verkställande direktör samt chef<br />
<strong>för</strong> farmaceutisk forskning och utveckling<br />
• Är en av Orexos grundare och var styrelseledamot mellan 1995 och<br />
2003.<br />
• Har varit VD <strong>för</strong> Orexo mellan 1997 och 2002 samt fem månader<br />
mellan december 2003 och april 2004<br />
• Har en lång erfarenhet från läkemedelsutveckling och har tidigare<br />
varit VD <strong>för</strong> NeoPharma Production AB. Dessutom har han mer än<br />
tio års erfarenhet från Läkemedelsverket<br />
• Aktie- och optionsinnehav i Orexo: 495.250 aktier och<br />
personaloptioner berättigande till täckning av 60.000 aktier<br />
Charlotte Edenius, chef <strong>för</strong> preklinisk och klinisk forskning och<br />
utveckling<br />
• Anställdes i dåvarande Biolipox år 2001 och följde med över till<br />
Orexo vid <strong>för</strong>värvet i november 2007<br />
• Har mer än 20 års erfarenhet inom inflammationsforskning, främst<br />
arakidonsyraområdet<br />
• Har en gedigen bakgrund inom läkemedelsutveckling med 15 års<br />
erfarenhet. Senast ledande befattning var inom experimentell<br />
medicin på AstraZeneca<br />
• Aktie- och optionsinnehav i Orexo: 9.587 aktier och<br />
personaloptioner berättigande till täckning av 54.902 aktier<br />
Robin Wright, chef <strong>för</strong> affärs- och kommersiell utveckling<br />
• Anställd sedan 2008 och kommer närmast från BioScience<br />
Managers Limited, fond<strong>för</strong>valtare och rådgivare inom corporate<br />
finance med speciellt fokus på läkemedelsbranschen, där han var<br />
Head of Corporate Advisory Services<br />
• Har lång erfarenhet av internationell corporate finance och<br />
affärsutveckling inom läkemedelsbranschen<br />
• Aktie- och optionsinnehav i Orexo: Äger inga aktier men har<br />
personaloptioner berättigande till täckning av 50.000 aktier<br />
Bolagsanalys<br />
74
Orexo<br />
Gunilla Ekström, chef <strong>för</strong> projekt- och portfölj<strong>för</strong>valtning<br />
• Anställd sedan 2008 och kommer närmast från Astrazeneca där<br />
hon sedan 2000 arbetat som Global Product Director med ansvar<br />
<strong>för</strong> projektportföljen inom smärtområdet. Sedan 2005 har hon varit<br />
medlem av ledningsgruppen <strong>för</strong> Therapeutic Area Neuroscience i<br />
Astrazeneca<br />
• Har mer än 20 års erfarenhet av läkemedelsutveckling inom<br />
smärtområdet<br />
• Aktie- och optionsinnehav i Orexo: Äger inga aktier men har<br />
personaloptioner berättigande till täckning av 40.000 aktier<br />
Bolagsanalys<br />
75
Orexo<br />
Appendix 9 - Historik<br />
1995: Orexo grundas av Thomas Lundqvist, Anders Petterson och Christer<br />
Nyström. Bakgrunden till initiativet var deras kombinerade kunskaper om<br />
olika sjukdomar, formuleringar av läkemedelssubstanser och hur läkemedel<br />
dokumenteras. Affärsidén var att utifrån ouppfyllda patientbehov utveckla<br />
läkemedel med betydande marknadspotential genom att kombinera<br />
egenutvecklad patenterad drug delivery-teknologi med redan kända och<br />
väldokumenterade aktiva läkemedelssubstanser.<br />
1997: Första licensavtalet tecknas med bolaget Kyowa Hakko <strong>för</strong><br />
utandningstest i Japan<br />
2000: Bolagets <strong>för</strong>sta kommersiella produkt lanseras, Diabact UBT, ett<br />
utandningstest <strong>för</strong> att diagnostisera bakterien Heliobacter pylori, den<br />
vanligaste orsaken till uppkomsten av magsår.<br />
2003: Bolagsnamnet ändras till Orexo. Licensierar ut de japanska<br />
marknadsrättigheterna <strong>för</strong> Abstral (tidigare Rapinyl, KW-2246 i Japan) till<br />
Kyowa Hakko<br />
2004: Tecknar ett licensavtal <strong>för</strong> Abstral med specialty pharma-bolaget<br />
Endo Pharmaceuticals <strong>för</strong> den nordamerikanska marknaden.<br />
2005: Orexo börsnoteras på Stockholmsbörsen. Dotterbolaget Kibion<br />
bildas, som ska fokusera på marknads<strong>för</strong>ing och <strong>för</strong>säljning av<br />
magsårsdiagnostiktestet Diabact UBT. Därtill tecknar Orexo sitt ett tredje<br />
licensavtal <strong>för</strong> Abstral, den här gången med Prostrakan <strong>för</strong> den europeiska<br />
marknaden.<br />
2006: Lämnar in en registreringsansökan på den europeiska marknaden<br />
<strong>för</strong> smärtprodukten Abstral. Tecknade ett distributionsavtal <strong>för</strong> Abstral med<br />
läkemedelsbolaget Gedeon Richter <strong>för</strong> CIS (Ryssland och övriga länder i<br />
forna Sovjetunionen), Bulgarien och Rumänien. Inleder ett nytt samarbete<br />
om en ny teknologiplattform med Doxa AB. Därtill genom<strong>för</strong> Orexos<br />
dotterbolag Kibion ett <strong>för</strong>värv av Noster System AB, <strong>för</strong> att stärka sin<br />
position inom magsårsdiagnostik.<br />
2007: Patent <strong>för</strong> OX17 godkänns i Europa. Bildar gemensamt<br />
marknadsbolag med ProStrakan och etablerar säljstyrkor på den nordiska<br />
marknaden. Registreringsprocessen av Abstral i EU över<strong>för</strong>s till EMEA’s<br />
Committee for Medicinal Products for Human Use (CHMP) efter att enighet<br />
bland medlemsländernas representanter inte kunde nås inom den<br />
decentraliserade proceduren. Orexo redovisar positivt resultat i jäm<strong>för</strong>ande<br />
klinisk fas-III studie <strong>för</strong> Edluar (Sublinox). Orexo <strong>för</strong>värvar Biolipox AB, ett<br />
bioteknikbolag som utvecklar nya behandlingsformer av inflammatoriska<br />
Bolagsanalys<br />
76
Orexo<br />
sjukdomar. Ny koncernledning etableras. Endo publicerar positiva resultat<br />
från interimsanalysen av fas III-studie <strong>för</strong> Abstral.<br />
2008: Abstral godkänns <strong>för</strong> marknads<strong>för</strong>ing i Sverige och kort därefter <strong>för</strong><br />
hela EU. Bolaget licensierar Sublinox och OX-NLA till det svenska specialty<br />
pharma-bolaget Meda. Orexo rapporterar resultat som bekräftar klinisk<br />
effekt av OX17 <strong>för</strong> behandling av refluxsjukdom (GERD). En registreringsansökan<br />
<strong>för</strong> den amerikanska marknaden <strong>för</strong> sömntabletten Sublinox<br />
(OX22) lämnas in till FDA. Ett snabbt byte av partner <strong>för</strong> den nordamerikanska<br />
marknaden från Endo som omprioriterar sina satsningar till<br />
Prostrakan där ett redan väl fungerande samarbete finns. Fas II-studie med<br />
läkemedelskandidat OX914 påbörjas <strong>för</strong> behandling av hösnuva. Under det<br />
andra halvåret påbörjas kommersiell lansering av Abstral i Europa.<br />
2009: Tecknar avtal <strong>för</strong> den kinesiska marknaden med Novamed<br />
Pharmaceuticals och <strong>för</strong> den Israeliska marknaden med Neopharm Ltd. I<br />
början av året köper Orexo det brittiska drug-delivery bolaget Pharmakodex<br />
och breddar med fler drug-delivery teknologier och projekt. Fas IIresultaten<br />
<strong>för</strong> OX914 nådde inte målet, bolaget fortsätter dock jakten i att<br />
finna en partner till projektet. Edluar (tidigare Sublinox och OX22)<br />
godkänns av FDA och partnern Meda inleder kommersialisering under det<br />
andra halvåret. Ett bolag inom Novartis koncernen tecknar licensavtal <strong>för</strong><br />
OX17. Positiva resultat <strong>för</strong> Abstral rapporteras från bolagets japanska<br />
partner och en registreringsansökan lämnas in till FDA av Prostrakan.<br />
Under året har Prostrakan fortsatt kommersialiseringen av Abstral i Europa<br />
och <strong>för</strong>säljningen uppvisar en hög tillväxttakt.<br />
2010: Registreringsansökan lämnas in i Kanada och Japan. Novo Growth<br />
Equity blir ny storägare i Orexo och tecknar en konvertibellån på 111<br />
miljoner kronor.<br />
Bolagsanalys<br />
77
Orexo<br />
Sammanfattning <strong>Redeye</strong> Rating<br />
<strong>Redeye</strong>s Rating utgörs av fem värderingsnycklar. Varje värderingsnyckel<br />
består av en sammanvägning av ett antal faktorer som värderas på en<br />
betygskala från 0 till 2p. Maxpoängen <strong>för</strong> en värderingsnyckel är 10 poäng.<br />
Rating<strong>för</strong>ändringar i denna rapport:<br />
Vi har höjt betyget <strong>för</strong> Ledning två steg, Tillväxtpotential med ett steg och<br />
Avkastningspotential med ett steg.<br />
Ledning 8,0p<br />
Kommentar: Ledningen har gedigen erfarenhet från branschen. Senaste<br />
året har Orexo lyckats få två produkter godkända och tecknat flera betydelsefulla<br />
avtal. VD Torbjörn Bjerke äger en väsentlig aktiepost, vilket talar<br />
<strong>för</strong> stark motivation.<br />
Tillväxtpotential 8,0p<br />
Kommentar: Orexo agerar på en stor marknad med god tillväxtmöjlighet.<br />
Inom bolagets drug delivery är konkurrens tuff, men det vägs upp av<br />
innovativa projekt inom astma och KOL.<br />
Lönsamhet 1,0p<br />
Kommentar: Likt forskningsbolag har Orexo ingen historik med lönsamhet<br />
att falla tillbaka på. Vi räknar med att bolaget under vissa kvartal i år<br />
kommer kunna uppvisa vinst, men att det dröjer till 2012 innan löpande<br />
intäkter bär kostnaderna.<br />
Trygg placering 7,0p<br />
Kommentar: Bolagets <strong>för</strong>säljningsintäkter ökar successivt under året och<br />
finanserna är stabila efter genom<strong>för</strong>d konvertibelemission. Likviditeten i<br />
aktien är dock svag, vilket utgör ett problem <strong>för</strong> större transaktioner.<br />
Avkastningspotential 9,0p<br />
Kommentar: Värderingen <strong>för</strong> Orexo är låg även jäm<strong>för</strong>t med andra bolag<br />
i sektorn. Marknads<strong>för</strong>väntningarna är i nuläget lågt ställda in<strong>för</strong> en<br />
mycket spännande period. En möjlighet <strong>för</strong> investerare att bygga position<br />
in<strong>för</strong> positiva nyheter.<br />
Bolagsanalys<br />
78
Orexo<br />
Resultaträkning, MSEK 2008 2009 2010e 2011e 2012e<br />
Omsättning 233 236 201 472 570<br />
Summa rörelsekostnader -335 -314 -235 -304 -343<br />
EBITDA -102 -78 -34 168 226<br />
Avskrivningar -11 -21 -19 -20 -20<br />
EBIT -112 -99 -53 148 206<br />
Resultatandelar 0,0 0,0 0,0 0,0 0,0<br />
Finansiella intäkter 9 2 -9 -8 -4<br />
Finansiella kostnader 0 0 0 0 0<br />
Resultat <strong>för</strong>e skatt -103 -97 -61 140 202<br />
Skatt 0 -1 0 0 0<br />
Nettoresultat -103 -98 -61 140 202<br />
Resultaträkning just, MSEK 2008 2009 2010e 2011e 2012e<br />
Jäm<strong>för</strong>elsestörande poster 4 0 0 0 0<br />
EBITDA just -106 -78 -34 168 226<br />
EBIT just -116 -99 -53 148 206<br />
PTP just -107 -97 -61 140 202<br />
Nettoresultat just -107 -98 -61 140 202<br />
Balansräkning, MSEK 2008 2009 2010e 2011e 2012e<br />
Tillgångar<br />
Omsättningstillgångar<br />
Kassa och bank 188 87 290 255 365<br />
Kundfordringar 58 61 55 70 80<br />
Lager 14 8 12 15 18<br />
Andra fordringar 0 0 0 0 0<br />
Summa omsättningstillg. 260 157 357 340 463<br />
Anläggningstillgångar<br />
Materiella anl.tillg. 50 46 43 39 35<br />
Finansiella anl.tillg. 0 0 0 0 0<br />
Goodwill 392 447 439 431 423<br />
Balans. utv. kostn. 0 0 0 0 0<br />
Övr. immateriella tillg. 0 0 0 0 0<br />
Summa anläggningstillg. 442 493 482 470 458<br />
Summa tillgångar 702 649 839 810 921<br />
Skulder<br />
Kortfristiga skulder<br />
Leverantörsskulder 0 0 0 0 0<br />
Övriga icke ränteb skulder 122 64 52 55 60<br />
Summa kortfristiga skulder 122 64 52 55 60<br />
Långa icke ränteb.skulder 1 21 78 20 25<br />
Räntebärande skulder 10 16 120 10 15<br />
Summa skulder 132 101 250 85 100<br />
Avsättningar 0 0 0 0 0<br />
Eget kapital 570 549 589 725 821<br />
Minoritet 0 0 0 0 0<br />
Minoritet & Eget Kapital 570 549 589 725 821<br />
Summa skulder och eget kapital702 649 839 810 921<br />
Fritt kassaflöde, MSEK 2008 2009 2010e 2011e 2012e<br />
Omsättning 233 236 201 472 570<br />
Summa rörelsekostnader -335 -314 -235 -304 -343<br />
Avskrivningar -11 -21 -19 -20 -20<br />
EBIT -112 -99 -53 148 206<br />
Skatt på EBIT (Justerad skatt) 0 -1 0 0 0<br />
NOPLAT -109 -90 -45 156 214<br />
Avskrivningar 8 11 11 12 12<br />
Bruttokassaflöde -101 -79 -34 168 226<br />
Förändring i rörelsekapital -11 -56 -10 -15 -8<br />
Investeringar -2 0 -8 -8 -8<br />
Fritt kassaflöde -115 -135 10 114 179<br />
Kapitalstruktur 2008 2009 2010e 2011e 2012e<br />
Soliditet 81% 84% 70% 90% 89%<br />
Skuldsättningsgrad 2% 3% 20% 1% 2%<br />
Nettoskuld -179 -71 -170 -245 -350<br />
Sysselsatt kapital 579 565 709 735 836<br />
Kapitalets oms. hastighet 0,4 0,4 0,3 0,7 0,7<br />
DCF värdering<br />
Kassaflöden, MSEK<br />
Riskpremie (%) 6,4 NV FCF (2010-2012) 239,5<br />
Betavärde 1,4 NV FCF (2013-2017) 1 011,7<br />
Riskfri ränta (%) 3,1 NV FCF (2018-) 1 243,5<br />
Räntepremie (%) 5,0 Rörelsefrämmade tillgångar 87,4<br />
WACC (%) 12,1 Räntebärande skulder 16,0<br />
Motiverat värde 2 566,1<br />
Antaganden 2013-2017 (%)<br />
Genomsn. <strong>för</strong>s. tillv. 20,9 Motiverat värde per aktie, SEK 102,7<br />
EBIT-marginal 45,0 Börskurs, SEK 41,0<br />
Lönsamhet 2008 2009 2010e 2011e 2012e<br />
Avk. på eget kapital (ROE) -17% -18% -11% 21% 26%<br />
ROCE -18% -17% -8% 20% 26%<br />
ROIC -17% -16% -7% 22% 27%<br />
EBITDA just-marginal -45% -33% -17% 36% 40%<br />
EBIT just-marginal -50% -42% -26% 31% 36%<br />
Netto just-marginal -46% -42% -31% 30% 36%<br />
Data per aktie, SEK 2008 2009 2010e 2011e 2012e<br />
VPA -4,77 -4,19 -2,46 5,12 7,41<br />
VPA just -4,94 -4,19 -2,46 5,12 7,41<br />
Utdelning 0,0 0,0 0,0 0,0 0,0<br />
Nettoskuld -8,3 -3,1 -6,8 -9,0 -12,8<br />
Antal aktier 21,6 23,4 25,0 27,3 27,3<br />
Värdering 2008 2009 2010e 2011e 2012e<br />
Enterprise value 846 953 896 896 896<br />
P/E -8,6 -9,8 -16,7 8,0 5,5<br />
P/E just -8,3 -9,8 -16,7 8,0 5,5<br />
P/S 4,4 4,3 5,1 2,2 1,8<br />
EV/S 3,6 4,0 4,4 1,9 1,6<br />
EV/EBITDA just -8,0 -12,2 -26,4 5,3 4,0<br />
EV/EBIT just -7,3 -9,6 -16,9 6,1 4,3<br />
P/BV 1,8 1,9 1,7 1,4 1,2<br />
Aktiens utveckling Tillväxt/år 08/10P<br />
1 mån 11,0% Omsättning -7,1%<br />
3 mån -4,0% Rörelseresultat, just -32,5%<br />
12 mån 11,0% V/A, just -29,5%<br />
Årets Början 13,0% EK 1,7%<br />
Aktiestruktur % Röster Kapital<br />
Health Cap 24,1 24,1<br />
Novo Growth Equity 10,7 10,7<br />
Sofinnova Capital 6,0 6,0<br />
Tredje AP-Fonden 5,4 5,4<br />
Staffan Rasjö 4,7 4,7<br />
Fjärde AP-Fonden 4,2 4,2<br />
Läns<strong>för</strong>säkringar fonder 3,9 3,9<br />
Credit Agricole Private Equity 2,5 2,5<br />
Thomas Lundqvist 2,1 2,1<br />
n.m.<br />
n.m.<br />
Aktien<br />
Reuterskod<br />
ORX.ST<br />
Lista<br />
Small cap<br />
Kurs, SEK 41,0<br />
Antal aktier, milj 25,0<br />
Börsvärde, MSEK 1 025<br />
Börspost 1<br />
Bolagsledning & styrelse<br />
VD<br />
CFO<br />
IR<br />
Ordf<br />
Nästkommande rapportdatum<br />
Torbjörn Bjerke<br />
Claes Wenthzel<br />
Johan Andersson<br />
Håkan Åström<br />
Rapport andra kvartalet, jan-juni 2010 2010-08-20<br />
Tillväxt 2008 2009 2010e 2011e 2012e<br />
Försäljningstillväxt 204% 1% -15% 134% 21%<br />
VPA-tillväxt (just) n.m. % n.m. % n.m. % n.m. % 45%<br />
Tillväxt eget kapital -15% -4% 7% 23% 13%<br />
Analytiker<br />
Klas Palin<br />
klas.palin@redeye.se<br />
Björn Fahlén<br />
bjorn.fahlen@redeye.se<br />
<strong>Redeye</strong> AB<br />
Mäster Samuelsgatan 42, 10tr<br />
114 35 Stockholm<br />
Bolagsanalys<br />
79
Orexo<br />
Omsättning & Tillväxt (%)<br />
EBIT (justerad) & Marginal (%)<br />
600<br />
500<br />
400<br />
300<br />
200<br />
100<br />
0<br />
2006 2007 2008 2009 2010e 2011e 2012e<br />
250%<br />
200%<br />
150%<br />
100%<br />
50%<br />
0%<br />
-50%<br />
-100%<br />
250<br />
200<br />
150<br />
100<br />
50<br />
0<br />
-50<br />
-100<br />
-150<br />
-200<br />
-250<br />
2006 2007 2008 2009 2010e 2011e 2012e<br />
100%<br />
50%<br />
0%<br />
-50%<br />
-100%<br />
-150%<br />
-200%<br />
-250%<br />
-300%<br />
Omsättning<br />
Försäljningstillväxt<br />
EBIT just<br />
EBIT just-marginal<br />
Vinst Per Aktie<br />
Soliditet & Skuldsättningsgrad (%)<br />
10<br />
8<br />
6<br />
25%<br />
20%<br />
100%<br />
90%<br />
80%<br />
4<br />
2<br />
15%<br />
70%<br />
60%<br />
0<br />
-2<br />
-4<br />
-6<br />
-8<br />
-10<br />
2006 2007 2008 2009 2010e 2011e 2012e<br />
10%<br />
5%<br />
0%<br />
-5%<br />
2006 2007 2008 2009 2010e 2011e 2012e<br />
50%<br />
40%<br />
30%<br />
20%<br />
10%<br />
0%<br />
VPA<br />
VPA just<br />
Skuldsättningsgrad<br />
Soliditet<br />
Intressekonflikter<br />
Klas Palin äger aktier i bolaget Orexo: Ja<br />
Björn Fahlén äger aktier i bolaget Orexo Nej<br />
<strong>Redeye</strong> ut<strong>för</strong>/har ut<strong>för</strong>t tjänster åt bolaget och erhåller/har erhållit<br />
ersättning från bolaget i samband med detta.<br />
Bolagsanalys<br />
80
Orexo<br />
DISCLAIMER<br />
Viktig information<br />
<strong>Redeye</strong> AB("<strong>Redeye</strong>" eller "Bolaget") är ett fristående analys<strong>för</strong>etag som står under Finansinspektionens (FI) tillsyn sedan juli 2007. Bolaget erbjuder<br />
aktierelaterade tjänster till börsbolag, investerare, media och den aktieintresserade allmänheten. <strong>Redeye</strong> har tillstånd att mottaga och<br />
vidarebefordra finansiella instrument, att lämna investeringsrådgivning avseende finansiella instrument samt att utarbeta och sprida investerings- och<br />
finansanalyser samt andra former av allmänna rekommendationer rörande handel med finansiella instrument, enligt 2 kap. 1-2 §§ lagen<br />
(2007:528) om värdepappersmarknaden.<br />
Ansvarsbegränsning<br />
Detta dokument är framställt i informationssyfte <strong>för</strong> allmän spridning och är inte avsett att vara rådgivande. Informationen i analysen är baserad på<br />
källor som <strong>Redeye</strong> bedömer som till<strong>för</strong>litliga. <strong>Redeye</strong> kan dock ej garantera riktigheten i informationen. Den framåtblickande informationen i analysen<br />
baseras på subjektiva bedömningar om framtiden, vilka innehåller en osäkerhet. <strong>Redeye</strong> kan inte garantera att prognoser och framåtblickande estimat<br />
kommer att bli uppfyllda. Varje investeringsbeslut fattas självständigt av investeraren. Denna analys är avsedd att vara ett av flera redskap vid ett<br />
investeringsbeslut. Varje investerare uppmanas att komplettera med ytterligare relevant material samt konsultera en finansiell rådgivare in<strong>för</strong> ett<br />
investeringsbeslut. <strong>Redeye</strong> frånsäger sig därmed allt ansvar <strong>för</strong> eventuell <strong>för</strong>lust eller skada av vad slag det må vara som grundar sig på användandet<br />
av analysen.<br />
Potentiella intressekonflikter<br />
<strong>Redeye</strong>s analysavdelning regleras av organisatoriska och administrativa regelverk som inrättats i syfte att undvika intressekonflikter och att säkerställa<br />
analytikernas objektivitet och oberoende. Bland annat gäller följande:<br />
• För bolag som är <strong>för</strong>emål <strong>för</strong> <strong>Redeye</strong>s analys gäller bl.a. de regler som Finansinspektionens har uppställt avseende<br />
investeringsrekommendationer och hantering av intressekonflikter. Vidare gäller <strong>för</strong> bolagets anställda handelsstopp i finansiella<br />
instrument <strong>för</strong> bolaget från och med den dag beslut tagits att en analys ska produceras på bolaget samt två bankdagar efter analysen<br />
publicerats.<br />
• En analytiker får inte utan särskilt tillstånd från ledningen medverka i corporate finance verksamhet och får inte erhålla ersättning som är<br />
direkt kopplad till sådan verksamhet.<br />
• <strong>Redeye</strong> kan genom<strong>för</strong>a analyser på uppdrag av, och mot en ersättning från, det bolag som belyses i analysen alternativt ett<br />
emissionsinstitut i samband M&A, nyemission eller en notering. Läsaren av dessa rapporter kan anta att <strong>Redeye</strong> har erhållit eller kommer<br />
att erhålla betalning <strong>för</strong> ut<strong>för</strong>andet av finansiella rådgivningstjänster från bolaget/bolag nämnt i rapporten. Ersättningen är ett på <strong>för</strong>hand<br />
överenskommet belopp och är inte beroende av innehållet i analysen.<br />
Angående <strong>Redeye</strong>s analysbevakning<br />
<strong>Redeye</strong>s analys präglas av case-baserad analys vilket innebär att frekvensen av analysrapporter kan variera över tiden. Om annat inte uttryckningen<br />
anges i analysen uppdateras analysen när Redeys analysavdelning finner att så är påkallat av t.ex. väsentliga <strong>för</strong>ändrade marknads<strong>för</strong>utsättningar<br />
eller händelser relaterade till analyserad emittent/analyserat finansiellt instrument.<br />
Rating/Rekommendationsstruktur<br />
<strong>Redeye</strong> utfärdar ej några investeringsrekommendationer <strong>för</strong> fundamental analys. Däremot så har <strong>Redeye</strong> utarbetat en proprietär analys och<br />
ratingmodell, <strong>Redeye</strong> Rating, där det enskilda bolaget analyseras, utvärderas och belyses. Analysen ska ge en oberoende bedömning av bolaget, dess<br />
möjligheter, risker mm. Syftet är att ge ett objektivt och professionellt beslutsunderlag <strong>för</strong> ägare och investerare.<br />
<strong>Redeye</strong>s rekommendationer <strong>för</strong> teknisk analys är: Köp (Buy) och Sälj (Sell). Placeringshorisonten <strong>för</strong> dessa rekommendationer är mycket kort, oftast<br />
mindre än 1 månad.<br />
<strong>Redeye</strong> Rating (2010-06-04)<br />
Rating<br />
Ledning<br />
Tillväxt-<br />
Trygg Avkastnings-<br />
Lönsamhet<br />
potential<br />
Placering potential<br />
7,5p - 10,0p 29 20 17 28 18<br />
3,5p - 7,0p 55 64 42 52 62<br />
0,0p - 3,0p 3 3 28 7 7<br />
Antal bolag 87 87 87 87 87<br />
*För investmentbolag byts Tillväxtpotential och Lönsamhet ut mot Portfölj<strong>för</strong>valtning och Direktavkastning.<br />
Mångfaldigande och spridning<br />
Detta dokument får inte mångfaldigas <strong>för</strong> annat än personligt bruk. Dokumentet får inte spridas till fysiska eller juridiska personer som är medborgare<br />
eller har hemvist i ett land där sådan spridning är otillåten enligt tillämplig lag eller annan bestämmelse.<br />
Copyright <strong>Redeye</strong> AB.<br />
Bolagsanalys<br />
81