Broschüre Achema - TTN-Hessen
Broschüre Achema - TTN-Hessen
Broschüre Achema - TTN-Hessen
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
Abb. 3: MTP-Photometer mit Messplatte eines<br />
p-Nitrophenylphosphat-Assays: links: p-Nitrophenol-<br />
Standard in steigender Konzentration, rechts:<br />
Inkubationsansätze mit steigenden Substratkonzentrationen,<br />
zu denen das Enzym alkalische Phosphatase<br />
pipettiert wurde.<br />
Chemische Reaktionen in lebenden Organismen<br />
werden durch Enzyme katalysiert.<br />
Diese erhöhen die Reaktionsgeschwindigkeiten<br />
um ein Vielfaches und gewährleisten<br />
meist eine hohe Selektivität: nur<br />
bestimmte Substrate (Edukte) werden zu<br />
definierten Produkten umgesetzt.<br />
Zum genauen Verständnis, zur exakten<br />
Bestimmung enzymatischer Aktivitäten<br />
können die gleichen Substrate außerhalb<br />
des Organismus – in vitro – vorgelegt und<br />
ihre Umsetzung mit geeigneten Assays<br />
erfasst werden. In vielen Fällen lassen sich<br />
die Produkte von den natürlichen Substraten<br />
nur durch aufwändige Methoden und<br />
zeitverzögert – z.B. durch chromatographische<br />
Aufreinigungen – unterscheiden.<br />
Um zeitnah viele enzymatische Reaktionsansätze<br />
parallel zu verfolgen, die Daten<br />
zudem durch Mehrfachbestimmung statistisch<br />
abzusichern, bewähren sich Testsysteme<br />
mit künstlichen Substraten, zu denen<br />
die photometrischen Mikrotiterplatten<br />
(MTP)-Assays mit Derivaten des para-<br />
Nitrophenols (pNP) gehören.<br />
NO 2<br />
OH<br />
-<br />
Enzymkinetische<br />
Messungen mit<br />
Mikrotiterplattenassays<br />
NO 2<br />
Abb. 2: Deprotononierung des p-Nitrophenols zum p-Nitrophenolatanion und dessen mesomere Resonanzstrukturen<br />
Mit diesen Verbindungen werden vorzugsweise<br />
Aktivitäten von Hydrolasen, der<br />
3. von insgesamt 6 Enzymklassen erfasst<br />
(Abb. 1).<br />
Das nach hydrolytischer Spaltung des<br />
pNP-Derivats freigesetzte p-Nitrophenol<br />
liegt im neutralen bis basischen Bereich<br />
als p-Nitrophenolatanion vor und weist<br />
eine wesentlich höhere Elektronendichte<br />
im aromatischen Kern auf (Abb. 2). Als<br />
Konsequenz intensiviert sich die Lichtabsorption<br />
und verschiebt sich vom UV-<br />
Bereich (Absorptionsmaximum: 320 nm)<br />
in den Bereich sichtbaren, blauen Lichts<br />
(Absorptionsmaximum: 400 nm), als starke<br />
Gelbfärbung erkennbar, und kann photometrisch<br />
erfasst werden (Abb. 3), zeit -<br />
aufgelöst während einer bei neutralen<br />
bis basischen pH-Werten durchgeführten<br />
Enzymreaktion. Bei Enzymreaktionen unter<br />
sauren Bedingungen wird die Reaktion<br />
durch Erhöhen des pH-Wertes beendet<br />
und unmittelbar im Anschluss photometrisch<br />
ausgewertet (Endpunkt-Assay).<br />
O -<br />
N +<br />
O<br />
O R<br />
+<br />
O<br />
H 2<br />
HO - C -<br />
H 2 O<br />
O -<br />
Hydrolase<br />
R OH<br />
Abb. 1: Enzymatische Hydrolyse eines p-Nitrophenolderivats (Ethers, Esters)<br />
O<br />
+<br />
O-<br />
N<br />
O<br />
CH -<br />
O -<br />
+ O<br />
N<br />
O<br />
+<br />
N + O -<br />
O<br />
OH<br />
Prof. Dr. Axel Blokesch<br />
blokesch@fb2.fh-frankfurt.de<br />
T 069 1533 3681<br />
Fachhochschule Frankfurt am Main<br />
University of Applied Sciences<br />
Fachbereich 2, Bioverfahrenstechnik<br />
Nibelungenplatz 1<br />
60318 Frankfurt am Main<br />
www.ttn-hessen.de | ACHEMA 2012 | Halle 9.2, Stand A66 7<br />
O<br />
HC -<br />
+<br />
O-<br />
N<br />
O<br />
O -<br />
+<br />
O-<br />
N<br />
O
8<br />
reaction rate<br />
reaction rate<br />
120 nmol/(l*s)<br />
100 nmol/(l*s)<br />
80 nmol/(l*s)<br />
60 nmol/(l*s)<br />
40 nmol/(l*s)<br />
20 nmol/(l*s)<br />
0 nmol/(l*s)<br />
0 µmol/l 100 µmol/l 200 µmol/l 300 µmol/l 400 µmol/l<br />
120 nmol/(l*s)<br />
100 nmol/(l*s)<br />
80 nmol/(l*s)<br />
60 nmol/(l*s)<br />
40 nmol/(l*s)<br />
20 nmol/(l*s)<br />
0 nmol/(l*s)<br />
0 mmol/l 5 mmol/l 10 mmol/l 15 mmol/l<br />
Preisgünstig und gut zu handhaben sind Assays mit dem Enzym<br />
Alkalische Phosphatase und dem Substrat p-Nitrophenylphos -<br />
phat, die in der medizinischen Diagnostik von Blutseren und als<br />
Hilfsmittel in der Immundiagnostik eingesetzt werden. Abweichend<br />
von den standardisierten Bedingungen dieser Routineassays<br />
variieren die Studierenden im Laborpraktikum des 3. Fachsemesters<br />
(Bachelorstudiengang Bioverfahrenstechnik) systematisch<br />
einzelne Parameter und erarbeiten sich grundlegende<br />
Kenntnisse der Enzymkinetik:<br />
p Erhöhung der Reaktionsgeschwindigkeit mit steigender<br />
Substratkonzentration bis zum Sättigungsbereich<br />
(Michaelis-Menten-Kinetik, siehe Abb. 4)<br />
p Einfluss von Cofaktoren auf die Enzymreaktion<br />
p Unterscheidung von kompetitiver (Beispiel: Abb. 5)<br />
und nicht-kompetitiver Hemmung<br />
In der Folge sind gezielt Enzyme und Assays ausgewählt worden,<br />
die für eine anwendungsorientierte Forschung relevant sind:<br />
p Auf dem Gebiet der roten (d.h. medizinischen) Biotechnologie:<br />
Erfassen einer spezifischen proteolytischen Aktivität, der Spaltung<br />
der Peptidbindung auf Carboxylseite der Aminosäure<br />
Lysin, die u.a. von einer Reihe von Matrix-Metalloproteasen<br />
(MMP) katalysiert wird. MMP spalten Strukturproteine (Kollagene,<br />
Elastine) der extrazellulären Matrix und sind für die<br />
Remodellierung des Gewebes wichtig. Erhöhte Werte im Blutserum<br />
oder anderen Körperflüssigkeiten weisen jedoch auf<br />
krankhafte Veränderungen wie Tumore oder Entzündungen<br />
ENZYME KINETIC ASSAYS ON MICROTITER PLATES<br />
Chemical reactions in living organisms<br />
are catalyzed by enzymes. Appropriate<br />
assays enable us to determine their activity<br />
– e.g. during a purification process or<br />
in a technical application, calculate kinetical<br />
constants and characterize the effect<br />
of inhibitors or activating cofactors.<br />
In photometric microtiter plate (MTP)<br />
assays using derivatives of p-nitrophenol<br />
as artificial substrates, many reactions<br />
reziprocal reaction rate<br />
2,5 E+07 (l*s)/mol<br />
2,0 E+07 (l*s)/mol<br />
1,5 E+07 (l*s)/mol<br />
1,0 E+07 (l*s)/mol<br />
5,0 E+06 (l*s)/mol<br />
y = 305,44x + 1E + 07<br />
R 2 = 0,9747<br />
0,0 E+00 (l*s)/mol<br />
0 l/mol 10000 l/mol 20000 l/mol 30000 l/mol 40000 l/mol 50000 l/mol<br />
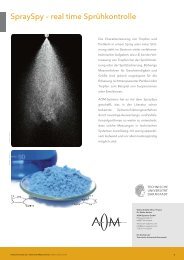
Abb. 4 (oben): Reaktionsgeschwindigkeit der Hydrolyse von p-Nitrophenylphosphat durch Alkalische<br />
Phosphatase in Abhängigkeit der Substratkonzentration – in direkter (links) und doppelt-reziproker<br />
(rechts) Auftragung<br />
Abb. 5 (links): Produkthemmung: Reaktionsgeschwindigkeit der Hydrolyse von p-Nitrophenylphosphat<br />
durch Alkalische Phosphatase in Abhängigkeit der Phosphatkonzentration – für zwei unterschiedliche<br />
Substratkonzentrationen: 50 µmol l -1 (◆) und 400 µmol l -1 p-Nitrophenylphosphat (●) – Bis zu einer<br />
Konzentration von ca. 0,1 mmol l -1 des Inhibitors Phosphat handelt es sich um eine kompetitive<br />
Hemmung, die durch Erhöhung der Substratkonzentration aufgehoben werden kann.<br />
Die Maximalgeschwindigkeiten v max liegen in diesem Bereich jeweils bei 100 nmol l -1 s -1 und sinken erst<br />
bei weiterer Erhöhung der Phosphatkonzentrationen (0,5 bis 12,5 mmol l -1 ) auf 30 bis 10 nmol l -1 s -1<br />
(nicht alle Daten und deren Auswertung hier aufgeführt).<br />
may be monitored simultaneously (timeresolved<br />
in case of neutral to alkaline<br />
reaction conditions, as end-point assays<br />
in case of acidic reaction conditions and<br />
subsequent addition of alkaline solution).<br />
Students start their laboratory course<br />
with alkaline phosphatase cleaving pnitrophenylphosphate<br />
to learn the fundamentals<br />
of enzyme kinetics. Assays with<br />
peptide derivatives of p-nitrophenol make<br />
hin. Ausgewählte MMP werden daher als Biomarker spezifisch<br />
mit Antikörpern detektiert. Diese Immundiagnostik – vorzugsweise<br />
direkt am Krankenbett (POC = Point of Care) durchgeführt,<br />
können Entwickler und Hersteller sinnvoll ergänzen,<br />
indem sie die Qualität der MMP, d.h. ihrer Antigene, durch<br />
Befunde der Enzymanalytik absichern.<br />
p Auf dem Gebiet der weißen Biotechnologie (Grund- und Feinchemikalien,<br />
Nutzung nachwachsender Rohstoffe):<br />
Bestimmung von Phospholipase- und Lipaseaktivitäten<br />
In der Halbraffinierung von Pflanzenölen ist die Entschleimung<br />
(engl. degumming) ein Prozessschritt, der sowohl für die<br />
anschließende Produktion von Speiseöl als auch von Biodiesel<br />
wichtig ist. Entfernt werden dabei Phospholipide (z.B: Phosphatidylinositole,<br />
Lecithine), die die Abtrennung der Fette von der<br />
wässrigen Phase behindern. Die Entfernung der Phospholipide<br />
lässt sich durch deren partielle enzymatische Hydrolyse effizienter<br />
gestalten. Für die anschließende Biodieselproduktion relevant<br />
ist die Umesterung der Fette (Triglyceride) zu Fettsäuremethylestern<br />
(FAME = Fatty Acid Methyl Ester), die von Lipasen<br />
katalysiert werden kann. Für Titerplattenassays wurde ein p-NP-<br />
Ester mit einer repräsentativen Fettsäure, der Palmitin- oder<br />
Hexadecansäure gewählt. Die Assays geben Auskunft über die<br />
Stabilität der Phospholipasen und Lipasen gegenüber den<br />
beim Emulgieren auftretenden mechanischen Beanspruchungen<br />
und den Temperaturen, pH-Werten, Solventien während<br />
der Reaktion. Sie helfen damit, ihren Einsatz zu optimieren.<br />
sure that matrix metalloproteases used as<br />
antigens in immuno assays (inflammation<br />
or tumor markers) have kept their enzymatic<br />
activity. Other assays involve fatty<br />
acid esters of p-nitrophenol as substrates<br />
for phospholipases and lipases, enzymes<br />
used e.g. in a semi refining step (degumming)<br />
of plant seed oil and in the transesterification<br />
of lipids to biodiesel (fatty acid<br />
methyl ester = FAME), respectively.
Split.It<br />
Automatisiertes System zur Zellpassage<br />
Ziel innerhalb des vom Bundesministerium<br />
für Wirtschaft und Technologie geförderten<br />
ZIM-Projekts Split.It ist die Entwicklung<br />
eines automatisierten Systems zur<br />
Passage von gängigen adhärenten Zelllinien.<br />
Die Firma InnoCyte kooperiert dabei<br />
mit dem biologischen Labor des Fachbereichs<br />
2, Bioverfahrenstechnik der Fachhochschule<br />
Frankfurt am Main, der Hochschule<br />
Esslingen (Institut für angewandte<br />
Forschung, IAF) sowie Geräteherstellern<br />
und Produktdesignern. Split.It stellt ein<br />
erschwingliches stand-alone Benchtop-<br />
Gerät dar, mit einfacher und flexibler<br />
Handhabung, welches durch in-situ Reinigung<br />
sicheres und kontaminationsfreies<br />
Arbeiten, mit dem Verzicht auf teure Verschleißteile<br />
garantiert.<br />
Für den zunehmenden Zellkulturbedarf an<br />
tierischen und humanen Zellen in der<br />
industriellen, biologischen und medizinischen<br />
Forschung, sowie bei der Produktion<br />
von Biopharmaceuticals, ist eine<br />
zukünftige automatisierte Herstellung großer<br />
Mengen an Zellmaterial unerlässlich.<br />
Auch im Hinblick auf Standardisierung<br />
und Qualitätssicherung der Produkte ähnlich<br />
GMP (Good Manufacturing Practise)<br />
und GLP (Good Laboratory Practise) bzw.<br />
GCCP (Good Cell Culture Practise) wird<br />
künftig eine Automatisierung der kritischen<br />
Routineprozesse erforderlich sein.<br />
Aus diesem Grund bestehen zahlreiche<br />
Bestrebungen, den Prozess der Zellkultur<br />
durch eine geeignete Automatisierung<br />
effizienter, standardisierter und kostengünstiger<br />
zu realisieren.<br />
Erste Systeme für die automatisierte Zellkultur<br />
umfassen vollautomatisierte industrielle<br />
Geräte für mittleren bis hohen<br />
Durchsatz (HTS = Hochdurchsatz-Screening),<br />
wohingegen teilautomatisierte<br />
Lösungen für die kritischen manuellen Prozessschritte<br />
zwar vom Markt gewünscht,<br />
aber noch nicht verfügbar sind. So stellt<br />
auch die routinemäßige Passage von Zellen<br />
einen nach wie vor langwierigen, arbeitsintensiven<br />
und manuellen Prozess dar, der<br />
unter strengen aseptischen Bedingungen<br />
durchgeführt werden muss. Hier setzt das<br />
Produkt Split.It – automatisierte Passage<br />
von Zellkulturen an, um in einer kleinen,<br />
flexiblen und kostengünstigen Lösung die<br />
Qualität und Produktivität von Zellkultur -<br />
laboren zu fördern und Forschung und<br />
Entwicklung nachhaltig zu verbessern.<br />
Cell line HeLa: Mycoplasmas negative DAPI-staining<br />
Cell line CHO: Mycoplasmas negative DAPI-staining<br />
Prof. Dr. Ilona Brändlin<br />
ilona.braendlin@fb2.fh-frankfurt.de<br />
Fachhochschule Frankfurt am Main<br />
University of Applied Sciences<br />
Fachbereich 2: Informatik und<br />
Ingenieurwissenschaften<br />
Studiengang Bioverfahrenstechnik<br />
Nibelungenplatz 1<br />
60318 Frankfurt am Main<br />
T 069 1533-2203 (Labor)<br />
T 0160 97030180<br />
www.fh-frankfurt.de<br />
InnoCyte GmbH<br />
Dr. Michael Fritsche, Dipl.-Ing. Roland Huchler<br />
Nobelstraße 12<br />
70569 Stuttgart<br />
T +49 711 970-1129<br />
info@innocyte.com<br />
www.ttn-hessen.de | ACHEMA 2012 | Halle 9.2, Stand A66 9
10<br />
Grundlage für dieses Forschungsprojekt war eine von der Firma<br />
InnoCyte entwickelte Basistechnologie, welche den zentralen Prozess<br />
der „Passage“ der automatisierten Zellkultur mit einem<br />
Bruchteil des bisher dafür notwendigen Aufwands realisiert. Der<br />
Ansatz basiert auf dem konsequenten Einsatz von fluidischen und<br />
pneumatischen Komponenten für alle Teilschritte der notwen -<br />
digen Umfüllprozesse.<br />
Das Funktionsmuster erlaubte eine prinzipielle Überprüfung der<br />
Arbeitsweise der Technologie in dem Sinne, dass die zentralen<br />
Schritte der Zellkulturpassage, wie<br />
p Entnahme des Kulturmediums und Spülung des Zellrasens,<br />
p Ablösen der Zellkultur durch Trypsin,<br />
p Abklopfen der Zellen durch mechanisch-pneumatische<br />
Aktoren,<br />
p Inhibierung des Trypsins durch Zugabe von serumhaltigem<br />
Kulturmedium,<br />
p Vereinzeln der Zellen durch Resuspension, und<br />
p Verteilen der Suspension auf neue Zellkulturflaschen<br />
abgebildet werden konnten.<br />
Cells/mm 2<br />
Amount of Cells x 10 6<br />
1000<br />
900<br />
800<br />
700<br />
600<br />
500<br />
400<br />
300<br />
200<br />
1,6<br />
1,4<br />
1,2<br />
1,0<br />
0,8<br />
0,6<br />
0,4<br />
0<br />
0,2<br />
13<br />
10.000.000.000<br />
Amount of Cells<br />
1.000.000.000<br />
100.000.000<br />
10.000.000<br />
1.000.000<br />
100.000<br />
0<br />
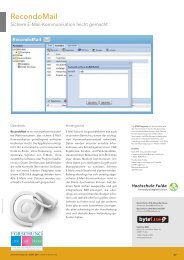
Proliferation Graph of A431-cell line<br />
Split.It<br />
Control<br />
1<br />
Day<br />
2 3<br />
Proliferation Graph of A431-cell line<br />
Split.It<br />
14 15 16 17 18 19<br />
Passage<br />
Proliferation Graph of HUVECs<br />
Control<br />
Control<br />
Split.It<br />
1 2 3 4 5 6<br />
Passage<br />
AUTOMATED CELL CULTURE TECHNIQUE<br />
The automated expansion of adherent<br />
cell lines in a simple, safe and time-saving<br />
manner was developed in cooperation<br />
with the University of Applied Sciences<br />
Frankfurt am Main, the Institute of Applied<br />
Sciences (AIF) Esslingen, InnoCyte GmbH<br />
and 2 renowned companies founded by<br />
BMWi. This brand-new innovative device<br />
Split.It automatically performs the central<br />
steps in the production of cell cultures,<br />
In Zukunft soll das System über seine Funktion hinaus auch durch<br />
die einfache Funktionsweise für den Anwender bestechen:<br />
p Einlegen der zu passagierenden, konfluenten Zellkultur -<br />
flasche („Mutterflasche“), eine Corning RoboFlask (100 cm 2 ),<br />
p Auswahl der gewünschten Anzahl „Tochterflaschen“,<br />
p Eingabe oder Auswahl des Protokolls,<br />
p STARTEN,<br />
p Entnahme der Tochterflaschen,<br />
p Automatischer Ablauf des Desinfektions- und Reinigungsprogramms.<br />
Die notwendigen Parameter werden dabei flexibel, das heißt<br />
zellspezifisch eingestellt, zum Beispiel:<br />
p Anzahl und Volumina der gewünschten Waschschritte,<br />
vor dem Passagieren,<br />
p Medienvolumina,<br />
p Reagenzienvolumina und dessen Inkubationszeit<br />
(z.B. Trypsin etc.),<br />
p Anzahl der Abklopfschritte („shake-off“),<br />
p Anzahl der Resuspensionsschritte,<br />
p Split-Verhältnis (von 1:1 bis 1:12).<br />
Das Forschungsprojekt hat nun zum Ziel, dieses Funktionsmuster<br />
in einen funktionstüchtigen Demonstrator zu überführen, der es<br />
der Firma InnoCyte ermöglicht ein Serienprodukt auf den Markt<br />
zu bringen und einen breiten Anwenderkreis zu erschließen!<br />
HeLa splitted<br />
automated with “Split.It”<br />
30 min.<br />
4h<br />
48 h<br />
HeLa splitted<br />
conservative – manually<br />
provided in an affordable stand-alone<br />
benchtop system. This reduces the risk of<br />
contamination and errors involved with<br />
manual processing, achieving improved<br />
productivity and quality of cell lines.