Formelsammlung Technische Verbrennung - Institut für Technische ...
Formelsammlung Technische Verbrennung - Institut für Technische ...
Formelsammlung Technische Verbrennung - Institut für Technische ...
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
<strong>Formelsammlung</strong><br />
<strong>Technische</strong> <strong>Verbrennung</strong><br />
Aachen, March 28, 2007
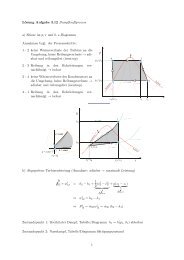
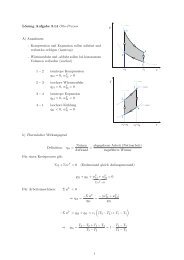
Kapitel 2<br />
Thermodynamik von <strong>Verbrennung</strong>sprozessen<br />
Molenbruch: n s =<br />
X i =<br />
n∑<br />
i=1<br />
n i<br />
n s<br />
n i<br />
Massenbruch: m i = M i n i<br />
m =<br />
Y i =<br />
m =<br />
n∑<br />
i=1<br />
m i<br />
m<br />
Mn s<br />
m i<br />
M =<br />
Y i =<br />
[<br />
n∑<br />
n<br />
] −1<br />
∑ Y i<br />
M i X i =<br />
M i<br />
i=1<br />
M i<br />
M X i<br />
i=1<br />
Massenbruch<br />
der Elemente: Z j =<br />
Z j =<br />
n∑<br />
i=1<br />
M j<br />
M<br />
Konzentration: C i = n i<br />
V<br />
a ij M j<br />
Y i<br />
M i<br />
n∑<br />
a ij X i<br />
i=1<br />
Volumenanteil: v i = V i<br />
V = X i<br />
Gasgesetz: p = ρRT<br />
M = C kJ<br />
sRT , R = 8.31451<br />
kmol · K
stöchiometrischer<br />
Koeffizient: ν i = ν i ′′ i<br />
n∑<br />
0 = ν ik [X i ]<br />
i=1<br />
Umsatzgleichung:<br />
dn i<br />
ν i<br />
= dn 1<br />
ν 1<br />
,<br />
dm i<br />
ν i M i<br />
= dm 1<br />
ν 1 M 1<br />
,<br />
dY i<br />
ν i M i<br />
= dY 1<br />
ν 1 M 1<br />
Y O2 − Y O2,u<br />
ν ′ O 2<br />
M O2<br />
= Y B − Y B,u<br />
ν ′ B M B<br />
Mindestluftbedarf: l min =<br />
o min<br />
Y O2,Luft<br />
, l min,m = o min,m<br />
X O2,Luft<br />
Luftzahl: λ =<br />
l<br />
=<br />
l m<br />
,<br />
l min l min,m<br />
φ = 1 λ<br />
Restsauerstoff: n O2,Rest = (λ − 1) ν′ O 2<br />
ν<br />
B<br />
′ n B,u ,<br />
m O2,Rest = (λ − 1) ν′ O 2<br />
M O2<br />
ν<br />
B ′ M m B,u<br />
B<br />
1.Hauptsatz der<br />
Thermodynamik: E = U + E kin + E pot<br />
Innere Energie<br />
und Enthalpie: H = U + pV<br />
U =<br />
H =<br />
c v =<br />
c p =<br />
n∑<br />
m i u i , U =<br />
i=1<br />
n∑<br />
m i h i , H =<br />
i=1<br />
n∑<br />
n i u i,m<br />
i=1<br />
n∑<br />
n i h i,m<br />
i=1<br />
n∑<br />
Y i c vi , c v,m =<br />
i=1<br />
n∑<br />
Y i c pi , c p,m =<br />
i=1<br />
n∑<br />
X i c vi,m<br />
i=1<br />
n∑<br />
X i c pi,m<br />
i=1
Reaktionsenthalpie<br />
und Heizwert: h u = (−∆h m)<br />
ν<br />
B ′ M B<br />
n∑<br />
h d = ∆h m = ν i h i,m<br />
i=1<br />
NASA-Polynome:<br />
c p,m<br />
R = a 1 + a 2 T/K + a 3 (T/K) 2 + a 4 (T/K) 3 + a 5 (T/K) 4<br />
h m<br />
RT =<br />
a 1 + a 2<br />
T/K<br />
2<br />
+ a 3<br />
(T/K) 2<br />
3<br />
+ a 4<br />
(T/K) 3<br />
4<br />
+ a 5<br />
(T/K) 4<br />
5<br />
+ a 6<br />
T/K<br />
s m<br />
R = a 1ln(T/K) + a 2 T/K + a 3<br />
(T/K) 2<br />
2<br />
+ a 4<br />
(T/K) 3<br />
3<br />
+ a 5<br />
(T/K) 4<br />
4<br />
+a 7 + ln p p 0<br />
adiabate<br />
Flammentemperatur: T b = T u + (−∆h m) ref Y B,u<br />
c p ν ′ B M B<br />
chemisches<br />
Gleichgewicht: 0 =<br />
n∑<br />
ν i µ i<br />
i=1
Massenwirkungsgesetz: K pk =<br />
π i (T ) =<br />
K p (T ) =<br />
n∏<br />
i=1<br />
(<br />
pi<br />
p 0<br />
) νik<br />
π i,A + π i,B lnT<br />
⎛<br />
∑<br />
− n ⎞ ⎛<br />
ν i µ 0 ∑<br />
i<br />
− n ⎞<br />
ν exp ⎜ i=1 ⎟<br />
⎝ RT ⎠ = exp i h i,mref ( ⎜ i=1<br />
n∑<br />
)<br />
⎟<br />
⎝ RT ⎠ exp ν i π i<br />
i=1<br />
K pk =<br />
B pk =<br />
n pk =<br />
(<br />
−∆hk,m,ref<br />
B pk T n pk<br />
exp<br />
RT<br />
( n<br />
)<br />
∑<br />
exp ν ik π iA<br />
i=1<br />
n∑<br />
ν ik π iB<br />
i=1<br />
)<br />
(Arrhenius-Ansatz)
Kapitel 3<br />
Reaktionskinetik homogener Gasreaktionen<br />
chem. Reaktionsgeschw.:<br />
dC A<br />
dt<br />
= −ν A ′ k f C ν′ A<br />
A<br />
C ν′ B<br />
B<br />
(<br />
B i T ni exp − E i<br />
RT<br />
k i =<br />
+ ν A ′ k bC ν′′ C<br />
)<br />
C<br />
Cν′′ D<br />
D<br />
= ν A w f − ν A w b = ν A w<br />
Konzentration inerter<br />
Stoßpartner: C M ′ =<br />
∑ n<br />
i=1<br />
z i C i<br />
Gleichgewichtskonstante: K C = k f (T )<br />
k b (T )<br />
chem. Produktionsdichte:<br />
.<br />
r∑<br />
m i = M i<br />
k=1<br />
ν ik w k<br />
reduzierter Methan-Mechanismus<br />
I : CH 4 + 2H ◦ + H 2 O = CO + 4H 2<br />
II : CO + H 2 0 = CO 2 + H 2<br />
III : 2H ◦ + M = H 2 + M<br />
IV : 3H 2 + O 2 = 2H ◦ + 2H 2 O
Kapitel 4<br />
Zünd- und Löschvorgänge in homogenen<br />
Systemen<br />
<strong>Verbrennung</strong> bei<br />
konst. Volumen:<br />
du<br />
dt = 0<br />
Temperaturgleichung:<br />
ρc v<br />
dT<br />
dt =<br />
=<br />
n − ∑<br />
u i M i<br />
i=1<br />
r∑<br />
n∑<br />
ν ik w k = −<br />
k=1<br />
r∑<br />
(−∆u k,m )w k<br />
k=1<br />
i=1<br />
u i<br />
.<br />
m i = −<br />
(<br />
r∑ ∑ n<br />
)<br />
M i u i ν ik w k<br />
k=1<br />
i=1<br />
adiabate therm.<br />
Explosion: w = B<br />
( ) ( ) (<br />
ρYB ρY02<br />
exp − E )<br />
M B M O2 RT<br />
Zündverzugszeit: t i = RT 2 0<br />
E<br />
( ) ( ) ( )<br />
c v MB MO2 E<br />
exp<br />
(−∆u m )Bρ Y B,0 Y O2,0 RT 0<br />
t i,q<br />
t i<br />
=<br />
∫ ∞<br />
0<br />
dz<br />
exp(z) − αz ,<br />
α = t i<br />
t q<br />
Reaktorgleichungen:<br />
dY<br />
(−<br />
dt = 1 − Y − Da Y exp E )<br />
T<br />
dT<br />
(−<br />
dt = 1 − T + Q Da Y exp E )<br />
T<br />
Y ∗ = Y Y u<br />
, Da = t v<br />
t r<br />
, E ∗ = E<br />
RT u<br />
, T ∗ = T T u<br />
, t ∗ = t<br />
t v<br />
,<br />
Q ∗ =<br />
(−∆h m)Y u<br />
c p MT u
Kapitel 5<br />
Bilanzgleichungen <strong>für</strong> laminare und turbulente<br />
Strömungen<br />
Turbulenzenergie: k = 1 2<br />
(<br />
)<br />
v 1 ′2 + v′2 2 + v′2 3<br />
Prandtlscher<br />
∣ Mischungswegansatz: τ t = ρlm<br />
2 ∂v 1 ∣∣∣ ∂v 1<br />
∣∂x 2 ∂x 2<br />
ν t = c 3 k 1/2 k 2<br />
l t , ν t = c D<br />
ɛ , ɛ = c 1<br />
k 3/2<br />
l t<br />
k-ɛ−Gleichung<br />
∂k<br />
∂t<br />
}{{}<br />
L<br />
+ v α<br />
∂k<br />
∂x α<br />
} {{ }<br />
K<br />
∂ɛ<br />
∂t + v ∂ɛ<br />
α =<br />
∂x α<br />
= − v<br />
β ′ ∂v β<br />
v′ α<br />
∂x α<br />
} {{ }<br />
P<br />
−<br />
}{{}<br />
ɛ + ∂ (<br />
νt<br />
∂x α Pr k<br />
DS<br />
)<br />
∂k<br />
∂x α<br />
} {{ }<br />
DF<br />
( )<br />
∂ νt ∂ɛ<br />
+ ɛ ∂x α Pr ɛ ∂x α k (c ɛ1P − c ɛ2 ɛ)<br />
c D = 0.09, c ɛ1 = 1.44, c ɛ2 = 1.9, c 1 = 0.2014,<br />
c 3 = 0.4469, Pr ɛ = 1.3, Pr k = 1.0<br />
Kolmogorov-Skalen: l k = η =<br />
( ) ν<br />
3 1/4 ( ν<br />
) 1/2<br />
, t η = , vη = (νɛ) 1/4<br />
ɛ<br />
ɛ
Kapitel 6<br />
Laminare und turbulente Vormischflammen<br />
Brennstoff-Luft-Verhältnis: φ =<br />
Z 1 − Z st<br />
1 − Z Z st<br />
T b = aT u + b + cφ + dφ 2 + eφ 3<br />
Approximationsformel: s L = Y m B,uA(T 0 ) T u<br />
T 0<br />
(<br />
Tb − T 0<br />
T b − T u<br />
) n<br />
, φ ≤ 1<br />
A(T 0 ) = F exp(−G/T 0 )<br />
T 0 =<br />
therm. Flammentheorie: ρ u s L =<br />
Ẽ<br />
−<br />
ln(p/B)<br />
√<br />
2 Bρ2 b λ bR 2 Tb<br />
4 (<br />
c p (T b − T u ) 2 E 2 exp − E )<br />
S<br />
RT b<br />
S = ν′ B Y O 2,b<br />
M O2<br />
S =<br />
⎧<br />
⎪⎨<br />
⎪⎩<br />
+ ν′ O 2<br />
Y B,b<br />
M B<br />
+ 2 ν′ O 2<br />
ν ′ B c pRT 2 b<br />
(−∆H)E<br />
ν ′ B Y O 2,b<br />
M O2<br />
<strong>für</strong> φ < 1,<br />
2 ν′ O 2<br />
ν B ′ c pRTb<br />
2<br />
(−∆H)E<br />
<strong>für</strong> φ = 1,<br />
ν O ′ 2<br />
Y B,b<br />
M B<br />
<strong>für</strong> φ > 1.<br />
( )<br />
Tb − T<br />
Zeldovich-Zahl: u<br />
Ze = n − 1 = E T b − T u<br />
T b − T 0 R Tb<br />
2<br />
Flammendicke: l F = D s L<br />
= λ b<br />
c p ρ u s L
Flammenzeit: t F = l F<br />
s L<br />
chem. Flammenzeit: t c = ρ uE 2 (T b − T u ) 2<br />
2Bρ 2 b (RT 2 b )2 S<br />
exp ( E<br />
RT b<br />
)<br />
s L =<br />
√<br />
D<br />
t c<br />
Kennzahlen: Re = v′ l t<br />
s L l F<br />
(Sc=1)<br />
Da =<br />
Ka =<br />
s Ll t<br />
v ′ l F<br />
t F<br />
t η<br />
= l2 F<br />
η 2 = v2 η<br />
s 2 =<br />
L<br />
(<br />
v ′3<br />
ν 3 l t<br />
) 1/2<br />
l 2 F<br />
Ka δ =<br />
l2 δ<br />
η 2 = δ2 Ka<br />
turbulente Brenngeschw.: s T ∼ v ′ grossballige Turbulenz (Damköhler)<br />
s T =<br />
√<br />
DT<br />
t c<br />
kleinballige Turbulenz (Damköhler)<br />
D T = 0.78v ′ l t turbulente Diffusivität<br />
l t = c 1<br />
k 3/2<br />
s T<br />
s L<br />
=<br />
ɛ<br />
1 − α l t<br />
l F<br />
+<br />
√<br />
(α l t<br />
l F<br />
) 2 + 4α v′<br />
s L<br />
l t<br />
l F<br />
allgemeingültig<br />
α = 0.195
Brennstoff B [bar] Ẽ [K] F [cm/s] G [K] m n<br />
CH 4 3, 1557 × 10 8 23873, 0 2, 21760 × 10 1 −6444, 27 0, 565175 2, 5158<br />
C 2 H 2 5, 6834 × 10 4 11344, 4 3, 77466 × 10 4 1032, 36 0, 907619 2, 5874<br />
C 2 H 4 3, 7036 × 10 5 14368, 7 9, 97890 × 10 3 263, 23 0, 771333 2, 3998<br />
C 2 H 6 4, 3203 × 10 6 18859, 0 1, 90041 × 10 3 −506, 97 0, 431345 2, 1804<br />
C 3 H 8 2, 2501 × 10 6 17223, 5 1, 27489 × 10 3 −1324, 78 0, 582214 2, 3970<br />
CH 3 OH 2, 1100 × 10 6 17657, 5 9, 99557 × 10 3 1088, 85 0, 91 2, 263<br />
n-C 7 H 16 1, 7000 × 10 6 17508, 0 7, 95600 × 10 3 912, 00 0, 52 2, 30<br />
i-C 8 H 18 3, 8000 × 10 7 20906, 0 2, 92600 × 10 3 −25, 60 0, 5578 2, 5214<br />
Table 1: Koeffizienten zur Berechnung der laminaren Brenngeschwindigkeit <strong>für</strong><br />
magere bis stöchiometrische Gemische<br />
Brennstoff a b [K] c [K] d [K] e [K] Le<br />
CH 4 0, 627 1270,15 −2449, 0 6776 −3556 0, 91<br />
C 2 H 2 0, 52 1646,0 −2965, 0 8187 −4160 1, 68<br />
C 2 H 4 0, 44 602,0 880, 0 2686 −1891 1, 21<br />
C 2 H 6 0, 526 1437,0 −2967, 0 7538 −3873 1, 32<br />
C 3 H 8 0, 53 1434,0 −2952, 0 7518 −3856 1, 63<br />
CH 3 OH 0, 77 1260,0 −2449, 0 6797 −3594 1, 68<br />
n-C 7 H 16 0, 49 758,7 −277, 8 4269 −2642 2, 056<br />
i-C 8 H 18 0, 61 936,0 −1127, 0 5326 −3044 2, 55<br />
Table 2: Koeffizienten zur Berechnung der adiabaten Flammentemperatur<br />
sowie Zahlenwerte <strong>für</strong> die Lewis-Zahl
Kapitel 7<br />
Laminare und turbulente Diffusionsflammen<br />
Mischungsbruch: Z =<br />
.<br />
m 1<br />
.<br />
m 2<br />
m 1 + .<br />
.<br />
m 1<br />
Brenngasstrom<br />
.<br />
m 2<br />
Oxidatorstrom<br />
Y B,u =<br />
Y B,1 Z<br />
Y O2,u = Y O2,2(1 − Z)<br />
Z st =<br />
[<br />
1 + ν Y ] −1 [<br />
] −1<br />
B,1<br />
= 1 + ν′ O 2<br />
M O2 Y B,1<br />
Y O2,2<br />
ν<br />
B ′ M BY O2,2<br />
λ =<br />
Z st<br />
Z<br />
1 − Z<br />
1 − Z st<br />
adiabate Flammentemperatur: T b (Z) = T u (Z) + (−∆h m) ref Y B,1<br />
c p ν<br />
B ′ M Z, 0 ≤ Z ≤ Z st<br />
B<br />
T u (Z) = T 2 + Z(T 1 − T 2 )<br />
Burke-Schumann-Lösung: T (Z) = T u (Z) + Z Z st<br />
[T st − T u (Z st )] , 0 ≤ Z ≤ Z st<br />
T (Z) =<br />
T u (Z) + 1 − Z<br />
1 − Z st<br />
[T st − T u (Z st )] , Z st ≤ Z ≤ 1
Flameletgleichungen:<br />
ρ ∂T<br />
∂t = ρχ 2<br />
∂ 2 T<br />
n<br />
∂Z 2 − ∑<br />
i=1<br />
h i<br />
c p<br />
.<br />
m i<br />
ρ ∂Y i<br />
∂t = ρχ 2<br />
∂ 2 Y i<br />
∂Z 2 + .<br />
m i<br />
(i=1,2,...,n)<br />
χ =<br />
( ) 2 ∂Z<br />
2D<br />
∂x α<br />
(skalare Dissipationsrate)<br />
Runde laminare Freistrahldiffusionsflamme<br />
Mischungsbruch: Z α (z) = 1 + 2 Sc<br />
32<br />
ρ 0 Re<br />
ρ ∞ C<br />
d<br />
ξ<br />
Sc =<br />
ρ 0 =<br />
C =<br />
ν D<br />
p<br />
RT 0<br />
M 0<br />
ρµr 2<br />
r∫<br />
2µ ∞ ρrdr<br />
0<br />
(Chapman-Rubesin-Parameter)<br />
Flammenlänge: L = 1 + 2 Sc ρ 0 u 0 d 2<br />
− a<br />
32Z st ρ ∞ C ν
Runde turbulente Freistrahldiffusionsflamme<br />
Mischungsbruch: Z α (z) = 1 + 2 Sc t<br />
32<br />
( )<br />
ρ 0 u0 d<br />
ρ ∞ C ν t,ref<br />
d<br />
z + a<br />
Sc t =<br />
ρ 0 =<br />
ν t<br />
D t<br />
p<br />
RT 0<br />
M 0<br />
Flammenlänge:<br />
L + a<br />
d<br />
C =<br />
ρ 2 ν t r 2<br />
r∫<br />
2ρ ∞ ν t,ref ρrdr<br />
= 1 + 2 Sc t<br />
32Z st<br />
0<br />
( )<br />
uo d ρ0<br />
ν t,ref ρ ∞ C<br />
(Chapman-Rubesin-Parameter)