Präparat 1 - Christopher Gallian, Diplom-Ingenieur der Chemischen ...
Präparat 1 - Christopher Gallian, Diplom-Ingenieur der Chemischen ...
Präparat 1 - Christopher Gallian, Diplom-Ingenieur der Chemischen ...
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
Name: <strong>Gallian</strong> Studiengang: Chemische Technik (4T) Datum: 19.10.04<br />
Vorname: <strong>Christopher</strong> Matrikelnummer: 0321296 Seite: 1 von 6<br />
<strong>Präparat</strong>: 1 Produkt: Chlorcyclohexan durchgeführt: 12.10.04<br />
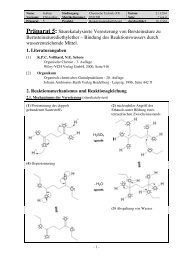
<strong>Präparat</strong> 1: Herstellung von Chlorcyclohexan durch<br />
nucleophile Substitution an Cyclohexanol<br />
1. Literaturangaben<br />
[1] K.P.C. Vollhard, N.E. Schore<br />
Organische Chemie - 3. Auflage<br />
Wiley-VCH Verlag GmbH, 2000<br />
[2] Gattermann, Wieland<br />
Die Praxis des organischen Chemikers - 43. Auflage<br />
DeGruyter-Verlag, 1982<br />
2. Reaktionsmechanismus und Reaktionsgleichung<br />
2.1.1. Mechanismus <strong>der</strong> Hauptreaktion (SN1)<br />
(1) Protonierung <strong>der</strong> OH-Gruppe, bilden<br />
von H2O als gute Abgangsgruppe<br />
ZnCl2<br />
HCl<br />
- 1 -<br />
(2) abspalten von Wasser<br />
- H2O<br />
(3) bilden des Carbenium-Ions<br />
(5) bilden des Produkts (4) Angriff des Nucleophils an das Carbenium-Ion<br />
„von Oben o<strong>der</strong> Unten“
Name: <strong>Gallian</strong> Studiengang: Chemische Technik (4T) Datum: 19.10.04<br />
Vorname: <strong>Christopher</strong> Matrikelnummer: 0321296 Seite: 2 von 6<br />
<strong>Präparat</strong>: 1 Produkt: Chlorcyclohexan durchgeführt: 12.10.04<br />
2.1.2. Reaktionsgleichung<br />
+ HCl<br />
ZnCl2<br />
2.2.1. Mechanismus <strong>der</strong> Nebenreaktion (E1 als Konkurrenzreaktion)<br />
(1) Protonierung <strong>der</strong> OH-Gruppe, bilden<br />
von H2O als gute Abgangsgruppe<br />
ZnCl2<br />
HCl<br />
-H +<br />
- 2 -<br />
(2) abspalten von Wasser<br />
- H2O<br />
(3) bilden des Carbenium-Ions<br />
+H2O<br />
(5) bilden des Nebenprodukts (4) stabilisieren des Carbenium-Ions durch umlagern<br />
eines Elektronenpaars und abspalten eines Protons<br />
2.2.2. Reaktionsgleichung<br />
+ H2O
Name: <strong>Gallian</strong> Studiengang: Chemische Technik (4T) Datum: 19.10.04<br />
Vorname: <strong>Christopher</strong> Matrikelnummer: 0321296 Seite: 3 von 6<br />
<strong>Präparat</strong>: 1 Produkt: Chlorcyclohexan durchgeführt: 12.10.04<br />
3. Ansatz<br />
Substanz Molmasse Dichte<br />
[g/mol] [g/cm 3 Stoffmenge Masse Volumen<br />
] [mol] [g] [ml]<br />
Cyclohexanol 110,16 0,94 0,2 20,4 22<br />
Zinkchlorid 136,28 2,91 0,4 54,4 - - -<br />
konz. Salzsäure - - - 1,15 ca. 0,22 - - - 20<br />
4. Versuchsdurchführung<br />
4.1. Aufbau <strong>der</strong> Reaktionsapparatur:<br />
Als Vorlagebehälter dient ein Dreihalskolben (250ml). Der Inhalt des<br />
Kolbens soll durch einen KPG-Rührer durchmischt werden. Außerdem<br />
werden an den Kolben noch ein Rückflusskühler und ein Tropftrichter<br />
angeschlossen. Im späteren Versuchsverlauf kann <strong>der</strong> Tropftrichter<br />
durch ein Thermometer ausgetauscht werden. Das Erhitzen des<br />
Reaktionsgemisches erfolgt durch einen Heizpilz.<br />
4.2. Durchführung:<br />
Im Vorlagebehälter wird das Zinkchlorid, unter Bildung einer<br />
gelblichen Lösung, in <strong>der</strong> Salzsäure gelöst. Danach wird innerhalb von<br />
5 Minuten das Cyclohexanol hinzu getropft, wobei eine rote bis<br />
braune Färbung entsteht. Der Tropftrichter wird entfernt und durch ein<br />
Innenthermometer ersetzt. Die Lösung wird dann aufgeheizt, wobei<br />
sich eine am Innenthermometer abgelesene Temperatur von 120°C<br />
einstellt. Die Lösung nimmt dabei eine dunkelgraue bis schwarze<br />
Farbe an.<br />
Nach einstündigem Kochen <strong>der</strong> Lösung wird die Wärmequelle entfernt und man lässt das<br />
Gemisch abkühlen. Nach dem Abkühlen lassen sich deutlich zwei Phasen erkennen. Eine<br />
grüne, organische Phase im oberen Teil und eine gelbliche, wässerige, Phase im unteren Teil.<br />
Die organische Phase enthält das Produkt und wird mittels eines Scheidetrichters von <strong>der</strong><br />
wässerigen Phase abgetrennt. Um eine bessere Trennung zu erzielen werden vor dem<br />
Überführen in den Scheidetrichter 60ml Wasser mit in den Vorlagebehälter gegeben.<br />
4.3. Reinigung des Produkts:<br />
Die organische Phase enthält außer dem Produkt noch Spuren an Wasser und sonstige<br />
Nebenprodukte wie z.B. Cyclohexen. Um das Produkt zu isolieren muss die Phase von<br />
Wasser befreit und anschließend einer Destillation unterzogen werden.<br />
Zum Entfernen des Wassers wird Calciumchlorid (wasserfrei u. fein gekörnt) zugegeben und<br />
geschwenkt. Um das Calciumchlorid wie<strong>der</strong> abzutrennen wird die Lösung mit einem<br />
Papierfilter filtriert. Für die folgende Destillation wird sie dann in einen 100ml Rundkolben<br />
gegeben.<br />
- 3 -<br />
Abb.1 Reaktionsaparatur
Name: <strong>Gallian</strong> Studiengang: Chemische Technik (4T) Datum: 19.10.04<br />
Vorname: <strong>Christopher</strong> Matrikelnummer: 0321296 Seite: 4 von 6<br />
<strong>Präparat</strong>: 1 Produkt: Chlorcyclohexan durchgeführt: 12.10.04<br />
4.4. Aufbau <strong>der</strong> Destillationsapparatur:<br />
Als Vorlagebehälter für die Destillation dient eine<br />
100ml Rundkolben. Über eine Claisenaufsatz wird<br />
<strong>der</strong> Kolben mit einem Liebigkühler verbunden. Der<br />
Claisenaufsatz wird mit einem Glasstopfen und<br />
einem Destillationsthermometer versehen. An das<br />
Ende des Liebigkühlers wird zum Abtrennen des<br />
Vorlaufs eine Spinne befestigt.<br />
4.5. Durchführung <strong>der</strong> Destillation:<br />
Die organische Phase wird mit einem Heizpilz<br />
erhitz. Um einem Siedeverzug entgegenzuwirken<br />
wird mit Magnetrührer und Rührfisch durchmischt.<br />
Die erste Fraktion erfolgt bei etwa 85°C<br />
abgelesener Temperatur. Sie macht sich durch einen<br />
plötzlichen, schnellen Anstieg und einem, nach<br />
Abdestillation <strong>der</strong> Fraktion, schnellen fall <strong>der</strong><br />
Temperatur bemerkbar.<br />
Eine weitere Fraktion tritt bei etwa 100°C auf. Durch drehen <strong>der</strong> Spinne wird sie in einem<br />
an<strong>der</strong>en Kolben aufgefangen. Das Produkt wird in <strong>der</strong> letzen Fraktion Abgetrennt bei einer<br />
Abgelesenen Temperatur von etwa 135°C (Lit. 139-141°C). Nach erfolgter Destillation sinkt<br />
die Temperatur auf 50°C ab. Im Kolben befindet sich noch ein Rest <strong>der</strong> organischen Phase,<br />
<strong>der</strong> sich nicht mehr verflüchtigt. Die Destillation wird an dieser Stelle beendet.<br />
4.6. Probe auf Doppelbindungen:<br />
Es werden je 1ml des Vorlaufs und des Produkts entnommen und jeweils in 10ml<br />
Diethylether gelöst. Danach werden einige Tropfen Bromwasser zu den Lösungen gegeben.<br />
Die Lösung aus dem Vorlauf entfärbt das Bromwasser. Die Lösung mit dem Produkt weist<br />
keine Reaktion auf.<br />
5. Ausbeute<br />
Masse [g] Stoffmenge [mol] Prozent [%]<br />
Theorie 23,7 0,2 100<br />
Literatur 14 - 15 0,12 - 0,13 59 - 63<br />
Versuch 9,3 0,08 40<br />
6. Eigenschaften des Produkts<br />
Form: flüssig<br />
Farbe: klar, farblos<br />
Brechungsindex: 1,4610<br />
- 4 -<br />
Abb.2 Destillationsaparatur
Name: <strong>Gallian</strong> Studiengang: Chemische Technik (4T) Datum: 19.10.04<br />
Vorname: <strong>Christopher</strong> Matrikelnummer: 0321296 Seite: 5 von 6<br />
<strong>Präparat</strong>: 1 Produkt: Chlorcyclohexan durchgeführt: 12.10.04<br />
7. Qualitativer Nachweis von Alkenen (Doppelbindungen)<br />
Die Entfärbung von Bromwasser ist ein qualitativer Nachweis für Doppelbindungen. Da im<br />
Vorlauf Cyclohexen enthalten ist entfärbt sich das Bromwasser bei dem Nachweis.<br />
7.1. Mechanismus <strong>der</strong> elektrophilen Addition (AE)<br />
(1) induzierter Dipol am Br2 Molekül,<br />
elektrophiler Angriff an Doppelbindung<br />
Diethylether<br />
- 5 -<br />
(2) bilden eines Bromium-Ions unter<br />
Dissoziation des Br2 Moleküls<br />
(5) bilden des Trans-1,2-Dibromcyclohexans (4) Angriff des Nucleophils (Br - ) von <strong>der</strong><br />
„Rückseite“<br />
8. Vergleich von SN1 und SN2<br />
Ob bei eine Reaktion nach SN1 o<strong>der</strong> SN2 abläuft hängt von mehreren Parametern ab.<br />
8.1. Stellung des elektrophilen Zentrums<br />
Das elektrophile Zentrum kann ein Methylkation o<strong>der</strong> ein primärer, sekundärer o<strong>der</strong> tertiärer<br />
Kohlenstoff sein. Die Stabilität des Carbeniumions nimmt vom Methylkation zum tertiären<br />
Kohlenstoff zu.<br />
Ein Methylkation und ein primärer Kohlenstoff reagieren also nach dem SN2 Mechanismus.<br />
Ein tertiärer Kohlenstoff wird hingegen nach dem SN1 Mechanismus reagieren. Beim Angriff<br />
an sekundäre Kohlenstoffe sind beide Reaktionen etwa gleich begünstigt. Hier entscheiden<br />
weitere Parameter darüber wonach die Reaktion verläuft.<br />
8.2. Sterische Hin<strong>der</strong>ung<br />
Eine sterische Hin<strong>der</strong>ung kann durch große Substituenden am elektrophilen Zentrum o<strong>der</strong><br />
auch am Nucleophil auftreten. Sterisch gehin<strong>der</strong>te Substituenden o<strong>der</strong> Nucleophile<br />
begünstigen einen SN1 Angriff.<br />
Bei <strong>der</strong> Reaktion ist we<strong>der</strong> das elektrophile Zentrum (sekundärer Kohlenstoff) noch das<br />
Nucleophil (Chlorid) sterisch gehin<strong>der</strong>t. Es besteht die Möglichkeit bei<strong>der</strong> Reaktionen.
Name: <strong>Gallian</strong> Studiengang: Chemische Technik (4T) Datum: 19.10.04<br />
Vorname: <strong>Christopher</strong> Matrikelnummer: 0321296 Seite: 6 von 6<br />
<strong>Präparat</strong>: 1 Produkt: Chlorcyclohexan durchgeführt: 12.10.04<br />
8.4. Das Lösungsmittel<br />
Lösungsmittel sind in drei Gruppen eingeteilt:<br />
- polar protische Lösungsmittel<br />
- polare Lösungsmittel<br />
- unpolare Lösungsmittel<br />
Polare und polar protische Lösungsmittel begünstigen die SN1 Reaktion, da sie Carbenium-<br />
Ionen und Abgangsgruppen stabilisieren.<br />
Unpolare Lösungsmittel begünstigen die SN2 Reaktion. Da sich in Unpolaren Lösungsmitteln<br />
keine Solvathüllen bilden, als polare Substanzen nicht in Lösung gehen kann die<br />
durchgeführte Reaktion nicht stattfinden, da sich sonst kein Zinkchlorid lösen würde.<br />
Bei <strong>der</strong> Reaktion wird Salzsäure eingesetzt die durch ihren Wasseranteil und Säurestärke ein<br />
polar protisches Lösungsmittel darstellt. Die Reaktion wird also mit Sicherheit nach SN1<br />
ablaufen.<br />
- 6 -