Nasschemisches Ätzen … - MicroChemicals GmbH
Nasschemisches Ätzen … - MicroChemicals GmbH
Nasschemisches Ätzen … - MicroChemicals GmbH
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
<strong>Nasschemisches</strong> <strong>Ätzen</strong> <strong>…</strong><br />
... chemische und physikalische Mechanismen<br />
Zuletzt aktualisiert am 25. 11. 2005<br />
Dieses Dokument vermittelt physikalisch-chemische Grundlagen zum nasschemischen <strong>Ätzen</strong> von<br />
Halbeitern, Metallen und Gläsern und stellt typische Ätzgemische und ihre Eigenheiten vor.<br />
n <strong>Ätzen</strong> und Lösen<br />
Während der Begriff ‚Lösen’ die Überwindung intermolekularer/-atomarer Wechselwirkung beschreibt, erfolgt<br />
beim <strong>Ätzen</strong> ein Brechen der chemischen Bindungen eines Festkörpers. Unabhängig davon erfolgt bei jedem<br />
nasschemischen Ätzvorgang auch ein Lösen der Ätzprodukte im Ätzmedium, welches zu diesem Zweck spezielle<br />
Additive enthalten kann.<br />
n Etwas Chemie und Physik zu Säuren und Basen<br />
Säuren und Basen: Oxidation und Reduktion<br />
Reines Wasser enthält über die Autoprotolyse H2O + H2O H3O + + OH - bei Raumtemperatur ca. 10 -7 mol<br />
H3O + und OH - pro Liter, was gemäß<br />
+<br />
pH = − log10<br />
[ H 3O<br />
]<br />
einem neutralen pH-Wert von 7 entspricht. Da die Autoprotolyse thermisch aktiviert ist, beträgt der pH-Wert<br />
von 100°C heißem Reinstwasser bereits ca. 6. Die folgende Tabelle gibt einige Beispiele für pH-Werte:<br />
Stoff HCl (20%) Magensaft Haushaltsessig H2O Seifenlauge KOH (1.4%) KOH (50%)<br />
pH-Wert -1 1-3 3 7 8-12 13 14.5<br />
Säuren sind Protonendonatoren und erhöhen in wässrigen Lösungen über die Abgabe (Dissoziation) von<br />
Protonen (Bsp. Salzsäure: HCl + H2O H3O + + Cl - ) die Konzentration der H3O + -Ionen, wodurch der pH-Wert<br />
sinkt. Ein Maß für die Stärke einer Säure ist der Dissoziationsgrad in wässrigen Lösungen, welcher über den<br />
pKs-Wert gemäß<br />
[ ] [ ]<br />
[ ] ⎟ +<br />
−<br />
⎛ H<br />
⎞<br />
3O<br />
⋅ dissoziierte<br />
Säure<br />
pK = − ⎜<br />
S log10<br />
⎝ undissoziierte<br />
Säure ⎠<br />
definiert ist. Sehr starke Säuren wie HClO4, HI, HCL oder H2SO4 sind als wässrige Lösung nahezu vollständig<br />
dissoziiert, den pKs-Wert einiger weniger starken Säuren bei Raumtemperatur zeigt folgende Tabelle:<br />
Starke Säuren <strong>…</strong><strong>…</strong><strong>…</strong> schwache Säuren<br />
Stoff HNO3 H3PO4 HSO4 - HF HNO2 CH3COOH H2CO3<br />
pKS-Wert -1.32 2.13 1.92 3.14 3.35 4.75 6.52<br />
Die starke Tendenz von H3O + , unter Aufnahme eines Elektrons Protonen abzugeben begründet die oxidierende<br />
Wirkung von Säuren.<br />
Basen als Protonenakzeptoren erhöhen in wässrigen Lösungen die Konzentration an OH - -Ionen. Nach dem<br />
Massenwirkungsgesetz bleibt bei gegebener Temperatur das Produkt [H3O + ]·[OH - ] konstant, so dass die H3O + -<br />
Konzentration sinkt, folglich der pH-Wert steigt. Analog zu Säuren lässt sich die Stärke einer Base in wässrigen<br />
Lösungen definieren über folgende Formel (mit einigen Zahlenbeispielen in der darauf folgenden Tabelle):<br />
−<br />
+<br />
[ OH ] [ dissoziierte<br />
Base ]<br />
[ ] ⎟ ⎛ ⋅<br />
⎞<br />
= −log<br />
⎜<br />
.<br />
⎝ undissoziierte<br />
Base ⎠<br />
pK B 10<br />
Starke Basen <strong>…</strong><strong>…</strong><strong>…</strong> schwache Basen<br />
Stoff NaOH KOH S 2- PO4 3- NH3 HS - F -<br />
pKB-Wert 0.2 0.5 1.0 1.67 4.75 7.08 10.86<br />
Die Tendenz der OH - -Ionen, ein Elektron abzugeben begründet die reduzierende Wirkung von Basen.<br />
Chemische Puffer sind Substanzen, welche den pH-Wert einer Lösung trotz der Zugabe oder Entnahme von<br />
H3O + - oder OH - Ionen (z.B. durch deren Verbrauch beim <strong>Ätzen</strong> oder über Verunreinigungen) auf einem vorgegebenen<br />
Wert annähernd konstant halten. Sie erfüllen diese Aufgabe, indem sie H3O + - und OH - -Ionen binden<br />
(bzw. über die Freisetzung derer konjugierten Säure/Base neutralisieren), wenn deren Konzentration steigt,<br />
und sie freisetzen, wenn sie sinkt. Pufferlösungen sind schwache (d.h. unvollständig dissoziierte) Säuren/Basen<br />
und deren konjugierte Basen/Säuren (bzw. Salze).<br />
Komplexbildung<br />
Zur Unterdrückung des den Wiedereinbaus bereits geätzter Teilchen in das zu ätzende Medium kann über entsprechende<br />
Additive in der Ätzlösung die Bildung sog. Komplexe mit den geätzten Teilchen ermöglicht wer-<br />
Positivlacke Negativlacke Umkehrlacke Entwickler<br />
Verdünner Lösemittel Ätzchemikalien Prozesschemikalien<br />
<strong>MicroChemicals</strong> <strong>GmbH</strong> www.microchemicals.com tech@microchemicals.com S. 1
den. Ein Komplex ist eine Struktur, bei der ein Zentralatom (meist ein Metallion = das geätzte Element), das<br />
in seiner Elektronenkonfiguration Lücken aufweist, von einem oder mehreren Molekülen oder Ionen (den Liganden)<br />
umgeben ist, die jeweils mindestens ein freies Elektronenpaar für die Bindung zur Verfügung stellen.<br />
Ein Beispiel ist die Bildung von Tetrachloroaurat beim <strong>Ätzen</strong> von Gold in Königswasser.<br />
Lösen, Diffusion und Konvektion<br />
Um eine Anlagerung (u.U. Passivierung) bereits geätzten Materials– als Ion oder Komplex – auf der Oberfläche<br />
des zu ätzenden Stoffes zu verhindern, muss die Ätzlösung eine ausreichende Löslichkeit für das geätzte Medium<br />
aufweisen. Mehr zu diesem Thema findet sich in unserem Infoblatt Lösemittel, erhältlich auf Anfrage.<br />
Um frische Ätzlösung an die Oberfläche des zu ätzenden Mediums gelangen zu lassen, als auch die Wiederanlagerung<br />
des bereits geätzten Materials zu unterdrücken muss dieses so rasch wie möglich von der zu ätzenden<br />
Oberfläche abtransportiert werden. Hierfür stehen zwei Mechanismen zur Verfügung:<br />
Diffusion: Bei Raumtemperatur besitzen Atome thermische Geschwindigkeiten von mehreren 100 m/s. Durch<br />
die in Flüssigkeiten geringe mittlere freie Weglänge resultiert daraus jedoch eine ungerichtete Zitterbewegung,<br />
welche Konzentrationsgradienten nur sehr langsam abbaut.<br />
Konvektion: Entweder durch Gasbildung beim <strong>Ätzen</strong>, Wärmeentwicklung exothermer Ätzreaktionen oder äußeren<br />
Einfluss ist Konvektion eine Voraussetzung dafür, dass der geätzte Stoff rasch auch über makroskopische<br />
Distanzen abtransportiert wird und eine räumlich und zeitlich homogene Ätzrate erzielt wird.<br />
n Metalle und Edelmetalle beim <strong>Ätzen</strong><br />
Energie, Entropie und Enthalpie<br />
Während z.B. beim <strong>Ätzen</strong> von SiO2 weniger die Protonenabgabe der (mit einem pKS-Wert >3 nicht sehr starken)<br />
Flusssäure, als vielmehr die F - -Ionen die Hauptrolle beim <strong>Ätzen</strong> spielen, ist das <strong>Ätzen</strong> von Metallen im<br />
Wesentlichen eine Oxidation des Metalls über vom H3O + abgegebene Protonen, welche dabei gemäß:<br />
Metall + H + Metall + + H<br />
zu H reduziert werden. Würde man nur energetische Aspekte des <strong>Ätzen</strong>s beachten, könnten nur Metalle geätzt<br />
werden, bei denen obige Reaktion exotherm (Änderung der inneren Energie ΔU < 0) abläuft, d.h. Metalle mit<br />
einem Normalpotential E 0 größer als das des Wasserstoffs (welches willkürlich auf Null festgelegt wurde). Zu<br />
diesen Metallen zählen alle unedlen Metalle.<br />
Dass auch Edelmetalle mit einem E 0 >0 (Beispiel: das leicht ätzbare Kupfer mit E 0 = +0.34) geätzt werden<br />
können liegt daran, dass – wie jede andere Reaktion auch - eine Ätzreaktion stattfindet, wenn die Änderung<br />
der freien Enthalpie ΔF=ΔU-T·ΔS negativ ist, d.h. das Produkt aus Temperatur T und Entropieänderung ΔS<br />
positiver als die Änderung der inneren Energie. Ein positives ΔS ist z.B. durch die Zunahme der Zahl der<br />
Translations- und räumlichen Freiheitsgrade durch den Übergang vom Festkörper in die Lösung oder der gelösten<br />
Stoffe in die Gasphase (H2-Bildung) gegeben.<br />
Elektronenschalen und Normalpotential<br />
Sowohl die sehr reaktiven Alkalimetalle (Li, K, Na<strong>…</strong>) als auch viele der inerten Edelmetalle (Au, Ag, Pt<strong>…</strong>) besitzen<br />
ein s-Orbital mit einem ungepaartes Elektron. Während dieses bei Alkalimetallen sehr leicht an Reaktionspartner<br />
abgegeben werden kann ( Oxidation), ist es bei Edelmetallen vergleichsweise stark gebunden (positives<br />
Normalpotential).<br />
Dies liegt u.a. daran, dass ein Edelmetallatom neben einem (im Falle von Au, Ag, Pt<strong>…</strong>) unvollständig gefüllten<br />
s-Orbital der Hauptquantenzahl n (‚Schale’) ein vollständig gefülltes d-Orbital der Hauptquantenzahl n-1<br />
besitzt (Beispiel Elektronenkonfiguration Gold: [Xe]4f 14 5d 10 6s 1 ). Dieses d-Orbital ragt teilweise über das s-<br />
Orbital hinaus und schirmt es räumlich gegen mögliche Reaktionspartner ab. Hinzu kommt, dass der Atomkern<br />
aus Sicht des ungepaarten s-Elektrons elektrostatisch nur durch den weiter innen liegenden Anteil des d-<br />
Orbitals abgeschirmt ist und das s-Elektron somit stärker an den Kern gebunden wird.<br />
Manche Edelmetalle besitzen keine ungepaarten Elektronen in ihrer Hülle. Das äußerste s-Orbital ist entweder<br />
leer (wie bei z.B. Palladium) oder vollständig mit einem Elektronenpaar gefüllt (z.B. bei Iridium), was die chemische<br />
Stabilität weiter erhöht. So löst sich Iridium erst in 100°C heißem Königswasser.<br />
n <strong>Ätzen</strong> von Aluminium<br />
Typische Al-<strong>Ätzen</strong> bestehen aus 1-5% HNO3* (Oxidation des Al), 65-<br />
75% H3PO4* (lösen des Al-Oxids), 5-10% Essigsäure* (zur Benetzung)<br />
und H2O zum Einstellen der Ätzrate bei gegebener Temperatur.<br />
Das <strong>Ätzen</strong> von Al ist stark exotherm. Ein (unvermeidliches, da isotroper<br />
Ätzvorgang) Unterätzen der Lackmaske führt ohne ausreichende mechanische<br />
Umwälzung der Ätze über lokale Erwärmung (Abb. rechts) der Ätze<br />
an diesen Stellen zu einem selbstverstärkten Unterätzen.<br />
Positivlacke Negativlacke Umkehrlacke Entwickler<br />
Verdünner Lösemittel Ätzchemikalien Prozesschemikalien<br />
<strong>MicroChemicals</strong> <strong>GmbH</strong> www.microchemicals.com tech@microchemicals.com S. 2
Starke H2-Bildung (Bläschen) verringert die Homogenität des Ätzvorgangs.<br />
Der eigentliche Al-Ätzvorgang startet erst, wenn durch das H3PO4<br />
die auf Al-Oberflächen grundsätzlich vorhandenen, wenigen nm Aluminiumoxid<br />
aufgelöst wurden. Aus diesem Grund wirkt sich auch die Fotolackprozessierung<br />
auf einen nachfolgenden Al-Ätzschritt aus: Alkalische<br />
Entwicklerlösungen greifen die Al-Oxidschicht verstärkt dort an,<br />
wo der Lack am ehesten durchentwickelt ist (z.B. an dünneren Lackstellen,<br />
an den Rändern entwickelter Strukturen oder an entwickelten Strukturen<br />
zunehmender Größe). Je nach Grad der Überentwicklung und der<br />
Wartezeit zwischen Entwicklung und Al-<strong>Ätzen</strong> kann dies dann zu einem<br />
räumlich inhomogenen Al-Ätzstart und damit zu unterschiedlich tief geätztem<br />
Al führen.<br />
HNO3* = 70% HNO3 in H2O H3PO4* = 85% H3PO4 in H2O CH3COOH* = 99% CH3COOH in H2O<br />
n <strong>Ätzen</strong> von Chrom<br />
n <strong>Ätzen</strong> von Gold<br />
Chromätzen sind meist Lösungen aus Perchlorsäure<br />
(HClO4, Schema des undissoziierten Moleküls rechts) und<br />
Ammoniumcernitrat (NH4)2[Ce(NO3)6].<br />
Perchlorsäure ist als äußerst starke Säure in wässriger<br />
Lösung vollständig dissoziiert (pKs-Wert < -8), Ammoniumcernitrat<br />
wie auch HClO4 ein sehr starkes Oxidationsmittel.<br />
Goldätzen sind üblicherweise Gemische aus Salpetersäure und Salzsäure<br />
(im Mischungsverhältnis 1:3 auch Königswasser genannt).<br />
Die starke oxidative Wirkung dieses Gemisches beruht auf der Bildung<br />
von Nitrosylchlorid (NOCl) im Gemisch über<br />
HNO3 + 3HCl NOCl + 2Cl + 2H2O,<br />
während ebenfalls gebildete freie Chloratome das gelöste Gold als Chloro-Komplex<br />
(Tetrachloroaurat) in der Lösung halten, damit den Wiedereinbau<br />
in das Gitter verhindern und so den Ätzvorgang mit einer Rate<br />
von einigen 10 μm/Minute selbst erst ermöglichen.<br />
Eine Alternative zu Königswasser für das <strong>Ätzen</strong> von Gold bildet eine wässrige KI/I2 Lösung, welche im Verhältnis<br />
KI:I2:H2O = 4:1:40 ca 1 μm/Minute ätzt.<br />
n <strong>Ätzen</strong> von Silber<br />
Silber kristallisiert wie Gold kubisch flächenzentriert. Die entsprechenden<br />
Ätzlösungen benötigen eine Komponente welche das Silber oxidiert,<br />
und eine weitere Komponente zum <strong>Ätzen</strong>/Lösen des Silberoxids:<br />
Neben der im Abschnitt ‚<strong>Ätzen</strong> von Gold’ beschriebenen KI/I2/H2O Ätzlösung<br />
wird Silber auch von NH4OH:H2O2:Methanol = 1:1:4 (wobei mit<br />
NH4OH und H2O2 jeweils deren 30%ige Lösungen gemeint ist) geätzt.<br />
Das giftige Methanol ist keine zwingende Voraussetzung und kann weggelassen<br />
bzw. durch H2O ersetzt werden.<br />
Ein weiteres Ätzgemisch für Silber ist eine wässrige HNO3:HCl:H2O = 1:1:1 Lösung (HNO3= 70% HNO3 in H2O,<br />
HCl = 37% HCl in H2O).<br />
n <strong>Ätzen</strong> von Titan<br />
20 24 28 32 36 40<br />
Ätzemperatur (°C)<br />
Titan, welches in der Mikrostrukturierung u.a. als Haftvermittler für darüber<br />
aufgewachsene Metallschichten Verwendung findet, kristallisiert in<br />
der hexagonal dichtesten Kugelpackung und bildet an Luft eine äußerst<br />
stabile Oxidschicht. Diese wird nur durch z.B. HF angegriffen wird, welches<br />
deshalb ein Bestandteil typischer Titanätzen darstellt. Zur Oxidation<br />
der darunter liegenden Schichten eignet sich als zweiter Bestandteil<br />
H2O2.<br />
In einem Mischungsverhältnis HF (50%ig) : H2O2 (30%ig) : H2O =<br />
1:1:20 lässt sich Titan bei Raumtemperatur mit etwa 1 μm/Minute ätzen.<br />
Positivlacke Negativlacke Umkehrlacke Entwickler<br />
Verdünner Lösemittel Ätzchemikalien Prozesschemikalien<br />
<strong>MicroChemicals</strong> <strong>GmbH</strong> www.microchemicals.com tech@microchemicals.com S. 3<br />
Ätzrate(10 3 Å/min)<br />
3.5<br />
3.0<br />
2.5<br />
2.0<br />
1.5<br />
1.0<br />
0.5<br />
74 ml H 3 PO 4 *<br />
2.5 ml HNO 3 *<br />
23.5 ml H 2 O
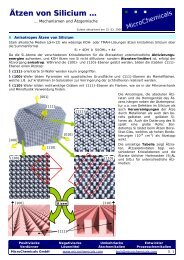
n Anisotropes <strong>Ätzen</strong> von Silicium<br />
[100]<br />
{100}<br />
[001]<br />
[111]<br />
[110]<br />
[010]<br />
[100] <strong>Ätzen</strong><br />
[110]<br />
{111}<br />
{111}<br />
{110}<br />
Stark alkalische Medien (pH>12) wie<br />
wässrige KOH- oder TMAH-Lösungen ätzen<br />
kristallines Silicium über die Summenformel<br />
Si + 4OH - Si(OH)4 + 4e -<br />
Da die Si-Atome der verschiedenen Kristallebenen<br />
für die Ätzreaktion unterschiedliche<br />
Aktivierungsenergien aufweisen,<br />
und KOH <strong>Ätzen</strong> von Si nicht diffusions-<br />
sondern Ätzraten-limitiert ist,<br />
erfolgt der Ätzvorgang anisotrop: Während<br />
die {100}- und {110}-Ebenen geätzt<br />
werden, bilden die stabilen {111}-<br />
Ebenen einen Ätzstop:<br />
§ (111)-orientierte Si-Wafer werden<br />
kaum angegriffen.<br />
§ (100)-Wafer bilden Pyramiden mit<br />
quadratischer Grundfläche und {111}-<br />
Ebenen als Mantelflächen, welche z.B.<br />
auf kristallinen Si-Solarzellen zur Verringerung<br />
der Lichtreflexion realisiert<br />
werden.<br />
§ (110)-Wafer bilden rechtwinklige<br />
Gräben mit {111}-Ebenen als Flanken,<br />
wie sie in der Mikromechanik und<br />
Mikrofluidik Verwendung finden.<br />
Die Anisotropie, die absoluten Ätzraten<br />
und die Homogenität des <strong>Ätzen</strong>s hängen<br />
neben der Ätztemperatur u.a. von Defekten<br />
im Silicium als auch Verunreinigungen<br />
der Ätze durch Metallionen als<br />
auch den bereits geätzten und gelösten<br />
Si-Ionen ab. Auch die Dotierung des Si<br />
spielt eine große Rolle: Bor-dotiertes Si<br />
bildet beim <strong>Ätzen</strong> Borsilikat-Glas, welches<br />
ab hohen Bordotierungen (10 19 cm -<br />
3 ) als Ätzstopp wirkt.<br />
Die folgende Tabelle zeigt Ätzraten, Ätzselektivitäten bzgl. verschiedener Kristallebenen und die Ätzrate üblicher<br />
Hartmasken (Si3N4 und SiO2) für unterschiedliche Ätzmedien:<br />
Ätzmedium<br />
KOH<br />
(44%, 85°C)<br />
TMAH<br />
(25%, 80°C)<br />
EDP<br />
(115°C)<br />
Ätzratenverhältnis Ätzrate (absolut)<br />
(100)/(111) (110)/(111) (100) Si3N4 SiO2<br />
300 600 1.4 μm/min
n Isotropes <strong>Ätzen</strong> von Silicium und SiO2 mit HF/HNO3<br />
Ätzmechanismus, Ätzraten und Selektivität<br />
Der grundlegende chemische Ätzmechanismus beim isotropen <strong>Ätzen</strong> von Si (Schritte 1-4) und SiO2 (nur<br />
Schritt 4) mit HF/HNO3-Gemischen gestaltet sich wie folgt:<br />
(1) Bildung von NO2 (HNO2 stets in Spuren in HNO3): HNO2 + HNO3 2NO2 + H2O<br />
(2) Oxidation von Silizium durch NO2: 2NO2 + Si Si 2+ + 2NO2 -<br />
(3) Bildung von SiO2: Si 2+ + 2(OH) - SiO2 + H2<br />
(4) <strong>Ätzen</strong> von SiO2: SiO2 + 6HF H2SiF6 + 2H2O<br />
Demnach dient HNO3 zur Oxidierung des Si zu SiO2,<br />
und HF zu dessen <strong>Ätzen</strong>.<br />
Wie das Ätzdreieck (rechts) zeigt, fördern hohe<br />
HF:HNO3-Verhältnisse über den Oxidationsschritt<br />
(1)-(3) das Raten-limitierte <strong>Ätzen</strong> von Si mit stark<br />
temperaturabhängiger Ätzrate.<br />
Geringe HF:HNO3-Verhältnisse fördern diffusionslimitiertes<br />
<strong>Ätzen</strong> geringerer Temperaturabhängigkeit<br />
über Schritt (4). HNO3-freie HF-<strong>Ätzen</strong> greifen Silizium<br />
nicht an.<br />
Die Ätzrate von SiO2 ist durch die HF-Konzentration<br />
bestimmt, da hier die Oxidation (1)-(3) keine Rolle<br />
spielt. Verglichen mit thermischem Oxid zeigt abgeschiedenes<br />
(z.B. CVD) SiO2 aufgrund seiner Porosität<br />
eine höhere Ätzrate; ‚nasses Oxid’ aus gleichem Grund<br />
eine etwas höhere Ätzrate als ‚trockenes Oxid’.<br />
Eine genaue Kontrolle der Ätzrate erfordert Temperaturgenauigkeiten<br />
von ± 0.5°C.<br />
Si Ätzrate<br />
[HF] Temperaturabhängigkeit<br />
der Ätzrate<br />
nimmt zu<br />
[H2O]+ [CH3COOH] [HNO3]<br />
Selektivität<br />
zu SiO2<br />
nimmt<br />
zu<br />
Die Verwendung von Essigsäure als Verdünner verbessert<br />
die Benetzung der hydrophoben Si-Oberfläche und erhöht so die Ätzrate bei verbesserter Homogenität.<br />
Dotiertes (n- und p-Typ) Si sowie Phosphor-dotiertes SiO2 ätzen schneller als undotiertes Si oder SiO2.<br />
Gepufferte Flusssäure<br />
<strong>Ätzen</strong> von Si- und SiO2 verbraucht über die Reaktion SiO2 + 4HF → SiF4 + 2H2O F - -Ionen. Mit Ammoniumfluorid<br />
gepufferte HF (BHF = NH4F + H2O + HF) bewirkt:<br />
§ Die Aufrechterhaltung der Konzentration freier F — -Ionen über NH4F → HF + NH3, für eine konstante und<br />
kontrollierbare Ätzrate sowie homogenes <strong>Ätzen</strong><br />
§ Eine Erhöhung der Ätzrate (Faktor ≈ 1.5-5.0) über hochreaktive HF2 - -Ionen<br />
§ Ein Anstieg im pH-Wert (→ verringerte Neigung zu Unterätzen u. Lackablösung)<br />
! Trotz der höheren Reaktivität hat stark gepufferte Flusssäure einen pH-Wert von bis zu 7 und kann über<br />
chemische Indikatoren u.U. nicht nachgewiesen werden !<br />
n <strong>Ätzen</strong> von Gläsern<br />
Gläser unterschiedlicher Zusammensetzung zeigen eine starke Abhängigkeit ihrer Ätzrate von Zusätzen in<br />
verwendeten HF-haltigen <strong>Ätzen</strong>. Solche Additive (z.B. HCl, HNO3) lösen beim Glasätzen gebildete, in reinem<br />
HF inerte (d.h. in HF als Ätzstopp wirksame) Oberflächenschichten und erlauben so eine homogen hohe Ätzrate<br />
ohne die (für die Lackschicht kritische) Notwendigkeit, die HF-Konzentration zu erhöhen:<br />
Ätzgemisch Ätzrate / Bemerkungen<br />
Borosilikat Glas<br />
HF*: HNO3*: H2O = 1:100:100<br />
HF*: HNO3*: H2O = 4.4:100:100<br />
300 Å/min (9 mol% B2O3), 50 Å/min (SiO2)<br />
750 Å/min(9 mol% B2O3), 135 Å/min (SiO2)<br />
Phosphorsilikat 28ml HF* + 113g NH4F + 170ml H2O 5500 Å/min für 8 mol% P2O5<br />
Glas HF*: HNO3*: H2O = 15:10:300 34000 Å/min (16 mol% P2O5), 110 Å/min (SiO2)<br />
Bleiglas<br />
HF*: HCl*: H2O = 18:46:75<br />
HF*: HCl*: CH3COOH* = 25:46:75<br />
ca. 70000 Å/min<br />
ca. 70000 Å/min<br />
HCl*=<br />
HNO3*=<br />
HF*=<br />
CH3COOH*=<br />
37% HCl in H2O<br />
70% HNO3 in H2O<br />
49% HF in H2O<br />
99% CH3COOH in H2O<br />
Positivlacke Negativlacke Umkehrlacke Entwickler<br />
Verdünner Lösemittel Ätzchemikalien Prozesschemikalien<br />
<strong>MicroChemicals</strong> <strong>GmbH</strong> www.microchemicals.com tech@microchemicals.com S. 5
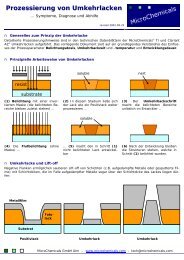
n Lackablösung (v.a. kleiner/schmaler Strukturen) bei nasschemischen Ätzprozessen<br />
Lösen sich bei nasschemischen Ätzprozessen zunächst (oder ausschließlich) kleine/schmale Lackstrukturen ab,<br />
deutet dies auf ein Unterätzen – beginnend von den frei entwickelten Bereichen – hin. Evtl. unterstützt von<br />
höheren Temperaturen oder/und Gasbildung, heben sich Lackstrukturen durch<br />
die Verringerung ihrer Kontaktfläche zum Substrat von diesem ab.<br />
Fotolack HF-Ätze<br />
Substrat<br />
Bei isotropen <strong>Ätzen</strong> lässt sich das Ausmaß des Unterätzens nicht beliebig verringern,<br />
jedoch die (verbliebene) Haftung der Lackstrukturen über die in diesem<br />
Dokument beschriebenen Hinweise.<br />
n (großflächige) Lackablösung bei nasschemischen (Ätz-)Prozessen<br />
Nasschemische (Ätz-)medien (v.a. HF) diffundieren in den Lack und können – entweder während des Prozesses<br />
oder beim anschließenden Spülvorgang – über zwei Mechanismen zur großflächigen Lackablösung führen:<br />
HF-Ätze<br />
F<br />
§ Durch das Eindiffundieren des Mediums<br />
quellen die Lackstrukturen auf<br />
Fotolack<br />
§ Gelangt das Medium bis zum Substrat und<br />
greift – wie im Falle HF auf SiO2 oder Glas –<br />
Substrat<br />
dieses großflächig unter der Lackschicht an,<br />
hebt sich die Lackschicht ab (Schema links).<br />
Beide Mechanismen lassen sich - neben einer<br />
mildern.<br />
angepassten (Ätz-)lösung - über eine größere<br />
Lackschichtdicke (Schema rechts) deutlich<br />
- Ionen<br />
Fotolack<br />
Substrat<br />
Zu dünne Fotolackschicht<br />
HF-Ätze<br />
F - Ionen<br />
Ausreichend dicker Fotolack<br />
Beidseitig metallisierte Substrate (z.B. Ag & Al) bilden in wässrigen Lösungen ein Galvanisches Element.<br />
Auf der einen Seite kann sich H2 bilden, welcher eine darüber liegende Lackschicht abhebt. In diesem Fall hilft<br />
eine geschlossene Schutzlackschicht auf der jeweils anderen Seite des Substrats.<br />
n <strong>Ätzen</strong> von Metallen (Übersicht)<br />
Ätzgemisch Ätzrate / Bemerkungen<br />
HCl*: Glyzerin = 1:1 800 Å/min nach Depassivierung<br />
Cr HCl*: CeSO4 (gesättigt) = 1:9 800 Å/min, nach Depassivierung<br />
Ce(NH4)2(NO3)6 + CH3COOH in 1L H2O 1000 Å/min (zuerst CH3COOH in 1L H2O lösen!)<br />
H3PO4*: HNO3*: CH3COOH* : H2O = 5:2:4:150 5000 Å/min<br />
Mo 11g K3Fe(CN)6 + 10g KOH in 150ml H2O<br />
HCl*: H2O2*: H2O = 1:1:1<br />
10000 Å/min<br />
W 34g KH2PO4*+ 13.4g KOH + 33g K3Fe(CN)6 in 1L H2O 1600 Å/min<br />
NH4OH*: H2O2* : CH3OH = 1:1:4<br />
Ag HCl*: H2O2*: H2O = 1:1:1<br />
KI : I2 : H2O = 4:1:40<br />
3600 Å/min, sofortiges Spülen mit H2O nach d. <strong>Ätzen</strong><br />
HCl*: HNO3 *= 3:1<br />
Au<br />
KI : I2 : H2O = 4:1:40<br />
‚Königswasser’, 25-50 μm/min<br />
0.5-1 μm/min<br />
HCl*: HNO3* = 3:1<br />
Pt<br />
HCl*: HNO3*: H2O = 7:1:8<br />
‚Königswasser’, 20 μm/min<br />
400-500 Å/min bei 85°C<br />
HCl*: HNO3*: CH3COOH* = 1:10:10 1000 Å/min<br />
Pd HCl*: HNO3* = 3:1 ‚Königswasser’<br />
KI : I2 : H2O = 4:1:40 1 μm/min<br />
150g Na2S2O8 in 1L H2O<br />
Cu<br />
1 μm/min bei 45°C, selektiv gegenüber Ni, falls Ätze Fe-frei<br />
H3PO4*:HNO3*:CH3COOH*:H2O = 3:3:1:1<br />
Ni<br />
H2O2*: HF*: H2O = 1:1:20<br />
65 nm/min bei 20°C, Kontakt mit Luft (O2) alle 15 Sekunden<br />
Ti H2O2*: HF*: H2O = 1:1:20 8800 Å/min bei 20°C<br />
Sb H3PO4*: HNO3*: CH3COOH*: H2O = 3:3:1:1 Kontakt mit Luft (O2) alle 15 Sekunden<br />
HCl* = 37% HCl in H2O HNO3* = 70% HNO3 in H2O H2SO4* = 98% H2SO4 in H2O<br />
HF* = 49% HF in H2O HClO4* = 70% HClO4 in H2O H3PO4* = 85% H3PO4 in H2O<br />
NH4OH* = 29% NH3 in H2O H2O2* = 30% H2O2 in H2O CH3COOH* = 99% CH3COOH in H2O<br />
Positivlacke Negativlacke Umkehrlacke Entwickler<br />
Verdünner Lösemittel Ätzchemikalien Prozesschemikalien<br />
<strong>MicroChemicals</strong> <strong>GmbH</strong> www.microchemicals.com tech@microchemicals.com S. 6
n <strong>Ätzen</strong> von III/V-Halbleitern (Übersicht)<br />
Material<br />
Ätze<br />
HCl* : H3PO4* : H2O<br />
H3PO4* : H2O2* : H2O<br />
H2SO4* : H2O2* : H2O<br />
C6H8O7 : H2O2*: H2O<br />
HCL* : HNO3* : H2O<br />
HNO3* : H2SO4* :H2O<br />
HCL* : *H2O2 : H2O<br />
HCL* : H2O<br />
BHF : H2O<br />
GaAs InP InGaAs InGaAsP GaInP GaAsP AlGaP AlGaAs AlInP InAlAs InGaAlAs<br />
ätzt abhängig von Zusammensetzung materialselektiv (Ätzstopp)<br />
HCl* = 37% HCl in H2O HNO3* = 70% HNO3 in H2O H2SO4* = 98% H2SO4 in H2O<br />
HF* = 49% HF in H2O HClO4* = 70% HClO4 in H2O H3PO4* = 85% H3PO4 in H2O<br />
NH4OH* = 29% NH3 in H2O H2O2* = 30% H2O2 in H2O CH3COOH* = 99% CH3COOH in H2O<br />
n Stabilität von Ätzmedien gegenüber Fotolackmasken<br />
Die folgenden Angaben beziehen sich auf Novolak basierte nicht-quervernetzende Positiv- und Umkehrlacke,<br />
sowie quervernetzende Negativlacke der AZ ® nLOF 2000 Serie.<br />
§ Nahezu alle organischen Lösemittel lösen Positiv- und Umkehrlacke in kurzer Zeit auf. Lediglich bei ausreichend<br />
hohen Temperaturen (>150°C) quervernetzte Negativlacke der AZ ® nLOF 2000 Serie sind genenüber<br />
organischen Lösemitteln in Grenzen stabil.<br />
§ HCl ist ein gegenüber Fotolacken sehr unkritisches Ätzmedium<br />
§ HF ist v.a. wegen seiner Permeabilität in/durch Fotolackschichten problematisch, lässt sich jedoch bei ausreichend<br />
dicken Fotolackschichten für viele Ätzprozesse problemlos einsetzen.<br />
§ Stark oxidierende Säuren wie HNO3 oder H2SO4, wie auch H2O2 greifen Fotolack stark an. Dennoch ist die<br />
Stabilität der Lackschicht bei richtiger Prozessierung (Haftung, Softbake) ausreichend für viele Ätzprozesse.<br />
n Vorsichtsmassnahmen im Umgang mit ausgewählten Ätzmedien<br />
HCl/H2O2/H2O Gemische reagieren beim/nach dem Durchmischen stark exotherm und können bei unzureichender<br />
Verdünnung mit H2O zur explosiven Zersetzung des H2O2 führen.<br />
H2SO4 reagiert stark exotherm mit H2O und sollte stets zum Verdünner (H2O, schwächere Säuren) gegeben<br />
werden, nie umgekehrt.<br />
HF verursacht bei Hautkontakt nicht ‚nur’ äußerst schmerzhafte und schwer heilende Verätzungen, sondern<br />
kann durch seine hohe Toxizität bei entsprechend hoher Konzentration bereits ab ca. Handtellergroßen Verätzungen<br />
zum Tod führen.<br />
n Gewährleistungsausschluss<br />
Alle in diesem Informationsblatt enthaltenen Zahlen und Beschreibungen sind nach bestem Wissen und Gewissen<br />
zusammengestellt. Dennoch können wir keine Garantie für die Korrektheit dieser Angaben übernehmen.<br />
Insbesondere bezüglich der Rezepturen für chemische (Ätz-)Prozesse übernehmen wir keine Gewährleistung<br />
für die korrekte Angabe der Bestandteile, der Mischverhältnisse, der Herstellung der Ansätze und deren Anwendung.<br />
Die sichere Reihenfolge des Mischens von Bestandteilen einer Rezeptur entspricht üblicherweise<br />
nicht der Reihenfolge ihrer Auflistung in Tabellen etc. Normalerweise werden Säuren in den Verdünner (z.B.<br />
Wasser) gegeben, stärkere Säuren in schwächere, und oxidierende Medien zuletzt zugegeben.<br />
Wir garantieren nicht für die Richtigkeit oder Vollständigkeit von Hinweisen auf (u.a. gesundheitliche, arbeitssicherheitstechnische)<br />
Gefahren, die sich bei der Anwendung der in diesem Informationsblatt beschriebenen<br />
Chemikalien ergeben (können).<br />
Grundsätzlich ist jeder Mitarbeiter dazu angehalten, sich im Zweifelsfall in geeigneter Fachlektüre über die beschriebenen<br />
Chemikalien und ihre Auswirkungen vorab ausreichend zu informieren, um Schäden an Personen<br />
und Material auszuschließen.<br />
Positivlacke Negativlacke Umkehrlacke Entwickler<br />
Verdünner Lösemittel Ätzchemikalien Prozesschemikalien<br />
<strong>MicroChemicals</strong> <strong>GmbH</strong> www.microchemicals.com tech@microchemicals.com S. 7