mito-extra® - medac GmbH
mito-extra® - medac GmbH
mito-extra® - medac GmbH
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
<strong>mito</strong>-<strong>extra®</strong><br />
<strong>mito</strong>-<strong>medac</strong> ®<br />
Basisdokumentation<br />
<strong>medac</strong>
Pharmazeutischer Unternehmer:<br />
<strong>medac</strong><br />
Gesellschaft für klinische<br />
Spezialpräparate mbH<br />
Fehlandtstraße 3<br />
D-20354 Hamburg<br />
Stand der Information:<br />
Februar 2006
INHALTSVERZEICHNIS<br />
1 <strong>mito</strong>-extra ® / <strong>mito</strong>-<strong>medac</strong> ® Auf einen Blick ............................ 03<br />
2 Entwicklungsgeschichte ............................................................ 04<br />
3 Produktbeschreibung .................................................................. 05<br />
3.1 Anwendungsgebiete ................................................................... 05<br />
3.2 Dosierung ................................................................................... 05<br />
3.3 Nebenwirkungen der intravesikalen Anwendung ......................... 05<br />
3.4 Wechselwirkungen mit anderen Mitteln ....................................... 07<br />
3.5 Gegenanzeigen für die intravesikalen Therapie ............................ 07<br />
3.6 Art und Dauer der Anwendung ................................................... 07<br />
3.7 Handhabung und Stabilität ......................................................... 08<br />
3.7.1 Das Geschlossene System / Sicherheitsaspekte .............. 09<br />
3.7.2 Applikationsanleitung von <strong>mito</strong>-extra ®<br />
und <strong>mito</strong>-<strong>medac</strong> ® ........................................................ 12<br />
4 Wirkmachnismus ...................................................................... 14<br />
5 Chemisch-physikalische Eigenschaften ............................... 17<br />
Bezeichnung des Arzneimittels ................................................. 17<br />
Chemische Bezeichnung ......................................................... 17<br />
Internationaler Freiname (INN) .................................................. 17<br />
Strukturformel ......................................................................... 17<br />
Summenformel ....................................................................... 17<br />
Molekulargewicht .................................................................... 17<br />
Beschreibung ......................................................................... 17<br />
Löslichkeit .............................................................................. 17<br />
6 Pharmakologie .......................................................................... 18<br />
6.1 Pharmakologische Eigenschaften ............................................. 18<br />
6.2 Pharmakokinetik ...................................................................... 18<br />
6.3 Toxikologie .............................................................................. 19<br />
7 Klassifikation von oberflächlichen Harnblasentumoren<br />
und risikoadaptierte Therapie ................................................ 19<br />
7.1 Neue WHO-Klassifikation ......................................................... 20<br />
8 Therapie des oberflächlichen Harnblasenkarzinoms<br />
mit Mitomycin ........................................................................... 21<br />
8.1 Frühinstallation ........................................................................ 21<br />
8.1.1 Worauf muss bei der Frühinstillation geachtet werden? .... 27<br />
8.2 Initialtherapie ........................................................................... 28<br />
8.2.1 Warum 40 mg Mitomycin? ............................................. 29<br />
8.3 Erhaltungstherapie .................................................................. 30<br />
8.3.1 Wie lange soll die Erhaltungstherapie dauern? ................. 32<br />
9 Vergleich mit anderen Chemotherapeutika ......................... 35<br />
9.1 Mitomycin vs. Doxorubicin ....................................................... 35<br />
9.2 Mitomycin vs. Epirubicin .......................................................... 37<br />
10 Mitomycin vs. Immuntherapeutika ........................................ 37<br />
10.1 Mitomycin vs. BCG ............................................................... 37<br />
10.2 Mitomycin vs. INTERFERON .................................................. 46<br />
10.3 Mitomycin vs. KLH ................................................................ 47<br />
11 Kombinationstherapien ........................................................... 47<br />
11.1 Sequenzielle Therapie ............................................................ 47<br />
11.2 Mitomycin und Hyperthermie ................................................. 50<br />
11.3 Mitomycin und EMDA ............................................................ 50<br />
12 Therapie von Tumoren des oberen Harntrakts ................... 52<br />
13 Zusammenfassung ................................................................... 53<br />
14 Stichwortverzeichnis ............................................................... 54<br />
15 Literaturverzeichnis ................................................................. 57<br />
1
1 <strong>mito</strong>-extra ® / <strong>mito</strong>-<strong>medac</strong> ® AUF EINEN BLICK<br />
Wirkstoff: MITOMYCIN<br />
Substanzklasse: Chemotherapeutikum zur intravesikalen<br />
(lokalen) Therapie des oberflächlichen<br />
Harnblasenkarzinoms<br />
Dosierung: <strong>mito</strong>-extra ® : 40 mg / <strong>mito</strong>-<strong>medac</strong> ® :<br />
20 mg Mitomycin, Trockensubstanz wird pro Instillation<br />
in 40 bzw. 20 ml physiolog. NaCl-Lösung gelöst.<br />
Handelsformen: Trockensubstanz/ Instillationssystem/<br />
Katheter mit Kathetersicherung/ Abfallbeutel in 1er und<br />
5er Packung.<br />
3
4<br />
2 ENTWICKLUNGSGESCHICHTE<br />
Die Mitomycine stellen eine Klasse von Antitumorantibiotika dar,<br />
die aus Streptomyces caespitosus isoliert wurden. Mitomycin C,<br />
1958 von Wakaki et al. entdeckt , stellt das effektivste und am<br />
besten untersuchte Zytostatikum aus dieser Substanzgruppe dar.<br />
Weiterhin bekannte Subspezies wie Mitomycin A und Mitomycin B<br />
haben klinisch keine Bedeutung gewonnen. Daher wird Mitomycin C<br />
nach der WHO-Nomenklatur häufig auch nur als Mitomycin<br />
bezeichnet.<br />
Seit mehr als 40 Jahren befindet sich Mitomycin in der klinischen<br />
Anwendung, seit mehr als 25 Jahren auch in Deutschland, wo es<br />
1978 durch die <strong>medac</strong> <strong>GmbH</strong> eingeführt wurde.<br />
Mitomycin wurde das erste Mal von Shida 1967 intravesikal<br />
gegen Blasentumoren verwendet.<br />
In den ersten Studien wurden tägliche oder wöchentliche i.v.<br />
Applikationen von relativ niedrigen Dosierungen angewandt. Dies<br />
führte zu teilweise ausgeprägten kumulativen Toxizitäten, insbesondere<br />
im Bezug auf das Knochenmark.<br />
Seit Mitte der siebziger Jahre wurden zunehmend intermittierende<br />
Dosisregimes angewandt, wobei sich in Kombinationsschemata<br />
die Gabe von ca. 10 mg/m 2 i.v. alle 4 - 6 Wochen als günstigster<br />
Applikationsmodus bezüglich Antitumoreffektivität und Toxizität<br />
herausstellte. Die Entwicklung dieser neuen Dosierungsregimes<br />
führte zu einem verstärkten Interesse an dieser Substanz und zu<br />
weiteren intensiven klinischen Untersuchungen.<br />
Mitomycin stellt heute eine der effektivsten Substanzen, sowohl in<br />
der Monotherapie als auch in Kombination mit anderen<br />
Zytostatika, u.a. bei der Behandlung des Harnblasenkarzinoms,<br />
des Mammakarzinoms und des nichtkleinzelligen Bronchialkarzinoms<br />
dar.<br />
Weitere häufige Einsatzgebiete für diese Substanz sind Tumoren<br />
des Gastrointestinaltraktes. Aufgrund seiner besonderen Wirksamkeit<br />
unter hypoxischen Bedingungen sowie seiner radiosensitivierenden<br />
Wirkung wird Mitomycin auch häufig in Kombination<br />
mit einer Strahlentherapie, z.B. bei Karzinomen im Kopf-Hals-<br />
Bereich bzw. beim Analkarzinom, eingesetzt.
3 PRODUKTBESCHREIBUNG<br />
3.1 Anwendungsgebiete:<br />
3.2 Dosierung<br />
Blasenkarzinom, Magenkarzinom, Bronchialkarzinom, Pankreaskarzinom,<br />
Kolon-Rektum-Karzinom, Mammakarzinom, Leberzellkarzinom,<br />
Zervixkarzinom, Oesophaguskarzinom, Karzinome im<br />
Kopf- und Halsbereich, chronisch myeloische Leukämie, Osteosarkom.<br />
Zur intravesikalen Therapie oberflächlicher Blasenkarzinome werden<br />
20-40 mg Mitomycin, gelöst in 20-40 ml 0,9% NaCl-Lösung,<br />
instilliert. Zur Rezidivprophylaxe, z.B. nach transurethraler<br />
Resektion, werden 20 bzw. 40 mg Mitomycin, gelöst in 20 bzw.<br />
40 ml 0,9% NaCl-Lösung, wöchentlich in die Blase instilliert.<br />
3.3 Nebenwirkungen der intravesikalen Anwendung<br />
Bei der intravesikalen Anwendung von Mitomycin ist, dank des<br />
hohen Molekulargewichts von 334 D, die systemische Absorption<br />
gering und die daraus resultierenden Nebenwirkungen sind erwartungsgemäß<br />
moderat (Thrasher & Crawford 1992, Huland<br />
1985, Huben 1996).<br />
Wajsman et al. 1984 untersuchten die Plasmakonzentration bei<br />
18 Patienten, die mit 40 mg Mitomycin behandelt wurden. In 30<br />
min Intervallen wurden Werte von 1,0 ng/ml bis 36,4 ng/ml<br />
gemessen. Höhere Konzentrationen wurden bei Patienten, die<br />
Verletzungen der Blasen-Mukosa nach der TUR hatten, festgestellt.<br />
Trotzdem wurden keine Knochenmark- und chromosomalen<br />
DNA-Veränderungen festgestellt.<br />
Gao et al. 1998 untersuchten die Konzentration im Urothel und im<br />
Plasma nach Instillation von 20 bzw. 40 mg Mitomycin und stellten<br />
einen max. Serumspiegel von 8,5 ng/ml fest. Diese Daten zeigen,<br />
dass die mediane Plasma-Konzentration 20-40-fach unter<br />
der toxischen Dosis von 400 ng/ml liegt.<br />
Allergische Reaktionen und Zystitis, unter Umständen hämorrhagischer<br />
Natur, begleitet von Dysurie, sind die häufigsten<br />
Nebenwirkungen der intravesikalen Therapie mit Mitomycin (ca.<br />
10%). Stenosen aufgrund einer direkt toxischen Wirkung von<br />
Mitomycin auf das Urothel sind als seltene Komplikationen nicht<br />
auszuschließen. Schmerzen beim Harnlassen, Harndrang und<br />
Exantheme können auftreten (Thrasher & Crawford 1992).<br />
5
6<br />
Mitomycin kann durch Auslösen von Übelkeit und Erbrechen indirekt<br />
zu einer Beeinträchtigung der Fahrtüchtigkeit oder der<br />
Bedienung von Maschinen führen.<br />
Im Zusammenhang mit einer Mitomycin-Behandlung sollten keine<br />
Impfungen mit Lebendvakzinen erfolgen.<br />
Die folgende Tabelle zeigt Häufigkeitsangaben zu den Nebenwirkungen<br />
der intravesikalen Anwendung:<br />
Quelle N mg Zystitis Allergie Kontakt- Leuko- Thrombo-<br />
(%) (%) Dermatitis penie penie<br />
Niessenkorn et al. 1981 29 40 3 (10) 1 (3) 3 0 0<br />
Heney et al. 1988 76 40 31 (41) 14 (19) - 1 2<br />
Eijstein et al. 1990 75 20-30 0 0 0 0 0<br />
Issell et al. 1984 60 40 (33) - 0 3 1<br />
DeBruyne et al. 1988 87 30 12 (14) 6 (7) 0 0 0<br />
Koontz et al. 1985 117 40 (6) 19 (16) - 0 0<br />
Huland & Otto 1985 54 20 9 (17) 3 (6) 0 0 0<br />
Prout et al. 1982 28 40 9 (32) 1 (4) 0 0 0<br />
Harrison et al. 1983 23 40 9 (32) 1 (4) 0 0 0<br />
DeFuria et al. 1980 63 20-60 4 (6) 0 3 (5) 0 0<br />
Krege et al. 1996 337 20 16 0 6 - -<br />
Vegt et al. 1995 437 20 26 (18) 7 (5) 0 - -<br />
Witjes et al. 1998 344 30 33 (19) 10 (6) 0 - -<br />
Nach intravesikaler Anwendung kann Mitomycin allergische<br />
Reaktionen hervorrufen. In den meisten Fällen handelt es sich<br />
dabei um eine Kontaktdermatitis, meist in Form von Palmar- und<br />
Plantarerythemen. Es können jedoch auch generalisierte<br />
Exantheme auftreten. Ebenfalls kann eine Zystitis auftreten, die<br />
symptomatisch durch antiphlogistische und analgetische<br />
Maßnahmen behandelt werden kann.<br />
In Einzelfällen wurde von schweren Unverträglichkeitsreaktionen<br />
(nekrotisierende Zystitis) berichtet.<br />
Eine seltene Nebenwirkung der Instillationstherapie mit Mitomycin<br />
ist die sog. Plaquebildung.<br />
Die Plaquebildung bzw. Fibrinbelegung und spätere Calcifizierung<br />
dieser Fibrinbelege ist im Wundbereich erstmals von Flüchter et<br />
al. 1982 beschrieben worden.<br />
Tierexperimentell konnten von Friedmann et al. 1991 fibröse<br />
Plaques in der Rattenblase nach Therapie mit Doxorubicin oder<br />
auch Mitomycin nachgewiesen werden.<br />
Für die Ausbildung dieser Plaques bzw. Belege existiert vermutlich<br />
eine sogenannte „Vulnerable Phase“. Es zeigt sich, dass vor allem<br />
dann, wenn die Mitomycin-Gabe zum Zeitpunkt der Bildung des<br />
Fibrinbelages im Rahmen der Wundheilung erfolgte, solche
Plaquebildungen vorkommen. Offensichtlich kommt es zu unbekannten<br />
Verbindungen zwischen dem Fibrinbelag und Mitomycin<br />
(Liu et al. 2001; See & Williams 1992). Erfolgt die erste<br />
Mitomycin-Instillation innerhalb von 24 Stunden, kommt es kaum<br />
zu diesen Plaquebildungen. Ebenso wenig, wie wenn die erste<br />
Instillation erst nach Abschluss der Wundheilung ca. 3 – 4<br />
Wochen post OP erfolgt.<br />
3.4 Wechselwirkungen mit anderen Mitteln<br />
Bei der i.v. Anwendung von Mytomycin wird die Knochenmarktoxizität<br />
durch zusätzliche Verabreichung myelosuppressiv wirksamer<br />
Arzneistoffe oder Strahlentherapie verstärkt.<br />
Die gleichzeitigen Gabe von Vincaalkaloiden oder Bleomycin und<br />
Mitomycin kann zu verstärkter pulmonaler Toxizität führen.<br />
Pyridoxinhydrochlorid (Vitamin B6) führte in Tierversuchen zu<br />
einem Wirkungsverlust des Mitomycins. Im Zusammenhang mit<br />
einer Mitomxcin-Behandlung sollten keine Impfungen mit<br />
Lebendvakzinen erfolgen.<br />
Die Kardiotoxizität von Adriamycin (Doxorubicin) kann durch<br />
Mitomycin verstärkt werden.<br />
3.5 Gegenanzeigen für die intravesikale Therapie<br />
Kontraindikation ist eine bestehende Harnblasenentzündung.<br />
Aufgrund seiner nachgewiesenen mutagenen, teratogenen und<br />
karzinogenen Wirkung darf Mitomycin in der Schwangerschaft<br />
und während der Laktation nicht gegeben werden. Außerdem<br />
sollten Patienten in geschlechtsreifem Alter während der Therapie<br />
kontrazeptive Maßnahmen treffen bzw. zur Abstinenz angehalten<br />
werden. Diese Maßnahmen sind bis 3 Monate nach Abschluss der<br />
Therapie fortzusetzen. Die Behandlung bei Säuglingen und<br />
Kleinkindern darf erst nach sorgfältiger Abwägung des Nutzen/<br />
Risiko-Verhältnisses erfolgen.<br />
3.6 Art und Dauer der Anwendung<br />
<strong>mito</strong>-extra ® , <strong>mito</strong>-<strong>medac</strong> ® und <strong>mito</strong>-<strong>medac</strong> ® pro infusione<br />
sind zur intravesikalen Instillation nach Auflösen bestimmt. Als<br />
Lösungsmittel eignen sich Wasser für Injektionszwecke bzw. isotonische<br />
Kochsalzlösung für Injektionszwecke. Die gebrauchsfertige<br />
Lösung sollte nicht mehr als 1 mg Mitomycin pro ml enthalten.<br />
Die gebrauchsfertige Lösung sollte sofort verbraucht werden.<br />
Verweildauer in der Blase (Dwell-time)<br />
Die gebrauchsfertige Lösung soll 2 Stunden in der Blase bleiben<br />
7
8<br />
Dauer der Haltbarkeit<br />
Substanz: 4 Jahre<br />
Lösungsmittel: 1 Jahr<br />
3.7 Handhabung und Stabilität<br />
Besondere Lager- und Aufbewahrungshinweise<br />
Vor Licht schützen<br />
Darreichungsformen und Packungsgrößen<br />
OP mit 1 Durchstechflasche mit 1000 mg (<strong>mito</strong>-extra ® ) bzw.<br />
500 mg (<strong>mito</strong>-<strong>medac</strong> ® ) Trockensubstanz und Lösungsmittelbeutel,<br />
1 Tiemann-Katheter beiliegend, 1 Kathetersicherung,<br />
1 Abfallbeutel.<br />
<strong>mito</strong>-<strong>medac</strong> ® pro infusione mit 1 Durchstechflasche mit 500<br />
mg Trockensubstanz ohne Instillationssystem, Katheter und<br />
Abfallbeutel.<br />
OP mit 5 Durchstechflaschen mit je 1000 mg (<strong>mito</strong>-extra ® ) bzw.<br />
500 mg (<strong>mito</strong>-<strong>medac</strong> ® ) Trockensubstanz und Lösungsmittelbeuteln,<br />
5 Tiemann-Katheter beiliegend, 5 Kathetersicherungen,<br />
5 Abfallbeutel.<br />
<strong>mito</strong>-<strong>medac</strong> ® pro infusione mit 5 Durchstechflaschen mit je<br />
500 mg Trockensubstanz ohne Instillationssystem, Katheter und<br />
Abfallbeutel.<br />
Bei der Therapie des oberflächlichen Harnblasenkarzinoms hat<br />
sich die intravesikale Gabe bewährt. Beim Umgang mit Mitomycin<br />
sollten Handschuhe getragen werden. Mitomycin kann auch intravenös<br />
als Bolus-Gabe bzw. Kurzinfusion angewendet werden.<br />
Eine Durchstechflasche <strong>mito</strong>-<strong>medac</strong> ® und <strong>mito</strong>-<strong>medac</strong> ® pro<br />
infusione bzw. <strong>mito</strong>-extra ® enthält:<br />
• 20 mg Mitomycin (<strong>mito</strong>-<strong>medac</strong> ® / <strong>mito</strong>-<strong>medac</strong> ® pro infusione)<br />
bzw. 40 mg Mitomycin (<strong>mito</strong>-extra ® ) (wirksamer<br />
Bestandteil)<br />
• 480 mg (<strong>mito</strong>-<strong>medac</strong> ® / <strong>mito</strong>-<strong>medac</strong> ® pro infusione) bzw.<br />
960 mg (<strong>mito</strong>-extra ® ) Natriumchlorid<br />
Die Stabilität von Mitomycin in wäßriger Lösung ist stark pHabhängig.<br />
Das pH-Optimum liegt bei pH 6,5 bis 7,5. Saure oder<br />
alkalische Lösungen führen zu einem raschen Wirkstoffabbau.<br />
Die mit Wasser für Injektionszwecke rekonstituierte Lösung hat<br />
einen pH-Wert im Bereich des pH-Optimums von 6,5 –7,5.
Stammlösungen sollten nach Möglichkeit nicht hergestellt werden.<br />
Falls dies unbedingt erforderlich ist, sollte Wasser für Injektionszwecke<br />
verwendet werden.<br />
Bei mehrstündiger Aufbewahrung muss auf jeden Fall ein neutraler<br />
pH-Wert und Lichtschutz gewährleistet sein.<br />
Die physikalisch-chemische Haltbarkeit von Lösungen mit 0,8<br />
mg/ml Mitomycin in 0,9%iger Kochsalzlösung beträgt bei Raumtemperatur<br />
unter Lichtschutz maximal 7 Stunden.<br />
In 5 %iger Glucoselösung ist Mitomycin dagegen aufgrund des<br />
ungünstigen pH-Wertes dieser Lösung weniger als 3 Stunden<br />
haltbar.<br />
Eine Lagerung der rekonstituierten Lösung im Kühlschrank ist<br />
nicht notwendig. Falls die Konzentration der Lösung höher als 0.6<br />
mg/ml ist, muss bei Kühlschranklagerung sogar mit irreversiblen<br />
Ausfällungen in Form feiner blauschwarzer Nadeln gerechnet werden.<br />
3.7.1 Das geschlossene System / Sicherheitsaspekte<br />
<strong>mito</strong>-<strong>medac</strong> ® und <strong>mito</strong>-extra ® zur Blaseninstillation werden mit<br />
einem geschlossenen Instillationssystem angeboten. Dieses<br />
System ermöglicht überall eine sichere und schnelle Instillation<br />
und umgeht die Notwendigkeit einer Zytostatika-Werkbank.<br />
Die Definition des geschlossenen Systems nach Merkblatt M620<br />
der Berufsgenossenschaft für Gesundheitsdienst und<br />
Wohlfahrtspflege über der sicheren Handhabung von Zytostatika<br />
lautet:<br />
1. Ein geschlossenes System ist ein System, bei dem während<br />
des Misch- bzw. Herstellungsvorganges zwischen dem kontaminierten<br />
Innenraum und der Umgebung keine betriebsmäßig<br />
offene Verbindung besteht. Für die Applikation darf erst nach<br />
der Herstellung einer Verbindung vom System zum Patienten<br />
mittels eines Fortleitungssystems (z.B. Katheter) das geschlossene<br />
System in Richtung Anwendungsteil geöffnet werden.<br />
Diese Verbindung muss definiert sicher sein.<br />
Das geschlossene System besteht aus definierten<br />
Konnektoren, Medikamentengefäßen, Trennelementen und<br />
einem Anwendungsteil.<br />
2. Geschlossene Systeme müssen für einen definierten<br />
Anwendungszweck zum einmaligen Gebrauch konzipiert sein<br />
(zum Beispiel intravesikale Instillationstherapie). Es muss<br />
9
10<br />
sichergestellt sein, dass sie nur für diesen beschriebenen<br />
Zweck verfügbar gemacht werden.<br />
3. Eine Mehrfachbenutzung muss technisch ausgeschlossen<br />
sein. Insbesondere ist eine Dekonnektierung von Medikamentenflaschen<br />
durch die konstruktive Gestaltung des / der<br />
Konnektors / en auszuschließen. Eine Anpassung an den jeweiligen<br />
Stand der Technik muss gewährleistet sein.<br />
4. Geschlossene Systeme müssen manipulationssicher sein. Öffnungsvorgänge<br />
dürfen nur im System möglich sein.<br />
5. Die Bedienungsschritte müssen sinnfällig und zwangsläufig<br />
sein. Bedienungsfehler dürfen nicht zu einer gefährlichen<br />
Situation führen.<br />
6. Geschlossene Systeme sind immer nur für ein Medikament<br />
einer Firma/ einer Herstellung mit definierten Flaschen, insbesondere<br />
Stopfen, Aluminiumkappenabmessungen und einem<br />
definiertem Fortleitungssystem zugelassen.<br />
7. Der Hersteller des Systems entscheidet über die Zulassung von<br />
Flaschen und Fortleitungssystemen.<br />
8. Konnektoren für Medikamentenflaschen und Fortleitungssysteme<br />
müssen so konstruiert sein, dass eine Verwechslung<br />
ausgeschlossen ist.<br />
9. Auf Anforderung der Berufsgenossenschaft muss ein Nachweis<br />
der Einhaltung der Anforderungen an ein geschlossenes<br />
System erbracht werden.
12<br />
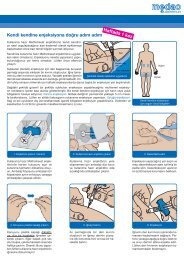
3.7.2 Applikationsanleitung von <strong>mito</strong>-extra ® und <strong>mito</strong>-<strong>medac</strong> ®<br />
1. Schützhülle aufreißen und nicht ganz<br />
entfalten! Die Spitze des Instillationssystems<br />
bleibt somit vor Keimen<br />
geschützt.<br />
3. Durchstechflasche fest in den Adapter<br />
des Instillationssystems drücken bis<br />
dieser einrastet und mindestens 1x<br />
komplett drehen.<br />
2. Die Abdeckkappen von der Durchstechflasche<br />
und vom Adapter des<br />
Instillationssystems entfernen. Entsorgungsbeutel<br />
zurechtlegen.
4. Verbindung herstellen: Sollbruchstelle<br />
im Schlauchteil des Adapters durch Hinund<br />
Herbiegen brechen.<br />
5. Lösen: Einen Teil Flüssigkeit in die Durchstechflasche<br />
pumpen. Wichtig: Etwas<br />
Luft in der Flasche belassen. Medikament<br />
vorsichtig lösen, nicht schütteln!<br />
6. Durchstechflasche nicht abnehmen!<br />
Flasche nach oben halten und Luft einpumpen.<br />
Das gelöste Medikament so in<br />
den Instillationssystem pumpen.<br />
7. Die Schützhülle vollständig entfernen.<br />
Katheter mit Instillationssystem verbinden.<br />
Bei Bedarf Kathetersicherung an die obere<br />
Kante des Katheters einschieben.<br />
13
14<br />
8. Instillation: Erst jetzt Verschlussmechanismus<br />
im Schlauchteil aufbrechen<br />
und Lösung instillieren. Katheter mit Luft<br />
freidrücken. Instillationssystem zusammengedrückt<br />
halten und mit dem Katheter in<br />
den Entsorgungsbeutel geben.<br />
4 WIRKUNGSMECHANISMUS<br />
Mitomycin hemmt selektiv die DNA-Synthese. Oxidiertes<br />
Mitomycin ist inaktiv; für eine optimale Wirkung dieser Substanz ist<br />
eine chemische oder enzymatische reduktive Aktivierung zum<br />
Semi- oder Hydrochinon erforderlich. Erst hierdurch wird eine<br />
mono- oder bifunktionelle Alkylierung der DNA ermöglicht.<br />
Einen möglichen Mechanismus der reduktiven Aktivierung zeigt<br />
Abbildung 1 (Rimpler 1990).<br />
Nach Reduktion zum Semi- bzw. Hydrochinon bildet sich intermediär<br />
ein hochreaktives Chinonmethid, das zunächst zu einem<br />
DNA-Monoaddukt führt. Anschließend kann eine intramolekulare<br />
Substitution der Carbamatgruppe zum Biaddukt führen. Die<br />
bifunktionelle Alkylierung ist wahrscheinlich die Grundlage für die<br />
Fähigkeit der Substanz, eine Quervernetzung zwischen den DNA-<br />
Strängen hervorzurufen (Verweij & Pinedo 1990).<br />
Die Bindungsstellen des Mitomycins an der DNA sind die N6-<br />
Position am Adenin sowie die N2- oder N7-Position am Guanin<br />
(Verweij & Pinedo 1990).<br />
Die Reduktion von Mitomycin, die notwendig für die alkylierende<br />
Wirkung dieser Substanz ist, hat zur Einführung des Begriffes<br />
„bioreduktive Alkylierung“ geführt, um den Wirkungsmechanismus<br />
dieses Zytostatikums zu beschreiben. Mitomycin<br />
stellt den Prototyp einer Substanzgruppe mit bioreduktiv alkylierender<br />
Wirkung dar (Lin et al. 1972)
Die reduktive Aktivierung von Mitomycin kann durch folgende<br />
Enzymsysteme initiiert bzw. moduliert werden: DT-Diaphorase,<br />
NADPH-Zytochrom, P-450 Reduktase, NADPH-Zytochrom C<br />
Reduktase, Xanthinoxydase sowie einige Flavoproteintranshydrogenasen<br />
(Verweij & Pinedo 1990).<br />
Mit der cytosolischen Mitomycin-Reduktase wurde kürzlich ein<br />
weiteres Enzym entdeckt, das an der Aktivierung von Mitomycin<br />
beteiligt ist (Joseph & Jaiswal 2000)<br />
Aktiviertes Mitomycin ist in der späten G1- und S-Phase des<br />
Zellzyklus am effektivsten (Wennerberg et al. 1984, Kimber<br />
et al. 1978).<br />
Obwohl ein definitiver Beweis noch aussteht, gibt es klare<br />
Anhaltspunkte dafür, dass Mitomycin besonders unter hypoxischen<br />
Bedingungen aktiviert wird. So wurde z.B. gezeigt, dass<br />
Dicumarol, ein Hemmstoff der DT-Diaphorase, die Zytotoxizität<br />
von Mitomycin gegenüber hypoxischen EMT-6-Zellen sowohl invitro<br />
als auch in-vivo steigert, möglicherweise durch Hemmung<br />
von Enzymen, die im Aktivierungs- bzw. Inaktivierungsprozeß von<br />
Mitomycin involviert sind. Diese Steigerung der Zytotoxizität<br />
gegenüber hypoxischen Tumorzellen ging nicht parallel mit einer<br />
gesteigerten Toxizität gegenüber gut mit Sauerstoff gesättigten<br />
Geweben, wie z. B. dem Knochenmark, einher. In Hinsicht auf die<br />
besondere Toxizität gegenüber hypoxischen Zellen erscheint die<br />
Kombination von Mitomycin und Strahlentherapie eine wirksame<br />
Behandlungsmethode solider Tumoren darzustellen, da die<br />
Bestrahlung gegenüber aeroben Tumorzellen effektiver ist<br />
(Brown 1999, Verweij & Pinedo 1990).<br />
Der Mechanismus einer Resistenzentwicklung gegenüber Mitomycin<br />
ist noch nicht komplett verstanden, schließt vermutlich aber<br />
Änderungen in der Substanzaufnahme, eine verminderte<br />
Bioaktivierung alkylierender Metaboliten sowie eine gesteigerte<br />
DNA-Reparatur ein (s. Abb. 1).<br />
15
16<br />
Abb.1:<br />
Reduktive Aktivierung von<br />
Mitomycin und Alkylierung der<br />
DNA
5 CHEMISCH-PHYSIKALISCHE EIGENSCHAFTEN<br />
Bezeichnung des Arzneimittels:<br />
<strong>mito</strong>-extra ® , <strong>mito</strong>-<strong>medac</strong> ® , <strong>mito</strong>-<strong>medac</strong> ® pro infusione<br />
Verschreibungsstatus: Verschreibungspflichtig<br />
Chemische Bezeichnung:<br />
(1R, 2R, 9R, 9aS)-7-Amino-2, 3, 5, 8, 9, 9a-hexahydro-9amethoxy-6-methyl-5,<br />
8-dioxo-1, 2-epimino-1-H-pyrrolo[1, 2-a]indol-<br />
9-ylmethylcarbamat<br />
Internationaler Freiname (INN):<br />
Mitomycin<br />
Synonyme: Mitomycin-C, Mutamycin, Mytomycin, MMC, Mito-C,<br />
MIT-C<br />
Strukturformel:<br />
Summenformel:<br />
C 15H 18N 4O 5<br />
Molekulargewicht:<br />
334,33<br />
Beschreibung:<br />
Blauviolettes, kristallines Pulver, Smp. >360 °C<br />
Löslichkeit:<br />
Löslich in Wasser, Methanol, Aceton und n-Butylacetat, wenig löslich<br />
in Äther, Benzol, und Tetrachlorkohlenstoff.<br />
17
18<br />
6 PHARMAKOLOGIE<br />
6.1 Pharmakologische Eigenschaften<br />
6.2 Pharmakokinetik<br />
Mitomycin liegt in inaktiver Form vor. Die Aktivierung zu einem trifunktionellen<br />
Alkylans erfolgt rasch, entweder bei physiologischem<br />
pH in Anwesenheit von NADPH im Serum oder praktisch in allen<br />
Körperzellen intrazellulär mit Ausnahme des Gehirns, da die Blut-<br />
Hirn-Schranke von Mitomycin nicht überwunden wird. Die 3 alkylierenden<br />
Radikale stammen je von einer Chinon-, einer Aziridinund<br />
einer Urethangruppe. Der Wirkungsmechanismus beruht<br />
überwiegend auf einer Alkylierung der DNA (weniger der RNS) mit<br />
entsprechender Hemmung der DNA-Synthese. Der Grad der<br />
DNA-Schädigung korreliert mit dem klinischen Effekt und ist in<br />
resistenten Zellen geringer als in sensiblen. Wie bei anderen<br />
Alkylantien werden proliferierende Zellen stärker geschädigt als<br />
solche, die sich in der Ruhephase (G0) des Zellzyklus befinden.<br />
Zusätzlich werden, insbesondere bei Anwendung höherer Dosen,<br />
freie Peroxidradikale freigesetzt, die zu DNA-Brüchen führen. Die<br />
Freisetzung von Peroxidradikalen wird mit dem organspezifischen<br />
Muster an Nebenwirkungen in Verbindung gebracht (Lown 1979,<br />
Beretta et al. 1990).<br />
Sowohl die intraperitoneale als auch intravesikale Applikationsroute<br />
führt zu einer signifikant höheren lokalen Exposition dieser<br />
Substanz bei gleichzeitig sehr niedrigen Plasmaspiegeln. Während<br />
die intravesikale Gabe erfolgreich in der Behandlung des oberflächlichen<br />
Blasenkarzinoms eingesetzt wird, muss die Bedeutung<br />
der intraperitonealen Gabe von Mitomycin noch in Studien geklärt<br />
werden (van Oosterom et al. 1984)<br />
Mitomycin ist in der Lage, auch in tiefere Regionen der<br />
Blasenwand (bis in die Muscularis) (Wientjes et al., 1993) zu diffundieren.<br />
Die Konzentrationsunterschiede zwischen Urothel und<br />
Lamina propria betragen das 35fache und in der Muscularis verringert<br />
sich die Konzentration um die Hälfte.<br />
Intervesikal verabreichtes Mitomycin kann auch nach 30 oder 60<br />
min Verweildauer in der Blase (dwell-time) innerhalb von 15min<br />
systemisch nachgewiesen werden (s. Abb. 2). C max beträgt nach<br />
60 min dwell-time nicht höher als 50 ng/ml. Die Konzentration<br />
sinkt dann 90min nach dem Beginn der Instillation schnell in den<br />
pg/ml Bereich (De Bruijn et al. 1992).
Abb. 2:<br />
Plasmakonzentrations-Kurve<br />
von MMC (40 mg/40 ml NaCl)<br />
nach intravesikaler Instillation<br />
(dwell-time 30min) (nach<br />
De Bruijn et al. 1992)<br />
6.3 Toxikologie<br />
Im Gegensatz zur intravenösen Gabe (100% Verfügbarkeit) liegt<br />
die Verfügbarkeit von Mitomycin nach intravesikaler Verabreichung<br />
sytemisch bei 1-5% vor (De Bruijn et al. 1992).<br />
Gao et al. 1998 untersuchten die Konzentration von Mitomycin im<br />
Urothel nach Instillation mit 20 bzw. 40 mg Mitomycin bei humanen<br />
Blasen. Sie stellten fest, dass durch die Instillation von 40 mg<br />
Mitomycin fast die doppelte Konzentration im Urothel vorhanden<br />
war (s. Abb. 11, Kap. 8.2.1).<br />
Mitomycin besitzt aufgrund seiner pharmakologischen<br />
Eigenschaften mutagene, karzinogene und teratogene<br />
Wirkungen, die in entsprechenden experimentellen Systemen<br />
nachweisbar sind.<br />
7 KLASSIFIKATION OBERFLÄCHLICHER HARNBLASENTUMOREN<br />
UND RISIKOADAPTIERTE THERAPIE<br />
Bei der Klassifikation der oberflächlichen Harnblasentumoren<br />
(HBCA) gemäß den Leitlinien der eau und DGU lassen sich die<br />
Tumoren in 3 Hauptgruppen unterteilen: low-risk, intermediaterisk<br />
und high-risk Karzinome.<br />
Die risikoadaptierte Therapie besteht einheitlich aus einer<br />
Frühinstillation (unmittelbar post OP oder max. 24h später) für alle<br />
HBCA-Tumoren z.B. mit 40 mg Mitomycin. Für low risk HBCA<br />
danach keine weitere Therapie, in einzelnen Fällen 6-wöchentliche<br />
Gaben z.B. von 20 mg Mitomycin.<br />
19
20<br />
Abb. 3:<br />
Risikoadaptierte Therapie<br />
des oberflächlichen HBCA<br />
Bei Intermediate risk HBCA wird eine lange Rezidivprophylaxe<br />
für bis zu 3 Jahre empfohlen, bestehend aus Initial- und<br />
Erhaltungstherapie z.B. mit 20 mg bzw. 40 mg Mitomycin.<br />
Bei high-risk HBCA besteht die adjuvante Therapie aus der<br />
Immunprophylaxe mit BCG. Eine 6-wöchige Initialtherapie gefolgt<br />
von 3-wöchentlichen Applikationen alle 3-6 Monate bis zu<br />
3 Jahren (am 3.,6.,12.,18.,24.,30.,36. Monat) (s. Abb. 3).<br />
7.1 Neue WHO-Klassifikation<br />
Die WHO veröffentlichte 1998 und 2004 eine Klassifikation, die<br />
sowohl das biologische Verhalten der Tumoren als auch die zytogenetischen<br />
und molekularbiologischen Veränderungen berücksichtigt.<br />
Die neue Klassifizierung unterscheidet zwischen zwei großen<br />
Gruppen, den nicht invasiven und den invasiven Tumoren.<br />
Die Gradings 1, 2 und 3 von 1973 entsprechen in der WHO-<br />
Nomenklatur die neuen Termini :<br />
- Nicht invasive papilläre urotheliale Neoplasie niedriger<br />
maligner Potenz (PUNLMP)<br />
- Nicht invasives papilläres Urothelkarzinom low grade<br />
(LGPUC)<br />
- Nicht invasives papilläres Urothelkarzinom high grade<br />
(HGPUC)
Die folgende Tabelle zeigt die WHO-Klassifikation der Tumoren im<br />
Laufe der Jahre und im Vergleich zur eau-Klassifizierung:<br />
8 THERAPIE DES OBERFLÄCHLICHEN HARNBLASENKARZINOMS<br />
MIT MITOMYCIN<br />
8.1 Frühinstillation<br />
Was versteht man unter Frühinstillation?<br />
Frühinstillation ist eine einzige Instillation eines Zytostatikums (z.B.<br />
Mitomycin), die im Idealfall unmittelbar (1) nach der TUR-Blase<br />
(TUR-B) durchgeführt werden soll. Diese Instillation kann abweichend<br />
6 Stunden (2) nach der TUR-B (z.B. bei der<br />
Nachmittagsvisite) oder spätestens 24h post OP (3) stattfinden<br />
(Kaasinen et al. 2002) (s. Abb. 4).<br />
21
22<br />
Abb. 4:<br />
Die 3 Chancen zur<br />
Frühinstillation<br />
Die Idee zur Frühinstillation basiert auf bereits seit Mitte der 70er<br />
Jahre bekannten Theorien, dass sich während der TUR Implantationsmetastasen<br />
durch in der Spülflüssigkeit befindliche Tumorzellen<br />
ausbilden können. Bei einer Frühinstillation werden einerseits<br />
diese Zellen frühzeitig durch direkte Zytotoxizität abgetötet<br />
und andererseits wird die Adhäsion dieser Zellen an das Urothel<br />
gehemmt (Soloway et al. 1980 und 1989, Solsona et al. 1999,<br />
Durek et al. 2002).<br />
Das Konzept der Tumorzellimplantation wird auf Beobachtungen<br />
von Albarran & Imbeck 1903 zurückdatiert. Sie beobachteten<br />
den Zusammenhang zwischen Urotheltumoren der Blase und<br />
dem Vorkommen von Tumoren im Nierenbecken.<br />
Hinman 1956 und Kiefer 1953 hoben die Bedeutung des iatrogenen<br />
urothelialen Traumas als den wichtigsten Faktor für die<br />
hohe Rezidivrate, die durch die Tumorzellimplantation induziert<br />
wird, hervor.<br />
Burnard et al. 1976 haben einen dramatischen Rückgang des<br />
Tumorvorkommens beobachtet, wenn unmittelbar nach der TUR<br />
mit einem hochdosierten Zytostatikum (in diesem Fall Thiotepa)<br />
instilliert wurde.<br />
In seinen Publikationen berichtete Soloway 1980 und 1989 u.a.<br />
über die Tumorzellimplantation während der TUR-Blase (TUR-B).<br />
Die Instillation von Urothelkarzinomzellen in Blasen (Tiermodell),<br />
die vorher mit N-methyl-N-nitroharnstoff (NMU) behandelt wurden<br />
und dadurch ihre Urothelschicht weitgehend verloren hatten,<br />
resultierte in einer Tumorbildung bei 60% der so behandelten
Abb. 5:<br />
Hemmung der Adhäsion von<br />
Tumorzellen u.a. durch<br />
Mitomycin (nach Pode et al.<br />
1987)<br />
Blasen. Wenn vor der Tumorzellimplantation nicht mit NMU<br />
behandelt wurde, waren nur 13% dieser Blasen mit Tumoren<br />
befallen. In einem weiteren Experiment zeigten 54% der Blasen<br />
Rezidive, wenn sie vor der Tumorzell-Instillation reseziert wurden.<br />
Dagegen hatten sich bei nur 12% der unbehandelten Blasen<br />
Tumoren entwickelt.<br />
Bei Menschen mit HBCA werden Tumorzellen aus der<br />
Blasenwand freigesetzt und durch die positive Urinzytologie nachgewiesen.<br />
Es ist also denkbar, so Soloway, dass durch die<br />
Elektroresektion eine fertile Oberfläche für die Tumorzellimplantation<br />
bereitet wird.<br />
Noch ein Indiz für die Existenz der Tumorzellimplantation konnten<br />
Müller et al. 1985 liefern. Sie untersuchten das Vorkommen von<br />
Tumorzellen mittels Urinzytologie bei 51 Patienten post OP 75%<br />
der Patienten, die 3 Tage nach TUR eine positive Urinzytologie<br />
zeigten, hatten nach 3-6 Monaten Rezidive. Im Gegensatz dazu<br />
hatten nur 26% der Patienten, die 3 Tage nach TUR eine negative<br />
Urinzytologie hatten, ein Rezidiv.<br />
Pode et al. untersuchten 1987 die Hemmung der Adhäsion von<br />
Tumorzellen durch verschiedene Chemotherapeutika, u.a.<br />
Mitomycin und Doxorubicin.<br />
Bereits nach 5 min waren mehr als 80% der Tumorzellen durch die<br />
Wirkung von Mitomycin nicht mehr adhärent. Dagegen benötigte<br />
Doxorubicin über 50 min, um die gleiche Wirkung zu erreichen<br />
(s. Abb. 5).<br />
23
24<br />
Tab. 1:<br />
Studienübersicht zur<br />
Frühinstillation<br />
Um die Reduktion der Tumorzellimplantation durch Zytostatika<br />
besser zu verstehen, haben Durek et al. 2002 den Effekt der<br />
Kurzzeit-Exposition von Blasentumorzellen mit Zytostatika (u.a.<br />
Mitomycin, Doxorubicin, Cisplatin ) in vitro untersucht. Es zeigten<br />
sich sowohl zeit- als auch konzentrationsabhängige Korrelationen<br />
bezüglich der Adhäsionsinhibition und der Zytotoxizität. Mitomycin<br />
zeigte eine starke Wirkung auf die Adhäsions- und Proliferationsfähighkeit<br />
von Tumorzellen schon bei kurzen Expositionszeiten<br />
innerhalb der ersten 30 min. Dabei wurde die Adhäsion der Zellen<br />
bis zu 90% inhibiert.<br />
Oosterlinck et al. publizierten die erste klinische Frühinstillationsstudie<br />
1993. Dabei wurden insgesamt 431 Patienten mit<br />
Ta/T1-Tumoren entweder mit 80 mg Epirubicin (205 Pat.) oder<br />
Wasser (215 Pat.) frühinstilliert (single shot). Die Rezidivrate der<br />
Chemotherapie-Gruppe war signifikant besser als die der Wasser-<br />
Gruppe und konnte um rund 50% gesenkt werden (s. Tab. 1).<br />
Diese Studie hat auch deutlich gezeigt, dass Wasser als Substanz<br />
nicht geeignet ist.<br />
Die erste große klinische Studie, die sich mit der Frühinstillation<br />
von Mitomycin befasste, war die EORTC-Studie von Bouffioux<br />
et al. 1995. Insgesamt wurden 834 Patienten in 4 Arme randomisiert<br />
und sowohl mit Mitomycin 30 mg (457 Pat.) als auch mit<br />
Doxorubicin 50 mg (377 Pat.) wie folgt behandelt:<br />
1. Frühinstillation + 6 Monate,<br />
2. Frühinstillation + 12 Monate,<br />
3. eine späte Instillation + 6 Monate,<br />
4. eine späte Instillation + 12 Monate
Abb. 6:<br />
Rezivifreies Interval für 122<br />
Patienten mit und ohne<br />
Früinstillation (nach Solsona et<br />
al. 1999)<br />
Die Ergebnisse der Frühinstillations-Arme mit 6 oder 12 Monate<br />
Therapie sowie die spät begonnene, aber 12 Monate durchgeführte<br />
Therapie waren signifikant besser als die spät begonnene<br />
mit 6 Monaten Therapiedauer. Die Rezidivrate konnte durch die<br />
Frühinstillation um 30% reduziert werden (s. Tab. 1).<br />
Die Autoren empfehlen die Frühinstillation als Methode, die<br />
Tumorzellimplantation zu unterbinden und somit die Rezidivrate zu<br />
erniedrigen.<br />
In einer weiteren Studie führten Tolley et al. 1996 die Frühinstillation<br />
mit Mitomycin 40 mg (z.B. <strong>mito</strong>-extra ® ) vs. Kontrolle<br />
(keine Instillation) bei 502 Patienten mit Ta/T1 Harnblasenkarzinom<br />
durch. Die Frühinstillationsgruppen wurden in zwei Gruppen<br />
unterteilt:<br />
1. Gruppe A: Nur Frühinstillation (innerhalb 24h)<br />
2. Gruppe B: Frühinstillation (innerhalb 24h) +<br />
4 weitere Instillationen (eine Instillation alle 3 Monate)<br />
Die Senkung der Rezidivrate durch die Frühinstillation mit 40 mg<br />
Mitomycin war signifikant besser als bei der Kontrollgruppe und<br />
betrug ca. 50%.<br />
Solsona et al. untersuchten 1999 die Effektivität einer Frühinstillation<br />
mit 30 mg Mitomycin ohne weitere Initial- und<br />
Erhaltungstherapie bei insgesamt 122 Patienten mit ≤ 3cm großen<br />
primären oder rezidivierenden Tumoren (kein G3 und CIS). Die<br />
Frühinstillationsgruppe (57 Patienten) wurde gegen die<br />
Kotrollgruppe ohne Instillation (64 Patienten) verglichen. Eine signifikante<br />
Reduktion der Rezidivrate bei der Frühinstillationsgruppe<br />
um ca. 50% in der ersten 2 Jahren konnte festgestellt werden<br />
(s. Abb. 6 & Tab. 1).<br />
25
26<br />
Abb. 7:<br />
Verlauf der Rezidivfreiheit bei<br />
Frühinstillation am Tag 0 und<br />
Instillation am Tag >0 (nach<br />
Kaasinen et al. 2002)<br />
In der Studie von Kaasinen et al. 2002 wurden 205 Patienten<br />
mit Ta/T1 Harnblasenkarzinomen behandelt. Von diesen Patienten<br />
bekamen 104 eine Frühinstillation (am Tag 0), alle andere wurden<br />
später instilliert.<br />
Die Rezidivrate konnte durch die Frühinstillation innerhalb 24h mit<br />
40 mg Mitomycin (z.B. <strong>mito</strong>-extra ® ) um ca. 50% gesenkt<br />
werden, unabhängig von der Art der weiteren Behandlung. Es<br />
zeigte sich, dass eine effektive Chemotherapie mit Frühinstillation<br />
von 40 mg Mitomycin das Risiko der Rezidiventstehung hoch signifikant<br />
reduziert (s. Abb. 7).<br />
Pan et al., untersuchten 1998 die Inhibierung der Zellimplantation<br />
in einem Tiermodel. Sie stellten fest, dass die Implantationsrate<br />
bei einer sofortigen Gabe eines Zytostatikums (in diesem Fall<br />
Thiotepa) bei 3,4%, nach 1 Stunde bei 6,5% und nach 24<br />
Stunden bei 26,9% lag. Die Implantationsrate der dazu verglichenen<br />
Kontrolle (ohne Frühinstillation) lag bei 30,4%.<br />
Der Zeitpunkt der Frühinstillation sollte innerhalb von 24h post OP<br />
liegen. Je früher eine Frühinstillation durchgeführt wird (optimal<br />
wäre unmittelbar post OP) desto besser.<br />
Sylvester et al. publizierten 2004 eine Metaanalyse über die<br />
Frühinstillation. In diese Metaanalyse wurden 7 Studien mit insgesamt<br />
1476 Patienten einbezogen.<br />
Demnach wird durch die Frühinstillation die Rezidivrate um durchschnittlich<br />
39% erniedrigt (s. Abb. 8).<br />
Nach Sylvester et al. ist die Frühinstillation die Therapie der Wahl<br />
bei allen Tumoren, allerdings reicht sie allein bei multiplen bzw.<br />
high risk Tumoren nicht aus und benötigt zusätzlich eine<br />
Erhaltungstherapie (s. Kap. 8.3).
Abb. 8:<br />
Ergebnisse der Metaanalyse<br />
über die Frühinstillation (nach<br />
Sylvester at al. 2004)<br />
Die Frühinstillation ist kostensparend. Die Anzahl der Patienten<br />
(number needed to treat, NNT), die behandelt werden müssten,<br />
um ein Rezidiv zu vermeiden beträgt 8,5. Das bedeutet, durch<br />
eine Frühinstillation werden ca. 12 TURs pro 100 Patienten eingespart.<br />
Die Kosten für eine TUR, Anästhesie und Krankenhausaufenthalt<br />
in den meisten europäischen Ländern betragen mehr<br />
als die Kosten für 8,5 Frühinstillationen (Sylvester et. al. 2004).<br />
Die Durchführung der Frühinstillation wird inzwischen auch in den<br />
europäischen Leitlinien (eau) und in den Leitlinien der Deutschen<br />
Krebsgesellschaft empfohlen (Oosterlinck et al. 2002, AWMF<br />
2002).<br />
8.1.1 Worauf muss bei der Frühinstillation geachtet werden?<br />
Die Durchführung der Frühinstillation bei perforierter Blasenwand<br />
ist grundsätzlich kontraindiziert, da sie zu Nekrosen oder irreparablen<br />
Schäden des benachbarten Gewebes führen kann (Doherty<br />
et al. 1999, Cliff et al. 2000, Nieuwenhuijzen et al., 2003,<br />
Oddens et al. 2004).<br />
Die TUR-B kann je nach Größe und Fläche des resezierten Tumors<br />
zu unterschiedlich starken Blutungen führen. Die Durchführung der<br />
Frühinstillation unmittelbar post OP hängt vom Grad der Blutung<br />
ab und den damit verbundenen Operationsgegebenheiten.<br />
Bei geringer Blutung kann die Durchführung der Frühinstillation auf<br />
die Visite am Nachmittag (
28<br />
8.2 Initialtherapie<br />
Abb. 9:<br />
Risikoadaptierte Therapie des<br />
Harnblasenkarzinoms<br />
Abb. 10:<br />
Schematische Darstellung<br />
der Initialtherapie mit<br />
<strong>mito</strong>-<strong>medac</strong> ® /<strong>mito</strong>-extra ®<br />
(F*= Frühinstillation mit<br />
<strong>mito</strong>-extra ® )<br />
Im Anschluss an die in der Klinik erfolgte Frühinstillation mit 40 mg<br />
Mitomycin (z.B. <strong>mito</strong>-extra ® ) sollte eine risikoadaptierte Therapie<br />
durchgeführt werden, d.h. beim intermediate risk Tumor Weiterbehandlung<br />
mit Mitomycin 20 bzw. 40 mg und beim high-risk<br />
Tumor T1G3 und/oder Carcinoma in situ Weiterbehandlung mit<br />
BCG. Wenn BCG kontraindiziert ist oder nicht vertragen wird,<br />
kann alternativ mit 40 mg Mitomycin (<strong>mito</strong>-extra ® ) instilliert werden<br />
(Baselli & Greenberg 2001; Gårdmark et al. 2004)<br />
(s. Abb. 9).<br />
Die Initialtherapie mit Mitomycin sollte 4 Wochen nach TUR und<br />
Frühinstillation beginnen.<br />
Ziel und Sinn der Initialtherapie ist die Behandlung von Resttumoren<br />
und die damit verbundene Reduktion der Frührezidive<br />
(Rübben & Otto, 2001).<br />
Bei der Initialtherapie werden in der Regel 8 Instillationen<br />
in wöchentlichem Abstand durchgeführt (Soloway 1985,<br />
Schwaibold et al. 1997, Witjes et al. 1998, Brausi et al. 1998,<br />
Malmström 2002) (s. Abb. 10).
8.2.1 Warum 40 mg Mitomycin?<br />
Abb. 11:<br />
Konzentrationsunterschiede<br />
nach Instillation mit 20 bzw.<br />
40 mg Mitomycin (nach Gao<br />
et al. 1998)<br />
Die großen internationalen Studien zur Frühinstillation sind, sofern<br />
sie mit Mitomycin durchgeführt wurden, entweder mit 30 oder mit<br />
40 mg dosiert worden (Bouffioux et al. 1995, Tolley et al. 1996,<br />
Solsona et al. 1999, Kaasinen et al. 2002). Es gibt keine Studie<br />
zur Frühinstillation, bei der eine Dosierung von 20 mg eingesetzt<br />
wurde. In Deutschland ist seit über 25 Jahren die 20 mg-Form in<br />
der adjuvanten Therapie zugelassen und bewährt. Im Ausland sind<br />
jedoch vielfach 30 oder 40 mg Dosierungen üblich (40 mg:<br />
Skandinavien, Spanien, England, Italien; 30 mg: Holland).<br />
Pharmakokinetische Daten sprechen ebenfalls für eine bessere<br />
Wirksamkeit der höheren Dosierung (Gao 1998, Au 2001).<br />
Gao et al. 1998, untersuchten die Konzentration von Mitomycin im<br />
Urothel nach Instillation mit 20 bzw. 40 mg Mitomycin an humanen<br />
Blasen. Sie stellten fest, dass sich durch die Instillation von 40 mg<br />
Mitomycin fast die doppelte Konzentration im Urothel erreichen<br />
ließ (s. Abb. 11).<br />
Den Konzentrationsabfall in der Blase durch den Verdünnungseffekt<br />
des nachproduzierten Urins lässt sich anhand der nachfolgenden<br />
Tabelle berechnen:<br />
Zulauf an Urin Instillation 20 mg/20 ml Instillation 40 mg/40 ml Faktor<br />
(<strong>mito</strong>-<strong>medac</strong> ® ) (<strong>mito</strong>-extra ® )<br />
+ 50 ml 20 mg/70 ml 40 mg/90 ml 1,57<br />
+ 100 ml 20 mg/120 ml * 40 mg/140 ml 1,68<br />
+ 200 ml<br />
* : 0,17 mg/ml<br />
20 mg/220 ml 40 mg/240 ml * 1,84<br />
29
30<br />
Abb. 12:<br />
Vergleich der Rezidivfreiheit<br />
und rezidivfreien Zeit nach<br />
Behandlung mit 40 bzw.<br />
20 mg Mitomycin<br />
(nach Au et al. 2001)<br />
8.3 Erhaltungstherapie<br />
Bei 100 ml Urin ist die Konzentration von 40 mg Mitomycin<br />
(<strong>mito</strong>-extra ® ) um den Faktor 1,68 höher als von 20mg Mitomycin,<br />
bei 200 ml Urin sogar um fast das Doppelte. Bei 40mg wird<br />
die Konzentration von 0,17 mg/ml erst mit 200 ml Urin erreicht (bei<br />
20 mg bereits mit 100 ml).<br />
Au et al. haben 2001 im Rahmen einer multizentrischen randomisierten<br />
Phase III Studie 209 Patienten mit 20 bzw. 40 mg<br />
Mitomycin für 6 Wochen behandelt.<br />
Es stellte sich heraus, dass der 40 mg-Arm signifikant längere Zeit bis<br />
zum ersten Rezidiv und signifikant weniger Rezidive nach 5 Jahren<br />
Nachbeobachtungszeit zeigte als der 20 mg Arm (s. Abb. 12).<br />
Auch supportive Maßnahmen zur Verbesserung der Effektivität der<br />
Mitomycin-Behandlung sind erwünscht. Die Erhöhung der<br />
Mitomycin-Konzentration durch die Reduktion der Trinkmenge<br />
schon am Abend vor der Instillation und die Stabilisierung der<br />
Substanz durch die Alkalisierung des Urins mit Na-Bikarbonat<br />
(jeweils eine orale Einnahme von 1,3 g am Abend und 30 min vor<br />
der Instillation) tragen entscheidend zur Verbesserung der<br />
Effektivität bei (Au et al. 2001).<br />
Nach der Initialtherapie und anschließenden Zystoskopie fällt die<br />
Entscheidung, ob die intravesikale Therapie im Sinne einer<br />
Erhaltungstherapie fortgesetzt wird.<br />
Im Gegensatz zur Frühinstillation und Initialtherapie, die die Tumorzellimplantation<br />
bzw. die Frührezidive reduzieren soll, ist das Ziel<br />
der Erhaltungstherapie die Reduktion der Spätrezidive (s. Tabelle<br />
gegenüberliegende Seite).
Abb. 13:<br />
Schematische Darstellung<br />
der Erhaltungstherapie mit<br />
<strong>mito</strong>-<strong>medac</strong> ® /<strong>mito</strong>-extra ®<br />
Frühinstillation Gegen die Tumorzellimplantation<br />
Initialtherapie Gegen Resttumoren / frühe Rezidive<br />
Erhaltungstherapie Gegen späte „echte“ Rezidive<br />
Die Erhaltungstherapie wird in der Regel ab dem 4. Monat post OP<br />
einmal im Monat bis zum Ende des dritten Jahres nach TUR<br />
durchgeführt (Schwaibold et al. 1997; Conrad et al. 2004) (s.<br />
Abb. 13).<br />
Huland & Otto 1983 berichteten über eine prospektive multizentrische<br />
Studie mit 58 Patienten.<br />
28 dieser Patienten wurden nach der TUR mit 20 mg MMC alle<br />
2 Wochen für das erste Jahr und einmal im Monat als Erhaltungstherapie<br />
für noch ein Jahr behandelt. Die restlichen 30 bekamen<br />
keine weitere Therapie außer der TUR. Der Unterschied der<br />
Rezidivraten in beiden Gruppen war hoch signifikant. Die Mitomycin-Gruppe<br />
zeigte eine Rezidivrate von 7% verglichen mit 50%<br />
in der Gruppe, die nicht weitertherapiert worden war. Keiner der<br />
Patienten in der Mitomycin-Gruppe zeigte Metastasen oder starb<br />
wegen seiner Blasentumor-Erkrankung. Nur ein Patient dieser<br />
Gruppe entwickelte ein Rezidiv höheren Differenzierungsgrades.<br />
Hamdy et al. stellten in ihrer Publikation 1993 die Frage, ob es sich<br />
lohnt, eine Erhaltungstherapie nach Initialtherapie durchzuführen.<br />
Sie behandelten insgesamt 72 Patienten mit 10 Instillationen zu<br />
40 mg Mitomycin in wöchentlichem Abstand als Initialtherapie,<br />
gefolgt von einer Erhaltungstherapie monatlich mit einer medianen<br />
Zeit von 16 Monaten (11-22 Monate). Die Ergebnisse dieser Studie<br />
zeigten, dass bei 30 Patienten (42%) allein durch die Initialtherapie<br />
und zusätzlich bei 14 weiteren Patienten (19%) durch die<br />
Erhaltungstherapie eine komplette Remission erreicht wurde. Nur<br />
12 Patienten (17%) zeigten eine Rezidivbildung.<br />
Bouffioux et al. konnten 1995 zeigen, dass eine relativ kurze<br />
Erhaltungstherapie von 12 Monaten in Kombination mit der<br />
Frühinstillation bessere Therapieergebnisse erzielen kann im<br />
Vergleich zu einer Erhaltungstherapie von 6 Monaten ohne<br />
Frühinstillation (s. Abb. 14).<br />
31
32<br />
Abb. 14:<br />
Kaplan Meier Kurven der<br />
Therapiegruppen (nach<br />
Bouffioux et al. 1995)<br />
8.3.1 Wie lange soll die Erhaltungstherapie dauern?<br />
Abb. 15:<br />
Kaplan-Meier Überlebensrateverlauf<br />
bei Patienten nach<br />
TUR bis zum ersten Rezidiv<br />
(nach Krege et al. 1996)<br />
Einer der ersten Langzeittherapiestudien wurde von der Arbeitsgruppe<br />
von Krege et al. 1996 publiziert. Diese randomisierte multizentrische<br />
Studie umfasste 337 Patienten mit pTa/T1 G1-G3<br />
außer primär pTaG1 Tumoren. Randomisiert wurde in 3 Gruppen:<br />
TUR-Gruppe Nur TUR, keine weitere Therapie<br />
MMC-Gruppe TUR + Mitomycin 20 mg alle 2 Wochen<br />
im 1. Jahr und 1x monatlich im 2. Jahr<br />
BCG-Gruppe TUR + BCG 6x in wöchentlichem Abstand +<br />
Erhaltungstherapie 1x monatlich für 4 Monate.<br />
Sowohl die MMC- als auch die BCG-Gruppe lieferten signifikant<br />
bessere Ergebnisse gegenüber der TUR-Gruppe (s. Abb. 15).
Tab. 2:<br />
Verteilung der<br />
Studienprotokolle (nach<br />
Schwaibold et al. 1997)<br />
Abb. 16:<br />
Progressionsfreies Überleben<br />
bei high-risk Patienten (nach<br />
Schwaibold et al. 1997)<br />
Die erste Langzeittherapie Studie mit einer Therapiedauer von<br />
3 Jahren wurde von Schwaibold et al. 1997 publiziert. Diese<br />
Gruppe behandelte im Rahmen einer prospektiven multizentrischen<br />
Studie 419 Patienten u.a. mit zwei Mitomycin 20 mg<br />
3-Jahres-Protokollen, einem 20-Wochen Mitomycin 20 mg<br />
Protokoll und einem 3 Jahres Doxorubicin Protokoll. Die mediane<br />
Nachbeobachtungszeit betrug 57 Monate (s. Tab. 2).<br />
M1 3 J. MMC: alle 2 Wochen für 1 J., + weiter alle<br />
4 Wochen für 1. J., + weiter alle 3 Monate für 1 J.<br />
M2 3 J. MMC: 8x in wöchentlichem Abstand, +<br />
1x monatlich bis Ende des 3. Jahres<br />
M3 MMC kurz & intensiv: 1x wöchentlich für 20 Wochen<br />
M4 3 J. Doxorubicin: wie M1<br />
Im Gesamtergebnis dieser Studie zeigte sich ein signifikanter<br />
Unterschied für die Zeit bis zur Progression abhängig vom<br />
Rezidivstatus vor der Behandlung.<br />
Die Mitomycin Gruppe, die 8 mal in wöchentlichem Abstand und<br />
zusätzlich eine Instillation in monatlichem Abstand als<br />
Erhaltungstherapie bekommen hatte, belegte die besten<br />
Ergebnisse. Diese Mitomycin Gruppe war auch überlegen gegenüber<br />
der Doxorubicin-Gruppe, die mit dem gleichen Protokoll therapiert<br />
wurde. Die nach Risikogruppen getrennte Betrachtung des<br />
Progressionsverhaltens zeigen die folgenden beiden Abbildungen<br />
(Abb. 16 & 17):<br />
33
34<br />
Abb. 17:<br />
Progressionsfreies Überleben<br />
bei low-risk Patienten (nach<br />
Schwaibold et al. 1997)<br />
2004 Präsentierten Conrad et al. die Zwischenergebnisse einer<br />
multizentrischen randomisierten Studie mit 373 Patienten mit<br />
TaG2-3 und T1G1-3 Harnblasenkarzinomen.<br />
Die Patienten wurden in drei Gruppen randomisiert: Zwei Gruppen<br />
mit kurzer Therapie und eine Gruppe mit langer Therapie von<br />
3 Jahren:<br />
1. Gruppe kurz (119 Patienten) TUR + Initialtherapie<br />
mit BCG (6x in wöchentlichem Abstand)<br />
2. Gruppe kurz (144 Patienten) TUR + Initialtherapie<br />
mit MMC 20 mg (<strong>mito</strong>-<strong>medac</strong> ® ) (6x in wöchentlichem Abstand)<br />
3. Gruppe lang (110 Patienten) TUR + Initialtherapie wie 2.<br />
mit MMC 20 mg (<strong>mito</strong>-<strong>medac</strong> ® ) + Erhaltungstherapie<br />
(1x pro Monat bis Ende 3. Jahres)<br />
Die Ergebnisse dieser Studie zeigen eine hoch signifikante Überlegenheit<br />
der 3 Jahres-Therapie mit MMC 20 mg (z.B. <strong>mito</strong>-<strong>medac</strong> ® )<br />
gegenüber der kurzen BCG- (p=0,0004) und Mitomycin-Therapie<br />
(p=0,0009) (s. Abb. 18).<br />
Die 3-Jahres Rezidivfreiheitsraten dieser Gruppen lagen bei 86%<br />
für die 3-Jahres MMC-Therapie, 68,6% für die kurze MMC- und<br />
63,5% für die kurze BCG-Therapie.
Abb. 18:<br />
Kaplan-Meier-Analyse der<br />
Rezidivfreiheit bei langer vs.<br />
kurzer Therapie (nach Conrad<br />
et al. 2004)<br />
9 VERGLEICH MIT ANDEREN CHEMOTHERAPEUTIKA<br />
Die Mehrheit der Studien, die sich mit der Chemotherapie des<br />
oberflächlichen Harnblasenkarzinoms beschäftigen, zeigt die<br />
Überlegenheit von Mitomycin gegenüber anderen Chemotherapeutika<br />
(Baseli & Greenberg 2001).<br />
9.1 Mitomycin vs. Doxorubicin<br />
Beide Substanzen werden zur Behandlung des oberflächlichen<br />
Harnblasenkarzinoms eingesetzt. Direkte Vergleichsuntersuchungen<br />
zwischen Mitomycin und Doxorubicin sind selten. Häufig werden<br />
Behandlungsgruppen lediglich nach Chemotherapie oder<br />
Immuntherapie verglichen, wobei in reinen Chemotherapie-<br />
Studien sogar Patienten unter Mitomycin-Behandlung und<br />
Doxorubicin-Behandlung fälschlicherweise gemeinsam ausgewertet<br />
werden (z. B. Bouffioux 1995).<br />
Pode et al. untersuchten 1987 die Hemmung der Adhäsion von<br />
Tumorzellen durch verschiedene Chemotherapeutika, u.a. Mitomycin<br />
und Doxorubicin.<br />
Bereits nach 5 min waren mehr als 80% der Tumorzellen durch die<br />
Wirkung von Mitomycin nicht mehr adhärent. Dagegen benötigte<br />
Doxorubicin über 60 min, um die gleiche Wirkung zu erreichen<br />
(s. Kap. 8.1).<br />
Ausfeld et al. behandelten 1987 insgesamt 120 Patienten mit<br />
Ta/T1 Tumoren mit Mitomycin (60 Pat.) oder Doxorubicin (60 Pat.).<br />
35
36<br />
Abb. 19:<br />
Wahrscheinlichkeit für<br />
Rezidivfreiheit in Tagen (nach<br />
Gustafson et al. 1991)<br />
Die Mitomycin-Gruppe zeigte eine Rezidivrate von 0,35/100<br />
Patienten–Monaten, dagegen zeigte die Doxorubicin-Gruppe eine<br />
Rezidivrate von 1,86/100 Patienten-Monaten.<br />
Gustafson et al. behandelten 1991 60 Patienten mit Ta/T1 G1-3<br />
HBCA mit TUR allein, TUR + Mitomycin oder TUR + Doxorubicin.<br />
Mediane Nachbeobachtungszeit war 47 Monate. Die Senkung der<br />
Rezidivrate durch Mitomycin war signifikant höher als durch<br />
Doxorubicin (p=0,002). Dagegen ergab sich kein signifikanter<br />
Unterschied zwischen der TUR- und Doxorubicin-Behandlungsgruppe<br />
(s. Abb. 19).<br />
Bei der multizentrischen prospektiven Studie von Schwaibold et<br />
al. 1997 konnte die Überlegenheit von Mitomycin gegenüber<br />
Doxorubicin untermauert werden (s. Kap. 8.3, Abb. 16 & 17).<br />
Auch die Leitlinien der American Urological Association (AUA),<br />
publiziert von Smith et al. 1999, bei der es sich im Prinzip ebenfalls<br />
um eine Metaanalyse handelt, kommen zu dem Schluss:<br />
Basierend auf Nachweisen in der Literatur und Sachverständigenmeinung<br />
sind BCG und Mitomycin dem Doxorubicin und<br />
Thiotepa bei der Reduzierung von Rezidiven überlegen.<br />
Auch das Nebenwirkungsprofil spricht für Mitomycin. Die folgende<br />
Tabelle zeigt die Häufigkeit von Chemocystitis in verschiedenen<br />
Studien:
9.2 Mitomycin vs. Epirubicin<br />
CHEMOCYSTITIS<br />
MITOMYCIN (%) DOXORUBICIN (%)<br />
Niijima 1983 11 31<br />
Akaza 1987 27 25-37<br />
Tsushima 1987 4 3<br />
Ausfeld 1987 18 19<br />
Rübben 1988 - 38<br />
Huland 1990 12-25 48<br />
Gustafson 1991 45 60<br />
Thraser 1992 6-41 4-56<br />
Boufioux 1995 6 9<br />
Epirubicin, ein Doxorubicin-Derivat, besitzt den gleichen Wirkungsmechanismus<br />
und ähnliche Wirkung wie Doxorubicin (Ramanathan-Girisch<br />
u. Boroujerdi 2001).<br />
Es gibt aber kaum Publikationen, die direkt beide Substanzen vergleichen.<br />
Es wird angenommen, dass die Wirksamkeit sowohl von<br />
Mitomycin als auch von Epirubicin (EPI) ähnlich ist.<br />
Da Silva et al. haben 1992 im Rahmen einer Phase III Studie, die<br />
allerdings nie zu Ende geführt wurde, 60 Patienten mit Mitomycin<br />
(n=28) oder Epirubicin (n=32) behandelt. Die MMC-Gruppe wurde<br />
mit 30 mg MMC zunächst für 4 Wochen und weiter 1x monatlich<br />
für 12 Monate instilliert. Die EPI-Gruppe wurde mit 50 mg EPI<br />
genauso wie die MMC-Gruppe therapiert. Follow-up war 17,7<br />
Monate für die EPI-Gruppe und 16,2 Monate für die MMC-<br />
Gruppe. Diese Arbeitsgruppe konnte zwar eine leicht höhere<br />
Remissionsrate bei der MMC-Gruppe von 64,2% vs. 62,5% bei<br />
der EPI-Gruppe feststellen, die allerdings keinen signifikanten<br />
Unterschied darstellt.<br />
10 MITOMYCIN VS. IMMUNTHERAPEUTIKA<br />
10.1 Mitomycin vs. BCG<br />
Der Vergleich beider Substanzen war und ist Mittelpunkt einer kontroversen<br />
Diskussion. Es sind bislang mehrere Arbeiten und<br />
Metaanalysen mit zum Teil konträren Ergebnissen publiziert worden.<br />
Welche der beiden Substanzen zeigt aber die bessere<br />
Wirkung und bei welchen Tumoren?<br />
37
38<br />
Diese Frage kann im Rahmen der risikoadaptierten Therapie nach<br />
entsprechend kritischer Analyse der Publikationen beantwortet<br />
werden<br />
Nach den Empfehlungen der eau sollte Mitomycin für die lowbzw.<br />
intermediate-risk Tumoren und BCG für die high-risk<br />
Tumoren risikoadaptiert verwendet werden (s. Abb. unten)<br />
In der Literatur sind bislang zu diesem Punkt unterschiedliche<br />
Ergebnisse publiziert worden.<br />
Debruyne et al. (1988) haben 308 Patienten mit primären oder<br />
rezidivierenden HBCA (inkl. CIS) mit BCG RIVM (165 Patienten)<br />
und Mitomycin 30 mg (160 Patienten) behandelt.<br />
44 (29,8%) Patienten der BCG-Gruppe und 40 (25%) der<br />
Mitomycin-Gruppe zeigten ein Rezidiv. Dieser Unterschied war<br />
nicht signifikant.<br />
Krege et al. (1996) untersuchten 337 Patienten mit oberflächlichem<br />
HBCA (pTaG2-3 und pT1G1-3), die in drei Therapiearme<br />
randomisiert wurden:<br />
A: Kontrolle (nur TUR)<br />
B: TUR + <strong>mito</strong>-<strong>medac</strong> ® 14-tägig im 1. Jahr, danach 1x monatlich<br />
im 2. Jahr<br />
C: TUR + BCG Connaught 1x wöchentlich für 6 Wochen, danach<br />
1x monatlich für 4 Monate<br />
Dabei wurde nach Ersttumor/Rezidiv sowie den behandelnden<br />
Kliniken stratifiziert. In den Kriterien Stadium, Grading,<br />
Tumorgröße und –anzahl wurde dadurch eine weitgehende<br />
Gleichverteilung erreicht. Von der Untersuchung waren Patienten<br />
mit Stadium pTaG1 ausgeschlossen, so dass hauptsächlich<br />
Patienten mit Risiken hinsichtlich Rezidivneigung und Progress<br />
behandelt wurden.
Abb. 20:<br />
Kaplan-Meier Kurven für<br />
Rezidivtumoren. Zeit in<br />
Monaten bis zum Rezidiv<br />
(nach Krege et al. 1996)<br />
Die Ergebnisse der Untersuchung zeigten keine signifikante<br />
Unterschiede zwischen den MMC/BCG Therapiearmen in der<br />
Behandlung von Ersttumoren. Auffällig war jedoch, dass im MMC-<br />
Arm erst nach Beendigung der Instillationstherapie ein Anstieg der<br />
Rezidivrate zu verzeichnen war, was für eine lange<br />
Erhaltungstherapie spricht.<br />
In der Behandlung von Rezidivtumoren konnte hingegen ein signifikanter<br />
Vorteil der MMC-Instillation hinsichtlich der Rezidivrate<br />
festgestellt werden. Die Wahrscheinlichkeit, rezidivfrei zu bleiben,<br />
betrug für Patienten mit MMC-Therapie ca. 60%, bei BCG 47%<br />
und bei alleinigen TUR nur 24%. Somit scheinen die mit BCG<br />
behandelten Patieten im Vergleich zur alleinigen TUR nicht von der<br />
Art der Prophylaxe zu profitieren (s. Abb. 20).<br />
Die Progressionsraten lagen für die alleinige TUR bei 6,1%, für<br />
BCG bei 4,5% und für MMC bei 2,0%. Diese Unterschiede sind<br />
jedoch nicht signifikant.<br />
Vegt et al. haben 1995 im Rahmen einer randomisierten Studie<br />
die Wirkung von MMC mit BCG-RIVM und BCG-Tice bei 437<br />
Patienten mit primären oder rezidivierenden pTa, pT1 Tumoren<br />
und CIS untersucht. 148 Patienten wurden mit 30 mg MMC 4x in<br />
wöchentlichem Abstand und danach 1x im Monat für 6 Monate<br />
therapiert. 149 Patienten wurden mit BCG-RIVM und 140<br />
Patienten mit BCG-Tice 6x in wöchentlichem Abstand behandelt.<br />
Bei papillären Tumoren waren MMC und BCG-RIVM gleich wirksam<br />
(p=0,53), MMC war allerdings effektiver als BCG-Tice<br />
(p=0,01) (s. Abb. 21).<br />
39
40<br />
Abb. 21:<br />
Kaplan-Maier Kurve des<br />
Anteils krankheitsfreier<br />
Patienten (Nach Vegt et al.<br />
1995).<br />
Eine weitere Studie, die sich mit dem Vergleich von Mitomycin und<br />
BCG befasste, war die von Witjes et al. 1993. 437 Patienten mit<br />
pTa, pT1 und CIS Blasentumoren wurden entweder mit 30 mg<br />
Mitomycin (156 Pat.) oder BCG-RIVM (159 Pat.) oder BCG-Tice<br />
(154 Pat.) therapiert.<br />
Bei dieser Studie konnten keine signifikanten Unterschiede beim<br />
krankheitsfreien Überleben zwischen den drei Armen festgestellt<br />
werden.<br />
Bei papillären Tumoren war BCG nicht besser als MMC. Letzteres<br />
konnte sogar bei G3 Tumoren grenzwertige Signifikanz erreichen<br />
(p=0,05). Die MMC-Gruppe zeigte auch die geringere Toxizität<br />
bzw. Nebenwirkungen.<br />
1998 hat die gleiche Gruppe eine weitere Studie zum Vergleich<br />
von Mitomycin 30 mg und BCG (Stämme RIVM & Tice) veröffentlicht.<br />
Die Ergebnisse der Studie aus dem Jahr 1993 konnten<br />
bestätigt werden.<br />
Die Effizienz von Mitomycin und BCG-RIVM (z.B. BCG-<strong>medac</strong>)<br />
im Bezug auf die Rezidivrate papillärer Tumoren war ähnlich<br />
(p=0,53) wohl aber signifikant besser verglichen mit BCG-Tice<br />
(p=0,01). Mitomycin zeigte eine leichte Überlegenheit bei<br />
papillären Tumoren gegenüber BCG. In puncto Progression war<br />
Mitomycin effektiver bei Patienten ohne CIS, BCG dagegen besser<br />
bei Patienten mit CIS (s. Abb. 22).
Abb. 22:<br />
Kaplan-Meier Diagramm des<br />
Progressionsverlaufs von<br />
Patienten ohne CIS (A) und<br />
Patienten mit CIS (B) (nach<br />
Witjes et al. 1998)<br />
Malmström et al. (1999) behandelten 250 Patienten mit primärem<br />
CIS, Dysplasie G2, T1G3 und häufig rezidivierenden Ta T1<br />
G1-2 Tumoren mit Mitomycin 40 mg und BCG (Dänischer Stamm<br />
1331) für 2 Jahre. Nachbeobachtungszeit war 64 Monate.<br />
BCG zeigte ein signifikant besseres krankheitsfreies Überleben<br />
(p=0,04), jedoch nicht bei Patienten mit CIS (p=0,07). Keine<br />
Unterschiede sind bei Progression und Gesamtüberleben festgestellt<br />
worden (s. Abb. 23).<br />
41
42<br />
Abb. 23:<br />
Krankheitsfreies Überleben bei<br />
allen Patienten (A), bei<br />
Patienten mit papillären<br />
Tumoren (B) und Patienten mit<br />
CIS (C) (nach Malmström et<br />
al. 1999).
Die Wirkung von Mitomycin und BCG wurde auch durch<br />
Metaanalysen genauer untersucht.<br />
Sylvester et al. veröffentlichten 2002 eine erste Metaanalyse<br />
über die Effektivität von BCG vs. TUR allein und BCG gegen<br />
Chemotherapie (u.a. Mitomycin). Diese Metaanalyse umfasste<br />
24 Studien mit insgesamt 4.863 Patienten. Ein positiver Effekt bei<br />
der Senkung der Progressionsrate konnte nur mit Erhaltungstherapie<br />
gezeigt werden (9,8% mit BCG vs. 13,8% ohne BCG).<br />
6 Studien wurden zum Vergleich BCG vs. Mitomycin herangezogen.<br />
Es konnte kein signifikanter Unterschied bei der Senkung der<br />
Progression festgestellt werden (9,3% mit BCG vs. 7,4% mit<br />
Mitomycin). Es konnte auch kein Unterschied bei der Überlebensrate<br />
festgestellt werden (26,7% ohne BCG vs. 23,2% mit BCG).<br />
Die Effizienz von BCG begrenzt sich auch bei den high-risk<br />
Tumoren.<br />
Böhle et al. publizierten 2003 eine Metaanalyse von 11 Studien<br />
und 2.749 Patienten zum Vergleich von BCG und Mitomycin und<br />
der Toxizität beider Therapien.<br />
Zu dieser Metaanalyse wurden auch unpublizierte Daten und auch<br />
Studien der Qualitätstufe B herangezogen. Es konnte ein positiver<br />
Effekt zugunsten von BCG festgestellt werden (38,5% vs. 46,4 %<br />
Rezidive in 24 Monaten). Dieser positive Effekt konnte aber nur<br />
festgestellt werden, wenn eine Erhaltungstherapie durchgeführt<br />
wurde. Man benötigt mindestens 12 BCG Instillationen, um einen<br />
Vorteil gegenüber Mitomycin zu erreichen. Die Toxizität von BCG<br />
war signifikant höher als die des Mitomycins (53,8% vs. 39,2%<br />
p= 0,001).<br />
2003 stellte die Arbeitsgruppe von Shelley ebenfalls eine Metaanalyse<br />
zum Vergleich beider Therapien vor.<br />
Die Autoren führten ein systematisches Review und eine<br />
Metaanalyse zum Vergleich von intravesikalem Mitomycin und<br />
Bacillus Calmette-Guerin in Bezug auf Tumorrezidiv, Progression<br />
und Gesamtüberleben bei Ta und T1 Blasenkarzinom durch.<br />
Behandlungsbedingte Toxizitäten sollten ebenfalls ausgewertet<br />
werden.<br />
Es wurde eine umfassende Suche in den Datenbanken MEDLINE,<br />
EMBASE, Healthstar, Cochrane Controlled Trials Register,<br />
Cancerlit und DARE durchgeführt. Zusätzlich wurden alle relevanten<br />
Zeitschriften von Hand durchsucht.<br />
Studien aller Sprachen wurden in die Metaanalyse aufgenommen<br />
sofern sie sauber randomisiert waren, intermediate bis high risk<br />
Patienten mit Ta oder T1 Blasenkarzinom umfassten und intravesikales<br />
MMC mit BCG verglichen.<br />
Die Eignung der Studien, deren methodische Qualität und<br />
Datenherkunft wurde unabhängig von 2 Reviewern eingeschätzt.<br />
Die Zeit bis zum Ereignis wurde mittels log hazard ratios analysiert<br />
43
44<br />
und eine Sensitivitätsanalyse für Subgruppen entsprechend dem<br />
Rezidivrisiko durchgeführt.<br />
25 Artikel wurden gefunden, aber nur 7 wurden als geeignet<br />
betrachtet. Diese umfassten insgesamt 1.901 Patienten, 820 randomisiert<br />
zu Mitomycin und 1.081 zu BCG. 6 Studien hatten ausreichend<br />
Daten für eine Metaanalyse und umfassten 1.527<br />
Patienten, 693 im Mitomycin-Arm und 834 im BCG-Arm. Das mittlere<br />
gewichtete log hazard ratio (Varianz) für ein Tumorrezidiv dieser<br />
6 Studien war –0,022 (0,005). Dies war nicht signifikant zwischen<br />
MMC und BCG (p = 0,76). Allerdings zeigte die Metanalyse signifikante<br />
Heterogenität zwischen den einzelnen Studien (p = 0,001).<br />
Eine Subgruppenanalyse von 3 Studien, die nur high risk Ta und<br />
T1 Patienten enthielten, zeigte keine Heterogenität (p = 0,25) und<br />
die log hazard ratio (Varianz) für ein Rezidiv von -0.371 (0,012).<br />
Nimmt man Mitomycin als Kontrolle in der Metaanalyse, zeigt eine<br />
negative Ratio einen Vorteil von BCG an, der in diesem Fall hoch<br />
signifikant ist (p = 0,0008).<br />
Die siebte Studie, die nur in Abstract-Form publiziert ist, benutzte BCG<br />
low dose in zwei Armen (27 mg und 13,5 mg) im Vergleich zu einer<br />
Standarddosis Mitomycin (30 mg). Sie gab eine signifikant reduzierte<br />
Rezidivrate mit BCG 27 mg im Vergleich zu Mitomycin an (p = 0,001).<br />
Nur zwei Studien lieferten genügend Daten zur Analyse der<br />
Progression und des Überlebens. Diese repräsentierten 681<br />
Patienten, 338 BCG und 343 MMC. Hier gab es keinen signifikanten<br />
Unterschied zwischen MMC und BCG für Progression (log<br />
hazard ratio und Varianz: 0,044 + 0,04, p = 0,16) und für Überleben<br />
(-0,112 + 0,03 p = 0,5). Lokale Nebenwirkungen (Dysurie,<br />
Zystitis, Pollakisurie und Hämaturie) waren sowohl mit MMC (30%)<br />
als auch BCG (44%) assoziiert. Systemische Nebenwirkungen wie<br />
Schüttelfrost, Fieber und allgemeines Krankheitsgefühl waren mit<br />
MMC und BCG zu 12 bzw. 19% assoziiert, wobei Hautausschläge<br />
häufiger bei Mitomycin vorkamen.<br />
Die Daten der vorliegenden Metaanalyse zeigen, dass ein<br />
Tumorrezidiv mit BCG im Vergleich zu MMC signifikant nur in der<br />
Subgruppe der high risk Patienten reduziert werden kann.<br />
Es gab jedoch keinen Unterschied in Bezug auf Tumorprogression<br />
oder Überleben und die Entscheidung, welche Substanz verwendet<br />
wird, könnte von Nebenwirkungen und Kosten abhängig<br />
gemacht werden.<br />
Huncharek & Kupelnick haben 2003 die Auswirkung der<br />
Chemotherapie vs. BCG bei rezidivierendem oberflächlichem<br />
Harnblasenkarzinom genauer untersucht.<br />
In dieser Arbeit wurde eine Metaanalyse zur Untersuchung der<br />
existierenden Daten zu dieser Thematik durchgeführt, um den<br />
relativen Effekt beider Behandlungsmodalitäten auf das Tumorrezidiv<br />
zu quantifizieren. Ein prospektives Protokoll für die Metaanalyse<br />
wurde entwickelt, gefolgt von einer sorgfältigen Recherche der
Abb. 24:<br />
Mitomycin-Vorteil bei unbehandelten<br />
(virginellen)<br />
Patienten (nach Huncharek et<br />
al. 2003)<br />
publizierten Literatur mit strengen Auswertekriterien. 9 randomisierte<br />
Studien wurden gefunden, die die Spezifikation des<br />
Protokolls erfüllten. Diese beinhalteten Daten von 2261 Patienten,<br />
die statistisch kombiniert wurden mit dem Peto-Modell. Endpunkt<br />
war der Anteil von Patienten mit Rezidiven nach 1, 2 und 3 Jahren<br />
intravesikaler Therapie (d.h. eine „Summen odds ratio“, ORp).<br />
Bei der Kombination aller 9 Studien zum 1-Jahres-Rezidivzeitpunkt<br />
zeigte sich eine kombinierte odds ratio zum Vorteil von BCG<br />
von 0,89 bei allerdings signifikanter statistischer Heterogenität.<br />
Letztere schließt ein statistisches Pooling der Daten aus. Es wurde<br />
daraufhin eine Sensitivitätsanalyse durchgeführt, um die Ursache<br />
für die Heterogenität zu finden. Es zeigte sich, dass eine<br />
Vorbehandlung der Patienten mit Chemotherapie in einer großen<br />
Zahl der randomisierten Studie einen Bias zugunsten von BCG<br />
bewirkte. Nachdem die Daten nach Vorhandensein und nicht<br />
Vorhandensein einer Vorbehandlung mit intravesikaler Chemotherapie<br />
stratifiziert wurden, zeigte die intravesikale Chemotherapie<br />
eine Reduktion der 1, 2 und 3 Jahresrezidive von 21-82%<br />
gegenüber BCG, abhängig vom Endpunkt.<br />
Die zur Verfügung stehenden Daten zeigen, dass klinische<br />
Untersuchungen, die intravesikales BCG mit intravesikaler<br />
Chemotherapie vergleichen, nach Vorhandensein oder nicht<br />
Vorhandensein einer Vortherapie mit Chemotherapie stratifiziert<br />
werden müssen. Rezidive nach Vorbehandlung mit intravesikaler<br />
Chemotherapie sprechen schlechter auf eine erneute Chemotherapie<br />
an als chemotherapie-naive Patienten (s. Abb. 24).<br />
Die z.Zt. empfundene Überlegenheit der BCG-Therapie könnte<br />
daher ein Artefakt dieses Phänomens sein, weil die meisten randomisierten<br />
Studien auch Chemotherapie-Versager in ihre<br />
Chemotherapie-Behandlungsarme randomisiert haben.<br />
45
46<br />
Abb. 25:<br />
Überlebensraten unter<br />
Therapie mit MMC 40 mg und<br />
BCG (nach Gardmark et al.<br />
2004)<br />
Bei der Arbeit von Gårdmark et al 2004 wurden 261 Patienten<br />
(T1G3, CIS und oft rezidivierende Ta/T1G1-2) entweder mit<br />
Mitomycin 40 mg (z.B. <strong>mito</strong>-extra ® ) oder mit BCG 2 Jahre lang<br />
therapiert. Nachbeobachtungszeit war 10 Jahre.<br />
Beide Arme wurden wie folgt therapiert:<br />
6x Initialtherapie + Erhaltungstherapie (1x monatlich für das<br />
1. Jahr + 1x alle 3 Monate für das 2. Jahr).<br />
Es ergaben sich keinerlei statistische Signifikanzen in den durchgeführten<br />
Analysen (s. Abb. 25).<br />
10.2 Mitomycin vs. Interferon<br />
Interferon (INF) wurde in mehreren Studien für die intravesikale<br />
Prophylaxe gegen das oberflächliche Harnblasenkarzinom verwendet.<br />
1992 wurden von Engelmann et al. 67 Patienten mit rezidivierendem<br />
pTa G1-G3 zu pT1G1-G3 Tumoren in drei Gruppen<br />
randomisiert und mit INF 10 MU (22 Pat.), INF 10MU + Mitomycin<br />
20 mg (22 Pat.) oder Mitomycin 20 mg allein (23 Pat.) behandelt.<br />
Nach einem medianen Followup von 6,5 Monaten zeigte sich,<br />
dass die Kombinationstherapie bessere Ergebnisse als die<br />
Monotherapie erzielte (0/22 Rezidive vs. 4/22 bei der INF-Gruppe<br />
und 5/23 bei der Mitomycin Gruppe).<br />
Boccardo et al. behandelten 1994 287 Patienten mit primären<br />
pTaG2 und pT1G1-2 nach TUR entweder mit Mitomycin 40 mg<br />
oder mit Interferon-alpha2b (50x106 IU) 8x in wöchentlichem<br />
Abstand.
10.3 Mitomycin vs. KLH<br />
Die Mitomycin-Gruppe zeigte bei der Reduzierung der Rezidivrate<br />
die besseren Ergebnisse als die Interferon-Gruppe. Die mediane<br />
Zeit bis zum ersten Rezidiv lag bei der Mitomycin-Gruppe bei 36<br />
Monate vs. 21 Monate bei der Interferon-Gruppe (p=0,04).<br />
Malmström publizierte 2002 die Ergebnisse einer Phase II<br />
Studie über die Wirkung von Mitomycin 40 mg/40 ml NaCl und<br />
drei Dosierungen von Interferon-� (30, 50, 80 MU) bei 115<br />
Patienten mit multifokalen Ta T1 G1-2 primären oder rezidivierenden<br />
Harnblasentumoren.<br />
Mitomycin-Patienten wurden nur für 8 Wochen, Interferon-<br />
Patienten hingegen für 12 Wochen therapiert. Bei kompletter<br />
Remission in der Woche 9 wurde die Interferon-Therapie allerdings<br />
gestoppt.<br />
Die Mitomycin-Gruppe erreichte die höchste Remissionsrate von<br />
72%, verglichen mit 43% unter der höchsten Dosis von Interferon-�<br />
(100 MU).<br />
Die Autoren berichten, dass die Mitomycin Konzentration von 1,0<br />
mg/ml u.a. auch für die guten Ergebnisse dieser Studie verantwortlich<br />
war. Im Vergleich dazu verwendeten andere Studien niedrigere<br />
Konzentrationen von 0,6 bis max. 1,0 mg/ml (Bird et al.<br />
2001).<br />
Zwischen beiden Therapeutika existieren kaum Vergleichsdaten<br />
im Rahmen von großangelegten Studien. Zwar konnte Jurincic<br />
et al. 1988 eine signifikant bessere Wirksamkeit von KLH (10 mg)<br />
gegenüber MMC (20 mg) in puncto Rezidivrate (14,2% für KLH vs.<br />
39,1% für MMC) feststellen, hatte aber realtiv geringe Patientenzahlen<br />
(insgesamt 44 Patienten, 21 für die KLH-Gruppe und 23 für<br />
die MMC-Gruppe). Neuere Daten sind zu diesem Thema noch<br />
nicht vorhanden.<br />
11 KOMBINATIONSTHERAPIEN<br />
11.1 Mitomycin und BCG<br />
Die Kombinationstherapie von Mitomycin mit anderen Chemound/oder<br />
Immuntherapeutika (sequenziell oder nicht) war<br />
Gegenstand anderer Studien.<br />
Van der Meijden et al. behandelten 1996 35 Patienten mit multiplen<br />
pTa/T1 Tumoren mit 4 Instillationen Mitomycin 40 mg in<br />
wöchentlichem Abstand, die von 6 Instillationen BCG (Stamm<br />
RIVM) in wöchentlichem Abstand gefolgt wurden.<br />
47
48<br />
Abb. 26:<br />
Therapieablauf der Initialund<br />
Sequenzialtherapie.<br />
R: Randomisierung,<br />
M: Mitomycin, B: BCG<br />
Abb. 27:<br />
Krankheitsfreies Intervall mit<br />
Mitomycin und Mitomycin +<br />
BCG (nach Rintala et al.<br />
1996)<br />
Eine komplette Remission wurde bei 16 der 35 Patienten beobachtet.<br />
Ein Patient zeigte Progression.<br />
Rintala et al. haben 1996 im Rahmen einer Studie 182 Patienten<br />
mit schnell rezidivierenden Ta/T1 zunächst 5x mit Mitomycin als<br />
Initialtherapie behandelt. Nach einer Randomisierung in zwei<br />
Gruppen wurden 90 Patienten mit Mitomycin (20-40 mg je nach<br />
Blasenkapazität) und 92 Patienten sequenziell mit Mitomycin und<br />
BCG (Stamm Pasteur) für 2 Jahren instilliert (s. Abb. 26).<br />
Medianes Follow up war 24 Monate.<br />
Obwohl die Mitomycin-Gruppe eine leichte Überlegenheit bei der<br />
Zeit bis zum ersten Rezidiv zeigte (12 vs. 7 Monate der Gruppe 2),<br />
war dieser Unterschied nicht signifikant (p=0,97). Ähnlich konnte<br />
auch kein signifikanter Unterschied bei der Rezidivrate (p=0,37)<br />
und beim krankheitsfreien Intervall (p=0,97) dokumentiert werden<br />
(s. Abb. 27).<br />
1998 veröffentlichte die Gruppe von Witjes et al. die Ergebnisse<br />
einer Studie mit 182 Patienten mit intermediate und high risk<br />
Blasentumoren randomisiert in zwei Gruppen. Gruppe 1 wurde 4x<br />
mit Mitomycin 40 mg und anschließend 6x mit BCG jeweils in<br />
wöchentlichem Abstand behandelt. Gruppe 2 wurde mit 10x
Abb. 28:<br />
Kaplan-Meier Kurven für das<br />
krankheitsfreie Überleben<br />
(nach Witjes et al. 1998)<br />
Mitomycin in wöchentlichem Abstand therapiert. Die Ergebnisse<br />
dieser Studie zeigten keinen signifikanten Unterschiede beim rezidivfreien<br />
Überleben (p= 0,53).<br />
Im Rahmen einer multizentrischen, prospektiven, randomisierten<br />
Studie (CUETO 93008) untersuchten Solsona et al. 2002 405<br />
Patienten mit multiplen oder rezidivierenden Tumoren TaG2-G3<br />
bzw. T1G1-3 und CIS.<br />
Im Arm A wurden 153 Patienten 6x in wöchentlichem Abstand mit<br />
Mitomycin instilliert gefolgt von einer 24 h späteren BCG-<br />
Instillation. Im Arm B wurden 173 Patienten mit BCG 6x in<br />
wöchentlichem Abstand instilliert.<br />
Obwohl eine signifikante Reduktion der Rezidivrate im Arm A<br />
erreicht wurde, konnte keine signifikante Reduktion der<br />
Progression festgestellt werden. Das ist ein sehr wichtiger Faktor<br />
vor allem für high-risk Patienten. Durch die hohen Toxizitätsraten,<br />
die beim Arm-A beobachtet wurden, ist dieses Therapieschema<br />
für high-risk Patienten nicht empfehlenswert.<br />
Kaasinen et al. publizierten 2003 die Ergebnisse einer Studie mit<br />
304 CIS-Patienten, die mit Mitomycin und BCG sequenziell oder<br />
mit BCG allein behandelt wurden.<br />
Beide Gruppen wurden 6x in wöchentlichem Abstand + einmal<br />
monatlich für ein Jahr (6x Mitomycin und 6x BCG bei der<br />
Kombinationsgruppe) instilliert.<br />
Bei dieser Studie war die BCG-Monotherapie gegenüber der<br />
sequenziellen Therapie in puncto krankheitsfreier Wahrscheinlichkeit<br />
signifikant überlegen (p=0,03). Es gab allerdings keine signifikanten<br />
Unterschiede in puncto Progression und Überlebensrate<br />
(s. Abb. 28). Die BCG-Monotherapie zeigte signifikant mehr<br />
Nebenwirkungen als die Kombinationstherapie.<br />
49
50<br />
11.2 Mitomycin und Hyperthermie<br />
Bei der Hyperthermie handelt es sich um ein Verfahren, das in der<br />
Lage ist, durch Temperaturerhöhung von 40-44°C in tumortragenden<br />
Körperregionen eine Tumorzellzerstörung zu initialisieren<br />
(Wust et al. 2003, v. der Heijden et al. 2004).<br />
In die Harnblase wird eine Mikrowellen-Sonde eingeführt, die eine<br />
gleichmäßige Temperatur zu gewährleisten vermag (v. d. Heijden<br />
et al. 2004).<br />
In vielen Studien wurde gezeigt, dass die Kombination von<br />
Chemo- & Thermotherapie mehrere Vorteile gegenüber der alleinigen<br />
Chemotherapie bieten kann.<br />
Leib et al. untersuchten 1996 33 Patienten mit Ta/T1 G1-3 in drei<br />
Zentren, die nach TUR randomisiert wurden:<br />
A: Mitomycin 40 mg allein und<br />
B: Mitomycin 40 mg + Hyperthermie (42,5-45°C)<br />
Therapiert wurde 8x in wöchentlichem Abstand plus 4x in monatlichem<br />
Abstand mit einem Follow up von 24 Monaten (inkl. monatlich<br />
Zystoskopien, Biopsien und Zytologie).<br />
Nur einer der Patienten aus der kombinierten Gruppe zeigte ein<br />
Rezidiv, verglichen zu 7 Patienten der Gruppe A, die nur mit<br />
Mitomycin therapiert wurden.<br />
Beide Therapien wurden gut vertragen mit minimalen Nebenwirkungen.<br />
Van der Heijden et al. veröffentlichten 2004 die Zwischenergebnisse<br />
einer Studie mit 90 Patienten mit multiplen oder rezidivierenden<br />
Ta/T1, die nach eau-Kriterien als intermediate oder<br />
high-risk klassifiziert wurden.<br />
Diese Patienten wurden mit einer Kombination von Mitomycin und<br />
Hyperthermie 6-8x in wöchentlichem Abstand behandelt.<br />
Eine Kaplan-Meier Analyse zeigte, dass ein Jahr nach Therapie<br />
nur 14,3% aller Patienten ein Rezidiv hatten. Nach 2 Jahren Nachbeobachtungszeit<br />
lag das Rezidivrisiko bei 24,6%. Es konnte<br />
keine Progression beobachtet werden.<br />
11.3 Mitomycin und EMDA<br />
Die sog. „Elektromotive Drug Administration“ (EMDA) ist eine<br />
zusätzliche Methode zur Verbesserung der Wirkungseffizienz von<br />
Mitomycin.
Brausi et al. instillierten 1998 13 Patienten mit Mitomycin 40 mg<br />
für 2 h und 15 Patienten mit EMDA-Mitomycin 40 mg/15 mA für<br />
20 min 8x in wöchentlichem Abstand. Alle Tumoren wurden vorher,<br />
außer einer Marker-Läsion, per TUR entfernt.<br />
Obwohl eine längere Zeit bis zum Rezidiv bei der EMDA-MMC-<br />
Gruppe zu beobachten war (24,5 vs. 10,5 Monate), gab es keine<br />
signifikanten Unterschiede zwischen den beiden Therapiearmen<br />
hinsichtlich der Remissionsrate (41,6 vs. 40%). Die relativ kleine<br />
Patientenzahl könnte dafür der Grund sein.<br />
Di Stasi et al. haben 2003 die passive Mitomycin- bzw. BCG-<br />
Applikation mit der EMDA-Mitomycin-Applikation verglichen.<br />
Sie behandelten 108 Patienten mit multifokalen CIS und T1<br />
Tumoren mit EMDA-MMC 40 mg/20 mA für 30 min oder 40 mg<br />
MMC passiv für 60 min oder BCG für 60 min.<br />
Als Therapieschema wurden 6x wöchentliche Instillationen und 6<br />
weitere monatliche Instillationen durchgeführt.<br />
Die komplette Remissionsrate von EMDA-MMC vs. passiver MMC<br />
lag nach 3 und 6 Monaten bei 53% vs. 28% und 58% vs. 31%<br />
entsprechend. Bei der BCG Gruppe lag die komplette<br />
Remissionsrate bei 56% und 64%. Die mediane Zeit bis zum<br />
Rezidiv war signifikant unterschiedlich (35 vs. 19,5 Monate)<br />
zugunsten von EMDA-MMC bei den MMC-Gruppen und bei der<br />
BCG-Gruppe 26 Monate. Die Plasmakonzentration lag bei 43 vs.<br />
8 ng/ml bei der EMDA-MMC- vs. passiven MMC-Applikation.<br />
Das Spektrum der Nebenwirkungen war bei der BCG-Gruppe signifikant<br />
höher als bei den beiden MMC-Gruppen. Obwohl sich bei<br />
der EMDA-MMC-Gruppe eine Tendenz zu höherer Toxizität zeigte,<br />
gab es insgesamt keine signifikanten Unterschiede zwischen<br />
den beiden MMC-Gruppen.<br />
Die gleiche Gruppe von Di Stasi et al. hat 2004 im Rahmen einer<br />
prospektiven kontrollierten Studie 185 Patienten mit T1G2-3 in<br />
zwei Gruppen randomisiert. Die erste Gruppe wurde mit BCG<br />
6x in wöchentlichen Intervallen behandelt.<br />
Die zweite Gruppe wurde sequenziell mit BCG und EMDA-<br />
Mitomycin in wöchentlichen Intervallen wie folgt therapiert:<br />
(1. Woche: BCG; 2. Woche: BCG; 3. Woche EMDA-MMC) 3x.<br />
Das bedeutet insgesamt 6 Instillationen BCG und 3 Instillationen<br />
EMDA-MMC.<br />
Bei Respondern wurde eine Erhaltungstherapie durchgeführt:<br />
monatlich 9x BCG bei der ersten Gruppe und 3x bei der zweiten<br />
Gruppe.<br />
51
52<br />
Die folgende Tab. zeigt die Ergebnisse dieser Studie:<br />
BCG-Monotherapie EMDA-MMC/BCG Signifikanz<br />
Rezidivrate 48% 28% s. p=0,013<br />
Monate z. 1. Rezidiv 11 20 s. p=0,01<br />
Progression 20% 14 n.s. p=0,312<br />
Monate z. Progression 17 46 s. p=0,02<br />
s. : signifikant/ n.s.: nicht signifikant<br />
Bei allen Parametern war außer der Reduktion der Progression die<br />
sequenzielle EMDA-MMC/BCG Therapie signifikant überlegen.<br />
12 THERAPIE VON TUMOREN DES OBEREN HARNTRAKTS<br />
Karzinome des oberen Harntraktes sind eher selten. Es gibt nur<br />
kleine retrospektive Studien und mit heterogenen Charakteristika.<br />
Die Ursachen für die unterschiedlichen Ergebnisse sind:<br />
1. zu wenig Patienten um eine Signifikanz zu zeigen<br />
2. Nicht genügend Dwell-time bei der Instillation<br />
3. Mögliche Unterschiede zwischen oberen Harntrakt- und Blasentumoren<br />
(O’Donoghue & Crew 2004, Bassi et al. 2001).<br />
Es wird angenommen, dass sich 5% der Urothelkarzinome im<br />
oberen Harntrakt befinden (Tawfiek & Bagley, 1997). Die<br />
Nephroureterektomie stellt die Therapie der Wahl dar. Nur in<br />
Ausnahmefällen kann oder muss eine organerhaltende Behandlung<br />
durchgeführt werden. Nach derartigen organerhaltenden<br />
Behandlungen oberflächlicher Tumoren wird die Rezidivhäufigkeit<br />
auf der ipsilateralen Seite mit 7-28% beschrieben. Tumoren im<br />
kontralateralen oberen Hohlsystem treten in 0,5 bis 2% auf (Blute<br />
et al., 1989; Kantor et al., 1986).<br />
Während die intravesikale Mitomycin-Instillationstherapie oberflächlicher<br />
Urothelkarzinome der Harnblase eine anerkannte und<br />
hoch effektive Therapie darstellt, ist diese Behandlung für<br />
Karzinome im oberen Harntrakt aufgrund der geringen Inzidenz<br />
bisher nicht etabliert. Es liegen in der Literatur diverse Berichte zu<br />
dieser Therapie vor (Hautumm et al., 1982, Smith et al. 1987,<br />
Eastham & Huffman 1993, Seaman et al. 1993, Martinez-<br />
Pineiro et al. 1996, Keeley & Bagley 1997, Patel & Fuchs<br />
1998).<br />
Hautumm et al. untersuchten 1982 in einem Tiermodell die<br />
Bedeutung des Refluxes bei der Rezidivprophylaxe des HBCA.
Tierexperimentel wurden bei 29 Kaninchen Doxorubicin,<br />
Mitomycin und physiol. NaCl mittels retrograder Sondierung in<br />
Harnleiter und Nierenbecken appliziert. Bei mechanisch bedingten<br />
Urothelverletzungen waren subepithelial entzündliche Veränderungen<br />
nachweisbar, die bei Doxorubicin graduell stärker ausgeprägt<br />
waren als bei Mitomycin.<br />
Smith et al berichteten 1987 von zwei Patienten mit rezidivierendem<br />
HBCA, die durch vesikoureteralen Reflux papilläre Tumoren<br />
in den distalen Harnleitern entwickelten. Sie verwendeten<br />
Mitomycin, das durch den Reflux zum Tumor gelangte. Es wurde<br />
keine Toxizität beobachtet und die Patienten waren für mehr als 2<br />
Jahre rezidivfrei.<br />
Eastham & Huffman untersuchten 1993 7 Patienten mit<br />
Tumoren des Nierenbeckens und Harnleiters. Nach operativer<br />
Entfernung der Tumoren durch endoskopische Resektion wurde<br />
Mitomycin 40 mg in 1000 ml Kochsalzlösung als Infusion (50 cc<br />
pro h) in die Blase instilliert. Trotz der kurzen Nachbeobachtungszeit<br />
(6-12 Monate) zeigte keiner von 6 Patienten eine Progression.<br />
Martinez-Pineiro et al. behandelten 1996 14 Patienten mit<br />
Tumoren des oberen Harntraktes mit Mitomycin 40 mg. Die<br />
Rezidivrate konnte auf 14,2% gesenkt werden, verglichen zu<br />
12,5% bei denen, die BCG bekamen (9 Patienten) und 60% bei<br />
Patienten, die Thiotepa erhielten (5 Patienten).<br />
Durch Keeley & Bagley wurden 1997 19 Patienten mit Tumoren<br />
des oberen Harntarktes (21 renale Einheiten) mit Mitomycin 40 mg<br />
behandelt. 11 von diesen Patienten blieben krankheitsfrei. Nach<br />
30 Monaten Follow-up zeigten 6 dieser Patienten Rezidive. 4<br />
Patienten wurden endoskopisch operiert und 7 blieben krankheitsfrei<br />
ohne weitere Eingriffe. Keiner der Patienten zeigte eine<br />
Progression.<br />
13 ZUSAMMENFASSUNG<br />
Die intravesikalle Therapie mit Mitomycin stellt heute eine sehr wirkungsvolle<br />
Möglichkeit für die Therapie des oberflächlichen<br />
Harnblasenkarzinoms dar.<br />
Die Halbierung der Rezidivrate allein durch die Frühinstillation und<br />
die weitere Reduktion durch die konsequente Durchführung der<br />
Initial- und Erhaltungstherapie sprechen dafür, dass Mitomycin (in<br />
20 oder 40 mg Form) die Therapie der Wahl zur Behandlung des<br />
oberflächlichen Harnblasenkarzinoms sein sollte.<br />
53
54<br />
14 STICHWORTVERZEICHNIS<br />
A<br />
B<br />
C<br />
D<br />
E<br />
F<br />
G<br />
H<br />
Seitenzahl<br />
Adhäsion ........................................................... 22, 23, 24, 35<br />
Adriamycin ......................................................................... 07<br />
Alkylantien .......................................................................... 18<br />
Antitumorantibiotika ............................................................ 04<br />
Applikation ............................................................ 4, 9, 20, 51<br />
BCG ............................. 20, 28, 32, 34, 36, 37, 38, 39, 40, 41,<br />
43, 44, 45, 46, 47, 48, 49, 51, 52, 53<br />
Bioreduktive Alkylierung ...................................................... 14<br />
Blasenwand ............................................................ 18, 23, 27<br />
Chemocystitis ............................................................... 36, 37<br />
CIS ................................ 24, 25, 38, 39, 40, 41, 42, 46, 49, 51<br />
Connaught .......................................................................... 38<br />
DNA .............................................................. 5, 14, 15, 16, 18<br />
Doxorubicin .............................. 6, 7, 23, 24, 33, 35, 36, 37, 53<br />
Dwell-time ........................................................... 7, 18, 19, 52<br />
EMDA ..................................................................... 50, 51, 52<br />
Epirubicin ...................................................................... 24, 37<br />
Erhaltungstherapie .. 20, 25, 26, 30, 31, 32, 33, 39, 43, 46, 51, 53<br />
Fibrinbelag ........................................................................ 6, 7<br />
Frühinstillation .. 19, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 53<br />
G1 ................................. 15, 32, 34, 36, 38, 41, 46, 47, 49, 50<br />
Geschlossenes System ................................................... 9, 10<br />
Hämaturie ........................................................................... 44<br />
Hämorrhagisch ................................................................... 05<br />
Haltbarkeit ......................................................................... 8, 9<br />
High risk .................. 19, 20, 26, 28, 33, 38, 43, 44, 48, 49, 50<br />
Hyperthermie ...................................................................... 50
I<br />
K<br />
L<br />
Initialtherapie .................................... 20, 28, 30, 31, 34, 46, 48<br />
Implantationsmetastasen .................................................... 22<br />
Interferon ...................................................................... 46, 47<br />
Intermediate risk .............................. 19, 20, 21, 38, 43, 48, 50<br />
KLH .................................................................................... 47<br />
Katheter .................................................................. 3, 8, 9, 14<br />
Kathetersicherung ............................................................. 3, 8<br />
Langzeittherapie ........................................................... 32, 33<br />
M<br />
Metaanalyse .......................................... 26, 27, 36, 37, 43, 44<br />
Mitomycin-Reduktase ......................................................... 15<br />
Mutamycin .......................................................................... 17<br />
N<br />
Nebenwirkungen ...................................... 5, 18, 40, 44, 49, 51<br />
nekrotisierend ................................................................. 6, 27<br />
O<br />
Oberer Harntrakt ........................................................... 52, 53<br />
P<br />
R<br />
S<br />
Pasteur ............................................................................... 48<br />
pTa ........................................................ 32, 38, 39, 40, 46, 47<br />
pT1 ................................................................... 38, 39, 40, 46<br />
Plasmaspiegel ..................................................................... 18<br />
Plaques .............................................................................. 06<br />
Pharmakokinetik ........................................................... 18, 29<br />
Pollakisurie .......................................................................... 44<br />
Progression ................... 33, 40, 41, 43, 44, 48, 49, 50, 52, 53<br />
Reflux ........................................................................... 52, 53<br />
Rezidiventstehung ............................................................... 26<br />
RIVM ................................................................. 38, 39, 40, 47<br />
S-Phase .............................................................................. 15<br />
Spülflüssigkeit ..................................................................... 22<br />
55
56<br />
T<br />
U<br />
V<br />
Z<br />
Tiermodell ..................................................................... 22, 52<br />
Toxizität ................................................ 4, 7, 15, 40, 43, 51, 53<br />
Trauma ............................................................................... 22<br />
Tumorzellimplantation ............................ 22, 23, 24, 25, 30, 31<br />
Überlebensrate ....................................................... 43, 46, 49<br />
Urinzytologie ....................................................................... 23<br />
Vitamin B6 .......................................................................... 07<br />
Zystitis ........................................................................ 5, 6, 44<br />
Zytotoxizitä ............................................................. 15, 22, 24
15 LITERATURVERZEICHNIS<br />
Albarran J, Imbert L<br />
Les Tumeurs de Rein<br />
Paris: Masson et Cie: 1903 452-459<br />
Ali-El-Dein B, Nabeeh A, El-Baz M, et al.<br />
Single-dose versus multiple instillations of epirubicin as prophylaxis for recurrence<br />
after transurethral resection of pTa and pT1 transitional-cell bladder tumours: a<br />
prospective, randomized controlled study<br />
Br-J-Urol 1997; 79: 731-735<br />
Au JLS, Badalament RA, Wientjes MG, Young DC, Warner JA, Venema PL,<br />
Pollifrone DL, Harbrecht JD, Chin J, Lerner SP, Miles BJ<br />
Methods to improve efficacy of intravesical Mitomycin: results of a randomized<br />
phase III trial<br />
J-Nat-Cancer-Inst; 2001, 93,8: 597-604<br />
Ausfeld R, Beer M, Mühlethaler JP, et al.<br />
Adjuvant intravesical chemotherapy of superficial bladder cancer with monthly<br />
Doxorubicin or intensive Mitomycin<br />
Eur-Urol 1987; 13: 10-14<br />
AWMF: ARBEITSGEMEINSCHAFT DER WISS. MED. FACHGESELLSCHAFTEN<br />
Leitlinien der Deutschen Krebsgesellschaft; Harnblasenkarzinom 2002, 3. Auflage<br />
http://www.uni-duesseldorf.de/WWW/AWMF/ll/032-038.htm<br />
Baselli EC, Greenberg RE<br />
Maintenance Therapy for superficial bladder cancer<br />
Oncology, 2001; 15: 85-91<br />
Bassi P, Iafrate M, Longo F, Ianello A, Mostaccio G, Ingrassia A, Repele M,<br />
Tavolini IM<br />
Intracavitary Therapy of Noninvasive transitional Cell Carcinoma of the Upper<br />
Urinary Tract<br />
Urol-Int 2001; 67: 189-194<br />
Beretta G, Cartei G, Giraldi T.<br />
Mitomycin. Pharmacology and Clinical Trials<br />
Minerva Medica Publishers 1990<br />
Berufsgenossenschaft für Gesundheitsdienst und Wohlfahrtspflege<br />
Merkblatt M620 Sichere Handhabung von Zytostatika 2000<br />
Bird V, Soloway M, Malmström PU.<br />
Intravesical chemotherapy in the treatment of supersicial bladder cancer.<br />
In Droller M ed. Bladder cancer : Current diagnosis and Treatment. Chapt 8.<br />
Tatowa NJ, USA: Humana Press Inc 2001: 183-223<br />
Blute ML, Segura JW, Patterson DE, Benson RC Jr, Zincke H.<br />
Impact of endourology on diagnosis and management of upper urinary tract urothelial<br />
cancer.<br />
J Urol. 1989 Jun;141(6):1298-301.<br />
Boccardo F, Cannata D, Rubagotti A, Guarneri D, Decensi-A et al.<br />
Prophylaxis of superficial bladder cancer with <strong>mito</strong>mycin or interferon Alfa-2b:<br />
Results of a multicentric italian study<br />
J-Clin-Oncol 1994; 12 (1): 7-13<br />
Böhle A, Jocham D, Bock PR<br />
Intravesical Bacillus-Calmette-Guerin versus Mitomycin for superficial bladder<br />
cancer: A formal meta-analysis of comparative studies on recurrence and toxicity<br />
J-Urol 2003; 169: 90 - 95<br />
57
58<br />
Bouffioux C, Kurth KH, Bono A, Oosterlinck W, Boeken Kruger C, De<br />
Pauw M, Sylvester RJ and the EORTC<br />
Intravesical adjuvant chemotherapy for superficial transitional cell bladder carcinoma:<br />
results of 2 European organisation for research and treatment of cancer<br />
randomized trials with Mitomycin and doxorubicin comparing early versus delayed<br />
instillations and short-term versus long-term treatment<br />
J-Urol, 1995; 153: 934 - 941<br />
Brausi M, Campo B, Pizzocaro G, et al.<br />
Intravesical electromotive administration of drugs for treatment of superficial bladder<br />
cancer: a comparative phase II study<br />
Urology, 1998; 51: 506-509<br />
Brown JM<br />
The Hypoxic Cell: A target for selective cancer therapy-18th Bruce F. Cain<br />
Memorial Award Lecture<br />
Cancer Res. 1999; 59: 5863-5870<br />
Burnand KG, Boyd PJR, Mayo ME, Shuttleworth KED, Lloyd-Davies RW<br />
Single dose intravesical Thiotepa as an adjuvant to Cystodiathermy in the treatment<br />
of transitional cell bladder cancer<br />
Br-J-Urol, 1976; 48: 55-59<br />
Cliff AM, Romaniuk CS, Parr NJ,<br />
Perivesical inflammation after early Mitomycin instillation<br />
BJU-International, 2000; 85: 556-557<br />
Conrad S, Friedrich MG, Schwaibold H, Pichlmeier U, Schildt K, Wolf N,<br />
Huland H<br />
Long term prophylaxis with Mitomycin (MCC) further reduces tumor recurrence<br />
compared to short term prophylaxis with MMC or Bacillus Calette-Guerin (BCG)<br />
J-Urol, 2004; 171, 4, Suppl.: Abstr. 271<br />
da Silva FC, Ferrito F, Brandao T, Santos A<br />
4'-epidoxorubicin versus Mitomycin intravesical chemoprophylaxis of superficial<br />
bladder cancer.<br />
Eur Urol, January 1, 1992; 21(1): 42-4.<br />
De Bruijn EA, Sleeboom HP, van Helsdingen PJRO, van Oosterom AT,<br />
Tjaden UR, Maes RAA<br />
Pharmacodynamics and pharmacokinetics of intravesical Mitomycin upon different<br />
dwelling times<br />
Int-J-Cancer 1992; 51: 359-364<br />
DeBruyne FMJ, van der Meijden APM, Geboers ADH et al.<br />
BCG (RIVM) vs. Mitomycin intravesical therapy in superficial bladder cancer. First<br />
results of randomized prospective trial.<br />
Urology 1988; 30: 20<br />
De Furia MD, Bracken RB, Johnson DE, Soloway MS, Merrin CE, Morgan LR,<br />
Miller HC, Crooke ST.<br />
Phase I-II study of Mitomycin topical therapy for low-grade, low stage transitional<br />
cell carcinoma of the bladder: an interim report.<br />
Cancer Treat Rep. 1980; 64(2-3):225-30.<br />
Di Stasi SM, Giannantoni A, Stephen RL, Capelli G, Navarra P, Massoud R,<br />
Vespasiani G<br />
Intravesical electromotive Mitomycin versus passive transport Mitomycin for high<br />
risk superficial bladder cancer: A prospective randomized study<br />
J-Urol 2003; 170: 777-782<br />
Di Stasi SM, Giannantoni A, Stephen RL, Virgili G, Giurioli A, Storti L<br />
Zampa G, Vespasiani G<br />
Sequential intravesical Bacillus Calmette-Guerin and electromotive Mitomycin-C<br />
for high risk superfical bladder cancer: A prospective controlled stude\NLN\<br />
J-Urol 2004; 171, 4, Suppl.: Abstr. 278
Doherty AP, Trendell-Smith N, Stirling R, Rogers H, Bellringer J<br />
Perivesical fat necrosis after adjuvant intravesical chemotherapy<br />
BJU-International, 1999; 83: 420-423<br />
Durek C, Sellmann K, Jocham D, Böhle A<br />
Effekt der Kurzzeit-Exposition von Blasentumorenzellen mit Zytostatika<br />
Urologe (A), 2002; 41, Suppl. 1: S. 21 (DGU-Abstract)<br />
Eastham JA, Huffman JL,<br />
Technique of Mitomycin instillation in the treatment of upper urinary tract urothelial<br />
tumors<br />
J-Urol 1993; 324 - 325<br />
Eijstein A, Knonagel H, Hotz E,<br />
Reduced bladder capacity in patients receiving intravesikal chemoprophylaxis<br />
with Mitomycin.<br />
Br J Urol 1990; 66: 386<br />
Engelmann U, Knopf HJ, Graff J<br />
Interferon-alpha 2b instillation prophylaxis in superficial bladder cancer - a prospective,<br />
controlled three-armed trial<br />
Anti-Cancer-Drugs 1992; 3: 33-37<br />
Flüchter STH, Harzmann R, Hlobil H, Erdmann W, Bichler KH<br />
Lokale Chemotherapie des Harnblasenkarzinoms mit Mitomycin<br />
Urologe (A) Jahr 1982; 21: 24-28<br />
Friedman D, Mooppan UMM, Rosen Y, Kim H<br />
The effect of intravesical instillations of thiotepa, Mitomycin, and adriamycin on<br />
normal urothelium: an experimental study in rats<br />
J-Urol 1991; 145: 1060 - 1063<br />
Gårdmark T, Malmström PU, Wiklund P, Jahnson S, Wijkström H,<br />
Wahlquist R<br />
Long term follow up of a randomized study of BCG versus Mitomycin-C in high<br />
risk superficial bladder cancer<br />
J-Urol, 2004; 171, 4, Suppl.: Abstr. 277<br />
Gao X, Au JLS, Badalament-RA, Wientjes-MG<br />
Bladder tissue uptake of Mitomycin during intravesical therapy is linear with drug<br />
concentration in urine<br />
Clin-Canc-Res 1998; 3: 139 - 143<br />
Gustafson H, Wijkström H, Nyman C, et al.<br />
Prophylactic instillation therapy of superficial bladder cancer<br />
Scan-J-Urol-Nephro-Suppl 1991; 138: 187-191<br />
Hamdy FC, Hastie KJ, Kerry R, Williams JL<br />
Mitomycin-C in superficial bladder cancer. Is long-term maintenance therapy<br />
worthwhile after initial treatment?<br />
Br-J-Urol, 1993; 71: 183-186<br />
Harrison GS, Green DF, Newling DW, Richards B, Robinson MR, Smith PH.<br />
A phase II study of intravesical Mitomycin in the treatment of superficial bladder<br />
cancer.<br />
Br J Urol. 1983; 55(6):676-9.<br />
Hautumm B, Birke F, Grauel H<br />
Experimentelle Untersuchungen zur Bedeutung des Refluxes bei der<br />
Rezidivchemoprophylaxe des Harnblasenkarzinoms<br />
Therapiewoche 1982; 32: 515-519<br />
Heney NM, Koontz WW, Barton B, Soloway M, Trump DL, Hazra T,<br />
Weinstein RS.<br />
Intravesical thiotepa versus Mitomycin in patients with Ta, T1 and TIS transitional<br />
cell carcinoma of the bladder: a phase III prospective randomized study.<br />
J Urol. 1988; 140(6):1390-3.<br />
59
60<br />
Hinman J<br />
Recurrence of bladder tumors by surgical implantation.<br />
J Urol. 1956 Apr;75(4):695-6.<br />
Huben RP.<br />
Intravesical chemotherapy versus immunotherapy for superficial bladder cancer.<br />
Semin Urol Oncol. 1996 Feb;14(1 Suppl 1):17-22.<br />
Huland H, Otto U, Paleske AV<br />
Chemotherapy and human bladder carcinoma transplanted into NMRI<br />
J-Urol 1985; 134: 601-606<br />
Huland H, Otto U<br />
Mitomycin Instillation to prevent recurrence of superficial bladder carcinoma<br />
Results of a controlled, prospecitve study 58 patients<br />
Eur-Urol, 1983; 9: 84-86<br />
Huland H, Otto U<br />
Use of <strong>mito</strong>mycin as prophylaxis following endosopic resection of superficial<br />
bladder cancer.<br />
Urology 1985; 26 (suppl): 32<br />
Huncharek M, Kupelnick B<br />
Impact of intravesical chemotherapy vs BCG immunotherapy on recurrence of<br />
superficial transitional cell carcinoma of the bladder. Metaanalytic Reevaluation<br />
Am-J-Clin-Oncol 2003; 26 (4): 402-407<br />
Issell BF, Prout GR, Soloway MS et al.<br />
Mitomycin intravesikal therapy in noninvasive bladder cancer after failure of<br />
Thiotepa.<br />
Cancer 1984; 53: 1025<br />
Joseph P, Jaiswal AK<br />
A unique cytosolic activity related but distinct from NQO1 catalyses metabolic<br />
activation of <strong>mito</strong>mycin C<br />
Br. J. Cancer, 2000; 82: 1305-1311<br />
Jurincic CD, Engelmann U, Gasch J, Klippel KF<br />
Immunotherapy in bladder cancer with keyhole-limpet hemocyanin: a randomized<br />
study.<br />
J Urol, April 1, 1988; 139(4): 723-6.<br />
Kaasinen E, Rintala E, Hellström P, Viitanen J, Juusela H, Rajala P,<br />
Korhonen H, Liukkonen T,<br />
Factors explaining recurrence in patients undergoing chemoimmunotherapy regimens<br />
for frequently recurring superficial bladder carcinoma<br />
Eur-Urol, 2002; 42: 167-174<br />
Kantor AF, McLaughlin JK, Curtis RE, Flannery JT, Fraumeni JF Jr.<br />
Risk of second malignancy after cancers of the renal parenchyma, renal pelvis,<br />
and ureter.<br />
Cancer. 1986 58(5):1158-61.<br />
Keeley FX, Bagley DH,<br />
Adjuvant Mitomycin fllowing endoskopic treatmen of upper tract transitional cell<br />
carcinoma.<br />
J Urol 1997; 158: 2074-2077<br />
Kiefer JH<br />
Bladder tumor recurrence in the urethra: a warning.<br />
J Urol. 1953 May;69(5):652-6.<br />
Kimber BF et al.<br />
Induction of concentration-dependent blockade in the G2 phase of the cell cycle<br />
by cancer chemotherapeutic agents<br />
Cancer Res,1978;38: 809-814
Koontz WW, Heney NM, Soloway MS, et al.<br />
Mitomycin for Patients that failed on Thiotepa.<br />
Urology 1985; 26 (suppl): 30<br />
Krege S, Giani G, Meyer R, Otto T, Rübben H<br />
A randomized multicenter trial of adjuvant therapy in superficial bladder cancer:<br />
transurethral resection only versus transurethral resection plus Mitomycin versus<br />
transurethral resection plus bacillus calmette guerin<br />
J-Urol 1996; 156: 962 - 966<br />
Leib Z, Baniel J, Servadio C, et al.<br />
Mitomycin (MMC) vs. MMC combined with local Microwave Hyperthermia<br />
(LMWH) as prophylaxis of recurrence of superficila transitional bladder cancer: A<br />
preliminary Report.<br />
Poster eau Kongress, 1996 Paris<br />
Lin, A. J. et al.<br />
Potential bioreductive alkylating agents 1: Benzoquinone derivatives<br />
J. Med. Chem., 1972; 15: 1247-1252<br />
Liu CC, Chou YH, Huang CH, Tsai KB<br />
Bladder wall calcification after intravesical chemotherapy with Mitomycin - a case<br />
report<br />
Kaohsiung J Med Sci 2001 17: 274 - 277<br />
Lown JW<br />
The molekular mechanism of antitumor action of the <strong>mito</strong>mycins<br />
In Carter & Crooke: Mitomycin current status and new developments. Academic<br />
Press1979: 5-26<br />
Malmström PU<br />
A randomized comparative dose-ranging study of interferon-alpha and <strong>mito</strong>mycin-C<br />
as an internal control in primary or recurrent superficial transitional cell carcinoma<br />
of the bladder<br />
BJU-Int 2002; 89: 681-686<br />
Malmström, PU, Wijkström H, Lundholm C, Wester K, Busch C, Norlen-<br />
BJ, Members of the Swedish-Norwegian Bladder Cancer Study Group<br />
5-Year Followup Of A Randomized Prospective Study Comparing Mitomycin And<br />
Bacillus Calmette-Guerin In Patients With Superficial Bladder Carcinoma \NLN\<br />
J-Urol, 1999; 161: 1124-1127<br />
Martinez-Pineiro JA, Justa Garcia Matres M, Martinez-Pineiro L<br />
Endourological treatment of upper tract urothelial carcinomas: analysis of a series<br />
of 59 tumors<br />
J-Urol 1996; 377 - 385<br />
Müller F, Kraft R, Zingg E,<br />
Exfoliative cytology after transurethral ressection of superficial bladder tumours<br />
Br-J-Urol, 1985; 57: 530-534<br />
Nieuwenhuijzen JA, Bex A, Horenblas S<br />
Unusual complication after immediate postoperative intravesical Mitomycin instillation<br />
Eur-Urol, 2003; 43: 711-712<br />
Nissenkorn I, Herrod H, Soloway<br />
Side effects associated with intravesical <strong>mito</strong>mycin.<br />
J Urol. 1981; 126(5):596-7<br />
Oddens JR, van der Meijden AP, Sylvester R.<br />
One immediate postoperative instillation of chemotherapy in low risk Ta, T1 bladder<br />
cancer patients. Is it always safe?<br />
Eur Urol, September 1, 2004; 46(3): 336-8.<br />
O'Donoghue JP, Crew JP<br />
Adjuvant topical treatment of upper urinary tract urothelial tumours<br />
BJU-International 2004; : 483-485<br />
61
62<br />
Okamura K, Ono Y, Kinukawa T, Matsuura O, Yamada S, Ando T, Fukatsu T,<br />
Ohno Y, Ohshima S<br />
Randomized Study of Single Early Instillation of (2"R)-4'-0-Tetrahydropyranyl-<br />
Doxorubicin for a Single Superficial Bladder Carcinoma<br />
Cancer 2002; 94: 2363-2368<br />
Oosterlinck W, Kurth KH, Schröder FH, et al.<br />
A prospective european organisation for research and treatment of cancer genitourinary<br />
group randomized trial comparing transurethral resection followed by a<br />
single intravesical instillation of epirubicin or water in single stage Ta, T1 papillary<br />
carcinoma of the bladder<br />
J-Urol, 1993; 149: 749-752<br />
Oosterlinck W, Lobel B, Jakse G, Malmström PU, Stöckle M, Sternberg C,<br />
EAU Working Group on Oncological Urology<br />
Guidelines on Bladder Cancer\NLN\<br />
Eur-Urol, 2002; 41: 105-112<br />
Pan JS, Slocum HK, Rustum YM, Greco WR, Gaeta JF, Huben RP,<br />
Inhibition of implantation of murine bladder tumor by thiotepa in cauterized bladder<br />
J-Urol, 1989; 142: 1589-1593<br />
Patel A, Fuchs GJ,<br />
New techniques for the administration of topical adjuvant therapy after endoscopic<br />
ablation of upper urinary tract transitional cell carcinoma<br />
J-Urol 1998; 159: 71-75<br />
Pode D, Shapiro A, Wald M, Nativ O, Laufer M, Kaver I<br />
Noninvasive detection of bladder cancer with the BTA stat test<br />
J-Urol, 1999; 161: 443-446<br />
Prout GR Jr, Griffin PP, Nocks BN, DeFuria MD, Daly JJ.<br />
Intravesical therapy of low stage bladder carcinoma with Mitomycin: comparison<br />
of results in untreated and previously treated patients.<br />
J Urol. 1982; 127(6):1096-8<br />
Rajala P, Kaasinen E, Raitanen M, Liukkonen T, Rintala-E, Finnbladder<br />
Group<br />
Perioperative single dose instillation of epirubicin or interferon-alpha after transurethral<br />
resection for the prophylaxis of primary superficial bladder cancer recurrence:<br />
A prospective randomized multicenter study- Finnbladder III long-term<br />
results<br />
J-Urol 2002; 168: 981-985<br />
Ramanathan-Girish S, M Boroujerdi<br />
Contradistinction between doxorubicin and epirubicin: in-vitro interaction with<br />
blood components.<br />
J Pharm Pharmacol, June 1, 2001; 53(6): 815-21.<br />
Rimpler, H.<br />
Pharmazeutische Biologie II: Biogene Arzneistoffe; G. Thieme Verlag Stuttgart,<br />
1. Auflage, 1990, S. 622<br />
Rintala E, Jauhiainen K, Kaasinen E, Nurmi M, Alfthan O<br />
Alternating MMC and BCG instillation prophylaxis for recurrent papillary (stage Ta<br />
- T1) superficial bladder cancer<br />
J-Urol 1996: Vol. 156, 56-60<br />
Rübben H, Lutzeyer W, et al.<br />
Natural History and the Treatment of low and high risk Superficial Bladder<br />
Tumors<br />
J Urol 1988; 139: 283-285<br />
Schwaibold H, Pichlmeier U, Klingenberger HJ, Huland H<br />
Long-Term Follow-Up of Cytostatic Intravesical Instillation in Patients with<br />
Superficial Bladder Carcinoma<br />
Eur-Urol, 1997; 31: 153-159
Seaman EK, Slawin KM, Benson MC<br />
Treatment options for upper tract transitional-cell carcinoma<br />
Urol-Clin-N-Am 1993; 20: 349-354<br />
See WA, Williams RD,<br />
Urothelial injury and clotting cascade activation: Common denominators in particulate<br />
adherence to urothelial surfaces<br />
J-Urol 1992; 147: 541-548<br />
Shelley MD, Court JB, Kynaston H, Wilt TJ, Coles-B, Mason M<br />
Intravesical Bacillus Calmette-Guérin vs Mitomycin for Ta and T1 bladder cancer<br />
https://gripsdb.dimdi.de/ww/fulltext/out.2003090109420400139.7551jskl2094434.cgi<br />
Cochrane Library 2003, Issue 3<br />
Shida K<br />
Treatment of the bladder cancer with instillation of Mitomycin (first report)<br />
Jpn J Clin Urol 1967;21:1075-1077<br />
Smith AY, Vitale PJ, Lowe BA, et al.<br />
Treatment of superficial papillary transitional cell carcinoma of the ureter by vesicoureteral<br />
reflux of Mitomycin<br />
J-Urol 1987; 138: 1231-1233<br />
Smith JA, Labasky RF, Cockett ATK, Fracchia JA, Montie JE, Rowland RG<br />
Bladder cancer clinical guidelines panel summary report on the management of<br />
nunuscle invasive bladder cancer (Stages Ta, T1 and TIS)<br />
J-Urol 1999; 162: 1697-1701<br />
Soloway MS<br />
The Management of Superficial Bladder Cancer<br />
Cancer, 1980; 45: 1856-1865<br />
Soloway MS<br />
Treatment of superficial bladder cancer with intravesical Mitomycin: Analysis of<br />
immediate and long-term responce in 70 Patients<br />
J Urol, 1985; 134: 1107-1109<br />
Soloway MS, Jordan AM, Murphy WM<br />
Rationale for intravesical chemotherapy in the treatment and prophylaxis of<br />
superficial transitional cell carcinoma<br />
EORTC-Gen-Group-Mono, 1989; 6: 215-236<br />
Soloway MS, Masters S<br />
Urothelial susceptibility to tumor cell implantation<br />
Cancer, 1980; 46: 1158-1163<br />
Solsona E, Iborra I, Ricos JV, Monros JL, Casanova J, Dumont R<br />
Effectiveness Of A Single Immediate Mitomycin Instillation In Patients with Low<br />
Risk Superficial Bladder Cancer: Short And Long-Term Followup<br />
J-Urol, 1999; 161: 1120-1123<br />
Sylvester RJ, Oosterlinck W, van der Meijden APM<br />
A single immediate postoperative instillation of chemotherapy decreases the risk<br />
of recurrence in patients with stage Ta T1 bladder cancer: a meta-analysis of<br />
published results of randomized clinical trials<br />
J-Urol, 2004; 171: 2186-2190<br />
Tawfiek ER, Bagley DH.<br />
Upper-tract transitional cell carcinoma.<br />
Urology. 1997 Sep;50(3):321-9. Review<br />
Thrasher JB, Crawford ED<br />
Complications of intravesical chemotherapy<br />
Urol-Clin-N-Am 1992; 19: 529 - 539<br />
Tolley DA, Parmar MK, Grigor KM, Lallemand G, and the MRC<br />
The effect of intravesical Mitomycin on recurrence of newly diagnosed superficial<br />
bladder cancer: a further report with 7 years of followup<br />
J-Urol, 1996; 155: 1233 - 1238<br />
63
64<br />
van der Heijden AG, Kiemeney LA, Gofrit ON, Nativ O, Sidi A, Leib Z, et al.<br />
Premilinary European Results of Local Microwave Hyperthermia and<br />
Chemotherapy Treatment in Intermediate or High Risk Superficial Transitional Cell<br />
Carcinoma of the Bladder<br />
Eur-Urol 2004; 46: 65-72<br />
van der Meijden APM, Hall RR, Pavone-Macaluso M, Pawinsky A,<br />
Sylvester RJ, van Glabbeke M<br />
Marker tumour response to the sequential combination of intravesical therapy<br />
with Mitomycin and BCG-RIVM in multiple superficial bladder tumours<br />
Eur-Urol 1996; 29: 199 - 203<br />
van Oosterom, A. T. et al.<br />
Pharmakokinetik intravenöser, intrahepatischer und intravesikaler Gabe von<br />
Mitomycin. In: Mitomycin-C - Profil eines Zytostatikums (Eds.: Nagel, Bartsch,<br />
Bach)<br />
Zuckschwerdt Verlag, München, 1984: 1-9<br />
Vegt DJ, Witjes JA, Witjes WPJ, et al.<br />
A randomized study of intravesical Mitomycin, bacillus calmette-guerin tice and<br />
bacillus calmette-guerin RIVM treatment in pTa-pT1 papillary carcinoma and carcinoma<br />
in situ of the bladder<br />
J-Urol 1995; 153: 929-933<br />
Verweij, J. & Pinedo, H. M.<br />
Mitomycin: mechanism of action, usefulness and limitations<br />
Anti-Cancer Drugs, 1990; 1: 5-13<br />
Wajsman Z, Dhafir RA, Pfeffer M, MacDonald S, Block A, Dragone N,<br />
Pontes JE.<br />
Studies of Mitomycin absorption after intravesical treatment of superficial bladder<br />
tumors.<br />
J Urol. 1984 Jul;132(1):30-3.<br />
Wakaki, S. et al.<br />
Isolation of new fractions of antitumor <strong>mito</strong>mycins<br />
Antibiotics and Chemotherapy;1958, 8: 228<br />
Wennerberg-J et al.<br />
Cell cycle perturbations in heterotransplanted squamous-cell carcinoma of the<br />
head and neck after <strong>mito</strong>mycin-c and cisplatin treatment<br />
Int. J. Cancer 1984; 33: 213-222<br />
Wientjes MG, Badalament RA, Wang RC, Hassan A, Au JLS<br />
Penetration of Mitomycin in human Bladder<br />
cancer-res 1993; 53: 3314-3320<br />
Witjes JA, van der Meijden APM, Collette L, Sylvester RJ, Debruyne FMJ,<br />
van Aubel A, Witjes WPJ, EORTC GU Group Durch south east cooperative<br />
urological group<br />
Long-term follow-up of an EORTC randomized prospective trial comparing intravesical<br />
bacille calmette-guérin-rivm an Mitomycin in superficial bladder cancer<br />
Urology 1998; 52: 403 - 410<br />
Wust P, Hegewisch-Becker S, Issels R.<br />
Hyperthermie- aktueller Stand und therapeutische Ergebnisse<br />
TumorDiagn u Ther 2003; 24: 177-184
<strong>mito</strong>-<strong>medac</strong> ® / <strong>mito</strong>-extra ® : Wirkst.: Mitomycin C Zus.: Arzneil. wirks. Best.: 1 Durchstechfl. <strong>mito</strong>-<strong>medac</strong> ®<br />
mit 500 mg Trockensubst. enth. 20 mg Mitomycin. 1 Durchstechfl. <strong>mito</strong>-extra ® mit 1000 mg Trockensubst. enth.<br />
40 mg Mitomycin C. And. Best.: NaCl. Zusätzl.: Applikationssystem mit 20ml (<strong>mito</strong>-<strong>medac</strong> ® ) bzw. 40 ml (<strong>mito</strong>extra<br />
® ) 0,9%iger NaCl-Lsg.. Anwendungsgebiet: Blasentumore Gegenanz.: Systemische Therapie:<br />
Panzytopenie, isolierte Leukothrombopenie, hämorrhag. Diathese, akute Infekte u. Überempf. geg. Mitomycin.<br />
Restriktive od. obstruktive Lungenventilations-, Nierenfunktions-, Leberfunktionsstörungen- u./od. schlechter<br />
Allgemeinzustand; in zeitl Zusammenh. stehende Radiotherapie oder andere zytostat. Therapie. Einsatz als<br />
Immunsuppressivum; intraarterielle Therapie. Intravesik. Therapie: Harnblasenentzündung. Schwangerschaft<br />
und Stillzeit. Für Pat. in geschlechtsreifem Alter während d. Therapie bis 3 Monate nach Abschluss kontrazeptive<br />
Maßnahmen bzw. Abstinenz. Behandl. bei Säugl. und Kleinkindern erst nach sorgfältiger Nutzen/Risiko-<br />
Abwägung. Nebenwirkungen: Bei systemischer Therapie regelmäßig Knochenmarksuppr. mit Leuko- und<br />
zumeist dominanter Thrombopenie, teils verzögert und kumulierend. Bei >50% gastro-intest. Toxizität mit<br />
Appetitlosigkeit, Übelkeit u. Erbrechen. Seltener Schleimhautschäden in Form einer Stomatitis u./od. Durchfälle.<br />
Bei bis zu 10 % schwerw. Organtox.: Pneumonitis od. Nephrotox. erfordert Therapieunterbrechung. Lungentox.<br />
bei präventiver Gabe von Steroiden sehr selten bzw. mit Steroiden gut behandelbar. Nierentoxizität als HUS<br />
(Thrombopenie, MAHA und Niereninsuffizienz), zumeist therapierefraktär und damit letal. Das MAHA-Syndrom<br />
wurde bisher bei Dosen >30 mg/m 2 KOF beobachtet und scheint dosisabhängig aufzutreten. Therapieversuch<br />
zur Entfernung von Immunkomplexen mittels Staphylococcus-Protein-A evtl. angezeigt. Selten: Herzinsuff.<br />
nach vorausgegang. Anthrazyklin-Therapie, venoocclusive Erkrankung der Leber, komplette Alopezie. Bei nicht<br />
sachger. Injektion Schädigungen des umliegenden Gewebes. Intravesikale Therapie: Dysurie od. Zystitis, unter<br />
Umständen hämorrhag. Natur. In Einzelf. schwere Unverträglichkeitsreaktionen (nekrotisierende Zystitis), selten<br />
Stenosen aufgrund einer direkt tox. Wirkung auf das Urothel. Schmerzen beim Harnlassen, Harndrang und<br />
Exantheme. Allerg. Erscheinungen, meist als Kontaktdermatitis, auch in Form von Palmar- und<br />
Plantarerythemen od. generalisierter Exantheme. Durch Auslösen von Übelkeit u. Erbrechen indirekt Beeinträchtigung<br />
der Fahrtüchtigkeit od. der Bedienung von Maschinen mögl.. Verschreibungspflichtig. <strong>medac</strong> <strong>GmbH</strong><br />
Fehlandtstr. 3, D-20354 Hamburg. 8/2003<br />
BCG-<strong>medac</strong>, Pulver und Lösungsmittel zur Herstellung einer Suspension zur intravesikalen Anwendung. Zus.:<br />
Arzneil. wirks. Best.: 1 Durchstechfl. BCG-<strong>medac</strong> enth. mind. 2 x 10 8 und nicht mehr als 3 x 10 9 lebensfähige<br />
Einh. BCG (Bacillus Calmette-Guérin) Bakterien (Stamm RIVM abgeleitet von Stamm 1173-P2). And. Best.:<br />
Pulver: Polygeline, wasserfreie Glucose, Polysorbat 80. Lösungsmittel: NaCl, Wasser f. Injektionszwecke.<br />
Anwendungsgebiete: Nicht-invasive urotheliale Harnblasenkarzinome: kurative Behandl. eines CIS.<br />
Rezidivprophylaxe: Ta G1-G2 multifokale Tu. u./o. Rezidiv-Tu.;Ta G3; T1; CIS. Gegenanz.: Überempfindlichk.<br />
geg. BCG od. Hilfsstoffe; angeborene od. durch Erkrank. od. Therapie erworbene Immunschwäche; aktive<br />
Tuberkulose (Ausschluss bei pos. Hauttest auf Tuberkulin erforderl.). Vorherig. Radiotherapie d. Blase;<br />
Schwangerschaft u. Stillzeit. Nebenwirkungen: häufig, aber meist milde u. vorübergehende Sympt.,<br />
Zunahme im Verlauf d. Therapie. Sehr häufig: Übelkeit; Zystitis, Granulomata der Blase, erhöhte<br />
Miktionsfrequenz mit Schmerzen u. Unwohlsein; asymptomatische granulomatöse Prostatitis. Fieber < 38.5°C,<br />
Unwohlsein, Fieber, Schüttelfrost als Zeichen der gewünschten beginnenden immunolog. Reaktion. Häufig:<br />
Fieber > 38.5°C. Gelegentlich: Zytopenie, Anämie; Reiter-Syndrom; miliare Pneumonie, Lungengranulomatose;<br />
Hepatitis. Exantheme, Hautabszesse; Arthritis, Arthralgie. HWI, Makrohämaturie, Einschränkung d.<br />
Blasenkapazität, Harnstauung; Orchitis, Epididymitis. Arterielle Hypotonie. Selten: BCG-Sepsis;<br />
Gefäßinfektionen, Nierenabszess; symptomatische granulomatöse Prostatitis. Sehr selten: BCG-Infektion von<br />
Implantaten u. umgebenden Gewebe. Zervikale Lymphadenitis, regionale Lymphknoteninfektion;<br />
Hypersensitivitätsreakt.; Osteomyelitis, Knochenmarkinfektion, Psoas-Abszess; Chorioretinitis, Konjunktivitis,<br />
Uveitis. Gefäßfisteln; Erbrechen, intestinale Fisteln, Peritonitis; gegenüber Tuberkulostatika resistente Orchitis<br />
od. Epididymitis, Infektion d. Glans Penis. Verschreibungspflichtig. <strong>medac</strong> <strong>GmbH</strong>, Fehlandtstr. 3, D-20354<br />
Hamburg. 2/2004
<strong>medac</strong><br />
Theaterstraße 6 · 22880 Wedel<br />
12.05<br />
Tel. 0800/10 30 300 · Fax 04103/80 06-328<br />
www.<strong>medac</strong>.de WU-1015