TỔNG HỢP ĐỀ THI HSG HÓA HỌC LỚP 12, LỚP 9 CÓ GIẢI CHI TIẾT TỈNH KIÊN GIANG
https://app.box.com/s/3dvq9gx6u8ns4t9pgomkownfybkc3fek
https://app.box.com/s/3dvq9gx6u8ns4t9pgomkownfybkc3fek
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
https://twitter.com/daykemquynhon<br />
plus.google.com/+DạyKèmQuyNhơn<br />
www.facebook.com/daykem.quynhon<br />
https://daykemquynhon.blogspot.com<br />
http://daykemquynhon.ucoz.com<br />
Nơi bồi dưỡng kiến thức Toán - Lý - Hóa cho học sinh cấp 2+3 /<br />
Diễn Đàn Toán - Lý - Hóa Quy Nhơn 1000B Trần Hưng Đạo Tp.Quy Nhơn Tỉnh Bình Định<br />
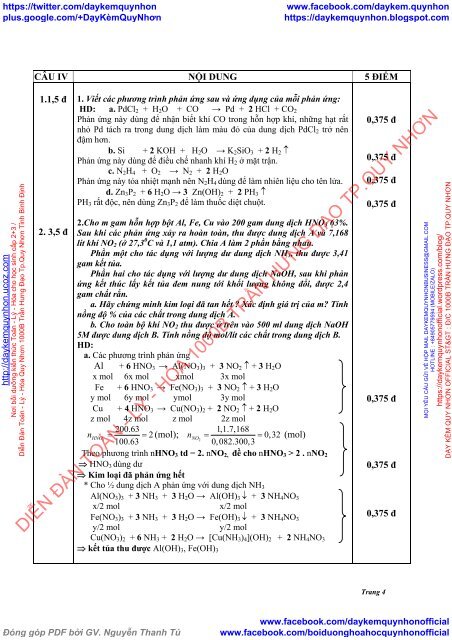
CÂU IV NỘI DUNG 5 ĐIỂM<br />
1.1,5 đ<br />
2. 3,5 đ<br />
1. Viết các phương trình phản ứng sau và ứng dụng của mỗi phản ứng:<br />
HD: a. PdCl 2 + H 2 O + CO → Pd + 2 HCl + CO 2<br />
Phản ứng này dùng để nhận biết khí CO trong hỗn hợp khí, những hạt rất<br />
nhỏ Pd tách ra trong dung dịch làm màu đỏ của dung dịch PdCl 2 trở nên<br />
đậm hơn.<br />
b. Si + 2 KOH + H 2 O → K 2 SiO 3 + 2 H 2 ↑<br />
Phản ứng này dùng để điều chế nhanh khí H 2 ở mặt trận.<br />
c. N 2 H 4 + O 2 → N 2 + 2 H 2 O<br />
Phản ứng này tỏa nhiệt mạnh nên N 2 H 4 dùng để làm nhiên liệu cho tên lửa.<br />
d. Zn 3 P 2 + 6 H 2 O → 3 Zn(OH) 2 + 2 PH 3 ↑<br />
PH 3 rất độc, nên dùng Zn 3 P 2 để làm thuốc diệt chuột.<br />
2.Cho m gam hỗn hợp bột Al, Fe, Cu vào 200 gam dung dịch HNO 3 63%.<br />
Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch A và 7,168<br />
lít khí NO 2 (ở 27,3 0 C và 1,1 atm). Chia A làm 2 phần bằng nhau.<br />
Phần một cho tác dụng với lượng dư dung dịch NH 3 , thu được 3,41<br />
gam kết tủa.<br />
Phần hai cho tác dụng với lượng dư dung dịch NaOH, sau khi phản<br />
ứng kết thúc lấy kết tủa đem nung tới khối lượng không đổi, được 2,4<br />
gam chất rắn.<br />
a. Hãy chứng minh kim loại đã tan hết ? Xác định giá trị của m? Tính<br />
nồng độ % của các chất trong dung dịch A.<br />
b. Cho toàn bộ khí NO 2 thu được ở trên vào 500 ml dung dịch NaOH<br />
5M được dung dịch B. Tính nồng độ mol/lít các chất trong dung dịch B.<br />
HD:<br />
a. Các phương trình phản ứng<br />
Al + 6 HNO 3 → Al(NO 3 ) 3 + 3 NO 2 ↑ + 3 H 2 O<br />
x mol 6x mol xmol 3x mol<br />
Fe + 6 HNO 3 → Fe(NO 3 ) 3 + 3 NO 2 ↑ + 3 H 2 O<br />
y mol 6y mol ymol 3y mol<br />
Cu + 4 HNO 3 → Cu(NO 3 ) 2 + 2 NO 2 ↑ + 2 H 2 O<br />
z mol 4z mol z mol 2z mol<br />
200.63<br />
1,1.7,168<br />
n<br />
HNO<br />
= = 2 (mol); n<br />
3<br />
NO<br />
= = 0,32 (mol)<br />
2<br />
100.63<br />
0,082.300,3<br />
Theo phương trình nHNO 3 td = 2. nNO 2, đề cho nHNO 3 > 2 . nNO 2<br />
⇒ HNO 3 dùng dư<br />
⇒ Kim loại đã phản ứng hết<br />
* Cho ½ dung dịch A phản ứng với dung dịch NH 3<br />
Al(NO 3 ) 3 + 3 NH 3 + 3 H 2 O → Al(OH) 3 ↓ + 3 NH 4 NO 3<br />
x/2 mol x/2 mol<br />
Fe(NO 3 ) 3 + 3 NH 3 + 3 H 2 O → Fe(OH) 3 ↓ + 3 NH 4 NO 3<br />
y/2 mol y/2 mol<br />
Cu(NO 3 ) 2 + 6 NH 3 + 2 H 2 O → [Cu(NH 3 ) 4 ](OH) 2 + 2 NH 4 NO 3<br />
⇒ kết tủa thu được Al(OH) 3 , Fe(OH) 3<br />
0,375 đ<br />
0,375 đ<br />
0,375 đ<br />
0,375 đ<br />
0,375 đ<br />
0,375 đ<br />
0,375 đ<br />
DIỄN ĐÀN TOÁN - LÝ - <strong>HÓA</strong> 1000B TRẦN HƯNG ĐẠO TP.QUY NHƠN<br />
MỌI YÊU CẦU GỬI VỀ HỘP MAIL DAYKEMQUYNHONBUSINESS@GMAIL.COM<br />
HOTLINE : +84905779594 (MOBILE/ZALO)<br />
https://daykemquynhonofficial.wordpress.com/blog/<br />
DẠY KÈM QUY NHƠN OFFICIAL ST> : Đ/C 1000B TRẦN HƯNG ĐẠO TP.QUY NHƠN<br />
Trang 4<br />
Đóng góp PDF bởi GV. Nguyễn Thanh Tú<br />
www.facebook.com/daykemquynhonofficial<br />
www.facebook.com/boiduonghoahocquynhonofficial