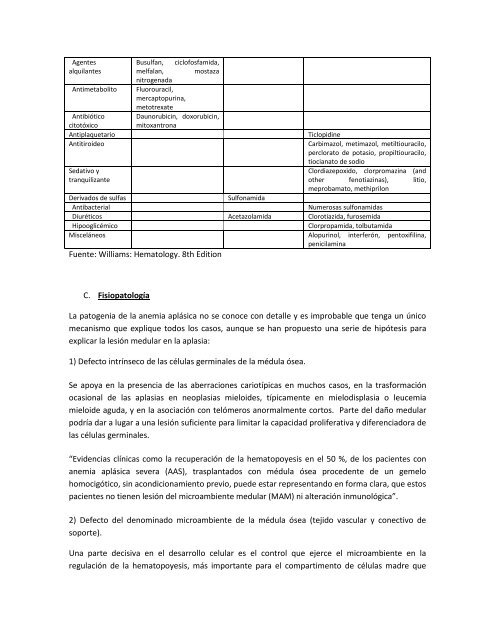
AgentesBusulfan, ciclofosfamida,alquilantesmelfalan, mostazanitrogenadaAntimetabolito Fluorouracil,mercaptopurina,metotrexateAntibióticocitotóxicoDaunorubicin, doxorubicin,mitoxantronaAntiplaquetarioTiclopidineAntitiroideoCarbimazol, metimazol, metiltiouracilo,perclorato de potasio, propiltiouracilo,tiocianato de sodioSedativo yClordiazepoxido, clorpromazina (andtranquilizanteother fenotiazinas), litio,meprobamato, methiprilonDerivados de sulfasSulfonamidaAntibacterialNumerosas sulfonamidasDiuréticos Acetazolamida Clorotiazida, furosemidaHipooglicémicoClorpropamida, tolbutamidaMisceláneos Alopurinol, interferón, pentoxifilina,penicilaminaFuente: Williams: Hematology. 8th EditionC. FisiopatologíaLa patogenia de la anemia aplásica no se conoce con detalle y es improbable que tenga un únicomecanismo que explique todos los casos, aunque se han propuesto una serie de hipótesis paraexplicar la lesión medular en la aplasia:1) Defecto intrínseco de las células germinales de la médula ósea.Se apoya en la presencia de las aberraciones cariotípicas en muchos casos, en la trasformaciónocasional de las aplasias en neoplasias mieloides, típicamente en mielodisplasia o leucemiamieloide aguda, y en la asociación con telómeros anormalmente cortos. Parte del daño medularpodría dar a lugar a una lesión suficiente para limitar la capacidad proliferativa y diferenciadora delas células germinales.“Evidencias clínicas como la recuperación de la hematopoyesis en el 50 %, de los pacientes conanemia aplásica severa (AAS), trasplantados con médula ósea procedente de un gemelohomocigótico, sin acondicionamiento previo, puede estar representando en forma clara, que estospacientes no tienen lesión del microambiente medular (MAM) ni alteración inmunológica”.2) Defecto del denominado microambiente de la médula ósea (tejido vascular y conectivo desoporte).Una parte decisiva en el desarrollo celular es el control que ejerce el microambiente en laregulación de la hematopoyesis, más importante para el compartimento de células madre que
para el resto de células. Esta hemopoyesis está regulada por mecanismos de gran complejidad, enlos que las células hemopoyéticas interactúan entre sí, con su microambiente, con factores decrecimiento y con la matriz extracelular.La célula germinal hematopoyética pluripotente, capaz de auto renovarse y dar lugar a todas laslíneas celulares sanguíneas, estará influida y condicionada por este microambiente en sudiferenciación. Por lo tanto, un daño en el microambiente puede generar una falta de crecimientode células hemopoyéticas como en el caso de la anemia aplásica.“Los ratones de cepa S1/S1, caracterizados por lesión del micro ambiente medular. (Está formadopor los fibroblastos, mastocitos, adipocitos, células endoteliales, macrófagos y células reticulares)MAM. Se ha observado lo siguiente: la médula ósea, de estos ratones tienen capacidad pararestaurar la hematopoyesis en ratones de otra cepa, irradiados letalmente. Sin embargo, lamédula ósea de estos últimos no es capaz de normalizar la hematopoyesis de los primeros, lo quesugiere lesión del MAM. Las células del MAM, tienen un papel fundamental en el estímulo de lahematopoyesis y por lo tanto su lesión podría desarrollar una insuficiencia medular”.3) Anomalías en la regulación inmunológica (humoral y/o celular) de la hemopoyesis.La alteración de la capacidad funcional de las células del compartimiento accesorio (comprendendiferentes subpoblaciones de linfocitos T, linfocitos B, células NK y monocitos) por un probablemecanismo inmunológico, corresponde a uno de los aspectos de la anemia aplásica másestudiados y es el que se considera más probable. Esta hipótesis está sustentada por larecuperación en pacientes que fueron tratados con terapia inmunosupresora.Se cree que ocurre ante la alteración antigénica por la exposición a fármacos, agentes infecciososu otros agentes nocivos ambientales no identificados, de manera adquirida, lo que provoca larespuesta inmunitaria celular durante la cual los linfocitos TH1 activados producen citocinas quepor acción directa o por activación de receptor FAS desencadena el daño celular, como interferóngamma y TNF, que suprimen y matan a los progenitores hematopoyéticos.Se ha descrito una población celular con actividad supresora y con capacidad de sintetizar IFN-ƴ,también se ha detallado un incremento del número de linfocitos activados (Tac +, HLA-DR +, CDS+) con niveles elevados de IFN-ƴ, la producción espontánea de IFN-ƴ de las células mononuclearesde la sangre periférica se encontraba elevado y el número de colonias mieloides en el cultivo demédula ósea se eleva en estos pacientes tras la adición de anti-IFN- ƴ.Otros trabajos han estudiado un posible compromiso de otras linfoquinas en la anemia aplásica,por que los niveles de IL-1 se hallan disminuidos, mientras que los de IL-2 y el Factor de necrosistumoral (TNF), se encuentran elevados.Los LT activados producen interferón (IFN), factor de necrosis tumoral (TNF) e interleuquina 2(IL-2), todas estas citoquinas son capaces de inhibir la proliferación de células hematopoyéticas ySC quiescentes. IFN-y TNF suprimen la hematopoyesis dañando el ciclo mitótico celular, además