Metabolismo de lípidos
Metabolismo de lípidos
Metabolismo de lípidos
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
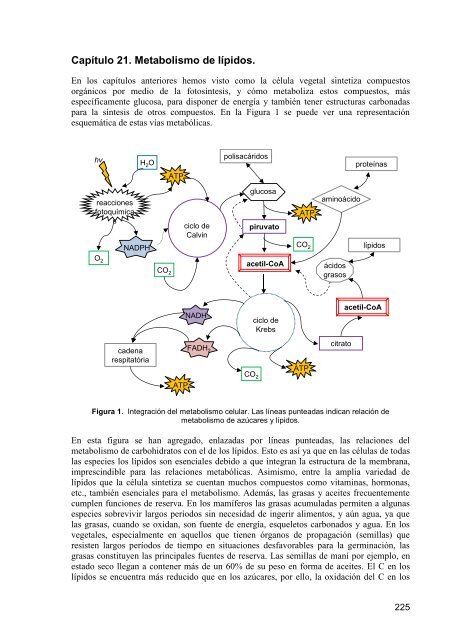
Capítulo 21. <strong>Metabolismo</strong> <strong>de</strong> <strong>lípidos</strong>.<br />
En los capítulos anteriores hemos visto como la célula vegetal sintetiza compuestos<br />
orgánicos por medio <strong>de</strong> la fotosíntesis, y cómo metaboliza estos compuestos, más<br />
específicamente glucosa, para disponer <strong>de</strong> energía y también tener estructuras carbonadas<br />
para la síntesis <strong>de</strong> otros compuestos. En la Figura 1 se pue<strong>de</strong> ver una representación<br />
esquemática <strong>de</strong> estas vías metabólicas.<br />
hv<br />
reacciones<br />
fotoquímica<br />
s<br />
O 2<br />
H 2O<br />
NADPH<br />
ca<strong>de</strong>na<br />
respitatória<br />
CO 2<br />
ATP<br />
ATP<br />
ciclo <strong>de</strong><br />
Calvin<br />
NADH<br />
FADH 2<br />
polisacáridos<br />
glucosa<br />
piruvato<br />
acetil-CoA<br />
CO 2<br />
ciclo <strong>de</strong><br />
Krebs<br />
ATP<br />
CO 2<br />
ATP<br />
aminoácido<br />
ácidos<br />
grasos<br />
citrato<br />
proteínas<br />
<strong>lípidos</strong><br />
acetil-CoA<br />
Figura 1. Integración <strong>de</strong>l metabolismo celular. Las líneas punteadas indican relación <strong>de</strong><br />
metabolismo <strong>de</strong> azúcares y <strong>lípidos</strong>.<br />
En esta figura se han agregado, enlazadas por líneas punteadas, las relaciones <strong>de</strong>l<br />
metabolismo <strong>de</strong> carbohidratos con el <strong>de</strong> los <strong>lípidos</strong>. Esto es así ya que en las células <strong>de</strong> todas<br />
las especies los <strong>lípidos</strong> son esenciales <strong>de</strong>bido a que integran la estructura <strong>de</strong> la membrana,<br />
imprescindible para las relaciones metabólicas. Asimismo, entre la amplia variedad <strong>de</strong><br />
<strong>lípidos</strong> que la célula sintetiza se cuentan muchos compuestos como vitaminas, hormonas,<br />
etc., también esenciales para el metabolismo. A<strong>de</strong>más, las grasas y aceites frecuentemente<br />
cumplen funciones <strong>de</strong> reserva. En los mamíferos las grasas acumuladas permiten a algunas<br />
especies sobrevivir largos períodos sin necesidad <strong>de</strong> ingerir alimentos, y aún agua, ya que<br />
las grasas, cuando se oxidan, son fuente <strong>de</strong> energía, esqueletos carbonados y agua. En los<br />
vegetales, especialmente en aquellos que tienen órganos <strong>de</strong> propagación (semillas) que<br />
resisten largos períodos <strong>de</strong> tiempo en situaciones <strong>de</strong>sfavorables para la germinación, las<br />
grasas constituyen las principales fuentes <strong>de</strong> reserva. Las semillas <strong>de</strong> maní por ejemplo, en<br />
estado seco llegan a contener más <strong>de</strong> un 60% <strong>de</strong> su peso en forma <strong>de</strong> aceites. El C en los<br />
<strong>lípidos</strong> se encuentra más reducido que en los azúcares, por ello, la oxidación <strong>de</strong>l C en los<br />
225
primeros lleva a la producción <strong>de</strong> una cantidad mayor <strong>de</strong> ATP, así como su biosíntesis<br />
requiere <strong>de</strong> una inversión mayor <strong>de</strong> energía metabólica.<br />
Síntesis <strong>de</strong> ácidos grasos<br />
Ya sea que las células sinteticen sus propias estructuras carbonadas, como es en el caso <strong>de</strong><br />
los organismos autótrofos, o bien que obtengan materia y energía a través <strong>de</strong> la<br />
incorporación <strong>de</strong> compuestos carbonados (organismos heterótrofos), la interconversión entre<br />
<strong>lípidos</strong> e carbohidratos resulta esencial. En animales, esta direccionalidad sólo es total en<br />
cuanto a la síntesis <strong>de</strong> grasas a partir <strong>de</strong> carbohidratos, mientras que no todas las grasas son<br />
llevadas nuevamente a glucosa <strong>de</strong>bido a la reacción irreversible catalizada por la citrato<br />
sintasa. En cambio en los vegetales, un ciclo similar (pero alternativo) al ciclo <strong>de</strong> Krebs,<br />
permite la disolución <strong>de</strong> las grasas y su transformación en glucosa.<br />
Esta interconversión comienza con la síntesis <strong>de</strong> ácidos grasos a partir <strong>de</strong> acetil-CoA.<br />
Tanto en células <strong>de</strong> mamíferos como <strong>de</strong> vegetales o aún <strong>de</strong> procariotas, la acetil-CoA<br />
proviene <strong>de</strong> la <strong>de</strong>carboxilación <strong>de</strong>l piruvato, por acción <strong>de</strong> la piruvato <strong>de</strong>shidrogenasa,<br />
proceso que ocurre en mitocondria (visto en el Capítulo 20), o bien <strong>de</strong> la oxidación <strong>de</strong><br />
ácidos grasos, proceso que veremos más a<strong>de</strong>lante en este capítulo. Si bien la síntesis <strong>de</strong><br />
ácidos grasos conceptualmente resulta similar (pero en sentido inverso) a la vía <strong>de</strong> oxidación<br />
<strong>de</strong> los mismos, ambas rutas difieren especialmente en las enzimas que intervienen y en la<br />
localización celular don<strong>de</strong> ocurren. De este modo, la vía <strong>de</strong> síntesis se pue<strong>de</strong> dividir en tres<br />
etapas, que son catalizadas por tres sistemas enzimáticos distintos y que ocurren en tres<br />
compartimentos diferenciados.<br />
La primera etapa, que ocurre en citosol en células animales y cloroplastos <strong>de</strong> células<br />
vegetales, consiste en la biosíntesis <strong>de</strong> palmitato. Esta etapa se <strong>de</strong>sarrolla en 4 pasos<br />
repetitivos (señalados <strong>de</strong>l 1 al 4 en la Figura 2) don<strong>de</strong>, en cada ciclo, la ca<strong>de</strong>na <strong>de</strong> ácido<br />
graso se extien<strong>de</strong> 2 carbonos. Estos pasos son catalizados por un complejo enzimático<br />
<strong>de</strong>nominado complejo ácido graso sintasa. En primera instancia, se lleva a cabo la<br />
formación <strong>de</strong> malonil-CoA a partir <strong>de</strong> acetil-CoA y bicarbonato (HCO3 - ) en una reacción<br />
irreversible catalizada por la enzima acetil-CoA carboxilasa, tal como se representa en la<br />
ecuación 1.<br />
226<br />
H3CCO-CoA + ATP + HCO3 - → HOOCCH2CO-CoA + ADP + Pi + H + {ecuación 1}<br />
El paso siguiente implica la unión <strong>de</strong>l acetil-CoA y <strong>de</strong>l malonil-CoA a la proteína<br />
transportadora <strong>de</strong>l acilo (ACP, <strong>de</strong>l inglés: acyl carrier protein), que integra el complejo<br />
enzimático. Esta reacción es catalizada por una transferasa que libera la Coenzima A (CoA)<br />
(ecuaciones 2 y 3 respectivamente) y se obtiene acetil-ACP y malonil-ACP.<br />
HOOCCH2CO-CoA + ACP → HOOCCH2CO-ACP + CoA {ecuación 2}<br />
H3CCO-CoA + ACP → H3CCO-ACP + CoA {ecuación 3}
Los grupos acetilo y malonilo quedan muy cercanos <strong>de</strong>ntro <strong>de</strong>l complejo y están activados<br />
por la unión a la ACP. A partir <strong>de</strong> aquí comienza el ciclo <strong>de</strong> 4 reacciones. El primer paso<br />
implica una con<strong>de</strong>nsación catalizada por una β-cetoacil-ACP sintasa (enzima con<strong>de</strong>nsadora),<br />
en la que el acetil-ACP, obtenido en la ecuación 3, se une a un residuo acetilo que resulta <strong>de</strong><br />
la <strong>de</strong>carboxilación <strong>de</strong>l malonil-ACP obtenido en la ecuación 2. De esta forma se obtiene un<br />
cetoacilo, el β-cetoacil-ACP, es <strong>de</strong>cir un compuesto <strong>de</strong> 4C que resulta <strong>de</strong> la con<strong>de</strong>nsación<br />
<strong>de</strong> 2 moléculas <strong>de</strong> acetato (ecuación 4) y una molécula <strong>de</strong> CO2.<br />
El CO2 liberado en esta reacción es el mismo carbono que se unió al acetil-CoA como<br />
HCO3 - para originar malonil-CoA. Este proceso <strong>de</strong> tomar CO2 y luego liberarlo, lo realiza la<br />
célula <strong>de</strong>bido a que la unión <strong>de</strong> dos moléculas <strong>de</strong> acetil-CoA es un proceso muy<br />
en<strong>de</strong>rgónico, mientras que la con<strong>de</strong>nsación <strong>de</strong> un grupo acetilo con un grupo malonilo le<br />
resulta termodinámicamente favorable.<br />
HOOCCH2CO-ACP + CH3CO-ACP→ H3CCOCH2CO-ACP + ACP + CO2 {ecuación 4}<br />
En los 3 pasos posteriores <strong>de</strong>l ciclo, el β-cetoacil-ACP formado sufreuna reducción, una<br />
<strong>de</strong>shidratación y una nueva reducción, originando butiril-ACP (ecuación 5). En esto pasos<br />
las enzimas reductasas (pasos 2 y 4) consumen NADPH para terminar <strong>de</strong> remover el grupo<br />
ceto <strong>de</strong>l carbono 3.<br />
H3CCOCH2CO-ACP + 2NADPH → H3C(CH2)2CO-ACP + H2O + 2NADP + {ecuación 5}<br />
El butiril-ACP constituye ahora un nuevo sustrato para la enzima con<strong>de</strong>nsadora (paso 1), al<br />
cual se le unirá un nuevo residuo acetato proveniente <strong>de</strong>l malonil-ACP. De esta forma y en<br />
una serie total <strong>de</strong> 7 ciclos, se van agregando residuos acetato hasta formar palmitoil-ACP,<br />
que sufre la hidrólisis <strong>de</strong> ACP para dar ácido palmítico (16:0, ecuación 6). Los carbonos 15<br />
y 16 <strong>de</strong> esta molécula, pertenecen al acetil-ACP que comenzó el primer ciclo, el resto <strong>de</strong> los<br />
carbonos provienen <strong>de</strong> la <strong>de</strong>carboxilación <strong>de</strong> malonil-ACP.<br />
H3CCO-CoA + 7 HOOCCH2CO-CoA + 14 NADPH →<br />
H3C(CH2)14COOH + 7 CO2 + 8 CoA + 14 NADP + + 6 H2O {ecuación 6}<br />
El ácido graso <strong>de</strong> 16C es el producto principal, y se produce una pequeña cantidad <strong>de</strong> ácidos<br />
grasos <strong>de</strong> mayor longitud. El segundo ácido graso más producido es el esteárico (18:0), el<br />
cual, antes <strong>de</strong> ser hidrolizado, es convertido en ácido graso insaturado (18:1) por una enzima<br />
<strong>de</strong>saturasa.<br />
En resumen, y tal como lo expresa la ecuación 6, en la serie <strong>de</strong> reacciones mencionadas se<br />
van agregando residuos acetato-activados a la ca<strong>de</strong>na carbonada, residuos que luego se<br />
reducen quedando el ácido graso completo (Figura 2).<br />
227
La estequiometría final <strong>de</strong>l proceso se resume en la ecuación 7.<br />
8 acetil-CoA + 7 ATP + 14 NADPH + 14 H + →<br />
228<br />
16:0 + 7 ADP + 7 Pi + 8 CoA + 14 NADP + + 7 H2O {ecuación 7}<br />
De la <strong>de</strong>scripción <strong>de</strong>l proceso <strong>de</strong> síntesis <strong>de</strong> <strong>lípidos</strong>, la adición <strong>de</strong> unida<strong>de</strong>s acetato<br />
<strong>de</strong>termina que, en términos generales, los ácidos orgánicos que se encuentran en la<br />
naturaleza tienen un número par <strong>de</strong> átomos <strong>de</strong> C.<br />
H 3 C<br />
1. El acetil-CoA se<br />
carboxila con gasto <strong>de</strong><br />
ATP<br />
2. El grupo malonil es<br />
transferido a una ACP<br />
CH 2<br />
CH 2<br />
C<br />
O<br />
HO<br />
O<br />
HO<br />
5. Comienzo <strong>de</strong>l segundo<br />
ciclo <strong>de</strong> biosíntesis<br />
7. En la última vuelta el<br />
ACP es removido para<br />
obtener el ácido graso<br />
ACP<br />
malonil-ACP<br />
butiril-ACP<br />
6. Los ciclos continuan<br />
adicionando grupos acetilos<br />
(2C) <strong>de</strong>l malonil-ACP<br />
SACP<br />
O<br />
Carboxilación<br />
ATP<br />
ADP + P i<br />
C<br />
ACP<br />
CoA<br />
C<br />
NAD +<br />
HCO 3 -<br />
CH 2<br />
malonil-CoA<br />
CH 2<br />
C<br />
malonil-ACP<br />
H 3 C C<br />
acetil-CoA<br />
carboxilasa<br />
SCoA<br />
C<br />
O<br />
SACP<br />
O<br />
O<br />
H 3 C<br />
O<br />
acetil-CoA<br />
Decarboxilación<br />
ACP, CO 2<br />
Continua por 6 u 8<br />
ciclos más para obtener<br />
ácidos grasos <strong>de</strong> 16 o<br />
18C, respectivamente<br />
4<br />
NADH<br />
3<br />
H 2O<br />
2<br />
SCoA<br />
1<br />
H 3 C<br />
C<br />
El grupo acetil es<br />
transferido a una ACP<br />
C<br />
CH 2<br />
ACP<br />
SACP<br />
O<br />
acetil-ACP<br />
3. Comienzo <strong>de</strong>l primer<br />
ciclo <strong>de</strong> biosíntesis<br />
ACP<br />
CO 2<br />
Decarboxilación<br />
C<br />
β-cetoacetil-ACP<br />
NAD +<br />
NADH<br />
SACP<br />
O<br />
4. El grupo cetona <strong>de</strong>l C3 es<br />
removido en 3 pasos: reducción,<br />
<strong>de</strong>shidratación, reducción<br />
Figura 2. Representación esquemática <strong>de</strong> la síntesis <strong>de</strong> ácidos grasos.
La segunda etapa consiste en el agregado <strong>de</strong> nuevos residuos acetato al palmitato, por<br />
medio <strong>de</strong> elongasas, para dar el resto <strong>de</strong> los ácidos orgánicos, proceso que ocurre tanto en en<br />
retículo endoplásmico liso (REL) y en menor medida en mitocondria. El proceso en ambas<br />
organelas es diferente, en mitocondria se elongan por el agregado <strong>de</strong> unida<strong>de</strong>s acetilos; en<br />
REL, se elongan por con<strong>de</strong>nsación <strong>de</strong> malonil-CoA.<br />
Finalmente, se producen las insaturaciones (dobles enlaces) <strong>de</strong> las ca<strong>de</strong>nas<br />
hidrocarbonadas por enzimas <strong>de</strong>saturasas.. Las insaturaciones normalmente se encuentran<br />
entre los carbonos 9-10, 12-13 y 15-16, y se dan en configuración cis, proceso que ocurre<br />
siempre en REL.<br />
Los ácidos grasos sintetizados en cloroplastos, son también utilizados para la síntesis <strong>de</strong><br />
glicero<strong>lípidos</strong>, como galactosilglicerol (gluco<strong>lípidos</strong>), que son componentes importantes en<br />
las membranas <strong>de</strong> estos plastidios. En retículo endoplasmico se forma diacilglicerol que<br />
lleva a la formación <strong>de</strong> otros <strong>lípidos</strong> <strong>de</strong> membrana como fosfatidilinositol, fosfatidilglicerol,<br />
fosfatidilcolina y fosfatidiletanolamina.<br />
Oxidación <strong>de</strong> <strong>lípidos</strong><br />
Ya dijimos que los <strong>lípidos</strong> cumplen con al menos tres funciones posibles en la química <strong>de</strong> la<br />
célula. Forman parte <strong>de</strong> la estructura <strong>de</strong> las membranas, constituyen moléculas que a su vez<br />
intervienen en la regulación <strong>de</strong>l metabolismo y actúan como elementos <strong>de</strong> reserva para<br />
situaciones <strong>de</strong> alta <strong>de</strong>manda tanto <strong>de</strong> materia como <strong>de</strong> energía. En los mamíferos, don<strong>de</strong> son<br />
usados como reserva <strong>de</strong> energía, son almacenados en células especializadas, los adipocitos,<br />
que se localizan en <strong>de</strong>terminadas partes <strong>de</strong>l cuerpo. Mientras que en las plantas, don<strong>de</strong> se<br />
utilizan principalmente como reserva <strong>de</strong> carbono, lo hacen en organelas llamadas<br />
oleosomas,que se encuentran en el citoplasma <strong>de</strong> las células <strong>de</strong>l endosperma (semilla) o en<br />
los tejidos <strong>de</strong> los frutos que protegen a las semillas, para aten<strong>de</strong>r el rápido crecimiento <strong>de</strong>l<br />
embrión que tendrá altas <strong>de</strong>mandas energéticas y <strong>de</strong> materia. Los oleosomas son estructuras<br />
con una simple capa lipídica, como una micela, con la porción hidrofílica hacia el<br />
citoplasma y las colas en el interior, y son estabilizados por proteínas.<br />
Los triacilgliceroles acumulados por la célula, <strong>de</strong>bido a sus propieda<strong>de</strong>s y estructura, son<br />
muy difíciles <strong>de</strong> movilizar a través <strong>de</strong> las membranas, por lo que son transformados en<br />
azúcares a través <strong>de</strong> tres procesos. El primero <strong>de</strong> ellos implica la <strong>de</strong>gradación <strong>de</strong> los ácidos<br />
grasos a acetil-CoA por β-oxidación en el glioxisoma <strong>de</strong> las células vegetales, o<br />
mitocondrias <strong>de</strong> células animales; luego el acetil-CoA es oxidado a CO2 en el ciclo <strong>de</strong> Krebs<br />
lo cual ocurre en la matriz <strong>de</strong> la mitocondria (Capítulo 20), y por último la transferencia <strong>de</strong><br />
electrones <strong>de</strong>s<strong>de</strong> el NADH y el FADH2, producidos en los dos procesos anteriores, a la<br />
ca<strong>de</strong>na respiratoria mitocondrial (Capítulo 20).Los <strong>lípidos</strong> <strong>de</strong> reserva son almacenados<br />
como triacilglicéridos, es <strong>de</strong>cir como ácidos grasos esterificados con glicerol. En el caso <strong>de</strong><br />
animales los ácidos grasos son saturados, <strong>de</strong> modo que son grasas. En cambio en los<br />
vegetales, los ácidos grasos tienen niveles variados <strong>de</strong> insaturaciones lo que los constituye<br />
en aceites.In<strong>de</strong>pendientemente <strong>de</strong> su localización, la oxidación <strong>de</strong> los <strong>lípidos</strong> comienza con<br />
la hidrólisis <strong>de</strong> los triacilglicéridos para liberar glicerol y ácidos grasos. Este proceso lo<br />
realizan tres enzimas, la triacilglicerol-lipasa (TGL), la diacilglicerol-lipasa (DGL) y la<br />
monoacilglicerol-lipasa (MGL), que van hidrolizando sucesivamente los enlaces éster<br />
establecidos entre los alcoholes <strong>de</strong>l glicerol y los carboxilos <strong>de</strong> los ácidos grasos (Figura 3).<br />
En las plantas las lipasas se pue<strong>de</strong>n encontrar en la membrana simple <strong>de</strong> los oleosomas, en<br />
el interior <strong>de</strong> los oleosomas o en los glioxisomas, aunque estos dos compartimentos se<br />
encuentran muy cercanos durante la <strong>de</strong>gradación <strong>de</strong> <strong>lípidos</strong>. La primera <strong>de</strong> estas enzimas es<br />
activada mediante fosforilación con ATP.<br />
229
230<br />
TGL ADP<br />
ATP<br />
P<br />
TGL DGL<br />
MGL<br />
Triacilglicerol Diacilglicerol Monoacilglicerol Glicerol<br />
=<br />
O<br />
C OH<br />
C OH<br />
Ac. graso Ac. graso<br />
Ac. graso<br />
Figura 3. Hidrólisis <strong>de</strong> triacilgliceroles por medio <strong>de</strong> lipasas.<br />
Los ácidos grasos así liberados son luego “activados” a través <strong>de</strong> la conjugación con CoA<br />
para formar tioésteres <strong>de</strong> acilo. Esta reacción es catalizada por ligasas específicas y<br />
necesitan <strong>de</strong> ATP. Esta activación <strong>de</strong>l ácido graso, permite la oxidación <strong>de</strong>l C3 o β, que,<br />
como veremos en el título siguiente, da nombre al proceso <strong>de</strong> β-oxidación. En el caso <strong>de</strong><br />
células <strong>de</strong> mamíferos, como la oxidación <strong>de</strong> los ácidos grasos ocurre en mitocondria y la<br />
membrana <strong>de</strong> esta organela es impermeable a los ácidos grasos, o a los acil-CoA, el<br />
transporte <strong>de</strong> los mismos a través <strong>de</strong> las membranas externa e interna lo realiza un<br />
aminoácido especial, la carnitina. En las células vegetales al estar en contacto los<br />
oleosomas con los glioxisomas, no requieren ningún sistema <strong>de</strong> transporte.<br />
β-oxidación <strong>de</strong> los ácidos grasos<br />
Una vez que los ácidos grasos han sido “activados” al conjugarse con CoA formando<br />
unida<strong>de</strong>s acil-CoA, comienzan a oxidarse en una ca<strong>de</strong>na secuencial <strong>de</strong> reacciones que van<br />
eliminando los C <strong>de</strong> dos en dos. Es <strong>de</strong>cir que, así como en la síntesis las unida<strong>de</strong>s <strong>de</strong> C se<br />
fueron agregando como residuos acetato, <strong>de</strong> la misma forma son oxidados. Cada paso está<br />
constituido por 4 reacciones enca<strong>de</strong>nadas, <strong>de</strong>shidrogenación, hidratación, <strong>de</strong>shidrogenación<br />
nuevamente, y finalmente fragmentación tiolítica. Como el ataque comienza en el tercer C<br />
<strong>de</strong> la ca<strong>de</strong>na, es <strong>de</strong>cir el Cβ respecto <strong>de</strong>l extremo en que se encuentra el carboxilo<br />
esterificado con CoA, <strong>de</strong> ahí el nombre que recibe, β-oxidación (Figura 4). Esta secuencia<br />
<strong>de</strong> reacciones ocurre por igual en mitocondrias y glioxisomas.<br />
En la primera reacción la enzima acil-CoA <strong>de</strong>shidrogenasa oxida el palmitoil-CoA. Esta<br />
<strong>de</strong>shidrogenación <strong>de</strong> los C2 (Cα) y C3 (Cβ), produce un doble enlace entre los mismos<br />
originando el trans-2-enoil-CoA y los electrones y protones reducen el FAD + (paso 1 <strong>de</strong> la<br />
Figura 4). El trans-2-enoil-CoA es luego hidratado, por la enoil-CoA hidratasa, a βhidroxiacil-CoA<br />
(paso 2). En este paso se agrega H2O al doble enlace. Posteriormente, una<br />
β-hidroxiacil-CoA <strong>de</strong>shidrogenasa produce β-cetoacil-CoA (paso 3). En este caso la energía<br />
es transferida al NAD + para dar NADH. En el cuarto paso ocurre la reacción <strong>de</strong>l β-cetoacil-<br />
CoA con una CoA libre, mediada por la acil-CoA acetiltransferasa (tiolasa), liberando<br />
acetil-CoA (2C) y <strong>de</strong>ja a una acil-CoA con 2 átomos <strong>de</strong> C menos que la original (14C). La<br />
repetición <strong>de</strong> estos cuatro pasos, en 6 ciclos adicionales (7 ciclos en total) se terminan <strong>de</strong><br />
liberar los residuos acetato los que pue<strong>de</strong>n tener diversos <strong>de</strong>stinos <strong>de</strong> acuerdo a la organela<br />
don<strong>de</strong> se <strong>de</strong>sarrolle y que iremos <strong>de</strong>scribiendo. En la ecuación 8 se resume un paso <strong>de</strong> la βoxidación<br />
<strong>de</strong>l palmitato activado, y en la ecuación 9 la oxidación total <strong>de</strong>l mismo.<br />
=<br />
O<br />
=<br />
O<br />
C OH
2. La oxidación comienza<br />
por el Cβ (C3)<br />
H3C (CH2 ) 11 CH2 CH2 CH2 C<br />
Deshidrogenación<br />
FADH 2<br />
FAD<br />
palmitoil-CoA<br />
H3C (CH2 ) 11 CH2 CH CH C<br />
H 2O<br />
1<br />
trans-2-enoil-CoA<br />
β-3-hidroxiacil-CoA Hidratación<br />
3. En una serie <strong>de</strong> 3 pasos:<br />
oxidación, hidratación,<br />
oxidación, se forma un grupo<br />
cetona en el C3 (Cβ).<br />
2<br />
OH<br />
H3C (CH2 ) 11 CH2 CH CH2 C<br />
β-3-hidroxiacil-CoA<br />
O<br />
SCoA<br />
5. El acil-CoA comienza<br />
un nuevo ciclo<br />
H3C (CH2 ) 11 CH2 C<br />
O<br />
SCoA<br />
O<br />
ácido graso<br />
H3C (CH2 ) 11 CH β-cetoacil-CoA<br />
2 C CH C<br />
O<br />
SCoA<br />
O<br />
CoASH<br />
miristoil-CoA acetil-CoA<br />
Se repite 5 veces el<br />
ciclo para liberar por<br />
último 2 acetil-CoA<br />
SCoA<br />
3<br />
NAD +<br />
β-cetoacil-CoA<br />
NADH<br />
Desidrogenación<br />
1. El ácido graso se<br />
une a la coenzima-A<br />
4. La molécula se cliva en<br />
acil-CoA y acetil-CoA<br />
H 3 C C<br />
4<br />
CoASH<br />
O<br />
SCoA<br />
O<br />
SCoA<br />
6. Los ciclos continúan<br />
liberando grupos acetilos<br />
(2C) en forma <strong>de</strong> acetil-CoA<br />
Figura 4. Representación esquemática <strong>de</strong> la β-oxidación <strong>de</strong> ácidos grasos.<br />
palmitoil-CoA + CoA + FAD + + NAD + + H2O →<br />
miristoil-CoA + acetil-CoA + FADH2 + NADH + H + {ecuación 8}<br />
palmitoil-CoA + 7 CoA + 7 FAD + + 7 NAD + + 7 H2O →<br />
8 acetil-CoA + 7 FADH2 + 7 NADH + 7 H + {ecuación 9}<br />
Si recordamos <strong>de</strong>l Capítulo anterior, por cada FADH2 que transfiere e - a la ca<strong>de</strong>na<br />
respiratoria mitocondrial se producen 2 ATP, y por cada NADH, 3 moléculas <strong>de</strong> ATP. Así<br />
obtenemos 5 ATP por vuelta <strong>de</strong> ciclo, lo que da un total <strong>de</strong> 35 ATP en la oxidación total <strong>de</strong>l<br />
palmitato.<br />
El acetil-CoA producido en la β-oxidación en mitocondria <strong>de</strong> células animales pue<strong>de</strong> ser<br />
oxidado a CO2 en el ciclo <strong>de</strong>l ácido <strong>de</strong> Krebs. Este ciclo produce 12 ATP por cada acetil-<br />
CoA, pero si observamos la ecuación 9, vemos que se producen 8 acetil-CoA por molécula<br />
231
<strong>de</strong> palmitato, lo que nos da un total <strong>de</strong> 96 ATP. La oxidación total <strong>de</strong>l ácido graso saturado<br />
16:0 a CO2 en mitocondria se muestra en la ecuación 10.<br />
palmitoil-CoA + 131 Pi + 131 ADP →<br />
232<br />
CoA + 131 ATP + 16 CO2 + 23 H2O {ecuación 10}<br />
Aquí se constata lo que se dijo al principio, la oxidación <strong>de</strong> ácidos grasos produce una<br />
cantidad mayor <strong>de</strong> energía metabólica (131 ATP por mol <strong>de</strong> palmitato) que la oxidación <strong>de</strong><br />
azúcares (38 ATP por mol <strong>de</strong> glucosa).<br />
Tanto en animales como en vegetales existen organelas en las que específicamente se<br />
oxidan los ácidos grasos por β-oxidación. Si bien los pasos <strong>de</strong> oxidación son iguales a los<br />
<strong>de</strong>scriptos, en estas organelas la transferencia <strong>de</strong> electrones y protones <strong>de</strong>l FADH2 se hace<br />
directamente al O2 que se reduce a peróxido <strong>de</strong> hidrógeno (H2O2, también conocido como<br />
agua oxigenada), <strong>de</strong> ahí que reciban el nombre <strong>de</strong> peroxisomas. Este H2O2 es una especie<br />
reactiva <strong>de</strong>l oxígeno (ROS) el cual produce daño celular por oxidación <strong>de</strong> compuestos como<br />
los <strong>lípidos</strong> <strong>de</strong> membrana y el ADN, por lo que es inmediatamente clivado por la enzima<br />
catalasa en H2O y O2, por lo tanto no se produce ATP sino que se libera energía como calor.<br />
En plantas, los peroxisomas están presentes en los tejidos <strong>de</strong> hojas, mientras que los<br />
glioxisomas están presentes sólo en semillas durante su germinación. Por lo que los<br />
glioxisomas se pue<strong>de</strong>n consi<strong>de</strong>rar peroxisomas especializados, siendo similares a estos en<br />
estructura y función. Al igual que los peroxisomas contienen alta concentración <strong>de</strong> catalasas.<br />
La β-oxidación en el glioxisoma ocurre con el objetivo <strong>de</strong> proveer metabolitos esenciales<br />
como glucosa. En el glioxisoma, el acetil-CoA producido es convertido en precursores que<br />
pue<strong>de</strong>n, por medio <strong>de</strong> por medio <strong>de</strong>l ciclo <strong>de</strong>l glioxilato y gluconeogénesis, dar glucosa.<br />
Más a<strong>de</strong>lante en este capítulo, se <strong>de</strong>tallaran los posibles <strong>de</strong>stinos <strong>de</strong>l succinato producido en<br />
el ciclo <strong>de</strong>l glioxilato.<br />
Un caso especial lo constituye la β-oxidación <strong>de</strong> ácidos grasos insaturados. Muchos <strong>de</strong> los<br />
ácidos grasos que constituyen los triacilgliceroles y fosfo<strong>lípidos</strong> contienen insaturaciones.<br />
Como la configuración <strong>de</strong> estos ácidos grasos es siempre en posición cis, no pue<strong>de</strong> unirse al<br />
sitio activo <strong>de</strong> la enzima enoil-CoA hidratasa encargada <strong>de</strong> catalizar la hidratación <strong>de</strong>l trans-<br />
2-enoil-CoA (paso 2 <strong>de</strong> la Figura 4). Se requiere <strong>de</strong> dos enzimas extras para la oxidación <strong>de</strong><br />
estos ácidos grasos. El ácido graso es <strong>de</strong>gradado por la serie <strong>de</strong> ciclos <strong>de</strong> la β-oxidación<br />
hasta llegar al doble enlace <strong>de</strong>l C9, que ahora queda en el C3 <strong>de</strong>l ácido graso insaturado.<br />
Allí, una enzima isomerasa, 3,2-enoil-CoA isomerasa, transloca el doble enlace trans <strong>de</strong>l C3<br />
a un enlace cis en el C2. De esta forma queda formado un trans-2-enoil-CoA sobre el que<br />
pue<strong>de</strong> actuar la hidratasa correspondiente. La segunda enzima, 2,4-dienoil-CoA reductasa,<br />
es requerida para la oxidación <strong>de</strong> ácidos grasos poliinsaturados (por ejemplo, dobles enlaces<br />
en C9 y C12) don<strong>de</strong> también actúa la isomerasa. Es normal que la mayoría <strong>de</strong> los ácidos<br />
grasos <strong>de</strong> origen vegetal <strong>de</strong> nuestra alimentación sean insaturados y tengan configuración cis.<br />
Por eso que se recomienda una ingesta rica en <strong>lípidos</strong> <strong>de</strong> origen vegetal sobre los <strong>de</strong> origen<br />
animal para disminuir los riesgos <strong>de</strong> enfermeda<strong>de</strong>s vasculares. Sin embargo hay que tener<br />
cuidado con ciertos procesos <strong>de</strong> modificación <strong>de</strong> los alimentos, tanto naturales como<br />
artificiales, ya que se obtienen ácidos grasos insaturados pero en posición trans. Este es el<br />
caso <strong>de</strong> la hidrogenación parcial <strong>de</strong> grasas y aceites para fabricar margarina, o <strong>de</strong> ciertos<br />
alimentos <strong>de</strong> origen <strong>de</strong> animales rumiantes en los que las bacterias <strong>de</strong>l rumen fabrican este<br />
tipo <strong>de</strong> <strong>lípidos</strong>.
Por otra parte, si bien la inmensa mayoría <strong>de</strong> los ácidos grasos tienen ca<strong>de</strong>na par, existe<br />
una pequeña proporción <strong>de</strong> ellos con ca<strong>de</strong>na impar, que son comunes entre los <strong>lípidos</strong> <strong>de</strong><br />
plantas y algunos organismos marinos. En el proceso <strong>de</strong> β-oxidación es claro entonces que<br />
quedará un último resto <strong>de</strong> ca<strong>de</strong>na con 5 átomos <strong>de</strong> C. En la reacción correspondiente se<br />
liberará acetil-CoA y propionil-CoA (3C). Este residuo propionilo sufre un proceso mediado<br />
por tres enzimas (carboxilasa, epimerasa y mutasa) para generar succinil-CoA. Así, ambos<br />
productos pue<strong>de</strong>n ingresar al ciclo <strong>de</strong> Krebs en los animales o al ciclo <strong>de</strong>l glioxilato en las<br />
plantas (el succinato es el producto <strong>de</strong> dicho ciclo).<br />
Ciclo <strong>de</strong>l glioxilato. Glioxisomas<br />
Ya señalamos anteriormente que las células vegetales tienen mecanismos especiales para el<br />
metabolismo <strong>de</strong> <strong>lípidos</strong> que permiten la conversión total <strong>de</strong> los aceites en glucosa. La<br />
liberación <strong>de</strong> los ácidos grasos comienza con la hidrólisis <strong>de</strong> los triacilglicéridos que<br />
transcurre en las mismas organelas en que se almacenan, los cuerpos lipídicos. Mientras que<br />
el mecanismo <strong>de</strong> β-oxidación <strong>de</strong> los ácidos grasos ocurre en los glioxisomas. Estas<br />
organelas son cuerpos esféricos, ro<strong>de</strong>ados por una membrana simple, en la que se acumulan<br />
los <strong>lípidos</strong> <strong>de</strong> reserva. Son especialmente abundantes en el endosperma (tejido <strong>de</strong> reserva)<br />
<strong>de</strong> las semillas <strong>de</strong> especies oleaginosas. Los <strong>lípidos</strong> almacenados son allí mismo oxidados<br />
para dar AcCoA por medio <strong>de</strong> la ca<strong>de</strong>na <strong>de</strong> reacciones ya explicadas (Figuras 3 y 4). La<br />
AcCoA ingresa luego en un ciclo <strong>de</strong> reacciones, conocido como Ciclo <strong>de</strong>l Glioxilato, que<br />
tiene gran<strong>de</strong>s similitu<strong>de</strong>s con el Ciclo <strong>de</strong> Krebs. La Figura 5 es una representación<br />
esquemática <strong>de</strong> las reacciones que ocurren en este ciclo. La mayoría <strong>de</strong> los intermediarios<br />
<strong>de</strong>l ciclo y las enzimas que catalizan las racciones son comunes a ambos ciclos. Sin embargo,<br />
las diferencias esenciales consisten en que al ciclo <strong>de</strong>l glioxilato ingresan dos moléculas <strong>de</strong><br />
AcCoA, que no se pier<strong>de</strong>n como CO2. En este ciclo se evitan los pasos <strong>de</strong> <strong>de</strong>carboxilación<br />
que van <strong>de</strong> isocitrato a succinato y en vez <strong>de</strong> ello el isocitrato se escin<strong>de</strong> en glioxilato y<br />
succinato.<br />
En la figura 5, se pue<strong>de</strong> observar que inicialmente, una molécula <strong>de</strong> AcCoA (proveniente <strong>de</strong><br />
la β-oxidación o directamente <strong>de</strong>l acetato) reacciona con oxalacetato (4C) para dar citrato<br />
(6C), el cual por acción <strong>de</strong> la enzima aconitasa se isomeriza a isocitrato. Posteriormente<br />
mediante una reacción catalizada por la isocitrato liasa, la molécula <strong>de</strong> isocitrato se divi<strong>de</strong><br />
para dar una molécula <strong>de</strong> succinato (4C) y una <strong>de</strong> glioxilato (2C). El succionato formado se<br />
trasporta a la mitocondria don<strong>de</strong> ingresa parcialmente al ciclo <strong>de</strong> Krebs y es convertido a<br />
malato. Ya en el citosol, el malato es oxidado a oxalacetato que sigue la via <strong>de</strong> la<br />
gluconeogénesis. Por otro lado, el glioxilato formado se combina con otra molécula <strong>de</strong><br />
AcCoA y también dá origen a una molécula <strong>de</strong> malato, que es oxidado por la malato<br />
<strong>de</strong>shidrogenasa para formar oxalacetato. Este pue<strong>de</strong> combinarse nuevamente con una<br />
molécula <strong>de</strong> AcCo y así comenzar nuevamente el ciclo.<br />
Como se mencionó anteriormente, la vía gluconeogénica no ocurre en glioxisoma, sino que<br />
el succinato se traslada a la mitocondria don<strong>de</strong> ingresa parcialmente al ciclo <strong>de</strong> Krebs y<br />
entrar ahora sí en esta vía <strong>de</strong> síntesis <strong>de</strong> glucosa. De esta manera, al ciclo <strong>de</strong>l glioxilato<br />
ingresan los residuos acetato “activados” producidos por la oxidación <strong>de</strong> <strong>lípidos</strong>, y se<br />
obtienen como producto neto, en vez <strong>de</strong> coenzimas reducidas y CO2, un mol <strong>de</strong> succinato.<br />
Este succinato, como se dijo, pue<strong>de</strong> ir a mitocondria para dar: a) malato y finalmente<br />
glucosa por medio <strong>de</strong> la gluconeogénesis en el citosol; b) ATP, en forma indirecta al<br />
ingresar al ciclo <strong>de</strong> Krebs y generando co-enzimas reducidas (NADH y FADH2); c) ATP,<br />
en forma directa al ce<strong>de</strong>r directamente alectrones a la ca<strong>de</strong>na <strong>de</strong> transporte respiratoria. Sin<br />
embargo, la mayoría <strong>de</strong>l C que proviene <strong>de</strong> la oxidación <strong>de</strong> <strong>lípidos</strong> <strong>de</strong> reserva en semillas va<br />
a la síntesis <strong>de</strong> glucosa para dar lugar a la síntesis <strong>de</strong> compuestos estructurales.<br />
233
234<br />
GLUCOSA<br />
COO -<br />
H C OH<br />
CH 2<br />
COO -<br />
Malato<br />
Acetato<br />
GLIOXISOMA Acetil-CoA<br />
Citrato<br />
sintasa<br />
CoA<br />
NADH<br />
NAD +<br />
Ácido<br />
Málico<br />
+ H +<br />
O<br />
COO -<br />
C<br />
CH 2<br />
COO - Ácido<br />
Oxaloacético<br />
Oxalacetato<br />
Malato<br />
<strong>de</strong>shidrogenasa<br />
Malato<br />
sintasa<br />
Gluconeogénesis<br />
Acetil-CoA(1)<br />
O<br />
CH 3<br />
C~S<br />
Acetil-CoA(2)<br />
CH 3<br />
O<br />
C~S<br />
Ácido Glioxílico<br />
O<br />
Isocitrato<br />
C H<br />
liasa<br />
COO -<br />
Glioxilato<br />
CH 2<br />
CoA<br />
COO -<br />
CH 2<br />
CoA<br />
Ácido Succínico<br />
COO -<br />
Succinato<br />
Figura 5. Ciclo <strong>de</strong>l glioxilato.<br />
Conexiones entre los ciclos <strong>de</strong>l glioxilato y <strong>de</strong> Krebs<br />
Ácidos<br />
grasos<br />
CH 2<br />
COO -<br />
HO C COO -<br />
CH 2<br />
Citrato<br />
Ácido Cítrico<br />
COO -<br />
H C<br />
H<br />
CH 2<br />
C<br />
Aconitasa<br />
OH<br />
Isocitrato<br />
La Figura 6 representa las conexiones entre los ciclos <strong>de</strong>l Glioxilato y <strong>de</strong> Krebs en células<br />
<strong>de</strong> tejidos <strong>de</strong> semillas. Esta conexión sirve para que las estructuras carbonadas con un alto<br />
potencial redox, es <strong>de</strong>cir los <strong>lípidos</strong> almacenados en cuerpos lipídicos como triacilglicéridos,<br />
sirvan para que el embrión germinante obtenga la materia y la energía necesarias para su<br />
crecimiento. Es a partir entonces <strong>de</strong> los ácidos grasos que la célula obtiene los<br />
monosacáridos (glucosa y fructosa) por medio <strong>de</strong> estos mecanismos concatenados. La<br />
con<strong>de</strong>nsación <strong>de</strong> dichos monosacáridos produce sacarosa, que es la forma <strong>de</strong> transporte <strong>de</strong><br />
sustancias <strong>de</strong> que disponen los tejidos vegetales, que abastecerán al resto <strong>de</strong> las estructuras<br />
<strong>de</strong> la joven planta en esta etapa heterotrófica <strong>de</strong>l crecimiento.<br />
COO -<br />
COO -<br />
COO -
Figura 6. Conexiones entre los ciclos <strong>de</strong>l Glioxilato y <strong>de</strong> Krebs en células <strong>de</strong> tejidos <strong>de</strong> semillas.<br />
235