Na+ Cl- Cu2+ Fe2+ Fe3+ H+ HO- Il faut utiliser des gants pour les ...
Na+ Cl- Cu2+ Fe2+ Fe3+ H+ HO- Il faut utiliser des gants pour les ...
Na+ Cl- Cu2+ Fe2+ Fe3+ H+ HO- Il faut utiliser des gants pour les ...
- No tags were found...
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
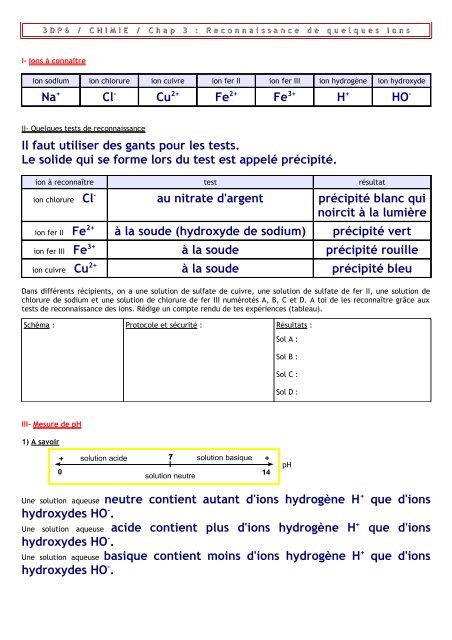
3 D P 6 / C H I M I E / C h a p 3 : R e c o n n a i s s a n c e d e q u e l q u e s i o n sI- Ions à connaîtreion sodium ion chlorure ion cuivre ion fer II ion fer III ion hydrogène ion hydroxydeNa + <strong>Cl</strong> - Cu 2+ Fe 2+ Fe 3+ H + <strong>HO</strong> -II- Quelques tests de reconnaissance<strong>Il</strong> <strong>faut</strong> <strong>utiliser</strong> <strong>des</strong> <strong>gants</strong> <strong>pour</strong> <strong>les</strong> tests.Le solide qui se forme lors du test est appelé précipité.ion à reconnaître test résultation chlorure <strong>Cl</strong> - au nitrate d'argent précipité blanc quinoircit à la lumièreion fer II Fe 2+ à la soude (hydroxyde de sodium) précipité vertion fer III Fe 3+ à la soude précipité rouilleion cuivre Cu 2+ à la soude précipité bleuDans différents récipients, on a une solution de sulfate de cuivre, une solution de sulfate de fer II, une solution dechlorure de sodium et une solution de chlorure de fer III numérotés A, B, C et D. A toi de <strong>les</strong> reconnaître grâce auxtests de reconnaissance <strong>des</strong> ions. Rédige un compte rendu de tes expériences (tableau).Schéma : Protocole et sécurité : Résultats :Sol A :Sol B :Sol C :Sol D :III- Mesure de pH1) A savoir+0solution acide7 solution basiquesolution neutre+14pHUne solution aqueuse neutre contient autant d'ions hydrogène H +hydroxy<strong>des</strong> <strong>HO</strong> - .Une solution aqueuse acide contient plus d'ions hydrogène H +hydroxy<strong>des</strong> <strong>HO</strong> - .Une solution aqueuse basique contient moins d'ions hydrogène H +hydroxy<strong>des</strong> <strong>HO</strong> - .que d'ionsque d'ionsque d'ions
2) Les dangers <strong>des</strong> solutions aci<strong>des</strong> et basiques concentréesLes aci<strong>des</strong> et <strong>les</strong> bases concentrés sont dangereux <strong>pour</strong>l'utilisateur et <strong>pour</strong> l'environnement. El<strong>les</strong> sont corrosives etirritantes. Le contact avec la peau provoque <strong>des</strong> brûlures.3) Reconnaissance de solutions aci<strong>des</strong> et basiquesOn a 5 solutions. On veut savoir si el<strong>les</strong> sont aci<strong>des</strong>, basiques ou neutres. Rédige un compte rendu.Schéma : Protocole et sécurité : Résultats (acide, basique ou neutre ?) :Sol E = solution de chlorure d'hydrogène : .............Sol F = eau distillée : .............Sol G = eau de chaux : .............Sol H = soude : .............Sol I = jus de fruit : .............4) Reconnaissance de solutions aci<strong>des</strong> et basiquesAttention : on ne verse jamais d'eau dans l'acide, car cela provoque <strong>des</strong>projections dangereuses.pHacide concentréacide diluéLorsqu'on dilue un acide, le pH se rapproche de 7 mais le nombred'ions H + et <strong>HO</strong> - ne change pas.2) Les dangers <strong>des</strong> solutions aci<strong>des</strong> et basiques concentréesLes aci<strong>des</strong> et <strong>les</strong> bases concentrés sont dangereux <strong>pour</strong>l'utilisateur et <strong>pour</strong> l'environnement. El<strong>les</strong> sont corrosives etirritantes. Le contact avec la peau provoque <strong>des</strong> brûlures.3) Reconnaissance de solutions aci<strong>des</strong> et basiquesOn a 5 solutions. On veut savoir si el<strong>les</strong> sont aci<strong>des</strong>, basiques ou neutres. Rédige un compte rendu.Schéma : Protocole et sécurité : Résultats (acide, basique ou neutre ?) :Sol E = solution de chlorure d'hydrogène : .............Sol F = eau distillée : .............Sol G = eau de chaux : .............Sol H = soude : .............Sol I = jus de fruit : .............4) Reconnaissance de solutions aci<strong>des</strong> et basiquesAttention : on ne verse jamais d'eau dans l'acide, car cela provoque <strong>des</strong>projections dangereuses.pHacide concentréacide diluéLorsqu'on dilue un acide, le pH se rapproche de 7 mais le nombred'ions H + et <strong>HO</strong> - ne change pas.