OH - Szerves Kémiai Tanszék
OH - Szerves Kémiai Tanszék
OH - Szerves Kémiai Tanszék
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
Fontos tudnivalók• Elérhetőség:– Iroda/: Kémia épület; E-423– Honlap: http://szerves.science.unideb.hu (előadás anyag)– e-mail: juhasz.laszlo@science.unideb.hu• Kötelező irodalom:–Tantermi előadás (katalógus; három hiányzást követően elégtelen A vizsga)• Ajánlott irodalom:– Paul M. Dewick: Medicinal Natural Products: A Biosynthetic Approach; Wiley (2009)– Satyajit D. Sarker, Lutfun Nahar: Chemistry for Pharmacy Students; Wiley (2007)– Antus Sándor, Mátyus Péter: <strong>Szerves</strong> Kémia I.- III.; Tankönyvkiadó, (2005)– Gergely Pál, Penke Botond, Tóth Gyula: <strong>Szerves</strong> és bioorganikus kémia; Alliter, (2006)• Kollokvium:– szóbeli; 2 tétel2
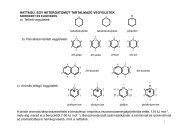
A természetes bilógiailag aktív vegyületek definíciója, szerepük.• A természetes eredetű szerves vegyületek („natural products”) valamely élő szervezetből (növény,mikróbák, állat, stb.) izolálható másodlagos anyagcseretermékek.• Fellehetőek akár ez egész organizmusban, vagy annak részében (pl: növényeknél virág, szár, stb;)• Lehetnek keverékek, vagy tiszta anyagok.• Általában 1500 ate-nél kisebb molekulatömegűek.• Az adott organizmusnak nem szükségesek az életben maradásukhaoz.Elsődleges és másodlagos anyagcsere folyamatok – elsődleges és másodlagos természetes anyagokÉlete során minden élő szervezet rengeteg szerves molekulát alakít át, amihez energiára van szüksége.Ezt az ATP-ből szerzik, és az energiát is ATP formájában képesek raktározni.Élőlénytől függetlenül vannak olyan vegyületek, melyek mindegyiknek szükségük van azéletfolyamataikhoz, illetve magukhoz az élő szervezetek felépítéséhez.Ilyen vegyületek a szénhidrátok; fehérjék, zsírok, nukleinsavakEzek a vegyületek általában egyszerűbb molekulákból épülnek fel (poliszacharidok – egyszerűcukrokból; fehérjék – aminosavakból; nukleinsavak – nukleitidokból, stb).Megfigyelték, hogy ezen biológiai szempontból nélkülözhetetlen vegyületek felépítése és lebontásaorganizmustól függetlenül hasonló módon játszódik le. (pl: glikolízis, citrátciklus; Zsírsavak b-oxidációja, stb). Ezeket a folyamatokat nevezik elsődleges anyagcsere folyamatoknak, és a bennükszereplő anyagokat elsődleges anyagcseretermékeknek.A másodlagos anyagcseretermékek keletkezése nem létszükséglete az organizmusoknak, nemtalálhatóak meg minden organizmusban, vagyis erős specifitást mutatnak. Az ezekfelépítésében/lebontásában résztvevő folyamatokat nevezzük másodlagos anyagcseretermékeknek.3
Másodlagos metabolitok építőköveiglikolízisHO<strong>OH</strong><strong>OH</strong>O<strong>OH</strong><strong>OH</strong>D-glükóz<strong>OH</strong><strong>OH</strong>OPO<strong>OH</strong><strong>OH</strong>glükóz-6-foszfátpentóz-foszfát ciklus<strong>OH</strong>POO<strong>OH</strong>eritróz-4-foszfátFotoszintézisL-glicinCO 2 H<strong>OH</strong>C <strong>OH</strong>NH 2POglicerinaldehid-3-foszfátCO 2 HCO 2 HNH 2L-fenilalaninCO 2 HHSCO 2 HNH 2HOCO 2 HNH 2HOOCPO<strong>OH</strong>HO <strong>OH</strong><strong>OH</strong>sikimsavHONH 2L-tirozinCO<strong>OH</strong>L- ciszteinL-szerin3-foszfoglicerinsavNH 2CO 2 HHOOCOPNHL-triptofánNH 2L-valinfoszfo-enolpiruvátCO 2 HNH 2L-alaninCO 2 HHOOC Opiruvátsav<strong>OH</strong>OPO <strong>OH</strong>deoxixilulóz-5-foszfát<strong>OH</strong>OP<strong>OH</strong> <strong>OH</strong>metileritritol-4-foszfátNH 2L-leucin CoAS Oacetil-koenzimA<strong>OH</strong>CO 2 H <strong>OH</strong>mevalonsav4
CoASOacetil-koenzimAKrebs ciklusCO 2 HHO 2 COoxaloecetsavHO 2 C CO 2 HO2-oxoglutársavHO 2 C CO 2 HNH 2L-glutaminsavHO 2 CCO 2 HNH 2NH 2CO 2 HH 2 NCO 2 HL-aszpartámsavL-isoleucinNH 2L-ornitinSCO 2 HH 2 NCO 2 HNH 2L-metioninNH 2L-lizinH 2 NNHNHNH 2CO 2 HL-arginin5
A természetes vegyületek építőelemei I.H 3 CSCO 2 HX CH 3 (X = O, N, S, C)NH 2C 1L-metioninOSCoAvagyCO 2 HSCoAOC CC 2acetil-CoAmalonil-CoA3 xOSCoACO 2 H<strong>OH</strong><strong>OH</strong>acetil-CoAmevalonsav<strong>OH</strong><strong>OH</strong>izoprén egységC 5OPOPO<strong>OH</strong><strong>OH</strong><strong>OH</strong>deoxixilulóz-5-foszfátmetileritritol-4-foszfát6
A természetes vegyületek építőelemei II.CO 2 HCO<strong>OH</strong>NH 2L-fenilalaninCO 2 HC 6 C 2 NNNHL-triptofánNH 2NHindol-C 2 NNHONH 2L-tirozinH 2 NNH 2CO 2 HH 2 NC 4 NNL-ornitinH 2 NNH 2L-lizinCO 2 HH 2 NC 5 NN7
Építőkövek a természetes vegyületekbenHOO OCO 2 HCukorO<strong>OH</strong>OO<strong>OH</strong> Oorsellinsavparthelinidenaringin4 x C 2 3 x C 5C 6 C 3 + 3 x C 2 + cukor<strong>OH</strong><strong>OH</strong> 2 C<strong>OH</strong> 3 CO<strong>OH</strong>OOOCH 3OCH 3podophyllotoxin2 x C 6 C 3 + 4 x C 1H 3 COtetrahidrokannabiolsavpapaverin6 x C 2 + 2 x C 5C 6 C 2 N + (C 6 C 2 ) + 4 x C 1<strong>OH</strong>CO 2 HH 3 C<strong>OH</strong> 3 CON<strong>OH</strong> 3 C<strong>OH</strong>O 2 C CH 3NCO 2 CH 3lizergsavkokainindol-C 2 N + C 5 + C 1C 4 N + 2 x C 2 + (C 6 C 1 ) + 2 x C 1NCH 3 ONHOC 6 C 3C 6 C 38
Felépítési reakciók mechanizmusai I.Alkilezési reakciók: nukleofil szubsztitúció – O-, N-alkilezésSAM képződéseHOS 2O OOP PNP O OO <strong>OH</strong>O N NH<strong>OH</strong>2<strong>OH</strong>NH 2N NHO <strong>OH</strong>NE1 H 2 NATPE1: SAM szintetázH 3 C S CO 2HL-MetAlkilezés és SAM regenerálódásaH 3 CSCO 2 HHOAd = adenozinO<strong>OH</strong>NN NH 2NS-adenozilmetionin(SAM; AdoMet)NXHX = O, NAdH 3 C SE1: metil-transzferázE2: SAH hidrolázE3: metioninszintázNH 2CO 2 HS N 2E1X CH 3HX CH 3+AdSNH 2CO 2 HS-adenozilhomocisztein(SAH)E2HS CO 2 HNH 2homociszteinN 5 -metil-FH 4E3FH 4S CO 2 HH 3 CNH 2L-Met9
Felépítési reakciók mechanizmusai II.C- alkilezés SAM-velAdH 3 C SNH 2CO 2 HOAdH 3 C SNH 2CO 2 HO<strong>OH</strong>O- alkilezés DMAPP-valPPOS N 1rezonancia stabilizált karbokationOPP: difoszfát- jó távozócsoport<strong>OH</strong><strong>OH</strong>O<strong>OH</strong><strong>OH</strong>O10
Felépítési reakciók mechanizmusai III.Alkilezés elektrofil addícióval – inter- és intramolekuláris addícióPPODMAPPS N 1PPOIPP(izopentenil-pirofoszfát)HOPP- H OPPGPP(geranil-pirofoszfát)S N 1Karbokationok generálása és megszüntetése• távozócsoport lehasadása• alkének protonálása• epoxidok protonálása• metilezés SAM-val• proton lehasadás - alkén képződés• protonlehasadás - gyűrűzáródás• kvencselés nukleofillel11
Wagner - Meerwein átrendeződésA karbokationok stabilitása a 1 < 2 < 3 irányba nő!RRHHR1,2-hidridvándorlásRRHHR2° kation 3° kationR H 1,2-metil RR vándorlásHRRR2° kation 3° kation1,2-alkilvándorlásH1,3-hidridvándorlás3° kation,4 tagú gyûrû2° kation,5 tagú gyûrû3° kationrezonancia stabilizûlt karbokationHkoncertikus 1,2-hidrid és metil vándorlásHHHAzonos építőkövekből változatos szerkezetű és szubsztituáltságú vegyületek keletkezhetnek.Lásd: terpének, szteroidok12
Aldol és Claisen kondenzációRHR<strong>OH</strong>BORXXHOXRHROXOXR<strong>OH</strong>XRHOXRRrezonanciastabilizált karbanionOR<strong>OH</strong>XR<strong>OH</strong><strong>OH</strong>XXX = jóltávozó csoportClaisen adduktX = rossz távozó csoportaldol addukt13
Ezen reakciók legtöbb esetben CoA észtereken játszódnak leHSNHONHO<strong>OH</strong>Coenzim AHSCoAOPO<strong>OH</strong>OPO<strong>OH</strong>HO<strong>OH</strong>O POO<strong>OH</strong>NNNH 2NNOkai: tioészterek a-helyzetbensavasabbak; tiolát jobb távozócsoport, mint az alkoholátH 3 COSCoAH +H 2 COSCoAH 3 COOEtH 3 COOEtcsökkenti a savasságotOOO<strong>OH</strong> 3 CSCoANu H 3 CNu OEtH 3 CSCoAH 3 CSCoAkevésbé kedvezõAz acil-nukleofil szubsztitúció az HSCoA- közreműködésével játszódik le.14
A malonil-CoA- keresztül lejátszódó Claisen reakciók kedvezőbbek az Ac-CoA-nál, ezért azAc-CoA enzimatikus úton malonil-CoA-vá alakul át.OATP + HCO 3ADP +E1aOPHO O <strong>OH</strong>O<strong>OH</strong><strong>OH</strong>N NHH HSbiotin-enzimCoASE1aCOEnzHOO ONHSNHHE1bCOEnzCAoSO<strong>OH</strong> OO N NHH HSE1bCOEnzE1a: biotin-karboxilázE1b: karboxyltranszferázCAoSOO<strong>OH</strong>+ biotin-enzimOmalonil-CoASCoASCoAOO <strong>OH</strong>-CO 2OCoASSCoAOO OSCoAacetoacetil-CoA15
Zsírsavak b-oxidációja és a retro-aldol és retro-Claisen reakció16
Imin képződés és Mannich-reakció17
Aminosavak deaminálása és dekarboxilezése21
Természetes vegyületek mint gyógyszerekA beteg azt mondja: Fáj a torkom!Erre az orvos:Kr.e. 2000: Tessék, edd meg ezt a gyökeret!Kr.u. 1000: Az a gyökér pogány dolog, mondj el egy imát!Kr. u. 1850: Az ima babonaság, idd meg ezt az elixírt!Kr. u. 1940: Az az elixír kígyóolaj, nem tesz jót, nyeld le ezt a pirulát!Kr. u. 1985: Az a pirula hatástalan, vedd be ezt az antibiotikumot!Kr. u. 2008: Az az antibiotikum nem természetes! Tessék itt egy gyökér…• A gyógynövények alkalmazása az egészség megőrzésében, és a betegségekgyógyításában Kr. előtt harmadik évezredig nyúlik vissza.• Hipokratesz (Kr.e. 460 – 377) mint egy 400 a gyógyításban is használttermészetes anyagot írt le.• A kínai és egyiptomi gyógyászat szerves részét képezte a gyógynövények,és egyéb természetes eredetű anyagok használata.• A fejlődő országok lakosainak a mai napig a gyógynövények alkalmazása azegyetlen elérhető lehetőség.• Kínában több mint 7000 növényt tartanak nyílván gyógynövényként• A természet által évezredek alatt kifejlesztett és előállított vegyületek jókiindulási alapot adhatnak gyógyszerek fejlesztéséhez, illetve ők maguk is jóhatóanyagok lehetnek.27
Rák ellenes szer(Vincarosea)Narkotikum(Papaver somniferum)Malária ellenes szer(Artemisia annua)28
Rák ellenes szer(Taxus brevifolia)Penicillin vázas antibiotikumok(Penicillium ssp)29
Gyógyszer fejlesztés és természetes eredetű vegyületek I.„Thus,the term natural product has become almost synonymous with the concept of drugdiscovery. In modern drug discovery and development processes, natural products play animportant role at the early stage of „lead”discovery, i.e. discovery of the active (determinedby various bioassays) natural molecule, which it self or its structural analogues could be anideal drug candidate.”• 1981 – 2002 között 877 új hatóanyagot vezettek be a piacra, ezek 61 %-a volt természetesanyag, vagy annak származéka, vagy mimetikuma.• Ebből 6% természetes anyag; 27% természetes vegyület származéka; 5% tartalmazottvalamilyen természetes vegyületből származó farmakofórt, 23% pedig úgynevezetttermészetes vegyület mimetikum.• Vannak területek, ahol sokkal magasabb a természetes vegyületek aránya:‣antibakteriális vegyületek 78%-a‣rák ellenes gyógyszerjelölt (drug candidate) molekulák 72%-a természetesvegyület, vagy annak analogonja.• 2001-ben a 30 legnagyobb bevételt hozó gyógyszer közül 8 természetes eredetű:• simvastatin, pravastatin, amoxycillin, klavualsav, clarithromycin, azithromycin, ceftriaxone,cyclosporin, paclitaxel (16 milliárd US$)HOOOO<strong>OH</strong>30
Gyógyszer fejlesztés és természetes eredetű vegyületek II.•A közelmúltban a gyógyszergyárak elhanyagolták a természetes vegyületeken alapuló gyógyszerfejlesztést.• A 90-es években több ok is hozzájárult a terület „hanyatlásához”:‣kompatibilitás hiánya a „high throughput screening (HTS)” módszerekkel‣kis fokú automatizálhatóság‣izolálási és szerkezet meghatározási nehézségek‣kombinatorikus kémia kifejlődése• DE! A gyógyszerfejlesztés újból a természetes vegyületek felé fordult:‣kombinatorikus kémia nem jött be.‣az elválasztási és azonosítási módszerek fejlődése‣elképzelhetetlen diverzitás‣több mint 250 000 növény faj él a földön, de ezek alig 10 %-át vizsgálták.‣Új lelőhelyek: tengeri élőlények31
Természetes vegyületek mint gyógyszer hatóanyagok I.Tradicionális út• lassú, kevés molekula33
Modern út:• automatizált, nagy áteresztőképességű módszerek alkalmazása• kis anyagmennyiség• sok molekulát tartalmazó molekulakönyvtárak34
Izoprén vázas vegyületek csoportosítása, szerkezete és hatásukA növényvilágban nagyon gyakoriak azok a szénvegyületek, amelyeknek szénváza két vagy többizoprén egységet foglal magában. Az öt szénatomos izoprénváz nagyszámú és igen változatosszerkezetű és biológiai hatású vegyület építőegysége. Ezek a vegyületek két csoportra oszthatók,mégpedig a terpenoidokra és a karotinoidokra.2-metilbuta-1,3-diénizoprénTerpenoidokKarotionidok• monoterpének : (C 5 H 8 ) 2• szeszkviterpének: (C 5 H 8 ) 3• diterpének: (C 5 H 8 ) 4• szesterterpének: (C 5 H 8 ) 5• triterpének: (C 5 H 8 ) 6• tetraterpének: (C 5 H 8 ) 8• politerpének (C 5 H 8 ) n ; n>8Leopold Ruzicka1887-1976<strong>Kémiai</strong> Nobel-díj(1939)Otto Wallach1847-1931<strong>Kémiai</strong> Nobel-díj• csak C és H atomot tartalmazókonjugált tetraterpének• heteroatomot is tartalmazókonjugált tetraterpének:xantofilek(1910)Izoprén szabály: a terpénekben az iziprén egységek „fej-láb” módon kapcsolódhatnak össze"fej" "láb" +"fej-láb"35
Terpenoidok bioszintéziseA terpenoidok bioszintézise szénhidrátokból kiindulva mevalonsavon át valósul meg, oly módon,hogy a mevalonsavból ún. aktív izoprén (izopentenil-pirofoszfát, IPP), keletkezik, ami a természetesizoprénvegyületek prekurzora.Az izopentenil-pirofoszfát (IPP) izomeráz enzim hatására savkatalizált folyamatban dimetilallilpirofoszfáttá(DMAPP) alakul. Ebből a pirofoszfát anion lehasadásával egy dimetilallil kationkeletkezik, ami prenil-transzferáz enzim közreműköfésével IPP-vel reagálva geranil-pirofoszfátott36ad. Ez lesz a különböző terpenoidok szintézisének kulcs intermediere.
a-pinénAd Eb-pinénAd EOPP-OPPGPPH 2 <strong>OH</strong> 2 O<strong>OH</strong><strong>OH</strong>geraniolnerolA geranil-pirofoszfátból (GPP) a pirofoszfát lehasadásával keletkező kationból számos monoterpénlevezethető. Amennyiben ez a kation egy IPP-vel reagál, akkor a szeszkviterpénekhez juthatunk.További láncnövekedéssel és enzimatikus átalakulással minden származék levezethető belőle.37
• A terpenoidok leggyakrabban növényekben fordulnak elő. A monoterpének általában alacsonyforráspontú, kellemes illatú vegyületek (illóolajok), melyek az izoprén egységeken kívül tartalmazhatnakegyéb funkciós csoportokat (<strong>OH</strong>; CHO; C=O)• A monoterpének (két izoprén egységből felépülő vegyületek) szerkezetük szerint lehetnek aliciklusosak,monociklusosak vagy bicuklusosak.R-(+)-limonénS-(-)-limonénociménmircénbabérfanarancs illatúcitromillatú<strong>OH</strong>Antiszeptikus,fungicid hatású<strong>OH</strong>geraniolkakukkfűtimolgeranialOcitromfűborsmentaHűsítő,csiraölőhatású<strong>OH</strong>(-)-mentol38
KitekintésAz enantiomerek nem feltétlenül rendelkeznek azonos biológiai hatással<strong>OH</strong>NO Otalidomid*NHO<strong>OH</strong>N(R)*O O<strong>OH</strong>N(S)*O OONHONH39
A biciklusos monoterpéneknek számos szerkezetileg érdekes képviselője ismert a természetben,melyek közül a tuján és a tujon (a tuja illóolajában fordul elő) ami biciklo[3,1,0]hexán gyűrűrendszerttartalmaz.HtujanHa-tujon<strong>OH</strong>b-tujonO• a tujon mentol illatú vegyület• a GABA (g-aminobutánsav – legfontosabbinhibitora az idegi ingerület átvitelnek)receptorra hat. Nem okoz halucinációkat• Erre a receptorra hatnak a barbiturátok,benzodiazepám, kébítószerek.• az abszint is tartalmazza elenyészőmennyiségben (szabályozzák a mennyiségét)Az abszint egy alkoholtartalmú ital, mely főleg fehér ürömből, ánizsból és édesköményből készül. Asmaragdzöld folyadék általában rendkívül magas (50%-nál több) alkoholtartalmú és kesernyés ízű.Ebből kifolyólag vízzel hígítva és cukor hozzáadásával fogyasztják. Amikor vízzel keverjük, érdekeshatásnak lehetünk tanúi, ugyanis az abszint a víz hatására opálos fehér-zöld színt vesz fel. Ennekoka az italban található illóolajok, főleg az ánizsolaj nagyon rossz vízoldhatósága, melyek a hígítássorán kicsapódnak az oldatból.40
O• Jellegzetes szagú, illékony, hűsítő és fertőtlenítő hatású vegyület.• Trópusi növényekben találhatókámforSzeszkviterpének: három izoprén egységből felépülő terpenoidok.HO<strong>OH</strong>farmezolnerolidolS-guajazulénkariofilllén• hársfavirág• ciklámen• narancsvirág41
Karotinoidok szerkezete és csoportosításukA karotinoidok zsírban oldódó természetes eredetű pigmentek. A nyolc izoprénegységből felépülőkarotinoidok közös szerkezeti sajátossága a folytonos konjugációt alkotó polién struktúra. Avegyületcsalád neve a sárgarépából (Daucus carota) izolált pigmentre, a karotinra utal. A karotin háromhasonló szerkezetű vegyület, mégpedig az a-, b- és g-karotin keveréke.bb-karotinb-jononb-karotinb-jononb-karotinb-jonona-karotina-jononb-karotinb-jonong-karotinlikopin42
Xantofilek<strong>OH</strong>OsárgaHOflavoxanthin (E161a)HOrubixanthinrozsdavörösO<strong>OH</strong>sárga<strong>OH</strong>Oviolaxanthin44
Az A-vitaminbb-karotin26 7 11 151O3 5 8 9 10 12 13 14retinal4oxOb-karotinOb-karotin<strong>OH</strong>OredA 1 -vitaminretinal<strong>OH</strong>A 2 -vitamin45
A látás fotokémiája (addíció, elimináció, izomerizáció):Az emberi szem kétfajta receptor sejtet tartalmaz: pálcikákat és csapokat• pálcikák (retina peremén helyezkednek el, gyenge fényviszonyoknál aktívakszínlátásra nem alkalmasak.)• csapok (retina központi részén találhatók, erős fényviszonyok között aktívak,színlátásért felelősek)Állatvilágban:• galambok (csak csapok: csak nappal látnak),• baglyok (csak pálcika: színvakság, viszont szürkületben is látnak)A pálcikákban található a rodopszin kromofórja a 11-cisz-retinal. A rodopszin kialakulása során aretinal karbonilcsoportjára addícionálódik a fehérje (opszin) egy aminocsoportja (AdN-reakció),majd egy vízmolekula eliminációjával jön létre az imin (ez a rodopszin, látóbíbor).A látást a pálcikákban található rodopszin biztosítja, mely fény hatására elhalványodik,lebomlik. A fényérzékeny komponens, a retinén, egy foton hatására cisz konfigurációja csupatranszkonfigurációra változik, elhagyja a fehérjemolekulát, melynek ekkor bekövetkezőkonfigurációváltozása megváltoztatja a membránpermeabilitást. Így alakul ki a látásinger.Sötétség hatására a rodopszin újratermelődik.46
SzteroidokA szteroidok a természetes szénvegyületek egyik legfigyelemreméltóbb csoportját alkotják, mivelfontos szerepet játszanak az életfolyamatokban és nélkülözhetetlenek a gyógyításban. A szteroid néva vegyületcsoport legrégebben izolált tagjára a koleszterinre utal, amit epekőből (görögül kholeepe,sztereoszszilárd) nyertek ki.Valamennyi szteroidmolekulára jellemző az ún. szteroid alapváz, ami kémiai szerkezetére nézveperhidro-1,2-ciklopentanofenantrén234110511 12 1396871714 1516perhidro-1,2-ciklopentanofenantréngonán-vázandrosztán-váz pregnán-váz kolesztán-vázösztrán-váz kolán-váz ergosztán-váz48
A tetraciklusos szénhidrogénben az egymáshoz kapcsolódó gyűrűk téralkata különböző lehet. Atermészetben előforduló szteroidok esetében ezek közül három lehetséges gyűrűkapcsolódás valósulmeg, amit az androsztán alapvázon mutatunk be.A gyűrűrendszer felső oldalán elhelyezkedő szubsztituensek b-, míg az alsó térfélen elhelyezkedőek 49 a-térállásúak
Bioszintézis1920 – cápa máj50
Szterinek: olyan szteroid alkoholok, melyek állatokban (zooszterinek), növényekben (fitoszterinek) vagygombákban (mikoszterinek) képződnek.Zooszterinek: legfontosabb képviselője a koleszterin, ami minden állati szervezetben előfordul, különösensok található például a tojássárgájában és az emberi epekőben. A koleszterin fontos szerepet játszik aszteroid hormonok és az epesavak bioszintézisében. A D 3 -vitamin ipari szintézisének is kiindulási anyaga.H<strong>OH</strong>Okoleszt-5-én-3b-olkoleszterinD 3 -vitamin•A koleszterin minden emberi és állati sejtben megtalálható. Különösen nagy mennyiségben fordul előegyes szervekben, pl. a mellékvesében, idegrendszerben.•A koleszterint a szervezet a májban állítja elő, és a sejthártyák felépítésében van fontos szerepe,valamint sokféle hormon alapanyaga.•A koleszterin meghatározásából következtetni lehet a máj működési állapotára.• A vér koleszterin tartalma cukorbetegség (diabetes), sárgaság, a pajzsmirigy csökkent működése,vesebetegségek és érelmeszesedés esetén fokozott lehet.•A koleszterin lerakódva az erek falában annak rugalmasságát csökkenti, és elősegíti azérelmeszesedés kialakulását.•A vizelet üledékvizsgálatakor gyakran találhatók kicsapódott koleszterin kristályok.•Csökken a koleszterinszint máj-, és fertőző betegségekben, és Basedowbetegségekben(hipertireózis).52
A mikoszterinek közül a legfontosabb az ergoszterin, amit elsőként egy a rozson élősködő gombából azanyarozsból (Claviceps purpurea) izoláltak. A vegyület neve az anyarozs francia nevéből (ergot)származik. Az ergoszterin UV-besugárzás hatására a C9–C10 kötés homolitikus hasadását követően D2-vitaminná alakulH<strong>OH</strong>OergoszterinD 2 -vitaminA fitoszterinek növényekben fordulnak elő. Egyik legelterjedtebb képviselőjük a stigmaszterin, amitszójaolajból állítanak elő, és egyes nemi hormonok előállításához használják kiindulási anyagként.A legfontosabb epesavak az 5b-androsztán hidroxikarbonsav származékai. Az epében aminosavakkal(glicin, taurin) képzett peptidszerű vegyületeik az ún. páros epesavak nátriumsó formájában fordulnakelő. Az epesavak szerepe a vízben nem oldódó zsírok felszívódásának elősegítése.<strong>OH</strong>CO<strong>OH</strong>CO<strong>OH</strong>HOsztigmaszterinH<strong>OH</strong>RR = <strong>OH</strong> - kolsavR = H - dezoxikolsavHkolánsav53
Szívre ható glikozidok és varangymérgek: gyógyászati szempontból nagyon fontosak. Növényekben (pl.a Digitalis- és Strophantus-fajokban), tengeri hagymákban (Scilla maritima) és egyes békafajokban(Bufo-fajok) fordulnak elő. A csoport valamennyi tagja 5b,14b-androsztán alapvázat tartalmaz, melyhez3b- és 14b-helyzetben két hidroxicsoport, 17-helyzetben pedig egy laktongyűrű kapcsolódik, valamint a3b-hidroxicsoport különböző szénhidrátokkal glikozidos kötést alkot. A glikozidos kötés már enyhesavas hidrolízis hatására is felszakad, és a szénhidrátok mellett aglikon (pl. genin) is izolálható. Egyiklegfontosabb képviselőjük a digitoxin.OO<strong>OH</strong>O<strong>OH</strong><strong>OH</strong>OO<strong>OH</strong>HO<strong>OH</strong><strong>OH</strong><strong>OH</strong><strong>OH</strong><strong>OH</strong>O<strong>OH</strong>Hdigitoxigenin+<strong>OH</strong>HOdigitoxinO H<strong>OH</strong>digitoxóz54
A szteroidszaponin gyűjtőnév az idesorolt vegyületek vizes oldatának szappanhoz hasonló habzásárautal. A szaponinok hatgyűrűs alapvázat tartalmazó glikozidok, melyeknek jellegzetes szerkezeti eleme aspiroketál gyűrűrész. Legfontosabb képviselőjük a Dioscorea-fajokban előforduló dioszcin, melynekaglikonja a dioszgenin. A dioszgenin fontos kiindulási anyaga a sztereoid hormonok, például aprogeszteron félszintetikus előállításának.OO<strong>OH</strong>OdioszgeninOprogeszteronA szteroid alkaloidok nitrogéntartalmú szteránvázas vegyületek, amelyek főként a Solanum fajokbanfordulnak elő glikozidjaik formájában. Néhány képviselőjük (pl.a szolaszodin és a tomatidin) szerkezetesok hasonlóságot mutat a szaponinok gyűrűrendszerével, csak a spiroketál rész hattagú gyűrűjébenoxigénatom helyett nitrogén található.<strong>OH</strong>N<strong>OH</strong>NHOszolaszidinHOtomatidin55
A szteroid hormonok egy része a nemi funkciókat szabályozza – ezek a nemi hormonok, más részükpedig a szervezet anyagcseréjét (cukor- és sóháztartás) befolyásolják – ezeket az előfordulásukra utalvamellékvesekéreg-hormonoknak (vagy kortikosztereoidoknak) nevezzük. A hormonok nagyon változatosfunkciókat töltenek be, ennek ellenére azonban szerkezetük sok tekintetben hasonló. A 17-helyzetben ahosszú oldallánc vagy gyűrű helyett általában hidroxi-, oxo- vagy acetil-csoportot tartalmaznak.A női nemi hormonok egy része (ösztrogének) a másodlagos nemi jelleg kialakulásáért felelősek – ezek azösztradiol, ösztriol és az ösztron. Közös jellemzőjük, hogy az A-gyűrű mindhárom vegyületben aromás.<strong>OH</strong><strong>OH</strong>O<strong>OH</strong>H<strong>OH</strong><strong>OH</strong>Oösztradiol ösztratriol ösztronA női nemi hormonok másik csoportját a terhesség fenntartását biztosító gesztagének alkotják,melyeknek egyetlen természetes képviselője a progeszteron.OOprogeszteron56
A férfi nemi hormonok (androgének) közé a másodlagos nemi jelleg kialakulásáért felelőstesztoszteron és annak átalakulásával képződő androszteron tartozik.<strong>OH</strong>O<strong>OH</strong>OtesztoszteronandroszteronA mellékvese nagy számú kortikoszteroidot termel. Közülük a kortizolt szintetikusan is előállítják, ez ahidrokortizon, amely gyulladáscsökkentő hatású szer. Néhány szintetikus szteroid hasonló hatástmutat, ilyen például a prednizolon.HOO<strong>OH</strong><strong>OH</strong>O<strong>OH</strong><strong>OH</strong>OOkortizol(hidrokortizon)Oprendnizolon57
Aminosavak, peptidek, fehérjékAminosavaknak nevezzük azokat a karbonsavakat, amelyekben a szénlánc egy vagy többhidrogénjét amino (NH 2 ) csoportra cseréljük. Csoportosításuk történhet az amino éskarboxilcsoportok száma és egymáshoz viszonyított helyzete alapján.NH 2 NH 2CO<strong>OH</strong>karbonsavCO<strong>OH</strong>NH 2aminokarbonsavaminosavCO<strong>OH</strong>CO<strong>OH</strong>CO<strong>OH</strong>NH 2a-aminosav b-aminosav g-aminosavAz aminosavak elnevezése történhet szubsztitúciós nomenklatúrával, azonban a természetesaminosavakat triviális névvel szokás elnevezni:hexánsavCO<strong>OH</strong>NH 2CO<strong>OH</strong>3-aminohexánsavCO<strong>OH</strong>2-aminobenzoesavantranilsavNH 2H 2 N CO<strong>OH</strong>aminoecetsavglicinJóllehet, a számtalan aminosav ismert, és bármilyen szerkezetű aminosav előállítása megoldható, afenti csoportból az a-aminosavak kiemelkedő fontossággal bírnak, mivel az élőszervezetekbentalálható fehérjék és peptidek a-aminosavakból épülnek fel. Eddig minegy 20-23 a-aminosavatizoláltak fehérjék hidrolízisével. Csoportosításuk történhet az amino és karboxilcsoportok számaszerint.58
Aminosavak fizikai tulajdonságai: Az a-aminosavak kristályos, magas olvadáspontú vegyületek.Olvadáspontjuk sokkal magasabb, mint azoké a karbonsavaké vagy aminoké, melyekbőlhelyettesítéssel levezethetők. Olvadáspontjuk fölött elbomlanak, gázhalmazállapotban nemlétképesek. Oldékonyságuk is a sókra emlékeztet. <strong>Szerves</strong> oldószerekben, például alkoholban aprolin és a hidroxiprolin kivételével gyakorlatilag oldhatatlanok, míg vízben valamennyi jól oldódik.Aminosavak optikai sajátságai: Az aminosavak királis vegyületek, és a természetben enantiomertiszta formában fordulnak elő. A fehérjék felépítésében csak az L konfigurációjú aminosavakvesznek részt.H 2 NCO<strong>OH</strong>HCH 3L-(+)-alaninCO<strong>OH</strong>H NH 2CH 3D-(-)-alanin[a] D = +1,8 [a] D = -1,8HCHO<strong>OH</strong>CH 2 <strong>OH</strong>D-glicerinaldehidA két kiralitáscentrumot tartalmazó vegyületek esetében (treonin és izoleucin) négy lehetségesszteroizomer létezik, azonban itt is csak az L konfigurációjú vegyület vesz részt a fehérjékfeléoítésében.H 2 NHCO<strong>OH</strong>H<strong>OH</strong>CH 3CO<strong>OH</strong>H NH 2HO HCH 3H 2 NHOCO<strong>OH</strong>HHCH 3CO<strong>OH</strong>H NH 2H <strong>OH</strong>CH 3L-treoninenatiomerD-treoninL-allo-treoninenatiomerD-allo-treonin59
Aminosavak sav-bázis sajátságai:NH 2NH 3<strong>OH</strong>Ikerionos formaOOOIzoelektromos pont: az a pH, ahol az adott aminosav csak ikerionos formában van jelen60
Elektroforézis vázlata
a-Aminosavak előállítása:Az a-halogénezett savak ammónium-hidroxiddal aminosavakká alakíthatók át. A keletkező aminosavaminocsoportja az ikerionos szerkezet miatt kevésbé bázisos, mint más aminokban, így a továbbialkilezési reakció lassú.BrCO<strong>OH</strong>NH 4 <strong>OH</strong>NH 3COOTisztább terméket kapunk a-bróm-karbonsavészterből kiindulva, ahol a nitrogénatomot az erősennukleofil ftálimid-kálium szolgáltatja.OONKBrCOOEtDMF/OONCOOEtH /H 3 NCOOEz tulajdonképpen a Gabriel-szintézis.• Kérdés: alkalmazható-e bonyolultabb aminosav származékok előállítására?62
Aminosavak előállítása malonészter szintézisselOOOOEtBr 2CCl 4OEtOOOEtOEtBr- KBrON KO EtONO EtOOONaOEtEt<strong>OH</strong>O EtONO EtOONaOOONOCOOEtCOOEt NaNaOEtC CH 2 CH 2 COOEtN C CH 2 CH COOEtEt<strong>OH</strong>COOEtCOOEt2. , - CO 2 CO<strong>OH</strong>O1. hidrolízisH 2 N CH CH 2 CH 2 CO<strong>OH</strong>OOEtglutaminsav (húsleves ízû, ételízesítõ)Malonészter szintézis elvi alapjai.Michael addíció63
Strecker–Zelinszkij-féle szintézis: Aldehidek ammóniumaddícióját kísérő eliminációjában a keletkezőaldimin cseppfolyós hidrogén-cianiddal a-aminonitrillé alakítható, melyből hidrolízissel aminosavnyerhetőHH NH 3R NHHCNH CNH 2 O/savH CO<strong>OH</strong>R OR NH 2R NH 2Erlenmeyer-féle azlakton szintézisPhHNO<strong>OH</strong>ONaOAcAc 2 ONPhOOPhCHONaOAcPhON OPhNa(Hg)PhON OPhNa<strong>OH</strong>H 2 NPhO<strong>OH</strong>64
a-Aminosavak rezolválása I.Az előzőekben ismertetett eljárások az aminosavak racemátjait eredményezik. Az enantiomerekszétválasztását (rezolválását) enzimekkel mint biokatalizátorokkal, vagy diasztereomer sóképzésselvalósítják meg.Aminosavak N-acetilszármazékainak racemátjai aciláz enzim jelenlétében úgy hidrolizálnak, hogy csakaz (S)-konfigurációjú enantiomer szenved hidrolízist, mely az (R)-N-acetilaminosavtól könnyenelválasztható. Az aciláz enzim sertésveséből nyerhető.<strong>OH</strong>N<strong>OH</strong><strong>OH</strong> 2 O aciláz enzimCOOCO<strong>OH</strong>H 3 NHHNHAcCH 3CH 3(S)-(+)-alaninetanolban oldhatatlan(R)-(-)-N-acetilalaninetanolban oldódik65
a-Aminosavak rezolválása II.További lehetőség a szétválasztásra a diasztereomer sóképzés, amely során először azaminosav amfoter jellegét, például N-benzoilezéssel megszüntetik. Az így nyert N-benzoilszármazékból molekvivalens mennyiségben vett optikailag tiszta bázissal [pl. (-)-brucin vagy (-)-sztrichnin] sót képeznek. Az diasztereomer sók 1:1 arányú keverékefrakcionált kristályosítással szétválasztható. A diasztereoegységes sókból a megfelelőkonfigurációjú N-benzoilaminosav savas kezeléssel szabadítható fel, és végül abenzoilcsoport hidrolízissel hasítható le.66
Aminosavak rezolválására használható bázisokNNH<strong>OH</strong>N H<strong>OH</strong>OsztrichninON HObrucin<strong>OH</strong>Aminosavak kimutatása: színreakció ninhidrinnel, csak rájuk jellemző (a prolin kivételével).67
Aminosavak kémiai tulajdonsága: Az aminosavak kémiai tulajdonságait elsősorban a reakcióképesamino- és karboxilcsoport határozza meg.Alkilezés: Az aminosavak, hasonlóan az aminokhoz, alkilezőszerekkel (pl. dimetil-szulfáttal) lúgosközegben negyedrendű ammóniumsókká, ún. betainokká alakíthatók.RCOO(CH 3 ) 2 SO 4 /Na<strong>OH</strong>RCOONH 3N(CH 3 ) 3Acilezés: Az aminosavak acilezőszerekkel savmegkötő jelenlétében acilezhetők.PhCOClRCOOSO 2 ClNaHCO 3MgO ClCOOBnNH 3K 2 CO 3RCOORCOORHNPh<strong>OH</strong>NOOBnHN COOO S OA klórhangyasav-benzilészterrel végzett acilezés különösen a peptidszintézisekbenjelentős.68
Reakció salétromsavval: A primer alifás aminokhoz hasonlóan az aminosavak salétromossavval márszobahőmérsékleten is pillanatszerűen reagálnak a megfelelő hidroxisav és nitrogén képződéseközben. Érdekes módon az aminosavak észterei hasonló körülmények között nem a megfelelőhidroxisavak észtereivé, hanem a rendkívül reakcióképes a-diazoészterekké alakulnak.R COO NaNO2 / HClNH 3R<strong>OH</strong>CO<strong>OH</strong>Oxidáció: Az élő szervezetekben fontos szerepet játszik az aminosavak oxidálása (dehidrogéneződése) a-iminosavakká, amelyek vizes közegben a-ketosavakká és ammóniává hidrolizálnak.RNH 3COOEtNaNO 2 / HClRNNCOOEtClR COO ASORCO<strong>OH</strong>H 2 ORCO<strong>OH</strong>NH 3NHOÉszteresítés: Az aminosavak legegyszerűbben a Fischer-féle módszerrel észteresíthetők, melyneksorán az aminosavészter kristályos hidrokloridját kapjuk.R COO R COOR'R'<strong>OH</strong> / HClNH 3NH 3 ClK 2 CO 3 R COOR'NH 269
Reakció ammóniával és hidrazinnal: Számított mennyiségű lúggal vagy kálium-karbonáttal hűtöttvizes oldatban az aminosavészter sójából a szabad aminocsoportot hordozó észter fel isszabadítható, melyből ammóniával aminosavamidok, hidrazinnal pedig aminosavhidrazidok állíthatókelő.R CONH NHR COOR'2 3NH 2 NH 2 R CONHNH 2NH 2NH 2NH 2Preparatív szempontból különösen az aminocsoportjukon védett (pl. acilezett) aminosavak észtereibőlelkészíthető hidrazidok értékesek. E vegyületekből enyhe körülmények között salétromossavval jónyeredékkel kristályos azidok képződnek, melyek a peptid szintézisekben nyernek alkalmazást.R COOR' NH 2 NH 2 R CONHNH 2 NaNO2 / HClNHAcNHAcR CON 3NHAcAminosavak nehéz fémekkel [pl. réz(II)-vel] vízben nagyon rosszul oldódó komplex sókat képeznek,melyekből savas közegben kén-hidrogénnel szabadítható fel a megfelelő aminosav.RCOOROONH 3NH 2Cu OONH 2R70
Peptidek, fehérjékA fehérjék (peptidek) olyan makromolekuák, melyek a-aminosavakból épülnek fel. A fehérjékben azaminosavak peptid kötéssel (amidkötés) kapcsolódnak össze.RNH 2CO<strong>OH</strong>+R'NH 2CO<strong>OH</strong>RONH 2NHR'CO<strong>OH</strong>N-terminális aminosavRONH 2NHR'<strong>OH</strong>NnRO<strong>OH</strong>C-terminális aminosavFehérjék csoportosítása összetétel alapján:• egyszerű fehérjék: hidrolízisükkel csak aminosavak keletkeznek• összetett fehérjék: hidrolízisükkel aminosavak mellett egyébb anyagok (szénhidrátok,nukleotidok, stb.) is keletkeznek.Fehérjék csoportosítása funkció alapján alapján:• enzimek : biológiai, kémiai folyamatot katalizálnak a szervezetben (pl: tripszin – hidroláz enzim)• transzportfehérjék: kis molekulák szállítását végzik (pl: hemoglobin)• kontraktilis fehérjék: mozgásban vesznek részt (pl: miozin)• vázfehérjék: kollagén (inak, porcok)• tartalékfehérjlék: ovalbumin (tojás)• védőfehérjék: ellenanyagok• hormonok: inzulin (glükózanyagcsere)71
A fehérjéket alkotó a-aminosavak csoportosításaMonoamino-monokarbonsavakH 2 NO<strong>OH</strong>glicin (gly)H 2 NOalanin (ala)<strong>OH</strong>NH 2<strong>OH</strong>Ovalin (val)H 2 N<strong>OH</strong>leucin (leu)<strong>OH</strong> 2 N<strong>OH</strong>isoleucinONH 2<strong>OH</strong><strong>OH</strong><strong>OH</strong>SNH 2<strong>OH</strong>OSONH 2<strong>OH</strong>Otreonin (thr)cisztein (cys)metionin (met)NH 2<strong>OH</strong>fenilalanin (phe)HONH 2<strong>OH</strong><strong>OH</strong>NNH 2<strong>OH</strong><strong>OH</strong>NO<strong>OH</strong>HOOtirozin (tyr)triptofán (trp)prolinNH 2<strong>OH</strong>szerin (ser)H<strong>OH</strong>NO<strong>OH</strong>hidroxiprolin (hyp)HOOSSNH 2H 2 Ncisztin<strong>OH</strong>O72
Monoamino-dikarbonsavak:Diamino-monokarbonsavak:<strong>OH</strong> NH 2OO<strong>OH</strong>aszparaginsav (asp)NH 2HO<strong>OH</strong>O Oglutaminsav (glu)HNNNH 2O<strong>OH</strong>H 2 NNHHNNH 2<strong>OH</strong><strong>OH</strong> 2 NNH 2<strong>OH</strong><strong>OH</strong> 2 NONH 2<strong>OH</strong>Ohisztidin (hys)arginin (arg)lizin (lys)glutamin (gln)Az aminosavak csoortosíthatóak az oldallánc jellege szerint is:• apoláris oldalláncot tartalmaznak: alanin; valin; leucin; izoleucin; propiln; metionon; fenilalanin;triptofán• poláros oldalláncot tartalmaznak: glicin; szerin; treonin; cisztein; tirozin; aszparagin; glutamin• savas oldalláncot tartalmaznak: aszparaginsav; glutaminsav• bázikus oldalláncot tartalmaznak: lizin; arginin; hisztidin• esszenciális aminosav: nem képes az emberi vagy állati szervezet szintetizálni, csak a táplálékkaljuttatható be megfelelő mennyiség a szervezetbe. Az emberi szervezet számára 9 esszenciális aminosavvan: metiomim, treonin, lizin, leucin, izoleucin, valin, fenilalanin, triptofán hisztidin73
Fehérjealkotóa-aminosavakcsoportosításahidrofóbhidrofil
*Hidropátiásindex:0 hidrofóbAz emberszámáraesszenciálisaminosavak
PeptidekPentapeptidserylglycyltyrosylalanylleucine,vagy Ser–Gly–Tyr–Ala–Leu,vagy SGYAL.
A fehérjék elsődleges szerkezetének (aminosavsorrendjének) megállapításaAz N-terminális aminosav meghatározása (Senger módszer):ONH 2O 2 N+NO 2FONHNO 2NO 2HOONHNO 2NO 2+ aminosavakA peptidet reagáltatjuk 2,4-dinitrofluorobenzollal, és a keletkezett termék hidrolizálva az N-terminálisaminosav jelzetten található.Az C-terminális aminosav meghatározása: a klasszikus módszer szerint redukáljuk a C-terminális végéta fehérjéknek, így a hidrolízis sorén az aminosavak mellett lesz egy aminoalkohol is, ami a C-terminálisaminosavból keletkezett.NH<strong>OH</strong> NH <strong>OH</strong>LiBH 4 H 2 N <strong>OH</strong>Oaminoalkohol+ aminosavakNH<strong>OH</strong>ON 2 H 4H 2 N<strong>OH</strong>O+ aminosavhidrazidokA fehérjék hidrazinnal is bonthatóak, ebben az esetben a C-terminális aminosav kivételévelmindegyik aminosav savhidrazid származékká alakul.77
Az aminosav szekvencia meghatározása Edman lebontással.H 2 NNH 2H 2 NO HNNH 2ONNHOOONHOS<strong>OH</strong>Na<strong>OH</strong>N C SH 2 NNHSO HNNHNNHOOOOONHSHCl<strong>OH</strong>O HN OOOO <strong>OH</strong>NNHS+SNNHOtiohidantoin származékA peptidet lúgos közegben izotiocianáttal reagáltatják, és a keletkező tiokarbamid származék savashidrolízisével az N-terminális aminosav lehasd és tiohidantoin struktúra alakul ki. Jólautomatizálható folyamat.78
•elsődleges szerkezet:• másodlagos szerkezet:• harmadlagos szerkezet• negyedleges szerkezet:79
Színreakciók fehérjék kimutatásáraXantoprotein-próba: tömény salétromsav hatására a tirozin vagy triptofán aromás gyűrűjéneknitrálódásával jellemző sárga szín keletkezik81
Biuret-próba: lúgos réz-szulfát oldattal élénk ibolyaszínű réz-komplex képződik.Általános reakció, valamennyi fehérjére pozitív. A reakció, neve onnan ered, hogy a biuret ugyanolyanszínnel adja a reakciót, mint a fehérjék. Ha fehérjét lúgos közegben kevés CuSO 4 oldattal kezeljük(biuret reagens), ibolyás szín figyelhető meg, amelyet a peptid kötés Cu 2+ ionokkal képzettkoordinációs komplexe ad.82
Peptid és fehérje szintézisekA legelső peptidszintézis Curtius (1888) azon megfigyelésén alapszik, hogy aminosavészterek alkoholkilépése közben diketopiperazin-származékokká alakulnak át, melyek híg lúggal vagy savval amegfelelő dipeptiddé hidrolizálhatók.RNH 2OEtOOEt<strong>OH</strong> 2 NR- 2 Et<strong>OH</strong>RONHNHORHO vagy HH 3 NRONHdipeptidSzintén a peptidszintéziseknél használják fel az aminosavakból klórhangyasav-metil-észterrelszulfuril-klorid jelenlétében nyerhető ún. Leuchs-féle anhidrideket.RNH 3OOI. ClCOOCH 3II. SOCl 2RNHOCOClOCH 3- CH 3 ClRNHOCOOLeuchs anhidridA molekulában ily módon kialakított karbonilcsoport egyrészt az aminosav aminocsoportját levédi,másrészt a karbonilcsoport reaktivitását anhidridként fokozza.ROO83
Az élő szervezetben a különböző peptidek (proteinek) többsége fontos biológiai hatást fejt ki. Relatívkis mennyiségben keletkeznek, éppen ezért szintetikus előállításuk a szerkezetbizonyításon túl,gyakorlati jelentőségű is (gyógyszerek előállítása!).A peptidek szintézisének nehézsége: már két aminosavból is négyféle dipeptid keletkezhet.O<strong>OH</strong> 2 NCHR 1CNHCHR 2C<strong>OH</strong>O<strong>OH</strong> 2 NCHR 1OC<strong>OH</strong> + H 2 N CHR 2CO<strong>OH</strong>H 2 N CH C NH CHH 2 NR 1R 2OCH C NH CHR 1R 1C<strong>OH</strong>OC<strong>OH</strong>O<strong>OH</strong> 2 N CH C NH CH CR 2R 2<strong>OH</strong>84
Aminocsoport védése, illetve a védőcsoport eltávolítása1.Ph O ClO+ H 3 N COONa<strong>OH</strong> Ph O NH CO<strong>OH</strong>H 2 O, 50 o Oklórhangyasav-benzil-észterN-(benziloxikarbonil)glicin (cbz-gly)H 2 / Pd- Ph-MeH 2 NCO<strong>OH</strong>- CO 2HOONHCO<strong>OH</strong>(N-karboximetil)karbamidsav(N-karboxi)glicin2.O N 3 H 3 N COO Et 3 N O NH CO<strong>OH</strong>+O Me - Et 3 NHN 3O Meterc-butil-azidoformiát alanin N-(terc-butoxikarbonil)alanin (boc-ala)F 3 CCO<strong>OH</strong> (TFA)H 2 NCO<strong>OH</strong>Me85
Kapcsolási módszerekAktiválás savkloridként vagy savazidként: A védett aminosavat foszfor-pentakloriddal reagáltatva a védettaminosav-kloridot kapjuk, amit aminosavval reagáltatunk.PhH 2 NOOCR 1O R O R3- HClH 3 N COOONH CO<strong>OH</strong> PCl 5Ph O NH CCl- POClR 2NH CO<strong>OH</strong>1. H 2 / Pd /(- PhMe)Ph O NH2. / - CO 2CNH CO<strong>OH</strong>1 1bázisR 2R 2dipeptidOR 1OA karboxilcsoport aktiválását végezhetjük a védett aminosav észteréből savazid képzéssel is.Ph O NHOMeOOMeN-(benziloxikarbonil)alanin-metil-észterdipeptidH 2 N NH 2 NaNO 2 , HClvédõcs.eltáv.Ph O NHHOORO"hidrazid"NHvédett dipeptidMeOONHHONH 2OR- HN 3NH 2N 3OONH- H 2 ONHNO86
Diciklohexilkarbodiimides eljárás: Az aminocsoporton védett aminosavat diciklohexilkarbodiimid(DCC) segítségével reagáltatjuk a másik aminosavval. A reagens az aminosavból O-acilizokarbamidszármazékot képez, ami a másik aminosavat acilezi.DCCOO NH CO MeONHCNOO NH CO MeNHO C NN-(terc-butoxikarbonil)alaninH 2 N<strong>OH</strong><strong>OH</strong>NCNHOdiciklohexilkarbamidONHala-glyTFAO NH COMeONHCO<strong>OH</strong>O NH CNHO MeO C NHCO<strong>OH</strong>boc-ala-gly87
Leuchs-anhidrides módszer: Az eljárásban az aminosavból levezethető oxazolidindion származékothasználjuk, amelyet az aminosavból klórhangyasav-metil-észterrel állítunk elő. A molekulában akarbonilcsoport egyrészt az aminosav aminocsoportját maszkírozza, másrészt a karboxilcsoportreaktivitását anhidridként fokozza.OMeO Cl + H 3 N COOOMeklórhangyasav-metil-észterNa<strong>OH</strong>H 2 O, 50 oMeO NH CO<strong>OH</strong>O MeN-(metiloxikarbonil)alaninNa<strong>OH</strong>MeOONa ONHMe- NaOMeH 2 NMeNH CO<strong>OH</strong>O MealanilalaninH- CO 2MeOOC NH COONHO MeH 3 N COOMeONa<strong>OH</strong>OON(a Na<strong>OH</strong> felszabadítja az amint)HMe88
Szilárd fázisú technika (Merrifi): A módszerben az egyik aminosavat olyan divinilbenzollal térhálósítottpolisztirol gyantához kötjük, amelynek kb. minden 100-adik fenilcsoportja klórmetilcsoportot tartalmaz.A kapcsolás után, amit DCC-vel végezhetünk, a szennyezések és melléktermékek a polimerből könnyenkimoshatók, és a peptid a polimerről HF-dal lehasítható. A kapcsolási lépést a polimerhez kötöttpeptiden – a védőcsoport eltávolítása után – ismételhetjük. Az eljárás hatékonyságát példázza a 124aminosav egységet tartalmazó nukleinsav bontó enzim – a pankreász-ribonukleáz – szintézise. Amódszer automatizálható, programozható, de időigényes a sok lépés miatt (inzulin = 21 + 30 aminosavkapcsolása, 19 napig tart).ClmûgyantaClRobert Bruce Merrifield(1921-2006) Nobel díj 198489
Ogyanta CH 2 Cl HO C- HClCHR 1NHCOOROgyantaCH 2OCCHNHCOORR 1hidrolízis/- CO 2Ogyanta CH 2 O CCH NH 2R 11. DCC,2. hidrol.OOgyanta CH 2 O CCHNHCCH NH 2R 1OOOgyanta CH 2 O CCHNHCCHR 2n-1NHCCH NH 2R 1RHJ v. HFOOOgyantaCH 2I+HOCCHR 1NHCCHRR nn-1NHCCH NH 2R n90
Néhány jelentős természetes peptidGlutation: tripeptid, glu-cys-gly, oxidációs-redukciós folyamatok partnere, aszulfidcsoport diszulfiddá oxidálódik. Természetes állapotban néhánygyümölcsben és zöldségben, továbbá növényi és állati szövetekben fordul elő.Nagyobb mennyiségben pedig fehérjetartalmú ételekben található meg. A májképes előállítani a három aminosavból.HOOCNH 2OSHA AH 2NH CO<strong>OH</strong> 2 G-SH G-S-S-GNHOB BH 291
Oxitocin és vazopresszin az agyalapi mirigy hormonjai. Oktapeptidek, majdnem azonos szerkezetűek, kétaminosav különbözik bennük.Oxitocin: az agyalapi mirigy hátulsó lebenyében tárolódó, a hipotalamuszból érkező hormon. Szabályozzaa simaizmok működését, fontos szerepe van a szülés megindításában.Vazopresszin: vérnyomás szabályozása és a vizelet kiválasztása (antidiuretikus hormon)oxitocinvazopresszin92
Inzulin (diabetes mellitis kezelése), (a latin insula = sziget szóból) a hasnyálmirigy Langerhansszigeteibentalálható béta-sejtek által termelt polipeptid hormon, amely a szénhidrátok, fehérjék észsírok anyagcseréjének szabályozásában vesz részt. A szervezet sejtjei (az agysejtek kivételével) csakinzulin jelenlétében képesek felvenni a vérből a glükózt.93
A flavonoidokOA C B• Difenil-propán (C 6 -C 3 -C 6 ) vázat tartalmazó O-heterociklusok, vagy azok nyílt láncú izomerjei:OOOneoflavonoidok izoflavonoidok flavonoidok
OOOOOflavon<strong>OH</strong>Oflavonol<strong>OH</strong>OflavanolOflavanonOOOOOOizoflavonizoflavanonkalkondihidrokalkonOOOOkatechin<strong>OH</strong><strong>OH</strong>antocianidin<strong>OH</strong><strong>OH</strong>leukoantocianidinOauronok95
Az alapvázak változatosságaOOOOOkromán izokromán 2H-kromén 4H-kromén izokroménOOOOOOOOkumarin kromon izokumarin kroman-2-on(dihidrokumarin)OOOOOOkromán-4-on izokromán-1-on kromiliumsó(benzpiriliumsó)izobenzpiriliumsó96
A flavomoidok bioszintézise I.CO 2 HCO 2 HCO 2 HNH 2ALCO 2 HHO<strong>OH</strong>kávésavMeOOMe<strong>OH</strong>sinapil savRR = H L-PheR = <strong>OH</strong> L-TyrRCO 2 HCO 2 HMeO<strong>OH</strong><strong>OH</strong>ferulasav4-<strong>OH</strong>-fahéjsavA flavonoidok bioszintézise a növényekben aminosavakból (fenilalanin, tirozin) történik. Ezek azaminosavak ammonialiáz enzim hatására a megfelelő fahéjsavvá alakulnak át, mely vegyületekaromás gyűrűje további enzimatikus lépésekben szubsztituálódik97
A flavonoidok bioszintézise II.<strong>OH</strong>CoASOO<strong>OH</strong><strong>OH</strong>malonil-CoAHOCoASOkalkon szintetázOO<strong>OH</strong>resveratrol<strong>OH</strong>HO<strong>OH</strong><strong>OH</strong>HOO<strong>OH</strong>O<strong>OH</strong>OnaringeninA fahéjsav származékok további enzimatikus lépések során alakulnak át a flavonoidszármazékokká. Ezen lépések nagy része laboratóriumban is megvalósuítható. Ezen alapul aflavonoidok előállítása (biomimetiukus szintézis)98
Az alapvázak szintézise I.CHO<strong>OH</strong>szalicilaldehidAc 2 O/NaOAcH 2 O- Ac<strong>OH</strong><strong>OH</strong> COOAc O O"vegyesanhidrid"kumarinH 2 /PdDIBAL-HOO<strong>OH</strong>OO4H-kroménkromán-2-on<strong>OH</strong>COOEtOCHOOO<strong>OH</strong>NaOEt<strong>OH</strong>O<strong>OH</strong>Okromon99
Az alapvázak szintézise II.OCHOOO<strong>OH</strong>+K<strong>OH</strong>Et<strong>OH</strong><strong>OH</strong>NaOAcO2'-hidroxikalkonflavanonH 2 O 2K<strong>OH</strong>, Me<strong>OH</strong>OO<strong>OH</strong>O<strong>OH</strong>O<strong>OH</strong>OOflavanonolflavonol100
Az alapvázak szintézise III.OC 5 H 11 ONONBS/HOON<strong>OH</strong>flavanonOBrOOAc<strong>OH</strong>/HO<strong>OH</strong>OOOflavonolflavon101
Az alapvázak szintézise IV.<strong>OH</strong> 2 /PdH 2 /PdOflavanonOflavánClOO<strong>OH</strong>Mg/HCl<strong>OH</strong>OflavonolMe<strong>OH</strong>ClO3-hidroxiflaviliom-klorid102
Az alapvázak szintézise IV.O<strong>OH</strong>OOTTNNaOMe<strong>OH</strong>Me<strong>OH</strong>CH(OMe) 2Me<strong>OH</strong>O2'-hidroxikalkonizoflavonH 2 /PdAc<strong>OH</strong>, rtOODIBAL-HizoflavonOONaBH 4 /Me<strong>OH</strong>rt.Oizoflavánizoflavon<strong>OH</strong>H 2 /PdMnO 2Me<strong>OH</strong>, rtOCH 2 Cl 2, rt.103
A flavonoidok szerepe az élő szervezetben I.• Szabályozza a hajszálerek áteresztőképességét és erősíti azok falát, csökkentitörékenységüket• Segíti a sima izmok relaxációját – vérnyomáscsökkentő hatás• Segíti a normális vérkeringés fenntartását• Csökkenti az LDL oxidációját –csökken az érszűkület kialakulásának veszélye• Csökken a vérlemezkék összetapadásának veszélye – véralvadás mérséklő hatású• Antioxidáns hatása révén gátolja a gyulladások kialakulásában felelős molekulák hatásánakérvényesülését (hisztaminok, prosztaglandinok, leukotriének)• Ösztrogén hatás• Daganat növekedés gátló hatásA flavonoidoknak nincs ismert mellékhatása!A flavonoid hiány nem értelmezhető fogalomA flavonoidok nem vitaminok! Univerzálisnak tűnnek, azonban hatásuk nem elég drasztikus a márkialakult betegséges teljes visszafordításához. Szerepük inkább a megelőzésben és kiegészítőkezelésként van.104
A flavonoidok szerepe az élő szervezetben II.Betegség, állapotFlavonoid, forrásÉrszűkületQuercetin, áfonyHorzsolások, zúzódásokÁfonyaHajszálértörékenységQuercetin, hesperidin, áfonyaSzürkehályogQuercetin, áfonyaCukorbetegségQuercetin, áfonyaVizesedésQuercetin, áfonyaZöldhályogRutinSzénanáthaQuercetin, rutin, hesperidinKlimaxHesperidinÉjszakai vakságÁfonyaGyomorfekélyQuercetinMájgyulladásCatechin, silybinMagas koleszterinszintQuercetin105
A flavonoidok természetes forrásai<strong>OH</strong><strong>OH</strong><strong>OH</strong><strong>OH</strong>HO<strong>OH</strong>OO<strong>OH</strong><strong>OH</strong><strong>OH</strong><strong>OH</strong><strong>OH</strong>epikatechinepigallokatechin<strong>OH</strong><strong>OH</strong>HO<strong>OH</strong>OOO<strong>OH</strong><strong>OH</strong>-Zöldtea-Szőlőmag-Fenyőkéreg<strong>OH</strong><strong>OH</strong>epigallokatechin gallátA szárított tealevél 30 m/m%-a különböző flavonoidokkeveréke106
HOO<strong>OH</strong><strong>OH</strong>HOO<strong>OH</strong><strong>OH</strong>HOO<strong>OH</strong>HO<strong>OH</strong>HO<strong>OH</strong><strong>OH</strong><strong>OH</strong> OQuercetin<strong>OH</strong><strong>OH</strong> OKaempferolHO<strong>OH</strong>O<strong>OH</strong>flavonolokproanthocyanidinekFenyőkéregZöldteaÁfonyaKörteGinko bilobaAlmaZöldteaGinko levelekSzőlőhéj107
HOFlavonok, biflavonokGinkolevelek és citrusfélék héja<strong>OH</strong>HOO OO<strong>OH</strong>O<strong>OH</strong><strong>OH</strong>O<strong>OH</strong>AmentoflavonHO H 3C<strong>OH</strong><strong>OH</strong>OO<strong>OH</strong><strong>OH</strong>OOO<strong>OH</strong>Oaglikon<strong>OH</strong>OCH 3Hesperidin108
FlavononolokFlavanolignánokHOO<strong>OH</strong><strong>OH</strong>HO<strong>OH</strong>O<strong>OH</strong>H<strong>OH</strong><strong>OH</strong>O<strong>OH</strong><strong>OH</strong><strong>OH</strong><strong>OH</strong>SilybinOCH 3<strong>OH</strong>TaxifolinFenyőkéregMária tövis„Silybum Marianum”109
<strong>OH</strong><strong>OH</strong>AnthocyaninokHOO<strong>OH</strong><strong>OH</strong>cyanidinOCH 3<strong>OH</strong>HOOOCH 3<strong>OH</strong><strong>OH</strong>malvidinOCH 3<strong>OH</strong>HOO<strong>OH</strong><strong>OH</strong><strong>OH</strong>petunidin110
Isoflavonok - szója<strong>OH</strong>O<strong>OH</strong>O<strong>OH</strong>HO<strong>OH</strong>OOGenisteinDiadzein<strong>OH</strong>HOÖsztradiol111
A francia paradoxonUSA : 350389480852Szív és érrendszeri megbetegedésbenelhunytak száma – (100 000 főreviszonyítva) – 2002•Stressz, mozgás szegényéletmód, zsírosételek!404275481560458601495534668359724AOC942768B• Eltérés: fejlet vörösbor fogyasztóiszokások (kultúra)!•Hasonló az eredmény a szintén vörösborfogyasztó Spanyolországgal!SÖR: prenilezett flavonoidok – rákellenes hatás309410470112
Flavonoidok mint színanyagokA flavonol és flavon származékok többnyire sárga színűek, a virágok és a termések színét adják.O<strong>OH</strong>OflavonolOOflavonAz antocianidinek vörös-kék színű színezőanyagok. Szinük és szerkezetük pH függést mutat.antocianidin (aglikon)<strong>OH</strong>OO Oantocian (glikozid)<strong>OH</strong><strong>OH</strong><strong>OH</strong>113
<strong>OH</strong><strong>OH</strong><strong>OH</strong>OO<strong>OH</strong>O<strong>OH</strong>O<strong>OH</strong>OOOC 6 O 5 H 11OC 6 O 5 H 11OC 6 O 5 H 11OC 6 O 5 H 11OC 6 O 5 H 11OC 6 O 5 H 11vörös (pH < 3) ibolya (pH = 7-8) kék (pH 9-10)O<strong>OH</strong>OOOC 6 O 5 H 11OC 6 O 5 H 11sárga (pH > 11)114
A biomassza összetételeA Földön évente újratermelődő biomassza mintegy 200 milliárd tonna/évtömegűnek becsülhető.Szénhidrátok75%Lignin20% Zsírok,Fehérjék,Terpenoidok,Alkaloidok,Nukleinsavak5%
SzénhidrátokA szénhidrátokat szerkezetük szerin két nagy csoportra oszthatjuk:• monoszacharidok. E vegyületekre jellemző, hogy savas hidrolízissel már nem bonthatók kisebbmolekulatömegű szénhidrátokra.• összetett szénhidrátok: Jellemzőjük, hogy savas hidrolízissel egyszerű cukrokká bonthatók. Azösszetett szénhidrátok egy részének fizikai és kémiai tulajdonságai még nagyon hasonlítanak amonoszacharidokéra. Ezeket oligoszacharidoknak nevezzük. Az összetett szénhidrátok másikcsoportját, melyek tulajdonságai számottevően eltérnek a mono- és oligoszacharidokétólpoliszacharidoknak hívjuk.<strong>OH</strong>H<strong>OH</strong>O<strong>OH</strong>O<strong>OH</strong><strong>OH</strong>H<strong>OH</strong>O<strong>OH</strong>O<strong>OH</strong>O<strong>OH</strong><strong>OH</strong>O<strong>OH</strong><strong>OH</strong>H<strong>OH</strong>O <strong>OH</strong>OO<strong>OH</strong> O<strong>OH</strong>O<strong>OH</strong><strong>OH</strong><strong>OH</strong>OO<strong>OH</strong><strong>OH</strong>O<strong>OH</strong>O<strong>OH</strong><strong>OH</strong>OO<strong>OH</strong>O<strong>OH</strong>O<strong>OH</strong>HO116
Szénhidrátok szerepe•energiahordozók•növényekben: fotoszintézis•vázanyagok: a szénhidrátokból keletkező polimerek (cellulóz, kitin)•Biológiai információk hordozói: A szénhidrátok és konjugátumaik (glikopeptidek, glikolipidek) az élősejt felületén gondoskodnak a sejt adhézióról (tapadás), részt vesznek a sejt osztódás gátlásában,szerepük van a vírusok, baktériumok és hormonok valamint toxinok sejten való megkötődésében ésirányítják az immunválaszt. Szerepük van az ivarsejtek egymásra találásában. Mint nukleozidokalkotóelemei közvetői a genetikai folyamatoknak (RNS, DNS, receptorok a sejt membrán felületén /glikolipidek, glikoproteidok)•Királis kiindulási anyagok(CO 2 )n + (H 2 O)nhklorofil(CH 2 O)n + (O 2 )niparbanüzemanyagpótlóEt<strong>OH</strong>keményítõSzervezetben: cukorlebontásglükóz H 2 O + CO 2 675 kcal / mol117
MonoszacharidokA monoszacharidok mint a-hidroxi-oxovegyületek az oxocsoport jellege szerint aldózokra és ketózokraoszthatók fel, melyek külön-külön tovább csoportosíthatók szénatomszámuk szerint. Tekintettel arra,hogy ezek a vegyületek több kiralitás centrumot is tartalmaznak, így több sztereo izomerrel isszámolnunk kell (2 n ).<strong>OH</strong>O<strong>OH</strong>HOCHOaldotriózH<strong>OH</strong>OCHO<strong>OH</strong><strong>OH</strong>O <strong>OH</strong>ketotriózH<strong>OH</strong>O<strong>OH</strong><strong>OH</strong>HO<strong>OH</strong>CHOaldopentóz<strong>OH</strong>HOO<strong>OH</strong>ketopentóz<strong>OH</strong>OaldotetrózH<strong>OH</strong>OCHO<strong>OH</strong>HOketotetrózH<strong>OH</strong>O<strong>OH</strong><strong>OH</strong><strong>OH</strong><strong>OH</strong>aldohexózketohexózAz azonos összegképletű aldózok és ketózok egymás izomerjei. Általános összegképletük(CH 2 O) n alakban is felírható.118
Az oxocsoporttól legtávolabb levőszénatom konfigurációja szerint: D-,vagy L-konfiguráció (a ketotriózkivételével minden molekula egy, vagytöbb aszimmetriás centrumottartalmaz)119
Szénhidrátok térszerkezetének ábrázolása:Fischer-féle vetítésoxCredHCHO<strong>OH</strong>CH 2 <strong>OH</strong>HOCH<strong>OH</strong>CH 2 <strong>OH</strong>DL2 CHOCHO2 x4 H C <strong>OH</strong> 1HO C CH 2 <strong>OH</strong>CH 2 <strong>OH</strong>H3HOCHOCH 2 <strong>OH</strong>R120
epimer cukrokHH<strong>OH</strong>HCHOCHOCHOCHO<strong>OH</strong>H<strong>OH</strong><strong>OH</strong>CH 2 <strong>OH</strong>CH 2 <strong>OH</strong>CH 2 <strong>OH</strong> CH 2 <strong>OH</strong>D-glükóz D-mannóz D-galaktóz2 4 =168 db D8 db Lepimer cukroknem epimerek121
A szénhidrátok egyensúlyi elegyében a nyílt láncú forma és a ciklofélacetál öt- vagy hattagú gyűrűsállapotban található →Haworth-Böeseken-képlet (piranóz, illetve furanóz, a megfelelő heterociklusokanalógiájára): IR spektroszkópiával ugyanis nem mutatható ki a karbonilcsoport, tehát spontán,reverzibilis intramolekuláris nukleofil addícióval ciklofélacetálokként vannak jelen.OOCHOCH 2 <strong>OH</strong>OOapirán piranóz furán furanóz2xcsereH<strong>OH</strong> 2 CCHO<strong>OH</strong>H<strong>OH</strong> 2 OO<strong>OH</strong>CHCH 2 <strong>OH</strong><strong>OH</strong><strong>OH</strong>O H O <strong>OH</strong>CH 2 <strong>OH</strong> HCH 2 <strong>OH</strong> H+<strong>OH</strong>Ha-anomerb-anomer122
MutarotációAz anomerek keletkezésére (és tulajdonképpen a gyűrűs szerkezet kialakulására) a mutarotációjelensége hívta fel a figyelmet. A kristályosítás módjától függően kétféle forgatóképességű D-glükóz(vagy egyéb cukor) ismeretes.HO H<strong>OH</strong>O H<strong>OH</strong>a-D-glükofuranózHHH<strong>OH</strong>HH<strong>OH</strong>O<strong>OH</strong><strong>OH</strong>H<strong>OH</strong>b-D-glükofuranózH<strong>OH</strong><strong>OH</strong>HJégecet oldat alkohol[a] = + 112,2° [a] = +52,2 o [a] = + 18,7 oa-D-glükózHOCHO<strong>OH</strong><strong>OH</strong><strong>OH</strong><strong>OH</strong>D-glükózb-D-glükózH<strong>OH</strong><strong>OH</strong>H<strong>OH</strong>O<strong>OH</strong>HHHO<strong>OH</strong>a-D-glükopiranózH<strong>OH</strong>HHHO<strong>OH</strong><strong>OH</strong>Hb-D-glükopiranózMutarotáció: a D-glükóz vizes oldatának optikai forgatása oldás után folyamatosan változik azegyensúly beállásáig ([a] D = 57).123H<strong>OH</strong>
Mutarotációs egyensúlyi elegyek összetétele
Hexózok konformációjaaeeOaOO4 C 1 konformer 4C 1 konformer(stabilabb)4<strong>OH</strong>5 O<strong>OH</strong><strong>OH</strong>3<strong>OH</strong>12<strong>OH</strong>54<strong>OH</strong>6<strong>OH</strong>3<strong>OH</strong>O2<strong>OH</strong>1<strong>OH</strong>H<strong>OH</strong>O43<strong>OH</strong>52O<strong>OH</strong>1<strong>OH</strong>4C 1b-D-glükopiranóz4 C 1legstabilabb szerkezetH mind axiális<strong>OH</strong>, CH 2 <strong>OH</strong> mind ekv.125csupa transz
Anomer effektusAz a-D-glükóz esetén is a 4 C 1 -konformáció a kedvezményezett, jóllehet ilyenkor a glikozidoshidroxilcsoport már nem ekvatoriális, hanem axiális térállású. A 4 C 1 -konformációban a glikozidoshidroxilcsoport és a C-3, valamint a C-5 szénatomokhoz kapcsolódó hidrogénatomok közelsége (1,3-diaxiális kölcsönhatás) a molekula energiatartalmát növeli. Az energiatartalom növekedését az ún.anomer effektus, mint energianyereség viszont ellensúlyozza. Az anomer effektus ugyanis azt jelenti,hogy a gyűrű oxigénatomjának axiális térhelyzetű nemkötő elektronpárja (mint HOMO-pálya),kölcsönhatásba lép a vele azonos síkban levő glikozidos <strong>OH</strong>-csoport szén-oxigén kötésének lazítópályájával (mint LUMO-pálya). A megfelelő előjelű pályarészek átlapolása jelentős energia nyereséggeljár.HH<strong>OH</strong><strong>OH</strong><strong>OH</strong>HO1 HH <strong>OH</strong><strong>OH</strong><strong>OH</strong><strong>OH</strong><strong>OH</strong>On1 O<strong>OH</strong><strong>OH</strong>O *Ha-D-glükóz126
Éter- és észterképzési reakciókH<strong>OH</strong><strong>OH</strong><strong>OH</strong>HHHO<strong>OH</strong><strong>OH</strong>H(CH 3 ) 2 SO 4K<strong>OH</strong>H 3 C<strong>OH</strong> 3 C<strong>OH</strong>OCH 3HHH<strong>OH</strong>OCH 3OCH 3híg HClH 3 C<strong>OH</strong> 3 C<strong>OH</strong>OCH 3HHHOOCH 3<strong>OH</strong>HH<strong>OH</strong>absz CH 3 <strong>OH</strong> / HClAc 2 O/piridinHOAcH<strong>OH</strong><strong>OH</strong>HH<strong>OH</strong><strong>OH</strong>OCH 3metil-a-D-glükopiranozidAcOAc<strong>OH</strong>HHOOAcOAcHA poranóz (furanóz) gyűrűvé záródás során félacetál keletkezik és az így keletkezett hidroxil csoportreaktivitása számottevően különbözik a többiétől.Azokat az étereket, melyek a glikozidos hidroxilcsoporton jönnek létre O-glikozideknek nevezzük.127
A primer hidroxilcsoport védésére használják a tritil-kloridot (trifenilklórmetán) is, amit katalitikushidrogénezéssel könnyen el lehet távolítani.<strong>OH</strong>OTrH<strong>OH</strong><strong>OH</strong>OOOMeTr-ClPyH<strong>OH</strong><strong>OH</strong>OOOMeTr = Ph 3 C-A benzil csoport is gyakran alkalmazott védőcsoport a szénhidrátkémiában is.H<strong>OH</strong><strong>OH</strong>O<strong>OH</strong>OOMePhCH 2 ClDMF/NaHkat. H 2- PhMeA benzil csoport eltávolítása másképpen is lehetséges:BnOBnOBnOOBnOOMeH O CH 2 PhBr 2 / hH O CH Ph<strong>OH</strong>H O CH PhBr<strong>OH</strong>H / H 2 <strong>OH</strong> <strong>OH</strong> PhCHO128
Egyéb észter származékokH<strong>OH</strong>R-SO 2 ClpiridinHOMs(Ts)NuS N 2NuHinverzióLiAlH 4Nu = Hlg, MeO, N 3 , CN, Ac<strong>OH</strong>HdezoxicukorH O MeONa OMe / Me<strong>OH</strong>kat. mennyiségHOOMeOMeHOMeOOMeMe<strong>OH</strong>Zemplén-féle deacetilezésMe<strong>OH</strong><strong>OH</strong>129
Acetál képzésH<strong>OH</strong><strong>OH</strong>O<strong>OH</strong>O<strong>OH</strong>Me 2 C<strong>OH</strong>CHOOO<strong>OH</strong>OO<strong>OH</strong>CH 2 <strong>OH</strong>PhCHOZnCl 2HNCrO31,2-5,6-diizopropilidén-D-glükóz(diacetonglükóz)Ac<strong>OH</strong> / vízkat. H 2OPhO<strong>OH</strong>O20 o CH<strong>OH</strong>O<strong>OH</strong><strong>OH</strong>O<strong>OH</strong><strong>OH</strong>4,6-benzilidén-D-glükózO<strong>OH</strong>OOOOOmonoacetonglükózred.HOO<strong>OH</strong>OO<strong>OH</strong>a diacetonglükóz epimerje(egy <strong>OH</strong> konfigurációjábankülönböznek csak)130
Oxocsoport reakcióiOxidációs és redukciós reakciók:CHOCO<strong>OH</strong>híg HNO 3 v.Br 2 / vízH<strong>OH</strong>O<strong>OH</strong>OOCH 2 <strong>OH</strong>CH 2 <strong>OH</strong><strong>OH</strong>glükóz glükonsav g-lakton(aldonsav)H<strong>OH</strong>O<strong>OH</strong>O<strong>OH</strong>red.laktol<strong>OH</strong>A cukrok redukcióval cukoralkoholokká, enyhe oxidációval aldonsavakká, míg erélyes oxidációvalaldársavakká alakíthatóak.131
CO<strong>OH</strong>CO<strong>OH</strong>CO<strong>OH</strong>CH 2 <strong>OH</strong>HNO3CO<strong>OH</strong>- H2<strong>OH</strong>O<strong>OH</strong>O<strong>OH</strong>monolaktonO+ O- H2O<strong>OH</strong>O<strong>OH</strong><strong>OH</strong>CO<strong>OH</strong>glükonsavglükársav(aldársav)H<strong>OH</strong>OO<strong>OH</strong><strong>OH</strong>OOdilakton<strong>OH</strong>OOCO<strong>OH</strong>132
Ezüst tükör póba: az aldózok az Ag(NH 3 ) 2 oldatából fém ezüstöt választanak ki miközben aldonsavakkáoxidálódnak.Fehling póba: az aldózok Cu(II)SO 4 -nak KNa-tartaráttal képzett komplexéból vörös színű Cu 2 O-tválasztanak le miközben aldonsavakká oxidálódnak.133
Redukciós átalakításokO<strong>OH</strong>C<strong>OH</strong>red.CH 2 <strong>OH</strong>cukoralkoholEpimerizációC<strong>OH</strong>CH<strong>OH</strong>C<strong>OH</strong>HC<strong>OH</strong>C<strong>OH</strong>HOCHD-glükóz endiol D-mannózCH 2<strong>OH</strong>COD-fruktóz134
Kondenzációs reakciókCHOPh-NH-NH 2HCHN<strong>OH</strong>NHPhCH NH NHPhCH NHO HO2 Ph-NH-NH 2ox.-red.- PhNH 2CH 2 <strong>OH</strong>CH 2 <strong>OH</strong>hidrazonCH 2 <strong>OH</strong>CH 2 <strong>OH</strong>Schiff bázis(imin)NH 2CHNNNHPhNHPhCH NH<strong>OH</strong>NH PhNH NH Ph- NH 3- H 2 OCH 2 <strong>OH</strong>D-glükóz-feniloszazonCH 2 <strong>OH</strong>135
Wohl-Zemplén féle lebontásCHOCH 2 <strong>OH</strong>NH 2 -<strong>OH</strong>CHN<strong>OH</strong>CH 2 <strong>OH</strong><strong>OH</strong>Ac 2 O- H 2 OAcOCNOAcOAcOAcCH 2 OAcNaOMeMe<strong>OH</strong>D-glükóz oxim nitril aldehid-ciánhidrinOCNOOOCH 2 <strong>OH</strong>HOCHO<strong>OH</strong><strong>OH</strong>CH 2 <strong>OH</strong>D-arabinóz136
Kiliani-féle felépítés (lánchosszabbítás)CH<strong>OH</strong>O<strong>OH</strong><strong>OH</strong>CH 2 <strong>OH</strong>D-arabinózHCNHHOCNC <strong>OH</strong><strong>OH</strong><strong>OH</strong>CH 2 <strong>OH</strong>+H<strong>OH</strong>OCNC H<strong>OH</strong><strong>OH</strong>CH 2 <strong>OH</strong>H- NH3HHOCO<strong>OH</strong>C <strong>OH</strong><strong>OH</strong><strong>OH</strong>CH 2 <strong>OH</strong>+H<strong>OH</strong>OCO<strong>OH</strong>C H<strong>OH</strong><strong>OH</strong>CH 2 <strong>OH</strong>HH<strong>OH</strong>HCHO<strong>OH</strong>H<strong>OH</strong><strong>OH</strong>CH 2 <strong>OH</strong>H<strong>OH</strong><strong>OH</strong>HCH<strong>OH</strong>H<strong>OH</strong><strong>OH</strong>CH 2 <strong>OH</strong>H<strong>OH</strong>Ored.Na(Hg) / H +<strong>OH</strong>O<strong>OH</strong>O+H<strong>OH</strong>O- H 2 O<strong>OH</strong>O<strong>OH</strong>OD-glükózD-mannóz137
DiszacharidokH<strong>OH</strong>ORedukáló diszacharidok<strong>OH</strong>O<strong>OH</strong><strong>OH</strong><strong>OH</strong>O<strong>OH</strong>cellobiózb-D-glükopiranozil (1-4)-b-D-glükopiranóz<strong>OH</strong>HO<strong>OH</strong>O<strong>OH</strong><strong>OH</strong>OO<strong>OH</strong>O<strong>OH</strong><strong>OH</strong>Laktózb-D-galaktopiranozil-(1-4)-b-D-glükopiranóz<strong>OH</strong>H<strong>OH</strong><strong>OH</strong>ONem redukáló diszacharidHO<strong>OH</strong><strong>OH</strong>O<strong>OH</strong>O<strong>OH</strong><strong>OH</strong>O<strong>OH</strong>O<strong>OH</strong>O<strong>OH</strong><strong>OH</strong><strong>OH</strong>a-D-glükopiranzozil-(1-2)-b-D-fruktofuranózSzacharózOA redukáló diszacharidok adják az ezüst tükör és aFehling próbát.<strong>OH</strong>maltóza-D-glükopiranozil (1-4)-b-D-glükopiranóz<strong>OH</strong>138
Invertcukor és műmézA szacharóz híg ásványi savakkal vagy enzimatikus úton D-glükózra és D-fruktózra hidrolizál. Ahidrolízis során a cukoroldat forgatóképessége folyamatosan csökken, eléri a nulla értéket, majd balraforgatóvá válik, mivel a fruktóz erősebben forgat balra, mint a glükóz jobbra. A forgatóképességelőjelének megváltozása miatt a szacharóz hidrolízisét invertálásnak, és az így nyert egyszerű cukorkeveréket invertcukornak („műméz”) nevezik.A mézhamisítás leggyakoribb módja a virágmézként árult műméz. A műméz invertcukorból aromásanyagok (néha zamatos méz) hozzákeverésével és festékanyagok színezésével készül. A hamisítástkönnyen felismerhetjük, ha egy kávéskanálnyi mézet tiszta szeszben feloldunk. Amennyiben teljesenoldódik, úgy a méz tiszta. Ellenkező esetben homályos lesz és rövid idő múlva a belekevert anyagleülepedik.139
Diszacharidok szintézise Koenigs-Knorr módszerrelNaOAc / NaOMeD-glükózTrCl / piridinAcOTrOOAcOAcOOAcH<strong>OH</strong><strong>OH</strong>O<strong>OH</strong>OAc<strong>OH</strong>HBr / jégecetAc 2 O / PyAcOTrOOAc<strong>OH</strong>OAcOOAcOAcOAcBrOAcOAcHHOkat. H 2 , Me<strong>OH</strong>Ag 2 CO 3CHCl 3 / C 6 H 624 o CAcOOAcOAcOOAcOAcHOOOAcOAcHOAcOAcOAcoktaacetilgenciobiózOOAcOAcHkat. NaOMeMe<strong>OH</strong>genciobióz140
Poliszacharidok**H<strong>OH</strong>O*HO<strong>OH</strong>O<strong>OH</strong><strong>OH</strong>ONHO<strong>OH</strong>HO<strong>OH</strong><strong>OH</strong>O<strong>OH</strong>OO<strong>OH</strong><strong>OH</strong><strong>OH</strong>O<strong>OH</strong><strong>OH</strong>OONHOOnn**Cellulóz: b-D-glükoporanozil-(1,4)-b-D-glükopiranózKitin: b-D-N-acetil-glükózamin b-(1,4)-kapcsolódású homopolimereKeményító: a-D-glükóz egyslgekből épül fel, melyekazamilózban a(1,4)-kötéssel kapcsolódnak össze.Helikális struktúra.Az amilopektinben az a-(1,4) kötések mellet 15-22egységenként a-(1,6) kötések is vannak.A keményítő a növényi tartaléktápanyag.Az állati megfelelője a glikogén, aminek a felépítésemegegyezik az amilopektinével.n141
Az anyatej oligoszacharidjaiVédő hatás bakteriálisfertőzések ellenA baktériumoklektinjeihez kötődvemegakadályozzák azokadhézióját azepithelialis sejtekhezForrás:J. Kemsley,Chem. Eng. News, 2008, 86, 13.
CiklooligoszacharidokCiklodextrinekagb
Ciklodextrinek
Monoszacharidok bioszintézisének útvonalai
Monoszacharidok bioszintézisének kulcsreakciói
Monoszacharidok bioszintézise – a Calvin-ciklus
Monoszacharidok bioszintézise – a CO 2 fixálásának első lépéseiH 2 COPH 2 COPH 2 CC OC <strong>OH</strong>OOC C <strong>OH</strong><strong>OH</strong>C <strong>OH</strong>C <strong>OH</strong>C O H+ CHC <strong>OH</strong> HC <strong>OH</strong>HC <strong>OH</strong><strong>OH</strong> 2 C O P H 2 C O PH 2 C O PRibulóz-1,5-biszfoszfátH 2 C O PH 2 C O PC O iC <strong>OH</strong> 2 C <strong>OH</strong> CO<strong>OH</strong>HO CHHC <strong>OH</strong>HC <strong>OH</strong>CHO H 2 C O PHC <strong>OH</strong>HC <strong>OH</strong>iiH 2 C O PH 2 C O PFruktóz-1,6-biszfoszfátiiiP = P(=O)<strong>OH</strong> 2OPHH<strong>OH</strong>OOCHOOCi: dihidroxiaceton-foszfátii: glicerinsav-3-foszfátiii: glicerinaldehid-3-foszfátH 2 CCCHCH 2 CH 2 CCHHO C+HCH 2 CO P<strong>OH</strong>O<strong>OH</strong>O PO P<strong>OH</strong>O<strong>OH</strong>O P
Oligoszacharidok bioszintézisének fontosabb reakcióiSzacharóz képződése UDP-vel aktivált D-glükóz anomer centrumánlejátszódó nukleofil szubsztitúcióval.Kérdés: Miért nem változik a<strong>OH</strong>konfiguráció?HO O<strong>OH</strong>H<strong>OH</strong><strong>OH</strong>O <strong>OH</strong>OOUDPH<strong>OH</strong>O+O<strong>OH</strong>OP OO<strong>OH</strong><strong>OH</strong>H<strong>OH</strong>O<strong>OH</strong><strong>OH</strong>OOP O OP ONHHOO N<strong>OH</strong> <strong>OH</strong>OP = P(=O)<strong>OH</strong> 2UDPHO<strong>OH</strong>
A glikogén bioszintéziseA glükóz anomer centrumának aktiválásaUDP-vel történik.Az újabb monoszacharid egységek a láncnem redukáló(!) végére épülnek be.
A keményítő bioszintéziseA glükóz anomer centrumának aktiválása ADP-vel történik.Az újabb monoszacharid egységek a lánc redukáló(!) végére épülnek be.H<strong>OH</strong>O<strong>OH</strong>NOOP O <strong>OH</strong>O P O O NHO<strong>OH</strong> <strong>OH</strong>OADPADPHO <strong>OH</strong>NH 2NN
Oligo- és poliszacharidok (ipari) felhasználása – válogatásCiklodextrinekanyagok védelme oxidáció és UV-degradáció ellen feldolgozás vagytárolás során; illat/aromaanyagok, fűszerek stabilizálása;élelmiszer/gyógyszer keserűségének vagy kellemetlen illatának elfedése;folyadékok száraz formába alakítása; vízoldhatóság növelése;szénhidrogének, szteroidok, zsírok, zsírsavak emulzifikálása; gyógyszerek,illat/aromaanyagok kontrollált kibocsátása; kémiai reakciók katalízise;elválasztástechnika (kromatográfia, kapilláris elektroforézis).Cellulózpapíripar, textilipar (pamut, len, stb), „nitrocellulóz” (cellulóz-nitrát;lőgyapot, celluloid); cellulóz-acetát (szigetelő filmek, lakkok, ragasztók,szálak); viszkóz (műselyem, cellofán).Keményítőélelmiszeripar (gélesítés, ételszerkezet módosítása, sörfőzés, stb);textilipar (szálak írezése: felületük lesimítása); gyógyszeripar (hordozó- éskötőanyag);bioetanol gyártás.Kitingyógyszeripar (hordozó- és kötőanyag, antibakteriális sebkötözőanyagok);biodegradábilis csomagoló anyagok.
Shown here is thepeptidoglycan of the cell wallof Staphylococcus aureus, agram-positive bacterium.Peptides (strings of coloredspheres) covalently link N-acetylmuramic acid residues inneighboring polysaccharidechains. Note the mixture of Land D amino acids in thepeptides.Szerkezeti (váz) poliszacharidok – peptidoglikán, murein (baktériumok) (egy vagytöbb oligoszaccharid lánc kovalensen kötve fehérjékhez (Asn, Ser, Thr))GlcNAcMur2AcPeptidoglycan
Proteoglikánok: glikóz-aminoglikánok+ extracelluláris proteinekProteoglycan aggregate of theextracellular matrixOne very long molecule ofhyaluronate is associatednoncovalently with about 100molecules of the core proteinaggrecan. Each aggrecan moleculecontains many covalently boundchondroitin sulfate and keratansulfate chains. Link proteins situatedat the junction between each coreprotein and the hyaluronatebackbone mediate the core protein–hyaluronate interaction.
Glikoproteinek – oligoszacharid-fehérje konjugátumok
A cukrok információhordozó kapacitásaA képződő izomerek száma sokszorosan felülmúlja bármely másbio(oligo)polimer lehetőségeitMonomer Termék Izomerek számaösszetétel Peptidek SzacharidokX 2 Dimer 1 11X 3 Trimer 1 176XYZ Trimer 6 1056H 2 NH 2 NH CRH CRCO<strong>OH</strong>CO<strong>OH</strong> szekvencia szekvenciaHO H<strong>OH</strong>O kapcsolódási pont anomer konfiguráció elágazásokO<strong>OH</strong><strong>OH</strong>HO H<strong>OH</strong>OO<strong>OH</strong> további módosítások: pl. szulfonil-, foszforil-,acetil-, metilcsoportokkal<strong>OH</strong>
Oligonukleotidok, oligopeptidek és oligoszacharidok sokféleségeA szénhidrátkódHO HO <strong>OH</strong>OD-Glc <strong>OH</strong> <strong>OH</strong>(2.5 %; a - 0.8 %)H<strong>OH</strong><strong>OH</strong>OD-GalO<strong>OH</strong> <strong>OH</strong>(24.8 %; b - 23 %)HO H<strong>OH</strong>O<strong>OH</strong>OD-Man <strong>OH</strong>(18.9 %; a - 8.2 %)H<strong>OH</strong>OD-Xyl(0.1 %)O<strong>OH</strong><strong>OH</strong>HO HO <strong>OH</strong>OAcNH <strong>OH</strong>D-GlcNAc(31.8 %; b - 8 %)H<strong>OH</strong>OOCHOD-GlcA(0.3 %)O<strong>OH</strong><strong>OH</strong>Forrás: P. H. Seeberger et al.,ACS Chem. Biol., 2007, 2, 685.H<strong>OH</strong>O<strong>OH</strong>OAcNH <strong>OH</strong>D-GalNAc(4.8 %; a - 2.3; b - 2.2 %)HO <strong>OH</strong><strong>OH</strong>OOC <strong>OH</strong> <strong>OH</strong>L-IdoA (0.1 %)HO <strong>OH</strong>CO<strong>OH</strong><strong>OH</strong>HO <strong>OH</strong> 3 C OAcNH<strong>OH</strong><strong>OH</strong><strong>OH</strong>HO <strong>OH</strong>D-Sia (8.3 %; a - 26.1 %) L-Fuc (7.2 %; a - 23.8 %)MonoszacharidElőfordulás (%)Végcsoportként (%)3299 emlősoligoszacharidstatisztikaielemzése alapján
Nukleinsavak, nukleotidok, nukleozidok1869-ben Miescher a sejtmagból egy savas természetű, lúgban oldódó foszfortartalmú anyagot izolált,amit később, eredetére utalva nukleinsavnak nevezetek el. Kiderült, hogy a nukleinsavak és különbözőszármazékaik minden sejtben előfordulnak és nélkülözhetetlen feladatokat látnak el.A nukleinsavak nagy molekulatömegű polimer molekulák. A különféle sejtekből nyert nukleinsavak teljeshidrolízisével pentózokat, purin- és pirimidinbázisokat, valamint foszforsavat lehet izolálni. A hidrolíziskörülményeinek (savas, lúgos vagy enzimatikus) változtatásával részleges lebontás is megvalósítható. Azígy nyerhető összetett építőegységek közül a nukleotidokban a cukormolekulához szerves bázis ésfoszforsav kapcsolódik, a nukleozidokban pedig a cukor szerves bázissal képez vegyületet.NukleinsavakHOO <strong>OH</strong>HOO <strong>OH</strong>NukleotidokRészleges hidrolízis<strong>OH</strong><strong>OH</strong>ribóz<strong>OH</strong>dezoxiribózRészleges hidrolízisNukleozidok + foszforsavRNNNNR H 3 PO 4N NHHidrolízisPentózok + purin vagypirimidin bázisDNS: dezoxiribonukleinsav - cukor komponense a dezoxiribózRNS: ribonukleinsav – cukor komponense a ribóz158
A nukleinsavakat felépítő bázisok szerkezeteBázisként pirimidin- és purinvázas vegyületek izolálhatók, mégpedig az előbbiek uracil, timin vagycitozin lehetnek, az utóbbiak adenin vagy guanin. A vegyületek jelölésére gyakran nevük kezdőbetűjét(U, T, C, A, G) használjuk.A bázisok jelenléte nem teljesen tetszőleges. Az uracil csak az RNS-ben, a timin csak a DNS-benfordul elő, a további három bázis pedig mindkét nukleinsavban megtalálható.<strong>OH</strong>NONH<strong>OH</strong>NONHONNH 2NHNNH 2NNHNH 2 NHNONNHNuracil timin citozinadeninguaninHOA nukleozidok nevét a bázisok nevéből képezzük úgy, hogy pirimidinbázis esetén idin végződést,purinbázis esetén pedig ozin végződést illesztünk a bázis nevének első részéhez. A DNS-ből nyertnukleozidok nevéhez dezoxi előtag járul.<strong>OH</strong>NOONHO<strong>OH</strong>NOONHOOONNH 2NHOONONH 2NNHONH 2NONNHONNH 2NONNH 2 NHNHOONONNH 2 NHNHOONONNH<strong>OH</strong><strong>OH</strong><strong>OH</strong><strong>OH</strong><strong>OH</strong><strong>OH</strong><strong>OH</strong>O<strong>OH</strong> <strong>OH</strong> <strong>OH</strong> <strong>OH</strong>uridin timidin dezoxicitidin citidin dezixiadenozin adenozin dezoxiguanozin guanozin159
Nukleozidok előállítása, fizikai és kémiai sajátságaA nukleinsavak szerkezetfelderítése szempontjából jelentős a nulkleozidok szintetikus úton történőelőállítása is. Ennek egyik lehetséges és gyakori módja, amikor acilezett a-d-ribofuranozil-kloridból és amegfelelően védett purin- vagy pirimidinszármazék klórmerkuri sójából kiindulva alakítják ki a b-glikozidos kötést.NHNHAc2NNNNNHAcAcO HON NN NClNN HgCl 2+Na<strong>OH</strong>xilol / <strong>OH</strong>N NAc<strong>OH</strong>AcOO2 OOOAcHgClAcO OAc<strong>OH</strong><strong>OH</strong>adenozinA nukleozidok magas olvadáspontú, vízben jól oldódó színtelen kristályos vegyületek. A glikozidoskötés lúggal szemben ellenálló, míg híg savval könnyen hidrolizálható, miközben pentóz és bázisképződik. A dezoxiribonukleozidok esetében kíméletes körülményeket kell alkalmazni, mivel aképződő 2-dezoxi-d-ribóz savérzékeny.160
A nukleotidok szerkezete, fizikai és kémiai sajátságaikA nukleotidok a nukleinsavak háromrészes építőegységei. Foszforsavészterek, melyek a nukleinsavakbólenyhe lúgos vagy enzimatikus hidrolízis hatására képződnek. A hidrolízistermékek között aribonukleinsavak esetében 2’-, 3’- és 5’-foszfátok, a dezoxiribonukleinsavak esetében pedig 3’- és 5’-foszfátok fordulnak elő.A nukleotidok nevét a nukleozidok nevéből képezzük úgy, hogy megjelöljük az észteresítetthidroxilcsoport helyét. Szokásos a nukleotidok nevét rövidítve megadni, például uridin-5’-foszfát = 5’UMP.OO<strong>OH</strong>NHNHNHO OOPHOOONuridin-5'-foszfátHO<strong>OH</strong><strong>OH</strong>O <strong>OH</strong>O <strong>OH</strong>HOPO <strong>OH</strong>ONuridin-3'-foszfátHOOONOOP <strong>OH</strong><strong>OH</strong>uridin-2'-foszfátA nukleotidok magas olvadáspontú, vízben oldódó kristályos vegyületek. A dihidrogénfoszfátcsoport jelenléte miatt erős savak. A nukleotidok óvatos savas hidrolízise a glikozidos kötéshasadásával bázist és pentózfoszfátot eredményez, lúgos hidrolízissel pedig a foszforsav sójamellett a megfelelő nukleozidot lehet izolálni.161
A nukleinsavak elsődleges szerkezeteA nukleinsavak nukleotidokból épülnek fel úgy, hogy a polinukleotid láncban a pentózok 5’ és 3’hidroxilcsoportja foszforsavdiészter-kötéssel kapcsolódik össze. A pentózok 2’ szénatomján a DNS-benhidrogén, az RNS-ben pedig szabad hidroxilcsoport található. Tehát a polimer molekula gerincét, primerszerkezetét mind a DNS-ben, mind az RNS-ben a pentóz-foszfát lánc alkotja, melynek változékonyságát acukorrészhez kapcsolódó bázisok jelentikBNO<strong>OH</strong>O P <strong>OH</strong>O<strong>OH</strong>nukleozid-3'-foszfátlép-foszfodiészteráz5' kötést hasítBNO5'-végBNOOO P <strong>OH</strong>O<strong>OH</strong>3'-végOOPO <strong>OH</strong><strong>OH</strong>OBNOOOP <strong>OH</strong>OOOPHOO<strong>OH</strong>OPO<strong>OH</strong>OOP OO ONOBkígyóméreg-foszfodiészterázNB3' kötést hasítOOPHOBNO<strong>OH</strong><strong>OH</strong>nukleozid-5'-foszfátNBONBA nukleinsavakat alkotó nukleotidegységek kapcsolódási módjának felismerését többek között aztette lehetővé, hogy találtak olyan specifikus enzimeket, melyek a polinukleotid lánc észterkötésétcsak az 5’-helyzetű vagy csak a 3’-helyzetű hidroxilcsoportnál hasítja el.162
A bázissorrend meghatározásaA nukleotidok kapcsolódási sorrendjét (szekvenciáját) ugyancsak enzimek segítségével derítettékfel. Az ún. restrikciós enzimek meghatározott szekvenciájú kisebb nukleotid láncokat hasítanak ki apolimerből. A szétszabdalt láncok újra egyesíthetők a DNS ligáz enzim segítségével, a DNS polimerázenzim pedig a DNS szintézist katalizálja.A DNS bázissorrendjének meghatározása Sanger nevéhez fűződik: szekvenálási eljárás alapelve nema lebontás, hanem az enzimkatalizált DNS-szintézis irányított megszakítása. A szintézismegszakítására 2’,3’-didezoxi-ribózt alkalmazott, ami a 3’ láncvégen nem tud észteresedni, ezért azeljárás didezoxi módszer néven vált ismertté.A különböző eredetű DNSmolekulákhidrolizátumában apurinbázisok (adenin és guanidin)moláris mennyisége mindigazonos a pirimidinbázisokéval(timin és citozin), sőt továbbiszabályosság, hogy az adeninmennyisége a timinével, valaminta guanin mennyisége a citozinévalazonos (Chargaff-szabályok 1950).Az RNS-ek esetében nincs ileynszabályserűségFrederick Sanger (1918 -)Nobel díj – 1958: inzulin aminosav sorrendjének meghatározásaNobel díj – 1980: DNS szekvencia meghatározásáértErwin Chargaff (1905 – 2002)163
3,4 nmA DNS másodlagos szerkezete - 19532 nmFrancis H.C. Crick (1916 – 2004)Nobel díj: Nukleinsavakszerkezeténekmeghatározásáért - 1962James D. Watson (1928 -)Nobel díj: Nukleinsavakszerkezeténekmeghatározásáért - 1962164
A DNS szerkezeteX-ray diffraction pattern ofDNA. The spots forming across in the center denote ahelical structure. The heavybands at the left and right arisefrom the recurring bases.
A DNS szerkezet változataiA-formaB-forma (balra)A-forma (középen)Z-forma (jobbra)B-formaZ-forma
A DNS szerkezet változataiB-forma A-forma Z-formaSzínkód: foszfodiészter lánc és a furanózgyűrűk – zöld; purin bázisok –piros; pirimidin bázisok – kék.
A DNS szerkezetek adatai
DNS szuperszerkezetekSchematic illustration of closed circular DNA in open conformation(left) and then in a negative supercoiled conformation (middle) andpositive supercoiled conformation (right).
Bázispárok a DNS-ben (Watson-Crick modell)
A DNS másodlagos szerkezet II.A DNS-t alkotó két polinukleotid lánc kettős helixet alkotva egymás mellé csavarodik. A hélix külsőpalástját a pentóz-foszfát polimer lánc alkotja, a paláston belül pedig a bázisok páronkénthidrogénkötésekkel kapcsolódnak össze. A bázisok mólarányainak megfelelően a bázispárokösszekapcsolódása nem lehet tetszőleges. Az adenin csak a timinnel, a guanin csak a citozinnal alkothatbázispárt.<strong>OH</strong> 2 NNNH 2ONC 1'NNH NO1,1 nmNNC 1'C 1'NNH NO H 2 N1,1 nmNNC 1'TACGA DNS-t alkotó két polinukleotid lánc kettős helixet alkotva egymás mellé csavarodik. A hélix külsőpalástját a pentóz-foszfát polimer lánc alkotja, a paláston belül pedig a bázisok páronkénthidrogénkötésekkel kapcsolódnak össze. E szabályos szerkezet kialakulásához az szükséges, hogy akét összecsavarodó lánc szerkezete pontosan megfeleljen egymásnak. A két szál bázissorrendjeegymást kiegészítő, azaz komplementer szerkezetű, tehát az egyik szál bázissorrendje szigorúanmegszabja a másik szál szekvenciájátA hélix szerkezet rögzítéséhez a bázispárok hidrogénkötésein kívül, a síkban egymás felettelhelyezkedő bázisok heteroaromás gyűrűi közötti erős van der Waals-kölcsönhatások ishozzájárulnak. A DNS külső palástján a poláris pentóz-foszfát láncok vízoldhatóvá teszik amakromolekulát, ugyanakkor megvédik a belső apoláris bázisokat a külső behatástól.171
Szemikonzervatív replikációvalAz a-helix struktúra a DNS topoizomeráz és helikáz enzimek hatására szűnik meg, majd a DNSpolimeráz a szétcsavarodott szálak mellé kiépíti azok komplemeterét. Így az eredetivel teljesen azonoskét új szálat kapunk.A DNS polimeráz mindig csak az 5’ → 3’ irányba képes felépíteni az új szálat. Így az egyik szál kiépülésefolyamatos az 5’ vége felől („leading-vezető”), addig a másik szál (lagging - követő) felépülése a széttekeredés felől történik, és a keletkező fragmenseket (Okazaki fragmensek) a DNS ligáz enzim kapcsoljaössze egységes szállá.172
A DNS biológiai funkciójaDNStranszkripciómRNStranszlációFehérjékA DNS szerepe a biológiai információ hordozásában van. Ez kódolja az élő szervezet felépítéséhezszükséges fehérjék szerkezetét.• Minden hírvivő RNS egyetlen génre vonatkozó információt kódol és szállít, ami egy darabpolipeptidlánc felépítéséhez elegendő.• Minden egyes bázishármas egy meghatározott aminosavat (vagy STOP-jelet) kódol (l.aminosav-kódszótár). A riboszóma ezt az aminosavat fogja a láncba építeni.Az mRNS-en a leolvasás egy START-jellel indul. Ez a bázishármas az AUG, ami a metionintkódolja.• Van három STOP-jel is, amik leállítják a folyamatot. Ezek nem kódolnak aminosavakat.• Az információ "pont-, vessző- és átfedésmentes". Ez annyit tesz, hogy a START- és STOP-jelközött nem állhat meg a leolvasás, egyetlen bázis sem maradhat ki a leolvasásból, és nemlehet bázist kétszer olvasni.• A kód (majdnem) univerzális, mert ugyanazok a bázishármasok ugyanazokat az aminosavakatkódolják minden élőlényben.• A kód degenerált, azaz egy aminosavat több bázishármas is kódolhat.• A kód lötyög. Ez azt jelenti, hogy gyakran elég az első kettő bázist leolvasni, mert nem számít,hogy mi a harmadik. (Mindenképp ugyanazt az aminosavat kódolja.)173
Aminosav kódszótár174
mRNS1. A hírvivő RNS vagy mRNS az RNS-molekulák azon csoportjába tartozik, amely a sejtekben alegkisebb arányban fordul elő. Az mRNS-en tárolt információ meghatározza, hogy a különbözőaminosavak milyen sorrendben épüljenek be a készülő polipeptid láncba.175
Az RNS típusai, másodlagos és harmadlagos szerkezeteHírvivő (messenger) mRNSRiboszomális rRNSTranszfer tRNSA-típusú kettős helix
RNS típusok jellemzői
tRNSA tRNS a legkisebb RNS-molekula: általában 75-80 nukleotid egységből épül fel, így tömege is alegkisebb. Szerepe a fehérjék építőegységeinek, az aminosavaknak a riboszómákhoz való szállítása.Mind a 20 fehérjékben előforduló aminosavat legalább egy specifikus tRNS köt meg.Funkcionális szempontból kétlegfontosabb molekularészletük azaminosav-kötőhely és a templátfelismerőhely.Az aminosavak kötése amolekula ún. 3’ végén történik (az egyesnukleotidegységek kapcsolódása a ribóz3’ szénatomjához és 5’ szénatomjáhozkapcsolódó <strong>OH</strong>- ill. PO4-csoportokonkeresztül történik. 3’ végnek nevezzük alánc azon végét, ahol a nukleotid 3’szénatomján elhelyezkedő <strong>OH</strong>-csoporthoznem kapcsolódik foszfát. A templátfelismerőhelyetantikodonnak is szoktáknevezni. Az mRNS molekula háromnukleotidjához (egy kodonjához)kapcsolódik. A kodont alkotó nukleotidoksorrendjének megfelelően egy specifikustRNS kötődik a riboszómához, és szállítjaa növekvő polipeptidlánc (fehérje) soronkövetkező aminosavegységét. Az RNSmolekulákössztömegének 15%-át adja.178
Riboszóma RNS (rRNS)Az összes RNS tömegének 85%-át e típus adja. A riboszómák felépítésében vesznek részt (a fehérjékmellett)Az RNS-molekulák szintézisét specifikus enzimek, azRNS-polimerázok katalizálják. A polimerázokműködéséhez a következő összetevőkre van szükség:• templátmolekula: templátnak nevezzük általánosértelemben a képződő makromolekula szerkezetétmeghatározó információt hordozó molekulát, jelenesetben a DNS-t.• a nukleotidok aktivált előalakjai (prekurzorai): anégyféle bázist tartalmazó nukleozid-trifoszfátok,• fémionok (E. coliban: Mg2+ vagy Mn2+)179
A DNS harmadlagos szerkezeteA DNS-molekula óriási méretű, a legkisebbek 5000 bázispárból (5 kb; kilobázis) állnak és 1700 nmhosszúak. Az emberi DNS – a teljes humán genom – közel 6 millió kb-ból épül fel és teljes hossza eléri a2 m-t. A szabályos kettős helix természetesen meghajlik, összetekeredik és ezt tekintjük a harmadlagosszerkezetnek. A DNS-molekula szervezettségének a legmagasabb szintje a kromoszóma, ami márfehérjéket is tartalmaz a DNS mellett.A teljes DNS lánc egy-egy rövidebb szakaszát tekintjük géneknek, a gének sorrendjét pedig genetikaitérképnek nevezzük.Az 1990-ben elindított átfogó kutatás, a humán genom (HUGO) program elvezetett mind a 23 emberikromoszóma csaknem teljes nukleotidsorrendjének feltárásához.180
Nuleotid koenzimekA nukleotidok nemcsak a nukleinsavak alkotórészeként fordulnak elő az élő természetben, hanem szabadállapotban vagy egyszerűbb vegyületek formájában is. Fontos származékaik az egyes anyagcserefolyamatokatkatalizáló enzimek koenzimjei.NH 2<strong>OH</strong>OOP O<strong>OH</strong>OP O<strong>OH</strong>OP O<strong>OH</strong>ATPenergia termelõfolyamatokNNHONN<strong>OH</strong>ATPADP+ H 2 O- H 2 <strong>OH</strong>OOP O<strong>OH</strong>energia felhasználófolyamatokNH 2NNN NOP OO<strong>OH</strong>HO <strong>OH</strong>ADP+ H 3 PO 4OOP<strong>OH</strong>ONONN N<strong>OH</strong>cAMPNH 2Az ATP ADP átalakulás során felszabaduló energia fedezi az élő szervezetben lejátszódószintézisfolyamatok energiaigényét, ugyanakkor az anyagcsere során a lebomlási folyamatokbanképződő energia az ADP ATP átalakulás során elraktározódik.A cAMP egy second messenger (második hírvívő) molekula, a sejten belüli jelátviteli folyamatokban,mint például olyan hormon, mint a glukagon és az adrenalin hatásának kiváltásában, de nem képesátjutni a sejtmembránon. Fő hatása a proteinkináz enzimek aktiválása. A Ca 2+ ioncsatornákonkeresztüli áthaladásának mértékét is szabályozza.181
NH 2<strong>OH</strong> 2 NONOOOP O<strong>OH</strong>OP O<strong>OH</strong>NNNNredoxH 2 NONOOOP O<strong>OH</strong>NOP O<strong>OH</strong>NH 2NONNHO<strong>OH</strong>NADHO<strong>OH</strong>HO<strong>OH</strong>NADHHO<strong>OH</strong>CH 3 CH 2 <strong>OH</strong> + NADCH 3 CHO +NADHNH 2<strong>OH</strong><strong>OH</strong>OO NHNO<strong>OH</strong>NNOO P O<strong>OH</strong>CH 3CH 3FADNO NP O<strong>OH</strong>HONN<strong>OH</strong>redox<strong>OH</strong>NH<strong>OH</strong><strong>OH</strong>NO<strong>OH</strong>NNHOO P O<strong>OH</strong>CH 3CH 3FADH 2NO NP O<strong>OH</strong>NH 2<strong>OH</strong>ONN<strong>OH</strong>COOCOOCOO+ FAD + FADH 2OOC182
AlkaloidokAzokat a nitrogéntartalmú növényi bázisokat, amelyek pontosan körülírt fiziológiás hatással bírnakalkaloidoknak nevezzük. Az alkaloidok különböző vegyületcsaládokba tartozhatnak, mivel nincs egységesszerkezetük. Csoportosításuk történhet szerkezet, biológiai hatás és bioszintézisük alapján.AlkaloidokValódi alkaloidokProto alkaloidokPszeudoalkaloidokN-heterociklusttartalmaznakAminosavakbólképződnekNem tartalmaznakN-heterociklustN-heterociklusttartalmaznak, denemaminosavakbólképződnekA pszeudo alkaloidok bioszintézise történhet terpenoidokból vagy purinból.Egy növényben általában több alkaloid is előfordulhat, melyek alapvázának szerkezeteszükségszerűen hasonló.A legnagyobb mennyiségben jelenlévő alkaloidokat fő alkaloidoknak, míg a kisebb mennyiségbenjelenlévőket mellék alkaloidoknak nevezzük.183
OOOValódi alkaloidNkokainOProto alkaloidH 3 C<strong>OH</strong>NO<strong>OH</strong>O<strong>OH</strong>NH 2<strong>OH</strong> 3 CO CH 3 O OCH 3colchicinetirozinPszeudo alkaloidOO<strong>OH</strong>OONtaxin-BO<strong>OH</strong> <strong>OH</strong>184
Heterociklusos vegyületekCsoportosításuk történhet a gyűrű tagszáma, a heteroatomok minősége és száma szerint. Lehetnektelítettlenek, részlegesen vagy teljesen telítettek.Gyűrűtagszám szerint:O O O O <strong>OH</strong>eteroatom minősége szerint: O NH SHeteroatom száma szerint:OONNNNSA molekula telítettségi foka szerint: O O OElnevezésükre triviális nevek mellet a Hantzsch–Widman nevezéktant használjuk, mely utal a molekulagyűrűtagszámára, heteroatom minőségére, számára, helyzetére és a gyűrű telítettségi fokára is.185
Hantzsch–Widman nevezéktanAz alapnevet a heteroatom(ok) nevéből származó előtag(ok)ból és a gyűrűtagszámára utaló szótövekbőlképezzük. A heteroatomok felsorolása megadott sorrendben történik, szükség esetén a név előttihelyzetszámokkal. A monociklusos vegyületek esetében a gyűrűt a legmagasabb rangú heteroatomtól(OSN) indulva számozzuk úgy, hogy a heteroatomok a lehető legkisebb helyzetszámot kapják.O oxigén oxa-S kén tia-N nitrogén aza-Gyűrűméret Telítetlen Telített Gyűrűméret Telítetlen Telített3 -irén -irán 7 -epin -epán4 -et -etán 8 -ocin -okán5 -ol -olán 9 -onin -onán6A f -in -án 10 -ecin -ekánA 3, 4, 7, 8, 9 és 10 tagú gyűrűk végződésének szótövét a megfelelő sokszorozó tagokból képezzük: ir-t atri-ből, et-et a tetrá-ból, ep-et a heptá-ból, ok (oc)-ot az oktá-ból, on-t a noná-ból, ek (ec)-et a deká-ból;ezekhez telítetlen gyűrűk esetén az in (a 3 tagú gyűrűk esetén az én), telített gyűrűk esetén az án utótagotkapcsoljuk.186
Háromtagú heterociklusos vegyületekA háromtagú, egy heteroatomot tartalmazó telítetlen vegyületek - oxirén, az 1H- és 2H-azirin és atiirén – rendkívül instabil vegyületek.1O3 2oxirénHN13 21H-azirin2-azirin31N22H-azirin1-azirinH1S3 2A háromtagú, egy heteroatomos telített rendszerek három alapvegyülete az oxirán, az aziridin és a tiirán.tiirén1ON H11S3 23 2oxiránetilén-oxidoxaciklopropánaziridinetilén-iminazaciklopropán3 2tiiránetilén-szulfidtiaciklopropánIsmeretesek két heteroatomos telített heterociklusok is, így a dioxirán, az oxaziridin) és a diaziridinszármazékai.11HOON 13O2dioxirán32NHoxaziridin32NHdiaziridin187
Négytagú heterociklusos vegyületekÁltalában a telítetlen alapvegyületek fokozott bomlékonyságuk miatt nem vagy csak különlegeskörülmények között állíthatók elő. Bizonyos származékaik viszont létképes, stabilis vegyületek.1O2NHNNS4 3oxet(én)1-azetin2-azetinazettiet(én)A négytagú egy heteroatomos telített heterociklusok három alapvegyülete az oxetán (trimetilén-oxid), azazetidin (trimetilén-imin) és a tietán (trimetilén-szulfid). Mindhárom vegyület a síkalkattól eltérőkonformerek különböző arányú elegyeként létezik.41O2341HN2341S23YYoxetántrimetilén-oxidoxaciklobutánazetidintrimetilén-iminazaciklobutántietántrimetilén-szulfidtiaciklobutánY = O, NH, S188
Öttagú, egy heteroatomot tartalmazó vegyületekAz öttagú, egy heteroaromás vegyületek közül a legjelentősebb a pirrol, a furán a tiofén és evegyületek gyakorlati szempontból legfontosabb származékai a tetrahidrofurán, a pirrolidin, atetrahidrotiofén, valamint benzokondenzáltjaik sorában a dibenzofurán, az indol és a karbazol.5O12HN15 2 5S124 3434 3furánpirroltiofén<strong>OH</strong>N5S12tetrahidrofurántetrahidropirrol(pirrolidin)43tetrahidrotiofén(tiolán)891267HH18N7 N29127O6 5 4dibenzofurán354indol365 4benzo[b]indol(karbazol)3189
A furán, pirrol és tiofén szerkezete és előállításaHSNHO122 KJ/mol 90 KJ/mol 68 KJ/molRO1 2RO+R' X R'bázisR'RXRR'12ROR = alkil3O4RP 2 X 5RXX = O, SRR` NH 2R` = alkilR = alkil R' = EWG, pl. COOEt X = O, S, NRR` NH 2R` = H, alkil, hidroxi, aminoRNR`R190
A furán, pirrol és tiofén kémiai tulajdonságaiNHHNHNHNHpolimerizáció<strong>OH</strong> /H 2 O<strong>OH</strong> HOgyűrűfelnyílásS100%-osH 3 PO 4SSSpolimerizációS EArXXYXa-helyzetű-komplexHEHEXHEHEXHEX = NHX = OX = SSzubsztrátfurán Cl 2- 40 °COtiofén H 3 C CReagenspirrol SO 2 Cl 2Cl0 °CNHClYReakciókörülményekXXX = NH,Ofurán/pirrolpiridin SO 3SO 3 Hb-helyzetű-komplexX = Stiofén H 2 SO 4X = S,O,NRtiofén, furán, Onitrogénenvédett pirrol R COCl/SnCl 4 R C191
Reakció bázisokkalXC 4 H 9 LiXLiEXYX = NR, O, SE = CH 3CO 2IY =CH 3CO<strong>OH</strong>NHbázis- HN N NNHRMgBrNMgBr1.) (RCO) 2 O2.) H 2 ONHORAddíciós reakciókXX+ +XXXRC C RXRRX = O,S,NHdihidroszármazékoktetrahidroszármazékX = NR, O, S192
Öttagú, több heteroatomot tartalmazó vegyületek54O 1 2N31,2-oxazol(izoxazol)5O1N24 31,3-oxazol(oxazol)5H1N N25S1N24 31,2-tiazol(izotiazol)5HN 1 254S 1 2N1,3-tiazol(tiazol)354X11,2,4-1,2,3-NN2345N1X 2 51,2,5-N3XNX1,3,4-O = oxadiazolS = tiadiazol1N24 3X 15 24NN34 34N3pirazol(1,2-diazol)imidazol(1,3-diazol)ENX NvagyEXNcc.HNO 3 /H 2 SO 4NNHO 2 NNH193
Hattagú, egy heteroatomot tartalmazó vegyületekA hattagú, egy heteroatomot tartalmazó heteroaromás vegyületek a -elektronhiányos heterociklusokközé tartoznak.61O O S S261261 126 2 6 2 6 265 3 5 3 5 3 5 35 3 5 34444442H-pirán 4H-pirán 2H-tiin 4H-tiin pirilium ion tiinium ion1O1Sa'b'51N234piridinab651HN423piridínium ion781O2781O2781N2781N2636363635 454545 42H-kromén4H-kroménkinolinizokinolin194
A piridin és származékainak kémiai tulajdonságaiR IH NO 2R 1 O C RH 2 SO 4250 o C 300 o CN NNNHBrH2 250 o CSO óleum3HgSO 4HNO 3 / H 2 SO 4Br+ H HONR C ClC OSO 3RRN-alkilpiridinium-sóNO 2NNN IHNON-acilpiridinium só390 o CR 1 <strong>OH</strong>NNNN+ HSO 3OOOOpiridium-N-szulfonsavNO 2OSO 3 HOSO 3 HNN<strong>OH</strong>O195
Nukleofil szubsztitúciós reakciókA piridingyűrű nukleofil reagensekkel viszonylag könnyen reagál SNAr reakcióban.Csicsibabin-reakcióNaNH H2 ; 110 o + NaHCN N NH N NH 22R Li Ziegler-reakcióNaH 2NRHNNH NaH 2 O, LiLi<strong>OH</strong>H 2 O, Na<strong>OH</strong>NHRHoxidáció2HNR2-alkilpiridinN NH 22-aminopiridin+ Nu XN X NXNuN NuX = halogén, Nu = NH 2 , HO , RO , RS , RLi, AlH 4 , NH 3 , aminok196
Ar C Hlúgos közegN CH 32-pikolin(2-metilpiridin)<strong>OH</strong>N CH 2COArHH 2 ONAr2-stilbazol (Ar = Ph)PhLiN CH 3C 6 H 6NCO 2CH 2 LiR XLiXX = Cl, BrN CH 2R2-alkilpiridinON CH 2CHOLiOCN 2 CH 21piridin-2-ecetsav<strong>OH</strong>197
Hattagú, több heteroatomot tartalmazó vegyületekA hattagú, két vagy több heteroatomot tartalmazó ciklusos vegyületek alapvázai a háromheteroatom; a nitrogén, az oxigén és a kén variálhatósága, valamint a telítettség és telítetlenséglehetőségei miatt nagy változatosságot mutatnak.65651X42NH3N2H-1,2- 4H-1,2- 6H-1,2- oxazin tiazin1X4N23651 1X 2641X6 2 654N33552H-1,3- 4H-1,3- 6H-1,3- oxazin tiazinX41X42NN323OXS61N54NN23NNNN N1,2,3-triazin 1,2,4-triazin 1,3,5-triazin65NNNN651 14261 123NNNN441,2,3,5-tetrazin 1,2,4,5-tetrazin356523N42361X2X5N 1 26 65N42H-1,4- 4H-1,4- oxazin tiazin4N335NH1N4N2365N 1 2N4312N6N354HNN97H-purin78768NN51N4pteridinN23piridazin1,2-diazinpirimidin1,3-diazinpirazin1,4-diazin198
HN(S) N(S)-nikotinPirrolidin alkaloidokNH(S) NH(S)-nornikotinNH(S)HN(S-anatabinNNanabasinA dohány fő alkaloidja a nikotin, míg a nornikotin, anatabin és azanabasin mellékalkaloidok. E vegyületek mindegyike tartalmaz egypiridin gyűrűt. Ezen kívül a nikotinban és a nornikotinban egypirrolidin, míg a anatabin és az anabasin esetébentetrahidropirimidin gyűrű található.Valamennyi dohány alkaloid bázikus sajátságú, olajos anyag.A nikotin kis mennyiségben serkenti az agyat. Ennek köszönhető adohányzás megszokása. Nagyobb mennyiségben azonban erősidegméreg, ezért rovarölő szerként is használják.NCO<strong>OH</strong>higrincuscohigrinA higrin és a cuscohigrin a koka cserje mellék alkaloidjai.Jelentőségük eltörpül a koka cserjében található tropánvázas alkaloidok mellettNON199
Tropánvázas alkaloidokA tropán vázas alkaloidik közös alapváza a 8-azabiciklo[3.2.1]oktán. Ezen alkaloidok legtöbbje aSolanaceae családhoz tartozó növényekben fordul elő.NOOatropin<strong>OH</strong>NOOOkokainONOecogonin<strong>OH</strong><strong>OH</strong>ONOOscopolamin<strong>OH</strong>A B C DR 1ONOOcatuabin A-DORRH 3 COOCH 3OCH 3H 3 COOCH 3OCH 3NHNH 3 CR 1NH 3 CNH 3 CNH200
AtropinMaszlagos nadragulya(Atropa belladona)NOO<strong>OH</strong>atropinA növényekben szekunderanyagcseretermék, gyógyszerkéntszámos hatása van. A muszkarinosacetilkolin receptoron kompetitívantagonista. Mivel potenciálisanhalálos méreg, Atroposzról, aMoirák egyikéről kapta a nevét; agörög mitológiában ő döntötte el kihogy fog meghalni.Agonisták: azok az anyagok, amelyek valamely receptorhoz kötődnek, és azon biológiai válaszreakciótidéznek elő. Az agonisták valamely endogén ligand (hormon vagy neurotranszmitter) hatását utánozzákazzal, hogy ugyanazon receptorhoz kötődnek.Antagonisták: azok a vegyületeket, amelyek megakadályozzák az agonisták által kiváltott hatásoknak alétrejöttét azáltal, hogy a receptorhoz kötődnek.A szemészetben az atropint sugárizom-bénítónak használják, mert átmenetileg bénítja az alkalmazkodásireflexet, valamint pupillatágítóként. Mivel az atropin hatása lassan cseng le (2-3 nap), ma már inkább atropicamideot vagy a phenylephrinet (α-adrenerg agonista) használják pupillatágítóként Az atropin hatásaikét hétig is eltrarthatnak.Az acetilkolin a paraszimpatikus idegrendszer fő neurotranszmittere.Az atropint alkalmazzák idegmérgek mint például a Tabun (GA), Sarin (GB), Soman (GD) and VXantidótumaként is.201
Erythroxylum cocaNOOOOkokainKokainA kokain helyi érzéstelenítő gyógyszervalamint drog. Ezt az alkaloidot ma már csak afül-orr-gégészek használják a központiidegrendszert erősen izgató hatása miatt.Az anyagot a dél-amerikaikokacserje(Erythroxylon coca) leveleiből vonják ki. Alegtöbb országban kábítószerlistán szerepel,használata az ellenőrizhetetlen mellékhatásokmiatt tiltott.A kokain erős tudatmódosító hatású szer, használatának több – a használók által is nemkívánatosnaktartott – mellékhatása van. A legnevezetesebb a „rovarhatás”: a kokainisták a szer hatása alatt úgyérzik, „mintha bogarak mászkálnának a bőrük alatt” (ezeket a szakirodalom „kokainbogaraknak”nevezi, bár természetesen nem valódi, létező rovarokról, hanem érzékcsalódásról van szó.)A kokain közvetlen hatását az agyban fejti ki. Főképpen a dopamin és a szerotonin nevű ingerületátvivőanyagokra hat. Mindkettő az idegsejtek kommunikációjáért felel. Előbbit alapesetben egyspecializált protein, az úgynevezett dopamin transzporter szállítja vissza a helyére, miután az elvégeztefeladatát. A kokain pont ezt a visszavételt gátolja meg, így a dopamin egyre csak szaporodik aszinapszisban, ettől alakul ki az eufória. A szerotoninra gyakorolt hatása, és annak szerepe még nemteljesen tisztázott.Élettani hatásai kis- és közepes mennyiség (20-99mg) esetén: az étvágy csökken, a pulzus és vérnyomásemelkedik, a vérerek szűkülnek, a testhőmérséklet emelkedik, a pupillák kitágulnak az energia-szintnövekszik.Élettani hatásai nagy mennyiség (>100mg) esetén: minden hatás a kis- és közepes mennyiségekből;valamint sokkal intenzívebb élmény (dózisfüggő), esetlegesen bizarr, kiszámíthatatlan viselkedésparanoia, izomgörcsök, szédülés, HALÁL202
H 2 NNH 2dekarboxilezõdésCO<strong>OH</strong>ornitinH 2 NputreszcinNH 2deaminálásoxidációONH 24-aminobutanalCO<strong>OH</strong>Schiff bázisképzésNNNNNN-metilezés(metionin)NnikotinOCO<strong>OH</strong>acetecetsavNCOOCH 3NCO<strong>OH</strong>kokainOOON<strong>OH</strong>OOatropin203
Piridinvázas alkaloidokA piridin vázas alkaloidok közé számos vegyület sorolható. Ezek közül csak néhánnyal ismerkedünkmeg.OOpiperinONA piperin a feketebors fő alkaloidja, ami szerkezeti szempontból egy karbonsav amid. Piperin számosenzim inhibitora mint például a CYP3A4 and és a P-glikoprotein melyeknek fontos szerepe van axenobiotikumok metabolizmusában és transzportjában. Számos a gyógyszerek metabolizmusábanszerepet játszó enzimnek is inhibitora, így fontos hatása van a gyógyszerek biológiaihasznosíthatóságában.NHkoniinA bürök a petrezselyemhez hasonló, de annál nagyobb, fehérvirágú növény. Magassága 100–120 cm vagy még magasabb,gyakorlatilag a világon mindenütt előfordul mint mezeigyomnövény. Fő hatóanyaga a koniin, mely a növény mindenrészében benne van Hatására először az alsó végtagok bénulnakmeg, majd ez felfelé halad, végül teljes öntudat mellettlégzésbénulás miatt beáll a halál.A régi görög törvénykönyvekben a „bürökpohár” a kiszabhatóhalálbüntetés egyik nemeként szerepelt, Szókratészt ezzelvégezték ki.204
Kinolinvázas alkaloidokNN<strong>OH</strong>ONkininN<strong>OH</strong>ONkinidinNN<strong>OH</strong>Hsztrichnin<strong>OH</strong>N<strong>OH</strong>HbrucinA kinin lázcsillapító, fájdalom csillapító és gyulladás csökkentő hatású alkaloid. Ez volt az elsővegyület, amit a malária kezelésére alkalmaztak. A kinidin a kinin sztereoizomerje.A sztrichnin nagyon erős méreg, amit növényvédőszerként is alkalmaztak (rágcsálók ellen).A sztricnin mérgezés végzetes lehet az ember számára. A szervezetbe belélegzés, lenyelés útjánkerülhet be, azonban a szem és a száj nyálkahártyáján keresztül is felszívódhat. A márgezés soránnagyon látványos és fájdalmas tünetek - viszonylag lassú és kellemetlen halált a vázizomzat és alégzorendszer megbénításával idézi elő - jelentkeznek - ezért népszerű az irodalomban és afilmművészerben.A brucin jóllehet szerkezetileg hasonló a sztrichninhez, azonban kevésbé toxikus vegyület.Az ábrán szereplő bázisok mivel királis vegyületek, ezért rezolválószerként alkalmazhatóak királiskarbonsavak racém elegyeinek az elválasztására.OO<strong>OH</strong>A kinin élelmiszeripari felhasználása: számosüditőital, mint például a tonik ízesítője, de avermutban is adalékanyagként alkalmazzák.205
Fenetilamin vázas protoalkaloidokFenilalaninból és tirozinból az egyszerűbb felépítésű protoalkaloidok (pl. efedrin, meszkalin) mellettbonyolult szerkezetű izokinolingyűrűs alkaloidok is képződnek.Az efedrin egy ősi gyógynövényben, a csikófarkban (Ephedra vulgaris) fordul elő, és érszűkítő, valamintgörcsoldó hatása miatt orrcseppekben alkalmazzák.<strong>OH</strong>HNONH 2CH 3OOefedrinmeszkalinA meszkalin Mexikóban honos kaktuszfaj (Anhalonium lewinii) hallucinogén hatóanyaga. Igen intenzív éssokrétű pszichedelikus élményt nyújthat. Elfogyasztás után kb. 1 órával kezd hatni, és 6-12 óra hosszantart. Néha előfordul, hogy a teljes visszatérés ezután még 10-12 órát is várat magára. A kezdeti fázisbankellemetlen fizikai hatások tapasztalhatók: légzési nehézségek, izommerevség, émelygés, hányinger.A meszkalin tartalmú kaktuszok aktív hatóanyagai közül egyedül a meszkalinnak van pszichedelikushatása; de ez nem jelenti azt, hogy a többi hatóanyag ne módosítaná az élmény természetét.Legjellemzőbb mentális élmények: nyugalom, az élettel való egység érzése, felfokozott figyelem, gyorsanváltozó gondolati folyamatok, csukott szemmel látható képek, nyitott szemmel látható képi változások.206
A dopaminH<strong>OH</strong>ONH 2H<strong>OH</strong>ONH 2CO<strong>OH</strong>dopaminlevodopaA dopamin testben termelődő vegyület, mely az idegrendszerben neurotranszmitter szerepet tölt be,aktiválva a dopamin-receptorokat. Az agyban neurohormonként van jelen, s a hipotalamusz termeli.Szerepe hormonként, hogy gátolja a prolaktin felszabadulást.Gyógyszerként is használható, mely a szimpatikus idegrendszerre fejti ki hatását, emelve a pulzust és avérnyomást. A dopamin nem képes átjutni a vérereken, kábítószerként vagy gyógyszerként valóhasználata nem befolyásolja közvetlenül a központi idegrendszert. Ahhoz, hogy bizonyos betegségekben(pl Parkinson-kór) szenvedő betegeknek a dopamin-szintjét növeljük, annak szintetikus prekurzorát (L-Dopa, másnéven levodopa), amolyan elő-dopamint adnak be, mivel ez képes átjutni a vér-agy gáton.Agyi szerepe: több funkciója van az agyban, mégis messze a legfontosabb az agyi jutalmazó hatása.Akkor aktiválódik, ha valamilyen pozitív hatás éri az élőlényt.Mozgás: a dopamin a szerepet játszik a mozgás koordinációban. Szerepet játszik a Parkinson kórkialakulásábanÉszlelés: Az elülső lebenyben a dopamin kontrollálja az információáramlást. Ebben a régióban a dopaminrendellenességhanyatlást idézhet elő olyan funkciókban, mint emlékezés, figyelem, valamintproblémamegoldó-képesség.Szabályozás: a dopamin a legfontosabb neuroendikrín, mely szerepet játszik az agyalapi mirigy elülsőlebenyének prolaktin elválasztásában, melyeket az itt található laktotróp-sejtek termelnek, méghozzá -dopamin hiányában- folyamatosan.Motiváció és gyönyör: A dopamint többnyire az agy örömközpontjával hozzák kapcsolatba, ahol élvezetet,örömet stimulál, hogy motiválja a személyt bizonyos cselekedetek végrehajtására, hogy így még többdopaminhoz jusson.207
Amfetamin és származékaiNH 2HNONH 2<strong>OH</strong>NCH 3CH 3OCH 3OCH 3amfetaminmetamfetaminMDAMDMAAz amfetamin az alkaloidok közé tartozó, mesterségesen előállított szerves vegyület, melyet korábbanelterjedten használtak gyógyszerek alapanyagaként, újabban viszont inkább mint stimuláló (élénkítő)hatású kábítószer ismert.Az amfetamin elnevezés – bár eredetileg csak egy vegyületet neveztek el így – mégsem pontos,ugyanis manapság értjük alatta ezen vegyület származékait, illetve a farmakológiában a hasonlóbiológiai hatású (bár kémiailag esetleg eltérő jellegű) drogokat, gyógyszereket is. Azamfetaminszármazékok közé tartozik maga az amfetamin is, valamint a metamfetamin ("Speed"),metiléndioxi-amfetamin (MDA) és a metiléndioxi-metamfetamin (MDMA, "Ecstasy", "Adam" stb.) is.Az amfetamin típusú szerek hatásai: stimuláló (élénkítő); anorexigén (étvágycsökkentő hatás);entaktogén (társas kapcsolatokat könnyítő). Az amfetaminszármazékok felszabadítják azidegvégződésekben a szerotonin, a dopamin valamint a noradrenalin raktárakat, egyben gátolják ezutóbbi két hírvivő-molekula visszavételét. Nagy dózisban pedig még ezek enzimatikus lebontását ismegakadályozzák (MAO-gátlók). A végerdmény tehát a serkentő hatású ingerület-átvivő anyagoknak amegnövekedett mennyisége.NH 2HONH 2H<strong>OH</strong>O<strong>OH</strong>NH 2HO<strong>OH</strong>HNHOdopaminNHszerotoninHOnoradrenalinHOadrenalin208
Izokinolinvázas alkaloidokA mákfélék (Papaveraceae) családjába tartozó növényekből izolálható alkaloidok többsége izokinolingyűrűt tartalmazó származék, mely vegyületek bioszintézise a növényekben tirozinból indul ki. Abioszintézis kulcsintermedierje a dopamin és a p-hidroxifenil-acetaldehid Manninch-kondenzációjávalkeletkező (S)-norkoklaurin, amely több lépésben (R)-retikulinná alakul.HOCO<strong>OH</strong>HOdopaminNH 2H<strong>OH</strong><strong>OH</strong>NHHONH 2CH<strong>OH</strong><strong>OH</strong>O4-hidroxibenzaldehid(S)-norkoklaurin<strong>OH</strong><strong>OH</strong>NH<strong>OH</strong>ONH<strong>OH</strong><strong>OH</strong>NHOOO(S)-retikulinenamin(R)-retikulin209
<strong>OH</strong>OONON<strong>OH</strong>OON RHORR = H morfinR = CH 3 kodeinOtebainizotebainOOOONONHH<strong>OH</strong>O(R)-retikulin<strong>OH</strong><strong>OH</strong>HNOkelidoninOOpapaverinOOONNOONberberinOOOOOröadinOOOOOOnarkotinO210
211
212
A máknövény főalkaloidját, a morfinánvázas morfint 1930-ig kizárólag az éretlen máktok bemetszésekorkifolyó tejnedvből, az ún. ópiumból nyerték ki, de azt követően Kabay János magyar gyógyszerésznekköszönhetően, a kicsépelt száraz máktok és mákszalma lett a fontos gyógyszer előállításának alapanyaga.N<strong>OH</strong>O<strong>OH</strong>morfinKabay János1896. 12. 27. – 1936. 01. 29.A morfin káros mellékhatásai (hozzászokás, eufória stb.) ellenére a mai gyógyászatnak is nélkülözhetetlenfájdalomcsillapítója. A morfin tömény savas közegben történő hevítése vízvesztéssel járó morfinán →aporfin vázátrendeződéshez vezet. A képződő apomorfint korábban hánytatószerként alkalmazták, alegutóbbi időben az impotencia gyógyszereként került forgalomba.<strong>OH</strong>NON<strong>OH</strong><strong>OH</strong><strong>OH</strong>morfinapomorfin213
A kodein gyenge fájdalomcsillapító hatású köhögéscsillapító. A tebain jelentéktelen analgetikus hatásamiatt közvetlenül nem használható gyógyszerként, de számos félszintetikus készítményt lehet belőleelőállítani, pl. a kábítószerbetegek gyógykezelésére alkalmas naloxont és a buprenorfint.HONOONOON<strong>OH</strong>OOOOOnoloxantebainbuprenorfinVérehulló fecskefűO<strong>OH</strong><strong>OH</strong>NHkelidoninOOröadinA vérehulló fecskefüvet (Chelidonium majus) a népi gyógyászat a szemölcs eltávolítására használta.Alkaloidja a benzofenantridinvázas kelidonin citotoxikus hatású.A pipacs (Papaver rhoeas) forrázatát szemborogatásra használták, hatóanyaga a benzazepin gyűrűttartalmazó röadin fokozza a szem belső nyomását.214OONOOOO
A máknövény benzilizokinolin-vázas alkaloidjai közül a gyógyászatban a papaverin ésszármazékai, mint simaizomgörcsoldók kerülnek alkalmazásra.OONOON<strong>OH</strong>O<strong>OH</strong>NHOOO<strong>OH</strong>HNHONo-SpaberberinOemetinA berberin legnagyobb mennyiségben a sóskaborbolyában (Berberis vulgáris) fordul elő. Biológiaihatása igen széles körű, többek között antibakteriális és citotoxikus hatást is mutat.A galajfélék (Rubiaceae) családjába tartozó hánytatógyökér (Cephaelis ipecacuanha) vizeskivonatát régóta használják köptetőszerként és a vérhas gyógyítására. Hatóanyaga abenzokinolizidin gyűrűt tartalmazó emetinAz ópiumszármazékokat, mint fájdalomcsillapítókat az orvostudomány nem nélkülözhette és sokesetben ma sem nélkülözheti. Bár nagyon sok szintetikus morfiumszármazékot sikerült előállítani,s majd mindegyiket valamilyen célra fel is használja az orvostudomány (némelyiketfájdalomcsillapítóként, másokat a műtéti érzéstelenítés során), de olyat még ez ideig nem sikerülttalálni, amelyik ha a morfiumnál kisebb mértékben is, de ne okozzon megszokást.215
HeroinAz ópiátok családjába tartozik, tehát az ópium finomított és módosított változata. 1874-ben állítottákelő először. Az 1900-as években terjedt el a heroin mint kábítószer. Az 1920-as években hoztakkorlátozásokat, törvényeket használatának visszaszorítására. Napjainkban legnagyobb mennyiségbenAfganisztánban termesztik a heroin alapanyagául szolgáló mákot.NOOOONOOheroinmetadonA heroin a szervezetbe jutva rendkívül gyorsan hat. A kialakuló állapot ismerős, megszűnik a belsőfeszültség, s túláradó önbizalom, eufória foglalja el a helyét. Ebben tehát a másik két szerhezviszonyítva nincs különbség. Más azonban a hatás időtartama, míg az ópium vagy a morfiumhatása kb. tíz óráig is eltart, addig a heroiné csak három órán keresztül. Az igazán tragikuskülönbség azonban abban van, hogy a heroin után vágy (mind a testi, mind a lelki függőségkövetkezményeként) a leghatalmasabb valamennyi ópiumszármazék közül.A metadon (INN: methadone) egy szintetikus opoid, fájdalom- és köhögéscsillapító, 1937-benállította elő először Max Bockmühl és Gustav Ehrhart német kutató. Függőséget okoz, de elvonásitünetek csak 2-4 nap elteltével jelentkeznek, és rendszerint enyhék. Kereszt-tolerancia révéneredményesen csökkenti a heroin megvonásakor keletkező súlyos tüneteket, ezért alkalmazzákelvonókúrák során (Dole-Nyswander módszer). A pácienseket először metadonra állítják át, majdfokozatosan csökkentve az adagot teljesen megszüntetik a kábítószer adását.216
Indolvázas alkaloidokA ma ismert alkaloidok többsége indolvázat tartalmaz, és triptofánból képződik. A növények közülkülönösen a tárnicsvirágúak (Gentianales) rendjébe sorolható télizöldfélék (Apocynaceae), asztrichninfafélék (Loganiaceae) és a galajfélék (Rubiaceae) családjába tartozó növények termelnekmonoterpén-indol alkaloidokat.NHHNHNNHHHH 3 COOC<strong>OH</strong>NH 3 COOC<strong>OH</strong>NH 3 CH 2 COOCjohimbinvinkaminCavintonA kongói johimbefa (Coryanthe yohimbe) kérgét afrodiziákumként használták. Hatóanyaga a johimbin afehér kvebracsófa (Aspidosperma quebracho-blanco) kérgében is megtalálható.A télizöldfélék családjába tartozó kis télizöld (Vinca minor) fő alkaloidja a vinkamin.Vérnyomáscsökkentő hatású, a gyógyászatban egyik származéka az etil-apovinkaminát (Cavinton®)keringésjavító szerként kerül forgalomba, ami a hazai gyógyszeripar egyik legsikeresebb készítménye.217
ErgotalkaloidokAz anyarozs (Secale cornutum) a Claviceps purpurea nevű gomba által okozott fertőzés agabonaszemeken. Szokás a vegyületeket az anyarozs angol és francia neve az ergot utánergotalkaloidoknak is nevezni. Az anyarozsból több mint 30 alkaloidot izoláltak, ezek között többsztereoizomer pár is található. A vegyületek többsége vagy savamid- (pl. az ergometrin), vagypeptidszerkezetű (pl. az ergotamin). A vegyületek erélyes lúgos hidrolízisének közös lebontási terméke alizergsav, vagy annak C-8 epimere, az izolizergsav. Az anyarozsban található epimerpárok közül csak alizergsavszármazékok mutatnak élettani hatást. Így például, a méhizomzatra kifejtett összehúzó hatásukmiatt a szülések utáni vérzések csillapítására használják.A lizergsav dietilamidja az LSD szintetikus termék, ami erős hallucinogén hatású.ONNOOO<strong>OH</strong>NHergotaminNHN HHO<strong>OH</strong>NHlizergsavNHHO<strong>OH</strong>NHizolizergsavNH<strong>OH</strong>NHNHNO HLSDNHNHergometrinNH218
Xantinvázas alkaloidokHN<strong>OH</strong>NNONHNONN<strong>OH</strong>NNONONHNONNONNONNONHNxantinkoffeinteobrominteofillinparaxantinA koffein a kávé (1-1,5%), tea (2-5%) és kóladió (kb. 1,5%) alkaloidja. Kis mennyiségben a kakaóbab istartalmazza. A központi idegrendszert izgatja (különösen az agykérget), élénkíti a szívműködést, javítjaa szellemi funkciókat, csökkenti a fáradtságot és álmosságot. Az izmok teljesítőképességét fokozza. Azagyalapi vegetatív központok izgatása révén emeli a testhőmérsékletet, a mellékveséből adrenalintmobilizál, hatására a vese erek tágulása miatt fokozódik a vizelet kiválasztás. A nem kábítófájdalomcsillapítók hatását erősíti (elsősorban fejfájás esetén hatásos).A teobromin a kakaó és a csokoládé főalkaloidja. A csokoládé 0,5-2,7% teobromint tartalmaz. Kismennyiségben jelen van a kóladióban (1.0-2.5%), a teanövényben is. Az emberi májban a koffein 10%-ban teobrominná, 4%-ban teofillinné, és 80%-ban paraxantinná metabolizálódikA teofillint légúti betegségek úgymint krónikus obstruktív tüdőbetegség és asztma kezelésérehasználnak. A teában is megtalálható csekély mennyiségben (~1mg/l), ami sokkal kisebb a terápiásadagnál.Hatásai: a hörgők simaizmainak ellazítása; pozitív inotróp hatás (a szívizom kontraktilitásának éshatékonyságának növelése); pozitív kronotróp hatás (a szívfrekvencia növelése); vérnyomás emelés;a vese véráramlásának fokozása; gyulladáscsökkentő hatás219
Mi az alkaloidok szerepe a növényekben?220
Fizikai és kémiai „hadviselés”• emészthetetlen sejtfal: cellulóz, lignin ,kallóz (b-1,3 kötésekkel összekapcsolódó glükóz polimer)• hidrofób réteg, ami megakadályozza a kórokozók behatolását, és a növények kiszáradását.• vastag kéreg a gyökereken, és a szárakon? Vízvesztés megakadályozása, mikrobák és növényevőktávoltartása• tüskék, tövisek, „szőrök” (kémiai anyagokkal töltve) a növényevők ellen• gyanták, mézszerű ragacsok• nagyfokú regenerációs képesség• Proteinek, enzimek:• Kitináz (gombák ellen)• b-1,3-glükanázok (baktériumok ellen)• peroxidázok, fenoláziok, proteáz inhibitorok;• toxalbuminok: toxikus proteinekLeucoagglutininVicia faba (lóbab)Ricinus communisricin221
• Több mint 100000 másodlagos anyagcsereterméket (secondary metabolits) izoláltak eddig anövényekből.• Ezeknek a vegyületeknek egy prominens csoportját alkotják az alkaloidok, melyek számameghaladja a 21000!• Ez csak a természetes forrásból izolált vegyületeket jelenti, nincsenek benne az előállítottszármazékok.• Egyéb N tartalmú vegyületek is ismertek: ~ 700 nem fehérjealkotó aminosav; ~ 100 amin; ~ 60cianogén glikozid; ~100 glükózinolát; ~ 150 alkilamidRO HglükózCNRCHO + glükóz + HCNGolgotavirág (passiflora kermesina)HO HO<strong>OH</strong>O<strong>OH</strong>SROO SN OOglükózinolát222
Magas fehérjetartalma miatt jó álattakatmány! DE!Quinolizidin alkaloidokat tartalmaz (2 – 6%) – neorotoxikusÉdes farkasbab alkaloid tartalma kisebb mint 0.02%!! DE!Farkasbab(lupin)Általában az alkaloidok multifunkcionálisak biológiai hatás szempontjából.Nem csak növényekben képződnek, baktériumok, gombák, tengeri szivacsok, emlősök istermelhetek.223
224
225
Tumor ellenes alkaloidok a klinikai használatban, vagy kipróbálás alatt.• 6 000000 új megbetegedés / év• sejtek kontrollálatlan burjánzása• USA-ban a vezető halálok• vinka alkaloidok és camptothecin és taxol származékok jelentős tumor ellenesaktivitással rendelkeznek.226
• A vinkaalkaloidok biokémiai hatása sokrétű:• mikrotubulusok rombolása• protein és nukleinsav szintézis gátlása• befolyásolja a lipid metabolizmust és a membránok lipid tartalmátMintegy 150 terpenoid és alkaloid származékotizoláltak belőle.Catharanthus roseusVinca / rózsameténg227
Camptothecin és analogjaiCamptotheca acuminataHappy tree; Cancer tree;Tree of LifeFőzete daganatellenes hatással rendelkezik. Belőle izolálták a Camptothecin-tAz 1960-as években írták le a vegyület daganatellenes hatását in vitro körülmények között, azonbanegészen a 80-as évek közepéig lényeges előrelépés nem történt. Ekkor fedezték fel, hogy a vegyület atopoizomeráz enzim inhibitora228
Multidrog rezisztenciaA cinkona alkaloidok (kinin, cinkonin) mint malária ellenes vegyületek váltak ismerté, azonban felfedeztékazt is, hogy a daganatos megbetegedésben szenvedő betegek esetében sikeresen vissza lehet velükfordítani a fellépő multidrog rezisztenciát (MDR). Pgp inhibitorok (P-glikoproteinek – bélrendszerbentalálhatóak; biológiailag aktív vegyületek eliminációjáért felelős fehérjék é transzportfehérjék)HONHONONkinincinkoninKlinikai I./II. fázis vizsgálatai azt mutatták, hogy a kinint együtt alkalmazva különbözőkemoterapetikumokkal (mitoxantrone, vincristine, adriamycin, vagy paclitaxel) kedvező hatás érhetőel rezisztens akut leukémia, tüdő daganat, és non-Hodgkin limfóma esetében.Későbbi klinikai vizsgálatok azt is kimutatták, hogy a cinkonin hatékonyabb a kininnél a mintmultidrog rezisztenciát csökkentő szer. Klinika I. fázisban sikeresen alkalmazták doxorubicin,vinblastine, cyclophosphamide, és methilprednisolonnal kombinálva.A fejlesztések ezután olyan származék előállítására fókuszálódott, amely szelektív Pgp inhibitorhatással rendelkezik. Így jutottak el az MS-209 vegyülethez, amely szelektív Pgp inhibitor, és nincsdaganatellenes hatása. Továbbá toxicitása is kicsi 2000mg/kg.NONNHOONXHOOCCO<strong>OH</strong>MS-209229
Alkaloidok a daganatos megbetegedések megelőzésébencelecoxib (28)tamoxifen (29)cyclooxygenase-2 inhibitoraromatase inhibitorsanastrozole (30), letrozole (31), exemestane (32)capsaicin (33)brassinin (34)sulforaphane (35), monofunctionalphase 2 enzim aktivátor.suforamate (36) – 1/3 toxicitásIndole-3-carbinol (37): brokkoli,karfiol230
Neurotoxikus alkaloidok a cianobaktériumbólA cianobaktériumok (Cyanobacteria) egy baktériumtörzs, amelyet korábban kékmoszatok (Cyanophyta)néven a növények soroltak az ide tartozó fajok megjelenése és életmódja alapján. Fotoszintetizálnak éssok faj képez fonál, lemez vagy tömlő alakú telepet. Sejtjeik klorofillt, valamint kék vagy piros színanyagottartalmaznak. Vízben vagy nedves helyeken élnek, egyesek növények szövetüregeiben. Vannak fajok,amelyek zuzmók felépítésében vesznek részt. Mintegy 2000 faj tartozik ide.A cianobaktériumoknak mintegy 40 nemzetsége ismert, amelyek az édes és tengervízben élvetoxinokat termelnek. Ezeket a toxinokat a gerincesekben kifejtett hatásuk alapján lehetcsoportosítani:• hepatotoxins (pl: microcystin, nodularin)• általános toxinok (pl: cylindrospermopsin)• neurotoxinok (pl: anatoxins, saxitoxins)• irritánsok és dermatoxinok (pl: lipopolyszaharidok és lyngbyatoxin)microcystins, nodularins, anatoxins, saxitoxins, és cylindrospermopsin potenciális veszélyforrásaz emberekre. Az ivó és fürdővizek monitorozása nagyon fontos.231
232
233
VitaminokA vitaminok az emberi szervezet számára nélkülözhetetlen, kis molekulájú, különféle kémiaiösszetételű biológiailag aktív szerves vegyületek.Az emberi szervezetbe a vitaminokat a táplálékkal kell bevinni. A vitaminok közül egyesek akémiailag hozzájuk hasonló szerkezetű anyagból, az elővitaminokból (provitaminok) képződnek.Antivitaminok (vitamin-antagonista):a vitaminokhoz hasonló szerkezetű antimetabolitok, amelyek akoenzimként működő vitaminnak a helyét elfoglalják, ennek következtében az enzim biológiailaghatástalanná válik. Vitaminhiányt, ill. vitaminelégtelenséget okoznak (pl: K-vitamin – szalicilsav).Vitaminhiányos táplálkozás esetén kóros tünetek jelentkezhetnek: enyhébb esetben avitaminszegénység (hipovitaminózis); súlyosabb esetben vitaminhiány (avitaminózis) léphet fel.Ugyanakkor túlzott bevitelük is káros lehet, ilyenkor hipervitaminózisról beszélünk (ez pl.vitamintabletták mértéktelen szedése esetén alakulhat ki), s ez szintén súlyos betegségtünetekkeljárhat.A vegyes táplálkozás általában fedezi a vitaminszükségletet, de az étrend összeállításánálnem csak arra kell törekedni, hogy a táplálék nyersanyaga vitaminban gazdag legyen, hanemfigyelemmel kell lenni arra is, hogy az ételek elkészítése során – főleg a hevítés hatására – a vitaminok10-50%-a is elbomolhat, elveszhet. Az egészséges szervezet működéséhez nemcsak vitaminokra,hanem ásványi anyagokra, kofaktorokra és nyomelemekre is szükség van.234
Vitaminok csoportosításaA vitaminokat oldhatóságuk alapján két nagy csoportra oszthatjuk:•Zsírban oldódó vitaminok (lipovitaminok),•Vízben oldódó vitaminok.A két csoport tagjai között aligha van szerkezeti rokonság, de a vízben oldódó vitaminok között semtalálunk ilyet. A vitaminok élettani hatására leginkább hiányuk (az avitaminózis) esetén fellépőbetegségekből következethetünk.A vitaminról alkotott fogalmunk, az utóbbi évtizedek kutatásainak eredményeivel, tovább módosul,Kiderült egyes vitamin jellegű anyagokról, bár ennek ellenkezőjét gondolhatnánk, hogy más állatfajokszámára egyáltalán nem nélkülözhetetlenek. Az emberben a B12-, és K-vitamin vitaminhiányos állapotáthiányos étrenddel nem lehet létrehozni, mert a normális bélbaktérium-flóra ezeket képes előállítani. Haazonban a szervezetben felszívódási zavarok lépnek fel, ha fertőzések következtében, antibiotikumokadagolása, vagy egyes gyógyszerek kölcsönhatásainak következtében elpusztul a bélflóra – kialakulhata hiánybetegség.Néhány hiánybetegség: skorbut (C-vitamin hiánya); angolkór (D-vitamin hiánya); farkasvakság (Avitaminhiánya).Léteznek dokumentációk arra, hogy egyes vitaminok nagy mennyiségű szedésének mellékhatásaivannak. Minél magasabb a túladagolás mértéke, annál erősebbek a mellékhatások.Kizárólag természetes élelmiszerfogyasztással általában nem érhető el a túladagolás.A vitaminok túladagolása csak ritkán okoz maradandó megbetegedést. Gyakran a vitaminkészítményekadalékanyagai okozzák a mellékhatásokat – néhány esetben maradandót is.Amerikában 2004-ben 62 562 esetet regisztráltak; a 80%-a 6 éven aluli gyermekeknél történt, 53 súlyosmegbetegedés volt, de 3 halálozás is bekövetkezett. (ismeretlen mérgezéssel csupán 19 250 főtkezeltek)Mindez vezetett oda, hogy megállapították a „tolerable upper intake level”-t (UL), azt az adagot, amelyeta lakosság még a mellékhatások jelentkezése nélkül elfogyaszthat egy nap.235
236
Ez a felsorolás nem tükrözi híven a vitaminok sajátságait, és megtévesztő is lehet. Csak a természetesvegyületekre igaz, a származékaira nem.Pl: vitamin készítményekben a C-vitamin mint aszkorbinsav-palmitát van jelen, ez pedig zsírbanoldódik, a K-vitamin hatású menadion-biszulfit vízben oldódikOOmenadion237
238
239
240
Az A-vitaminA karotinoid származék, táplálékkal bevitt retinol gyakorlatilag teljesen felszívódik. Aprovitaminok vitaminná történő átalakítása során a b-karotin kb. 1/6-a, az egyéb karotinoknak csupánaz 1/10-e alakul át retinollá. Mivel a karotinok fontos szerepet töltenek be a szükséglet kielégítésében,bevezették a retinol-ekvivalens fogalmát. A retinol-ekvivalens a hasonló kémiai szerkezetű, azonosbiológiai hatású vegyületek közös neve.A legfontosabb A-vitamin hatású vegyületek: a retinol, retinal, és provitaminok: alfa-, bétaésgamma-karotin, egyéb karotinoidok. Biológiailag a legaktívabb a béta-karotin.Az A-vitamin szükségletet a vegyes táplálkozás fedezi. A szükséglet növekedésével kellszámolni a zsíremésztés, felszívódás zavarai, vagy számos idegen anyag, gyógyszer fogyasztásaesetén.A túlzott A–vitamin bevitel súlyos toxikus tüneteket okoz. Az A-vitamin hiánya a koraiszakaszában az ún. farkasvakságot okozza, amikor szürkületben, vagy gyenge világítás eseténlátászavar következik be. Az A-vitamin nélkülözhetetlen a szemideghártya (retina) fényérzékenyanyagának, a látóbíbornak a felépítésében.Jellemző még az A-vitamin hiányra a hámszövet-, könnymirigy-elsorvadása, a verejték- ésfaggyúmirigyek megbetegedése, a bőr kiszáradása, a szőrzet és a hajszálak törékenysége, kihullása.Gyermekeknél a csontosodási folyamat sérülése következtében növekedési zavar is bekövetkezhet.A felnőtt ember napi szükséglete kb. 1,5 mg (más források szerint csupán 900 µg),terhesség és a szoptatás ideje alatt 2,0-2,5 mg.Túladagolás esetén hipervitaminózis: sárgás bőrszín, hajhullás, bőrgyulladás stb. léphet fel.<strong>OH</strong>241
242
A-vitamin természetes forrásaiAz A-vitamin jellemző mennyisége 100 gélelmiszerben:• gabonafélék, hüvelyesek és őrleményeik,kenyerek, péksütemények: nyomokban• száraztésztákban: 0-0,04 μg• sajtos, túrós sütemények: 5-50 μg• zöldség, gyümölcs: 0-0,01 μg• vaj, margarinféleségek: 250-650 μg• húsok, húsipari termékek: 0,3-70 μg• májak, májkészítmények: 1500-1600 μg• szív, vese és készítmények: 5-500 μg• halak: 10-60 μg• tej: 30-100 μg• tojás: 350-600 μgAz A-provitamin (karotin formában) jellemzőmennyisége 100 g élelmiszerben:• gabonafélék, hüvelyesek és örleményeik,kenyerek, péksütemények: 0-1,5 mg• száraztésztákban: 0-0,04 mg• sajtos, túrós sütemények: 0 mg• zöldség, gyümölcs: 0,1-12 mg (felső érték asárgarépa)• vaj, margarinféleségek: 0,2-0,5 mg• húsok, húsipari termékek: nem jellemző• halak: 0,5-2 mg• tej: 0,005-0,1 mg• tojás: 0,5-1,2 mg243
A D-vitamin (kalciferol)A kalciferol gyűjtőnév. Több azonos biológiai hatású, de kémiailag egymástól különböző anyagot jelölnekvele. Először a csukamájolajról állapították meg, hogy gyógyítja az angolkórt, majd a napfénnyelbesugárzott táplálékról is megállapították ugyanezt. Az utóbbiból kristály formájában előállított anyagotD 1 -vitaminnak nevezték el, mely kalciferolt és lumiszterint tartalmaz. Az erősebb hatású kalciferol a D 2 -vitamin nevet kapta. A további kutatások még egy anyagot fedeztek fel, a 7-dehidrokoleszterint, amely abőrben ultraibolya sugárzás hatására, D 3 -vitaminná alakul. Az állati eredetű élelmiszerek D 3 - és D 2 -vitamint, a növényi eredetűek D 2 -vitamint tartalmaznak.H<strong>OH</strong>O<strong>OH</strong>calciferolHH HlumiszterinA D-vitamin-hatású vegyületekszteroidszármazékok. Táplálkozásélettaniszempontból a D 2 -HO(ergokalciferol) és a D 3 - (kolekalciferol)vitamin jelentős. Biológiai hatásukattekintve aktívabb a D 3 -vitamin, amely abőrben az ultraibolya sugárzáshatására keletkezik, előanyagából a 7-dehidrokoleszterinből.A D-vitamin elősegíti a kalcium és HOfoszfor felszívódását a bélcsatornából,és közvetlenül befolyásolja acsontképződést.D 2 -vitaminD 3 -vitamin244
245
A D-vitamin elősegíti a kalcium és foszfor felszívódását a bélcsatornából, és közvetlenül befolyásoljaa csontképződést. A szervezetbe kerülő egyes idegen anyagok (ólom, kadmium), valamint egyesgyógyszerek növelik a vitaminszükségletet. A legbőségesebb kalciferol-források a halmájolajok, máj,tojás, tej és tejtermékek, de egyes élelmiszereket (pl. gyermektápszereket, tejtermékeket,margarinokat) is D-vitaminnal dúsítanak.Hiánya gyermekekben angolkórt, felnőttekben csontlágyulást okozhat, de az általános tüneteken túl avesekőképződés veszélye is fennáll.Hipervitaminózisa azt eredményezi, hogy megemelkedik a vér kalcium-szintje, túl sok épül be acsontokba, az érfalakba; növeli az érelmeszesedés kockázatát, növekedési zavarokat okozhat.Az D-vitamin (kalciferol formában) jellemző mennyisége 100 g élelmiszerben:• gabonafélék, hüvelyesek és őrleményeik, kenyerek, péksütemények: nem jellemző• száraztésztákban: 0-0,4 μg• zöldség, gyümölcs: nem jellemző• vaj, margarinféleségek: 0,5-7,5 μg• húsok, húsipari termékek: 1-4 μg• halak: 0,5-10 μg• tej: 0,05-0,3 μg• tojás: 5-25 μgGyermek0 - fél év: 7,5 µgfél - 1 év: 10 µg1 - 3 év: 10 µg4 - 6 év: 10 µg7 - 10 év: 10 µgNő11 - 14 év: 10 µg15 - 18 év: 10 µgfelnőtt: 10 µgterhesség: 10 µgszoptatás: 10 µgFérfi11 - 14 év: 10 µg15 - 18 év: 10 µgfelnőtt: 10 µg246
E-vitaminTokoferolok: számos E-vitamin hatású vegyület ismert, így az a-, b-, g-, és -tokoferol, valamint aszintetikus úton előállított észter-származékok, pl. tokeferol-acetát.Legjobb E-vitamin forrásaink a növényi olajok, tehát a napraforgó-, búzacsíra-, tökmag-, olíva-,kukoricaolaj, a búzacsíra és az egyéb gabonacsírák, a zöld növények, a hús, a máj és a tojás.Az emberben a tokoferol hatása kevéssé ismert, hiánya nem okoz jellemző tüneteket. A tokoferolokkönnyen oxidálódnak, miközben antioxidáns hatást fejtenek ki, így megakadályozzák a többszörösentelítetlen zsírsavak oxidációját. Biológiailag a D-a-tokoferol a leghatásosabb. Gyulladásgátló hatása isismert.A vegyes táplálék E-vitamin tartalma nagymértékben függ az elfogyasztott zsír mennyiségétől ésminőségétől (állati zsír, vagy növényi olaj). A többszörösen telítetlen zsírsavakban gazdag étrend mellettnagyobb az E-vitamin szükséglet. 1g többszörösen telítetlen zsírsav, 0,5-0,8 mg-al növeli a tokoferolszükségletet.Embernél nem fordulnak elő hiánytünetek, mert a normális vegyes étrend tartalmazza, illetve azegészséges szervezet ezekből képes előállítani a neki szükséges mennyiséget.Hiánya vérszegénységet, meddőséget, izomsorvadást okoz. Túladagolása nem ismertE-vitaminban gazdagok a növényi olajok, zöldnövények, gabonamagvak, de főleg a csíráztatottmagvakból nyert olajok.HOR 3HOR 3R 2OR 2OR 1R 1a-tokoferol: R 1 = R 2 = R 3 = CH 3b-tokoferol: R 1 = R 3 = H; R 2 = CH 3g-tocoferol: R 1 = R 2 = H; R 3 = CH 3-tocoferol: R 1 = R 2 = R 3 = Ha-tokotrienol: R 1 = R 2 = R 3 = CH 3b-tokotrienol: R 1 = R 3 = H; R 2 = CH 3g-tocotrienol: R 1 = R 2 = H; R 3 = CH 3-tocotrienol: R 1 = R 2 = R 3 = H247
Hiánya vérszegénységet, meddőséget, izomsorvadást okoz. Túladagolása nem ismert.E-vitaminban gazdagok a növényi olajok, zöldnövények, gabona magvak, de főleg a csíráztatottmagvakból nyert olajok.Az E-vitamin (tokoferol formában) jellemző mennyisége 100 g élelmiszerben:• gabonafélék, hüvelyesek és őrleményeik, kenyerek, péksütemények: 0,1-12 mg• száraztésztákban: 0-0,6 mg• sajtos, túrós sütemények: 0,05-1 mg• diós, mákos sütemények: 0,3-3 mg• zöldség, gyümölcs: 0-3 mg• vaj, margarinféleségek, szalonna, növényi olaj: 0,5-84 mg• húsok, húsipari termékek: 0,5-2,5 mg• halak: 0,2-3,5 mg• tej: 0,1-1,6 mg• túrók, sajtok: 0-1 mgtojás: 0,5-1,5 mg248
H- és a K-vitaminA H-vitamin a (biotin – B 7 -vitamin) A hámszövet védelmi vitaminja,baktériumok, élesztőgombák fontos koenzimje. Az anyagcserében játszikfontos szerepet. Hiánya étvágytalanságot, bőrelváltozásokat okozhat,gyulladások lépnek fel, esetenként gerincvelői bántalmakat okoz. Azélesztőkivonat az embernél gátolja az őszülés kialakulását.Legjobb biotinforrásaink a máj, a vese, a tojássárgája, az élesztő, a karfiol,a dió- és mogyorófélék, a gabonafélék. A gyümölcsök és a húsfélék igenkeveset tartalmaznak.HNHONHHSCO<strong>OH</strong>H-vitamin (biotin)A K-vitamin a természetben két formában fordul elő: K 1 -vitamin(fillokinon), amit a zöld növények, valamint a K 2 -vitamin (menakinon),melyet baktériumok szintetizálnak. A természetes K-vitaminok csakzsírban, a mesterségesen előállított származékok vízben is oldódhatnak.Az ember K-vitamin szükségletét a táplálék K 1 -vitaminja és abélbaktériumok által előállított K 2 -vitamin kb. fele-fele arányban fedezi.Normális bélflóra és vegyes táplálkozás esetén a szervezet K-vitaminellátottsága megfelelő. A K-vitamin 10-70%-a szívódik fel.Felnőttekben a hosszantartó antibiotikus kezelés és a csökkent K-vitaminbevitel hiánytüneteket okozhat. Gyermekeknél és koraszülöttekben abélbaktériumok csekély száma miatt előfordulhat K-vitamin hiányonalapuló vérzékenység.K-vitaminforrások: brokkoli, fejes saláta, káposzta, paraj, tejtermékek, ésmáj.OOOOfilokinonmenokion3n249
B 1 -vitamin (tiamin)NNH 2NtiaminNS<strong>OH</strong>Vízben jól oldódó, hőre érzékeny vegyület. Jelentős szerepe van a szénhidrátanyagcserében,miután a piroszőlősav dekarboxilezését végző enzim koenzimje,energiát generál, segíti a szénhidrátok elégetését, valamint létfontosságúszerepet tölt be az idegrendszer, az izmok és a szív normális működésében.A tiamin szükséglet a szénhidrátbevitellel függ össze, a gyakorlatban az energia bevitellelszámolnak. Felnőttek számára 0,125/1000 kJ tiamin bevitele ajánlott, ami legalább 1 mg tiamintjelent naponta. Az idős emberekben a rosszabb tiamin felhasználás miatt 1 mg/nap bevitel javasoltmég akkor is, ha energia bevitelük kisebb, mint 8 MJ/nap.A hiánybetegség a tejsav és a piroszőlősav felhalmozódását okozza a szervezetben, neuraszténiástünetekkel, étvágytalansággal jár, szívgyengeség és keringési elégtelenség léphet fel. Ennekeredménye a fáradtság, a gyengeség, a depresszió, valamint egyes bélrendszeri problémák.A B 1 -vitamin hiánya okozza – főleg a keleti országokban – a beriberi nevű betegséget.Tiaminban gazdag a máj, a teljes kiőrlésű liszt, a barnakenyér, a hüvelyesek az élesztő.• gabonafélék, hüvelyesek és őrleményeik, kenyerek, péksütemények, száraztészták: 30-800 μg• zöldség, gyümölcs: 15-300 μg• dió, olajos magvak: 100-2020 μg (felső érték a napraforgó)• vaj, margarinféleségek, olaj, szalonna: 0-30 μg• húsok, húsipari termékek, máj, szív, vese: 80-800 μg• halak: 20-100 μg• tej: 50-180 μg• tojás: 50-150 μg250
251
ONNHN N O<strong>OH</strong>HO<strong>OH</strong><strong>OH</strong>riboflavinB 2 - és B 3 -vitaminA riboflavin (B 2 vitamin) koenzimek része (FAD – FADH), a piroszőlősav, zsírsavakés az aminosavak oxidatív lebontását végzik, fontos szerepet töltenek be aszöveti légzésben és méregtelenítésben. Az ember bélflórája is termel riboflavint,ezért hiánytünetek ritkán fordulnak elő. Hosszantartó, széles spektrumúantibiotikum-kezelés azonban elpusztítja a bélflórát, így riboflavin-hiányt idézhetelő. Hiánya az embernél bőrelváltozásokat, szemlencse-elváltozásokat,szemviszketést, szemégést, szemvörösödést, emésztési zavarokat és kirepedtajkakat okoz. Közrejátszhat az ízületi gyulladás kialakulásában is. Életkortólfüggetlenül 0,15 mg/1000 kJ riboflavin bevitel ajánlott, idős korban nem lehetkevesebb, mint 1,2 mg/nap. Főbb riboflavin források: tej és tejtermékek, máj,vese, tojás, hüvelyesek.ONH 2NnikotinamidO<strong>OH</strong>Nnikotinsav (niacin)Nikotinsav (B 3 -vitamin), a szöveti oxidredukciós folyamatokban résztvevő koenzimekalkotórésze (NAD – NADH). Az elfogyasztott táplálék minden 1 MJ energiájára 1,6 mgniacinekvivalens-bevitel ajánlott. A szükségletek megállapításánál figyelembe kell venni atriptofánból történő képzést: 60 mg triptofánból 1 mg nikotinamid képződik, az átalakuláspiridoxint, tiamint, riboflavint igényel. A legtöbb esetben a vitaminkészítményekben aniacin helyett niacin-amidot találunk, mely egyes vélemények szerint a szervezetszámára nem kellően helyettesíti a vitamint. A niacin-amidot azért fejlesztették ki, hogykiküszöböljék az allergén reakciónak hitt bőrvörösödést, amit a niacin okoz, de aniacinamid nem.Hiányában bélrendszeri zavarok, fáradékonyság, depresszió, étvágytalanság, fejfájásalakulhat ki. A pellagra (pelle agra = durva bőr) a (B 3 -vitamin) hiánya okozta betegség.Niacinban gazdag a hús, máj, vese, zöldségfélék és a barnakenyér. Triptofán-forrás: ahús, a növényi fehérjék, kivéve a kukoricát.252
H<strong>OH</strong>ONpiridoxin<strong>OH</strong>B 6 - és B 7 -vitaminA piridoxin (B 6 -vitamin) koenzimek alkotórésze melyek résztvesznek az aminosav anyagcserében,bevitelük a fehérje-bevitellel arányos kell, hogy legyen, miután a legfőbb feladata az aminosavakátalakítása: 1 g fehérje mellé 0,015-0,02 mg B 2 -vitamint rendelnek. A piridoxinnál felszívódási veszteséggelnem kell számolni.Hiánya ún. pellegrás nyelv- és bőrtüneteket, a perifériás idegek gyulladását, vérszegénységgel ésidegrendszeri zavarokkal járó epilepsziás görcsöket okozhat, de az úgynevezett „fekete nyelv”kialakulásában is szerepet játszik. További hiánytünetek lehetnek: az ajkak nyálkahártyájánakberepedezése, fokozott faggyúmirigy-működés, idegesség, álmatlanság, izomgyengeség, hajhullás,végtaggörcs. B 6 -vitamin adását javasolják migrénes fejfájás esetén, a terhesség alatt, de a röntgenbesugárzásés a narkózis után bekövetkező hányások csillapítására is.Bőséges forrás a máj, hús, tejtermékek, hüvelyesek és az élesztő, kisebb mértékben a tej és a tojás.A biotin (H-, B7 vitamin) számos karboxiláló enzim koenzimje, melyeknek reguláló szerepük van aszénhidrát- és lipid anyagcserében. A biotinszükséglet és a javasolt bevitel megállapítását nehezíti, hogyaz ember bélflórája is termeli. Felszívódási vesztesége 50% körül van. A biotin szabad és kötött formábanis jelen lehet az élelmiszerekben. Jó biotinforrás a máj, a vese, a tojássárgája, és néhány zöldség. A búzais tartalmaz biotint, de kötött formában, ami felszívódásra nem alkalmas. A hús, a gyümölcsök biotinbanszegények.Hiányakor túlzott kimerültség, álmosság, izomfájdalmak, hajhullás, depresszió, és szürkés bőrszínjelentkezhet.HNHOSNHHB 7 -vitamin (biotin)CO<strong>OH</strong>253
B12-vitaminNH 2ONH 2ONH 2N NCCoNNH 2ONNONH 2H 2 NOONHOO OPO ONNO<strong>OH</strong>Kobalaminok, a gyomor és a vékonybél nyálkahártyájaáltal kiválasztott glikoproteinhez kapcsolódvaszívódnak fel. Az esetek többségében vitaminhiányakkor lép fel, ha nem képződik a kobalaminokat szállítófaktor, így a táplálékban jelen lévő vitamin nem tudbejutni a szervezetbe. A kobalaminok koenzimformájában kapcsolódnak be a fehérjék, a szénhidrátokés más nitrogéntartalmú anyagok anyagcseréjébe. Akobalaminnak nevezett anyag 4,5%-ban tartalmazkobaltot, innen származik a neve.B 12 -vitamint a növények nem tartalmaznak, aszükségletet csak állati eredetű élelmiszerekkel lehetfedezni. Normális körülmények között a tápláléknaknem kell kobalamint tartalmaznia, mert a bélbennaponta 20-szor annyi keletkezik, mint amennyi atáplálékkal kerül a szervezetbe.Innen rendkívül nehezen szívódik fel, a felszívódása csak belső faktor jelenlétében megy végbe, és abélben képződő mennyiség tizede szívódik csak fel, a többi kiürül a szervezetből. Az ember éviszükséglete kb. 1 mg-ra tehető. Vészes vérszegénységben szenvedő betegnek havonta kb. 100 mg-otkell kapnia.A B 12 -vitamin részt vesz a nukleinsavak felépítésében, befolyásolja a szervezet fehérjeszintézisét,elősegíti az aminosavak fehérjékbe való beépülését és fokozza ezek hasznosítását, de az egészszervezetet érintő hatása van. Az orvosi gyakorlatban a vészes vérszegénység, általános testi leromlás,kimerültség, ideggyulladás, hosszabb betegség utáni lábadozás esetén használják. Az egész szervezetrekiterjedő erősítő, roboráló hatása van.254
<strong>OH</strong><strong>OH</strong>ONHCO<strong>OH</strong>pentoténsav (B 5 -vitamin)B 5 -, B 9 -, B 13 -vitaminA pentoténsav a koenzim A alkotórésze. Szerepe van az energiahordozószénhidrátok lebontásában, zsírsavak szintézisében és lebontásában, akülönböző szterolok, szteroid-hormonok, porfirinek szintézisében. Emberbenvalódi hiánytünetek vegyes táplálkozás mellett nem lépnek fel, bár apantoténsav-szükséglet nem tisztázott kellőképpen. A fizikai erőkifejtés és astresszhelyzetek növelik a szükségletet.2NN<strong>OH</strong>NNNNHONHfolsav (B 9 -vitamin)CO<strong>OH</strong>CO<strong>OH</strong>B 9 -vitamin (M-vitamin) a folsav vízben oldódó vitamin. Nagyonfontos szerepe van a szervezetben, különösen a várandósédesanyáknál, mert a terhesség korai szakaszában a fejlődőembrió gerincét, a velőcsövet lezáró folyamat csak folsavjelenlétében megy végbe hibátlanul. Ezért várandósédesanyáknak mindenképpen ajánlott a folsav pótlása.Szerepe van még a fehérvérsejtek, vörösvértestek, vérlemezkék képzésében, az aminosavak, ésnukleinsavak anyagcseréjében, de hozzájárul a gyomor-bélrendszer, és a szájnyálkahártya épségéhez is.A mesterséges készítményekből felszívódása jobb, mint a természetes forrásokból. A szervezet jó folsavellátottsága mellett elfedheti a B12-vitamin hiányában kialakuló tüneteket. Ez különösen vegetáriánustáplálkozás esetén lehet veszélyes. Legjobb folsavforrásaink a máj, a leveles zöldségek (különösen aparaj), a gyümölcsök, és az élesztő. A túl nagy folsavbevitel csökkentheti a cink hasznosulását.HNOO N CO<strong>OH</strong>Horotsav (B 13 -vitamin)Az orotsav antzioxidáns hatása révén megvéd bizonyos májműködési zavaroktól és akorai öregedéstől, elősegíti a szklerózis multiplex kezelését. A felnőttek ajánlottadagja 0,003 mg. Hiánytünet egyelőre nem ismert. Megtalálható agyökérzöldségekben és a tejsavóban. Magnézium-orotát formájában adva oldja aszorongást és feszült állapotokat, enyhíti a pszichovegetatív kimerültséget, gátolja akoncentráló- és emlékezőképesség csökkenését.255
Szent-Györgyi Albert1893-1986Nobel-díj - 1937HO<strong>OH</strong>HOO<strong>OH</strong>aszkorbinsavOA C-vitaminA C-vitamin -aszkorbinsav- a hexonsav laktonja. Vízben jól oldódó, erősenredukáló vegyület. Teljesen eloxidált formájában elveszti vitaminhatását. Azaszkorbinsav a sejtek biokémiai folyamataiban mint hidrogéndonor veszrészt, ez adja meg elsőrendű biológiai jelentőségét. 85%-a szívódik fel.Elősegíti a vas felszívódását a bélrendszerből. Az aszkorbinsavat számosállatfaj szintetizálja, ugyanakkor az ember és néhány állatfaj nem képes erre.A környezeti stressz hatások, a dohányzás, egyes gyógyszerek, (pl. orálisfogamzásgátlók), lázas állapot, műtéti beavatkozások növelik a szükségesadag mértékét. A C-vitaminnal jól ellátott anya tejének aszkorbinsav-tartalma30...55 ml/l.Szent-Györgyi Albert biokémikus az 1930-as években izolálta a C-vitamint,munkásságát 1937-ben orvosi és élettani Nobel-díjjal ismerték el.Az egészséges ember napi C-vitamin szükségletét a helyesen összeállított ésjó konyhatechnikával elkészített ételekkel még a tél végi és tavaszihónapokban is fedezni lehet.Aszkorbinsavban gazdag zöldségfélék: a zöldpaprika, paradicsom, burgonya,saláta, és a káposztafélék: (káposzta, brokkoli, kelbimbó), friss gyümölcsök,(elsősorban áfonya, ribizli, a vadrózsa termése, a csipkebogyó, narancs,citrom, grapefruit), télen ezek, vagy az ezekből úgynevezett „hideg”eljárással készült teák, szörpök, gyümölcsborok fogyasztását kellszorgalmazni. A zöldségféléket lehetőleg nyersen, salátának elkészítve, vagypároltan célszerű fogyasztani.A C-vitamin hiány hatására kialakuló betegség a skorbut. Jellemzője akiszáradt bőr, emésztési zavarok, fogínysorvadás következtében meglazultfogak. Éveken, évtizedeken keresztül fennálló C-vitamin hiány esetén,rendkívüli mértékben megemelkednek a szív- és érrendszeri kockázatok.256
A P-vitaminA rutin (más néven citrin) a flavonoidok családjába tartozó vegyület. <strong>Kémiai</strong> szempontból egy glikozidEgyes vérzékenységgel járó, a skorbuthoz hasonló betegségek tiszta C-vitaminnal nem gyógyíthatók, decitromlé vagy paprikakivonat adására javulnak. A P-vitamint a paprikából sikerült kivonni. Ez az anyagcsökkenti a hajszálerek áteresztőképességét (permeabilitását), innen az elnevezése is.A P-vitamin segíti a C-vitamin felszívódását és megvédi az oxidációtól, ezenkívül erősíti a hajszálereket. AC-vitamin kísérője, általában ugyanazokban az élelmiszerekben fordul elő. Legbővebben a citrusfélék, acsipkebogyó, az áfonya, a brokkoli, a paradicsom, valamint más gyümölcsök és zöldségek tartalmazzák –elsősorban a gyümölcs húsa gazdag ebben a vitaminban.Emberben kifejezetten P-vitamin hiánybetegség vagy túladagolás nem ismert, de feltételezhető, hogyhiányában a C-vitamin felszívódása és felhasználása zavart szenvedhet, éppen ezért tüneteik átfedhetikegymást. A vízben oldódó vitaminok esetében nincsen túladagolás mert a vízben oldódó vitaminokat nemtudja tárolni a szervezet.<strong>OH</strong>HO<strong>OH</strong>OO<strong>OH</strong>OO<strong>OH</strong><strong>OH</strong> <strong>OH</strong> <strong>OH</strong>OO<strong>OH</strong><strong>OH</strong>rutin257
Vegetáriánus étrend hátrányai1. A növényeket általában hosszú ideig kell főzni az emészthetetlen anyagok miatt. Ez az előkészítésifolyamat roncsolja a bennük található, a szervezet számára értékes anyagokat.2. A B 12 vitamin teljesen hiányzik a növényekből.3. Telítetlen és többszörösen telítetlen zsírsavakat tartalmaz, amely terhet jelent a szervezetre nézve,mert több antioxidáns hatású vitamint igényel.4. Aminosavakat tekintve a lizin, cisztin, metionin szinte teljesen hiányzik a növényekből; aminosavak,mikro- és makroelemek nem megfelelő arányban vannnak jelen.5. Az arachidonsav esszenciális zsírsav nem található meg növényekben.6. Makroanyagokat tekintve sok kálium és kevés kalcium vagy foszfor jellemző. Nincs benne koleszterin,de van benne fitosztein.7. Sok rostot tartalmaznak, amelyek jó hatása ismert, de csökkentik a zsír, ásványi anyagok és fehérjékemészthetőségét.8. Az ovovegetariánus étrend – mely tartalmaz tojást és tejet is – kielégítő lehet.CO<strong>OH</strong>arachidonsav258
Antibiotikumok I.Az antibiotikumok az élő szervezetek – elsősorban mikroorganizmusok – általtermelt úgynevezett másodlagos anyagcseretermékek (szekundermetabolitok) legfontosabb csoportja. Ökológiai szerepük, képződésük oka,célja nem teljesen tisztázott. Egyes nézetek szerint a termelő szervezetekbiológiai védekezésének részét képezik, mások szerint az antibakteriális hatásés antibiotikum termelés csak véletlenszerűen kapcsolódik egyesmikroorganizmusokhoz.Waksman (1945): streptomycin és számos egyéb antibiotikum felfedezője(aktiomycin, neomycin).Definíciója: antibiotikum, vagy antibiotikus hatású anyag az amelyetvalamilyen mikroorganizmus termel és azzal a képességgel rendelkezik, hogymikroorganizmusok szaporodását képes gátolni illetve el is pusztítja azokat.Selman AbrahamWaksman1888 - 1973Baron szerint: antibiotikumnak tekinthető egy olyan anyag:• Valamilyen élőlény (alacsonyabb és magasabb rendű) anyagcsereterméke• Biokémiai mechanizmuson keresztül gátolja egy vagy több mikroorganizmus szaporodását• Alacsony koncentrációban is hatásos• Magasabb rendű növényekre vagy állatokra terápiás szinten nem vagy alig hat.Antibiotikum nem azonos a kemoterápiás szerekkel. Ez utóbbiak a teljesen mesterségesen előállítotthatóanyagok, míg az antibiotikum elnevezést célszerű a természetes eredetű vegyületekre fenntartani,jóllehet a félszintetikus és a teljesen szintetikus antibiotikumok megjelenésével egyre nagyobb azösszemosódás.259
Az antibiotikumok csoportosítása1. Előállítási módjuk alapján:• Bioszintetikus úton nyert antibiotikumok (fermentációval)• Félszintetikus antibiotikumok• Szintetikus antibiotikumok2. Hatásuk alapján:• Major (nagy) antibiotikumok: ezeket szokás széles spektrumú antibiotikumoknak is nevezni, mertsokféle mikroorganizmusra hatnak. Pl: Penicillinek; Streptomicin; Chloramphenicol; Tetraciklinek• Minor (kicsi) antibiotikumok: szűk spektrumú antibiotikumok, kis számú mikroorganizmusrahatnak. Pl: Erythromycin; Novobiocin; Vancomycin• Baktérium-, gomba-, rák- vírusellenes szerek• Gyógyászati, mezőgazdasági vagy egyéb céllal előállított vegyületek.3. Hatásmechanizmusuk alapján:Nukleinsavszintézis-gátlók: szulfonamidok; trimethoprim, kinolinok.Sejtfalszintézis-gátlók: penicillinek, cefalosporinok, vancomycin.Fehérjeszintézis-gátlók: aminoglikozidok, tetraciklinek.4. Szerkezetük alapján:• szénhidrát vázas antibiotikumok (aminoglikozidok, linkozaminidek, vankomicinek)• makrociklusos lakton/laktám vázas antibiotikumok ( makrolidok, poliének, anzamicinek)•kinonvázas antibiotikumok ( antraciklinek, tetraciklinek)• aminosav, peptid, polipeptid antibiotikumok (laktámok, bactoracin, graminicidin, polimixin)• nitrogén tartalmú antibiotikumok (nukleozid antibiotikumok)• aliciklusos antibiotikumok (fusidinsav)• aromás antibiotikumok (klóramfenikol)• alifás antibiotikumok (foszfonomicin)• oxigéntartalmú heterociklusok (poliéterek)260
Alexander Fleming1881 - 1955Penicillium notatumA penicillinek felfedezéseFleming 1928-ban a londoni St. Mary kórházban vette észre, hogy aStaphylococcus tenyészetébe került kékes-zöldes penész szennyeződés körül abaktériumok nem növekednek. Fleming arra a következtetésre jutott, hogy apenész olyan anyagot bocsát ki, mely gátolja a baktériumok növekedését, éselpusztítja a baktériumokat. A penészt tiszta kultúrában is kitenyésztette, ésfelfedezte, hogy a Penicillium családba tartozó fajról van szó, melyet maPenicillium notatum fajként ismerünk.A baktériumokat különböző festési eljárásokkal szembeni viselkedés alapján isszokták csoportosítani. Az egyik ilyen eljárás a Gram-festés, melyet 1884-benHans Christian Gram fejlesztett ki. Ez a módszer a baktériumokat a sejtfalstrukturális sajátosságai alapján különíti el. A festés során kristályibolya (vagygenciánaibolya)-festékkel festik meg a baktériumkészítményt, majd etanollalmosási próbát végeznek. Gram-pozitív baktériumok esetén a festék a sejtfalbólnem mosható ki, míg a Gram-negatív baktériumoknál igen. A Gram-negatívbaktériumok láthatóvá tétele érdekében további fukszinos festést alkalmaznak. AGram-pozitív baktériumok vastag peptidoglikán sejtfala lilának látszik, míg aGram-negatív fajok sejtfala rózsaszínű lesz a festés után.261
A b-laktám antibiotikumok csoportosítása,hatásmechanizmusa és bioszintéziseRO<strong>OH</strong> HH HHO H HSSHNR HNSNN R'H 3 C NOOOCO<strong>OH</strong> NHRCO<strong>OH</strong>CO<strong>OH</strong>penicillinekkefalosporinoktienamicinekR 3 R 2HNNO R'monobaktámokHatásmechanizmusa: A β-laktám antibiotikumok a baktériumok sejtfalában a peptidoglikánok közöttikeresztkötések kialakulását gátolják. A penicillin β-laktám része ahhoz a transzpeptidáz enzimhez kötődik,mely a baktérium peptidoglikán molekuláit kötné össze. Az enzim így nem tud megfelelően működni és abaktárium sejtfala osztódás során meggyengül (másképp fogalmazva az antibiotikum citolízist,sejtpusztulást eredményez, mikor a baktérium megpróbál osztódni). Ezen felül a felhalmozódottpeptidoglikán prekurzorok a baktériumban aktiválják a sejtfal hidrolázok működését, amelyek továbbrombolják a baktérium meglevő peptidoglikánját.O<strong>OH</strong>HONH 2 <strong>OH</strong> 2 NOL-a-aminoadipinsavSH<strong>OH</strong>L-ciszteinH 2 NOD-valin<strong>OH</strong>HOONH 2<strong>OH</strong>NONHSHO<strong>OH</strong>HOONH 2<strong>OH</strong>NONSO<strong>OH</strong>262
RO<strong>OH</strong>FermentációTermészetes penicillinekR<strong>OH</strong>N<strong>OH</strong> HNSCO<strong>OH</strong>penicillin származékA kutatások során felfedezték, hogy afermentációhoz használt Penicilliumchrysogenum táptalajához adagoltkarbonsavakkal befolyásolni lehet abioszintézis irányát és hozamát.Ezeket az anyagokat prekurzoroknaknevezzük, és a gombák nem bontjákle őket, hanem változtatás nélkülbeépítik. A tapasztalat szerintazonban csak apoláros oldalláncottartalmazó karbonsavakat alkalmazhatunkprekurzorként.R:HOSOF G X K O V• Igen nagy gond, hogy a baktériumok rezisztenciájának kifejlődése következtében a természetespenicillinek alkalmazhatósága erőteljesen korlátozódott. Amíg 1941-ben a Staphylococcus törzseknekcsak 1%, 1946-ban 14%-a, addig napjainkban már több mint 80%-a penicillinrerzisztens.•További probléma volt, hogy ezek a származékok meglehetősen szűk hatásspektrumuak voltak,túlnyomóan csak a Gram-negatív baktériumokkal szemben voltak hatásosak voltak.• Problémát jelentett az allergizáló hatás, amit antihisztaminokkal sem sikerült kiküszöbölni.• Megoldás új, félszintetikus penicillinekre van szükség!263
Félszintetikus penicillinekA variálható oldallánc módosításai a természetes penicillinekhez képest növelik az orálisbiohasznosultságot, ellenállóbbá teszik a molekulát a β-laktamáz enzim ellen, és növelik az antimikróbáshatásspektrumot. A félszintetikus penicillinszármazékokat úgy hozzák létre, hogy fermentációval azoldalláncmentes 6-amino-penicillánsavat termelik, és ehhez csatolják a variábilis oldalláncokat.<strong>OH</strong> HSHNNOCO<strong>OH</strong>G-penicillinpenicillin-amidázH HSH 2 NNOCO<strong>OH</strong>6-aminopenicillánsavROClOR H HSHNNOCO<strong>OH</strong>félszintetikus penicillinekClNO<strong>OH</strong>N<strong>OH</strong> HcloxacillinNSCO<strong>OH</strong>Rezisztens staphylococcusok törzsekellen használják. A gyógyszernek kisebbaz antibakteriális hatása, mint a G-penicillinnek, de a mellékhatása is.SHO<strong>OH</strong>NOOO HNHOOCtemocillinDirekt Gram-negatív korokozók ellen fejlesztették ki, deGram-pozitívak ellen, Acinetobacter fajok, ésPseudomonas aeruginosa ellen nem hatásos.Multirezisztens Gram-negatív korokozók ellen hasznosgyógyszer a klinikumban.S264
Penicillin rezisztenciaAz elmúlt évtizedekben egyre több, korábban ampicillin, amoxacillin-érzékeny Gram-negatívbaktériumról (H. influenzae, E. coli, Shigella, Salmonella törzsek) mutatták ki, hogy b-laktamáz enzimettermelnek, melyek inaktiválják az antibiotikumokat.HOONH 2NHH HOSNamoxacillinCO<strong>OH</strong>b-laktamázHO<strong>OH</strong> HSN NH HNH 2O <strong>OH</strong>penicillosavCO<strong>OH</strong>A penicillinek kombinálhatók β-laktám inhibitorokkal, amelyek megvédik a hatásosgyógyszermolekulákat a bontó enzimtől, és így a szer β-laktám termelő organizmusok ellen is hatásoslesz. Tág hatásspektrummal rendelkeznek, az elsődlegesen választandó szerek közé tartóznak.<strong>OH</strong>ONCO<strong>OH</strong>klavulánsav<strong>OH</strong><strong>OH</strong>O OSNCO<strong>OH</strong>sulbactam<strong>OH</strong>O OSN NCO<strong>OH</strong> N Ntazobactamamoxacillin + klavulánsavb-laktamáz gátlók265
Tetraciklin antibiotikumokA penicillin után legismertebb antibiotikumok. A tetraciklint a Streptomyces aurofciens, majd aklórtetraciklint Str. viridifaciens kultúrájából izolálták. Három különböző tetraciklint ismerünk: tetraciklin(TC), oxitetraciklin (OTC), 7-klór-tetraciklin (CTC). Félszintetikus származékai közül igen népszerű adoxiciklin. Széles spektrumú fehérjeszintézis inhibítor (a riboszóma 70S alegységéhez kötődve)antibiotikumok, jól hatnak a Gram–pozitív és Gram–negatív baktériumok, rickettsiák, mikoplazmák,leptospirák és spirochéták ellenH 3 CHO CH 3 HN CH 3<strong>OH</strong>H 3 CN CH 3HO CH 3 <strong>OH</strong><strong>OH</strong>H 3 CCl HO CH 3HN CH 3<strong>OH</strong>CH 3HN<strong>OH</strong><strong>OH</strong><strong>OH</strong> O <strong>OH</strong> OONH 2<strong>OH</strong><strong>OH</strong> <strong>OH</strong> O OONH 2<strong>OH</strong><strong>OH</strong> O <strong>OH</strong> OONH 2<strong>OH</strong><strong>OH</strong> O <strong>OH</strong> OONH 2tetraciklinoxitetraciklin7-klórtetraciklindoxyciklinA tetraciklinek a legrégebbi, kifejezetten széles spektrumú antibiotikumok közé tartoznak, amelyek közülcsak néhány származék maradt meg a klinikai gyakorlatban. A korai, gyorsan eliminálódó, csak vesénkeresztül ürülő és vesekárosodás esetén kumulálódó származékok, mint a tetraciklin vagy oxitetraciklinitthon már nincsenek forgalomban. A későbbi származékok, köztük a doxyciclin ma is kiterjedten használtantibiotikum, de indikációs területe az eredeteihez képest jelentősen megváltozott.A tetraciklinek korábban igen hatékonyak voltak a Gram-pozitívok közül a staphylococcusok,streptococcusok ellen, ma ezen törzsek 30-40%-a rezisztens. A Gram-negatívok közül az E.coli, Klebsiellaspp, Enterobacter spp-k 30%-a, a Proteus mirabilis több mint 90%-a rezisztens. A H.influenzae viszonylagérzékeny maradt (6% rezisztens).266
Aminoglikozid antibiotikumokAz aminoglikozidok az egyik legrégibb antibiotikum családot alkotják. Az első képviselőjüket asztreptomicint Waksman izolálta 1944-ban. A legjelentősebbek és a legismertebbek a sztreptomicin,gentamicin, tobramicin. Hatásspektrumuk széles, elsősorban Gram-negatív baktériumok ellenhasználatosak, Gram-pozitívok ellen is hatnak. Gram-negatív erős fertőzés esetén a cefalosporinok mellettezek az antibiotikumok jelentik a megfelelő hatásos anyagokat. Elsősorban tuberkulumok, mellékhatásaikmiatt (vese és fülkárosító toxinok), valamint plazmidon hordott rezisztencia átadó képességük miatthasználatuk korlátozott. Baktérium ellenes hatásuk különleges: az arra érzékeny baktériumokfehérjeszintézisét gátolja, ahol a riboszómákon a fehérje molekula szekvencia leolvasásában hibákatokoz, ezért leállítja a fehérjemolekulák szintézisét.H 2 NN<strong>OH</strong><strong>OH</strong> <strong>OH</strong>NH 2<strong>OH</strong>C <strong>OH</strong>NH 2H 2 N NO<strong>OH</strong>O OONH<strong>OH</strong><strong>OH</strong>HONHOOO<strong>OH</strong>H 2 NONH 2ONH 2NH 2 NHOONH 2H 2 NO<strong>OH</strong>NH 2OO<strong>OH</strong><strong>OH</strong>NH 2<strong>OH</strong>szterptomicingentamicintobramicinAz aminoglükozid antibiotikumok túlnyomó részét a Streptomyces kisebb mértékben Micromonosporafajok termelik közvetlen vagy irányított fermentációval. Általában izomerek és/vagy közeli homológokalkotta komplex keveréket termelnek, nem ritka 10-15 sőt 30-40 különböző minorkomponens izolálása sema fermentléből.267
Makrolid-antibiotikumokA makrolidek közül az erythromycin jelent meg elsőnek 1952-ben, de két évtizeden keresztül csak apenicillin alternatívája volt penicillin allergiás betegek kezelésében. A makrolidek kiterjedt alkalmazása ésigazi fejlődése a 70-es évek második felére tehető, mikor kiderült , hogy a leghatékonyabb antibiotikum azakkor felismert legionellosis kezelésében és realizálták az ún. atípusos kórokozók (mycoplasmák,chlamydiák) klinikai jelentőségét.A makrolideket a laktongyűrűben levô szénatomok száma szerint 14, 15, 16 szénatom számúszármazékokra osztjuk. Az azithromycinben nitrogén helyettesít egy szénatomot, ezzel alcsoportot, azazalideket képezve. A makrolidek a baktérium fehérjeszintézisét gátolják. A makrolidekkel szembenszámos rezisztencia mechanizmus alakult ki, melyek többsége keresztrezisztenciát okoz - a baktériumklinikailag az összes makrolid származékkal szemben rezisztenssé válik.NO<strong>OH</strong>OO<strong>OH</strong><strong>OH</strong>NHOOOO OO <strong>OH</strong><strong>OH</strong>ONHO HOOO<strong>OH</strong>OOOO<strong>OH</strong>etritromicinazithromycin268
Számos szulfonamid ismert, ebbôl ismertetünk néhányat általános képletükkel együtt (fent jobbra).Ezek a vegyületek a baktériumok folsavszintéziséhez nélkülözhetetlen a p-amino-benzoesav szerkezetianalógjai (fent balra). A szulfonamidok szelektív toxicitása azon a tényen alapszik, hogy az emlôssejtek atáplálékban folátot vesznek fel, míg az érzékeny baktériumok nem képesek erre, és a folsavat magukszintetizálják. A szulfonamidok kompetitíve gátolják a dihidropteroát-szintetázt ( ), és ezzelmegakadályozzák a DNS szintéziséhez szükséges folát képzôdését. A szulfonamidok bakteriosztatikushatású szerek. Leglényegesebb mellékhatásaik a (gyakori) bôrkiütések, veseelégtelen-ség és különbözôvérdyscrasiák.269
270
A penicillinek (fent balra) és cefalosporinok (fent jobbra) szerkezetének közös jellemzôje a ß-laktámgyûrû (B), amelynek épsége nélkülözhetetlen az antibakteriális aktivitáshoz. Az R 1 és R 2 csoportokmódosítása számos félszintetikus, közülük néhány savrezisztens (és orálisan aktív)antibiotikumot eredményezett, amelyek szélesspektrumú antibakteriális aktivitással rendelkeznek,vagy rezisztensek a bakteriális β-laktamázra. A penicillinek (balra) a legfontosabb antibiotikumok * ,míg a cefalosporinok (jobbra) néhány specifikus indikációs területtel rendelkeznek. A β-laktámgyûrûsantibiotikumok baktericid hatásúak. Antibakteriális hatásukat a lineáris peptidoglikánpolimerláncok közötti keresztkötések kialakulásának gátlása révén fejtik ki, amelyek a sejtfalat építikfel, pl. pentaglicin híd révén ( ). E hatás annak köszönhetô, hogy szerkezetük egy részeésze ( )hasonlít a baktérium sejtfal peptidláncának D-alanil-D-alanin részéhez.271
272
Az antibiotikumok ezen csoportja a baktérium fehérjeszintézisének gátlása révén hat. Avegyületek szelektíven toxikusak a baktériumokra, mivel a bakteriális ribosomák (ahol a fehérjeszintézistörténik) egy 50S és 30S alegységbôl állnak, míg az emlôsök ribosomái egy 60S és 40S alegységbôl.A fehérjék aminosavakból épülnek fel a ribosomákon. A ribosomák a messengerribonukleinsavlánc (mRNS) mentén mozognak elôre (1-2-3) úgy, hogy az egymást követô a specifikustransfer-RNS- (tRNS-) molekulák számára kötôhelyet biztosító akceptoron haladnak keresztül. Afehérjelánc meghosszabbításához szükséges következô aminosavat a tRNS-ek hordozzák.A Tetraciklinek (fent jobbra) és az aminoglikozidok (balra lent) a ribosoma 30S-alegységéhezkapcsolódnak és az amino-acil-tRNS kötôdését gátolják. Az aminoglikozidok emellett hibás mRNSolvasást eredményeznek, amely mûködésképtelen fehérjék szintéziséhez vezet.A fehérjeszintézis következô lépése a transzpeptidáció (2), amelyben a növekvô peptidlánchozzákötôdik a P-kötôhelyhez, majd átkerül az A-kötôhelyen lévô amino acil-tRNS-hez kötött aminosavhozA chloramphenicol a ribosoma 50S alegységének peptidil-transzferáz aktivitását gátolja.A transzpeptidációt követôen a peptidlánc az A-kötôhelyrôl a P-kötôhelyre (3)transzlokálódik, így az A-kötôhely alkalmassá válik a következô amino-acil-tRNS fogadására. A makrolidek(lent jobbra) a ribosoma 50S alegységéhez kötôdve a transzlokációt gátolják.273
energiaenergiaenergiaenergia<strong>Szerves</strong> vegyületek fényelnyelésehKromofór: a molekulaönállófényelnyelésselrendelkező része.CH 2 =CH 2CH 2 =CH 2Auxokróm: nincs önállóelnyelése, de módosítja akromofór elnyelését. hCH 2 =CH 2 CH 2 =CH 2
l l ..l nfényelnyelésl l ..l nElnyelt fény hullámhossza Színe A tárgy színe400 nm Ibolya Sárgászöld425 nm Kék Sárga450 nm Búzavirágkék Narancssárga490 nm Kékeszöld Vörös510 nm Zöld Bíbor530 nm Sárgászöld Ibolya550 nm Sárga Kék590 nm Narancssárga Búzavirágkék640 nm Vörös Kékeszöld730 nm Bíbor Zöld
Növényi színezékek• A magasabb rendű növények színanyagai két fő csoportba oszthatók:– A fotoszintetikus apparátus pigmentjei: klorofillok; karotinoidok ésxantofilok– Polifenolok és flavonoid származékok: döntően a termések és virágokszínét adjákAz adott szint a jelenlévő növényi festékek keveréke határpzza meg.
Klorofill-a és Klorofill-bCHCH 2RKlorofill-a: R = CH 3H 3 CH 3 CHHN NMgN NCH 2COOCH 3CH 2 COOCH 2CH 2 CH 3CH 3OCH 3Klorofill-b: R = CHOPorfirin vázCH 3CH 3CH 3 CH 3
• C 5 izoprén egységből felépülő C 40 láncokKarotinoidok• A láncvégi egység lehet nyílt (pl.: likopin) vagy gyűrűs (a-, b-és g-karotin), de csak C és Hatomokat tartalmazz!likopina-karotinb-karoting-karotin
Xantofilok<strong>OH</strong>OsárgaHOflavoxanthin (E161a)rozsdavörösHOrubixanthinO<strong>OH</strong><strong>OH</strong>Oviolaxanthin
PolifenolokHOOCO<strong>OH</strong><strong>OH</strong>O 2HOOCOO<strong>OH</strong>O<strong>OH</strong>OOboletol (sárga)kékO<strong>OH</strong><strong>OH</strong>Sátán gombavörösOalkannaO<strong>OH</strong>alizarinO<strong>OH</strong><strong>OH</strong><strong>OH</strong>O<strong>OH</strong>O<strong>OH</strong>purpurinbíborfestőbuzérshikonalkanin, shikoninvörös
FlavonoidokA flavonol és flavon származékok többnyire sárga színűek, a virágok és atermések színét adják.O<strong>OH</strong>OflavonolOOflavonAz antocianidinek vörös-kék színű színezőanyagok. Szinük és szerkezetükpH függést mutat.antocianidin (aglikon)<strong>OH</strong>OO Oantocian (glikozid)<strong>OH</strong><strong>OH</strong><strong>OH</strong>
<strong>OH</strong><strong>OH</strong><strong>OH</strong>OO<strong>OH</strong>O<strong>OH</strong>O<strong>OH</strong>OOOC 6 O 5 H 11OC 6 O 5 H 11OC 6 O 5 H 11OC 6 O 5 H 11OC 6 O 5 H 11OC 6 O 5 H 11vörös (pH < 3) ibolya (pH = 7-8) kék (pH 9-10)O<strong>OH</strong>OOOC 6 O 5 H 11OC 6 O 5 H 11sárga (pH > 11)
A gyógyszerkémia történeteA gyógyszerkémia definíciója:„A gyógyszerkémia a biológiailag aktív vegyületek felfedezésével,azonosításával, kifejlesztésével és hatásmechanizmusánaktisztázásával foglalkozó tudomány” (Burger, A.: MedicinalChemistry. 2nd Edition Intersc. New York, 1960)A gyógyszerkémia „feladatai” közé tartozik a természetes anyagokizolálása, az új vegyületek szintézise, biológiai hatásának elemzése,szerkezet-hatás összefüggések keresése, a különböző receptorokkal valókölcsönhatás feltérképezése, a transzport és eloszlási folyamatokfeltárása, valamint a metabolikus transzformáció más vegyületekké.Határterületen mozgó tudomány: szerves-, fizikai-, analitikai-, biokémia,farmakológia, mikrobiológia, biofizikaA természeti népek gyógyításában a pszichés hatású elemek és aracionális tapasztalatok keveredtek. A gyógyítást a varázsló vagy a sámánvégezte és az általuk alkalmazott növényi, állati és ásványi termékekvoltak a mai értelemben vett gyógyszereink elődei. A kultúra fejlődésévelaz orvos-gyógyszerészi hivatás már az ókorban (i.e. 3500-i.u. 476)kettévált.
A gyógyszerkémia történeteÓkori Kína: ismerték a diétásétkezés, napfürdőzés kedvezőhatásait; alkalmazták a himlőellen a vakcinációt.Az ópiumot, hasist,mandragórát műtéti narkózisrahasználták. Gyógyszerkönyvük(kínai nagy füvészkönyv, PenCao Csing) kb. ötezer éves.zöld mákindiai kenderCannabis sativamandragóragyümülcseimorfintetrahidrokannabinolatropin
A gyógyszerkémia történeteA zsidók: az egészségügyiintézkedéseket a Talmud vallásiparancsaival vitték keresztül.Tiltották a – forró égöv alatt gyorsanromló – sertéshús fogyasztását.Megkövetelték a fiúgyermekekkörülmetélését, a nők rituálisfürdését, valamint a betegekelkülönítését.Ókori Egyiptom: 800 orvosirecept; hagyma, fokhagymarendszeres fogyasztása;trachomás szembetegségellen a szemhéjmalachitzöldes festése. Agyógyítás egyiptomi istenePharmaki (biztonságnyújtó) a gyógyszerészitudományos tevékenységnemzetközileg használt“Farmacia” megjelölése.malachit ásványbázisos rézkarbonátCu 2 CO 3 (<strong>OH</strong>) 2malachitzöldMalachit ásvány őrleményéből az ókor óta készítenekpigmentet (malachitzöld). Egyiptomban szemfestéknek ishasználták, és ez volt a Nílus színe.
A gyógyszerkémia történeteRicinus communisZingiber officinalegyömbérIndia: a “gyógyszerkészítők” akasztrendszer legfelsőbb fokánálltak Alkalmazták a ricinust és agyömbért, az ásványi eredetűanyagok közül pedig a bóraxot, atimsót, a szódát és azarzénessavat. Ismerték avászonfehérítést, a kelmefestést, aszappanfőzést, erjesztéssel pedigsört tudtak előállítani.BóraxNa 2 B 4 O 7 •10H 2 OTimsó(KAl(SO 4 ) 2·12H 2 O)SzódaNa2CO3
A gyógyszerkémia történeteÓkori görögök: alkalmazták az egyiptomiakismereteitHIPPOKRATESZ (i.e. 460-370) receptjeibenfelfedezhető az indiai és egyiptomi eredet.Tanításának egyik alaptétele: az emberi test képessaját erőből legyőzni a betegségeket, az orvoslegfontosabb feladata ezt elősegíteni.(Hipokrateszi eskü: ókori görög orvosok esküje)Hippokratesz gyógyszerészeti ismereteit GALENUSnak(i.sz. 130-200) a gyógyítás módszereiről írtmunkája őrizte meg.A gyógyszereket ő először rendszerbe foglalta.Szerinte a növényi, az állati és az ásványi eredetűanyagokban meg kell találni a gyógyításraalkalmas hatóanyagokat és azokat az emberiszervezet számára hasznosíthatóvá kell formálni.Neki tulajdoníthatóan a laboratóriumban készültgyógyszereket galenikumoknak nevezzük. Anapjainkban készült tablettákat, injekciókat stb.pedig a neogalenikum elnevezéssel illetjük.HippokrateszGalenus
Hippokrateszi eskü„Esküszöm Apollora, az orvosra, Aesculapiusra, Hygeiara és Panaceára – és tanúimul hívokminden istent és istennőt --, hogy értelmi képességemnek megfelelően tartom magam akövetkező eskühöz:Mesteremet és tanítómat éppúgy tiszteletben tartom, mint saját szüleimet, s életemetmegosztom vele és mindent megfizetek neki, amivel tartozom és amit kér. Gyermekeittestvéreimnek fogom tekinteni, s tanítom őket erre a mesterségre, ha kívánják, fizetség ésszerződés nélkül. Tanítani fogom ezt a művészetet a gyermekeimnek, s az engem tanító mesterfiainak és a tanítványoknak, akik elkötelezték magukat és elfogadták a szakma szabályait; desenki másnak nem tanítom. Képességemnek és ítéletemnek megfelelően előírom mindazt, amiszükségesnek tűnik pácienseim javára és senkinek sem fogok ártani. Még kérésre sem fogokhalálos gyógyszert felírni senkinek, s nem adok olyan tanácsot sem, amely valakinek halálátokozhatja. Nőnek nem adok eszközöket az abortuszhoz. Megőrzöm életem és működésemtisztaságát. Nem használok kést, még az olyan betegeknél sem, akik kőtől szenvednek; az ilyenoperációt a sebészeknek hagyom. Csakis a betegeim érdekében lépek be minden házba , desohasem azért, hogy ártsak valakinek. Nem csábítom el, s nem létesítek szexuális kapcsolatot aháztartás női vagy férfi tagjaival, akár szabadok, akár rabszolgák. Bármilyen szakmai vagymagánéleti titkokat látok vagy hallok, a titkokat megőrzöm és nem mondom el senkinek. Hahűséges maradok eskümhöz, akkor boldogulhatok életemben és munkásságomban, tisztelni fogmindig mindenki; de ha áthágom vagy megsértem azt, az ellenkezője történhet velem.”
A gyógyszerkémia történeteAz alkímia (az anyag átalakításának tudománya; XIV – XVI. század): Fő célja: azaranykészítés közönséges fémekből a “bölcsek kövé”-nek segítségével. Vizsgálódásaiksorán számos hasznos kémiai ismeretet szereztek; felfedezték a cukrot.A reneszánszkori természettudományos gondolkodásfejlődésének eredményekéntkialakult a jatrokémia (orvosi kémia, XVI.-XVIII. sz.). Célja a kémia gyógyászatialkalmazása és gyógyszerek előállítása volt. Legfőbb képviselője PARACELSUS (svájciszármazású) volt.Az alkímiát a gyógyszerkészítés szolgálatábakívánta állítani. Gyógyszerei elsősorbangyógynövényekből és fémekből készültek (agyógyászatban elsőként alkalmazottkülönböző fémsókat, mégpedig sikerrel),amelyek közvetlenül a természetbenmegtalálható formában nem használhatókgyógyításra, ezért szükség van az orvosra –mint alkimistára – aki belőlük megfelelőfőzetet, kenőcsöt készít. Helyesenkövetkeztetett a foglalkozási betegségekre.Nevéhez fűződik a hatóanyag fogalma,továbbá neki is köszönhető, hogy a kémia1493-1541megbecsült tudománnyá vált.
A gyógyszerkémia történeteAz orvosi és gyógyszerészi foglalkozás ebben az időben kezdett elkülönülni egymástól,megjelentek az önálló gyógyszertárak és gyógyszerészek.1742-1786SCHEELE (német származású gyógyszerész):14 éves korában gyógyszertárigyakornokként kezdte pályafutásátNémetországban.A tűzről és levegőről szóló tanulmányánakköszönhetően 33 éves korában a SvédTudományos Akadémia tagjai sorábaválasztotta. Az ő nevéhez fűződik a glicerin,a szerves savak (pl. citromsav, tejsav,borkősav), az oxigén („tűz-levegő”), a klór,a hidrogén-cianid, stb. felfedezése (szokásavolt, hogy az általa felfedezett kémiaianyagokat meg is kóstolta, korai halálátfeltehetően higanymérgezés okozta.)
A gyógyszerkémia történeteA XIX. századtól a gyógyszerészet a kémiától külön úton járt, de mégis a gyógyszerészettudományos alapjait változatlanul a kémia adta.1803-1873LIEBIG-et (német vegyész) tekintjük az elsőegyetemi kémiai iskola megalapítójának. Őállította elő először a klorál-hidrátot(triklóracetaldehid-monohidrát), amit harmincévvel később már altatóként alkalmaztak.Ugyancsak nevéhez fűződik a szervesmikroanalitika alapelveinek kidolgozása(analitikai módszert dolgozott ki a szén, ahidrogén és a halogének meghatározására).SERTÜRNER (német vegyész, gyógyszerész)1806-ban máktokból izolálta az ópium főhatóanyagát, egy rendkívül erősfájdalomcsillapító és bódító hatású szert.Morpheus, a jó álmok istene utánmorfiumnak nevezte. Ez volt az első alkaloid!1783-1841
A gyógyszerkémia története1800-1882WÖHLER (német kémikus) kísérletesen döntöttemeg a “vis vitalis” (életerő) elméletet /azokat avegyületek tekintették szervesnek, amelyekelőállítására csak az élő szervezetek életerejeképes/. 1824-ben először állította elő diciánbóla növényi eredetű oxálsavat, majd 1828-ban azásványi eredetű (szervetlen) ammóniumcianátbóla vizeletben előforduló karbamidot(szerves). Ezzel szintézissel a szintetikus kémiaés a gyógyszerek előállításának új korszakavette kezdetét, amelyet ma is a fejlődésrugójának tekintünk.Oxálsav előállításaKarbamid előállításaCCNCO<strong>OH</strong>4 H 2 ON + CO<strong>OH</strong>+2 NH 3NH 4 OCNH 2 NCONH 2
A gyógyszerkémia története1854-1915HO As As <strong>OH</strong>HCl*H 2 NNH 2 *HClSalvarsan3,3'-diamino-4,4'-dihidroxi-arzenobenzol-dihidrokloridPAUL ERLICH (német tudós) atudományos gyógyszerkutatás, akemoterápia meg-alapítója. 1908-banorvosi-élettani Nobel díjat kapott.Szerinte az eredményes kutatásfeltétele: a pénz, a türelem, azügyesség és a szerencse, melyek akísérletes tudományos munkának mais fontos elemei. Ő fogalmazta meg a„mágikus golyó” elvét. Szerinte ha csakabba a sejtbe juttatjuk a hatóanyagotamelyikbe kell, akkor csak a beteg sejtpusztul el és a szervezet más sejtjeinem károsodnak. Tanítványával, Hatavalvégzett kísérletei során; a 606-osszámú kísérletben sikerültelőállítaniuk azt az arzeno-benzolszármazékot(Salvarsan-naknevezték), amely a szifiliszkórokozójára hat, és „bámulatosan”gyógyítja a betegséget.
A gyógyszerkémia története1895-1964H 2 NON NH 2O S NNH 2* HClProntosil4-[(2,4-diaminofenil)azo]benzolszulfonamidGERHARD DOMAGK (német tudós) Ehrlichtapasztalatait követve kereste azt agyógyszert, amely képes lesz aszervezeten belül a bakteriális fertőzéslegyőzésére. 1939-ben orvosi-élettaniNobel díjat kapott a Prontosil – az elsőszulfonamid alapú gyógyszerantibakteriálishatásának felfedezéséért.Szisztematikus mód-szerrelúj festék- és gyógyszer-molekulákatkeresett, és észrevette, hogy az egyiknarancsvörös színű festéknekantibakteriális hatása van az egerekStreptococcus-fertőzésével szemben.Később megállapították, hogy ebből afestékből a szervezetben redukció útjánp-amino-benzol-szulfonsavamid (PABS)hasad le, amely valójában a gyógyhatáshordozója.
1893-1986H<strong>OH</strong>O O<strong>OH</strong>O<strong>OH</strong>aszkorbinsav(R)-3,4-dihidroxi-5-((S)- 1,2-dihidroxietil)furán-2(5H)-onA gyógyszerkémia történeteSZENT-GYÖRGYI ALBERT (magyar kutató orvos) asejtlélegzés tanulmányozása során bizonyosnövényekből - narancs, citrom - sikerültizolálnia egy redukáló "ágens"-t, amelyblokkolja a peroxidáz típusú enzimek hatását.Ezt a hexuronsavval (az 1920-as években,amikor felfedezték, de még a szerkezetét nemismerték, így nevezték) azonos anyagotnevezte el, utalva az anyag skorbutotmegszüntető hatására, aszkorbinsavnak,vagyis C-vitaminnak. Előállításához bőségesforrást jelentett a Szeged környéki paprika.1937-ben orvosi-élettani Nobel díjat kapott a„biológiai égésfolyamatok terén tettfelfedezéseiért, különösen a C-vitamin,valamint a fumársav-katalízisvonatkozásában”.A C-vitamin szerkezetének felderítéséért1937-ben, W. Haworth kémiai Nobel díjatkapott.
A gyógyszerkémia történeteRO1881-1955HNONSOCH 3CH 3<strong>OH</strong>Az antibiotikum-kutatás és - ipartörténete FLEMING (skót orvos,1945-ben orvosi Nobel díjatkapott) véletlen felfedezésévelkezdődött 1928-ban. Megálapította,hogy a Staphylococcusbaktérium tenyészetében megtelepedettpenész gomba olyananyagot termel, amely abaktériumokat elpusztítja. Későbbezt az anyagot H.W. FLOREY és E.B.CHAIN izolálta, melyet azantibiotikumot termelő Penicilliumnotatum gomba neve utánpenicillinnek neveztek el.Penicillin alapváz
A magyar gyógyszeripar fejlődéseGyógyszeriparunk Európában a legrégebbiek közé tartozik. Már 1867-ben működöttgyógyszergyár Magyarországon.A hazai gyógyszeripar megteremtése Richter Gedeon (1872-1944)gyógyszerész nevéhez fűződik (Kőbányai Gyógyszerárugyár, alapítva 1907,mai Richter Gedeon Rt.), akinek első saját gyári készítménye az állatimellékveséből kinyert adrenalin volt, melynek oldata Tonogén ® néven kerültforgalmazásra (a mai napig forgalmazott, ismert termékei: Hyperol(hatóanyaga: karbamid-hidrogén peroxid), Kalmopyrin(hatóanyaga:kalciumacetilszalicilát).<strong>OH</strong>NH(R)HO<strong>OH</strong>adrenalinRichter Gedeon
A magyar gyógyszeripar fejlődéseA Chinoin Gyógyszer és Vegyészeti Termékek Gyárát (1913-ban vette fel ezt anevet) Wolf Emil alapította 1910-ben Alka Vegyészeti Gyár néven, akitjelentős személyes és szakmai kapcsolatok fűztek a magyar szerves kémiaalapítójához, Zemplén Gézához. A Chinoin-gyár kezdeti gyógyszertermékeiközött találjuk a johimbint, az atropint stb., a későbbiekben pedig ahúgyhajtókat, az altatókat, a szulfonamidokat, antidiuretikumokat, ahormonokat, a vitaminokat, stb. A II. világháborút követően ugyancsak ittoldották meg a penicillin ipari termelését.Wolf Emil1886-1947Zemplén Géza1883-1956atropin
A magyar gyógyszeripar fejlődése1912-ben alapították a Phylaxia Szérumtermelő Rt.-t., amely az elsőállatgyógyászati oltóanyagokat, valamint laboratóriumi diagnosztikumokatelőállító intézet volt. Az idő előrehaladtával egyre nagyobb teret nyert azembergyógyászatban is az állati immunszérumok terápiás alkalmazása (pl.diftheria, tetanusz) a gyógykezelésben, így végül is a Phylaxiából 1954-benkivált az ezzel foglalkozó Human Osztály (szérumokat, vakcinákat gyártottak)és HUMAN Oltóanyagtermelő és Kutató Intézet néven (ma HUMAN Rt.) önállóválalattá alakult .Az 1913-ban alapított Egyesült Gyógyszer-és Tápszergyár (Egyt) az ipari méretűtápszergyártás hazai megteremtője. Fenállásának első 20 évében csakgyermektápszereket, malátakészítményeket és galenikus preparátumokatállított elő. 1985-ben felvette az EGIS nevet. A névváltoztatás fő indoka az volt,hogy az EGYT-t sok külföldi partner egyiptomi cégnek hitte. (Az EGIS a görögaigis szóból ered, mely Pallasz Athéné pajzsára utal és a védelem szimbóluma).Ismertebb sikeres készítményei: Radipon, Germicid.
A magyar gyógyszeripar fejlődéseMagyarországon a tiszavasvári (akkori Büdszentmihály) Alkaloida ésVegyészeti Gyár alapítása (1927) Kabay János gyógyszerész nevéhez fűződik, akiaz értéktelen mákszalmából a morfin kinyerésére világszabadalmat dolgozottki.Kabay János(1896-1936)morfin
A magyar gyógyszeripar fejlődéseA penicillin nagyüzemi előállítására létesítették 1952-ben Debrecenben aBIOGAL Gyógyszergyárat (eredeti nevén Hajdúsági Gyógyszergyárat, amely aRex Gyógyszerüzemmel 1963-ban egyesülve vette fel az említett nevet). Maineve: TEVA Gyógyszergyár Zrt.; a debreceni Biogal és a gödöllői Human gyógyszergyármellett az egykori Humanpharma és Humantrade gyógyszerforgalmazó vállalatokból jöttlétre 1993-ban. A több mint száz éves Teva, a világ vezető innovatív generikusgyógyszervállalata. Magyarország a TEVA európai gyártási és kutatásfejlesztési központja.Hazai hatóanyaggyártásunk fő felvevő piaca az Európai Unió és az Amerikai EgyesültÁllamok.penicillin
Magyarország gyógyszeripara napjainkban1989-ben megalakul napjaink gyógyszeriparának újabb nagy szereplője aBéres Rt. a Béres-csepp gyártására. 1993-ban kezdi el a pezsgőtablettákgyártását, 1998-ban pedig betör a multivitaminok piacára a Béres Activáltermékével. 1998-2000 között a termékpaletta tovább bővül (BéresCsonterősítő, stb.). A cég nagy állomását jelenti 2000. január 27.-e, amikorBéres József (1920-2006) találmányát, a Béres Cseppet az OrszágosGyógyszerészeti Intézet gyógyszerként törzskönyvezi. Ez az első termék avilágon, amely a gyógyhatású készítmény kategóriából gyógyszerré, ráadásulhazánkban elsőként úgynevezett roboráló gyógyszerré válik.Az 1990-től bekövetkezett változások egyik legfőbb eleme a cégekprivatizációja volt. A magyarországi gyárak mindegyikét 1991-1996 közöttprivatizálták, mely során a külföldi tőke dominanciáját megjelenítőtulajdonosi szerkezet alakult ki. Az elsőként privatizált vállalat a Chinoin volt.Az Országos Gyógyszerészeti Intézet (OGYI) 2002. novemberi adatai szerintMagyarországon 54 vállalkozásnak van gyógyszergyártási engedélye. A kisebb(50 fő alatti) vállalatok főként generikus gyógyszerek gyártásával
A magyar gyógyszeripar fejlődéseA táblázatból látható, hogy egyedül az Egis Rt. és a Richter Gedeon Rt. esetébenmaradt viszonylag jelentős a hazai tőke aránya. A Richter Rt. az egyedüli vállalat,amely a külföldi szakmai befektetők nélküli stratégiát választotta a privatizációsfolyamatok során.A hét vezető magyarországi gyógyszergyártó tulajdonosi szerkezeteVállalatFő tulajdonosTEVA Gyógyszergyár Zrt. Teva (Izrael) 99,1%Chinoin/Sanofi-Aventis Sanofi-Aventis (Francia) 99,1%Egis Rt. Servier (Francia) 51,0%Humán Rt. Teva (Izrael) 97,98%ICN Magyarország ICN Pharmaceuticals (USA) 90,97%Pharmavit Rt. Bristol Meyers Squibb (USA) 99,9%Richter Gedeon Rt. Külföldi pénzügyi befektetők 59,92%ÁPV Rt. 27,11%
Gyógyszergyártás MagyarországonMagyarországi gyógyszergyártás napjainkbanA gyógyszergyártás Magyarországon főként generikumok (az eredetikészítmény szabadalmának lejárta után bárki által szabadon gyárthatógyógyszer) gyártására szakosodott, azonban emellett a hazai gyártók nagyhangsúlyt fektetnek az eredeti vegyületek, az ún. originális molekulák,hatóanyagok kutatására, illetve a különböző kémiai eljárások fejlesztésére is. Amagyar gyógyszeripar legalább 20 originális gyógyszer kifejlesztésévelbüszkélkedhet. Többségüket Magyarországon és a közép-kelet-európaiországokban hozták forgalomba, egy részüket azonban stratégiai partnerekkelközösen fejlesztették ki és vezették be, például az USA-ban, Nyugat Európábanés Japánban. Mivel az originális fejlesztés sok időt (10-12 év) és rengeteg pénzt(kb. 900 millió Eur/ készítmény) emészt fel, ilyen tevékenységet legtöbbszörcsak tőkeerős partnerrel együttműködve lehet végezni.
Gyógyszergyártás MagyarországonA generikus gyógyszerEgyes elnevezésekben "másolt gyógyszer" vagy "hasonmás gyógyszer" néven is ismert.Az originális gyógyszer termékszabadalmi oltalmának lejárta után gyártott, az originálisgyógyszerrel azonos hatóanyagú készítményeket nevezzük generikus gyógyszernek. Agenerikus gyógyszerek tehát az originális gyógyszerek másolatai. A generikusgyógyszerek kifejlesztése az innovatív, originális gyógyszerek kifejlesztésének töredékébekerül, hiszen az innovatív gyógyszercég már elvégezte a szükséges állatkísérleteket és azemberi kipróbálást. Ezeket nem kell a generikus cégnek megismételnie - e helyett azt kelligazolnia, hogy a generikus gyógyszer az originálissal biológiailag egyenértékű - ezkisszámú betegen vagy egészséges önként jelentkezőn végzett vizsgálatokat igényel. Atermék-szabadalmi oltalom mindig a hatóanyagra vonatkozik. 1994-tőlMagyarországon is termékszabadalmi oltalom van érvényben.
A gyógyszerkutatás mai helyzeteA gyógyszerkutatás rendkívül komplex tevékenység, egy-egy gyógyszertermékkidolgozásában közel 200 különböző szakterület vesz részt, több mint 10 évet veszigénybe. A kutatás és fejlesztés legerősebb motivációja az új terápiák kereséséből indulki. Jelenleg a szakértők szerint a 30 ezer ismert kórképből csak 12 ezer kezelhetőgyógyszeresen. Jelentős motiváció a más gyógyszer-előállítókkal való verseny is, ami igazmind kutatásorientáltnak is nevezett originális, mind a generikus gyártókra.Az innovációs folyamat lépéseipreklinikai kutatás preklinikai fejlesztés klinikai-farmaklológiaikutatásA gyógyszertervezés jelentőségeszéleskörű klinikai vizsgálatok„drug design”: egy receptor, egy enzim vagy egy DNS-szekvencia aktív helyénekpontos térszerkezetét ismerve, olyan hatóanyagot kell konstruálnunk, amelyegzakt komplementer módon erre az aktív helyre illik.A gyógyszerek előállításaJelenleg a gyógyszerek előállításában a klasszikus kémiai módszerek kb. 75 %-kal részesednek. A jövő a biotechnológiai eljárásoké? Csak akkor, ha azok abiotechnológiailag előállítható gyógyszerek terápiás értékben felülmúlják akémiai úton előállítottakat.
A gyógyszerkutatás mai helyzeteA gyógyszeres terápia kockázata, költségek növekedéseContergan botrány (‘50-es évek vége) társadalom követelése: minimálisegészségügyi kockázat preklinikai, klinikai vizsgálatokkal kapcsolatoskövetelmények drámai növekedése a szabadalmi bejelentés és az újgyógyszer forgalomba hozatala közötti időtartam az elmúlt 30 évben a 3-szorosára nőtt K+F (kutatási+fejlesztési tevékenység) költségei nagymértékben nőttek a gyógyszerkutatás azokra projektekre koncentrálódik,ahol rövid a fejlesztési idő, ill. ahol jelentős piacok várhatók! új gyógyszerekre éppen a ritka betegségek (kis felvevő piac) és a krónikusbetegségek (ált. hosszú fejlesztési idő) vonatkozásában van szükség!Fejlesztési költségekA legújabb vizsgálatok szerint egy új gyógyszer fejlesztésének átlagosköltsége 874 millió euró. Ez 247%-a az 1987 évinek. A hatalmas emelkedés okaia klinikai vizsgálatok iránti fokozott biztonsági követelmények, másrésztegyre több kísérleti személyt tesztelnek több vizsgálati központban.A gyógyszercégeknek gyakran 10-30 ezer különböző anyagot kellkikísérletezniük és letesztelniük ahhoz, hogy közülük egyből piaci termékváljék.A hosszan tartó fejlesztési folyamat során az alapkutatásban azonosítottvegyületeket preklinikai és klinikai vizsgálatok alá kell vetni. Többségükfennakad a szigorú vizsgálati kritériumainkon; a továbbjutók azonban a jobb
Az innovációs folyamat lépéseiAlapkutatásAz alapkutatásban dolgozó biokémikusok és molekuláris vagy sejtbiológusok – ahumán megbetegedések kórélettanának ismeretében – azonosítják a kutatási ésgyógyszeres célpontokat:•A kutatás a normális és kóros szervi működések tanulmányozásával kezdődik.•A betegségnek minden jellemzőjét – tüneteit, okait, az érintett szervet és a biokémiaimechanizmusokat – megvizsgálják.•A korábbi kutatásokból és közleményekből nyert információ felhasználásávalmeghatározzák azt a lépést, melynél a betegség progressziója vagy kialakulásameggátolható – ez a kutatás terápiás célpontja.•Olyan vegyületet keresnek, mely hatással van a célpontra. A vegyületeket kémiaiszintézissel, biológiai szintézissel vagy számítógépes szimulációval állítják elő.•Izolálják a vegyületet.•Állatkísérleteket végeznek a vegyület toxicitására és karcinogenitására vonatkozóbiztonságossági adatok megállapítása céljából.Hatósági jóváhagyást szereznek a humán vizsgálatokra.
Az innovációs folyamat lépéseiKlinikai kutatásokA klinikai vizsgálatok nagyszabásúak és összetettek. Egy új gyógyszer klinikaivizsgálatában részt vevő betegek száma a 80-as évekre jellemző 1300-ról mára 4000 főreemelkedett egy tipikus esetet figyelembe véve. A mérni kívánt paraméterek növekvőbonyolultságát jelzi az is, hogy a vizsgálatokban részt vevő betegeken végrehajtott orvosibeavatkozások – például vérvételek és egyéb mérések – száma a 90-es évek elejérejellemző 100-ról mára már 140-re emelkedett.I. fázis: Biztonságosság20-100 egészséges önkéntes kb. 1 hónapon át szedi a gyógyszert.Célja: Információgyűjtés a különböző dózisokban adott gyógyszer felszívódásáról ésmetabolizmusáról, a szervekre és szövetekre gyakorolt hatásáról, ill. mellékhatásairól.II. fázis: HatásosságTöbb száz önkéntes beteg (a vizsgált betegségben szenvedő egyén) bevonásával zajlik.Célja: Az adott betegség kezelésére alkalmazott gyógyszer hatékonyságának és a rövidtávú melléhatásoknak a megismerése.
Az innovációs folyamat lépéseiIII. fázis: Kiterjedt vizsgálatokTöbb száz vagy több ezer – kezelt és kontrollcsoportba sorolt – önkéntes betegbevonásával zajlik.Célja: A gyógyszer kockázat/haszon-arányának, valamint a kevésbé gyakori és a hosszabbtávon kialakuló mellékhatásainak megismerése, a gyógyszer alkalmazási előírásánakmegfogalmazása.IV. fázis: Folyamatos megfigyelésNagy számú beteg bevonásával zajlik, rendszerint a gyógyszer törzskönyvezése után ajóváhagyott indikációban.Célja: A jóváhagyott indikációban történő alkalmazás támogatása; a biztonságosság éshatásosság igazolása az új indikációkban; új hatáserősségű kiszerelések vizsgálata;valamint hosszú távú biztonságossági adatok összegyűjtése és elemzése.
FarmakológiaFarmakokinetika és -DinamikaPaul Erlich (a farmakológia tudományosmegalapozója): A gyógyszerhatás a szervezetés a gyógyszer kölcsönhatásán alapuló kémiaiinterakció.„Corpora non agunt nisi fixata”;gyógyszerkötődés nélkül nincs gyógyszerhatás1854-1915A farmakológia (gyógyszerhatástan) a kémiai anyagok (gyógyszerek) és az emberiszervezet kölcsönhatásával foglalkozó tudomány.Farmakodinamika: a gyógyszer hatása a szervezetreFarmakokinetika: a szervezet időbeni hatása a gyógyszerre (felszívódás /abszorpció/,megoszlás /disztribúció/, metabolizmus és kiválasztás /exkréció/)
FarmakológiaA farmakológia alaptörvénye: a hatás kiváltásához a gyógyszernek kapcsolódnia kell asejtek felszínén (sejtmembránban) vagy belsejében elhelyezkedő makromolekulákhoz(fehérjékhez), amelyeket receptoroknak nevezünk.A kapcsolódás következtében megváltozik a receptor konformációja vagytöltéseloszlása, és ez a történések láncolatát, a farmakológiai választ indítja el asejtben.A sejtmembrán mozaikmodelljeA biológiai membránmozaik felépítésű, bimolekulárislipidrétegből áll.Nem merev struktúrainkább folyadék konzisztenciájú.A lipidrétegben amembránt átérő fehérjemolekulák és lipoproteinekvannak, amelyek amembrán mindkét oldalánpoláris csoportokat istartalmaznak.
FarmakológiaA receptorok fiziológiás körülmények között a szervezet endogén anyagaira reagálnak.Endogén kémiai anyagokIngerületátvivő (transzmitter)molekulák;olyan vegyületek amelyek azidegvégződésekből szabadulnakfel, és a szinaptikus résenátdiffundálva kötődnek areceptor molekulákhoz ésaktiválják azokat, és így olyanposztszinaptikus változásoksorozatát indítják el amely pl.izomösszehúzódást vált ki.Hormonok;felszabadulásukat követően avéráramba jutnak, és fiziológiaihatásukat a megfelelő, hormonspecifikusreceptort tartalmazószöveten fejtik ki.
FarmakológiaIngerületátvivő anyagok<strong>OH</strong>OON<strong>OH</strong>HO<strong>OH</strong>(R)NH 2HO<strong>OH</strong>NH 2acetilkolin (ACh)L-noradrenalin (NA)dopamin (DA)NH 2HONHH 2 NO<strong>OH</strong>HOOO(S)NH 2<strong>OH</strong>szerotonin (5HT)g-amino-vajsav (GABA)L-glutaminsav (Glu)
HormonokHOIO<strong>OH</strong>IOIOI H 2 N <strong>OH</strong><strong>OH</strong><strong>OH</strong>HH<strong>OH</strong>Oinzulin tiroxin kortizol<strong>OH</strong>OO<strong>OH</strong>H<strong>OH</strong>HHH HH HH H<strong>OH</strong>Oaldoszteron tesztoszteron ösztradiol<strong>OH</strong>
FarmakológiaHormonokNH 2N NH 2 HOCO<strong>OH</strong>HNNHhisztamin szerotonin prosztaglandinok
A gyógyszer-receptor kapcsolat tulajdonságaiA gyógyszer-receptor kapcsolat az ismert kémiai kötések révén jön létre:1. Kovalens kötés; ritka, a szervezet hőmérsékletén stabil kötés bontása csakenzimatikus úton lehetséges irreverzíbilis gyógyszer-receptor kapcsolat végérvényesen tönkreteszi a receptort. Pl.: alkilező, daganatkemoterápiás vegyületek(nitrogén-mustár-származékok)ClRNR = MeClClClNn = 3(CH 2 )n CO<strong>OH</strong>mechlorethaminechlorambucil2. Ionos kötés; a makromolekulák sok a szervezet pH-ján ionizálódó csoporttalrendelkeznek (amino-, karboxil-, hidroxil-, foszforilcsoport) elektrosztatikusinterakciókra ad lehetőséget a gyógyszer és receptor között3. Hidrogénhídkötés; energiája kicsiny, de sok ilyen kapcsolat létrejöhet a gyógyszer ésreceptor között összességében jelentős, reverzíbilis kötési energiát képvisel4. Van der Waals-kötés; csak akkor jön létre ha a gyógyszer és receptor között szorosilleszkedése alakul ki csak nagyon szelektív, egymást kiegészítő szerkezetek estébenjöhet létre (kulcs-zár)
A gyógyszer-receptor kapcsolat tulajdonságaiA gyógyszerek az endogén ligandumokhoz fennálló kémiai szerkezeti hasonlóságukalapján hatnak a receptorokon, az endogén anyag által regulált (szabályozott) fiziológiaifolyamatot indítják el vagy gátolják.Agonisták: azok a vegyületek , ill. gyógyszerek, amelyek a receptort aktiválva hozzáklétre a választ.Antagonisták: azok a molekulák, gyógyszerek, amelyek kacsolódnak ugyan areceptorhoz, de nem aktiválják azt. Az antagonisták csökkentik az agonistákreceptorkötődési esélyeit, és ezzel csökkentik, vagy meggátolják azok hatását.
A gyógyszer-receptor kapcsolat tulajdonságaiTeljes agonisták az adott receptoron maximális biológiai hatást váltanak ki.Részleges (parciális) agonisták szintén kötődnek és aktiválják a receptorokat, de nemképesek azt a biológiai hatást létrehozni, mint a teljes agonisták. Teljes agonistajelenlétében a parciális agonisták kompetitív antagonistaként viselkednek, mert a teljesagonista hatását csökkentik azáltal, hogy versenyeznek a receptorkötődési helyekért.Dózis-hatás görbeLog dózis-hatás görbe
A gyógyszer-receptor kapcsolat tulajdonságaiA parciális agonista hatás lehetséges magyarázataagonistareceptoragonista/receptorkomplexközvetítőagonista/receptorközvetítő komplexk 1+ +válaszk -1K A = k 1 /k -1K A : affinitás (intermolekuláris erők)Belső hatékonyságK AR = az AR komplexaffinitása a közvetítőhözAz affinitás (K A ) a vegyület receptorhoz való kötődésének a mértéke. Az agonistaamellett, hogy affinitást mutat a receptorhoz, rendelkezik egy másik belső (intrinsic)hatékonyságnak nevezett kémiai tulajdonsággal is, amely a receptorhoz kötődőagonista választ kiváltó (receptor konformációt megváltoztató) képessége. Ezt másszóval az agonista-receptor komplex közvetítő molekulához való affinitásaként (K AR )definiálhatjuk.Az agonista hatás tehát az agonista-receptor komplexnek a közvetítő (transducer)molekulához való affinitásától is függ. A parciális agonisták esetében ez az affinitás (K AR )kisebb, és ezért nem tudnak teljes hatást kiváltani.
A gyógyszer-receptor kapcsolat tulajdonságaiA kompetitív antagonisták reverzibilisen kötődnek a receptorokhoz, hatásosancsökkentik a receptor koncentrációt, a szöveti válasz az agonista koncentrációjánaknövelésével a normális szintre visszaállítható a log dózis-hatásgörbe jobbra,párhuzamosan tolódik el, úgy hogy a maximális válasz nem csökkenAz irreverzíbilis antagonisták csökkentik a maximális választ. Alacsonykoncentrációjuk esetén azonban a log dózis-hatás görbe jobbra történő párhuzamoseltolódása a maximális válasz csökkenése nélkül is bekövetkezhet létezik ún.receptortartalékAntagonisták hatásai
GyógyszerekGyógyszernek tekintünk minden olyan anyagot, amelyet• az élő szervezet befolyásolására gyógyászati céllalalkalmazunk• a betegség megállapítása céljából az élő szervezetbejuttatunk, vagy•A betegség megelőzése céljából használunkprevenció + diagnózis + terápiaA beteg azt mondja: Fáj a torkom!Erre az orvos:Kr.e. 2000: Tessék, edd meg ezt a gyökeret!Kr.u. 1000: Az a gyökér pogány dolog, mondj el egy imát!Kr. u. 1850: Az ima babonaság, idd meg ezt az elixírt!Kr. u. 1940: Az az elixír kígyóolaj, nem tesz jót, nyeld le ezt a pirulát!Kr. u. 1985: Az a pirula hatástalan, vedd be ezt az antibiotikumot!Kr. u. 2008: Az az antibiotikum nem természetes! Tessék itt egy gyökér…
GyógyszerekGyógyszerek felosztásaEredetük szerintásványi ( NaCl)állati (csukamájolaj, méhviasz)növényi (kamilla, csipkebogyó)szintetikus (kémiai, mikrobiológiai)félszintetikus (természetes alapanyagból)Felhasználási terület alapjánembergyógyászatiállatgyógyászatiPhCH 2 CONHONSPenamecillinMaripenCOOCH 2 OCOCH 3Hatásuk szerint (ld. később)<strong>Kémiai</strong> szerkezet alapjánpl.: penicillinek, szteroidok, fehérjék, benzodiazepinekAlkalmazás módja alapjánGyógyszerforma: a hatóanyagból megfelelő technológiaieljárással közvetlen felhasználásra alkalmas készítmény
GyógyszerekA gyógyszerformák alkalmazási helye és módjaalkalmazási hely alkalmazási mód gyógyszerformaszájüreg orális (szájban, pl. nyelv) szublingvális tablettaszájon át a gyomor-béltraktusvégbélper os, vagyis orálisalkalmazásper rectum, vagyis rektálisalkalmazásoldatok, pirulák, drazsék,stb.végbélkúpokhüvely (vagina) vaginális hüvelykúpizom és bőr alattikötőszövetintramuszkuláris ésszubkutáninjekciós oldatvivőér (véna) intravénás injekció vagy infúziótüdő inhaláció inhalasolum, aerosolumbőr felület kenőcs,paszta,rázókeverék
GyógyszerekA gyógyszer megítéléseHatás szélesség (jó ha nagy!): káros következmény nélkül még eltűrhető adag – gyógyítóadagHatáserősség: az ED 50 (effektív dózis) értékkel jellemezzük. Az ED 50 megadja azt a dózist,amely a maximális hatás 50%-át hozza létre. Az ED 50 érték jól használható azonosindikációban használt gyógyszerek összehasonlítására. Ha egy gyógyszernek kisebb azED 50 értéke, akkor ugyanazt a hatáserősséget kisebb koncentrációban tudja létrehozni,vagyis adott szerből kevesebbet kell a betegnek fogyasztania.Terápiás index (jó ha nagy!): Ha egy gyógyszert a terápiában használnak fontosmegállapítani azt a koncentráció sávot, ahol az adott szer kiváltja a kívánt hatást és mégnem okoz veszélyes mellékhatást. Az ED 50 analógiájára bevezethetjük a TD 50 (toxikusdózis) értékét is, amely a kísérleti állatok 50%-ban vált ki egy toxikus hatást. A terápiásindex a TD 50 és az ED 50 aránya. A vegyületek használhatóságát korlátozza, ha terápiásindexük kicsi, hiszen ilyenkor a dózis kis mértékű változása már toxikus hatást válthat ki.
FarmakokinetikaA gyógyszerek sorsa a szervezetben I.• Liberáció (felszabadulás a gyógyszerformából)• Felszívódás (abszorpció)Ha a gyógyszer nem az alkalmazás helyén fejti ki a hatását, először be kell jutniaa véráramba, hogy a keringés révén eljusson a hatás helyére. Az alkalmazáshelyéről a vérbe jutás folyamatát nevezzük felszívódásnak.A gyógyszerek felszívódása történhet: szájüregből; gyomorból; belekből;tüdőből; bőr felületéről, ill. parenterális felszívódás (izomba, bőr alattikötőszövetbe, intravénásan adott injekció)• Eloszlás (disztribúció)Eloszláson azt a folyamatot értjük, amikor a gyógyszer a vérkeringésből a hatáshelyére (szövetekbe) jut.A gyógyszerek nem egyenletesen oszlanak el a szervezetben, hanem az egyesszervekben szelektív felhalmozódásuk tapasztalható. Ez a szervek szövettani,kémiai felépítésétől, és részben a vérellátásától függ.A felszívódás és az eloszlás során a gyógyszermolekuláknak biológiaibarriereken, membránokon kell átjutniuk.
FarmakokinetikaA gyógyszerek sorsa a szervezetben II.• Metabolizáció (biotranszformáció)A metabolizmus a vegyületek kémiai szerkezetét és fizikai-kémiai tulajdonságátmegváltoztató folyamat. Ált. csökkenti vagy megszünteti a gyógyszerhatást, de vanolyan eset is amikor a metabolit hatékonyabb, mint az eredeti vegyület. Ilyenkor aterméket aktív metabolitnak nevezzük, a beadott gyógyszer neve pedig prodrug (L-DOPA /3,4-dihidroxi -(L)-fenilalanin / dopamin)A metabolizmus, ha nem is mindig inaktivál, mindig fokozza a vegyületek polaritását(vízoldékonyságát) és ezáltal növeli a kiürülés esélyét. A gyógyszerekbiotranszformációját ún. gógyszer-metabolizáló enzimek végzik.A biotranszformáció lehet: oxidáció, redukció, hidrolízis, izomerizáció, hidratáció,konjugáció a szervezet endogén anyagaival stb.A gyógyszer-metabolizmus fő szerve a máj, de más szervek mint pl. a gyomor-béltraktus és a tüdő is számottevő metabolikus aktivitású.• Elimináció (kiürülés a szervezetből)A kiürülés a végleges megszabadulást jelenti az idegen anyagoktól. Fontos szerepetjátszik benne a vese, az epe, a bélcsatorna. Kisebb jelentőségű a tüdő, a nyál, azizzadságmirigyek és a tejmirigyek szerepe.A gyógyszerhatás megszűnéséért a metabolizmus és a kiürülés a felelős.