AGGIORNAMENTO NOTE LIMITATIVE AIFA Nota n. 1 ... - ASL CN1
AGGIORNAMENTO NOTE LIMITATIVE AIFA Nota n. 1 ... - ASL CN1
AGGIORNAMENTO NOTE LIMITATIVE AIFA Nota n. 1 ... - ASL CN1
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
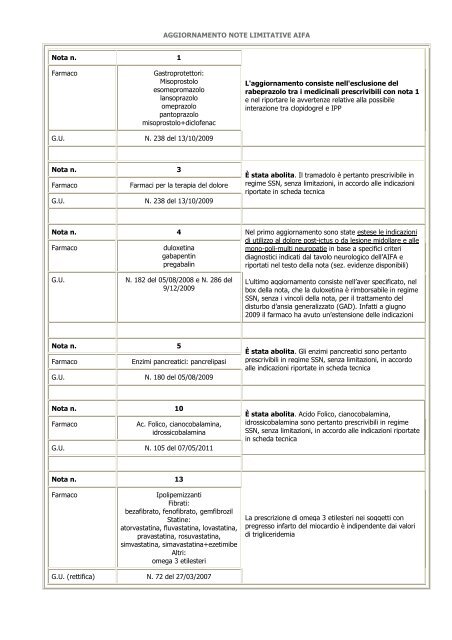
<strong>Nota</strong> n. 1<br />
Farmaco Gastroprotettori:<br />
Misoprostolo<br />
esomepromazolo<br />
lansoprazolo<br />
omeprazolo<br />
pantoprazolo<br />
misoprostolo+diclofenac<br />
G.U. N. 238 del 13/10/2009<br />
<strong>Nota</strong> n. 3<br />
Farmaco Farmaci per la terapia del dolore<br />
G.U. N. 238 del 13/10/2009<br />
<strong>Nota</strong> n. 4<br />
Farmaco duloxetina<br />
gabapentin<br />
pregabalin<br />
G.U. N. 182 del 05/08/2008 e N. 286 del<br />
9/12/2009<br />
<strong>Nota</strong> n. 5<br />
Farmaco Enzimi pancreatici: pancrelipasi<br />
G.U. N. 180 del 05/08/2009<br />
<strong>Nota</strong> n. 10<br />
Farmaco Ac. Folico, cianocobalamina,<br />
idrossicobalamina<br />
G.U. N. 105 del 07/05/2011<br />
<strong>Nota</strong> n. 13<br />
<strong>AGGIORNAMENTO</strong> <strong>NOTE</strong> <strong>LIMITATIVE</strong> <strong>AIFA</strong><br />
Farmaco Ipolipemizzanti<br />
Fibrati:<br />
bezafibrato, fenofibrato, gemfibrozil<br />
Statine:<br />
atorvastatina, fluvastatina, lovastatina,<br />
pravastatina, rosuvastatina,<br />
simvastatina, simavastatina+ezetimibe<br />
Altri:<br />
omega 3 etilesteri<br />
G.U. (rettifica) N. 72 del 27/03/2007<br />
L'aggiornamento consiste nell'esclusione del<br />
rabeprazolo tra i medicinali prescrivibili con nota 1<br />
e nel riportare le avvertenze relative alla possibile<br />
interazione tra clopidogrel e IPP<br />
È stata abolita. Il tramadolo è pertanto prescrivibile in<br />
regime SSN, senza limitazioni, in accordo alle indicazioni<br />
riportate in scheda tecnica<br />
Nel primo aggiornamento sono state estese le indicazioni<br />
di utilizzo al dolore post-ictus o da lesione midollare e alle<br />
mono-poli-multi neuropatie in base a specifici criteri<br />
diagnostici indicati dal tavolo neurologico dell’<strong>AIFA</strong> e<br />
riportati nel testo della nota (sez. evidenze disponibili)<br />
L’ultimo aggiornamento consiste nell’aver specificato, nel<br />
box della nota, che la duloxetina è rimborsabile in regime<br />
SSN, senza i vincoli della nota, per il trattamento del<br />
disturbo d’ansia generalizzato (GAD). Infatti a giugno<br />
2009 il farmaco ha avuto un’estensione delle indicazioni<br />
È stata abolita. Gli enzimi pancreatici sono pertanto<br />
prescrivibili in regime SSN, senza limitazioni, in accordo<br />
alle indicazioni riportate in scheda tecnica<br />
È stata abolita. Acido Folico, cianocobalamina,<br />
idrossicobalamina sono pertanto prescrivibili in regime<br />
SSN, senza limitazioni, in accordo alle indicazioni riportate<br />
in scheda tecnica<br />
La prescrizione di omega 3 etilesteri nei soggetti con<br />
pregresso infarto del miocardio è indipendente dai valori<br />
di trigliceridemia
<strong>Nota</strong> n. 36<br />
Farmaco Testosterone<br />
G.U.<br />
N. 270 del 22/11/2010<br />
<strong>Nota</strong> n. 39<br />
Farmaco Ormone della crescita (somatropina)<br />
G.U.<br />
N. 238 del 13/10/2009<br />
N. 286 del 9/12/2009<br />
N. 270 del 18/11/2010<br />
<strong>Nota</strong> n. 42<br />
Farmaco Bifosfonati:<br />
acido etidronico<br />
acido clodronico<br />
G.U. N. 238 del 13/10/2009<br />
<strong>Nota</strong> n. 55<br />
Farmaco Antibiotici iniettabili per uso extraospedaliero:<br />
ceftazidime<br />
cefepime<br />
mezlocillina<br />
piperacillina<br />
ampicillina-sulbactam<br />
piperacillina+tazobactam<br />
amikacina<br />
gentamicina<br />
netilmicina<br />
tobramicina<br />
G.U. N. 238 del 13/10/2009<br />
- Eliminato il principio attivo metiltestosterone<br />
- Specificata la tipologia di ipogonadismi primitivi e<br />
secondari che devono essere caratterizzati da “ridotte<br />
concentrazioni di testosterone totale (< 12 nmoli/L o 350<br />
mg/dl), in presenza di sintomi tipici (riduzione desiderio e<br />
potenza sessuale, osteoporosi, riduzione forza muscolare,<br />
obesità viscerale, alterazioni del tono dell’umore)”<br />
- Eliminata la condizione di pubertà ritardata<br />
Nella prima revisione sono state estese le indicazioni<br />
dell’età evolutiva includendo i bambini nati piccoli per l’età<br />
gestazionale (GSA) con età ≥ a 4 anni (autorizzazione al<br />
trattamento per 2 anni e relativo monitoraggio) ed è stata<br />
introdotta l’età di transizione<br />
Nella seconda revisione sono state riportate modifiche al<br />
testo in riferimento al trattamento dei soggetti prepuberi<br />
affetti dalla sindrome di Prader Willi (PWS).<br />
Nella terza revisione è stat inserita l’età neonatale, in<br />
individui con evidenza neuroradiologica di<br />
malformazioni/lesioni ipotalamo-ipofisarie e segni clinici<br />
laboratoristici compatibili con la diagnosi di<br />
panipopituitarismo congenito<br />
L’aggiornamento consiste nell’aver aggiunto, nella sezione<br />
particolari avvertenze, la seguente frase: “Di recente,<br />
l’Advisory Committee dell’FDA ha pubblicato un warning<br />
circa l’eventuale insorgenza di dolore severo, talora<br />
disabilitante, a livello osseo, articolare o muscolare<br />
associato alla assunzione di bifosfonati. Tale<br />
sintomatologia differisce dalla sindrome acuta similinfluenzale<br />
(acute-phase reaction APR) caratterizzata da<br />
febbre, raffreddore, dolore osseo, artralgia e mialgia che<br />
comunemente si osserva in seguito a somministrazione<br />
endovenosa dei bifosfonati iniettabili"<br />
Sono state tolte tutte le cefalosporine di II generazione e<br />
tra quelle di III/IV sono rimaste solo ceftazidime e<br />
cefepime<br />
La prescrizione a carico del SSN è limitata alle seguenti<br />
condizioni:<br />
-trattamento iniettivo di infezioni gravi delle vie<br />
respiratorie, delle vie urinarie, dei tessuti molli, intraaddominali,<br />
ostetrico-ginecologiche, ossee e articolari;<br />
-trattamento iniettivo delle infezioni causate da<br />
microrganismi resistenti ai più comuni antibiotici,<br />
particolarmente nei pazienti immunocompromessi
<strong>Nota</strong> n. 56<br />
Farmaco Antibiotici per continuità<br />
ospedale-territorio<br />
Aztreonam<br />
ertapenem<br />
imipinem+ cilastatina<br />
meropenem<br />
rifabutina<br />
teicoplanina<br />
G.U. N. 268 del 17/11/2009<br />
<strong>Nota</strong> n. 57<br />
Farmaco Antiemetici (antagonisti dei recettori<br />
serotoninegici)<br />
G.U. n. N.180 del 05/08/2009<br />
<strong>Nota</strong> n. 59<br />
Farmaco Lattilolo, lattulosio<br />
G.U. n. N.104 del 07/05/2011<br />
<strong>Nota</strong> n. 65<br />
Farmaco Farmaci per la sclerosi multipla:<br />
glatiramer acetato<br />
interferoni beta 1a e beta 1b<br />
ricombinanti<br />
G.U. N. 182 del 05/08/2008<br />
N. 75 del 31/03/2009<br />
<strong>Nota</strong> n. 74<br />
Farmaco Farmaci per l’infertilità femminile e<br />
maschile:<br />
follitropina α ricombinante<br />
follitropina β ricombinante<br />
lutropina α<br />
menotropina<br />
urofollitropina<br />
follitropina α + lutropina α<br />
coriogonadotropina α<br />
G.U. N. 81 del 05/04/2008,<br />
N. 156 del 08/07/2009,<br />
N.113 del 17/05/2010<br />
La variazione è di tipo formale; nella sezione "evidenze<br />
disponibili" al punto 2) è stato riportato:<br />
monobattami (aztreonam); efficaci verso i soli gramnegativi<br />
“difficili”<br />
anzichè<br />
farmaci efficaci verso i soli gram-negativi “difficili", simili,<br />
nei riguardi di questi, alle cefalosporine di III e IV<br />
generazione (aztreonam)<br />
È stata abolita. Gli antagonisti dei recettori<br />
serotoninergici sono pertanto prescrivibili in regime SSN ,<br />
senza limitazioni, in accordo alle indicazioni riportate in<br />
scheda tecnica<br />
È stata abolita. Lattulosio e lattilolo sono pertanto<br />
prescrivibili in regime SSN , senza limitazioni, in accordo<br />
alle indicazioni riportate in scheda tecnica<br />
Nella prima revisione è stato specificato che la sclerosi<br />
multipla recidivante-remittente è diagnosticata secondo<br />
i criteri di Polman (Polman, 2005) con punteggio<br />
sull’Expanded Disability Status Scale (EDSS) tra 1.0 e 5.5<br />
Nella seconda revisione sono state apportate delle<br />
modifiche alle sezioni evidenze disponibili e bibliografia.<br />
Rispetto alla nota originaria, sono soggetti alla nota 74<br />
anche l’associazione follitropina α + lutropina α<br />
(Pergoveris) entrata in commercio nel 2008 e la<br />
coriogonadotropina α (Ovitrelle) che è stata riclassificata<br />
in fascia A a luglio 2009<br />
L’ultima modifica riguarda l'integrazione dell'indicazione<br />
all'utilizzo dei farmaci per il trattamento dell'infertilità<br />
maschile. Nella nota è specificato che il trattamento va<br />
effettuato " in maschi con ipogonadismo-ipogonadotropo<br />
con livelli di gonadotropine bassi o normali o comunque<br />
con FSH non superiore a 8 mUI/ml."
<strong>Nota</strong> n. 75<br />
Farmaco Farmaci per la disfunzione erettile:<br />
alprostadil<br />
sildenafil<br />
vardenafil<br />
tadalafil<br />
G.U. N. 279 del 29/11/2010<br />
<strong>Nota</strong> n. 76<br />
Farmaco Ferrico gluconato, ferromaltoso,<br />
ferroso gluconato, ferroglicinalsolfato<br />
G.U. N. 106 del 09/05/2011<br />
<strong>Nota</strong> n. 78<br />
G.U. N.284 del 04/12/2010<br />
<strong>Nota</strong> n. 79<br />
Farmaco Bifosfonati:<br />
ac. alendronico<br />
ac. risedronico<br />
ac. ibandronico<br />
ac. Alendronico vitamina D3<br />
ac. zoledronico<br />
raloxifene<br />
ranelato di stronzio<br />
teriparatide<br />
ormone paratiroideo<br />
G.U. N. 150 del 01/07/2009<br />
N. 180 del 05/08/2009<br />
<strong>Nota</strong> n. 83<br />
Farmaco Sostituti lacrimali<br />
G.U. N. 286 del 09/12/2009<br />
La prescrizione di alprostadil a carico del SSN è limitata ai<br />
pazienti con disfunzione erettile da lesioni permanenti e<br />
complete del midollo spinale o del plesso pelvico<br />
iatrogene, traumatiche o infiammatorie/degenerative.<br />
La prescrizione di inibitori della PDE5 (sildenafil, tadalafil,<br />
vardenafil) a carico del SSN è limitata ai pazienti con<br />
disfunzione erettile da danno transitorio o parziale del<br />
midollo spinale o del plesso pelvico secondo un piano<br />
terapeutico specialistico (andrologo, endocrinologo,<br />
neurologo o urologo)<br />
È stata abolita. Ferrico gluconato, ferromaltoso, ferroso<br />
gluconato, ferroglicinalsolfato sono pertanto prescrivibili in<br />
regime SSN , senza limitazioni, in accordo alle indicazioni<br />
riportate in scheda tecnica<br />
Abolita dal 5/12/2010<br />
I colliri antiglaucoma di cui alla ex nota 78 sono pertanto<br />
prescrivibili in regime SSN , senza limitazioni, in accordo<br />
alle indicazioni riportate in scheda tecnica<br />
Nella prima revisione sono state estese le indicazioni della<br />
teriparatide:<br />
Soggetti di età superiore a 50 anni in trattamento da più<br />
di 12 mesi con dosi > 5 mg/die di prednisone o dosi<br />
equivalenti di altri corticosteroidi e che si presentano con<br />
una frattura vertebrale severa o due fratture vertebrali<br />
moderate.<br />
La nota si applica su diagnosi e piano terapeutico, della<br />
durata di 6 mesi prolungabile di ulteriori periodi di 6 mesi<br />
per non più di altre due volte (per un totale complessivo<br />
di 18 mesi), di centri specializzati, Universitari o delle<br />
Aziende Sanitarie, individuate dalle Regioni e dalle<br />
Province autonome di Trento e Bolzano<br />
Nella seconda revisione è stato eliminato l'acido<br />
zolendronico dall'elenco dei principi attivi, erroneamente<br />
inserito nella precedente versione<br />
È stata aggiunta, nella sezione background, la frase:<br />
"Il carbopol è un polimero che ha dimostrato una certa<br />
efficacia nel trattamento della xeroftalmia di pazienti<br />
affetti da malattia di Sjögren”
<strong>Nota</strong> n. 85<br />
Farmaco Inibitori dell'acetilcolinesterasi:<br />
donezepil<br />
galantamina<br />
rivastigmina<br />
Antagonisti del recettore per il<br />
glutammato:<br />
memantina<br />
G.U. N. 65 del 19/03/2009 e N. 238 del<br />
13.10.2009<br />
<strong>Nota</strong> n. 90<br />
Farmaco Metilnaltrexone<br />
G.U. N. 141 del 20/06/2009<br />
<strong>Nota</strong> n. 91<br />
Farmaco Febuxostat<br />
G.U. N. 265 del 12/11/2010<br />
[ultimo aggiornamento maggio 2011]<br />
Nella prima revisione è stata introdotta la memantina tra<br />
i farmaci rimborsabili per la terapia della malattia di<br />
Alzheimer limitandola al trattamento della malattia di<br />
Alzheimer di grado moderato con MMSE tra 10 e 20.<br />
Donezepil, rivastigmina, galantamina rimangono<br />
prescrivibili nei pazienti con malattia di Alzheimer di grado<br />
lieve, ma sono specificati i valori di MMSE (tra 21 e 26) e<br />
di grado moderato con MMSE tra 10 e 20<br />
La seconda revisione è di tipo formale in quanto hanno<br />
aggiunto la classe farmacologica di appartenenza della<br />
memantina ovvero gli antagonisti del recettore del<br />
glutammato<br />
La prescrizione di metilnaltrexone a carico del SSN è<br />
limitata alle seguenti condizioni:<br />
Costipazione indotta da oppiacei in soggetti con malattia<br />
in stato terminale che rispondano contemporaneamente<br />
alle seguenti caratteristiche:<br />
- terapia continuativa con oppiacei della durata di almeno<br />
di 2 settimane;<br />
- resistenza al trattamento con lassativi ad azione<br />
osmotica per più 3 giorni.<br />
La prescrizione di febuxostat a carico del SSN è limitata<br />
alla seguente condizione:<br />
trattamento dell’iperuricemia cronica con anamnesi o<br />
presenza di tofi e/o di artrite gottosa in soggetti che non<br />
siano adeguatamente controllati con allopurinolo o siano<br />
ad esso intolleranti