Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
NPWT la scelta<br />
delle impostazioni e<br />
delle medicazioni<br />
Introduzione<br />
L’ultimo decennio ha visto un considerevole<br />
aumento dell’uso della terapia a pressione negativa<br />
per le ferite (NPWT). Questa tecnologia innovativa<br />
ha rivoluzionato la cura di molti pazienti con ferite<br />
sia croniche che acute 1,2 . L’ampio ricorso alla NPWT<br />
degli ultimi 15 anni è scaturito più da esperienze<br />
cliniche positive che da studi clinici randomizzati<br />
o da conoscenze scientifiche. Ora tuttavia appare<br />
evidente che, per applicare la NPWT con risultati<br />
ottimali e complicazioni minime, è necessario che<br />
il medico comprenda i meccanismi tramite i quali<br />
la pressione negativa agisce sul letto della ferita,<br />
scegliendo così le medicazioni e le impostazioni di<br />
pressione più appropriate.<br />
Autori: Malmsjö M, Borgquist O.<br />
Informazioni complete sugli autori a pag. 4.<br />
Che cos’è la NPWT?<br />
Nel 1989 Chariker presentò una terapia di drenaggio a pressione<br />
negativa su base di garza per la guarigione delle ferite 3 .<br />
Precedentemente Miller aveva descritto l’uso della NPWT su base<br />
di garza in Unione Sovietica 4 . Nel 1997 la terapia a pressione<br />
negativa per il trattamento delle ferite è stata poi resa popolare<br />
da Argenta e Morykwas, che hanno descritto l’uso di pressione<br />
sub-atmosferica applicata attraverso una struttura porosa in<br />
schiuma di poliuretano per accelerare la guarigione delle ferite,<br />
gettando così le basi per una comprensione scientifica della<br />
terapia 5,6 .<br />
Oggigiorno la NPWT viene usata per il trattamento clinico di vari<br />
tipi di ferite 1 , fra cui traumi ortopedici 7 , traumi dei tessuti molli 8 ,<br />
innesti cutanei 9 , ulcere da pressione 10 , ulcere vascolari 11 , ulcere<br />
del piede diabetico 12 , ustioni 13 ed infezioni chirurgiche 14 , e per la<br />
gestione di altre gravi ferite post-chirurgiche 15-17 .<br />
La NPWT si avvale di un sistema chiuso di drenaggio per<br />
applicare una suzione controllata (vuoto) al letto della ferita.<br />
La perdita di sostanza della ferita viene riempita con un filler<br />
(garza o schiuma) che permette una distribuzione uniforme<br />
della pressione sul letto della ferita, poi ricoperta con una<br />
pellicola aderente di materia plastica. Il tubo di drenaggio viene<br />
quindi collegato ad una pompa che genera pressione negativa.<br />
L’essudato viene aspirato attraverso il tubo di drenaggio e<br />
raccolto in un contenitore.<br />
resa<br />
<strong>facile</strong><br />
Volume 1 | Numero 3 | Maggio 2010 www.woundsinternational.com<br />
Quali sono i meccanismi di azione della<br />
NPWT?<br />
I meccanismi con i quali si ritiene che la NPWT acceleri la<br />
guarigione delle ferite sono i seguenti: la NPWT crea un ambiente<br />
umido 18 , rimuove l’essudato 5,6,19 , riduce l’edema tissutale 20 , causa la<br />
contrazione dei margini della ferita 5,6,19 , fornisce una stimolazione<br />
meccanica del letto della ferita 21-23 , modifica il flusso sanguigno dei<br />
margini della ferita 6,24-26 , stimola l’angiogenesi 27,28 e la formazione<br />
di tessuto di granulazione 6 . Finché la ferita è sigillata, la NPWT è<br />
spesso in grado di fornire protezione contro le infezioni; inoltre<br />
la minore frequenza di cambi di medicazione può contribuire<br />
a ridurre ulteriormente il rischio di contaminazione. Gli effetti<br />
biologici della NPWT sul letto della ferita dipendono dal tipo di<br />
medicazione scelta e dal livello di pressione negativa applicato<br />
(descritto più avanti).<br />
Che cos’è l’interfaccia di ferita?<br />
La medicazione che si trova a diretto contatto con il letto della<br />
ferita, e perciò interagisce con esso, è chiamata interfaccia. Essa<br />
può essere costituita dal filler (di solito schiuma poliuretanica<br />
strutturata o garza imbevuta di soluzione salina) o da uno strato<br />
di contatto a bassa aderenza collocato al di sotto del filler a<br />
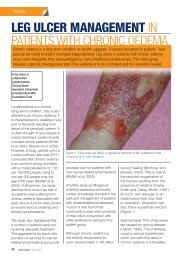
copertura del letto della ferita (Figura 1).<br />
Le proprietà dell’interfaccia di ferita determinano in gran parte<br />
gli effetti esercitati dalla NPWT sul letto della ferita. L’interazione<br />
fra l’interfaccia e il letto della ferita è stata descritta in modo<br />
approfondito per quanto riguarda schiuma e garza 21,29 . Entrambi<br />
questi filler esercitano un’azione meccanica sulla ferita 21 .<br />
La superficie tessutale viene stimolata dalla struttura della<br />
medicazione, e ciò induce una divisione cellulare che ricostituirà e<br />
rafforzerà il tessuto.<br />
Qual è la funzione delle vari tipi di<br />
interfaccia?<br />
Filler di riempimento (solitamente schiuma o garza)<br />
La funzione del filler consiste nel trasmettere la pressione negativa<br />
al letto della ferita. Studi sperimentali indicano che la pressione<br />
viene distribuita altrettanto bene attraverso la schiuma che<br />
attraverso la garza 22 . La forza di suzione generata dalla pressione<br />
negativa porta al drenaggio attivo dell’essudato dalla ferita,<br />
provocando la riduzione di vari composti che possono inibire la<br />
guarigione, ad esempio enzimi proteolitici e metalloproteinasi 30,31 .<br />
È importante collocare il filler a diretto contatto con tutte le aree di<br />
tessuto sulle quali si desidera che agisca la NPWT.<br />
Strato di contatto<br />
Se si prevedono complicanze, al di sotto del filler viene collocato<br />
uno strato di contatto non aderente 32,33 . Lo strato di contatto può<br />
essere posto sopra alle strutture vulnerabili 33 , ma anche sopra<br />
al letto della ferita, dato che si ritiene eviti la proliferazione del<br />
1
tessuto di granulazione all’interno del<br />
filler. È stato infatti dimostrato come<br />
il tessuto del letto della ferita possa<br />
proliferare nella schiuma ma non nella<br />
garza34 . Le complicanze associate alla<br />
proliferazione nella schiuma sono le<br />
seguenti:<br />
■■ dolore nei cambi di medicazione,<br />
perchè il tessuto di proliferazione<br />
viene strappato via dalla ferita35 .<br />
Il dolore richiede spesso un<br />
trattamento drastico36,37 ■■ danneggiamento del letto della<br />
ferita e danno meccanico ai tessuti<br />
quando si rimuove la schiuma<br />
strappandola dal letto della ferita<br />
durante il cambio di medicazione<br />
■■ frammenti residui di schiuma che<br />
rimangono aderenti al letto della<br />
ferita e, se non rimossi, possono<br />
fungere da corpi estranei ed<br />
ostacolare la guarigione della ferita<br />
stessa.<br />
Di quali evidenze si<br />
dispone circa l’uso delle<br />
varie interfacce?<br />
Fino a questo momento, l’evidenza<br />
scientifica riguardante l’effetto biologico<br />
della NPWT sul letto della ferita era<br />
circoscritta all’uso di schiuma di<br />
poliuretano o di garza come filler 21,34,38 .<br />
Pellicola adesiva<br />
A<br />
NPWT la scelta<br />
delle impostazioni e<br />
delle medicazioni<br />
Figura 1 Medicazioni per la NPWT<br />
Schiuma<br />
Tubo di drenaggio<br />
verso la pompa del vuoto<br />
Ferita<br />
Tessuto<br />
resa<br />
<strong>facile</strong><br />
Va ricordato che nella pratica clinica la<br />
schiuma usata nella NPWT viene molto<br />
probabilmente abbinata ad uno strato<br />
di contatto non aderente. Sebbene sia<br />
ben noto che la pressione negativa<br />
viene trasmessa attraverso gli strati<br />
di contatto usati normalmente 39,40 ,<br />
ancora non sono disponibili studi che<br />
esaminino formalmente gli effetti<br />
esercitati dalla combinazione schiuma<br />
e strato di contatto sul letto della<br />
ferita e sulla formazione di tessuto di<br />
granulazione.<br />
Come si sceglie la<br />
medicazione di interfaccia<br />
appropriata?<br />
Paglinawan et al hanno dimostrato che<br />
sia impiegando garza che schiuma si<br />
determina un aumento della formazione<br />
di tessuto di granulazione 38 . In una serie<br />
di casi di ferite trattate con NPWT, il<br />
tasso di guarigione con l’uso di garza<br />
è risultato simile a quello ottenuto<br />
con l’uso di schiuma 41 . Tuttavia stanno<br />
emergendo studi indicanti che la quantità<br />
e la natura del tessuto di granulazione<br />
formatosi possono variare a seconda della<br />
medicazione usata. L’applicazione della<br />
NPWT con interfaccia di schiuma porta alla<br />
formazione di un tessuto di granulazione<br />
spesso ed ipertrofico 21,34,42 . La garza con la<br />
B<br />
Schiuma<br />
Strato di<br />
contatto<br />
C<br />
NPWT produce un tessuto di granulazione<br />
meno spesso ma più denso 21,34 .<br />
Interfaccia di schiuma<br />
Lo spesso tessuto di granulazione che<br />
si forma sotto alla schiuma durante una<br />
NPWT 34,42 può essere talvolta vantaggioso,<br />
ma essere anche fonte di problemi, come<br />
ad esempio la fibrosi, che può provocare<br />
cicatrici e successiva contrazione nel corso<br />
della guarigione 42 .<br />
La schiuma può essere una scelta<br />
opportuna quando si trattano ferite per le<br />
quali uno spesso tessuto di granulazione<br />
può rappresentare un vantaggio mentre<br />
la formazione di cicatrici non costituisce<br />
un problema, ad esempio da fasciotomia<br />
per sindrome compartimentale degli<br />
arti superiori od inferiori, nelle quali la<br />
contrazione è un fenomeno positivo 16,43 . In<br />
ferite acute con ampia perdita di tessuto<br />
la schiuma può rappresentare una terapia<br />
ponte per riavvicinare i margini della<br />
ferita 7,8 .<br />
Interfaccia di garza<br />
La garza viene usata spesso grazie alla sua<br />
adattabilità e facilità di applicazione su<br />
ferite di dimensioni ampie ed irregolari 44 ,<br />
ed ha goduto di un certo favore fra i<br />
chirurghi plastici per la preparazione del<br />
letto della ferita prima di un innesto 45 .<br />
L’ interfaccia di ferita può essere costituita da un filler, di solito schiuma (A e B) o garza (C), o da uno strato di contatto non aderente collocato sotto alla schiuma (B) in<br />
modo da proteggere le strutture più fragili o evitare la proliferazione di tessuto di granulazione nel filler.<br />
Garza<br />
2
La garza può inoltre rappresentare una buona scelta quando i<br />
risultati estetici sono di primaria importanza, o nei casi in cui il<br />
tessuto cicatriziale potrebbe ostacolare i movimenti, ad esempio<br />
sulle giunture. Durante la NPWT il filler viene spinto nella ferita,<br />
ed è stato ipotizzato che la tecnica che prevede l’uso di garza<br />
sottoposta a pressione negativa possa tamponare i sanguinamenti<br />
superficiali 46 .<br />
La garza costituisce un buon filler per ferite, specialmente in<br />
circostanze estreme. L’uso della NPWT con garza è stato descritto<br />
da Jeffery et al, 2009, nel trattamento di personale militare con<br />
ferite causate da mine terrestri ed altri ordigni esplosivi 44 . Non<br />
sono stati segnalati problemi di proliferazione del tessuto di<br />
granulazione nella garza usata con la NPWT 34 e perciò non è<br />
necessario alcuno strato di contatto. Va sottolineato che la garza<br />
usata con la NPWT è stata quasi sempre un tipo particolare<br />
di garza di cotone (Kerlix AMD) 41 che, essendo impregnata di<br />
poliesametilene biguanide (PHMB), può svolgere un’azione di<br />
controllo antimicrobico.<br />
Con quale frequenza va cambiata la<br />
medicazione nella NPWT?<br />
La frequenza di cambio richiesta dipenderà non solo dal tipo<br />
di medicazione usato ma anche dal tipo di ferita. Normalmente<br />
si raccomanda di cambiare le medicazioni di schiuma ogni 48<br />
ore 47,48 . Questa raccomandazione deriva dal fatto che è necessario<br />
cambiare la medicazione di schiuma prima che la proliferazione<br />
diventi un problema 49 .<br />
Con la garza o uno strato di contatto non aderente non è<br />
probabile che si verifichi proliferazione, e perciò i cambi di<br />
medicazione potranno essere meno frequenti. Attualmente si<br />
raccomanda di cambiare le medicazioni di garza due o tre volte<br />
alla settimana 41 .<br />
Quale livello di pressione negativa deve<br />
essere applicato?<br />
Qual è il gold standard per la pressione?<br />
Per ora non esistono linee guida cliniche particolareggiate indicanti<br />
come regolare i livelli di pressione negativa in modo da adattarli<br />
alle singole ferite. Il livello di pressione usato più comunemente<br />
(-125 mmHg) è basato su uno studio limitato su maiali, condotto<br />
nel 1997 6 . Livelli così elevati di pressione negativa possono talvolta<br />
provocare dolore e devono perciò essere ridotti 48,37 .<br />
Studi preclinici hanno indicato che la massima azione biologica<br />
sui margini della ferita, in termini di contrazione 50 , circolazione<br />
regionale 51 e formazione di tessuto di granulazione 21,34 si<br />
ottengono con una pressione di -80 mmHg. Inoltre, gli studi clinici<br />
hanno dimostrato che con livelli di pressione negativa inferiori a<br />
-125 mmHg si è ottenuta un’eccellente guarigione della ferita 52 .<br />
In una serie di casi clinici è emerso che la ferita guarisce con<br />
un decorso simile sia con una pressione di -125 mmHg che di<br />
-75 mmHg 48 .<br />
Che pressione si può applicare in presenza di dolore<br />
o di rischio ischemico?<br />
È noto che negli strati tessutali più superficiali del letto della<br />
ferita il flusso sanguigno risulta ridotto (0,5 cm dal margine<br />
della ferita), mentre aumenta negli strati più profondi (2,5 cm<br />
dal margine) 25,26,51,53 (Figura 2). Il calo di flusso sanguigno è<br />
determinato dal fatto che la medicazione viene spinta contro i<br />
tessuti, comprimendoli 54 . In una ferita senza rischio di ischemia<br />
è probabile che questa combinazione di diminuzione ed<br />
incremento del flusso sanguigno rappresenti un vantaggio ai fini<br />
della guarigione. L’incremento del flusso sanguigno comporta<br />
un miglioramento dell’apporto di ossigeno e nutrienti ai tessuti,<br />
migliorando anche la penetrazione degli antibiotici e la rimozione<br />
dei prodotti di scarto. La riduzione stimola invece l’angiogenesi,<br />
che a sua volta favorisce la formazione di tessuto di granulazione.<br />
Se il paziente lamenta dolore, oppure se il tessuto è scarsamente<br />
irrorato (ad esempio nelle ulcere del piede diabetico e nei trapianti<br />
cutanei), può essere necessario ridurre il livello di pressione<br />
negativa applicata per minimizzare il rischio di ischemia 24,54,55 . Una<br />
pressione negativa pari a -40 mmHg sembra una scelta adeguata,<br />
dato che, come sappiamo, questo valore riduce il rischio di<br />
ischemia pur mantenendo le proprietà terapeutiche ai fini della<br />
guarigione della ferita 51 . Il processo di guarigione può essere<br />
osservato anche con una pressione negativa di -20 mmHg; questo<br />
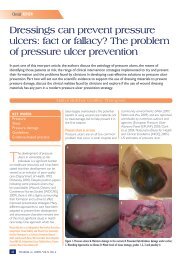
Figura 2 Effetto del flusso sanguigno nel margine nella ferita<br />
Effetto sul flusso sanguigno dell’applicazione di pressione negativa<br />
elevata (-80 mmHg) (A) e bassa (-40 mmHg) (B): il flusso sanguigno vicino al<br />
margine della ferita diminuisce (blu) mentre più lontano aumenta (rosso). L’effetto<br />
massimo sul flusso sanguigno si ottiene con -80 mmHg. Riducendo la pressione<br />
negativa ad esempio a -40 mmHg si riducono anche gli effetti sul flusso sanguigno<br />
ed il rischio di ischemia. Un valore di pressione negativa pari a -40 mmHg può<br />
essere opportuno per tessuti scarsamente irrorati (come ulcere del piede diabetico e<br />
trapianti cutanei sottili).<br />
-80 mmHg<br />
A Letto della ferita<br />
-40 mmHg<br />
B Letto della ferita<br />
3
è probabilmente il valore minimo di<br />
pressione utilizzabile per la NPWT 21,50 .<br />
Qual è il valore di pressione più<br />
indicato per rimuovere elevate<br />
quantità di essudato?<br />
È raro che vi sia motivo di utilizzare<br />
una pressione negativa superiore<br />
a -80 mmHg 34,50,51 ; visto però che il<br />
drenaggio di essudato può migliorare a<br />
-125 mmHg 50 , questo potrebbe essere<br />
il livello di pressione negativa da usare<br />
durante il trattamento iniziale di ferite<br />
altamente essudanti.<br />
Il livello di pressione<br />
negativa da applicare<br />
viene influenzato dalla<br />
medicazione scelta come<br />
interfaccia (schiuma o<br />
garza)?<br />
Si inizia appena a comprendere la<br />
natura dell’interazione fra pressione ed<br />
interfaccia. Una convinzione erronea<br />
molto diffusa è che una ferita con un filler<br />
in schiuma debba essere trattata con<br />
una pressione negativa di -125 mmHg<br />
mentre una con riempimento di garza<br />
vada sottoposta ad una pressione di<br />
-80 mmHg. Recenti evidenze indicano<br />
chiaramente che il livello di pressione<br />
negativa può essere regolato esattamente<br />
a seconda del rischio di ischemia 24,51,54,55<br />
e del dolore patito dal paziente 37,48 e<br />
che la scelta dell’interfaccia può basarsi<br />
sugli effetti che si desidera ottenere<br />
in termini di formazione di tessuto di<br />
granulazione 21,34,42 .<br />
Sono dunque necessarie ulteriori ricerche<br />
per approfondire il meccanismo con il<br />
quale l’interfaccia di ferita e la pressione<br />
negativa influenzano la guarigione.<br />
Qual è la differenza<br />
fra pressione negativa<br />
continua, intermittente e<br />
variabile?<br />
Attualmente la pressione negativa<br />
continua è l’impostazione usata più<br />
di frequente per la NPWT. Il livello di<br />
pressione viene mantenuto costante, ad<br />
esempio a -80 mmHg. Se la pressione<br />
negativa viene accesa e spenta<br />
ripetutamente (ed alterna perciò ad<br />
esempio fra 0 e -80 mmHg), questo<br />
metodo viene chiamato terapia a<br />
pressione intermittente.<br />
La terapia a pressione intermittente non<br />
viene usata spesso nella pratica clinica,<br />
dato che l’alternanza provoca picchi<br />
improvvisi di pressione negativa, facendo<br />
sì che il filler sul tessuto di granulazione<br />
si espanda e si contragga ripetutamente<br />
causando dolore al paziente.<br />
La finalità della terapia a pressione<br />
variabile consiste nel fornire<br />
un’alternanza regolare fra due differenti<br />
livelli di pressione negativa (ad<br />
esempio -10 e -80 mmHg), mantenendo<br />
così un ambito di pressione negativa<br />
per tutta la durata della terapia 56 .<br />
In modelli preclinici sia la NPWT<br />
intermittente che quella variabile<br />
hanno stimolato in misura rilevante la<br />
formazione di tessuto di granulazione<br />
nel letto della ferita 6,57 . Ciò può<br />
risultare sia dallo stimolo meccanico<br />
a cui viene sottoposto il letto della<br />
ferita (effetto di massaggio) 57 sia dal<br />
miglioramento del flusso sanguigno,<br />
che può incrementare l’ossigenazione<br />
dei tessuti e l’angiogenesi 58 .<br />
L’uso della NPWT in futuro<br />
Sebbene l’efficacia della NPWT<br />
richieda ulteriori studi 59 , questo<br />
trattamento avanzato per le ferite<br />
continua a suscitare l’interesse della<br />
maggioranza dei medici coinvolti nella<br />
cura di pazienti portatori di ferite. Un<br />
importante elemento per perfezionare a<br />
beneficio dei pazienti questa modalità di<br />
trattamento consiste nel comprendere<br />
il ruolo svolto dall’interfaccia di ferita e<br />
dall’impostazione dei livelli di pressione.<br />
Questo articolo è stato supportato da<br />
Smith & Nephew.<br />
Riassunto<br />
Per raggiungere i migliori<br />
risultati, l’impostazione<br />
della NPWT va adattata in<br />
modo mirato alle esigenze<br />
della singola ferita. Ai fini<br />
dell’esito è importante<br />
anche il tipo di medicazione<br />
posta a diretto contatto<br />
con la ferita (l’interfaccia<br />
di ferita). L’interfaccia può<br />
consistere in schiuma,<br />
garza o strato di contatto. Si<br />
possono regolare anche il<br />
livello di pressione negativa<br />
e l’impostazione del<br />
vuoto (pressione negativa<br />
continua, intermittente<br />
o variabile). Grazie allo<br />
sviluppo di nuovi filler e allo<br />
studio del loro impiego, e<br />
alla raccolta di dati clinici<br />
circa le varie impostazioni si<br />
prevedono rapidi progressi<br />
nel campo della NPWT.<br />
Per citare questo articolo<br />
Malmsjö M, Borgquist O.<br />
NPWT settings and dressing<br />
choices made easy. <strong>Wounds</strong><br />
<strong>International</strong> 2010; 1(3):<br />
Disponibile su http://www.<br />
woundsinternational.com<br />
Informazioni sugli autori<br />
Malmsjö M, MD, PhD<br />
Borgquist O, MD<br />
Clinical Sciences, Lund, Università di Lund,<br />
Svezia<br />
Inviare la corrispondenza a:<br />
malin.malmsjo@med.lu.se<br />
4
Bibliografia<br />
1. Argenta LC, Morykwas MJ, Marks MW, et<br />
al. Vacuum-assisted closure: state of clinic<br />
art. Plast Reconstr Surg 2006; 117(suppl 7):<br />
127S-142S.<br />
2. Banwell P, Téot L. Topical negative pressure<br />
(TNP): the evolution of a novel wound<br />
therapy. J Tissue Viability 2006; 16(1): 16-24.<br />
3. Chariker ME, Jeter KF, Tintle TE, Ottisford<br />
JE. Effective management of incisional<br />
and cutaneous fistulae with closed suction<br />
wound drainage. Contemp Surg 1989(34):<br />
59-63.<br />
4. Miller MS, Lowery CA. Negative pressure<br />
wound therapy: ‘a rose by any other name’.<br />
Ostomy Wound Manage 2005; 51(3): 44-6,<br />
48-9.<br />
5. Argenta LC, Morykwas MJ. Vacuumassisted<br />
closure: a new method for wound<br />
control and treatment: clinical experience.<br />
Ann Plast Surg 1997; 38(6): 563-76;<br />
discussion 577.<br />
6. Morykwas MJ, Argenta LC, Shelton-Brown<br />
EI, McGuirt W. Vacuum-assisted closure:<br />
a new method for wound control and<br />
treatment: animal studies and basic<br />
foundation. Ann Plast Surg 1997; 38(6):<br />
553-62.<br />
7. Bollero D, Carnino R, Risso D, et al. Acute<br />
complex traumas of the lower limbs: a<br />
modern reconstructive approach with<br />
negative pressure therapy. Wound Repair<br />
Regen 2007; 15(4): 589-94.<br />
8. Stannard JP, Robinson JT, Anderson ER, et<br />
al. Negative pressure wound therapy to<br />
treat hematomas and surgical incisions<br />
following high-energy trauma. J Trauma<br />
2006; 60(6): 1301-6.<br />
9. Scherer LA, Shiver S, Chang M, et al. The<br />
vacuum assisted closure device: a method<br />
of securing skin grafts and improving graft<br />
survival. Arch Surg 2002; 137(8): 930-3;<br />
discussion 933-4.<br />
10. Joseph E, Hamori C, Bergman S, et al.<br />
A new prospective randomized trial of<br />
vacuum assisted closure versus standard<br />
therapy of chronic nonhealing wounds.<br />
<strong>Wounds</strong> 2000; 12: 60-7.<br />
11. Vuerstaek JD, Vainas T, Wuite J, et al. Stateof-the-art<br />
treatment of chronic leg ulcers:<br />
A randomized controlled trial comparing<br />
vacuum-assisted closure (V.A.C.) with<br />
modern wound dressings. J Vasc Surg 2006;<br />
44(5): 1029-37; discussion 1038.<br />
12. Armstrong DG, Lavery LA, Diabetic Foot<br />
Study Consortium. Negative pressure<br />
wound therapy after partial diabetic foot<br />
amputation: a multicentre, randomised<br />
controlled trial. Lancet 2005; 366(9498):<br />
1704-10.<br />
13. Kamolz LP, Andel H, Haslik W, et al. Use<br />
of subatmospheric pressure therapy<br />
to prevent burn wound progression in<br />
human: first experiences. Burns 2004; 30(3):<br />
253-8.<br />
14. Ozturk E, Ozguc H, Yilmazlar T. The use of<br />
vacuum assisted closure therapy in the<br />
management of Fournier’s gangrene. Am J<br />
Surg 2009; 197(5): 660-5; discussion 665.<br />
15. Wild T, Stortecky S, Stremitzer S, et al.<br />
[Abdominal dressing -- a new standard in<br />
therapy of the open abdomen following<br />
secondary peritonitis?] [Articolo in<br />
Tedesco]. Zentralbl Chir 2006; 131(suppl 1):<br />
S111-4.<br />
16. Gustafsson RI, Sjögren J, Ingemansson R.<br />
Deep sternal wound infection: a sternalsparing<br />
technique with vacuum-assisted<br />
closure therapy. Ann Thorac Surg 2003;<br />
76(6): 2048-53; discussion 2053.<br />
17. Sjögren J, Gustafsson R, Nilsson J, Malmsjö<br />
M, Ingermansson R. Clinical outcome after<br />
poststernotomy mediastinitis: vacuumassisted<br />
closure versus conventional<br />
treatment. Ann Thorac Surg 2005; 79(6):<br />
2049-55.<br />
18. Banwell PE. Topical negative pressure<br />
therapy in wound care. J Wound Care 1999;<br />
8(2): 79-84.<br />
19. Morykwas MJ, Simpson J, Punger K, et al.<br />
Vacuum-assisted closure: state of basic<br />
research and physiologic foundation. Plast<br />
Reconstr Surg 2006; 117(suppl 7): 121S-6S.<br />
20. Lu X, Chen S, Li X, et al. The experimental<br />
study of the effects of vacuum-assisted<br />
closure on edema and vessel permeability<br />
of the wound. Chin J Clin Rehab 2003; 7:<br />
1244-5.<br />
21. Borgquist O, Ingemansson R, Malmsjö<br />
M. Micro- and macromechanical effects<br />
on the wound bed by negative pressure<br />
wound therapy using gauze and foam. Ann<br />
Plast Surg In press.<br />
22. Malmsjö M, Ingemansson R, Martin<br />
R, Huddleston E. Negative-pressure<br />
wound therapy using gauze or open-cell<br />
polyurethane foam: similar early effects<br />
on pressure transduction and tissue<br />
contraction in an experimental porcine<br />
wound model. Wound Repair Regen 2009;<br />
17(2): 200-5.<br />
23. Saxena V, Hwang CW, Huang S,<br />
et al. Vacuum-assisted closure:<br />
microdeformations of wounds and cell<br />
proliferation. Plast Reconstr Surg 2004;<br />
114(5): 1086-96; discussion 1097-8.<br />
24. Kairinos N, Voogd AM, Botha PH, et al.<br />
Negative-pressure wound therapy II:<br />
negative-pressure wound therapy and<br />
increased perfusion. Just an illusion? Plast<br />
Reconstr Surg 2009; 123(2): 601-12.<br />
25. Wackenfors A, Gustafsson R, Sjogren J, et<br />
al. Blood flow responses in the peristernal<br />
thoracic wall during vacuum-assisted<br />
closure therapy. Ann Thorac Surg 2005;<br />
79(5): 1724-30; discussion 1730-1.<br />
26. Wackenfors A, Sjogren J, Gustafsson R, et al.<br />
Effects of vacuum-assisted closure therapy<br />
on inguinal wound edge microvascular<br />
blood flow. Wound Repair Regen 2004;<br />
12(6): 600-6.<br />
27. Chen SZ, Li J, Li XY, Xu LS. Effects of vacuumassisted<br />
closure on wound microcirculation:<br />
an experimental study. Asian J Surg 2005;<br />
28(3): 211-7.<br />
28. Greene AK, Puder M, Roy R, et al.<br />
Microdeformational wound therapy:<br />
effects on angiogenesis and matrix<br />
metalloproteinases in chronic wounds of<br />
3 debilitated patients. Ann Plast Surg 2006;<br />
56(4): 418-22.<br />
29. Wilkes R, Zhao Y, Kieswetter K, Haridas<br />
B. Effects of dressing type on 3D tissue<br />
microdeformations during negative<br />
pressure wound therapy: a computational<br />
study. J Biomech Eng 2009; 131(3): 031012.<br />
30. Yager DR, Nwomeh BC. The proteolytic<br />
environment of chronic wounds. Wound<br />
Repair Regen 1999; 7(6): 433-41.<br />
31. Armstrong DG, Jude EB. The role of matrix<br />
metalloproteinases in wound healing. J Am<br />
Podiatr Med Assoc 2002; 92(1):12-8.<br />
32. Blakely M, Weir D. The innovative use of<br />
Safetac soft silicone in conjunction with<br />
negative pressure wound therapy: three<br />
case studies. Poster presentato al 20th<br />
Symposium on Advanced Wound Care<br />
(SAWC), Tampa, Florida, 2007.<br />
33. Dunbar A, Bowers DM, Holderness H Jr.<br />
Silicone net dressing as an adjunct with<br />
negative pressure wound therapy. Ostomy<br />
Wound Manage 2005; 51(suppl 11A): 21-2.<br />
34. Borgquist O, Gustafsson L, Ingemansson<br />
R, et al. Tissue ingrowth into foam but<br />
not into gauze during negative pressure<br />
wound therapy. <strong>Wounds</strong> 2009; 21(11):<br />
302-9.<br />
35. Malmsjö M, Ingemansson R. Tissue trauma<br />
and pain during NPWT and wound filler<br />
5
emoval (foam and gauze) – examined by<br />
immunohistochemistry for substance P and<br />
CGRP. Abstract presentato al Symposium<br />
on Advanced Wound Care and the Wound<br />
Healing Society Meeting in Orlando, Florida,<br />
17-20 Aprile 2010.<br />
36. Franczyk M, Lohman RF, Agarwal JP, et al.<br />
The impact of topical lidocaine on pain<br />
level assessment during and after vacuumassisted<br />
closure dressing changes: a doubleblind,<br />
prospective, randomized study. Plast<br />
Reconstr Surg 2009; 124(3): 854-61.<br />
37. Krasner DL. Managing wound pain in<br />
patients with vacuum-assisted closure<br />
devices. Ostomy Wound Manage 2002;<br />
48(5): 38-43.<br />
38. Paglinawan R, Colic M, Simon M. A<br />
comparative study of the influence of<br />
different pressure levels combined with<br />
various wound dressings on negative<br />
pressure wound therapy driven wound<br />
healing. Presentato al congresso European<br />
Tissue Repair Society, Malta, September<br />
2008.<br />
39. Jones SM, Banwell PE, Shakespeare PG.<br />
Interface dressings influence the delivery<br />
of topical negative-pressure therapy. Plast<br />
Reconstr Surg 2005; 116(4): 1023-8.<br />
40. Petzina R, Ugander M, Gustafsson L, et<br />
al. Hemodynamic effects of vacuumassisted<br />
closure therapy in cardiac surgery:<br />
assessment using magnetic resonance<br />
imaging. J Thorac Cardiovasc Surg 2007;<br />
133(5): 1154-62.<br />
41. Campbell PE, Smith GS, Smith JM.<br />
Retrospective clinical evaluation of gauzebased<br />
negative pressure wound therapy.<br />
Int Wound J 2008; 5(2): 280-6.<br />
42. Fraccalvieri M. Negative pressure<br />
wound therapy using the gauze and<br />
the foam: immunohistological and<br />
ultrasonography morphological analysis<br />
of the granulation tissue and the scar<br />
tissue. Rapporto preliminare di uno studio<br />
clinico presentato al congresso CORTE 4-6<br />
March 2010. Disponibile da: http://www.<br />
corteitalia.org/ (accesso Aprile 2010).<br />
43. Zannis J, Angobaldo J, Marks M, et al.<br />
Approfondimenti<br />
Comparison of fasciotomy wound closures<br />
using traditional dressing changes and the<br />
vacuum-assisted closure device. Ann Plast<br />
Surg 2009; 62(4): 407-9.<br />
44. Jeffery S. Advanced wound therapies in the<br />
management of severe military lower limb<br />
trauma: a new perspective. Eplasty 2009;<br />
9: e28.<br />
45. Chariker ME, Gerstle TL, Morrison CS. An<br />
algorithmic approach to the use of gauzebased<br />
negative-pressure wound therapy as<br />
a bridge to closure in pediatric extremity<br />
trauma. Plast Reconstr Surg 2009; 123(5):<br />
1510-20.<br />
46. Sjogren J, Gustafsson R, Koul B,<br />
Ingemansson R. Selective mediastinal<br />
tamponade to control coagulopathic<br />
bleeding. Ann Thorac Surg 2003; 75(4):<br />
1311-3.<br />
47. World Union of Wound Healing Societies.<br />
Principles of best practice: Vacuum assisted<br />
closure: recommendations for use: A<br />
consensus document. London: MEP Ltd,<br />
2008.<br />
48. McCord SS, Naik-Mathuria BJ, Murphy KM,<br />
et al. Negative pressure therapy is effective<br />
to manage a variety of wounds in infants<br />
and children. Wound Repair Regen 2007;<br />
15(3): 296-301.<br />
49. Morykwas M. Sub-atmospheric pressure<br />
therapy: research evidence. Presentato<br />
al First <strong>International</strong> Topical Negative<br />
Pressure Therapy ETRS Focus Group<br />
Meeting. London: ETRS; 2003; 39-44.<br />
50. Borgquist O, Ingemansson R, Malmsjö M.<br />
The influence of low and high pressure<br />
levels during negative pressure wound<br />
therapy on wound contraction and fluid<br />
evacuation. Wound Repair Regen In press.<br />
51. Borgquist O, Ingemansson R, Malmsjö M.<br />
Wound edge microvascular blood flow<br />
during negative-pressure wound therapy:<br />
examining the effects of pressures from -10<br />
to -175 mmHg. Plast Reconstr Surg 2010;<br />
125(2): 502-9.<br />
52. Nease C. Using low pressure, negative<br />
pressure wound therapy for wound<br />
preparation and the management of split-<br />
Malmsjö M, Ingemansson R, Sjögren J. Mechanisms governing the effects of vacuum-assisted closure in cardiac<br />
surgery. Plast Reconstr Surg 2007; 120(5):1266-75.<br />
thickness skin grafts in three patients with<br />
complex wounds. Ostomy Wound Manage<br />
2009; 55(6): 32-42.<br />
53. Malmsjö M, Ingemansson R, Martin R,<br />
Huddleston E. Wound edge microvascular<br />
blood flow: effects of negative pressure<br />
wound therapy using gauze or<br />
polyurethane foam. Ann Plast Surg 2009;<br />
63(6): 676-81.<br />
54. Kairinos N, Solomons M, Hudson DA.<br />
Negative-pressure wound therapy I: the<br />
paradox of negative-pressure wound<br />
therapy. Plast Reconstr Surg 2009; 123(2):<br />
589-98; discussion 599-600.<br />
55. Kairinos N, Solomons M, Hudson DA. The<br />
paradox of negative pressure wound<br />
therapy - in vitro studies. J Plast Reconstr<br />
Aesthet Surg 2010; 63(1): 174-9.<br />
56. Eberlein T, Fendler H. Using a new<br />
technique of negative pressure wound<br />
therapy (NPWT), variable pressure therapy<br />
(VPT), for the management of chronic,<br />
non-healing wounds. Presentato al<br />
Symposium for Advanced Wound Care<br />
(SAWC), Dallas, Texas, Aprile 2009.<br />
57. Malmsjö M, Ingemansson R. Variable,<br />
intermittent and continuous negative<br />
pressure wound therapy using foam or<br />
gauze: the biological effects on the wound<br />
bed including, blood flow, micro and<br />
macrodeformation, granulation tissue<br />
quantity, wound bed characteristics and<br />
tissue ingrowth into the wound filler.<br />
Abstract presentato al Symposium on<br />
Advanced Wound Care and the Wound<br />
Healing Society Meeting in Orlando,<br />
Florida, 17-20 Aprile 2010.<br />
58. Borgquist O, Ingemansson R, Malmsjö<br />
M. The effect of intermittent and<br />
variable negative pressure wound<br />
therapy on wound edge microvascular<br />
blood flow. Ostomy Wound Manage 2010;<br />
56(3): 60-7.<br />
59. Ubbink DT, Westerbos SJ, Nelson EA,<br />
Vermeulen H. A systematic review of<br />
topical negative pressure therapy for<br />
acute and chronic wounds. Br J Surg 2008<br />
95(6): 685-92.<br />
Per ulteriore documentazione si prega di visitare i siti www.woundsinternational.com oppure www.wounds-uk.com<br />
© <strong>Wounds</strong> <strong>International</strong> 2010<br />
6