You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
SESTA EDIZIONE<br />
<strong>Chimica</strong><br />
Principi e reazioni
Dello stesso Editore:<br />
ABBOTTO/PAGANI – <strong>Chimica</strong> eterociclica<br />
ABELES – Biochimica<br />
ALESCIO – Biologia dinamica<br />
AMEND/MUNDY/ARMOLD – <strong>Chimica</strong> generale,<br />
organica e biologica<br />
ARANEO – <strong>Chimica</strong><br />
ARIENTI – Le basi molecolari della nutrizione<br />
ARIENTI – Un compendio di Biochimica per le<br />
lauree triennali<br />
BATSCHELET – Matematica per biologi<br />
BAUER et al. – Analisi strumentale<br />
BERCHIESI/SANTINI – L’acustica molecolare in<br />
chimica<br />
BERGMEYER – Principi di analisi enzimatica<br />
BOLOGNANI – Bioenergetica<br />
BOLOGNANI/VOLPI – Tavole metaboliche<br />
BROWN – Genetica molecolare<br />
BRUNI – Farmacognosia generale<br />
BUCHNER et al. – <strong>Chimica</strong> inorganica industriale<br />
CABRAS/MARTELLI – <strong>Chimica</strong> e tecnologia degli<br />
alimenti<br />
CABRAS/MARTELLI – Analisi chimica<br />
degli alimenti<br />
CALDERA/BURTI – Manuale di chimica<br />
e biochimica clinica<br />
CASTINO/ROLETTO – Statistica applicata<br />
CHARLOT – Analisi chimica qualitativa<br />
CHRISTIAN – <strong>Chimica</strong> analitica<br />
CLIFFORD – La chimica inorganica dell’analisi<br />
qualitativa<br />
COLTON – Statistica in medicina<br />
COOPER – Biologia molecolare e cellulare<br />
CROMER – Fisica per medicina e per corsi<br />
ad indirizzo biologico<br />
D’ISCHIA – La chimica inorganica in laboratorio<br />
DEWICK – <strong>Chimica</strong>, biosintesi e bioattività delle<br />
sostanze naturali<br />
DUFF – Principi di geofisica<br />
DURANTI/PAGANI – Enzimologia<br />
EVANGELISTI/RESTANI – Prodotti dietetici<br />
FABBRI – La trasformazione chimica<br />
FESSENDEN/FESSENDEN – <strong>Chimica</strong> organica<br />
FOYE - <strong>Chimica</strong> farmaceutica<br />
FREISER/FERNANDO – Gli equilibri ionici nella<br />
chimica analitica<br />
FREUND/WILSON – Metodi statistici<br />
FURLANUT – Farmacologia generale e clinica<br />
per le lauree triennali<br />
GALZIGNA – Introduzione alla biochimica clinica<br />
e patologica<br />
GALZIGNA – Principi di enzimologia<br />
GARRETT – Principi di biochimica<br />
GREENWOOD/EARNSHAW – <strong>Chimica</strong><br />
degli elementi<br />
HEIMLER/BANDINELLI – <strong>Chimica</strong> inorganica<br />
HOGNESS – Analisi qualitativa<br />
HUHEEY – <strong>Chimica</strong> inorganica: principi, strutture,<br />
reattività<br />
JOHNSTONE/WEBB – Energia caos e reazioni<br />
chimiche<br />
KEISLER – Elementi di analisi matematica<br />
KOLTHOFF – Analisi chimica quantitativa<br />
LEE – Compendio di chimica inorganica<br />
MAFFEI – Biochimica vegetale<br />
MANAHAN – <strong>Chimica</strong> ambientale<br />
MANGIAROTTI – Biologia molecolare<br />
MARZONA – <strong>Chimica</strong> delle fermentazioni<br />
MAUGINI – Botanica farmaceutica<br />
McMURRY – <strong>Chimica</strong> organica<br />
MICHELIN LAUSAROT/VAGLIO – Stechiometria<br />
per la <strong>Chimica</strong> Generale<br />
MOORE – <strong>Chimica</strong> fisica<br />
MORASSI/SPERONI – Il laboratorio chimico<br />
NORMAN/COXON – <strong>Chimica</strong> organica<br />
PEDULLI – Metodi fisici in chimica organica<br />
PETRUCCI – <strong>Chimica</strong> generale<br />
PONTICELLI/USAI – <strong>Chimica</strong> generale<br />
e inorganica con elementi di chimica organica<br />
(per lauree trieannali)<br />
RADAELLI/CALAMAI – <strong>Chimica</strong> del terreno<br />
SAMAJA – Biochimica per le lauree triennali<br />
SANTAGADA/CALIENDO – Peptidi<br />
e peptidomimetici<br />
SAVELLI-BRUNO – Analisi chimica farmaceutica<br />
SENATORE – Biologia cellulare<br />
e Botanica farmaceutica<br />
SIENKO et al. – Esercitazioni di chimica<br />
SILIPRANDI/TETTAMANTI – Biochimica medica<br />
SKOOG/WEST – Introduzione alla chimica analitica<br />
SLOWINSKI/WOLSEY/MASTERTON – Esperimenti<br />
di laboratorio di chimica generale e inorganica<br />
con analisi qualitativa per il I anno<br />
SPANDRIO – Principi e tecniche di chimica clinica<br />
WEISSERMEL/ARPE – <strong>Chimica</strong> organica industriale<br />
WHITTEN – <strong>Chimica</strong>:<br />
ZIEGLER – Conoscenze attuali in nutrizione
SESTA EDIZIONE<br />
<strong>Chimica</strong><br />
Principi e reazioni<br />
William L. Masterton<br />
University of Connecticut<br />
Cecile N. Hurley<br />
University of Connecticut<br />
Edizione italiana a cura del<br />
Prof. Gino Paolucci<br />
Università Ca’ Foscari di Venezia<br />
Aggiornamenti della sesta edizione italiana<br />
a cura di<br />
Valerio Causin<br />
Università degli Studi di Padova
Titolo originale<br />
Chemistry: Principles and Reactions, Sixth Edition<br />
by William L. Masterton & Cecile N. Hurley<br />
© 2009 Brooks/Cole Cengage Learning<br />
Tutti i diritti sono riservati<br />
È VIETATA PER LEGGE LA RIPRODUZIONE IN FOTOCOPIA<br />
ED IN QUALSIASI ALTRA FORMA<br />
È vietato riprodurre, archiviare in un sistema di riproduzione<br />
o trasmettere sotto qualsiasi forma o con qualsiasi mezzo elettronico,<br />
meccanico, per fotocopia, registrazione o altro,<br />
qualsiasi parte di questa pubblicazione<br />
senza autorizzazione scritta dell’Editore.<br />
Ogni violazione sarà perseguita secondo le leggi civili e penali.<br />
ISBN 978-88-299-2041-9<br />
Stampato in Italia<br />
© Copyright 2010 by <strong>Piccin</strong> Nuova Libraria S.p.A., Padova<br />
www.piccin.it
Dedica<br />
In memoria di William Lewis Masterton<br />
Insegnante senza pari<br />
Didatta senza paragoni<br />
Amico e mentore<br />
Ci manchi
Sommario<br />
1 La materia e la sua misura 1<br />
2 Atomi, molecole e ioni 24<br />
3 Relazioni di massa in chimica; stechiometria 50<br />
4 Reazioni in soluzione acquosa 74<br />
5 I gas 102<br />
6 Struttura elettronica e la tavola periodica 132<br />
7 Il legame covalente 164<br />
8 Termochimica 196<br />
9 Liquidi e solidi 226<br />
10 Le soluzioni 258<br />
11 Velocità di reazione 284<br />
12 Equilibrio chimico dei gas 322<br />
13 Acidi e basi 352<br />
14 Equilibri nelle soluzioni acido-base 382<br />
15 Ioni complessi 408<br />
16 Equilibri di precipitazione 430<br />
17 Spontaneità di una reazione 450<br />
18 Elettrochimica 480<br />
19 Reazioni nucleari 512<br />
20 La chimica dei metalli 534<br />
21 La chimica dei non metalli 554<br />
22 La chimica organica 578<br />
23 Polimeri organici, naturali e sintetici 610<br />
Appendice 1: Unità, costanti e dati di riferimento 635<br />
Appendice 2: Proprietà degli elementi 641<br />
Appendice 3: Esponenti e logaritmi 643<br />
Appendice 4: Nomenclatura di ioni complessi 648<br />
Appendice 5: Orbitali molecolari 650<br />
Appendice 6:<br />
Riconoscimenti 677<br />
Indice analitico/Glossario 681<br />
Risposte ai quesiti e problemi con numeri pari e ai problemi<br />
sfida 656<br />
vi
Indice generale<br />
1 LA MATERIA E LA SUA MISURA 1<br />
1.1 Tipi di materia 2<br />
1.2 Misure 6<br />
1.3 Proprietà delle sostanze 13<br />
<strong>Chimica</strong>: Il lato umano: Antoine Lavoisier 14<br />
<strong>Chimica</strong> fuori dell’aula: Titanio: un metallo dell’era spaziale 18<br />
Sommario del capitolo 19<br />
Problema riassuntivo 19<br />
Quesiti e problemi 20<br />
Charles D. Winters<br />
2 ATOMI, MOLECOLE E IONI 24<br />
2.1 Gli atomi e la teoria atomica 25<br />
2.2 I componenti dell’atomo 25<br />
<strong>Chimica</strong>: Il lato umano: John Dalton 27<br />
2.3 Introduzione alla tavola periodica 31<br />
<strong>Chimica</strong>: Il lato umano: La storia della tavola periodica 32<br />
2.4 Molecole e ioni 34<br />
2.5 Formule dei composti ionici 38<br />
2.6 Nomi dei composti 39<br />
<strong>Chimica</strong> fuori dell’aula: L’alcol etilico e la legge 43<br />
Sommario del capitolo 44<br />
Problema riassuntivo 44<br />
Quesiti e Problemi 45<br />
vii
3 RELAZIONI DI MASSA IN CHIMICA; STECHIOMETRIA 50<br />
3.1 Masse atomiche 51<br />
3.2 La mole 55<br />
3.3 Le relazioni di massa nelle formule chimiche 56<br />
3.4 Le relazioni di massa nelle reazioni 60<br />
<strong>Chimica</strong> fuori dell’aula: Gli idrati 66<br />
Sommario del capitolo 67<br />
Problema riassuntivo 67<br />
Quesiti e Problemi 68<br />
4 REAZIONI IN SOLUZIONE ACQUOSA 74<br />
4.1 Concentrazione dei soluti; molarità 75<br />
4.2 Reazioni di precipitazione 78<br />
4.3 Reazioni acido-base 81<br />
<strong>Chimica</strong>: Il lato umano: Svante August Arrhenius 86<br />
4.4 Reazioni di ossidazione-riduzione 86<br />
<strong>Chimica</strong> fuori dell’aula: Cambiamenti di colore reversibili 92<br />
Sommario del capitolo 94<br />
Problema riassuntivo 94<br />
Quesiti e problemi 95<br />
Charles D. Winters<br />
5 I GAS 102<br />
5.1 Misurazioni nei gas 103<br />
5.2 La legge dei gas ideali 105<br />
5.3 Calcoli con la legge dei gas 107<br />
5.4 Stechiometria delle reazioni in fase gassosa 111<br />
<strong>Chimica</strong>: Il lato umano: Amedeo Avogadro 113<br />
5.5 Le miscele di gas: pressioni parziali e frazioni molari 114<br />
5.6 La teoria cinetica dei gas 117<br />
5.7 I gas reali 122<br />
<strong>Chimica</strong> fuori dell’aula: Airbag 124<br />
Sommario del capitolo 125<br />
Problema riassuntivo 126<br />
Quesiti e problemi 126<br />
viii<br />
Indice generale
6 STRUTTURA ELETTRONICA E<br />
LA TAVOLA PERIODICA 132<br />
6.1 Luce, energie dei fotoni e spettri atomici 133<br />
6.2 L’atomo di idrogeno 137<br />
6.3 Numeri quantici 140<br />
6.4 Orbitali atomici: forma e dimensioni 143<br />
6.5 Configurazioni elettroniche negli atomi 143<br />
<strong>Chimica</strong>: Il lato umano: Glenn Theodore Seaborg 147<br />
6.6 Diagrammi orbitalici degli atomi 148<br />
6.7 Disposizione elettronica negli ioni monoatomici 150<br />
6.8 Andamenti periodici nelle proprietà degli atomi 152<br />
<strong>Chimica</strong> fuori dell’aula: Perchè le aragoste diventano rosse da cotte? 157<br />
Sommario del capitolo 158<br />
Problema riassuntivo 158<br />
Quesiti e problemi 159<br />
7 IL LEGAME COVALENTE 164<br />
7.1 Le strutture di Lewis; la regola dell’ottetto 166<br />
<strong>Chimica</strong>: Il lato umano: Gilbert Newton. Lewis 174<br />
7.2 Geometria molecolare 175<br />
7.3 Polarità delle molecole 182<br />
7.4 Orbitali atomici; ibridizzazione 185<br />
<strong>Chimica</strong> fuori dell’aula: I gas nobili 190<br />
Sommario del capitolo 191<br />
Problema riassuntivo 191<br />
Quesiti e problemi 192<br />
S. Ruven Smith<br />
8 TERMOCHIMICA 196<br />
8.1 Principi del flusso di calore 197<br />
8.2 Misura del flusso di calore; calorimetria 200<br />
8.3 Entalpia 203<br />
8.4 Equazioni termochimiche 204<br />
8.5 Entalpie di formazione 208<br />
8.6 Entalpia di legame 212<br />
Indice generale<br />
ix
8.7 La prima legge della termodinamica 214<br />
<strong>Chimica</strong> fuori dell’aula: Bilancio energetico nel corpo umano 218<br />
Sommario del capitolo 219<br />
Problema riassuntivo 220<br />
Quesiti e problemi 220<br />
9 LIQUIDI E SOLIDI 226<br />
9.1 Equilibrio liquido-vapore 227<br />
9.2 Diagrammi delle fasi 233<br />
9.3 Sostanze molecolari; forze intermolecolari 235<br />
9.4 Solidi a reticolo covalente, ionici e metallici 240<br />
9.5 Strutture cristalline 245<br />
<strong>Chimica</strong>: Il lato umano: Dorothy Crowfoot Hodgkin 248<br />
<strong>Chimica</strong> fuori dell’aula: Allotropia 250<br />
Sommario del capitolo 252<br />
Problema riassuntivo 252<br />
Quesiti e problemi 253<br />
George Semple<br />
10 LE SOLUZIONI 258<br />
10.1 Unità di concentrazione 259<br />
10.2 Principi di solubilità 264<br />
10.3 Proprietà colligative dei non elettroliti 267<br />
10.4 Proprietà colligative degli elettroliti 274<br />
<strong>Chimica</strong> fuori dell’aula: Lo sciroppo d’acero 277<br />
Sommario del capitolo 278<br />
Problema riassuntivo 279<br />
Quesiti e problemi 279<br />
11 VELOCITÀ DI REAZIONE 284<br />
11.1 Significato di velocità di reazione 285<br />
11.2 Velocità di reazione e concentrazione 287<br />
11.3 Concentrazione dei reagenti e tempo 292<br />
11.4 Modelli per la velocità di reazione 298<br />
<strong>Chimica</strong>: Il lato umano: Henry Eyring 301<br />
11.5 Velocità di reazione e temperatura 301<br />
11.6 Catalisi 305<br />
Charles D. Winters<br />
x<br />
Indice generale
11.7 Meccanismi di reazione 307<br />
<strong>Chimica</strong> fuori dell’aula: La storia dell’ozono 310<br />
Sommario del capitolo 312<br />
Problema riassuntivo 312<br />
Quesiti e problemi 313<br />
12 EQUILIBRIO CHIMICO DEI GAS 322<br />
12.1 Il sistema in equilibrio N 2 O 4 –NO 2 323<br />
12.2 L’espressione della costante di equilibrio 326<br />
12.3 Determinazione di K 331<br />
12.4 Applicazioni della costante di equilibrio 333<br />
12.5 Effetto delle variazioni delle condizioni su un sistema in equilibrio 337<br />
<strong>Chimica</strong> fuori dell’aula: Un’applicazione industriale dell’equilibrio gassoso 342<br />
Sommario del capitolo 343<br />
Problema riassuntivo 344<br />
Quesiti e problemi 345<br />
13 ACIDI E BASI 352<br />
13.1 Il modello acido-base di Brønsted-Lowry 353<br />
13.2 Il prodotto ionico dell’acqua 354<br />
13.3 pH e pOH 355<br />
13.4 Acidi deboli e loro costanti di equilibrio 359<br />
13.5 Basi deboli e loro costanti di equilibrio 368<br />
13.6 Proprietà acido-base delle soluzioni saline 372<br />
<strong>Chimica</strong> fuori dell’aula: Acidi e basi organici 374<br />
Sommario del capitolo 376<br />
Problema riassuntivo 376<br />
Quesiti e problemi 377<br />
14 EQUILIBRI NELLE SOLUZIONI ACIDO-BASE 382<br />
14.1 I tamponi 383<br />
14.2 Indicatori acido-base 391<br />
14.3 Titolazioni acido-base 394<br />
Indice generale<br />
xi
<strong>Chimica</strong> fuori dell’aula: Piogge acide 400<br />
Sommario del capitolo 401<br />
Problema riassuntivo 401<br />
Quesiti e problemi 402<br />
15 IONI COMPLESSI 408<br />
15.1 Composizione degli ioni complessi 409<br />
15.2 Geometria degli ioni complessi 413<br />
15.3 Struttura elettronica degli<br />
ioni complessi 416<br />
<strong>Chimica</strong>: Il lato umano:<br />
Alfred Werner 417<br />
15.4 Costanti di formazione degli<br />
ioni complessi 422<br />
<strong>Chimica</strong> fuori dell’aula: I chelati: naturali e sintetici 424<br />
Sommario del capitolo 425<br />
Problema riassuntivo 426<br />
Quesiti e problemi 426<br />
Charles D. Winters<br />
16 EQUILIBRI DI PRECIPITAZIONE 430<br />
16.1 Formazione del precipitato; costante del prodotto di solubilità (K ps ) 431<br />
16.2 Solubilizzazione di precipitati 439<br />
<strong>Chimica</strong> fuori dell’aula: Analisi qualitativa 443<br />
Sommario del capitolo 445<br />
Problema riassuntivo 445<br />
Quesiti e problemi 446<br />
17 SPONTANEITÀ DI UNA REAZIONE 450<br />
17.1 Processi spontanei 451<br />
17.2 Entropia, S 453<br />
17.3 Energia libera, G 458<br />
<strong>Chimica</strong>: Il lato umano: J. Willard Gibbs 459<br />
17.4 Variazione di energia libera standard, G° 460<br />
17.5 Effetto di temperatura, pressione e concentrazione<br />
sulla spontaneità di una reazione 463<br />
Charles D. Winters<br />
xii<br />
Indice generale
17.6 Variazione di energia libera e la costante di equilibrio 467<br />
17.7 Additività delle variazioni di energia libera; reazioni accoppiate 468<br />
<strong>Chimica</strong> fuori dell’aula: L’elasticità della gomma: un fenomeno entropico 470<br />
Sommario del capitolo 472<br />
Problema riassuntivo 472<br />
Quesiti e problemi 473<br />
18 ELETTROCHIMICA 480<br />
18.1 Celle voltaiche 481<br />
18.2 Potenziali standard 485<br />
18.3 Relazioni tra E°, G° e K 491<br />
18.4 Effetto della concentrazione sul potenziale 492<br />
18.5 Celle elettrolitiche 496<br />
18.6 Pile commerciali 499<br />
<strong>Chimica</strong>: Il lato umano: Michael Faraday 501<br />
<strong>Chimica</strong> fuori dell’aula: Cella a combustibile: la prossima frontiera nella conversione da energia<br />
chimica a energia elettrica? 503<br />
Sommario del capitolo 505<br />
Problema riassuntivo 505<br />
Quesiti e problemi 506<br />
19 REAZIONI NUCLEARI 512<br />
19.1 La radioattività 513<br />
<strong>Chimica</strong>: Il lato umano: I Curie 517<br />
19.2 La velocità del decadimento radioattivo 518<br />
19.3 Relazioni massa-energia 520<br />
19.4 Fissione nucleare 523<br />
19.5 Fusione nucleare 526<br />
<strong>Chimica</strong> fuori dell’aula: Effetti biologici<br />
delle radiazioni 528<br />
Sommario del capitolo 529<br />
Problema riassuntivo 530<br />
Quesiti e problemi 530<br />
NASA<br />
Indice generale<br />
xiii
20 LA CHIMICA DEI METALLI 534<br />
20.1 La metallurgia 535<br />
20.2 Le reazioni dei metalli alcalini e alcalino-terrosi 541<br />
20.3 La chimica di ossidoriduzione dei metalli di transizione 544<br />
<strong>Chimica</strong> fuori dell’aula: Metalli essenziali<br />
nell’alimentazione 550<br />
Sommario del capitolo 551<br />
Problema riassuntivo 551<br />
Quesiti e problemi 552<br />
21 LA CHIMICA DEI NON METALLI 554<br />
21.1 Gli elementi e la loro preparazione 555<br />
21.2 I composti con idrogeno dei non metalli 559<br />
21.3 I composti con ossigeno dei non metalli 563<br />
21.4 Ossiacidi e ossianioni 566<br />
<strong>Chimica</strong> fuori dell’aula: Arsenico e selenio 573<br />
Sommario del capitolo 574<br />
Problema riassuntivo 574<br />
Quesiti e problemi 575<br />
22 LA CHIMICA ORGANICA 578<br />
22.1 Gli idrocarburi saturi: alcani 580<br />
22.2 Gli idrocarburi insaturi: alcheni e alchini 585<br />
22.3 Gli idrocarburi aromatici e loro derivati 588<br />
22.4 Gruppi funzionali 590<br />
22.5 Isomeria nei composti organici 597<br />
22.6 Reazioni organiche 601<br />
<strong>Chimica</strong> fuori dell’aula: Colesterolo 603<br />
Sommario del capitolo 605<br />
Problema riassuntivo 605<br />
Quesiti e problemi 606<br />
Charles D. Winters<br />
xiv<br />
Indice generale
23 POLIMERI ORGANICI, NATURALI E SINTETICI 610<br />
23.1 Polimeri sintetici di addizione 611<br />
23.2 Polimeri sintetici di condensazione 614<br />
23.3 Carboidrati 617<br />
23.4 Proteine 621<br />
<strong>Chimica</strong> fuori dell’aula: Identificazione attraverso il DNA 628<br />
Sommario del capitolo 630<br />
Problema riassuntivo 630<br />
Quesiti e problemi 631<br />
Appendici<br />
1 Unità, costanti e dati di riferimento 635<br />
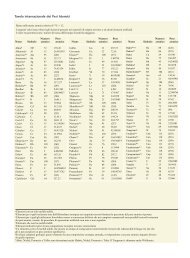
2 Proprietà degli elementi 641<br />
3 Esponenti e logaritmi 643<br />
4 Nomenclatura di ioni complessi 648<br />
5 Orbitali molecolari 650<br />
6 Risposte ai quesiti e problemi con numeri pari e ai problemi sfida 656<br />
Riconoscimenti 677<br />
Indice analitico/Glossario 681<br />
Indice generale<br />
xv
Prefazione<br />
L<br />
a prefazione di un libro di testo è una delle sezioni più difficili da scrivere. In occasione<br />
delle ultime cinque edizioni, io e Bill Masterton ci siamo incontrati per<br />
un lungo pranzo e per parlare degli argomenti che avremmo voluto introdurre<br />
nella prefazione. Il pranzo (sempre cheeseburger e patatine per Bill, a meno che nel menu<br />
non ci fossero sgombro e okra fritta) finiva sempre con la stessa frase di Bill: “tu intanto<br />
scrivi una bozza della prefazione, ed io la aggiusterò”. Per questa edizione non c'è stato il<br />
pranzo, non c'era nessuno con cui discutere e nessuno ad aggiustare la mia bozza. Allora<br />
cercherò io di aggiustare le idee di cui io e Bill abbiamo parlato in una lunga conversazione<br />
telefonica. Queste sono le domande cui abbiamo cercato di rispondere.<br />
Perché continuare a scrivere un libro breve?<br />
La risposta è ovvia, se si pensa ai costi crescenti delle tasse universitarie, allo sfruttamento<br />
delle foreste e alle schiene doloranti degli studenti. La vignetta in questa pagina illustra la<br />
nostra opinione. Siamo rimasti convinti del fatto che sia possibile coprire completamente<br />
(od almeno quasi completamente) gli argomenti di un corso annuale con un solo libro di<br />
testo. Gli studenti si domandano giustamente perché debbano pagare per un libro di 1000<br />
pagine con “roba” che non vedranno mai durante il corso. Non abbiamo ancora trovato<br />
una valida risposta, quindi il nostro obiettivo è stato un libro di poco più di 600 pagine.<br />
Come scriveremo questa edizione di questo libro breve?<br />
Dopo aver superato la convinzione che un libro breve sia un libro di basso livello, abbiamo<br />
rinnovato il nostro impegno a trattare concetti generali in modo conciso, ma senza sacrificare<br />
profondità, rigore e chiarezza. I nostri criteri su quale materiale includere continuano<br />
ad essere l'importanza e la rilevanza per lo studente, non la difficoltà. Per raggiungere tale<br />
scopo, abbiamo adottato un approccio su tre fronti:<br />
Dato il peso dei libri di testo in continuo<br />
aumento, molti studenti stanno<br />
cercando un’alternativa agli zaini.<br />
1. Eliminare le ripetizioni e le duplicazioni, ove possibile. Come nelle edizioni precedenti<br />
questo testo usa:<br />
■<br />
■<br />
■<br />
■<br />
Solo un metodo per bilanciare le reazioni redox, il metodo delle semi-equazioni introdotto<br />
nel Capitolo 4.<br />
Solo un metodo per lavorare su problemi inerenti la legge dei gas, usando la legge<br />
dei gas ideali in tutti i casi (Capitolo 5).<br />
Solo un modo di calcolare H (Capitolo 8), usando le entalpie di formazione.<br />
Solo una costante di equilibrio per reazioni in fase gas (Capitolo 12), la costante<br />
termodinamica K, spesso indicata come K p . Questo semplifica non solo il trattamento<br />
degli equilibri in fase gas, ma anche la discussione della spontaneità delle<br />
reazioni (Capitolo 17) e l'elettrochimica (Capitolo 18).<br />
2. Relegare alle appendici o agli inserti “<strong>Chimica</strong> fuori dall'aula” gli argomenti normalmente<br />
affrontati da testi di più di 1000 pagine. Gli argomenti in questa categoria includono:<br />
■ La teoria degli orbitali molecolari (Appendice 5). La nostra esperienza è stata (e<br />
continua ad essere) che nonostante questo approccio sia importante per il legame<br />
xvi
■<br />
■<br />
■<br />
chimico, la gran parte degli studenti di chimica generale non lo capiscono, ma ne<br />
memorizzano soltanto i principi discussi in classe.<br />
La nomenclatura degli ioni complessi e dei composti organici. Crediamo che questo<br />
materiale sia di scarso valore in un corso iniziale. Gli studenti dimenticano presto<br />
come si nomina uno ione complesso, perché hanno poche occasioni di applicare<br />
queste regole. È sembrato meglio lasciare la nomenclatura organica ad un<br />
corso di chimica organica.<br />
Analisi qualitativa. È riassunta in un paio di pagine nella sezione “<strong>Chimica</strong> fuori<br />
dall'aula” del Capitolo 16. Una discussione estesa dello schema di analisi qualitativa<br />
e della chimica su cui si basa devono essere oggetto di un manuale di laboratorio,<br />
non di un libro di testo di un corso d'aula.<br />
Biochimica. Questa materia è tradizionalmente trattata nell'ultimo capitolo dei testi<br />
di chimica generale. Mentre abbiamo introdotto molti argomenti biochimici nel<br />
testo (tra questi la discussione del gruppo eme nel Capitolo 15 ed i carotenoidi nel<br />
Capitolo 6), non troviamo sia il caso di inserire un intero capitolo di biochimica. È<br />
un argomento indubbiamente interessante, ma richiede un background di chimica<br />
organica che uno studente del primo anno non ha.<br />
3. Evitare divagazioni superflue, applicazioni al mondo reale e aneddoti sugli scienziati<br />
durante l'esposizione dei principi. Abbiamo inserito molte applicazioni all'interno dei<br />
problemi e in alcuni punti del testo. In generale, però, ci siamo attenuti ad un approccio<br />
molto scarno. Gli studenti possono essere distratti da questi interessanti intermezzi,<br />
proprio mentre stanno faticando per capire i concetti. Abbiamo inserito le nostre applicazioni<br />
al mondo reale preferite e le storie personali degli scienziati in sezioni separate,<br />
“<strong>Chimica</strong> fuori dall'aula” e “<strong>Chimica</strong>: il lato umano”. I nostri studenti dicono che<br />
leggono sempre per prime queste sezioni e che sono tra le parti del libro che preferiscono.<br />
Apprezzano anche le note a lato del testo.<br />
Come si differenzia la sesta edizione rispetto alla quinta?<br />
Nonostante i principi della chimica generale non cambino, ci sono sempre molti modi per<br />
migliorare un libro, renderlo più facile da usare e più interessante. La nostra speranza era<br />
che uno studente, confrontando la sesta edizione con la quinta, concludesse “era proprio il<br />
caso di fare una revisione. Ora capisco meglio”. (Dubitavamo che gli studenti sarebbero<br />
stati così benevoli, ma lo speravamo!) I cambiamenti che abbiamo apportato per realizzare<br />
questa speranza sono:<br />
■<br />
Aggiornare gli esempi nel testo. Circa il 30% è stato rivisto, per aumentare il rigore<br />
degli esempi quantitativi ed approfondire la comprensione concettuale degli<br />
argomenti. Molti studenti hanno ammesso (per la proverbiale mancanza di<br />
tempo) che invece di risolvere i problemi alla fine del capitolo, facevano gli<br />
esempi (perché avevano la soluzione sotto gli occhi). Si lamentavano però che<br />
alcuni degli esempi erano troppo semplici per prepararli ai compiti per casa ed<br />
agli esami.<br />
■ Aggiungere nuove domande ed esercizi alla fine dei capitoli. Ci sono circa 200<br />
nuove domande o esercizi alla fine dei capitoli, molti di essi concettuali.<br />
■<br />
■<br />
■<br />
■<br />
Continuare il processo di aggiornamento da immagini statiche ad immagini<br />
“autoesplicanti”, in cui i commenti prima inseriti nel testo, sono stati introdotti<br />
nell'immagine stessa. Crediamo che un tale approccio sia più adatto per gli studenti<br />
di oggi.<br />
Aggiornamento ed ammodernamento delle fotografie e dei modelli molecolari.<br />
Revisione dello stile dei grafici per renderli più chiari.<br />
Invitare altri autori a scrivere degli inserti sulla loro attività di ricerca recente od<br />
attuale. Ci sono quattro nuovi contenuti per le sezioni “<strong>Chimica</strong> fuori dall'aula”.<br />
Prefazione<br />
xvii
Ringraziamenti<br />
M<br />
olte delle persone che hanno utilizzato questo libro, sia docenti che studenti,<br />
hanno scritto lettere ed email per dare dei suggerimenti su come<br />
migliorare l’opera. Altri hanno semplicemente chiamato per porgere le<br />
loro condoglianze in occasione della scomparsa del mio co-autore. Sono grata a tutti loro.<br />
Tra i revisori che hanno supportato la preparazione di questa edizione vi sono:<br />
Christopher Babb, Berry College<br />
Kathleen Brunke, Christopher Newport University<br />
Kevin Cantrell, University of Portland<br />
S. Michael Condren, Christian Brothers University<br />
Becky A. Gee, Long Island University<br />
Richard L. Nafshun, Oregon State University<br />
Edward J. Neth, University of Connecticut<br />
James A. Phillips, University of Wisconsin, Eau Claire<br />
David Treichel, Nebraska Wesleyan University<br />
Will Wickun, Montana State University, Billings<br />
Sono particolarmente grata ai Professori Fatma Selampinar (University of Connecticut)<br />
e David Shinn (University of Hawaii, Manoa) per le loro accurate revisioni. La loro<br />
precisione ed attenzione ai dettagli è incredibile.<br />
I Professori Harry Frank (University of Connecticut), Steven Shaw (Montana State<br />
University), Greg Sotzing (University of Connecticut), e Leslie Sperling (Lehigh University)<br />
hanno gentilmente acconsentito a scrivere dei brevi saggi sui loro ambiti di ricerca.<br />
Ne sono scaturiti dei lavori interessanti e comprensibili anche a studenti del primo anno<br />
(non certo un compito facile!).<br />
Molte persone hanno lavorato a questo testo in ambito editoriale e di produzione.<br />
Hanno raccolto pagine di manoscritto, idee, schemi improvvisati e lunghe liste di desideri,<br />
li hanno messi assieme e hanno creato questa edizione. Hanno pungolato, blandito e fissato<br />
termini temporali impossibili da onorare, il tutto con incredibile pazienza. Non avrei<br />
potuto fare tutto ciò senza di loro. Si tratta di: Lisa Lockwood, chemistry editor; Ashley<br />
Summers, assistant editor; Lisa Weber, technology project manager; Teresa Trego, content<br />
project manager; Amee Mosely, marketing manager; e Dan Fitzgerald, production editor<br />
alla Graphic World Publishing Services.<br />
Manca da questa lista Peter McGahey, il mio developmental editor, che si merita un<br />
ringraziamento speciale. Ha calmato i miei nervi logorati e mi ha rincuorato con la sua<br />
personalità ottimistica e positiva. Il suo umorismo ha fornito anche una dose in più di<br />
energia. E mi ha permesso di distrarmi un po’ chiacchierando di bulbi di tulipano in primavera<br />
e di piante perenni in estate. Grazie Peter. Sei stato un’oasi di calma quando ne<br />
avevo bisogno.<br />
Due persone che non appartengono a nessuna squadra richiedono un riconoscimento<br />
speciale. A Joseph Hurley, miglior correttore di bozze, grazie per aver impiegato i tuoi<br />
weekend per prestarmi un altro paio di occhi. A Jim Hurley, che ha battuto a macchina il<br />
manoscritto, letto le bozze con la visione di un non-chimico (è un matematico) ed ha<br />
ascoltato le mie infinite lamentele, grazie per aver intrapreso questo viaggio con me.<br />
Cecile N. Hurley<br />
University of Connecticut<br />
Storrs, CT<br />
Novembre 2007<br />
xviii<br />
Ringraziamenti
Per lo studente<br />
Hai probabilmente sentito molto parlare del corso di chimica generale. Molti<br />
pensano che sia più difficile degli altri corsi. Ci può essere una qualche giustificazione<br />
per questa opinione. Oltre ad avere il suo vocabolario specializzato,<br />
la chimica è una scienza quantitativa, quindi richiede la matematica come strumento per<br />
capire i concetti. Come risultato, probabilmente riceverai molti consigli dai tuoi docenti e<br />
dai tuoi colleghi studenti su come studiare chimica. Noi esitiamo ad aggiungere la nostra<br />
opinione; l'esperienza di insegnanti e genitori ci ha insegnato che gli studenti se la cavano<br />
benissimo da soli. Vorremmo però presentarti alcuni strumenti didattici di questo testo,<br />
che descriveremo nelle pagine seguenti.<br />
Strumenti didattici in <strong>Chimica</strong>: principi e reazioni, sesta edizione<br />
Esempi<br />
In un capitolo tipico, troverai dieci o più esempi, ciascuno predisposto per illustrare un<br />
particolare principio, con le risposte evidenziate a colori. La maggior parte degli esempi<br />
contiene una strategia da seguire nel procedimento, che descrive il ragionamento che sta<br />
dietro la soluzione. In questo modo ti abituerai a risolvere così tutti i problemi. Per prima<br />
cosa, rifletti un momento per decidere in che modo si potrebbe risolvere il problema. Poi,<br />
e solo poi, utilizza la matematica per risolverlo.<br />
Molti degli esempi terminano con una verifica, che ti incoraggia a controllare se la risposta<br />
ha un senso. Speriamo che ti abituerai a utilizzare questo procedimento nel risolvere<br />
i problemi a casa o agli esami.<br />
Esempi graduati<br />
All’interno del testo ci sono anche circa 20 Esempi graduati. Sono costituiti da due a quattro<br />
parti (a, b, c, d) concatenate. Un tipico esempio graduato potrebbe essere il seguente:<br />
Esempio 1.4 Graduato<br />
Per la reazione<br />
Determina<br />
A 2B 9: C<br />
*(a) Il numero di moli di A che reagiscono con 5.0 mol di B.<br />
**(b)Il numero di grammi di A che reagiscono con 5.0 g di B.<br />
***(c)Il volume di una soluzione 0.50 M di A che reagisce con 5.0 g di B.<br />
****(d)Il volume di una soluzione 0.50 M di A che reagisce con 25 ml di una soluzione<br />
che ha una densità di 1.2 g/ml e che contiene il 32% in massa di B.<br />
Ci sono due vantaggi a lavorare con gli esempi graduati.<br />
1. Risolvendo le parti da (a) a (d) in successione, ti renderai conto di quanti modi diversi<br />
ci sono di porre le domande sulle relazioni tra le masse in una reazione, partendo da<br />
un’equazione bilanciata. Questo ti servirà a dominare lo shock quando ti ritrovi davanti<br />
ad una sola domanda del tipo (d) in sede di esame.<br />
2. Le parti di un esempio graduato non sono una semplice progressione da domande<br />
semplici a domande più difficili. Il valore di un esempio graduato sta nel fatto che l'ul-<br />
xix
tima domanda presuppone l'abilità di rispondere a quelle precedenti. Potresti essere in<br />
grado di rispondere alle parti (a) e (b) con una limitata comprensione del materiale,<br />
ma per rispondere alla parte (d) devi padroneggiare la materia.<br />
Usa gli esempi graduati come ripasso per gli esami. Prova a saltare le prime domande –<br />
in questo caso (a), (b) e (c) – e vai direttamente all'ultima parte, (d). Se puoi risolvere (d),<br />
non sarà necessario risolvere (a), (b) e (c); sai già come farli. Se non ce la fai, prova con (c)<br />
per vedere dove può essere il problema. Se non ce la fai con (c) prova con (b). Come ultima<br />
risorsa, comincia con (a) e ricostruisci la soluzione fino a (d).<br />
Note a margine<br />
Sparse per tutto il libro ci sono numerose note poste a margine. Molte di queste sono del<br />
tipo “adesso senti questa”; altre sono dei promemoria; altre riportano dei punti che ci<br />
siamo scordati di inserire nel testo; (queste sono state segnalate dai tuoi colleghi studenti)<br />
alcune ti aggiornano sulle ricerche di chimica in corso attualmente e altre, probabilmente<br />
meno di quante noi riteniamo, sono inserite a scopo umoristico. Prova a vedere la nota sul<br />
pattinaggio a pagina 239: WLM è ancora convinto che sia terribilmente spiritosa.<br />
<strong>Chimica</strong>: il lato umano<br />
In tutto il testo, delle sezioni con questo titolo riportano brevi biografie dei pionieri della<br />
chimica. Enfatizzano non soltanto i risultati da loro ottenuti, ma anche le loro personalità.<br />
<strong>Chimica</strong> fuori dall'aula<br />
Ogni capitolo contiene una sezione “<strong>Chimica</strong> fuori dall'aula”. È un contributo che illustra<br />
un esempio o dell'uso della chimica nel mondo che ci circonda o un'area di ricerca attuale.<br />
Non interferisce nella spiegazione dei concetti, quindi non ti distrarrà. Però ti promettiamo<br />
che questi inserti – se li leggerai – aumenteranno la tua cultura scientifica.<br />
Sommario del capitolo<br />
Una revisione è sempre utile, non soltanto per rinfrescarti la memoria, ma anche per organizzare<br />
il tuo tempo e gli appunti per prepararti all'esame. Il sommario del capitolo include:<br />
■<br />
■<br />
■<br />
I Termini Chiave del capitolo. Se un particolare termine non ti è familiare, fai riferimento<br />
all'indice analitico al termine del libro. Troverai il termine nel glossario incluso<br />
nell'indice ed anche le pagine del testo nelle quali quel termine appare (se ti servissero<br />
ulteriori spiegazioni).<br />
I Concetti Chiave e le Equazioni chiave del capitolo. Questi sono elencati con i corrispondenti<br />
esempi ed i problemi a fine capitolo. Se hai difficoltà nel risolvere un particolare problema,<br />
ti può essere d'aiuto rivedere l'argomento e l'esempio che riguarda quel concetto.<br />
Ogni capitolo è riassunto da un Problema riassuntivo organizzato in diversi step che<br />
copre tutti o quasi tutti i concetti chiave del capitolo. Puoi valutare la tua comprensione<br />
del capitolo lavorando su questo problema. Uno dei principali vantaggi dei problemi<br />
riassuntivi è che legano assieme diverse idee, mostrando come si correlano le une alle<br />
altre. Un docente di esperienza che insegni chimica generale ed usi questo libro potrà<br />
dire alla sua classe: “se potete risolvere il problema riassuntivo senza aiuto, allora siete<br />
pronti all'esame per quanto riguarda quel capitolo”.<br />
Quesiti e problemi<br />
Al termine di ogni capitolo c'è una serie di quesiti e problemi che il tuo docente ti può assegnare<br />
come compiti per casa. Sono anche utili per verificare la profondità della tua conoscenza<br />
degli argomenti del capitolo. Queste serie includono:<br />
■ Quesiti che testino la tua conoscenza del vocabolario specializzato che i chimici usano<br />
(per esempio scrivere i nomi delle formule, scrivere l'equazione chimica della reazione<br />
che viene descritta).<br />
xx<br />
Per lo studente
■<br />
■<br />
■<br />
■<br />
■<br />
Problemi quantitativi che richiedono una calcolatrice ed alcune manipolazioni algebriche.<br />
Problemi classificati che danno inizio alla serie e sono raggruppati per tipo sotto un<br />
particolare titolo che indica l'argomento del capitolo cui si riferiscono. I problemi classificati<br />
sono raggruppati a coppie. Il secondo membro di ciascuna coppia illustra lo<br />
stesso principio del primo. Questo significa avere più di una opportunità per metterti<br />
alla prova. Il secondo problema (di numero pari) è evidenziato dal colore del suo numero<br />
e la sua risposta è riportata nell'appendice 6. Se il tuo docente ti assegna i problemi<br />
di numero dispari senza soluzione per casa, aspetta finché la soluzione del problema<br />
verrà discussa in classe, e intanto risolvi quello corrispondente di numero pari<br />
per capire se sai come risolvere un problema di quel tipo.<br />
Ogni capitolo contiene inoltre un numero più ridotto di problemi non classificati, che<br />
possono richiedere più di un concetto, inclusi, forse, anche alcuni dei capitoli precedenti.<br />
I quesiti concettuali verificano la tua comprensione dei principi. Non è necessaria (o almeno<br />
non dovrebbe essere necessaria) una calcolatrice per rispondere a queste domande.<br />
La sezione dei problemi sfida presenta problemi che richiedono competenze più avanzate<br />
e/o impegno e riflessione. La risposta a tutti questi problemi è in appendice 6.<br />
Appendici<br />
Le appendici alla fine del libro danno non soltanto le risposte ai quesiti e problemi di numero<br />
pari, ma contengono dei materiali integrativi che puoi trovare utili. Tra questi ci sono:<br />
■ L'appendice 1, che contiene un richiamo sulle unità del SI, oltre a tabelle di dati termodinamici<br />
e di costanti di equilibrio.<br />
■ L'appendice 3, che contiene dei richiami sulla matematica di cui hai bisogno in chimica<br />
generale. Particolare enfasi viene posta sulla notazione esponenziale e sui logaritmi<br />
(naturali e in base 10).<br />
Per lo studente<br />
xxi