I materiali possono essere: Amorfi: gli atomi sono disposti in modo ...
I materiali possono essere: Amorfi: gli atomi sono disposti in modo ...
I materiali possono essere: Amorfi: gli atomi sono disposti in modo ...
- No tags were found...
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
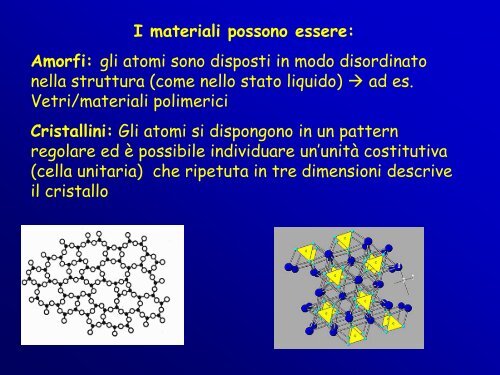
I <strong>materiali</strong> <strong>pos<strong>sono</strong></strong> <strong>essere</strong>:<strong>Amorfi</strong>: <strong>gli</strong> <strong>atomi</strong> <strong>sono</strong> <strong>disposti</strong> <strong>in</strong> <strong>modo</strong> disord<strong>in</strong>atonella struttura (come nello stato liquido) ad es.Vetri/<strong>materiali</strong> polimericiCristall<strong>in</strong>i: Gli <strong>atomi</strong> si dispongono <strong>in</strong> un patternregolare ed è possibile <strong>in</strong>dividuare un’unità costitutiva(cella unitaria) che ripetuta <strong>in</strong> tre dimensioni descriveil cristallo
Sistemi amorfiSi def<strong>in</strong>iscono amorfi i sistemi <strong>in</strong> cu<strong>in</strong>on vi è un ord<strong>in</strong>e strutturaleperiodico Le molecole costituenti il solidorisultano <strong>essere</strong> orientate <strong>in</strong> <strong>modo</strong>essenzialmente disord<strong>in</strong>ato (casuale)tra loroMMMMMMMMMMMMM
Sistemi cristall<strong>in</strong>iUn solido è def<strong>in</strong>ito cristall<strong>in</strong>oquando è possibile riconoscere <strong>in</strong>esso una regolarità strutturale(ord<strong>in</strong>e spaziale) che siriproduce periodicamente nellospazio
Lo stato solidoDist<strong>in</strong>guiamo essenzialmente quattro classi di sistemisolidi <strong>in</strong> base ai legami che sussistono tra le loroparticelle:Solidi ioniciSolidi molecolariSolidi covalenti o reticolariSolidi metallici
Solidi metallicimetalli: <strong>sono</strong> costituiti da cationi metallici tenuti<strong>in</strong>sieme da un mare di elettroni; malleabili,duttili,conducono l'elettricità ed il calore Legame metallico Opacità e lucentezza Densità elevata Conducibilità elettrica etermica Duri, duttili, malleabili,elastici
Struttura compatta
Numero dicoord<strong>in</strong>azione12Struttura esagonale compatta
Numero dicoord<strong>in</strong>azione12Struttura cubica compatta
Conducibilitàelettrica etermica<strong>in</strong>ferioriLega di sostituzione
Lega <strong>in</strong>terstiziale r A ≤ 60% r B
Reticoli di Bravais
Il tipo di cella elementare adottato da unmetallo si determ<strong>in</strong>a mediante misure di densità
Solidi ioniciSono contraddist<strong>in</strong>ti essenzialmente dalleseguenti proprietà: Cristall<strong>in</strong>i Fragili Altobollenti Conduttori allo stato fusoNaCl, KNO 3 , CuSO 4·5H 2 O
Numero di coord<strong>in</strong>azione 6,6
Numero di coord<strong>in</strong>azione 8,8
Solidi molecolariBeCl 2 , S 8 ,P 4 , I 2 ,ghiaccio,glucosioSono solidi <strong>in</strong> cui, nel caso cristall<strong>in</strong>o, le unità molecolari siimpaccano ord<strong>in</strong>atamente <strong>in</strong> un reticolo cristall<strong>in</strong>o (si riscontraperiodicità spaziale) e <strong>sono</strong> tenute <strong>in</strong>sieme dalle diverse<strong>in</strong>terazioni <strong>in</strong>termolecolari operanti nel cristallo.
Solidi covalentiDiamanteGrafiteSono strutture costituite da un reticolo <strong>in</strong>def<strong>in</strong>ito di<strong>atomi</strong> legati fra loro <strong>in</strong> <strong>modo</strong> covalente, come ad esempioavviene per <strong>gli</strong> <strong>atomi</strong> di carbonio ne<strong>gli</strong> allotropi deldiamante e dei piani reticolari della grafite.
Fase nematica
Fase smectica
Fase colesterica
Cristalli liquidi Liotropici
Lo stato liquidoLe molecole dei liquidi <strong>sono</strong> a contatto tra loro,dato che le <strong>in</strong>terazioni <strong>sono</strong> più forti che nei gas,ma libere di scorrere e rotolare rispetto alleproprie vic<strong>in</strong>e.All'aumentare delle <strong>in</strong>terazioni aumenta laviscosità del liquido, f<strong>in</strong>o alla solidificazione.
In un recipiente chiuso:V evaporazione = V condensazioneQuando si raggiungono le condizioni di equilibrio, lapressione esercitata dalle molecole nella fase vapore èchiamata Pressione di vapore del liquido.
Equazione di Clausius-Clapeyron
Si def<strong>in</strong>isce viscosità di un liquido la sua resistenza allo scorrimentoLo zolfo fa eccezione!