Tópico 4 - Editora Saraiva
Tópico 4 - Editora Saraiva
Tópico 4 - Editora Saraiva
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
80 PARTE I – TERMOLOGIA<br />
a)<br />
19,68<br />
9,84<br />
b)<br />
39,36<br />
9,84<br />
c)<br />
14,76<br />
9,84<br />
P (atm)<br />
0 3 6 V ()<br />
P (atm)<br />
0 3 6 V ()<br />
P (atm)<br />
d)<br />
9,84<br />
4,92<br />
e)<br />
9,84<br />
2,46<br />
P (atm)<br />
0 3 6 V ()<br />
P (atm)<br />
0 3 6 V ()<br />
0 3 6 V ()<br />
Resolução:<br />
Na primeira transformação (isométrica), podemos aplicar a Equação de<br />
Clapeyron para o cálculo do volume do gás ideal: p V = n R T<br />
9,84 V = 1 · 0,082 · 360 ⇒ V = 3,0 L<br />
Na segunda transformação (isotérmica), o diagrama é expresso por:<br />
P (atm)<br />
9,84<br />
4,92<br />
0 3,0 6,0 V ()<br />
Observemos que, na transformação isotérmica, quando duplicamos o<br />
volume, a pressão cai à metade do valor inicial.<br />
Resposta: d<br />
80 (Ufl a-MG) A teoria cinética dos gases propõe um modelo microscópico<br />
para um gás ideal, baseado nas leis da mecânica e em alguns<br />
postulados. Admite-se que o gás é composto de um grande número<br />
de partículas separadas por distâncias consideráveis, se comparadas<br />
às dimensões dessas partículas. Estas se movimentam rapidamente e<br />
ao acaso, não exercendo forças entre si, exceto quando colidem. Por<br />
f im, admite-se também que as colisões entre as partículas, ou com<br />
as paredes do recipiente que as contém, são perfeitamente elásticas.<br />
Dessa forma, o gráf ico que melhor representa a relação entre a energia<br />
cinética média (E) do gás e sua temperatura é:<br />
a)<br />
c)<br />
e)<br />
E<br />
E<br />
E<br />
b)<br />
E<br />
T<br />
T<br />
d)<br />
E<br />
i<br />
T<br />
T<br />
f<br />
T<br />
Resolução:<br />
E = cm 3<br />
k T<br />
2<br />
Resposta: a<br />
E<br />
0<br />
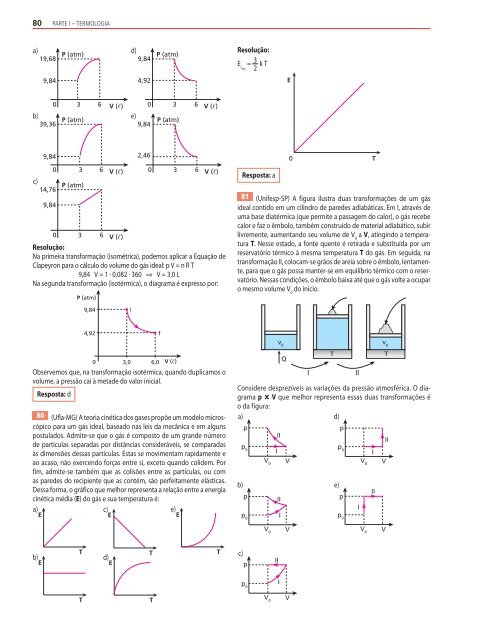
81 (Unifesp-SP) A f igura ilustra duas transformações de um gás<br />
ideal contido em um cilindro de paredes adiabáticas. Em I, através de<br />
uma base diatérmica (que permite a passagem do calor), o gás recebe<br />
calor e faz o êmbolo, também construído de material adiabático, subir<br />
livremente, aumentando seu volume de V 0 a V, atingindo a temperatura<br />
T. Nesse estado, a fonte quente é retirada e substituída por um<br />
reservatório térmico à mesma temperatura T do gás. Em seguida, na<br />
transformação II, colocam-se grãos de areia sobre o êmbolo, lentamente,<br />
para que o gás possa manter-se em equilíbrio térmico com o reservatório.<br />
Nessas condições, o êmbolo baixa até que o gás volte a ocupar<br />
o mesmo volume V 0 do início.<br />
v 0<br />
Q<br />
I II<br />
T<br />
v 0<br />
T T<br />
Considere desprezíveis as variações da pressão atmosférica. O diagrama<br />
p V que melhor representa essas duas transformações é<br />
o da f igura:<br />
a)<br />
d)<br />
p<br />
p<br />
II<br />
II<br />
p0 I<br />
p0 I<br />
V<br />
V<br />
b)<br />
c)<br />
p<br />
p 0<br />
p<br />
p 0<br />
V 0<br />
V 0<br />
V 0<br />
II<br />
II<br />
I<br />
I<br />
V<br />
V<br />
e)<br />
p<br />
p 0<br />
I<br />
V 0<br />
V 0<br />
II<br />
V