2010 - 1º Ano (Prova) - ITnet
2010 - 1º Ano (Prova) - ITnet
2010 - 1º Ano (Prova) - ITnet
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
1<br />
H<br />
1,01<br />
3<br />
Li<br />
6,94<br />
11<br />
Na<br />
23,0<br />
19<br />
K<br />
39,1<br />
37<br />
Rb<br />
85,5<br />
55<br />
Cs<br />
133<br />
87<br />
1<br />
Fr<br />
(223)<br />
IA VIIIA<br />
2<br />
4<br />
2<br />
Be<br />
IIA<br />
9,01<br />
12<br />
Mg<br />
24,3<br />
20<br />
Ca<br />
40,1<br />
38<br />
Sr<br />
87,6<br />
56<br />
Ba<br />
137<br />
88<br />
Ra<br />
(226)<br />
Número Atômico<br />
Símbolo<br />
Massa Atômica<br />
( ) = Nº de massa do<br />
isótopo mais estável<br />
IIIB IVB VB VIB VIIB VIIIB VIII VIII IB IIB<br />
21<br />
Sc<br />
22<br />
Ti<br />
23<br />
V<br />
24<br />
Cr<br />
25<br />
Mn<br />
26<br />
Fe<br />
27<br />
Co<br />
28<br />
Ni<br />
29<br />
Cu<br />
30<br />
Zn<br />
45,0 47,9 50,9 52,0 54,9 55,8 58,9 58,7 63,5 65,4<br />
39 40 41 42 43 44 45 46 47 48<br />
Y Zr Nb Mo Tc Ru Rh Pd Ag Cd<br />
88,9 91,2 92,9 96,0 (99) 101 103 106 108 112<br />
57-71 72 73 74 75 76 77 78 79 80<br />
Hf Ta W Re Os Ir Pt Au Hg<br />
179 181 184 186 190 192 195 197 201<br />
Série dos<br />
Lantanídeos<br />
89-103<br />
Série dos<br />
Actinídeos<br />
31. Considere a seguinte composição do ar atmosférico seco:<br />
Componente % (em volume)<br />
N 2<br />
O 2<br />
104<br />
78<br />
21<br />
Ar 0,9<br />
CO 2 0,03<br />
Outros Gases Traços<br />
Analise as afirmativas abaixo.<br />
105 106 107 108 109<br />
Rf Db Sg Bh Hs Mt<br />
Série dos Lantanídeos<br />
57<br />
La<br />
139<br />
Série dos Actinídeos<br />
89<br />
Ac<br />
(227)<br />
58<br />
Ce<br />
140<br />
90<br />
Th<br />
232<br />
0 0 - O ar atmosférico é uma mistura de substâncias<br />
simples e compostas.<br />
1 1 - Os componentes do ar podem ser separados por<br />
liquefação fracionada.<br />
2 2 - Os gases componentes do ar são formados somente<br />
por moléculas monoatômicas e diatômicas.<br />
3 3 - Uma amostra de ar contendo 100 litros de gás N ,<br />
2<br />
contém, aproximadamente, 27 litros de gás O .<br />
2<br />
4 4 - A combustão é um processo físico que pode ser uti-<br />
lizado para separar o gás O 2 dos demais componentes<br />
do ar.<br />
59<br />
Pr<br />
141<br />
91<br />
Pa<br />
(231)<br />
60<br />
Nd<br />
144<br />
92<br />
U<br />
238<br />
61<br />
Pm<br />
(147)<br />
93<br />
Np<br />
(237)<br />
QUÍMICA<br />
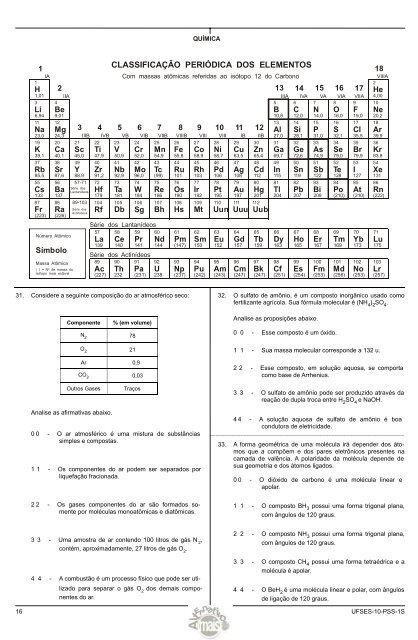
CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS<br />
Com massas atômicas referidas ao isótopo 12 do Carbono<br />
3 4 5 6 7 8 9 10 11 12<br />
62<br />
Sm<br />
150<br />
94<br />
Pu<br />
(242)<br />
110 111 112<br />
Uun Uuu Uub<br />
32. O sulfato de amônio, é um composto inorgânico usado como<br />
fertilizante agrícola. Sua fórmula molecular é (NH 4) 2SO 4.<br />
Analise as proposições abaixo.<br />
0 0 - Esse composto é um óxido.<br />
1 1 - Sua massa molecular corresponde a 132 u.<br />
2 2 - Esse composto, em solução aquosa, se comporta<br />
como base de Arrhenius.<br />
3 3 - O sulfato de amônio pode ser produzido através da<br />
reação de dupla troca entre H 2 SO<br />
4 e NaOH.<br />
4 4 - A solução aquosa de sulfato de amônio é boa<br />
condutora de eletricidade.<br />
________________________________________________________________<br />
33. A forma geométrica de uma molécula irá depender dos átomos<br />
que a compõem e dos pares eletrônicos presentes na<br />
camada de valência. A polaridade da molécula depende de<br />
sua geometria e dos átomos ligados.<br />
0 0 - O dióxido de carbono é uma molécula linear e<br />
apolar.<br />
1 1 - O composto BH 3 possui uma forma trigonal plana,<br />
com ângulos de 120 graus.<br />
2 2 - O composto NH 3 possui uma forma trigonal plana,<br />
com ângulos de 120 graus.<br />
3 3 - O composto CH 4 possui uma forma tetraédrica e a<br />
molécula é apolar.<br />
4 4 - O BeH<br />
2 é uma molécula linear e polar, com ângulos<br />
de ligação de 120 graus.<br />
16 UFSES-10-PSS-1S<br />
63<br />
Eu<br />
152<br />
95<br />
Am<br />
(243)<br />
64<br />
Gd<br />
157<br />
96<br />
Cm<br />
(247)<br />
65<br />
Tb<br />
159<br />
97<br />
Bk<br />
(247)<br />
13 14 15 16 17<br />
5<br />
B<br />
10,8<br />
13<br />
Al<br />
27,0<br />
31<br />
Ga<br />
69,7<br />
49<br />
In<br />
115<br />
81<br />
Tl<br />
204<br />
66<br />
Dy<br />
163<br />
98<br />
Cf<br />
(251)<br />
IIIA IVA VA VIA VIIA<br />
6 7 8 9<br />
C<br />
12,0<br />
14<br />
Si<br />
28,1<br />
32<br />
Ge<br />
72,6<br />
50<br />
Sn<br />
119<br />
82<br />
Pb<br />
207<br />
67<br />
Ho<br />
165<br />
99<br />
Es<br />
(254)<br />
N<br />
14,0<br />
15<br />
P<br />
31,0<br />
33<br />
As<br />
74,9<br />
51<br />
Sb<br />
122<br />
83<br />
Bi<br />
209<br />
68<br />
Er<br />
167<br />
100<br />
Fm<br />
(253)<br />
O<br />
16,0<br />
16<br />
S<br />
32,1<br />
34<br />
Se<br />
79,0<br />
52<br />
Te<br />
128<br />
84<br />
Po<br />
(210)<br />
69<br />
Tm<br />
169<br />
101<br />
Md<br />
(256)<br />
F<br />
19,0<br />
17<br />
Cl<br />
35,5<br />
35<br />
Br<br />
79,9<br />
53<br />
I<br />
127<br />
85<br />
At<br />
(210)<br />
70<br />
Yb<br />
173<br />
102<br />
No<br />
(253)<br />
18<br />
He<br />
4,00<br />
10<br />
Ne<br />
20,2<br />
18<br />
Ar<br />
39,9<br />
36<br />
Kr<br />
83,8<br />
54<br />
Xe<br />
131<br />
86<br />
Rn<br />
(222)<br />
71<br />
Lu<br />
175<br />
103<br />
Lr<br />
(257)