Humant papillomvirus och kampen mot cancer
Humant papillomvirus och kampen mot cancer
Humant papillomvirus och kampen mot cancer
- No tags were found...
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
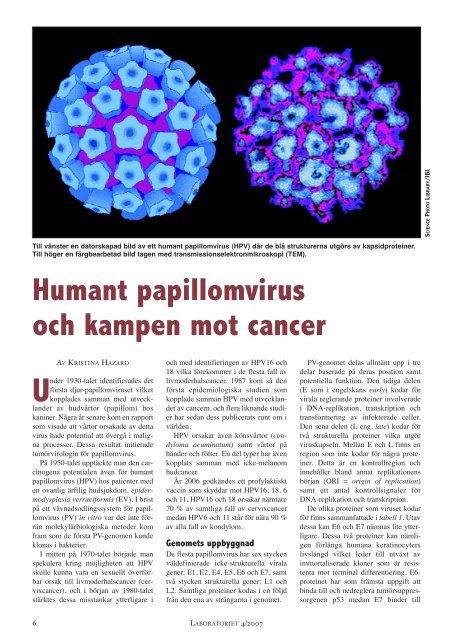
SCIENCE PHOTO LIBRARY/IBL<br />
Till vänster en datorskapad bild av ett humant <strong>papillomvirus</strong> (HPV) där de blå strukturerna utgörs av kapsidproteiner.<br />
Till höger en färgbearbetad bild tagen med transmissionselektronmikroskopi (TEM).<br />
<strong>Humant</strong> <strong>papillomvirus</strong><br />
<strong>och</strong> <strong>kampen</strong> <strong>mot</strong> <strong>cancer</strong><br />
AV KRISTINA HAZARD<br />
Under 1930-talet identifierades det<br />
första djur-<strong>papillomvirus</strong>et vilket<br />
kopplades samman med utvecklandet<br />
av hudvårtor (papillom) hos<br />
kaniner. Några år senare kom en rapport<br />
som visade att vårtor orsakade av detta<br />
virus hade potential att övergå i maligna<br />
processer. Dessa resultat initierade<br />
tumörvirologin för <strong>papillomvirus</strong>.<br />
På 1950-talet upptäckte man den carcinogena<br />
potentialen även för humant<br />
<strong>papillomvirus</strong> (HPV) hos patienter med<br />
en ovanlig ärftlig hudsjukdom, epidermodysplasia<br />
verruciformis (EV). I brist<br />
på ett vävnadsodlingssystem för <strong>papillomvirus</strong><br />
(PV) in vitro var det inte förrän<br />
molekylärbiologiska metoder kom<br />
fram som de första PV-genomen kunde<br />
klonas i bakterier.<br />
I mitten på 1970-talet började man<br />
spekulera kring möjligheten att HPV<br />
skulle kunna vara en sexuellt överförbar<br />
orsak till livmoderhals<strong>cancer</strong> (cervix<strong>cancer</strong>),<br />
<strong>och</strong> i början av 1980-talet<br />
stärktes dessa misstankar ytterligare i<br />
<strong>och</strong> med identifieringen av HPV16 <strong>och</strong><br />
18 vilka förekommer i de flesta fall av<br />
livmoderhals<strong>cancer</strong>. 1987 kom så den<br />
första epidemiologiska studien som<br />
kopplade samman HPV med utvecklandet<br />
av <strong>cancer</strong>n, <strong>och</strong> flera liknande studier<br />
har sedan dess publicerats runt om i<br />
världen.<br />
HPV orsakar även könsvårtor (condyloma<br />
acuminatum) samt vårtor på<br />
händer <strong>och</strong> fötter. En del typer har även<br />
kopplats samman med icke-melanom<br />
hud<strong>cancer</strong>.<br />
År 2006 godkändes ett profylaktiskt<br />
vaccin som skyddar <strong>mot</strong> HPV16, 18, 6<br />
<strong>och</strong> 11. HPV16 <strong>och</strong> 18 orsakar närmare<br />
70 % av samtliga fall av cervix<strong>cancer</strong><br />
medan HPV6 <strong>och</strong> 11 står för nära 90 %<br />
av alla fall av kondylom.<br />
Genomets uppbyggnad<br />
De flesta <strong>papillomvirus</strong> har sex stycken<br />
väldefinierade icke-strukturella virala<br />
gener: E1, E2, E4, E5, E6 <strong>och</strong> E7, samt<br />
två stycken strukturella gener: L1 <strong>och</strong><br />
L2. Samtliga proteiner kodas i en följd<br />
från den ena av strängarna i genomet.<br />
PV-genomet delas allmänt upp i tre<br />
delar baserade på deras position samt<br />
potentiella funktion. Den tidiga delen<br />
(E som i engelskans early) kodar för<br />
virala reglerande proteiner involverade<br />
i DNA-replikation, transkription <strong>och</strong><br />
transformering av infekterade celler.<br />
Den sena delen (L eng. late) kodar för<br />
två strukturella proteiner vilka utgör<br />
viruskapseln. Mellan E <strong>och</strong> L finns en<br />
region som inte kodar för några proteiner.<br />
Detta är en kontrollregion <strong>och</strong><br />
innehåller bland annat replikationens<br />
början (ORI = origin of replication)<br />
samt ett antal kontrollsignaler för<br />
DNA-replikation <strong>och</strong> transkription.<br />
De olika proteiner som viruset kodar<br />
för finns sammanfattade i tabell 1. Utav<br />
dessa kan E6 <strong>och</strong> E7 nämnas lite ytterligare.<br />
Dessa två proteiner kan nämligen<br />
förlänga humana keratinocyters<br />
livslängd vilket leder till utväxt av<br />
immortaliserade kloner som är resistenta<br />
<strong>mot</strong> terminal differentiering. E6-<br />
proteinet har som främsta uppgift att<br />
binda till <strong>och</strong> nedreglera tumörsuppressorgenen<br />
p53 medan E7 binder till<br />
6 LABORATORIET 4/2007
TABELL 1. Virala proteiner <strong>och</strong> deras funktion.<br />
Protein<br />
Funktion/egenskaper<br />
E6 Inaktiverar tumörsuppressorproteinet p53.<br />
Onkogent protein.<br />
E7<br />
E1<br />
E2<br />
E4<br />
E5<br />
L2<br />
L1<br />
Inaktiverar pRb. Onkogent protein.<br />
Största proteinet i genomet. Enda proteinet med<br />
enzymatisk aktivitet (ATPas <strong>och</strong> DNA helikas).<br />
Viktigt för virusets replikation.<br />
Reglerar viral transkription <strong>och</strong> replikation.<br />
Överlappar E2 proteinet. Okänd funktion.<br />
Uttrycks av de typer som infekterar slemhinnor,<br />
men inte av hudtyper.<br />
Utgör del av kapseln. Stabiliserar tomma viruspartiklar<br />
bildade av L1.<br />
Utgör cirka 80 % av kapseln.<br />
Kan bilda tomma viruspartiklar.<br />
Datorskapad modell, baserad på<br />
röntgenkristallografi, av ett komplex<br />
av kapsidproteinet L1. Sådana<br />
komplex liknar HPV <strong>och</strong> bildas<br />
spontant av L1-proteiner, vilket har<br />
utnyttjats för att skapa vaccin <strong>mot</strong><br />
viruset.<br />
tumör-suppressorproteinet retinoblastom<br />
(pRb). Dessa båda moment påverkar<br />
värdcellens cellcykel vilken förs in<br />
i S-fas (mitos).<br />
Fylogeni<br />
Papillomvirus grupperas inte serologiskt,<br />
utan klassificeras genom arten<br />
som infekteras samt identiteten av<br />
virusgenomet i jämförelse med andra<br />
PV-typer, se tabell 2. År 2004 introducerades<br />
ett nytt klassificeringssystem,<br />
<strong>och</strong> numera delas de olika typerna i<br />
olika genus ex. Alfa-, Beta- <strong>och</strong><br />
Gamma-<strong>papillomvirus</strong>. Varje genus<br />
delas vidare in i species innehållande en<br />
eller flera genotyper. Utöver genotyper<br />
grupperas <strong>papillomvirus</strong>en även in i<br />
subtyper <strong>och</strong> varianter.<br />
Till dags dato har mer än 100 olika<br />
genotyper av humant <strong>papillomvirus</strong><br />
identifierats <strong>och</strong> karakteriserats, d v s<br />
hela genomet har klonats <strong>och</strong> sekvensbestämts.<br />
Papillomvirus kodar inte sitt eget<br />
DNA-polymeras utan använder sig av<br />
värdcellens enzym för replikation av<br />
det virala genomet. Detta medför att<br />
viruset även nyttjar korrekturläsning<br />
samt DNA-reparationsmekanismer<br />
efter replikation som värdcellens DNA<br />
polymeras utför. Detta bidrar i allra<br />
högsta grad till den stabilitet som<br />
karakteriserar <strong>papillomvirus</strong>.<br />
Rekombination mellan olika genotyper<br />
har inte påvisats <strong>och</strong> därav kan man<br />
sluta sig till att de olika typer som cirkulerar<br />
idag bland annat har genererats<br />
genom långsam ackumulering av mutationer.<br />
Virusets livscykel<br />
Papillomvirusens livscykler är nära länkat<br />
med differentieringsprogrammet<br />
hos värdcellen. I avseende att inducera<br />
en persistent infektion måste viruset<br />
infektera basalcellerna i epitelet eftersom<br />
de är de enda som har förmåga att<br />
TABELL 2. Klassificeringsschema för <strong>papillomvirus</strong> baserat på identitet i<br />
L1-genens sekvens.<br />
Klassificeringsgrupp<br />
Sekvenslikhet i L1-proteinet<br />
Genus < 60 %<br />
Species 60 – 70 %<br />
Genotyp 70 – 90 %<br />
Subtyp 90 – 98 %<br />
Variant 98 – 99 %<br />
genomgå fullständig differentiering.<br />
DNA-syntes, syntes av kapselprotein<br />
samt ansamling av virusproteiner sker<br />
dock uteslutande i differentierade keratinocyter.<br />
På grund av den strikta kopplingen<br />
till differentierade celler har den<br />
replikativa fasen av <strong>papillomvirus</strong>ens<br />
livscykel varit svår att studera.<br />
Virusen når troligtvis basalcellerna<br />
antingen genom små sår, s.k. mikrotraumas,<br />
i huden eller slemhinnan eller<br />
via hårsäckar. Receptorn vilken förmedlar<br />
<strong>papillomvirus</strong>ens intrång i cellerna<br />
är inte känd, men vidhäftning av<br />
viruset till cellytan har tillskrivits ett<br />
par möjliga receptorer, ex. heparinytproteoglykaner.<br />
Efter vidhäftningen internaliseras<br />
viruset från cellytan <strong>och</strong> transporteras<br />
till endosomer. L2-proteinet förstör<br />
sedan endosom-membranet <strong>och</strong> det<br />
virala genomet förs med hjälp av L2 till<br />
värdcellens kärna. Väl där replikerar<br />
viruset till 50-100 kopior vartefter det<br />
slår sig till ro som en stabil episom<br />
(vilofas). Nästa steg sker i delande<br />
basalceller i nedre delen av epidermis.<br />
I dessa celler förhåller sig det virala<br />
DNAt som en stabil multikopie-plasmid.<br />
Det virala genomet delar sig i snitt<br />
en gång per cellcykel under S-fas, i synkroni<br />
med värdkromosomerna. Denna<br />
typ av DNA-replikation medför en persistent<br />
latent infektion i stamcellerna i<br />
epidermis.<br />
Den tredje typen av replikation sker i<br />
de mer differentierade epitelcellerna.<br />
Dessa celler genomgår inte längre cel-<br />
LABORATORIET 4/2007 7
Faktaruta<br />
Papillomvirus<br />
●<br />
●<br />
●<br />
●<br />
●<br />
●<br />
Tillhör familjen Papillomaviridae.<br />
Små virus. Viruskapseln mäter ca 55 nm i diameter <strong>och</strong><br />
innehåller en molekyl av det dubbelsträngade DNAt<br />
bestående av ca 8000 baspar (att jämföras med<br />
Herpesgruppens virus som varierar mellan 105 000 <strong>och</strong><br />
235 000 baspar i storlek).<br />
Saknar hölje.<br />
Infekterar en mängd olika arter – ex. människa, boskap,<br />
katter, kaniner <strong>och</strong> apor.<br />
Är artspecifika. Det finns inga kända fall där papillomavirus<br />
från en art orskar en infektion hos en annan art.<br />
Infekterar enbart epitelceller, antingen i slemhinnor eller<br />
på huden.<br />
lulär DNA-syntes, men det sker en<br />
explosion av viral DNA-syntes vilket<br />
resulterar i genom som är färdiga att<br />
packas i omogna viruspartiklar.<br />
Mekanismerna som reglerar övergången<br />
mellan den latenta fasen till<br />
viral DNA-replikation är inte kända.<br />
Papillomvirus är troligtvis inte cytolytiska,<br />
<strong>och</strong> frisläppandet av nya viruspartiklar<br />
sker inte förrän cellerna nått<br />
det yttersta cellagret av keratiniserade<br />
epitel.<br />
HPV-orsakade sjukdomar<br />
HPV är en av de vanligast sexuellt<br />
överförbara sjukdomsalstrarna världen<br />
över. Virusen delas in i antingen slemhinne-<br />
eller hudtyper beroende på vilket<br />
epitel de vanligtvis infekterar. Slemhinnetyperna<br />
infekterar genital hud, genitala<br />
samt icke-genitala slemhinnor.<br />
Dessa typer delas vidare in i högrisk<br />
respektive lågrisktyper med avseende<br />
på deras förmåga att inducera elakartade<br />
infektioner. Alla slemhinnetyper kan<br />
tillfälligt inducera cellulär proliferation,<br />
men det är bara högrisktyperna som har<br />
förmåga att förlänga livslängden <strong>och</strong><br />
därmed ge upphov till immortaliserade<br />
cellinjer som inte längre lyder under<br />
värdcellens differentieringssignaler.<br />
LIVMODERHALSCANCER<br />
(CERVIXCAN-<br />
CER). Livmoderhals<strong>cancer</strong> är den näst<br />
vanligaste <strong>cancer</strong>typen hos kvinnor<br />
världen över, <strong>och</strong> den vanligaste formen<br />
av <strong>cancer</strong> hos kvinnor i utvecklingsländer.<br />
Ungefär 85 % av cancrarna är skiv-<br />
epitelcancrar medan resten till största<br />
delen består av adenocarcinom.<br />
Etiologiskt har ett antal HPV-typer<br />
kopplats samman med utvecklandet av<br />
livmoderhals<strong>cancer</strong>. Exempelvis står<br />
det två högrisktyperna HPV16 <strong>och</strong> 18<br />
för ca 70 % av samtliga fall av <strong>cancer</strong>n<br />
i världen.<br />
En persisterande infektion med<br />
någon av högrisktyperna är en förutsättning<br />
för utvecklandet av <strong>cancer</strong>n, men<br />
även andra så kallade co-faktorer krävs.<br />
Exempel på dessa är bland annat mångfödslar,<br />
rökning, p-pilleranvändning<br />
samt andra sexuellt överförbara sjukdomar<br />
så som herpes simplex typ 2 <strong>och</strong><br />
Chlamydia trachomatis.<br />
GENITALA VÅRTOR (CONDYLOMA ACU-<br />
MINATUM). Lågrisktyperna HPV6 <strong>och</strong><br />
11 orsakar nära 90 % av samtliga fall av<br />
kondylom. De allra flesta av dessa<br />
infektioner är självläkande medan<br />
andra kräver en lokal behandling.<br />
I undantagsfall kan infektionen dock<br />
persistera <strong>och</strong> i vissa extrema fall även<br />
utvecklas till så kallade jättekondylom,<br />
Buschke-Löwensteintumörer.<br />
ORALA CANCRAR. Det är relativt vanligt<br />
med HPV-infektioner oralt, <strong>och</strong> HPV16<br />
<strong>och</strong> 18 är vanliga fynd i orala carcinom.<br />
Intressant är också det faktum att även<br />
de två lågrisktyperna HPV6 <strong>och</strong> 11 ofta<br />
återfinns i dessa infektioner.<br />
Ett annat sjukdomstillstånd som<br />
HPV orsakar oralt är respiratorisk<br />
papillomatos. Det är en ovanlig infektion<br />
som angriper luftvägarna <strong>och</strong> drabbar<br />
främst små barn. De flesta av dessa<br />
infektioner orsakas av HPV6 <strong>och</strong> 11,<br />
<strong>och</strong> i värsta fall kan infektionen leda till<br />
döden.<br />
HUDINFEKTIONER. Frisk hud hyser ett<br />
stort spektrum av olika HPV-typer <strong>och</strong><br />
den solbelysta pannan har visat sig<br />
innehålla större mängder virus än andra<br />
kroppsdelar så som armar <strong>och</strong> lår med<br />
betydligt mindre solexponering. Även<br />
dessa infektioner har visat sig persistera<br />
över en längre tid.<br />
HUDVÅRTOR. Vårtor på händer <strong>och</strong> fötter<br />
är inget ovanligt, <strong>och</strong> orsakas till<br />
stor del av HPV. De flesta infektionerna<br />
läker ut spontant, medan en del kan<br />
kvarstå på obestämd tid.<br />
En speciell typ av vårtor uppstår nästan<br />
uteslutande hos slaktare <strong>och</strong> kötthandlare,<br />
<strong>och</strong> orsakas av HPV7, en<br />
HPV-typ som normalt inte orsakar vårtor.<br />
Individer med nedsatt immunförsvar<br />
har en hög prevalens av HPV-orsakade<br />
godartade lesioner <strong>och</strong> tumörer. Detta<br />
är speciellt vanligt hos njurtransplanterade<br />
av vilka mer än 90 % utvecklar<br />
hudvårtor, <strong>och</strong> 40 % utvecklar hud<strong>cancer</strong><br />
inom 15 år efter transplantationen.<br />
Dessa siffror representerar 50-100<br />
gångers ökad risk jämfört med normalbefolkningen.<br />
EPIDERMODYSPLASIA<br />
VERRUCIFORMIS<br />
(EV). Sambandet mellan HPV <strong>och</strong> <strong>cancer</strong><br />
upptäcktes på 1950-talet hos individer<br />
med den ovanliga ärftliga sjukdomen<br />
EV. Hudcarcinom uppstår hos<br />
cirka en tredjedel av dessa patienter,<br />
<strong>och</strong> de uppstår främst på solbelyst hud.<br />
HPV5 <strong>och</strong> 8 associeras med hud<strong>cancer</strong><br />
med sitt ursprung i benigna lesioner hos<br />
dessa patienter. EV-specifika HPVtyper<br />
<strong>och</strong>/eller antikroppar <strong>mot</strong> dessa<br />
har också påvisats hos individer med<br />
psoriasis <strong>och</strong> andra tillstånd med snabb<br />
epidermal cellproliferation. Sambandet<br />
mellan HPV <strong>och</strong> dessa tillstånd är dock<br />
oklart.<br />
HUDCANCER. Icke-melanom hud<strong>cancer</strong><br />
(eng. non-melanoma skin <strong>cancer</strong> =<br />
NMSC) är den vanligaste <strong>cancer</strong>former<br />
hos kaukasier, <strong>och</strong> en ökad prevalens<br />
har setts i Europa under de senaste åren.<br />
NMSC innefattar basalcells<strong>cancer</strong><br />
(BCC) <strong>och</strong> skivepitel<strong>cancer</strong> (SCC), <strong>och</strong><br />
den normala ration dem emellan är 1:4.<br />
NMSC är 18-20 gånger vanligare än<br />
8 LABORATORIET 4/2007
malignt melanom. Det finns inga kända<br />
förstadier till BCC, medan SCC föregås<br />
av aktiniska keratoser <strong>och</strong>/eller SCC in<br />
situ. BCC har en relativt god prognos<br />
medan SCC svara för ca 20 % av samtliga<br />
dödsfall av hud<strong>cancer</strong>.<br />
Epidemiologiskt är hud<strong>cancer</strong> kopplat<br />
till UV-strålningen från solen. Vidare<br />
är ljus hy samt immunstatusen hos<br />
individen riskfaktorer. Immunosupprimerade<br />
individer har upp till 100 gånger<br />
ökad risk för SCC jämfört med 10<br />
gånger ökad risk för BCC, vilket resulterar<br />
i ett omvänt ratio av SCC <strong>och</strong><br />
BCC jämfört med normalbefolkningen.<br />
Ett flertal studier har visat på förekomst<br />
av HPV i icke-melanom hud<strong>cancer</strong>.<br />
Världen över jobbar forskare med<br />
att undersöka huruvida HPV har del i<br />
<strong>cancer</strong>ns utveckling, eller om viruset<br />
helt enkelt bara utnyttjar det faktum att<br />
den normala cellcykeln slagits ut av<br />
tumörcellerna.<br />
Immunologi<br />
Papillomvirus infekterar epiteliala<br />
basalceller, men produktionen <strong>och</strong><br />
uttrycket av de flesta virala proteinerna<br />
samt packningen av virala delar sker i<br />
de yttersta lagren av epitelet. Tidsspannet<br />
från infektion till avknoppning av<br />
nya viruspartiklar är ca 3 veckor, vilket<br />
<strong>mot</strong>svarar den tid som krävs för de<br />
basala keratinocyterna att genomgå<br />
komplett proliferation.<br />
Eftersom <strong>papillomvirus</strong> inte infekterar<br />
<strong>och</strong> replikerar i antigenpresenterande<br />
celler i epitelet, <strong>och</strong> viruset inte lyserar<br />
värdcellen för att sprida nya viruspartiklar<br />
finns det inte någon chans för<br />
antigen-presenterande celler att plocka<br />
upp <strong>och</strong> sedan presentera virala antigen<br />
till det övriga immunförsvaret. Vidare<br />
orsakar inte viruset någon blodburen<br />
fas, <strong>och</strong> därför har immunsystemet<br />
utanför epitelet små chanser att hitta<br />
viruset. Därav följer att en HPV-infektion<br />
inte orsakar någon inflammation,<br />
<strong>och</strong> det avges heller ingen uppenbar<br />
signal till immunsystemet om virusets<br />
närvaro. Detta resulterar i persistenta,<br />
kroniska infektioner <strong>och</strong> individen kan<br />
förbli omedveten om infektionen under<br />
en längre tid.<br />
Allmänt brukar man säga att en<br />
infektion med en genital högrisktyp<br />
persisterar i 12-18 månader innan den<br />
läker ut. Detta är betydligt längre än de<br />
5-6 månader som krävs för en infektion<br />
med en lågrisktyp.<br />
Ett fullt fungerande immunsystem<br />
verkar vara nödvändigt för att läka ut en<br />
HPV-infektion i epidermis. Detta kan<br />
enkelt illustreras med betydelsen av det<br />
cellmedierad immunsvaret i läkningsprocessen<br />
<strong>och</strong> kontrollen av HPVinfektioner<br />
hos immunosupprimerade<br />
patienter, av vilka ca 70 % utvecklar<br />
hudvårtor.<br />
Det humorala immunsystemet är av<br />
vikt för neutralisation <strong>och</strong> inaktivering<br />
av virioner, vilket hindrar att viruset<br />
sprids inom individen vilket i sin tur<br />
reducerar sannolikheten för en re-infektion.<br />
En genital HPV-infektion ger upphov<br />
till serumantikroppar hos de flest men<br />
inte alla infekterade individer. Förekomsten<br />
av HPV-antikroppar är långlivad,<br />
men den bidrar inte till att en<br />
etablerad infektion läker ut.<br />
Virus-neutraliserande anti-L1-antikroppar<br />
genereras <strong>mot</strong> epitoper på ytan<br />
av viruskapseln <strong>och</strong> är typspecifika.<br />
Vaccin<br />
Nyligen godkändes ett profylaktiskt<br />
vaccin bestående av tomma viruspartiklar<br />
utan viralt DNA, så kallade viruslika<br />
partiklar (VLPs) av högrisktyperna<br />
HPV16 <strong>och</strong> 18 samt lågrisktyperna<br />
HPV6 <strong>och</strong> 11. Vaccinet har testats i<br />
flera studier <strong>och</strong> har visat sig resultera i<br />
en väsentlig nedgång i incidensen av<br />
HPV16 <strong>och</strong> 18-infektioner. Vaccinet<br />
har visat sig vara aktivt i upp till 36<br />
månader efter vaccinationstillfället.<br />
Ytterligare ett vaccin har producerats,<br />
men väntar fortfarande på godkännande.<br />
Detta andra vaccin bygger<br />
enbart på VLPs från HPV16 <strong>och</strong> 18,<br />
men har förutom skydd <strong>mot</strong> dessa två<br />
typer även visat på ett visst skydd <strong>mot</strong><br />
HPV31, 45 <strong>och</strong> 52.<br />
Kristina Hazard är biomedicinsk<br />
analytiker <strong>och</strong> disputerade den<br />
4 maj vid Universitetssjukhuset<br />
MAS, Malmö, på en avhandling<br />
med titeln ”Cutaneous Human<br />
Papillomaviruses”.<br />
LABORATORIET 4/2007 9