Φ Φ Φ Φ - FSB
Φ Φ Φ Φ - FSB
Φ Φ Φ Φ - FSB
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
Mirko Tadić<br />
Termodinamika<br />
6 Otvoreni sustavi<br />
Premda je teorija termodinamike postavljena na modelu zatvorenog sustava, dobivene<br />
termodinamičke relacije mogu se uz dodatne pretpostavke primijeniti i na tehnički značajnije<br />
otvorene sustave. Njih karakterizira protok mase, ṁ (kg/s), kroz granične plohe sustava, koji<br />
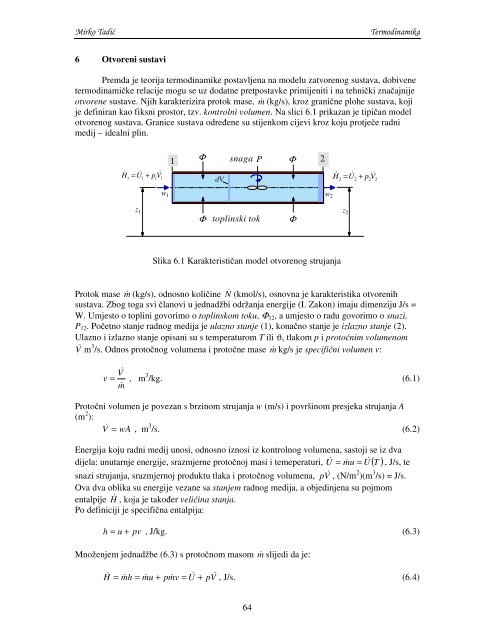
je definiran kao fiksni prostor, tzv. kontrolni volumen. Na slici 6.1 prikazan je tipičan model<br />
otvorenog sustava. Granice sustava određene su stijenkom cijevi kroz koju protječe radni<br />
medij – idealni plin.<br />
Ḣ ̇ +<br />
̇<br />
1<br />
= U1<br />
p1V<br />
1<br />
1<br />
Φ snaga P Φ 2<br />
dV<br />
Ḣ ̇ +<br />
̇<br />
2<br />
= U2<br />
p2V<br />
2<br />
w 1 w 2<br />
z 1 z 2<br />
Φ toplinski tok<br />
Φ<br />
Slika 6.1 Karakterističan model otvorenog strujanja<br />
Protok mase ṁ (kg/s), odnosno količine Ṅ (kmol/s), osnovna je karakteristika otvorenih<br />
sustava. Zbog toga svi članovi u jednadžbi održanja energije (I. Zakon) imaju dimenziju J/s =<br />
W. Umjesto o toplini govorimo o toplinskom toku, Φ 12 , a umjesto o radu govorimo o snazi,<br />
P 12 . Početno stanje radnog medija je ulazno stanje (1), konačno stanje je izlazno stanje (2).<br />
Ulazno i izlazno stanje opisani su s temperaturom T ili ϑ, tlakom p i protočnim volumenom<br />
V̇ m 3 /s. Odnos protočnog volumena i protočne mase ṁ kg/s je specifični volumen v:<br />
V̇<br />
v = , m 3 /kg. (6.1)<br />
ṁ<br />
Protočni volumen je povezan s brzinom strujanja w (m/s) i površinom presjeka strujanja A<br />
(m 2 ):<br />
V ̇ = wA , m 3 /s. (6.2)<br />
Energija koju radni medij unosi, odnosno iznosi iz kontrolnog volumena, sastoji se iz dva<br />
U̇ = mu ̇ = U̇<br />
T , J/s, te<br />
dijela: unutarnje energije, srazmjerne protočnoj masi i temeperaturi, ( )<br />
snazi strujanja, srazmjernoj produktu tlaka i protočnog volumena, pV<br />
̇ , (N/m 2 )(m 3 /s) = J/s.<br />
Ova dva oblika su energije vezane sa stanjem radnog medija, a objedinjena su pojmom<br />
entalpije Ḣ , koja je također veličina stanja.<br />
Po definiciji je specifična entalpija:<br />
h = u + pv , J/kg. (6.3)<br />
Množenjem jednadžbe (6.3) s protočnom masom ṁ slijedi da je:<br />
H ̇ = mh ̇ = mu ̇ + pmv ̇ = U̇<br />
+ pV̇<br />
, J/s. (6.4)<br />
64
Mirko Tadić<br />
Termodinamika<br />
Kako je entalpija veličina stanja to se ona matematički klasificira kao totalni diferencijal, što<br />
znači da je promjena entalpije:<br />
( − )<br />
∆Ḣ = ̇ , (6.5)<br />
12<br />
m h2<br />
h1<br />
neovisna o procesu, tj. načinu promjene stanja radnog medija od ulaza do izlaza iz otvorenog<br />
sustava. Zbog toga se kaže da je entalpija konzervativno svojstvo, poput mase. Uz to, entalpija<br />
je ekstenzivna veličina, jer njena numerička vrijednost ovisi o masi.<br />
Apsolutna vrijednost specifične entalpije h nema značaja pri opisu procesa, već samo<br />
promjena njene vrijednosti tijekom procesa, ∆h 12 . Stoga je sasvim svejedno koje se toplinsko<br />
stanje smatra nultim stanjem entalpije (označeno indeksom 0), tj. stanjem pri kojem je<br />
entalpija h 0 = 0. Do izražaja dolazi samo razlika entalpija stanja (1) i (2):<br />
( h − h ) − ( h − h ) = h − h = c ( T − T ) = C ( ϑ − )<br />
∆h , J/kg. (6.6)<br />
12<br />
=<br />
2 0 1 0 2 1 p 2 1 p 2<br />
ϑ1<br />
Izborom nultog stanja entalpije s h 0 = 0, tom stanju je istovremeno pripisana određena<br />
vrijednost specifične unutarnje energije u 0 , sukladno relaciji:<br />
u = = , J/kg. (6.7)<br />
0<br />
h0<br />
+ p0v0<br />
p0v0<br />
To nema utjecaja na oblik računa, jer do izražaja dolazi samo razlika specifične unutarnje<br />
energije, ∆u 12 , za koju vrijedi:<br />
( u − u ) − ( u − u ) = u − u = c ( T − T ) = C ( ϑ − )<br />
∆u , J/kg. (6.8)<br />
12<br />
=<br />
2 0 1 0 2 1 v 2 1 v 2<br />
ϑ1<br />
Vidi se da je stvarna vrijednost u 0 potpuno nevažna.<br />
Na temelju jednadžbi (6.6) i (6.8) nastaju relacije koje su korisne za proračun otvorenih<br />
sustava:<br />
( − h ) = mc ̇ ( T − T ) = Ṅ<br />
C ( ϑ − )<br />
∆Ḣ ̇<br />
, J/s = W. (6.9)<br />
12<br />
= m h2<br />
1 p 2 1<br />
p 2<br />
ϑ1<br />
( − u ) = mc ̇ ( T − T ) = Ṅ<br />
C ( ϑ − )<br />
∆U̇ ̇<br />
, J/s = W. (6.10)<br />
12<br />
= m u2<br />
1 v 2 1 v 2<br />
ϑ1<br />
Primjenom jednadžbe (6.4) na stanja (1) i (2) dobijaju se dvije jednadžbe, pa se razlika stanja<br />
(2) prema stanju (1) može izraziti kao:<br />
∆ Ḣ<br />
̇ ̇ ̇ . (11)<br />
12<br />
= ∆U12<br />
+ p2V2<br />
− p1V<br />
1<br />
Promjena entalpije obuhvaća i promjenu unutarnje energije i razliku energije strujanja s<br />
istovremenim promjenama volumena. Radi jasnoće možemo promotriti diferencijalni oblik<br />
jednadžbe (6.11):<br />
( pV̇<br />
) = dU̇<br />
+ pdV̇<br />
V̇<br />
dp<br />
dH<br />
̇ = dU̇<br />
+ d<br />
+ . (6.12)<br />
65
Mirko Tadić<br />
Termodinamika<br />
Značenje dU<br />
̇ (W) jasno je od ranije, s jedinom razlikom što se preko protočne mase uvela<br />
jedinica vremena. Član pdV<br />
̇ je očito energija (po vremenu) koju radni medij uzima (daje) za<br />
porast (smanjenje) svog volumen. Dakle taj član je snaga, povezana s promjenom volumena.<br />
Posljednji član, V̇ dp , je snaga čistog strujanja bez volumenske promjene, tj. samo kao<br />
transport u smjeru pada tlaka.<br />
Uvođenjem pojma entalpije nestaje potreba da sve te efekte razmatramo pojedinačno!<br />
Stanje radnog medija na ulaznom (1) i na izlaznom (2) presjeku nije jednoznačno, jer su<br />
stanja materijalnih čestica po istom presjeku različita i po brzinama i po temperaturi!<br />
Uzimanje u obzir tih činjenica vodi jako kompliciranom proračunu. Sukladno dosadašnjem<br />
principu idealiziranja fizikalnog modela možemo pretpostaviti da je stanje materije po<br />
presjeku, tj unutar proizvoljno malog volumena, dV, jedinstveno. Time će se proračun bitno<br />
pojednostaviti, ali uz izvjesnu netočnost rezultata koja se može ustanoviti eksperimentalno.<br />
Po potrebi, uvijek se može primijeniti kompleksniji pristup.<br />
U narednim razmatranjima polazi se od pretpostavke jedinstvenog stanja po presjeku.<br />
U odnosu na fizikalni model prikazan na slici 6.1 vidljivo je da zbog toplinske i mehaničke<br />
interakcije s okolišem može doći ne samo do promjene entalpije, ∆ Ḣ12<br />
, već i do promjene<br />
kinetičke ∆ Ė k , 12<br />
i potencijalne ∆ Ė p, 12<br />
energije radnog medija. Primjena I. Zakona na takav<br />
fizikalni model rezultira jednadžbom:<br />
Φ − P = ∆Ḣ<br />
+ ∆Ė<br />
k<br />
+ ∆Ė<br />
, W. (I. Zakon za otvoreni sustav). (6.13)<br />
12 12 12 , 12 p,<br />
12<br />
Promjena kinetičke energije može se odrediti iz jednadžbe:<br />
2 2<br />
w2<br />
− w1<br />
∆E ̇ k , 12<br />
= ṁ<br />
2<br />
, W, (6.14)<br />
pri čemu se za određivanje brzina može koristiti veza s protočnim volumenom prema<br />
jednadžbi (6.2):<br />
V̇<br />
w = , m/s. (6.15)<br />
A<br />
Promjena potencijalne energije postoji, ako postoji razlika u poziciji presjeka, z,<br />
( z − )<br />
∆ ̇ ̇ , W. (6.16)<br />
E p,<br />
12<br />
= mg<br />
2<br />
z1<br />
Toplinska interakcija s okolišem, u obliku toplinskog toka, Φ 12 (W), odvija se pri konačnoj<br />
razlici temperatura radnog medija (RM) i toplinskih sudionika (TS) u okolišu, tj.<br />
ireverzibilno.<br />
Mehanička interakcija s okolišem, u obliku snage P 12 (W), prepoznaje se kao neposredni<br />
dodir radnog medija s pomičnim mehaničkim sudionikom (MS) i smatra se reverzibilnom, tj.<br />
bez gubitaka.<br />
Razmotrit će se odvojeno dvije vrste procesa radnog medija:<br />
• ravnotežne promjene stanja (politropske),<br />
• neravnotežne promjene stanja, kod kojih nisu ispunjeni uvjeti unutarnje toplinske<br />
mehaničke ravnoteže.<br />
66
Mirko Tadić<br />
Termodinamika<br />
Politrope otvorenih sustava<br />
Proces u nekim važnim tehničkim uređajima može se klasificirati kao proces idealnog<br />
radnog medija u otvorenom sustavu. Kao primjer spomenimo zračni kompresor koji je<br />
pokretan električkim motorom. Radnom mediju, zraku, pripisuje se idealno ponašanje budući<br />
da su stvarni tlak i temperatura tijekom procesa daleko od uvjeta pretvorbe u kapljevito stanje<br />
(sudionika u zraku). Kao sastav zraka obično se uzima molni sastav s 21% O 2 i 79% N 2 .<br />
Standardni sastav zraka ponešto je drugačiji. Za svojstva takvog zraka postoje numerički<br />
podaci u odgovarajućim tablicama, pa se pri proračunu zrak smatra jednim plinom.<br />
Radi lakšeg razumijevanja opisa rada stapnog kompresora prikazan je na slici 6.2 presjek<br />
cilindra. Otvaranje i zatvaranje usisnog (UV) i tlačnog (TV) ventila određeno je razlikom<br />
tlaka zraka u cilindru i tlakova u usisnom (p u ), odnosno tlačnom (p t ) vodu.<br />
tlačni vod<br />
štetni prostor<br />
cilindar<br />
p t<br />
TV<br />
STAPAJICA<br />
p u<br />
usisni vod<br />
UV<br />
STAP<br />
s<br />
stapaj<br />
Slika 6.2 Stapni kompresor<br />
Realni i teorijski proces zraka u kompresoru prikazani su u p-V dijagramu na slici 6.3.<br />
Na realni proces utječu dva faktora:<br />
• postojanje štetnog prostora u kojem uvijek ostaje dio komprimiranog zraka, koji se pri<br />
usisu miješa s usisanim zrakom,<br />
• inertnost usisnog i tlačnog ventila zbog koje pri usisu nastaje potlak, a pri ispuhu<br />
pretlak – u odnosu na tlakove u usisnom i tlačnom vodu.<br />
Teorijski proces aproksimira usis kao punjenje cilindra sa zrakom čiji se tlak i temperatura pri<br />
tome ne mijenjaju, tj. zrak je istog stanja kao u usisnom vodu. Stoga je sekvenca usisa čisti<br />
transport vanjskog zraka, koji je uzrokovan pokretom stapa. Stanje plina nije pod utjecajem<br />
bilo kakve mehaničke i toplinske interakcije iz okoliša, pa zbog toga usis nije politropska<br />
promjena. Sve točke na liniji usisa su istog stanja kao i točka označena s (1).<br />
Nakon završetka usisa, stap kreće u suprotnom smjeru, a oba ventila su zatvorena.<br />
Smanjivanjem volumena zrak se komprimira pri čemu raste tlak. Sekvenca kompresije smatra<br />
se ravnotežnom promjenom, tj. politropom, pV n = konst.<br />
Njen eksponent n ovisi o izmjeni<br />
topline, tj. hlađenju tijekom kompresije, Φ 12 . Kompresija završava u trenutku kada je tlak u<br />
cilindru dostigao vrijednost tlaka u tlačnom vodu.<br />
Rad ventila kompresora nije dirigiran nikakvim drugim mehanizmom, već samo razlikama<br />
tlaka, koje se u teorijskom procesu smatraju zanemarivo malenim, a reakcije ventila<br />
trenutnim.<br />
67
Mirko Tadić<br />
Termodinamika<br />
p<br />
2<br />
Realni proces<br />
Teorijski proces<br />
p 1<br />
p 2<br />
V 1<br />
dp<br />
{ P } okret<br />
P = 12<br />
n0<br />
12<br />
{ P } okret<br />
= −∫V( p)<br />
12<br />
dp<br />
2<br />
1<br />
V 2<br />
n = konst.<br />
V<br />
1<br />
V, m 3 /okret<br />
motor<br />
ispuh<br />
usis<br />
kompresija<br />
ZRAK<br />
Slika 6.3 Realni i teorijski proces u kompresoru<br />
Tlačni ventil se podiže s ispušnog otvora i zrak se istiskuje u tlačni vod, prema<br />
odgovarajućem spremniku komprimiranog zraka. Sekvenca ispuha nije politropska promjena,<br />
već transport zraka stanja (2), kakvo je dostignuto na kraju kompresije.<br />
Procesi koji su prikazani na slici 6.3 odnose se na jedan puni okret vratila kompresora. Zbog<br />
toga su na apscisi volumeni po okretu, V (m 3 /okret), pa se za zadani broj okretaja n 0 (okret/s)<br />
mora izračunati protočni volumen V̇ (m 3 /s) pomoću relacije:<br />
V̇ = n 0<br />
V = mv ̇ , (m 3 /s). (6.17)<br />
Snaga motora za pogon kompresora troši se tijekom kompresije i ispuha, a dio snage se<br />
dobiva tijekom usisa efektom inercije. Mehanička interakcija prema okolišu, tj. zatvorenom<br />
prostoru kućišta u kome se nalazi vratilo kompresora (na slici 6.3 opisan kao zrak), se<br />
poništava budući da se stap giba jednako u dva suprotna smjera, a gubici zbog trenja<br />
zanemaruju.<br />
Razultantni utrošak snage za pogon kompresora pri teorijskom procesu prikazan je u p-V<br />
dijagramu kao površina omeđena linijama usisa, kompresije i ispuha. Ta se površina može<br />
prikazati kao zbroj niza malih površina koje imaju smisao diferencijalno male utrošene snage,<br />
Vdp = dP. Stoga za utrošak snage po jednom okretu vratila vrijedi jednadžba:<br />
2<br />
= −∫<br />
1<br />
{ } V ( p)<br />
P okret<br />
, J/okret. (6.18)<br />
12<br />
dp<br />
Negativan predznak u jednadžbi (6.18) uveden je iz slijedećih razloga. Matematički se dp<br />
uvijek izražava prema + p smjeru, pa bi produkt Vdp imao pozitivan smisao. Kako postojeći<br />
dogovor o smislu mehaničkog rada (snage), propisuje negativan predznak svakom utrošenom<br />
radu (snazi) to se taj smisao mora osigurati i u jednadžbi (6.18).<br />
68
Mirko Tadić<br />
Termodinamika<br />
Za ukupni utrošak snage pri n 0 (okret/s) vrijedi relacija:<br />
2<br />
{ P } = −n<br />
V ( p) dp = − V ( p) dp = − mv ̇ ( p) dp = −m<br />
v( p)<br />
P12 = n<br />
̇ ̇<br />
0 12 okret 0<br />
dp , W. (6.19)<br />
∫<br />
1<br />
2<br />
∫<br />
1<br />
Lako je uočljivo, prama slici 6.3, da je površina koja odgovara utrošku snage jednaka površini<br />
koja nastaje projekcijom politropske kompresije (1)-(2) na ordinatnu os p.<br />
Za politropu vrijedi jednadžba pv n = konst.<br />
na osnovu koje se diferenciranjem dobiva:<br />
n<br />
v dp + npv<br />
iz čega slijedi<br />
n<br />
2<br />
∫<br />
1<br />
− 1<br />
dv = 0 , (6.20)<br />
vdp = −npdv . (6.21)<br />
Za cijelu politropu između (1) i (2) vrijedi:<br />
2<br />
1<br />
2<br />
( p) dp −n<br />
p( v) dv = −nw12<br />
∫ v = ∫<br />
, (6.22)<br />
1<br />
gdje je w 12 (J/kg) specifični mehanički rad politrope čija se površina dobija projekcijom na<br />
apscisnu os. Sukladno tome, može se jednadžba (6.19) pisati u obliku:<br />
2<br />
12<br />
−ṁ v<br />
= W<br />
P<br />
1<br />
( p) dp = nmw ̇<br />
12<br />
n ̇<br />
12<br />
= ∫ , W. (6.23)<br />
2<br />
∫<br />
1<br />
P<br />
P<br />
3<br />
= −∫<br />
1<br />
2<br />
= −∫<br />
1<br />
p<br />
N/m 2<br />
3<br />
p<br />
2<br />
3<br />
−∫ V̇<br />
p dp = P12<br />
= nẆ<br />
12<br />
= n<br />
V̇<br />
1<br />
( p)<br />
n<br />
2 13<br />
p 2<br />
V̇<br />
( p)<br />
n 12<br />
1<br />
13<br />
dp<br />
12<br />
dp<br />
p 1<br />
V 2 =V 3<br />
2<br />
( ) ∫ p( V̇<br />
)<br />
V 1<br />
Ẇ<br />
2<br />
= ∫<br />
1<br />
( ̇)<br />
̇<br />
12<br />
p V dV<br />
V, m 3 /okret<br />
1<br />
dV̇<br />
Slika 6.4 Prikazi snage i mehaničkog rada politropa u p – V dijagramu<br />
Uočimo da se u jednadžbi (6.23) nalazi mehanička snaga politrope Ẇ<br />
12<br />
, zbog utjecaja protoka<br />
mase ṁ (kg/s).<br />
Ako se politropi pridruže usis i ispuh, tada se množenjem snage, Ẇ 12<br />
, s eksponentom<br />
politrope n dobiva snaga, P<br />
12<br />
, takvog otvorenog politropskog procesa.<br />
69
Mirko Tadić<br />
Termodinamika<br />
To znači da se za otvorene politropske procese mogu koristiti sve ranije izvedene relacije za<br />
mehanički rad zatvorenih sustava, ali se pri tome umjesto mase m (kg) treba uvrstiti protočna<br />
masa ṁ (kg/s), kako bi se dobila snaga Ẇ 12<br />
. Jedini izuzetak je otvoreni sustav s izohorom<br />
( V ̇ = konst.<br />
) kod koje je eksponent n = ± ∞, a mehanička snaga Ẇ 0 , tako da je umnožak<br />
nW ̇ 12<br />
neodređen. U tom slučaju treba koristiti jednadžbu (6.23) koja omogućava dobijanje<br />
rezultata:<br />
2<br />
2<br />
12<br />
= −m∫<br />
vdp = −mv<br />
̇ dp = −V̇<br />
∫<br />
2<br />
p1<br />
1<br />
1<br />
P<br />
( p − )<br />
̇ , W, (izohorni otvoreni proces). (6.24)<br />
Budući da su usis i ispuh samo transportne sekvence procesa, to pri tome nema izmjene<br />
topline. Jedina izmjena topline postoji, eventualno, samo tijekom politropske promjene koja<br />
se odvija pri zatvorenim ventilima. Stoga se toplinski tok, Φ 12 (W), računa potpuno isto kao<br />
kod zatvorenih sustava, tj. vrijede iste jednadžbe uz zamjenu mase m s protočnom masom ṁ .<br />
Isto vrijedi i za proračun promjene entropije, ∆ Ṡ12<br />
(J/K), radne tvari od usisnog stanja (1) do<br />
ispušnog stanja (2). Transportne sekvence procesa, usis i ispuh, pretpostavljene su bez<br />
gubitaka (∆S = 0).<br />
Teorijski gubitak snage uslijed nepovratnosti izmjene topline (samo pri politropi) računa se<br />
prema referentnom prirodnom toplinskom spremniku temperature T 0 = konst. pomoću<br />
relacije:<br />
∆P<br />
= T ∆ ̇<br />
0<br />
, W, (teorijski gubitak snage). (6.25)<br />
S s<br />
12<br />
=<br />
Otvoreni procesi specijalnih politropa<br />
Ostajući pri aproksimaciji procesa u otvorenim sustavima, kao kombinaciji ravnotežne<br />
promjene (politrope) idealnog plina s dvije transportne sekvence, usisom (ulazom) i ispuhom<br />
(izlazom), promotrit ćemo procese sa specijalnim politropama.<br />
Postoje i sličnosti i razlike između politropskih procesa u otvorenim i onih u zatvorenim<br />
sustavima. Kod otvorenih sustava uvodi se putem protočne mase ṁ (kg/s) utjecaj vremena i<br />
ponavljanje procesa, dok se kod zatvorenih sustava proces s konstantnom masom m (kg)<br />
odvija jednokratno, bez ponavljanja.<br />
U oba slučaja politropska promjena se odvija potpuno identično, jer se i kod otvorenih<br />
sustava ta sekvenca odvija pri zatvorenim ventilima, kao što je to slučaj kod zatvorenih<br />
sustava. Stoga je početno i konačno stanje radnog medija identično u oba slučaja. Sukladno<br />
usvojenim pretpostavkama kod otvorenih sustava ta stanja nisu pod utjecajem transportnih<br />
sekvenci, usisa i ispuha.<br />
Promjena energije radnog medija: unutarnje, kinetičke i potencijalne, tijekom politropskog<br />
procesa računa se po istom principu, tj. s istim jednadžbama u oba slučaja. Pod utjecajem<br />
protočne mase ṁ (kg/s), umjesto mase m (kg), nastaje samo razlika u dimenziji tih energija.<br />
Jednako tako, umjesto topline, Q 12 (J), sada govorimo o toplinskom toku, Φ 12 (J/s). Kako<br />
ćemo zanemariti izmjenu topline pri transportnim sekvencama usisa i ispuha to je grafički<br />
70
Mirko Tadić<br />
Termodinamika<br />
prikaz politropskog procesa u ravnini T-s identičan onom kod zatvorenih sustava. Ukratko,<br />
usis i ispuh se ne vide u dijagramu.<br />
Jedina razlika očituje se u promjeni grafičkog prikaza u ravnini p-V, budući da se transportne<br />
sekvence (usis i ispuh) kod otvorenih sustava odražavaju na ukupni mehanički efekt, tj. snagu.<br />
Zbog ponavljanja procesa poništava se mehanička interakcija prema okolišnjem zraku, koja<br />
kod jednokratnih procesa u zatvorenim sustavima dolazi do izražaja kao rad W 0 .<br />
Grafički prikazi otvorenih procesa u p-V i T-s dijagramu dani su u nastavku za posebne<br />
politropske procese.<br />
Izohora (V = konst.; n = ± ∞)<br />
p<br />
N/m 2<br />
n = ±∞<br />
ispuh 2<br />
2<br />
p 2 T 2<br />
ϑ 2<br />
2<br />
{ P } okret<br />
= −∫ V dp<br />
OS<br />
12<br />
1<br />
1<br />
p 1<br />
1<br />
T<br />
usis<br />
1<br />
p 1<br />
2<br />
ϑ 1<br />
q 12<br />
= ∫Tds<br />
1<br />
V, m 3 V1 = V /okret<br />
2<br />
s 1 s 2<br />
Izobara (p = konst.; n = 0)<br />
2<br />
12<br />
= n0<br />
12<br />
0∫<br />
1<br />
p2<br />
1<br />
{ P } = −n<br />
V dp = V̇<br />
( p )<br />
P<br />
okret<br />
−<br />
T<br />
K<br />
OS<br />
v 1 = v 2<br />
n = ±∞<br />
p 2<br />
( T )<br />
Φ = ̇ ̇<br />
v<br />
−<br />
12<br />
mq12<br />
= mc<br />
2<br />
T1<br />
Slika 6.5 Otvoreni izohorni proces u p-V i T-s dijagramu<br />
s, J/(kg K)<br />
p<br />
N/m 2<br />
p<br />
T 2<br />
1 2<br />
s 1<br />
T<br />
K<br />
v 2<br />
V 1 V 2 V, m 3 /okret<br />
s 2<br />
OS<br />
OS<br />
2<br />
usis n = 0<br />
ϑ 1<br />
ispuh<br />
ϑ 2 v 1<br />
T 1<br />
1<br />
q 12 > 0<br />
p 1 = p 2<br />
P<br />
12<br />
= 0<br />
Φ = ṁ<br />
q = mc ̇<br />
p<br />
( T − )<br />
12 12<br />
2<br />
T1<br />
s, J/(kg K)<br />
Slika 6.6 Otvoreni izobarni proces u p-V i T-s dijagramu<br />
71
Mirko Tadić<br />
Termodinamika<br />
Izentropa (S = konst.; n = κ)<br />
p<br />
T<br />
N/m 2<br />
K<br />
v<br />
usis<br />
1<br />
1<br />
p 1<br />
p 1 1<br />
MS<br />
dp<br />
ϑ 1<br />
T 1<br />
2<br />
n = κ<br />
2<br />
{ P } okret ∫ V<br />
12<br />
= −κ ( p)dp<br />
2<br />
1<br />
p 2<br />
ispuh ϑ 2<br />
T 2<br />
v 2<br />
p 2<br />
V 1<br />
V<br />
V 2<br />
κ<br />
P12<br />
= n<br />
̇<br />
0 12 okret 1<br />
−<br />
κ −1<br />
{ P } = mR( T T )<br />
V, m 3 /okret<br />
2<br />
s 1 = s 2<br />
q 12 = 0<br />
s, J/(kg K)<br />
Izoterma (T = konst.; n = 1)<br />
Slika 6.7 Otvoreni izentropski proces u p-V i T-s dijagramu<br />
p<br />
ϑ T<br />
N/m 2 1<br />
K<br />
usis<br />
p 1 1<br />
OS<br />
MS<br />
dp<br />
v 2<br />
p 1 p<br />
1<br />
2 2<br />
T 1 = T 2<br />
2<br />
{ P } okret ∫ V<br />
12<br />
= − ( p)dp<br />
1<br />
2<br />
p q 2 12 > 0<br />
ispuh<br />
ϑ 2<br />
n =1<br />
v 1<br />
s 1<br />
V 1 V<br />
V2<br />
p<br />
P12<br />
= n0{ P12<br />
} = mRTln ̇<br />
okret<br />
p<br />
1<br />
2<br />
V, m 3 /okret<br />
Φ<br />
= ̇ ̇<br />
s 2<br />
( s − )<br />
12<br />
mq12<br />
= mT<br />
2<br />
s1<br />
s, J/(kg K)<br />
Slika 6.8 Otvoreni izotermni proces u p-V i T-s dijagramu<br />
Maksimalni rad i eksergija<br />
Već smo upoznali način određivanja teorijskog gubitka na radu u zatvorenim, odnosno<br />
snazi u otvorenim sustavima, pomoću kojih se ocjenjuje termodinamička valjanost procesa u<br />
odnosu na nepovratnost izmjene topline.<br />
72
Mirko Tadić<br />
Termodinamika<br />
Preostaje nam da razmotrimo kriterij vrednovanja zadanog stanja radnog medija, polazeći od<br />
činjenice da sva moguća početna stanja nisu jednako vrijedna u odnosu na mogućnost<br />
dobijanja korisnog rada, odnosno snage.<br />
Očito je, da kriterij ne smije imati nikakve realne karakteristike koje bi utjecale na rezultat<br />
procjene. Stoga je logično da se kao osnova kriterija uzme idealni teorijski proces radnog<br />
medija u kojem nema nepovratne izmjene topline. Mehanička interakcija tijekom procesa<br />
smatra se reverzibilnom, tj. bez gubitaka, kao i u svim prethodnim razmatranjima. Tijekom<br />
procesa radni medij prolazi kroz stanja u unutarnjoj ravnoteži.<br />
Radni sustav uključuje samo nužne sudionike: sam radni medij, neopisanog mehaničkog<br />
sudionika čije su osobine idealizirane (bez trenja), te postojeći prirodni toplinski spremnik<br />
(okolišnji zrak) temperature T 0 = konst., koji je ujedno i mehanički sudionik tlaka p 0 = konst..<br />
Sustav je potpuno izoliran od drugih utjecaja. Pretpostavit ćemo da radni medij zadanog<br />
stanja (T 1 , p 1 , V 1 ) nije u ravnoteži s okolišem, jer u protivnom slučaju ne bi bio moguć<br />
nastanak procesa niti teorijski. Neravoteža s okolišem pruža mogućnost provođenja procesa i<br />
dobivanja korisnog mehaničkog rada, odnosno snage. Proces traje do uspostave ravnoteže s<br />
prirodnim spremnikom (okolišnjim zrakom), kada radni medij postiže temperaturu T 0 i tlak<br />
p 0 .<br />
Stanje plina u potpunosti je zadano podacima temperature T 1 , tlaka p 1 i volumena V 1 , odnosno<br />
V̇ 1, na osnovu čega se iz jednadžbe stanja može izračunati masa m, odnosno protočna masa<br />
ṁ , plina:<br />
p1V<br />
1<br />
m = , kg,<br />
RT1<br />
(zatvoreni sustav), (6.26)<br />
p1V̇<br />
1<br />
ṁ = , kg/s,<br />
RT<br />
(otvoreni sustav). (6.27)<br />
1<br />
Da bi se izbjegli gubici na radu, odnosno snazi, koji su spomenuti na početku, tijekom procesa<br />
ne smije doći do nepovratne izmjene topline. Teorijski zamišljena povratna izmjena topline<br />
mogla bi biti samo pri istoj temperaturi radnog medija i toplinskog spremnika. Ta je<br />
temperatura zadana zadavanjem stanja prirodnog toplinskog spremnika, okolišnjeg zraka.<br />
Tamperatura T 0 je upravo ta povratna izoterma po kojoj smije teći proces plina. Naravno,<br />
proces uravnotežavanja može koristiti i bilo koju politropu bez izmjene topline, tj. izentropu,<br />
S = konst., dS = 0. Promjena entropije takvog izoliranog sustava jednaka je nuli, ∆S s = 0 ili<br />
Ṡ = 0 , kao i teorijski gubitak na radu, ∆W = 0, odnosno snazi, ∆P = 0.<br />
∆ s<br />
S postavljenim uvjetom reverzibilnosti izmjene topline uklonjena je poslijednja realna<br />
karakteristika, pa takav proces ima samo teorijski smisao. Pri takvom procesu teorijski se<br />
dobiva najveći mogući mehanički rad, odnosno najveća moguća snaga (eksergija), s obzirom<br />
na zadana stanja radnog medija i prirodnog spremnika.<br />
Maksimalni rad – zatvoreni sustav<br />
Teorijski idealan proces u zatvorenom sustavu smije biti samo kombinacija bilo koje<br />
izentrope, pri kojoj nema izmjene topline, dok se izmjena topline smije odvijati samo tijekom<br />
povratne izoterme T 0 , koja je zadana temperaturom prirodnog spremnika, okolišnjim zrakom.<br />
U posebnim slučajevima bit će dovoljna samo jedna od tih promjena.<br />
73
Mirko Tadić<br />
Termodinamika<br />
Na slici 6.10 prikazan je jedan slučaj takvog idealnog procesa za zadano stanje (1) radnog<br />
medija i zadano stanje (0) prirodnog spremnika, okolišnjeg zraka temperature T 0 i tlaka p 0 .<br />
p<br />
p 1<br />
1<br />
p 1<br />
1<br />
T 1<br />
ϑ 1<br />
v 0 p 0<br />
2<br />
0<br />
T 0<br />
2<br />
W max<br />
0<br />
p q 0<br />
ϑ o<br />
20 > 0<br />
n = κ<br />
p 2<br />
W 0<br />
s 1 = s 2<br />
v<br />
T<br />
1<br />
V V, m 3 1<br />
V0 s 0<br />
s, J/(kg K)<br />
Slika 6.9 Idealni proces zatvorenog sustava u ravnini p-V i T-s<br />
Dogod je temperatura radnog medija različita od temperature T 0 smije se koristiti samo<br />
izentropski proces bez izmjene topline. Tek kada plin postigne tu temperaturu (stanje 2 u<br />
dijagramima) može se zamisliti teorijska izmjena topline, pri istim temperaturama plina i<br />
toplinskog spremnika, okolišnjeg zraka. Proces se po toj povratnoj izotermi odvija sve dok se<br />
ne uspostavi potpuna ravnoteža plina i okoliša, tj. plin poprimi stanje s temperaturom T 0 i<br />
tlakom p 0 (stanje 0 u dijagramima).<br />
Položaj stanja (2) u ravnini p-V može se procijeniti ako se izračuna pripadni tlak p 2 :<br />
κ<br />
⎛ T<br />
κ−1<br />
0<br />
⎞<br />
p<br />
2<br />
= p1<br />
⎜<br />
⎟ ,<br />
T1<br />
(za sjecište izentrope 1-2 i izoterme 2-0). (6.28)<br />
⎝<br />
⎠<br />
Teorijski rad plina je, po definiciji, površina ispod linija procesa (1-2-0). Kako se proces (1-2)<br />
odvija po zakonu izentrope, a proces (2-0) po zakonu izoterme, to se mehanički rad može<br />
izračunati samo odvojeno za svaku sekvencu. Stoga je<br />
W , J. (mehanički rad plina pri idealnom procesu). (6.29)<br />
1− 2−0<br />
= W1<br />
−2<br />
+ W2−0<br />
No, W 1-2-0 se može izraziti i na drugi način, kako će se pokazati u nastavku.<br />
U promatranom primjeru ovaj je rad pozitivan tj. predaje se prisutnim mehaničkim<br />
sudionicima. Dio tog rada troši se na potiskivanje okolišnjeg zraka u iznosu W 0 , a ostatak se<br />
može iskoristiti. Zbog idelnog procesa taj koristana rad je ujedno i najveći mogući rad, W max ,<br />
koji se teorijski može dobiti od plina zadanog stanja – u odnosu na zadano stanje prirodnog<br />
spremnika, okolišnjeg zraka (T 0 , p 0 ).<br />
Odnos teorijskog rada plina W 1-2-0 , rada okoline W 0 i maksimalnog korisnog rada W max , uvijek<br />
je određen jednadžbom oblika:<br />
W max<br />
= W 1 − 2−0<br />
+ W0<br />
, (6.30)<br />
Rad prema okolini može se izraziti, pomoću definicije mehaničkog rada, na slijedeći način:<br />
74
Mirko Tadić<br />
Termodinamika<br />
0,ok<br />
W0 p0<br />
dV0<br />
= p0<br />
0,ok<br />
−<br />
1,ok<br />
1,ok<br />
( V V )<br />
= ∫ , J, (rad prema okolini). (6.31)<br />
Razliku volumena okolišnjeg zraka moramo zamijeniti s istom takvom razlikom volumena<br />
radnog medija, ali suprotnog smisla:<br />
V<br />
( V )<br />
0, ok<br />
V1,<br />
ok<br />
= −<br />
0<br />
−V1<br />
− , (6.32)<br />
pa umjesto jednadžbe (6.31) možemo pisati:<br />
W<br />
( V − )<br />
0<br />
p0<br />
1<br />
V0<br />
= , J, (rad prema okolini). (6.33)<br />
Za određivanje teorijskog rada plina W 1-2-0 , tijekom procesa (1-2-0), iskoristit ćemo jednadžbu<br />
I. Zakona:<br />
Q − W = ∆U<br />
, J, (6.34)<br />
1−2−0<br />
1−2−0<br />
1−2−0<br />
koju možemo uskladiti s procesom u dvije sekvence, (1-2) i (2-0):<br />
Q + Q −W<br />
= ∆U<br />
+ ∆U<br />
, J. (6.35)<br />
1−2<br />
2−0<br />
1−2−0<br />
1−2<br />
2−0<br />
Na sekvenci izentrope (1-2) nema izmjene topline, Q 1-2 = 0, dok se toplina na sekvenci (2-0)<br />
odvija pri konstantnoj temperaturi, pa se može izračunati primjenom II. Zakona:<br />
( S − S ) = T ( S − )<br />
Q<br />
−<br />
, J, (jer vrijedi: S 2 = S 1 ). (6.36)<br />
2 0<br />
= T0∆S<br />
2−0<br />
= T0<br />
0 2 0 0<br />
S1<br />
Promjena unutarnje energije radnog medija tijekom procesa (1-2-0) iznosi:<br />
( U<br />
2<br />
−U1) + ( U<br />
0<br />
−U<br />
2<br />
) = U<br />
0<br />
−<br />
1<br />
∆U<br />
−<br />
, J, (jer vrijedi: U 2 = U 0 ). (6.37)<br />
1 2<br />
+ ∆U<br />
2−0<br />
=<br />
U<br />
Rezultate jednadžbi (6.35) i (6.37) možemo uvrstiti u jednadžbu (6.35) i preoblikovati u izraz<br />
kojim se izražava W 1-2-0 :<br />
( S − )<br />
W<br />
−<br />
, J. (6.38)<br />
1 2−0<br />
= U1<br />
−U<br />
0<br />
− T0<br />
1<br />
S0<br />
Konačno, uvrštavanjem jednadžbi (6.38) i (6.33) u jednadžbu (6.29) dobivamo izraz za<br />
izračunavanje maksimalnog rada za proces između zadanih stanja 1-0:<br />
( S − S ) + p ( V − )<br />
W max, 1 0<br />
= U1<br />
−U<br />
0<br />
− T0<br />
1 0 0 1<br />
V0<br />
−<br />
, J, (maksimalni rad). (6.39)<br />
Sve veličine na desnoj strani jednadžbe se odnose na radni medij, a pojedini članovi se<br />
računaju prema slijedećim relacijama:<br />
( T )<br />
U −<br />
v<br />
− , J, (6.40)<br />
1<br />
U<br />
0<br />
= mc<br />
1<br />
T0<br />
75
Mirko Tadić<br />
Termodinamika<br />
⎛ T p ⎞<br />
T<br />
p<br />
, J, (6.41)<br />
0<br />
1<br />
1<br />
( S − ) =<br />
⎜ − ⎟ 1<br />
S0<br />
mT0<br />
c ln R ln<br />
⎝ T0<br />
p0<br />
⎠<br />
( V )<br />
p − , J, pomoću:<br />
0 1<br />
V0<br />
mRT<br />
1<br />
V<br />
1<br />
= i<br />
p1<br />
mRT<br />
0<br />
V<br />
0<br />
= . (6.42)<br />
p0<br />
U dijagramu p-V uvijek se W max,1-0 može prikazati površinom, koja je omeđena s linijama<br />
idealnog procesa (1-2-0) i s dvije pomoćne linije (nisu linije procesa): izohorom V 1 i izobarom<br />
p 0 .<br />
Radi ilustracije prikazan je na slici 6.10 proces dobijanja maksimalnog rada u slučaju kada je<br />
zadano stanje plina (T 1 , p 1 , V 1 ) ispod stanja prirodnog spremnika, okolišnjeg zraka (T 0 , p 0 ).<br />
p<br />
p 0<br />
p 0<br />
2<br />
q v 20 < 0 1 p 1<br />
p 2<br />
v 0<br />
0<br />
T<br />
0<br />
T 0<br />
W max<br />
ϑ o<br />
2<br />
ϑ 1<br />
V V, m 3 0<br />
s 0<br />
n = κ<br />
p 1<br />
1<br />
T 1<br />
1<br />
V1 s 1 = s 2<br />
s, J/(kg K)<br />
Slika 6.10 Idealni proces s plinom stanja ispod okolišnjeg<br />
Za teorijski proces (1-2-0) potrebno je utrošiti rad W 1-2-0 (površina ispod procesa – bez oznake<br />
u dijagramu). Pri tome okolina pomaže dajući rad W 0 = p 0 (V 1 – V 0 ). Razlika je koristan<br />
(pozitivan) rad W max .<br />
Minimalni rad<br />
U slučaju da je početno stanje radnog medija u ravnoteži s prirodnim spremnikom<br />
(stanje s oznakom 0 u dijagramima) može se po istom principu odrediti teorijski minimalan<br />
rad, W min , da bi se radni medij doveo u stanje (1). Idealni proces je identičan, ali se odvija u<br />
suprotnom smjeru, pa je konačni rezultat za W min,0-1 jednak rezultatu za W max,1-0 , samo<br />
suprotnog, negativnog predznaka.<br />
( S − S ) + p ( V − )<br />
W min, 0 1<br />
= U<br />
0<br />
−U1<br />
− T0<br />
0 1 0 0<br />
V1<br />
−<br />
, J, (minimalni rad). (6.43)<br />
Eksergija – otvoreni sustav<br />
Ako raspolažemo sa stalnim dotokom ṁ (kg/s) radnog medija zadanog stanja, (T 1 , p 1 ),<br />
može se primjenom istog principa idealnog procesa odrediti eksergija (= maksimalna snaga),<br />
koja pripada tom stanju u odnosu na referentno stanje prirodnog spremnika, okolišnjeg zraka,<br />
76
Mirko Tadić<br />
Termodinamika<br />
(T 0 , p 0 ). Zbog ponavljanja, idealnom procesu pripadaju transportne sekvence usisa i ispuha.<br />
Primjer eksergijskog procesa prikazan je na slici 6.10.<br />
p<br />
p<br />
T<br />
1<br />
usis 1<br />
p 1<br />
1<br />
T 1<br />
ϑ 1<br />
v 0 p 0<br />
{ E} okret<br />
2<br />
0<br />
T 0<br />
2<br />
p 2<br />
ϑ 0<br />
0<br />
p q 0 20 > 0<br />
ispuh<br />
n = κ<br />
V, m 3 /okret<br />
s 1 = s 2<br />
V 1<br />
v 1<br />
V0 s 0<br />
s, J/(kg K)<br />
Slika 6.11 Eksergijski proces (1-0) u p-V i T-s ravnini<br />
Budući da se radi o otvorenom sustavu grafički prikaz eksergije (po okretu) u ravnini p-V<br />
predstavlja površinu, dobivenu projekcijom idealnog procesa (1-2-0) na ordinatnu os p.<br />
Prema I. Zakonu za otvorene sustave je:<br />
Φ1 −2−0<br />
− P1<br />
−2−0<br />
= ∆Ḣ 1−2−0<br />
, W, (6.44)<br />
odnosno<br />
Φ + Φ − P = ∆Ḣ + ∆Ḣ<br />
, W. (6.45)<br />
1−2<br />
2−0<br />
1−2−0<br />
1−2<br />
2−0<br />
Za pojedine sekvence idealnog procesa vrijedi:<br />
0 Φ = mT ̇ s − s = mT ̇ s − s = T S − , W, (6.46)<br />
Φ , ( ) ( ) ( )<br />
1 −2<br />
=<br />
2−0<br />
0 0 2 0 0 1 0 0<br />
S1<br />
∆Ḣ<br />
1 2<br />
= Ḣ<br />
2<br />
− Ḣ<br />
− 1<br />
, ∆H<br />
̇ 2 − 0<br />
= Ḣ<br />
0<br />
− Ḣ<br />
2<br />
= 0 , W, ( Ḣ 2<br />
= Ḣ<br />
). (6.47)<br />
0<br />
Snaga idealnog procesa je eksergija stanja (1) u odnosu na referentni prirodni spremnik stanja<br />
(0):<br />
P ≡ E , W, (6.48)<br />
1−2−0<br />
1−0<br />
Uvrštavanjem jednadžbi (6.46), (6.47) i (6.48) u jednadžbu (6.44) dobiva se:<br />
E<br />
( S − )<br />
̇ ̇<br />
, W, (eksergija). (6.49)<br />
1−0<br />
= H1<br />
− H<br />
0<br />
− T0<br />
1<br />
S0<br />
Računanje pojedinih članova vrši se pomoću jednadžbi:<br />
( T )<br />
Ḣ ̇ ̇<br />
p<br />
− , (6.50)<br />
T<br />
1<br />
− H<br />
0<br />
= mc<br />
1<br />
T0<br />
0<br />
⎛ T p ⎞<br />
̇ , (6.51)<br />
1<br />
1<br />
( S − ) =<br />
⎜ − ⎟ 1<br />
S0<br />
mT0<br />
c<br />
p<br />
ln R ln<br />
⎝ T0<br />
p0<br />
⎠<br />
koje zahtijevaju poznavanje samo svojstava početnog (1) i konačnog (0) stanja.<br />
77