13. ÐÑоизводнÑе каÑбоновÑÑ ÐºÐ¸ÑÐ»Ð¾Ñ 13.1. РаÑположиÑе киÑлоÑÑ ...
13. ÐÑоизводнÑе каÑбоновÑÑ ÐºÐ¸ÑÐ»Ð¾Ñ 13.1. РаÑположиÑе киÑлоÑÑ ...
13. ÐÑоизводнÑе каÑбоновÑÑ ÐºÐ¸ÑÐ»Ð¾Ñ 13.1. РаÑположиÑе киÑлоÑÑ ...
- No tags were found...
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
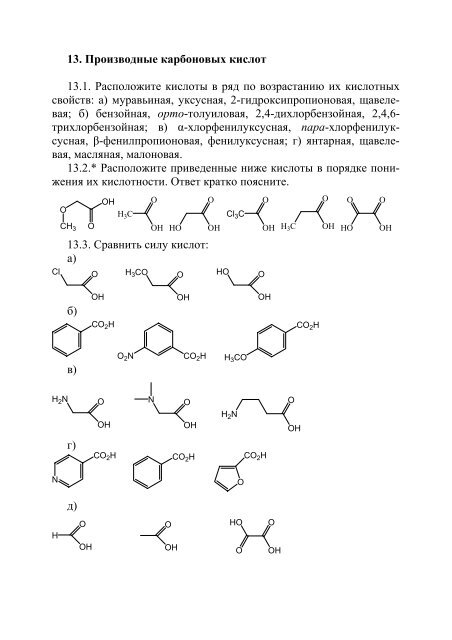
<strong>13.</strong> Производные карбоновых кислот<strong>13.</strong>1. Расположите кислоты в ряд по возрастанию их кислотныхсвойств: а) муравьиная, уксусная, 2-гидроксипропионовая, щавелевая;б) бензойная, орто-толуиловая, 2,4-дихлорбензойная, 2,4,6-трихлорбензойная; в) α-хлорфенилуксусная, пара-хлорфенилуксусная,β-фенилпропионовая, фенилуксусная; г) янтарная, щавелевая,масляная, малоновая.<strong>13.</strong>2.* Расположите приведенные ниже кислоты в порядке пониженияих кислотности. Ответ кратко поясните.OCH 3OOHH 3 COOHHOOOHCl 3 COOHH 3 COOHOHOOOH<strong>13.</strong>3. Сравнить силу кислот:а)ClOH 3 COOHOOб)OHOHOHCO 2 HCO 2 Hв)O 2 NCO 2 HH 3 COH 2 NOOHNOOHH 2 NOOHг)CO 2 HCO 2 HCO 2 HNOд)HOOHOOHHOOOOH
е)CO 2 HCO 2 HCO 2 HClHOHO 3 Sж)HOOOOHOOз)OHOHOOHCO 2 HHO 2 CCO 2 HCO 2 HHO 2 CCO 2 H<strong>13.</strong>4. Расположите следующие соединения в порядке увеличенияих кислотности: α-хлорфенилуксусная кислота, пара-хлорфенилуксуснаякислота, фенилуксусная кислота, фенол, пара-нитрофенол,бензиловый спирт.<strong>13.</strong>5. С какими из следующих реагентов может взаимодействоватьхлорангидрид масляной кислоты: этанол; толуол и AlCl 3 ; глицин;пара-нитрофенол; нитробензол и AlCl 3 ; фенилмагнийбромид?Напишите уравнения реакций.<strong>13.</strong>6. Предложите не менее четырех различных механизмов гидролизасложных эфиров. В каком случае скорость гидролиза практическине зависит от рН среды?<strong>13.</strong>7. Предложите механизм гидролиза трет-бутоксикарбонильнойзащитной группы в составе молекулы аминокислоты, защищеннойпо атому азота. С чем связана легкость гидролиза?<strong>13.</strong>8. Скорость гидролиза этилового эфира уксусной кислоты зависитот рН (каким образом?), а бензилового эфира – нет, объясните.<strong>13.</strong>9. Как зависит легкость реакции декарбоксилированияβ,γ-ненасыщенных циклоалкенилкарбоновыхкислот от размера цикла? Каков механизмCO 2 Hэтой реакции?<strong>13.</strong>10. Предложите механизм внутримолекулярной этерификацииγ-оксикарбоновой кислоты до γ-лактона.<strong>13.</strong>11.* Укажите строение всех продуктов полного кислотногогидролиза соединений, представленных ниже:
а)H 3 COб)H 3 Cв)*OOOSNHONHOHNNHOOOCH 3HNCH 3H 3 C N NH H OCH O3O OOO<strong>13.</strong>12.* Напишите структуры всех продуктов полного кислотногогидролиза противоракового препарата широкого спектра действия –Dolastatin и охарактеризуйте их с точки зрения оптической активности.OONHONHHNOOONHHO<strong>13.</strong><strong>13.</strong> Напишите все продукты гидролиза ацетилкофермента А вкислой среде.OSNHOONHOHOOOPOOOOO OPO OPOHNONOHNPhSNNNNH 2
<strong>13.</strong>14. Напишите продукты реакции, образующиеся при гидролизеданного соединения в щелочных условиях.OH 3 C OOHO ON CH 3NH OO OCH 3CH 3 CH 3<strong>13.</strong>15. Определите строение продуктов полного гидролиза приведенныхниже соединений: а) в кислой среде и б) в щелочной среде.BrH 3 CONOOOCH 3NHNHOHNOOO<strong>13.</strong>16. Приведите структуры продуктов кислотного гидролизаампициллина (ранее широко используемого антибиотика) и артикаина(анестетика, используемого в стоматологической практике),триметина – вещества, обладающего противосудорожным действием,и дульцина – вещества, которое в 200 раз слаще сахара.H 2 NC 6 H 5OHNONАмпициллинOONSCOOHOТриметинHNOOOOSOOCH3OHNOCOOCH 3ONH HClC 3 H 7АртикаинNHNHДульцинNH 2
<strong>13.</strong>17. Напишите уравнения реакций, при помощи которых указанныениже соединения можно превратить в масляную кислоту: а) бутиловыйспирт; б) пропиловый спирт (два способа); в) метилпропилкетон.Какой из перечисленных методов можно использовать для получениятриметилуксусной кислоты?<strong>13.</strong>18. Укажите, с какими из перечисленных ниже веществами будетреагировать бензойная кислота, напишите уравнения реакций:а) Na 2 CO 3 ; з) PCl 3 ;б) NH 3 (aq.); и) SOCl 2 ;в) продукт (д) + нагрев; к) Br 2 /Fe;г) H 2 /Ni, 20 °C, 1 атм.; л) Br 2 + P;д) LiAlH 4 ; м) HNO 3 /H 2 SO 4 ;е) горячий водный раствор KMnO 4 ; н) дымящая H 2 SO 4 ;ж) PCl 5 ; о) CH 3 Cl/AlCl 3 ;п) пропиловый спирт, H + .<strong>13.</strong>19. Укажите все стадии возможных лабораторных синтезовследующих кислот с использованием любых необходимых алифатическихи неорганических реагентов: а) фенилуксусной; б) паратолуиловой;в) мета-хлорбензойной.<strong>13.</strong>20. Напишите полные уравнения реакций (если они происходят)и назовите все органические продукты, образующиеся привзаимодействии бутирилхлорида со следующими реагентами:а) H 2 O; з) спирт. раствор AgNO 3 ;б) изопропиловый спирт; и) CH 3 NH 2 ;в) п-нитрофенол; к) (CH 3 ) 2 NH;г) аммиак; л) (CH 3 ) 3 Nд) толуол, AlCl 3 ; м) продукт (к) + LiAlH 4 ;е) нитробензолом, AlCl 3 ; н) (C 6 H 5 ) 2 Cd;ж) водным раствором NaHCO 3 ; о) C 6 H 5 MgBr;п) продукт (к) + Li[HAl(OEt) 3 ].<strong>13.</strong>21. Напишите полные уравнения реакций метилбутирата (еслиони происходят) с указанными ниже реагентами и назовите всеобразующиеся органические продукты:а) горячий водный раствор H 2 SO 4 ; е) фенилмагнийбромид;б) горячий водный раствор KOH; ж) изобутилмагнийбромид;в) изопропиловый спирт + H 2 SO 4 ; з) аммиак;
г) бензиловый спирт +и) H 2 , CuO CuCr • 2 O 4 , нагревание,давление;C 6 H 5 CH 2 ONa;д) LiAlH 4 , затем кислота; к) Na, C 2 H 5 OH.<strong>13.</strong>22. Предскажите, какие соединения образуются при взаимодействииглицина со следующими реагентами:а) aq. NaOH; д) NaNO 2 + HCl;б) aq. HCl; е) C 2 H 5 OH + H 2 SO 4 ;в) бензоилхлорид + aq. NaOH; ж) продукт (е) + NaNO 2 + HCl;г) уксусный ангидрид; з) бензилхлоркарбонат(C 6 H 5 CH 2 OCOCl).<strong>13.</strong>23. Укажите структуры соединений, которые образуются принагревании следующих аминокислот:а) глицин → C 4 H 6 N 2 O 2 (дикетопиперазин);б) CH 3 CH(NH 2 )CH 2 COOH → C 4 H 6 O 2 ;в) CH 3 CH(NH 2 )CH 2 CH 2 COOH → C 5 H 9 NO (лактам);г) H 2 NCH 2 CH 2 CH 2 CH 2 COOH → C 5 H 9 NO (лактам).Дайте объяснения различному поведению этих соединений принагревании.<strong>13.</strong>24. Напишите уравнения реакций, при помощи которых можнопревратить в аланин следующие соединения: а) α-бромпропионоваякислота; б) ацетальдегид; в) 2-оксопропановая кислота.<strong>13.</strong>25. Напишите структуры всех промежуточных и конечногопродуктов, образующихся в приведенной цепи превращений, ведущейк транквилизатору – мепробамату.CO 2 EtCO 2 Et1. EtONa2. CH 3 I?1. EtONa2. n-C 3 H 7 Br ? LiAlH 4? COCl 2(изб.)? NH 3(изб.)мепробомат<strong>13.</strong>26. При окислении перманганатом калия одного из изомеровметилциклогексена образуется вещество состава С 7 Н 12 О 3 , растворимоев щелочи и реагирующее с гидроксиламином и фенилгидразином.Окисление С 7 Н 12 О 3 сильными окислителями приводит ксмеси кислот, среди которых присутствует глутаровая и адипиновая.Напишите структурную формулу исходного соединения иуравнения всех упомянутых реакций.<strong>13.</strong>27. Нарисуйте проекцию Фишера природной глутаминовойкислоты. Какое строение будет иметь эта кислота в изоэлектрическойточке (рН ~ 3,2)? Как изменится строение при увеличении ки-
слотности среды? При добавлении щелочи? Какое превращениепроизойдет при нагревании этой аминокислоты?<strong>13.</strong>28. Реакция бромирования алифатических карбоновых кислотбромом по α-углеродному атому может катализироваться не толькофосфором, но и, например, хлористым бензоилом. Предложите схемуэтой реакции.<strong>13.</strong>29. С какими из следующих реагентов может взаимодействоватьбензамид: а) метанол в кислой среде; б) алюмогидрид лития;бром в щелочной среде; в) триэтиламин; г) хлористый тионил; д) метилмагнийиодид(1 М)? Напишите уравнения реакций.<strong>13.</strong>30. Какие из перечисленных ниже соединений могут быть полученыперекрестной конденсацией? Напишите соответствующиепары реагентов-предшественников.а)C 2 H 5 OO 2 Nб)ACNAOOOOOOCH 3PhB C DOOPhOOOCNOC 2 H 5PhOPhEB C D<strong>13.</strong>31. Предложите метод синтеза указанного ниже соединения сиспользованием циклогексанона, диэтилкарбоната и (или) метилвинилкетона.OONO 2<strong>13.</strong>32.* Синтезировать (если это возможно):* *OOOOOCH*3OCH 3<strong>13.</strong>33.* Что вы можете сказать об оптической активности продуктовгидролиза оптически активных эфиров уксусной кислоты,изображенных ниже?OH*OH
OHOPh<strong>13.</strong>34. Расшифруйте цепочку превращений; А – альдегид, В –карбоновая кислота.OOOHOOHCl (газ)Ph 3 PNa (изб.) 1. O? ? ? 3NH?3 (ж)2. H 2 O/Zn(C 9 H 14 O)- АH 2 O 2AcOH?HO - /H 2 O-B?CutA<strong>13.</strong>35.* Определите структуру соединения А и укажите продуктыего превращений после стандартной обработки реакционныхсмесей.а)*?KMnO 4t? SOCl 2A?EtMgBr(изб.)CO 2 HA1.NaN 3, t2. H 2 OH 2?Pd/BaSO 4LiAlH 4б)??LiAlH 41. BuLi2. H2 OSn? 1. HNO HO2H + 2. CuCN A A-?PhNO 2 H 2 O 21. LiAlH(OEt) 3CH 3 OH2. H 3 O + H +????
в)CH 3 COCl??NHEtCH 2 3 Li(изб.)C 6 H 6 PhCO 3 H OEt A A-??AlCl 3C 2 H 5 OH (изб.)NEt 3 , H 2 OH +?<strong>13.</strong>36. Укажите строение продуктов следующих превращений:а)? CH1. CH 3 MgI (2M)3 COCH 3??HN(CH 3 ) 2PhCO 2 EtEtONaLiAlH 4?2. H 3 O + ?б)??Na Br 2 CO 32HO 2 CAg 2 OPhSOCl 2?в)?(CH 3 ) 2 CHOHH +NH 3tCO 2 Et??1. NH 32. NaOBrNaNH 2H 2?хромит меди<strong>13.</strong>37.* Предложите метод синтеза соединений, структуры которыхприведены ниже, из неорганических реагентов:?
PhOOOOHO 2 COа)б) Phв)OOCO 2 HCO 2 HCO 2 HPhPhOг)CO 2 H д) CO 2 Hе)Phж)*Oз)*HNHNHNи)OH 2 NNHO к)H 2 NNH 2PhCOOHOл)NPhNH 2м)OOн)OOо)*HOHOOп) H 3 COOOOOHNOOOPhOр) FУказание: прежде чем приступать к построению последовательностиреакций, приводящей к соединению п, изобразите строениепродуктов гидролиза этого соединения.
<strong>13.</strong>38.* Предложите метод синтеза этилового эфира 2-метил-3-оксо-2,3-дифенилпропановой кислоты из неорганических соединенийи изобразите структуры продуктов, образующихся при взаимодействииэтого соединения с водными растворами кислоты и щелочипри нагревании. Приведите механизм этих превращений.<strong>13.</strong>39.* Предложите метод синтеза из неорганических соединенийпрактолола – β-адреноблокатора.H 2 NOOПрокталолNHH NHCH 3HPhOHЭфедринОхарактеризуйте с помощью структур Фишера и R,S-номенклатурыстереоизомерный состав синтезированного вами проктолола.Как можно выделить энантиомерно чистый препарат с использованиемнабора оптически индивидуальных кислот и оснований,например, L(-)яблочной кислоты HСOOCH 2 CHOHCOOH и(-)эфедрина? Все реакции напишите для конкретных соединений.<strong>13.</strong>40. Приведите строение всех соединений в следующих превращениях:H 3 COCH I 2 (0,5 M)AOEt - B COH -3 COCl PhCO 2 Et CHOEt -D 3 NH 2AlCl t3 t- EСоединение E, образующееся наряду с D, является солью карбоновойкислоты. Объясните направление реакции, приводящей кэтим продуктам.<strong>13.</strong>41. Изобразите строение всех возможных продуктов, образующихсяпри взаимодействии этилацетата с этилизобутиратом вприсутствии этилата натрия. Укажите, какой (какие) из них являетсяосновным и почему.<strong>13.</strong>42. Приведите примеры реакций конденсации следующих парреагентов, которые могут быть проведены с приемлемым выходом:а) альдегид + альдегид; б) альдегид + кетон; в) альдегид + сложныйэфир; г) кетон + сложный эфир; д) сложный эфир + сложный эфир.<strong>13.</strong>43.* Укажите строение продуктов в следующих цепочках превращений:F
а)CO 2 H PCl 5 1. (CH 3 ) 2 Cd? ?2. H 2 OCl 2 (1M)H +1. KCN? 2. H3 O + , t?б)H 3 COBr 2 (1M)hν?1. NaCN 1. CH 3 OH?2. H 3 O + 2. LiAlH 4?PBr 31. Mg (эфир)? ?2. CO 23. H 2 Oв)Oг)O1. CH 3 OH?2. SOCl 2OH 2 ? 1. PhNH 2, H +?Pd/BaSO 4 2. LiAlH 4CO 2 EtCO 2 Et1. OEt -?2. CH 3 I (1 M)1. OEt -2. CH 3 ONO 2OH - (конц.)? ?д)Oе)NRON 2 H 4RNH 2 + ?tHNO 2?NaNaKCN? PhCO 2 Et?EtOHтолуолж)PhCHO1. HCN2. H 3 O + ?OH - H 3 O +Fe 3+ ?NaEt 2 OCO 2 EtCO 2 EtOEt - ?з)*t1. O 32. H 2 O A EtOH, H + Бt1. EtONa2. H 3 O + , tГ 1. NH 2OH2. H 2 SO 4, tД
и)CO 2 EtNaNO 2 HH 3 O + A Б 1. EtONa 2 /PdCH 3 OH Na 2 CO 3B H 3O +Г ДAc 2 O 2. EtBr tH +tCO 2 Etк)EKMnO 4H 3 O +AEtOH, H +tБ1. EtONa2. H 3 O + , tГ1. PhCO 3 H2. H 2 O, OH -Дл)*ONKCO 2 EtCO 2 EtPhCHONHOA Б H 3O + , t 1. SOCl 2B- CO 2 2. CH 2 N 23. Ag 2 OГ_OH - , tДSOCl 2пиридинCO 2-Eм)PhOK CO 2tH 2 Nн)о)CO 2 HCO 2-A CH 3I (изб.)OH - Б 1. H 3O +2. SOCl 23. (CH 3 ) 2 CdtA1. PhCHO (2M), OH-2. HI, P3. H 3 O + , tCO 2 EtВБOEt - Г 1. PhNH 22. H + , tБ 1. CH 3OH, H +2. CH 3 ONOДВ 1. CH 3CO 2 H2. H 3 O +3. tГCH CO 2 EtH 2 /PdA Б B ГCH 2 NCH 2 Д NaH3 NO 2 O H 3 O +2H + EtONa t Ac 2 Ott=20 oE
п)OSO 2 Cl1.NKOр)HBrA CH 3COCl1 экв.tPhCO 2 H 1. HNO 3/H 2 SO 42. N 2 H 4 /Ni1. LiAlH 42. SOCl 23. KCN4. LiAlH 4 (изб.)с)ГCH 3 CHOH +Б2. OH - , t3. H 2 OA 1. HNO 22. H 3 O + , tДOБ (CH 3O) 2 SO 2 (изб.)Na 2 CO 3(2 M) NaHВ Г ДtPhCHO 1. Ac 2O, NaOAc, tA CH 3NO 2 1. Zn/H + 1. NaHБ В Г2. H 2 OOEt - 2. t 2. PhCH 2 Cl3. CH 2 N 2т)CO 2 EtCO 2 Etу)1. OEt -2. CO 2 Et+3. PhN 2CO 2 H Br 2 / CCl 4HgO1. H 3 O + , t 1. CH 3 OH, H + LiAlH 4 (изб.)A Б В Г2. Zn/H + 2. Na 2 CO 3, tA PhCO 2 - Na +БNaEt 2 OВВ + Гф)CNNa / EtOHГ + Д1. EtMgBr CO 1. H 3 O +2. H 3 O + A 2 Et, t PClБ 5 1. NHCH 33 CNВ Г Д2. H 2 / Ni 2. PCl 520 o , 1 атм.NH
х)OOOEtCO 2 CH 31. LiAlH 42. PBr 3AtNa + Б H 3O + Г + ДВц)NaOH конц.1. LDA (2 M) 1. SOCl 2 AmONO Zn H 3 O +PhCH 2 CO 2 H A Б B Г Д2. CO 22. EtOH OEt - AcOH tAc3. H 2 O2 Oч)CO 2 EtI 2 (0.5 экв.) 1. OEt - (2 экв.) HOEt - A Б 3 O + H 3 PO 4 /P 2 O 5В Г2. PhCOCl (2 экв.) tCO 2 EtOOOДH 3 O +tЕш)O1.NKCH 3 CO 2 H Cl 2 (2 M)P (0.3 M)ы)*EtOHА БO t 1. PhCHO (2M)В Г Д2. OH - , t2. HI, P3. H + 3. H 3 O +O MgClOCH 3 CHOэ)PhOH -O1. OEt -CO 2 Et2. PhCH 2 Cl1. O Cu + AgA Б 2 O NaBH 4 HВ Г + NHД 3Е2. H 3 O + tC 12 H 14 O 2CH 3 ONO 2 OEt -А Б ВNaH1. H 2 / Pt (20 o , 1 атм.) 1. NaH (2 экв.)ГД2. t o (-2C 2 H 5 OH) 2. CH 3 I (2 экв.)3. H 3 O +t o
ю)OONKBrCO 2 C 2 H 5CO 2 C 2 H 5АBr2.1. EtO -CO 2 C 2 H 5Б H 3O +t- CO 2глутаминоваякислота<strong>13.</strong>44.* Укажите строение продуктов в следующих цепочках превращений:а)Phб)Oв)Ph 2 CHClг)д)е)OOOONKBrCH 3 CO 2 EtNaOEtCO 2 C 2 H 5CO 2 C 2 H 51. NaOEtA2. C2 H 5 Br1. EtO -NH 3А Б В H 3O +G2.NaCN 1. EtOH, H + 1. EtONa?2. H 3 O + ?2. H 2 OOCH 3 COCH 3OH - , tNaOBrCH 2 O(CH 3 ) 2 NH + Cl -Br1 мольBr1. NaOEt OHBC-D2. I 2 (0.5 M) tCH 3 NHNH 2NH 3 t? H 3O +t1. NaOBr?2. H 3 O + ? SOCl 2? EtOHH + ??t1. NaOEt2. H 3 O + , tt- CO 2E 1. CH 3MgI2. CH 3 I1. NH 2 OH? ? LiAlH 42. H + , tлизин? NH 2CH 3 H 2, Pt?20 o ?, 1 атм.O? ? Ag 2O ?NaOEt1. NaOCl 1. Na 2 CO 3?2. H 3 O + ?2. EtBr(C 3 H 6 O 3 )?F?1. NaH2. CH 3 I1. LiAlH? 4?2. H 2 O
ж)O1. Mg (эфир)EtBr ? EtBr 1. NaOEt? ?2. CO 2 2. PhCO 2 Etз)*NaOEt? H 3O +t?CHO Ac 2ONaOAc, t? 1. CH 3Li (изб.)2. H 2 Oи)к)CO 2 EtO?CO 2 Et1. OEt -2. CH 3 ICO 2 Et Br Br(0.5 M)л)? H 3O + 1. Na 2 CO 3 1. EtONa??(C 2. EtI7 H 14 O 3 )2. CH 3 I? H 3O + , t? NH 2OH ?H 2 SO 4 (к.) HNO 2? ?1. OEt - ? H 3O + , t CH ? 2 N 2 (изб.) 1. OEt -? ? LiI ?2. PhCH 2 Cl1. LDA (2 M)PhCH 2 CO 2 H2. CO 23. H 2 Oм)н)CO 2 EtCO 2 Etо)1. O 3А EtOH2. H 2 OH +1. SOCl 2 AmONO Zn H? 3 O +? ?2. EtOH OEt - ? ?CH 3 CO 2 H t(CH 3 CO) 2 OБ1. N 2 H 4 (2 M)2. HNO 2 (изб.),3. tВ1. H + (1 экв.)2. tBr(1 M)BrА LiAlH 4 (изб.) PBr Б 3 (изб.) ВCO 2 Et(1 M)CO 2 EtOEt - (изб.)OEt - (изб.)?Г?H 3 O +Г H 3O + ДtNH 4 OH, H 2 O5 o CO 2?V 2 O 5NH 32PhOH ZnCl 21.KOH, EtOH?2.Cl(CH 2 ) 5 OMe? KOHt??
п)OCO 2 Et1. LiAlH 41. PBr 3 изб.H 3 O? +? ? ?2. H 2 OCO 2 Et2. CH 2 (COOEt) 2 (2 M) tNH/NaH (2 M)1.EtOH / H + H 3 O? +?2. EtO - tAр)EtCO 2 H Br 2 (2 M)P (0.3 M)EtOHH + ?с)NaCNH 3 O +t = 30 oCH 3 CO 2 H Br 2 (2 M)P (0.3 M)? EtOH ? NEt3 ?t?A? H 3O +NEt 3 t = 100 ? o1. EtOH, H +? EtOH KCN 1. EtO -A ? ? ?2. H 2 O 2. AH 3 O +t = 100 o ?т)*PhCH 3Br 2hνP 2 O 5t?NH 3?NaOBrtLi +1. -78 o1. Mg (эфир) EtBr? ? ?N2. CO 2 2. CO 23. H 3 O +?SOCl 2 EtOH? ? Br 2 (0.5 M)EtO - ? H 3O +t<strong>13.</strong>45.* Установите структуру соединения А. Укажите условия, вкоторых А превращается в В и С. Предложите соединения, из которыхА может быть получено в одну стадию (сборка углеродногоскелета!).а)*OO?A??- O 2 CCO 2-CO 2-BCCO 2-
б)HO 2 CPhв)OBBOOPh?A? A??CH 3 CO 2-C+ - O 2 C(CH 2 ) 3 CO 2--PhCO 2 +-Ph(CH 2 ) 2 CO 2C<strong>13.</strong>46. Напишите все необходимые уравнения реакций и условияих проведения (не обязательно в одну стадию):а)б)O? ?а бO??CH 2 N 2CN? Ag+ ?NH 2 ClвгдУсловия реакций:? ??а)б)в)г)д)(CH 3 ) 3 COK;SnCl 2, H 3 O + ;1. EtMgBr; 2. H 2 O;1. LiAlH 4 (недост.); 2. H 2 O;EtOH (изб.), H + .CN?вагOбOH?д? ??DУсловия реакций:б) CaO, t;в) SOCl 2 ;г) Ag(OH), Br 2 ;д) CH 2 N 2 .DNCO CH 3OH HO - ? H2 O ?а) 1. CH 3 Li (изб.), t; 2. H 2 O;
в)CO 2 EtCO 2 Et? ?CO 2 Et?в?аг?б?д?ONHOHУсловия реакций:CH 3 COCl-HClCH? 3 ONaа) EtONa (0.1 M), CH 3 (CH 2 ) 3 OH (изб.);б) 1. CH 3 MgBr (изб.); 2. H 2 O;в) EtONa (1 M), t;г) Na, C 2 H 5 OH;д) NH 2 NH 2 .<strong>13.</strong>47. Предложите ряд превращений, позволяющих последовательноотделить атомы углерода от молекулы соединения А.HOOCONH 2OCOOHа)A б) A<strong>13.</strong>48.* Предложите метод синтеза соединения А из бензола илюбых органических соединений С 1 –С 2 . Укажите строение продуктареакции А с гидразином в указанных условиях.FHO 2 COAOCO 2 HFN 2 H 4 , 1 MH +<strong>13.</strong>49. Предложите метод синтеза диэтилового эфира α,α'-диметиладипиновой кислоты из малонового эфира и любых другихреагентов. Какое соединение образуется из этого эфира при нагреванииего с натрием в толуоле (с последующей обработкой водой)?Напишите уравнение реакции.<strong>13.</strong>50. Предложите метод синтеза диэтилового эфира α-метилянтарнойкислоты из малонового эфира и любых других реагентов.Какое соединение образуется из этого эфира в условияхреакции сложноэфирной конденсации? Напишите уравнение реакций.?
<strong>13.</strong>51.* Исходя из Ca 14 CO 3 и любых органических и неорганическихреактивов, предложите метод синтезапропионовых кислот сизотопной меткой в различных положениях.CH 3 CH 2 * COOH CH 3 * CH 2 COOH * CH 3 CH 2 COOH<strong>13.</strong>52. Предложите метод синтеза из пропионовой кислоты, меченойизотопом 14 С (положение метки неизвестно), минимум трехсоединений, включающих в каждом случае только один из углеродныхатомов исходной пропионовой кислоты.3 CH 3 2 CH 2 1 COOH A( 1 C) B( 2 C) C( 3 C)<strong>13.</strong>53. Предложите метод синтеза 2,5-дикарбэтоксициклогександиона-1,4исходя из этанола с использованием необходимыхнеорганических реагентов и напишите реакцию его взаимодействияс водной кислотой при нагревании.<strong>13.</strong>54. Предложите метод синтеза 2-карбэтоксицикло-пентанонаисходя из бензола и этанола с использованием неорганических реагентови напишите реакцию его взаимодействия с водной кислотойпри нагревании.<strong>13.</strong>55.* Предложите метод синтеза из бензола и этанола диэтиловогоэфира α,α`-диэтил-α,α`-дибензоилянтарной кислоты и напишитереакцию его с концентрированной щелочью и разбавленнойкислотой при нагревании.<strong>13.</strong>56. Предложите метод синтеза 2-карбэтоксициклогептанонаисходя из малонового эфира с использованием необходимых неорганическихреагентов и напишите реакцию его с водной кислотойпри нагревании.<strong>13.</strong>57. Предложите метод синтеза этилового эфира 2-ацетилциклогексанон-2-карбоновойкислоты с использованием этанола инапишите реакцию его с концентрированной щелочью и разбавленнойкислотой при нагревании.<strong>13.</strong>58. Предложите метод синтеза с использованием бензола иэтанола этилового эфира α-ацетил-α-бензоилмасляной кислоты инапишите реакцию его с концентрированной щелочью и разбавленнойкислотой при нагревании.<strong>13.</strong>59. Предложите метод синтеза метилциклобутилкетона изацетоуксусного эфира и любых других доступных реагентов. Какиепродукты образуются в реакции этого кетона с этилацетатом в присутствиинатрия в диэтиловом эфире (с последующей обработкойводой)? Напишите уравнение реакции.
<strong>13.</strong>60. Предложите метод синтеза с использованием в качествеисходных соединений простых альдегидов и / или кетонов С 1 – С 4 ,этилмалоновой кислоты, адипиновой кислоты.<strong>13.</strong>61. Приведите схему синтеза следующих кислот из малоновогоэфира и любых других реагентов: а) α,β-диметилмасляной кислоты;б) α,β-диметилянтарной кислоты; в) 2-этилбутановой кислоты;г) циклобутанкарбоновой кислоты.<strong>13.</strong>62.* Предложите метод синтеза α,α'-диметиладипиновой кислотыс использованием простейших органических и любых неорганическихреагентов двумя способами – с использованием ибез использования малонового эфира.<strong>13.</strong>63. Предложите метод синтеза 1,2-бис(карбоксиметил)-циклогексана с использованием простейших органических и любыхнеорганических реагентов двумя способами - с использованиеми без использования малонового эфира.<strong>13.</strong>64. Предложите метод синтеза β,β’-диметиладипиновой кислотыс использованием только простейших органических и любыхнеорганических реагентов двумя способами – с использованиеми без использования малонового эфира.<strong>13.</strong>65. Приведите уравнения реакций в том случае, когда онипроисходят, отметьте случаи, когда превращения не происходят.а)??PCl 5HHOCHNH 2 CONH 2 CH 2 OH, H +2OHLiAlH 4OOC 6H 5NHNH 2HCN???б)AZn (Hg)H 3 O +HOHOCH 3NH 2 OHC?ClCH 2 OCH 3BNaHCO 3OOCH 3 COClNEt 3D
<strong>13.</strong>66.* 1,3-Индандион используют в синтезе алифатических нитросоединений.Ниже приведен пример реализации такого синтеза:O1. OEt -2. PhCH 2 ClA1. OEt-B OHt2. CH 3 ONO 2PhNO 2 + COа) Укажите строение всех продуктов приведенной цепи превращений.б) Предложите метод синтеза 1,3-индандиона, используя соединениеС (на схеме), этанол и этилацетат.в) 1,3-Индандион может быть превращен с использованиемдвухстадийного синтеза в нингидрин – реагент для определенияα-аминокислот. Первая стадия – взаимодействие с NaNO 2 в кислойсреде, а вторая – кислотно-катализируемый гидролиз. Первая стадияпроисходит по механизму, аналогичному реакции сложноэфирнойконденсации. Нингидрид – трикетон, существующий в видемоногидрата. Изобразите структурную формулу этого моногидратаи объясните, почему устойчива именно гидратная форма.<strong>13.</strong>67. Простейшая аминокислота глицин может быть использованав синтезе других аминокислот в соответствии со следующейсхемой:H 2 NCO 2 HPhCOClA H+- H 2 OB 1. OEt -(C 9 H 7 NO 2 ) 2. PhCHO C 1. H 2 (1 M)PdHD 3 O +- PhCO 2 HPhNH 2CO 2 Hа) Укажите строение всех продуктов в приведенной цепи превращений.б) Циклическое соединение В называется азлактоном, и его молекуламожет выступать в качестве активной метиленовой компоненты.Объясните, почему, и приведите механизм реакции, приводящейк образованию соединения С.в) Одним из процессов, в котором участвуют α-аминокислоты ворганизме, является их взаимопревращение с участием пиридоксаля(одного из соединений, входящих в группу витаминов В 6 ) и ферментатрансаминазы. Это превращение на примере аланина и фенилаланинаможно описать следующей схемой:
PhNH 2RCHO гидролизA A'CO 2 H изомеризацияOпиридоксаминCO 2 HгидролизC C'изомеризация - RCHOB + пиридоксаминPhNH 2CO 2 HHOCHONпиридоксаль(RCHO)Укажите строение всех участвующих в приведенной схеме соединений.<strong>13.</strong>68. В результате окисления кетокислоты A состава С 5 H 8 O 3KMnO 4 в кислой среде при нагревании была получена смесь уксусной,янтарной и малоновой кислот. При восстановлении кетокислотыА NaBH 4 получено соединение, которое при нагревании (160 °С)образует циклический продукт. Напишите упомянутые в задаче веществаи реакции.<strong>13.</strong>69.* Предложите методы и реагенты, необходимые для проведенияуказанных превращений (не обязательно в одну стадию).а)*OOб)OOEtHNOONHEtOOCH 3CH 3OOOOHOHOHOHв)COOHCH 3OOHNH 2CH 3O
<strong>13.</strong>70. Предложите метод синтеза: а) бромбензола-1-С 13 ; б) фторбензола-2-С13 ; в) анилина-3-С 13 . В качестве источника изотопа углеродаиспользовать карбонат (С 13 ).<strong>13.</strong>71. В приведенных схемах каждой букве соответствуетодин из типов производных карбоновых кислот, причем каждойбукве – свой тип. Предложите значение для каждой из букв, еслиА – бензойная кислота, а каждая из линий обозначает, что соединенныеею буквы (вещества) могут быть получены одно из другого.Укажите условия, в которых могут происходить эти превращения.A B CABCDа)D E F б)АFEВББВАв)Г Д г) ДГ<strong>13.</strong>72. Определите, что скрывается за каждым знаком вопроса вприведенных схемах.а)PhCO 2 Hб)PhCO 2 H????? ????? ??PhCONH 2 ???PhCOClPhCNPhCO 2 CH 3???
<strong>13.</strong>73. Определите структуру соединения А и укажите продуктыего превращений после стандартной обработки реакционных смесей.а)б)O 2V 2 O 5?tNH 3ABrt2, NaOH?tCl 2, NaOH EtOH, H + ?1. KOH2. EtBrLiAlH 4охлаждение???? ?1. PhMgBr EtOH2. EtOH H +в)CH 2 OHCl, ZnCl 2?OCH 31. ДМФА, POCl 3 HCO 2 H/H 2 O 2NaCNA 1. SnCl 2 , H +1.EtONa2. H 2 O ?LiAlH 42. EtBr???1. SOCl 2NH 32. NHEt 2 t?A2. H 3 O + ?1. EtOH, H +?2. EtOAc, EtONa1. SOCl 2OCH 3 HNO 32. CH 2 N 2 H 2 SO 4?3. Ag 2 O?<strong>13.</strong>74. Предложите способ синтеза указанных ниже соединенийисходя из бензола, метилового и этилового спиртов и необходимыхнеорганических реагентов.OONа)Oб) N
<strong>13.</strong>75. Предложите метод синтеза соединений, структура которыхпредставлена ниже, из неорганических соединений. Напишитереакции этих соединений: а) с концентрированной водной щелочью;б) с водным раствором кислоты при нагревании.а) ClOCO 2 EtCl б)CNCO 2 Et<strong>13.</strong>76. Предложите метод синтеза этилового эфира 2-бензил-3-оксо-2-фенилбутановой кислоты из простых органических соединений(бензол, С 2 ).<strong>13.</strong>77.* Предложите метод синтеза из неорганических реагентовсоединений, структура которых представлена ниже:OOOа)O б)*в)г)OO 2 NOOд)OOе)ж)OOOз)*NHOOи)<strong>13.</strong>78.* Предложите способ получения указанного ниже соединенияисходя из бензола и любых неорганических реагентов.
а)*PhPhPhO O б)HO 2 CCO 2 HCO 2 HHO 2 CFк)в) HO 2 C CO 2 H г)PhO 2 NHCCOOC 2 H 5EtOOCHOCH 3д)*е)*OHOOCHOOCPhPhPhж)COOH з)COOH и) COOHCOOHNOHCOOH NCHOOCPh л)NH 2COOHРешения некоторых задач<strong>13.</strong>2. Положение кислотно-основного равновесия определяется вслучае диссоциации кислот стабильностью карбоксилат-аниона –чем он устойчивее, тем сильнее кислота. Акцепторные (по индуктивномуэффекту) заместители стабилизируют анион, донорные –напротив, дестабилизируют.Cl 3 CH 3 COOH (1) >OOH (5) >OHOOOHOH 3 C OH (6)OOH(2) > HO OH (3) > CH 3 O (4) >O
Гидроксиуксусная кислота (3) заметно сильнее, чем метоксиуксусная(4), потому что, помимо стабилизирующего анион акцепторноговлияния атома кислорода, существенное влияние на его стабилизациюоказывает внутримолекулярная водородная связь. Важноотметить, что и в недепротонированной форме водородная связьтакже существует, но она более слабая, чем в анионе, поскольку впоследнем случае донорно-акцепторное взаимодействие атома водородапроисходит с отрицательно заряженным атомом кислорода.OOHOH<strong>13.</strong>11. в.O± H + OCH 3H 3 C N NH H OOO OCH 3OOHOCH 3 OH + CO 2 + H 3 NOHH 3 O + H 3 C NH 3O + +O OH<strong>13.</strong>12. На рисунке приведены продукты гидролиза с указаниемабсолютной конфигурации асимметрических центров. Гидролизпростых эфиров требует очень жестких условий и в данном случаене происходит. В процессе гидролиза возможна рацемизация α-аминокислота и б. Гидролиз ароматического гетероцикла тиазола вмолекуле соединения д также маловероятен.OCH 3+OHOHHSNCO 2 HSH NH 2CO 2 HH 3 CHNOC 3 H 7RHRHCO 2 HHNH OSRHCO 2 Hа б в гPhH 2 NRдSN
<strong>13.</strong>32. Синтез соединений а и б возможен, синтезировать индивидуальныесоединения в и г невозможно, поскольку между ними существуетбыстрое равновесие.O* *OOOOCH*3OCH 3OH*OH(а) (б) (в) (г)CH* CH 3 OH H +3 OH H +O*OOH*OH*<strong>13.</strong>33. В случае соединения А гидролиз как в щелочной, так и вкислой среде происходит по типу присоединения-отщепления покарбонильной группе сложноэфирной группировки. Поэтому в щелочнойсреде рацемизация не происходит вовсе, в кислой она возможнав незначительной степени вследствие дегидратациии и последующейгидратации образующегося спирта.OOHOH -HOOOH- CH 3 CO 2 HHOHAВ случае гидролиза соединения Б в кислой среде реакция можетпроисходить по механизму S N 1 с образованием устойчивого третичногокатиона, в результате чего образуется рацемический спирт.В щелочной среде реакция может проходить как по типу присоединенияотщепления, так и по механизму S N 1, вследствие чего будетнаблюдаться частичная рацемизация продукта.HOOH -- CH 3 CO 2 HS N 1- CH 3 CO 2 H H 2 O- H + OHРацематOOБH 3 O +OHO
Гидролиз соединения В может происходить тремя путями: в кислойсреде реализуется механизм S N 1 (образуется устойчивый бензильныйкатион), т. е. происходит рацемизация. В щелочной средевозможна реакция как по типу присоединения-отщепления, так инуклеофильное замещение по бимолекулярному механизму (бензильноеположение!), приводящее к обращению конфигурации. Соотношениеэтих процессов зависит от растворителя – при проведенииреакции в воде вклад механизма S N 2 меньше (вода – протонныйрастворитель), при взаимодействии же эфира В со щелочью в апротонномдиполярном растворителе бимолекулярный процесс будетпреобладающим.OHOHPhH 3 O +OOВHPhHO - S N 2HO -- CH 3 CO 2 HHHOOHHPhОбращениеконфигурацииPhHOHPhS N 1- CH 3 CO 2 HPhH 2 OPh- H + OHРацемат<strong>13.</strong>35. а)OEtPhOHEtEtMgBrPhNH 2PhCHO1. NaN 3, t2. H 2 OKMnO 4SOCl 2PhCH 3 PhCO 2 H PhCOCltH 2Pd/BaSO 4CO 2 HLiAlH 4PhCH 2 OHCOCl + PhCO 2 H
<strong>13.</strong>37. ж) Ретросинтетическая схема:OOCO 2 HCO 2 EtCO 2 EtHO 2 C O O CO 2 HC 6 H 6Полная схема синтеза:C 6 H 6O 2V 2 O 5HO 2 CBrEtO 2 CCO 2 HBrOOOEtOHH +OOEtO -OHCO 2 EtCO 2 EtCO 2 EtHO - , tHO 2 CH +H 2PdHO 2 CHOCO 2 HNCSCO 2 EtCO 2 EtEtO -CO 2 HHO 2 CEtO 2 COOBr 2 (1M)PCO 2 HClCO 2 EtH 2, Ni20 o , 1 атм.HO 2 CCO 2 H1.HO -2. H +ClOCO 2 Hз) Ретросинтетическая схема:OCO 2 EtHNHNEtOOOEtCO 2 EtHNEtOOOCO 2 Et
Полная схема синтеза:CH 3 CO 2 HBr 2P (0,3 M)BrCH 2 COBr1. EtOHCO2. NaCN2 Et3. EtOH, H +4. H 3 O + CO 2 Et1. EtO -2. CH 3 Br3. H 3 O + , tBrCO 2 HBr 2P (0,3 M)COBr1. EtOH2. EtO - CO 2 EtOOEtOEtOCO 2 EtCO 2 EtCO 2 EtEtO -CO 2 EtCO 2 Et1. H 3 O + , t2. EtOH, H + CO 2 EtEtOEtOOOHNHN1. CH 3 NH 22. LiAlH 43. H 2 OHNо) Ретросинтетическая схема:OOOHOCNEtOOHOHO+CH 3 CO 2 EtПолная схема синтеза:C 6 H 6H 2 SO 4SO 3C 6 H 5 SO 3 H HOtPhOH H 2Pd/COHCrO 3H 2 SO 4OCH 3 CO 2 HBr 2P (0.3 M)BrCH 2 COBrEtOHBrCH 2 CO 2 EtZnO2.H 3 O +
HO 2 COHtHO 2 CKCNHO 2 CCNHO 2 C1. LiAlH(OEt) 3 (2 экв.)2. H 3 O +OH<strong>13.</strong>38.C 6 H 6Br 2 / FeC 6 H 5 Br1. Mg / (эфир)2. CO 23. EtBrC 6 H 5 CO 2 EtCaC 2H 2 O C2 H 2Ct1. EtOH, H +C 6 H 62. H 3 O + PhCH 2 CO 2 EtOCH 2 O, HClZnCl 2C 6 H 5 CO 2 EtEtO -PhCH 2 ClOPhPhNaCNCO 2EtPhCH2 CNCH 3 IСхема кислотного а и кетонного б расщепления β-кетоэфира:PhPhCO 2 EtPhHO -tO-CO 2а)PhHOPhPhCO 2-OPhO - - PhCO 2-PhCO 2 EtPhCO 2-H 3 O +tб)PhOHPhOO- CO 2PhOHPh<strong>13.</strong>39. Полная схема синтеза:PhMg 2 C 3H 2 O H 2Pd/BaSO 4O 2AgOPhOH 3 O + Hg 2+ONHH 2 , NH 23CuO, Cr 2 O 3
OHONH 2 HONH p-TsClNEt 3TsONTsEtO 2 CNa 2 CO 3OTsNHO -OHNO1. CH 2 N 22. NH 3*HNCO 2 EtCO 2 HCONH 2В молекуле присутствует один асимметрический центр (отмечен«*»), образуется рацемическая смесь, разделить которую можнос использованием оптически активной кислоты, например L(-)-яблочной.При взаимодействии с этой кислотой образуются две соли,являющиеся диастереомерами. Эта смесь может быть разделенаобычными физико-химическими методами (например, перекристаллизацией).После гидролиза каждого из диастереомера регенерируетсяисходная оптически активная кислота, которую можноотделить от основания промыванием водным раствором соды, в результатечего можно выделить энантиомерночистый амин.<strong>13.</strong>43. з)1. O 3EtOH, H +2. H 2 O CO 2 H tCO 2 HCO 2 EtCO 2 Et1. EtONa2. H 3 O + , tO1. NH 2 OH2. H 2 SO 4, tNHОсновнойпродуктO+ONH
л)OCO 2 EtPhCHOCO 2 EtNHPhEtO 2 COCO 2 EtNKPhH 3 O + , t 1. SOCl 2N- CO 2 2. CH 2 N 2CO 2 H 3. Ag 2 OOPhPhы)CO 2 HSOCl 2OпиридинNH 2NPh HOOPh<strong>13.</strong>44. з)CH 3 CHOOH -PhOOOMgClONOOONPhCO 2 EtPhCO 2 HCO 2 EtOH - , tCHO1. O Cu + OAg 2 O2. H 3 O + PhOCO 2 HCO 2 HOHNaBH 4 H + O NH 3 HNtPhPhPhCHO Ac 2ONaOAc, tOHCO 2 H H 3 O + CO 2 H 1. Na 2 CO 32. EtIOOHCO 2 Et1. EtONa2. CH 3 IOCH 3CO 2 EtH 3 O +OCH 3CO 2 H1. CH 3 Li (изб.)2. H 2 O?OCH 3 O
т)PhCH 3Br 2hν1. Mg (эфир)- EtBrPhCH 2 Br PhCH 2 CO 22. CO 2PhCH 2 CO 2 EtLi +1. -78 oPh CO 2 HNSOCl 22. CO 23. H 3 O + CO 2 HPhCO 2 EtCO 2 Et<strong>13.</strong>45. а.PhCOClCOClPh PhBr 2 (0,5 M)H 3 O +EtO - EtO 2 C CO 2 EttEtO 2 C CO 2 EtEtO 2 COEtOHPhPhCO 2 HCO 2 HOOH 3 O + tOCO 2 EtA- O 2 CHO -tCO 2-CO 2-BBr BrCO 2 EtEtO -CO 2 EtCO 2 Et (0,5 M)OO<strong>13.</strong>48. Ретросинтетическая схема:CO 2 HCO 2 EtHO 2 CFEtO 2 CCEtO 2 CCO 2 EtACO 2 EtOCO 2-OFOOFOCO 2 EtF
EtO 2 CCO 2 EtFEtO 2 CCO 2 HFOOПолная схема синтеза:FOFCO 2 HC 6 H 6-EtBrMnO 4AlCl 3 tPhCO 2 H 1. HNO 3/H 2 SO 42. H 2, Pd/C1. HNO 22. HBF 4NH 2 3. tCO 2 HEtO 2 CCH 2 N 2FCO 2 CH 3FCH 3 CO 2 EtNaI 2 (0,5 M)EtO -OFEtO 2 CEtO 2 CCO 2 EtFCO 2 EtEtO 2 CCO 2 EtFOOEtO - 2 MFOOCO 2 EtFH 3 O +tHO 2 CCO 2 HFN 2 H 4 (1 M)HO 2 CCO 2 HFFOOPrMgBr 1. CO 2Et CO 2 H2. H 3 O +Br 2BrFP (0,3 M) Et COBr1. EtOH2. EtO -NNCO 2 Et
<strong>13.</strong>51.Ca*CO 3HCl*CO 2C 2 H 5 Br1. Mg (эфир)CH 3 CH * 1. SOCl 22 COOHCH 3 *CO 2 H2. *CO 22. CH 2 N 23. H 3 O + 3. Ag1. EtOH, H +2. LiAlH 43. SOCl 21. Mg (эфир)2. *CO 23. H 3 O +CH 3 ICH 3 *CH 2 CO 2 H*CO 2 + H 2 *CH 3 OH NaIH +1. Mg (эфир)2. *CO 23. H 3 O +CH 3 *CH 2 Cl1. Mg (эфир)*CH 3 I *CH 3 CO 2 H2. CO 23. H 3 O +1. EtOH, H +2. LiAlH 43. SOCl 2*CH 3 CH 2 ClEtBr<strong>13.</strong>55. Схема синтеза:1. EtONa2. EtBrNaBrH 2 SO 4COCl 2CO(OEt) 2PhPh1. Mg (эфир)*CH 3 CH 2 CO 2 H2. CO 23. H 3 O +EtOH [O] CH 3 CO 2 H SOCl 2OPhOEtONaCO 2 EtPhO1. EtONa2. EtBrCO 2 EtCO 2 EtPhPhC 6 H 6CH 3 COClAlCl 3OI 2 (0,5 M)EtONaCO 2 EtCO 2 EtPhPhPhOOOCO 2 EtCO 2 EtOO
«Кислотное расщепление»:OPhPhOO 2 CCO 2 EtCO 2 EtCO 2- OHH 2 OPhPhOCO 2CO 2OO 2 CCO 2- OHH 2 OHOPhPhOOCO 2CO 2- PhCO 2 H- PhCO 2 HOPh OH«Кетонное расщепление»:OOHOOPhCO 2 EtH 3 O + PhOPh CO 2 Et Ph CO 2 Ht- CO 2PhPhtO - CO 2OOOHOOOPh Ph<strong>13.</strong>62. Способ 1:2CO 2 EtCO 2 Et1. EtONa (2 M)Br2.BrEtO 2 CCO 2 EtCO 2 EtCO 2 Et1. EtONa (2 M)2. CH 3 I (2 M)EtO 2 CCO 2 EtCO 2 EtCO 2 EtH 3 O +tCO 2 HCO 2 H
2Способ 2:OCO 2 Et1. EtONa (2 M)Br2.BrOCO 2 EtOCO 2 Et1. EtONa (2 M)2. CH 3 I (2 M)OCO 2 HOCO 2 EtСпособ 3:CO 2 EtHO -tCO 2 HH 2Pd/BaSO 4NBSRO . Br MgCO 2 HHBr (2 M)BrBrKCNCNCNH 3 O +t<strong>13.</strong>66.а)OCO 2 HOOPhб, в)CO1. OEt -2. PhCH 2 ClNO 2+CO 2-CO 2-EtBr (2 M)CCO 2-CO 2-OAPh1. OEt -2. CH 3 ONO 2BOONO 2PhOCO 2 EtCH 3 CO 2 EtEtO - CO 2 Et H 3O +tCO 2 EtOH -t
OHNO 2EtOHONOH H 3O + OOH 2OOOOOOHOHOНингидринПоложение равновесия смещено в сторону гидратной формывследствие акцепторного влияния двух карбонильных групп. Именнопоэтому присоединение воды происходит по средней карбонильнойгруппе.<strong>13.</strong>69. а)CH 3COClCH 3O 2Co 2+KOHtCO 2 - K +CO 2 HCO 2 HCHO1. SOCl 22. H 2 /Pd/BaSO 41. HO -2. H 3 O +CHOOH1. H 3 O +2. SOCl 2OHCOClCO 2 - K +OCOClCd(CH 3 ) 2OPhCO 3 HOOOOCOClO
<strong>13.</strong>77. а)CaC 2H 2 O C2 H 2CtC 6 H 5 BrBr 2Fe1. Mg (эфир)2. CO 23. H 3 OPhCO 2 H 1. SOCl 22. H 2 O 2PhCO 3 HO1. H 2 SO 4, SO 3, tC 6 H 6C 6 H 5 OH 1. H 2/Ni2. NaOH, t2. H 2 Cr 2 O 73. H 3 O +O Si(CH 3) 3O(CH 3 ) 3 SiClNaH1. CH 3 I2. H 2 O(CH 3 ) 3 SiClNaHSi(CH 3 ) 31. CH 3 I2. H 2 OOOPhCO 3 HOз)EtOH1. H 2 /Pd/BaSO 42. H 3 O +OCaC 2H 2 O C2 H 2CtCH 3 Cl1. H 2 SO 4, SO 3, tC 6 H 6C 6 H 5 OH 1. H 2/Ni2. NaOH, t2. H 2 Cr 2 O 73. H 3 O +HO 2 CAlCl 3H +t1. Br 2 (1 M), hν2. KCN3. H 3 O + , t1. EtOH, H +2. LiAlH 43. PBr 3BrC 2 H 4Br 2BrBrKCNCNCNLiAlH 4 (изб.) NH 2NH 2H +t NH
ONHH +NO1.Br2. H 3 O +1. NH 2 OH2. H +HNNHO<strong>13.</strong>78. а)PhCO 2 EtPhH 1. Br 2/FePhCO 2 H 1. SOCl 2PhCH 2 CO 2 H2. Mg (эфир)2. CH 2 N 23. CO 23. Ag +4. H 3 O +PhHPhCO 2 EtEtO -EtOH H +EtO 2 CCH 3COClAlCl 3 PhOPhOPhOCH 2 O(CH 3 ) 2 NH + Cl - PhEtOHH +NPhCH 2 CO 2 Et1. CH 3 I2. HO - , tPhPhPhOEtO 2 COEtO -PhPhOPhPhCO 2 EtOOH 3 O +tOPhPh
д)OH1. HNO 3 (разб.), t2. EtOH, H +3. EtONaOCO 2 Et1. Br 22. H 3 O + , t3. пиридин, tO1. H 2 SO 4, SO 3, t2. HO - , t3. H 2 /Ni-Re, t, pC 6 H 5CH 2 OHClZnCl 2PhCH 2 ClLiAlH 4PhCH 3CH 2 OHClZnCl 2Cl+ орто-изомерCH 3 CO 2 H 1. Br 2/P2. NaCN3. EtOH, H +4. H 3 O + (разб.)CO 2 EtCO 2 Et1. EtONa2.ClCO 2 EtCO 2 EtOEtONaOEtO 2 CCO 2 EtCH 3 1. H 3 O + , t2. CH 3 NO 2 /HO -3. EtOH, H +EtO 2 Cе)H 3 CEtOH1. H 2 /Pd/BaSO 42. H 3 O +CaC 2H 2 O C2 H 2CtCHNO 2PhCHO CH 3NO 2HO -CO, HClAlCl 3 , CuPhNO 21. H 2 SO 4 , SO 3 , tC 6 H 6 C 6 H 5 OH 1. H 2/Ni2. NaOH, t2. HNO 33. H 3 O + 3. EtOH, H +CO 2 EtCO 2 Et
EtO -OCO 2 EtPhEtO -NO 2OPh NO 21. H 2 /PdCO 2 Et2. NaBH 4PhEtO 2 CHONH 2