Auto-Antikörper-Messungen: Bei welchen klinischen Symptomen?
Auto-Antikörper-Messungen: Bei welchen klinischen Symptomen?
Auto-Antikörper-Messungen: Bei welchen klinischen Symptomen?
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
PRAXIS Mini-Review Praxis 2010; 99 (23): 1429–1434 1429<br />
Universitätsklinik für Rheumatologie, Klinische Immunologie & Allergologie,<br />
Inselspital Bern<br />
M. Seitz<br />
<strong>Auto</strong>-<strong>Antikörper</strong>-<strong>Messungen</strong>:<br />
<strong>Bei</strong> <strong>welchen</strong> <strong>klinischen</strong><br />
<strong>Symptomen</strong>?<br />
Which Clinical Symptoms Suggest Distinct <strong>Auto</strong>antibody Measurements?<br />
Zusammenfassung<br />
Die Messung von <strong>Auto</strong>antikörpern<br />
stellt einen wesentlichen Eckpfeiler der<br />
Diagnostik systemischer <strong>Auto</strong>immunerkrankungen<br />
wie den autoimmunen<br />
Konnektivitiven (= Kollagenosen) und<br />
den systemischen Kleingefässvaskulitiden<br />
dar. Geeignete Screening-Untersuchungen<br />
sind der Nachweis der<br />
antinukleären <strong>Antikörper</strong> (ANA) bei<br />
den Konnektivitiden sowie der antineutrophilen<br />
zytoplasmatischen <strong>Antikörper</strong><br />
(p+c-ANCA) bei den Kleingefässvaskulitiden.<br />
Eine erweiterte<br />
<strong>Auto</strong>antikörperdiagnostik sollte aus<br />
gesundheitsökonomischen wie auch<br />
aus intellektuell/didaktischen Gründen<br />
ausschliesslich zielgerichtet erfolgen<br />
auf der Basis von Anamnese und<br />
klinischem Untersuchungsbefund und<br />
auf daraus abzuleitenden diagnostischen<br />
Verdachtsmomenten.<br />
Schlüsselwörter: <strong>Auto</strong>antikörper –<br />
Arthritis, rheumatoide – Konnektivitiden,<br />
autoimmune – Vaskulitiden<br />
Anamnestische und klinische<br />
Verdachtsmomente<br />
<strong>Bei</strong>m Vorliegen von B-<strong>Symptomen</strong> (Fieber,<br />
Nachtschweiss, Gewichtsabnahme,<br />
Malaise) und bei gleichzeitigem Vorhandensein<br />
von rheumatologischen<br />
<strong>Symptomen</strong> im engeren Sinne wie polymyalgischen<br />
Beschwerden, Polyarthralgien<br />
oder Arthritiden liegt der differentialdiagnostische<br />
Verdacht auf eine<br />
rheumatologische Systemerkrankung<br />
(Konnektivitis, Vaskulitis) nahe. In<br />
diesem Falle lohnt es sich neben dem<br />
Infekt- und Tumorausschluss ein labormässiges<br />
«<strong>Auto</strong>immun-Screening» mit<br />
der Bestimmung von ANA und ANCA<br />
durchzuführen.<br />
<strong>Auto</strong>antikörper bei autoimmunen<br />
Konnektivitiden<br />
(Kollagenosen)<br />
Das Vorliegen einer autoimmunen<br />
Konnektivitis wird umso wahrscheinlicher,<br />
je mehr der folgenden spezifischeren<br />
zusätzlichen Krankheitssymptome<br />
vorliegen:<br />
Raynaud-Symptomatik<br />
Sicca-Symptomatik<br />
Keratokonjunktivitis<br />
Entzündliche Arthralgien (Ruheschmerz<br />
und Morgensteifigkeit),<br />
Arthritiden (Gelenkschwellung, Ruheschmerz,<br />
Morgensteifigkeit)<br />
Hautexanthem nach Sonnenexposition<br />
(bei SLE, entzündlichen Myopathien)<br />
Haarausfall<br />
Hautulzerationen, Enanthem<br />
Rasch progrediente proximale Muskelschwäche<br />
(Dermato- oder Polymyositis)<br />
Skleroderme Hautveränderungen, Sklerodaktylie<br />
und Teleangiektasien (diffuse<br />
oder limitierte Systemsklerose)<br />
Trockener unproduktiver Reizhusten,<br />
Dyspnoe, Sklerosiphonie (interstitielle<br />
Lungenerkrankung)<br />
Dysphagie, verkürztes und verdicktes<br />
Zungenbändchen, Tabaksbeutelmund/<br />
Mikrostomie, Refluxbeschwerden, Flatulenz,<br />
Diarrhöe (Systemsklerose)<br />
Thoraxschmerzen, thorakales Druckgefühl<br />
(Pleuritis, Perikarditis)<br />
Arterielle Hypertonie, Proteinurie,<br />
Ödeme, Mikrohämaturie (Glomerulonephritis)<br />
Neurologische Defizite, Wesensveränderungen<br />
(ZNS-Befall)<br />
Rezidivierende Thromboembolien,<br />
Spontanaborte (Antiphosphoplipid-<br />
Syndrom)<br />
Im Artikel verwendete Abkürzungen:<br />
ANA antinukleäre <strong>Antikörper</strong><br />
ANCA antineutrophile zytoplasmatische<br />
<strong>Antikörper</strong><br />
anti-ccP <strong>Antikörper</strong> gegen zyklisches<br />
citrulliniertes Peptid<br />
aPTT partielle Thromboplastinzeit<br />
MCTD mixed connective tissue disease<br />
MPO Myeloperoxidase<br />
PR3 Proteinase 3<br />
RA rheumatoide Arthritis<br />
RF Rheumafaktoren<br />
SLE systemischer Lupus erythematodes<br />
SRP signal recognition particle<br />
© 2010 by Verlag Hans Huber, Hogrefe AG, Bern DOI 10.1024/1661-8157/a000311
PRAXIS Mini-Review Praxis 2010; 99 (23): 1429–1434 1430<br />
<strong>Bei</strong> persistierenden symmetrischen Gelenkschwellungen<br />
während mehr als<br />
sechs Wochen muss die differentialdiagnostische<br />
Möglichkeit einer beginnenden<br />
rheumatoiden Arthritis (RA)<br />
erwogen werden und neben der allgemeinen<br />
Entzündungsdiagnostik, dem<br />
Gelenkultraschall und dem Gelenkröntgen<br />
eine <strong>Auto</strong>antikörper-Diagnostik mit<br />
Bestimmung der Rheumafaktoren (RF;<br />
routinemässig IgM-Subtyp ausreichend),<br />
der <strong>Antikörper</strong> gegen zyklisches citrulliniertes<br />
Peptid (anti-ccP) und der ANA<br />
erfolgen. Mit der kombinierten Bestimmung<br />
von RF und anti-ccP-<strong>Antikörper</strong>n<br />
kann heute mit einer hohen Sensitivität<br />
(ca. 75%) und Spezifität (ca. 96%) die<br />
Diagnose einer RA untermauert werden.<br />
In über 60% der Fälle von initial RFnegativer<br />
RA können anti-ccP <strong>Antikörper</strong><br />
nachgewiesen werden. Neben ihrem<br />
Nutzen in der Frühdiagnostik der RA hat<br />
der positive Nachweis von anti-ccP-<br />
<strong>Antikörper</strong>n auch eine prognostische<br />
Bedeutung im Hinblick auf eine zu erwartende<br />
erosive Erkrankung und eine<br />
daraus abzuleitende aggressive initiale<br />
Behandlung.<br />
Tab. 1: <strong>Auto</strong>antikörper beim SLE.<br />
<strong>Auto</strong>antikörper Sensitivität (%) Spezifität (%) Kommentare<br />
ANA 100 Screening<br />
ds-DNS 70 95 niedrige Affinität<br />
Crithitien 40 100 hohe Affinität<br />
SS-A 25–35 87–94 kongenitaler AV-Block<br />
Sm 30 95<br />
anti-C1q<br />
100% NPV für renalen Befall<br />
Histon 30–80 50<br />
U1-RNP 60 50 hochtitrig bei MCTD<br />
Histon 95 85 medikamentös induzierter Lupus<br />
NPV = negative predictive value; MCTD = mixed connective tissue disease<br />
An eine autoimmune Konnektivitis<br />
(Kollagenose) im engeren Sinne, z.B. an<br />
einen systemischen Lupus erythematodes<br />
(SLE), muss man denken, wenn<br />
ein(e) Patient(in) sich mit B-<strong>Symptomen</strong>,<br />
entzündlichen Arhralgien, einem<br />
typischen Schmetterlingserythem im<br />
Gesicht (oft nach Sonnenexposition),<br />
einer Sicca-Symptomatik von Augen<br />
(Xerophthalmie, Keratokonjuktivitis),<br />
Mund (Xerostomie) und mit weiteren<br />
organspezifischen <strong>Symptomen</strong> präsentiert<br />
(z.B. Pleuritis/Perikarditis, Ödeme,<br />
arterielle Hypertonie, neurologische und/<br />
oder psychische Auffälligkeiten, thromboembolische<br />
Ereignisse und rezidivierende<br />
Spontanaborte). In diesem Falle<br />
ist zusätzlich zur Bestimmung der ANA<br />
eine erweiterte <strong>Auto</strong>antikörper-Diagnostik<br />
gerechtfertigt mit der Bestimmung<br />
von: anti-ds-DNS-<strong>Antikörper</strong>n<br />
mittels ELISA (niedrigaffine, pathogenetisch<br />
weniger bedeutende <strong>Auto</strong>antikörper)<br />
und Crithitien-Assay (hochaffine,<br />
pathogenetisch relevante <strong>Auto</strong>antikörper),<br />
<strong>Antikörper</strong> gegen Sm, SS-A (anti-<br />
Rho), SS-B (anti-La), anti-C1q (100%<br />
negativer prädiktiver Wert für Nierenbefall;<br />
Titerhöhe korreliert mit Aktivität<br />
der Nephritis) sowie die Komplementfaktoren<br />
C3, C4 bzw. die gesamthämolytische<br />
C-Aktivität (CH50). Anti-Histon-<br />
<strong>Antikörper</strong> sind falls in hohen Titern<br />
auftretend eher beim medikamentös<br />
induzierten SLE anzutreffen, können<br />
niedrigtitrig aber auch bei der idiopathischen<br />
Form der Erkrankung gefunden<br />
werden. Aus prognostischen und therapeutischen<br />
Gründen ist es sehr wichtig,<br />
bei thromboembolischen Ereignissen,<br />
unklarer Thrombopenie, bei rezidivierenden<br />
Aborten und bei klinischer<br />
Livedo der Haut an eine sekundäres Antiphospholipid-<strong>Antikörper</strong>syndrom<br />
zu<br />
denken. In diesem Falle ist die Bestimmung<br />
der folgenden <strong>Antikörper</strong> vor<br />
einer oralen Antikoagulation oder präventiven<br />
Heparinisierung sinnvoll: Anti-<br />
Cardiolipin-<strong>Antikörper</strong>, <strong>Antikörper</strong> gegen<br />
2 Glycoprotein I sowie als Suchtest<br />
für das Lupus-Antikoagulans die Bestimmung<br />
der partiellen Thromboplastinzeit<br />
(aPTT). Die Sensitivität und Spezifität<br />
der einzelnen <strong>Auto</strong>antikörper bei<br />
SLE sind in einer Übersicht in Tabelle 1<br />
dargestellt.<br />
Eine dem SLE verwandte Konnektivitis<br />
ist die Mischkonnektivitis (MCTD =<br />
mixed connective tissue disease), welche<br />
serologisch zusätzlich neben hochtitrigen<br />
ANA auch durch hohe Titer von<br />
<strong>Auto</strong>antikörpern gegen U1RNP charakterisiert<br />
ist. Differenzierungsmerkmale<br />
gegenüber einem SLE sind der fehlende<br />
Nierenbefall, diffuse Hand-und Fingerödeme<br />
sowie häufiger als beim SLE eine<br />
Begleitmyositis mit Muskelschwäche<br />
und auch das Vorhandensein von Halsschmerzen,<br />
Heiserkeit und Dysphagie<br />
(vor allem im Entzündungsschub).<br />
An ein primäres Sjögren-Syndrom muss<br />
man denken, wenn eine ausgeprägte<br />
Sicca-Symptomatik von Augen und<br />
Mund und allenfalls auch des oberen<br />
Respirationstrakts besteht (durch pathologischen<br />
Schirmer-Test und Saxon-Test<br />
zu objektivieren) und gleichzeitig eine<br />
rezidivierende Schwellung von Ohrund/oder<br />
Mundspeicheldrüsen vorliegt.<br />
Die Diagnose wird durch den histologischen<br />
Nachweis einer autoimmunen<br />
Sialadenitis gestellt (z.B. mittels Lippenschleimhaut-Biopsie),<br />
kann aber auch<br />
zusätzlich durch die typische <strong>Auto</strong>antikörper-Konstellation<br />
mit Nachweis von<br />
<strong>Antikörper</strong>n gegen SS-A und SS-B wie<br />
sie in Tabelle 2 dargestellt ist, untermauert<br />
werden.<br />
Präsentiert sich ein Patient mehr mit diffusen<br />
Ödemen, einer lokalisierten oder<br />
diffusen Hautinduration, mit einer<br />
progressiven Sklerodaktylie und Finger-
PRAXIS Mini-Review Praxis 2010; 99 (23): 1429–1434 1431<br />
beugekontrakturen, einer Raynaud-<br />
Symptomatik mit oder ohne akrale<br />
Ulzerationen an Fingern oder Zehen,<br />
einer fibrosierenden Tendovaginitis oder<br />
weist Zeichen einer viszeralen Organbeteiligung<br />
auf (GIT: Dysphagie, Reflux,<br />
Flatulenz, Obstipation/Ileussymptomatik,<br />
Diarrhöe, Analinkontinenz; Lunge:<br />
unproduktiver trockener Reizhusten,<br />
zunehmende Dyspnoe bei Belastung;<br />
Niere: Hypertonie, Ödeme, rasches Nierenversagen),<br />
dann liegt mit allergrösster<br />
Wahrscheinlichkeit eine Systemsklerose<br />
vor. Aus prognostischen Gründen und<br />
wegen des unterschiedlichen Organbefallmusters<br />
ist die Unterscheidung von<br />
limitierter und diffuser Systemsklerose<br />
wichtig. Neben der Klinik helfen hierbei<br />
auch bestimmte <strong>Auto</strong>antikörper. So<br />
ist die limitierte Form der Erkrankung<br />
charakterisiert durch das Vorhandensein<br />
von anti-Centromeren-<strong>Antikörper</strong>n mit<br />
einer hohen Spezifität, aber einer nur<br />
maximal 30%igen Sensitivität und einer<br />
Assoziation mit pulmonal-arterieller<br />
Hypertonie, Teleangiektasien und einer<br />
Calcinosis cutis. <strong>Bei</strong> ca. 20% der Patienten<br />
mit einer diffusen Systemsklerose<br />
lassen sich <strong>Auto</strong>antikörper gegen Scl-70<br />
(Topoisomerase 1) nachweisen, die<br />
prädiktiv sind für die Entwicklung einer<br />
interstitiellen Pneumopathie und als<br />
protektiv gelten gegen die Entwicklung<br />
einer isolierten pulmonal-arteriellen<br />
Hypertonie. <strong>Bei</strong> der diffusen Form können<br />
auch in 20% der Fälle <strong>Antikörper</strong><br />
gegen die RNA-Polymerase III nachgewiesen<br />
werden, die wiederum in 25% der<br />
Fälle mit einer renalen Krise einhergehen<br />
können und deswegen bereits prophylaktisch<br />
mit einem ACE-Hemmer behandelt<br />
werden sollten. Diese Untergruppe<br />
weist zusätzlich einen starken<br />
Hautbefall auf, entwickelt aber nur sehr<br />
selten eine interstitielle Pneumopathie.<br />
Tabelle 3 zeigt die systemsklerose-assoziierten<br />
<strong>Auto</strong>antikörper im Überblick.<br />
<strong>Bei</strong> Verdacht auf eine autoimmune<br />
Myositis, d.h. eine Dermatomyositis<br />
oder Polymyositis (rasch progrediente<br />
proximal betonte Muskelschwäche von<br />
Tab. 2: <strong>Auto</strong>antikörper beim primären Sjögren-Syndrom.<br />
<strong>Auto</strong>antikörper Sensitivität (%) Spezifität (%) Kommentare<br />
ANA 100 Screening<br />
SS-A (Ro) 70 87<br />
SS-B (La) 60 94<br />
RF 30<br />
Thyreoglobulin, 80–100 Hashimoto Hypothyreose<br />
Mikrosomen<br />
Tab. 3: <strong>Auto</strong>antikörper bei Systemsklerose.<br />
<strong>Auto</strong>antikörper Sensitivität (%) Spezifität (%) Kommentare<br />
ANA 60–80 Screening<br />
Centromeren 25–30 100 Limit. Form, PAH<br />
Scl70 15–20 100 Diffuse Form, ISLD<br />
RNA Polymerase III 20 Renaler Befall/Krise, starker<br />
Hautbefall<br />
PAH = pulmonal arterielle Hypertonie; ISLD = interstitial lung disease<br />
Armen und <strong>Bei</strong>nen, Dysphagie, typisches<br />
Exanthem mit Heliotropismus,<br />
periorbitales Ödem mit livider Verfärbung,<br />
Gottron-Papeln, schmerzhaftes<br />
Nagelhäutchen, trockener Reizhusten,<br />
Dyspnoe, Raynaud- und Sicca-Symptomatik)<br />
kann in der Minderheit der Fälle<br />
eine prognostische Subgruppen-Zuordnung<br />
mittels <strong>Auto</strong>antikörpern erfolgen.<br />
Anti-Jo1-<strong>Antikörper</strong> sind bei dieser<br />
Krankheitsgruppe die häufigsten <strong>Auto</strong>antikörper,<br />
die gegen die Histidyl-tRNA-<br />
Synthetase gerichtet sind und assoziiert<br />
auftreten mit dem anti-Synthetase-<br />
Syndrom (30% bei Polymyositis, 5% bei<br />
Dermatomyositis, 15% bei Overlap-<br />
Syndromen mit einer 70%igen 5-Jahres-<br />
Überlebensrate). Dieses Syndrom umfasst<br />
als klinische Einzelsymptome<br />
interstitielle Pneumopathie, Raynaud,<br />
Arthritis, Fieber und «mechanic hands».<br />
Die myositische Komponente ist häufig<br />
nur zu Krankheitsbeginn klinisch evident<br />
und tritt im weiteren Krankheitsverlauf<br />
gegenüber der interstitiellen<br />
Pneumopathie meistens in den Hintergrund.<br />
Anti-M2-<strong>Auto</strong>antikörper sind<br />
gegen nukleäre Helicase gerichtet und<br />
treten ausschliesslich auf in Assoziation<br />
mit einer klassischen Dermatomyositis<br />
mit akuter Erythrodermie, Schal- oder<br />
V-Zeichen (5 Jahres-Überleben bei<br />
100%). <strong>Bei</strong> weniger als 5% der Polymyositis-Patienten<br />
findet man <strong>Auto</strong>antikörper<br />
gegen SRP (signal recognition<br />
particle). Diese Patienten leiden an einer<br />
schweren rasch progredienten Myopathie<br />
mit myokardialer Beteiligung und<br />
sind ausgesprochen therapieresistent.<br />
Die Prognose ist mit einem 5-Jahresüberleben<br />
von 25% ausgesprochen<br />
schlecht.<br />
In Tabelle 4 sind <strong>Auto</strong>antikörper aufgelistet,<br />
welche zur Differenzierung der<br />
autoimmunen Lebererkrankung beitragen.<br />
Diese <strong>Auto</strong>antikörper lohnt es<br />
sich zu bestimmen, wenn anamnestische<br />
und klinische Verdachtsmomente bestehen<br />
wie die folgenden: uncharakteristische<br />
Müdigkeit, Leistungsintoleranz<br />
gepaart mit Abdominalbeschwerden,<br />
Juckreiz, Übelkeit, Hyperpigmentation<br />
der Haut, polymylagische Beschwerden<br />
und/oder Polyarthralgien, Hepatosplenomegalie,<br />
Teleangiektasien, Spider<br />
naevi oder Aszites. Im Rahmen eines<br />
Overlap-Syndromes kann eine autoimmune<br />
Lebererkrankung jederzeit auch<br />
mit einer anderen definierten <strong>Auto</strong>im-
PRAXIS Mini-Review Praxis 2010; 99 (23): 1429–1434 1432<br />
munerkrankung assoziiert auftreten (z.B.<br />
primäres Sjögren-Syndrom, SLE etc.)<br />
Mit Ausnahme der <strong>Antikörper</strong> gegen<br />
ds-DNS und C1q (renaler Befall bei SLE)<br />
sind alle aufgeführten <strong>Auto</strong>antikörper<br />
rein diagnostisch, d.h. eine wiederholte<br />
Bestimmung ist i. d. R. sinnlos und unökonomisch,<br />
da für die Beurteilung des<br />
Krankheitsverlaufes irrelevant.<br />
<strong>Auto</strong>antikörper bei systemischen<br />
Kleingefässvaskulitiden<br />
Eine systemische Kleingefässvaskulitis ist<br />
dann evident, wenn die folgenden organspezifischen<br />
Krankheitssymptome<br />
zusätzlich zu B-<strong>Symptomen</strong> vorhanden<br />
sind:<br />
Episkleritis, Skleritis, Keratitis, Uveitis,<br />
Vitritis, Retinitis<br />
Chronische antibiotikaresistente Otitis<br />
media, Mastoiditis, purulente und/<br />
oder hämaorrhagische Rhinitis und<br />
Sinusitis, Hörverlust, Schwindel<br />
Hämoptysen, Dyspnoe<br />
Palpable Hautpurpura (nicht wegdrückbar<br />
mit dem Glasspatel), Hautulzera<br />
an atypischer Stelle und nach<br />
banalen Traumen auftretenden,<br />
schlecht heilend<br />
Ödeme, arterieller Hypertonus, Proteinurie,<br />
Mikrohämaturie, rasch progrediente<br />
Niereninsuffizienz (Glomerulonephritis)<br />
Progressive senso-motorische Ausfälle<br />
(Mononeuritis multiplex, sensomotorische<br />
Polyneuropathie)<br />
Perimyokarditis<br />
Tab. 4: <strong>Auto</strong>antikörper bei autoimmunen Lebererkrankungen.<br />
<strong>Auto</strong>antikörper Sensitivität (%) Spezifität (%) Kommentare<br />
ANA 30–50% <strong>Auto</strong>immunhepatitis I<br />
SMA, Actin, SLA/LP<br />
ANA 20 <strong>Auto</strong>immunhepatitis II<br />
LKM<br />
ANA<br />
AMA, SMA,<br />
atypische p-ANCA<br />
Primär bil. Zirrhose/<br />
autoimmune Cholangiopathie<br />
SMA = smooth muscle cell antibody; SLA = soluble liver antigen; LP = liver pancreas; LKM = liverkidney<br />
microsomal antibody; AMA = Anti-mitochondriale <strong>Antikörper</strong>; ANCA = Antineutrophilen<br />
cytoplasmatische <strong>Antikörper</strong><br />
Tab. 5: ANCA-assoziierte Kleingefässvaskulitiden.<br />
Wegener MPA CSS<br />
Sensi- Spezi- PPV Sensi- Spezi- PPV Sensi- Spezi- PPV<br />
tivität fität tivität fität tivität fität<br />
c-ANCA 81.3 99.5 93.7 2.5 92.8 0.3 6.5 92.8 0.9<br />
p-ANCA 3.6 94.0 4.8 65.0 94.2 8.9 6.5 92.8 0.9<br />
+MPO-ANCA 1.8 99.3 17.5 47.5 99.5 47.5 4.3 99.2 5.0<br />
MPA = mikroskopische Polyangiitis; CSS = Churg-Strauss; PPV = positive predictive value; MPO =<br />
Myeloperoxidase; ANCA = Antineutrophilen cytoplasmatische <strong>Antikörper</strong>; c = cytoplasmatisch;<br />
p = perinukleär<br />
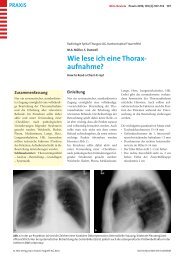
Abb. 1: Indirekter Immunfluoreszenznachweis von c-ANCA (links) und p-ANCA (rechts).<br />
Mit der Entwicklung des serologischen<br />
Nachweises von p- (perinukleären) und<br />
c- (cytoplasmatischen) Neutrophilen-<br />
<strong>Antikörper</strong>n (p + c-ANCAs) wurden<br />
ganz wesentliche Fortschritte in der<br />
Diagnostik der Kleingefässvaskulitiden<br />
bei Morbus Wegener, mikroskopischer<br />
Polyangiitis und bei dem Churg-Strauss-<br />
Syndrom erzielt.<br />
<strong>Bei</strong>de <strong>Antikörper</strong> werden mit mässiger<br />
bis hoher Sensitivität (67–81%) durch<br />
den indirekten Immunfluoreszenz-Test<br />
(IIF) nachgewiesen. Eine hohe diagnostische<br />
Spezifität von 94–99% weisen die<br />
ELISA-Testmethoden auf, die als spezifisches<br />
Zielantigen der c-ANCA die<br />
zytoplasmatische lokalisierte Proteinase<br />
3 (PR3) detektieren und als Zielantigen<br />
der p-ANCA die perinukleär lokalisierte<br />
Myeloperoxidase (MPO). Im <strong>klinischen</strong><br />
Alltag werden in der Regel bei den obengenannten<br />
<strong>Symptomen</strong> einer Kleingefässvaskulitis<br />
beide <strong>Antikörper</strong> mittels<br />
IIF (Abb. 1) und ELISA gleichzeitig bestimmt.<br />
Die p-ANCA sind diagnostisch<br />
für die mikroskopische Polyangiitis<br />
(Leitsymptome von alveolärer Hämorrhagie<br />
und Glomerulonephritis) und die<br />
c-ANCA für den Morbus Wegener, vor
PRAXIS Mini-Review Praxis 2010; 99 (23): 1429–1434 1433<br />
allem in der generalisierten Form. Die<br />
rein lokoregionären Formen der Erkrankung<br />
können in bis zu 50% der<br />
Fälle ANCA-negativ verlaufen. <strong>Bei</strong>m<br />
Churg-Strauss-Sydrom können p- und<br />
c-ANCA in einem geringen Prozentsatz<br />
ebenfalls vorkommen. Eine ganze Reihe<br />
nicht MPO-spezifischer p-ANCA kann<br />
bei chronischen Darmerkrankungen<br />
oder bei der rheumatoiden Arthritis<br />
vorkommen, welche aber bei diesen<br />
Erkrankungen weder diagnostische<br />
noch prognostische Bedeutung haben.<br />
Die verschiedenen Sensitivitäten und<br />
Spezifitäten der ANCA sind auf Tabelle 5<br />
im Überblick dargestellt.<br />
Eine Persistenz oder ein Anstieg der AN-<br />
CA-Titer im Krankheitsverlauf weist auf<br />
ein erhöhtes Rezidivrisiko hin, kann aber<br />
auf Einzelpatientenebene nicht immer<br />
gleichgesetzt werden mit einem unmittelbar<br />
drohenden Rezidiv der Erkrankung.<br />
Anders verhält es sich allerdings,<br />
wenn nach eingetretener Seronegativierung<br />
unter Therapie ein erneuter AN-<br />
CA-Anstieg zu beobachten ist. In diesem<br />
Fall sind engmaschigere klinische Kontrollen<br />
erforderlich, um ein Rezidiv<br />
frühzeitig zu erfassen und die Immunosuppression<br />
anzupassen. Somit sind<br />
periodische Bestimmungen der ANCA<br />
zur Beurteilung des Krankheitsverlaufes<br />
grundsätzlich sinnvoll.<br />
Wenn irgend möglich, sollte die Diagnose<br />
einer Kleingefässvaskulitis jedoch<br />
immer histologisch untermauert werden<br />
und nicht alleine auf der Klinik und der<br />
ANCA-Positivität basieren.<br />
Key messages<br />
● Die gleichzeitige Bestimmung von Rheumafaktoren und anti-ccP-<strong>Antikörper</strong>n<br />
weist die höchste Sensitivität und Spezifität in der Frühdiagnostik der<br />
rheumatoiden Arthritis auf.<br />
● In der <strong>Auto</strong>antikörper-Diagnostik des systemischen Lupus erythematodes<br />
ist die Bestimmung der ANA sowie der spezifischen <strong>Auto</strong>antikörper gegen<br />
ds-DNS, Crithidien, C1q und die Bestimmung der Komplementfaktoren C3<br />
und C4 am wichtigsten.<br />
● Die limitierte und die diffuse Form der Systemsklerose lassen sich serologisch<br />
durch den Nachweis von <strong>Auto</strong>antikörpern gegen Centromeren bzw. gegen<br />
Scl70 (Topoisomerase I) unterscheiden.<br />
● c- und p-ANCA sind geeignet als diagnostische «screening marker» beim<br />
<strong>klinischen</strong> Verdacht auf eine Kleingefässvaskulitis.<br />
Lernfragen<br />
1. Welche Aussage zu den folgenden <strong>Auto</strong>antikörpern ist FALSCH?<br />
a) C-ANCA sind beim M. Wegener immer positiv.<br />
b) Das spezifische Zielantigen der c-ANCA ist die lysosomale Proteinase 3.<br />
c) MPO-spezifische p-ANCA sind diagnostisch für die mikroskopische<br />
Polyangitis.<br />
d) Unspezifische p-ANCA sind diagnostisch irrelevant.<br />
e) Die wiederholte Bestimmung der c-ANCA ist sinnvoll, da die <strong>Auto</strong>antikörperspiegel<br />
mit der Krankheitsaktivität korrelieren können.<br />
2. Welcher der folgenden <strong>Auto</strong>antikörper ist geeignet für die Beurteilung der<br />
Krankheitsaktivität?<br />
a) Anti-Scl70<br />
b) Anti-SS-A<br />
c) Anti-C1q<br />
d) Anti-Cardiolipin<br />
e) Anti-Histon<br />
3. Welche Assoziation spezifischer <strong>Auto</strong>antikörper mit bestimmten Krankheitsmanifestationen<br />
trifft NICHT zu?<br />
a) Anti-Scl70 und interstitielle Pneumopathie<br />
b) Anti-C1q und Nephritis<br />
c) Anti-Centromeren und pulmonal arterielle Hypertonie<br />
d) Anti-RNA Polymerase III und renale Krise<br />
e) Anti-SS-A und pulmonal arterielle Hypertonie<br />
Abstract<br />
The detection of autoantibodies is an<br />
important cornerstone in the diagnosis<br />
of systemic autoimmune disorders<br />
such as autoimmune connectivitides<br />
and small vessel vasculitides. Antinuclear<br />
antibodies (ANAs ) and antineutrophil<br />
cytoplasmic antibodies (c+<br />
p-ANCAs) are appropriate diagnostic<br />
screening tools for autoimmune connectivites<br />
and small vessel vasculitides.<br />
For economic and intellectual/didactic<br />
reasons more extensive autoantibody<br />
diagnostics should be performed only<br />
in particular situations when patients<br />
history and clinical exam lead to<br />
strong diagnostic suspicion.<br />
Key words: autoantibodies – rheumatoid<br />
arthritis – connectivitides – vasculitides
PRAXIS Mini-Review Praxis 2010; 99 (23): 1429–1434 1434<br />
Résumé<br />
La recherche d’auto-anticorps est une<br />
étape centrale dans le diagnostic de<br />
maladies systémiques auto-immunes<br />
comme les collagénoses auto-immunes<br />
et les vasculites des petits vaisseaux.<br />
Les anticorps anti-nucléaires (ANA) et<br />
les anticorps antineutrophiles cytoplasmatiques<br />
(c + p ANCA) sont des<br />
tests de dépistage et de diagnostic pour<br />
des collagénoses auto-immunes et les<br />
vasculites des petits vaisseaux. Pour<br />
des raisons économiques et intellectuelles/didactiques,<br />
d’autres auto-anticorps<br />
ne devraient être recherchés<br />
pour l’obtention d’un diagnostic que<br />
dans des situations particulières, où<br />
l’anamnèse et l’examen clinique des<br />
patients permettent de soupçonner<br />
fortement un certain diagnostic.<br />
Mots-clés: auto-anticorps – arthrite<br />
rhumatoide – connectivitides autoimmune<br />
– vasculitides<br />
Bibliographie<br />
1. Nielen MMJ, et al. Specific autoantibodies precede the symptoms of rheumatoid arthritis:<br />
A study of serial measurements in blood donors. Artthritis Rheum 2004;50:380.<br />
2. Avouac J, et al. Diagnostic and predictive value of anti-cyclic citrullinated protein antibodies in<br />
rheumatoid arthritis: a systematic literature review. Ann Rheum Dis 2006;65:84.<br />
3. Meyer OC, et al. Anti-C1q antibodies antedate patent active glomerulonephritis in patients<br />
with systemic lupus erythematosus. Arthritis Res Ther 2009;11:R8.<br />
4. Harley JB. <strong>Auto</strong>antibodies are central to the diagnosis and clinical manifestations of lupus.<br />
J Rheumatol 1994;21:118.<br />
5. Schönermarck U, et al. Prevalence and spectrum of rheumatic diseases associated with<br />
proteinase 3 – antineutrophil antibodies (ANCA) and myeloperoxidase-ANCA. Rheumatology<br />
2001;40:178.<br />
Korrespondenzadresse<br />
Prof. Dr. med. Michael Seitz<br />
Chefarzt-Stv.<br />
Universitätsklinik für Rheumatologie,<br />
Klinische Immunologie & Allergologie<br />
Inselspital<br />
3010 Bern<br />
michael.seitz@insel.ch<br />
Antworten zu den Lernfragen<br />
1. Aussage a) ist falsch.<br />
2. Antwort c) ist richtig.<br />
3. Aussage e) trifft nicht zu.