EPIDEMIERS DYNAMIK
EPIDEMIERS DYNAMIK
EPIDEMIERS DYNAMIK
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
<strong>EPIDEMIERS</strong> <strong>DYNAMIK</strong><br />
AF<br />
Kasper Larsen, Bjarke Vilster Hansen<br />
Henriette Elgaard Nissen, Louise Legaard og<br />
Charlotte Pletscher-Frankild<br />
1. Miniprojekt<br />
Sidefagssupplering, RUC<br />
December 2007
INDLEDNING<br />
Matematisk modellering kan anvendes til at forsimple virkeligheden, derefter regne på den<br />
forsimplede virkelighed, og til sidst ud fra disse beregninger konkludere noget om virkeligheden på<br />
den forsimplede matematiske baggrund. Det betyder, at der skal foretages en del begrænsninger og<br />
antagelser, når virkeligheden omsættes til den matematiske model.<br />
I denne opgave anvendes matematisk modellering til at kunne forudsige noget om epidemier og<br />
deres udvikling og betingelserne for, at en epidemi i det hele taget vil opstå. Epidemier er<br />
karakteriseret ved, at de starter med at vokse eksponentielt med større eller mindre hastighed, hvor<br />
antallet af smitteramte vokser med en fordoblingstid. Efter en tid når epidemien et maksimum,<br />
hvorefter epidemien dør ud igen.<br />
Det er et meget vigtigt at vide noget om epidemier, da det er et område, der har krævet og kræver<br />
mange menneskeliv på verdens plan. Man kan bare tænke på et historisk eksempel som ”Den Sorte<br />
Død” i det 14. århundrede. Et nutidigt og meget bekymrende eksempel kan være AIDS-epidemien,<br />
som hærger i store dele af specielt Afrika og Asien. Det er dermed tydeligt, at epidemier kan have<br />
vidtrækkende samfundsmæssig betydning, og på den baggrund er det af vital betydning at kunne<br />
forudsige noget om epidemiers opståen og udvikling, og det kan en matematisk modellering af<br />
systemet give os et bud på.<br />
PROBLEMFORMULERING<br />
I dette projekt ses der på en matematisk model for udviklingen af epidemier udviklet af Kermack-<br />
Mckendrick i 1927, den såkaldte SIR-model.<br />
Der ses på spørgsmålene:<br />
• Hvordan kan en model for udviklingen af en epidemi se ud?<br />
• Hvilke parametre styrer dynamikken i en epidemi?<br />
Formålet med dette projekt er at gennemgå en matematisk model for en generel epidemi og dens<br />
udvikling og derefter at analysere modellen ved flere eksempler. Til sidst foretages der en udvikling<br />
til en lidt anden type model.<br />
2
Den overordnede gennemgang af modellen opdeles i følgende punkter<br />
- SIR-modellen og dens parametre gennemgås<br />
- Modellens differentialligninger gennemarbejdes<br />
- Modellens begrænsninger gennemgås<br />
- Modellens antagelser belyses<br />
- Modellen analyseres ved hjælp af eksempler og fortolkning af disse<br />
SIR-MODELLEN<br />
SIR-modellen er en simpel, klassisk model, der har udbredelsen af epidemier som overordnet<br />
genstandsområde. Vi vil karakterisere SIR-modellen som en forklarende/deterministisk epidemisk<br />
model, der behandler epidemier af typen, hvor smitten overføres i et møde mellem et smittende og<br />
et modtageligt individ, og hvor der efter en periode udvikles resistens. Gennem anvendelse af<br />
sandsynlighedsteori har man opstillet en model, som beskriver deterministiske sammenhænge og<br />
altså ”i princippet afgiver deterministiske kausalitetsudsagn og deterministiske prædiktioner”<br />
Det samlede antal individer inddeles i tre grupper (kompartments) til brug for den videre model:<br />
S: Individer, der er modtagelige for sygdommen (Susceptibles)<br />
I: Individer, der er smittede og smittende (Infected)<br />
R: Individer, der er immune (eller døde) (Removals)<br />
Det samlede antal individer, N, som indgår i undersøgelsen (dvs. en hel befolkning eller blot en<br />
risikogruppe, som udgør en afgrænset del af befolkningen), udgøres af de tre grupper, hvilket giver<br />
følgende:<br />
N= S+I+R<br />
Modellen bygger på, at der sker en bevægelse af individer fra S-gruppen henover I-gruppen til R-<br />
gruppen. Dette forklares med, at der i kontakten mellem en inficeret (I) og en modtagelig (S) kan<br />
ske overførsel af smitte, hvorved et individ overgår fra S-gruppen til I-gruppen. Tilsvarende vil der<br />
fra I-gruppen ske en bevægelse af individer til R gruppen pga. udvikling af immunitet eller død.<br />
Modellen kan beskrives som en kompartmentmodel med følgende udsende:<br />
3
Vi skal nu på en eller anden måde modellere bevægelsen fra S til I og fra I til R. Bevægelsen fra S<br />
til I afhænger af både S og I, idet det virker logisk, at antallet af nyligt inficerede bestemmes af,<br />
hvor mange der kan smittes, og hvor mange der er smittet (i hvert fald hvis smitten sker fra person<br />
til person). Et møde, som foregår mellem en smittet person og en modtagelig person, og som fører<br />
til, at den modtagelige person bliver smittet, kalder vi et effektivt møde. Antallet af effektive møder<br />
en person fortager pr. tidsenhed kalder vi kontaktraten c. Kontaktraten afhænger derfor af mange<br />
adfærdsmæssige og biologiske faktorer. I denne rapport tager definitionen af c sit udgangspunkt i, at<br />
alle medlemmer af befolkningsgruppen har lige chancer for at møde alle andre medlemmer af<br />
befolkningsgruppen. En modtagelig person foretager i tidsrummet Δt·c kontakter. Hvis N er det<br />
samlede befolkningstal, vil brøkdelen I / N være kontakter med smittede personer. I / N betegner<br />
sandsynligheden for på et givent tidspunkt, at en tilfældig person er smittende. Da der er S personer,<br />
som kan udføre en given kontakt, er sammenhænget mellem flowet af personer fra I til S:<br />
c<br />
N<br />
⋅ I ⋅ S ⋅ Δt<br />
c<br />
hvor betegner infektionsraten. Infektionsraten er et udtryk for, hvor smitsom en sygdom er. Des<br />
N<br />
c c ⋅ ∆t<br />
mere smitsom en sygdom er, jo større bliver . Det vil sige, at<br />
N<br />
N<br />
4<br />
udtrykker sandsynligheden<br />
for, at et inficerende individ inficerer et modtageligt individ inden for et givent tidsrum Δt.<br />
I stedet for infektionsraten kan man i stedet, formulere sig ved brug af infektionsstyrken også kaldet<br />
c<br />
smitteraten. Smitteraten er givet ved udtrykket Λ = ⋅ I<br />
N<br />
er den rate, hvormed modtagelige individer bliver smittet, og er altså den komponent, der styrer<br />
flowet fra S til I.<br />
S I R<br />
Bevægelsen fra I til R, altså hvor mange af de smittede der bliver resistente eller dør, afhænger kun<br />
af, hvor mange der er syge, og ikke hvor mange der allerede er resistente (eller døde). Bevægelsen<br />
fra I til R kan beskrives som, at en bestemt andel (procentdel) af de smittede bliver raske i løbet af
en tidsenhed. Andelen af smittede der bliver raske i løbet af en tidsenhed, kaldes removalrate og<br />
betegnes med symbolet ν. Dermed kan vi beskrive overgangsstrømmen fra I til R som værende lig<br />
I·ν.<br />
Den samlede SIR model kommer skematisk til at se således ud:<br />
og modellens ligninger, der beskriver S, I og R til det efterfølgende tidsskridt som værende<br />
funktioner af det nuværende tidsskridt og ændringen i de givne grupper i løbet af tidsskridtet ∆t:<br />
S(<br />
t + Δt)<br />
I ( t + Δt)<br />
R(<br />
t + Δt)<br />
Med lidt omskrivninger er differensligningerne:<br />
=<br />
=<br />
=<br />
S(<br />
t + Δt)<br />
− S(<br />
t)<br />
Δt<br />
I(<br />
t + Δt)<br />
− I(<br />
t)<br />
Δt<br />
R(<br />
t + Δt)<br />
− R(<br />
t)<br />
Δt<br />
c ⋅ S(<br />
t)<br />
⋅ I ( t)<br />
S(<br />
t)<br />
−<br />
⋅ Δt<br />
N<br />
c ⋅ S(<br />
t)<br />
⋅ I ( t)<br />
I ( t)<br />
+<br />
⋅ Δt<br />
− I(<br />
t)<br />
⋅ν<br />
⋅ Δt<br />
N<br />
R(<br />
t)<br />
+ I(<br />
t)<br />
⋅ν<br />
⋅ Δt<br />
=<br />
=<br />
=<br />
5<br />
c ⋅ S(<br />
t)<br />
⋅ I(<br />
t)<br />
−<br />
N<br />
c ⋅ S(<br />
t)<br />
⋅ I(<br />
t)<br />
− I(<br />
t)<br />
⋅ν<br />
N<br />
I(<br />
t)<br />
⋅ν<br />
Lader vi nu tidsskridtet gå mod nul, altså Δt → 0 , får vi differentialkvotienterne til S, I og R og<br />
dermed følgende diffentialligningssystem:<br />
S´(<br />
t)<br />
I´(<br />
t)<br />
R'(<br />
t)<br />
=<br />
=<br />
=<br />
c ⋅ S(<br />
t)<br />
⋅ I(<br />
t)<br />
−<br />
N<br />
c ⋅ S(<br />
t)<br />
⋅ I(<br />
t)<br />
− I(<br />
t)<br />
⋅ν<br />
N<br />
I ( t)<br />
⋅ν<br />
Vi har kun brug for to af dem, idet vi ved at summen af de tre grupper altid er N, altså N = S(t) + I(t)<br />
+ R(t) og dermed at S´(t) + I´(t) + R´(t) = N´ = 0.<br />
c<br />
⋅ I ⋅ S<br />
ν<br />
⋅ I<br />
N<br />
S I R
MODELLENS ANTAGELSER<br />
Før vi ser nærmere på selve modellen, vil vi se lidt på de antagelser, der er gjort i forbindelse med<br />
SIR-modellen. Opbygningen af SIR-modellen giver ikke mulighed for igen at miste sin resistens<br />
(hvilket sker for nogle sygdomme, der f.eks. skyldes bakterieinfektioner), man kan altså ikke vende<br />
tilbage til S-gruppen.<br />
De resterende antagelser omhandler typisk bevægelser mellem grupperne S, I og R, som ikke alle<br />
har været eksplicit formulerede. I forbindelse med nogle af antagelserne, vil der desuden blive givet<br />
eksempler på hvor disse antagelser er eller kan være problematiske.<br />
A. Grupperne er homogent blandede.<br />
Det er klart, at sandsynligheden for kontakt mellem to individer fra forskellige grupper afhænger af<br />
fordelingen af gruppernes individer. Hvis koncentrationen af S-individer er stor, vil et enkelt I-<br />
individ have større ”chance” for at møde et S-individ, end hvis koncentrationen er lille. Er<br />
grupperne derimod homogent fordelt, og individerne møder hinanden tilfældigt (og altså har lige<br />
stor chance for at mødes), da vil infektionsraten være ensartet. Er der tale om sygdomme, der oftest<br />
rammer bestemte befolkningsgrupper, kan denne antagelse være problematisk Et eksempel kunne<br />
være, at visse kønssygdomme er overrepræsenteret blandt bøsser.<br />
B. Infektionsrate og removalrate er konstante med hensyn til tiden.<br />
Afhængigt af sygdomstypen kan smittefarligheden ændres med tiden. Hvis sygdommen f.eks. som<br />
udgangspunkt er forårsaget af en bakterie, kan bakterien med tiden blive mere aggressiv som følge<br />
af tilpasning til de nye livsbetingelser (et eksempel er malariamyggens udvikling af resistens mod<br />
bestemte insekticider). Dette vil betyde, at den relative removalraten øges, og begyndelsesværdien<br />
for antal modtagelige, S(0), tilsvarende falder. Det er naturligvis af altafgørende betydning, at man<br />
kender til muligheden for ændringer i disse kritiske parametre.<br />
C. De smittede individer bliver straks smittende.<br />
I virkeligheden er der en latenstid, hvor de smittede individer går over til også at blive smittende, og<br />
afhængig af denne latenstid størrelse, kan antagelsen resultere i en overvurdering af, hvor<br />
fremskredet sygdommen vil være til et givet tidspunkt. Det vil dog kun have begrænset betydning,<br />
6
idet der så vil gå tilsvarende længere tid, før et I-individ flyttes til R-gruppen og ikke længere udgør<br />
en risiko. Dermed vil effekten i ”S-enden” udlignes af effekten i ”R-enden”.<br />
D. Sygdommen smitter direkte fra person til person.<br />
Denne antagelse kan diskuteres, idet modellen ikke definerer elementerne i S, I og R-grupperne. I<br />
princippet kunne der således være smittefarlige dyr blandet ind i grupperne af mennesker, men i<br />
realiteten vil det være umuligt med tilstrækkelig stor nøjagtighed at sætte give et skøn på antallet af<br />
individer i de enkelte grupper. Antagelsen betyder, at modellen ikke tager højde for smitte, der<br />
spredes fra dyr til mennesker, hvilket ofte vil være tilfældet (f.eks. Fugleinfluenza, hvor smittevejen<br />
oprindeligt kun var gennem fugle, senere andre dyr, der er herunder nu også sjældne eksempler på<br />
smitte gennem mennesker).<br />
E. Alle personer er lige modtagelige for sygdommen.<br />
Risikoen for smitte afhænger naturligvis bl.a. af immunforsvaret og af den menneskelige adfærd.<br />
Man kan derfor ikke regne med en fast infektionsrate helt uafhængigt af det enkelte møde mellem et<br />
smittende og et modtagende individ. Man kan dog bruge en gennemsnitlig infektionsrate for<br />
beregningerne af sygdomsudviklingen i den samlede befolkning, og det er i realiteten også sådan<br />
modellen anvendes.<br />
F. Antallet af modtagelige er konstant.<br />
Ser vi på epidemiologiske undersøgelser og beregninger, der strækker sig over generationer, kan<br />
antallet af individer i risikogruppen ændre sig, hvilket vil have betydning for det endelige billede af<br />
sygdomsudviklingen. F.eks. er fødselsraten faldet markant bl.a. i de vestlige lande og i Japan, men<br />
dette modsvares delvist af en forøget levetid. Befolkningen vil i lande, hvor det samlede antal<br />
individer reduceres (og det er jo faktisk det, vi ser mange steder i Europa) være mindre sårbar for<br />
smitte end modellen antager. Dette faktum skal man naturligvis tage højde for, når man laver<br />
fremtidsprognoser.<br />
7
MODELLENS OPFØRSEL<br />
Hvordan ændrer de forskellige gruppers størrelse sig med tiden, og hvilken betydning har de<br />
forskellige indgående parametre (c, ν) og begyndelsesbetingelserne S(0), I(0), R(0). For at få en ide<br />
hertil vil vi se på en række eksempler.<br />
Vi vil betragte en række tilfælde, hvor vi ved at ændre på nogle af parametrene vil se, om og i så<br />
fald hvordan epidemier – ifølge modellen – vil udvikle sig. I de første seks eksempler, vil vi lade<br />
c c<br />
infektionsraten og removalraten v være konstante, og vi sætter = 0,0003 og v = 0,55. Vi vil i<br />
N<br />
N<br />
alle eksemplerne lade R(0) = 0, altså at der ikke er nogle resistente til at begynde med. I det første<br />
eksempel vil vi lade S(0) = 3500, I(0) = 50. Dette første eksempel vil vi betragte som vores<br />
”standardeksempel”, dvs. i forhold til hvilket vi vil sammenligne ved justeringen af de to parametre<br />
S(0) og I(0).<br />
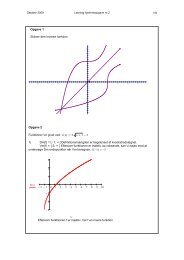
SIR modellen, eksempel 1<br />
På Figur 1 kan forløbet af S(t), I(t) og R(t) følges, når S(0) = 3500 og I(0) = 50. Hvis vi skal se på<br />
det som et ”virkeligt” eksempel, er der til starttidspunktet tale om en population bestående af 3550<br />
individer, hvoraf de 50 er inficerede. Det ses, at antallet af inficerede individer hurtigt stiger fra de<br />
50 til et antal på ca. 500 ved t = 7,5. Derefter falder antallet af individer, der er modtagelige overfor<br />
sygdommen kraftigt, idet antallet af individer, der er resistente eller døde, er steget. Antallet af<br />
inficerede individer falder herefter igen og går mod nul, hvilket betyder, at epidemien udryddes.<br />
Hvis vi udelukkende betragter R(t) som antallet af døde individer, vil altså en stor del af<br />
befolkningen blive udryddet (ca. 2825 individer), mens antallet af modtagelige S(t) vil være<br />
aftagende og stabilisere sig på ca. 725 individer.<br />
8
Figur 1: Illustration af eksempel 1. De tre gruppers (S(t), I(t) og R(t)) størrelse afbilledet som funktion af tiden.<br />
S(0) = 3500, I(0) = 50, R(0) = 0, N = 3550, c/N = 0,0003 og ν = 0,55.<br />
SIR modellen, eksempel 2<br />
I dette eksempel lader vi populationen være 3600 individer, hvoraf 100 er smittede/smittende og<br />
ingen er resistente. Dvs. vi har N = 3600, I(0) = 100, R(0) = 0, og altså S(0) = 3500. Infektionsraten,<br />
c/N, er stadig 0,0003, mens removalraten, ν, er fastholdt på 0,55. Parametrene S(t), I(t) og R(t) vil<br />
nu udvikle sig som vist på Figur 2.<br />
9
Figur 2: Illustration af eksempel 2. De tre gruppers (S(t), I(t) og R(t)) størrelse afbilledet som funktion af tiden.<br />
S(0) = 3500, I(0) = 100, R(0) = 0, N = 3600, c/N = 0,0003 og ν = 0,55.<br />
På figuren ser vi at S(t) er aftagende gennem hele intervallet og stabiliserer sig ved ca. 750<br />
individer, mens R(t) er stigende i hele intervallet og stabiliserer sig ved ca. 2850 individer.<br />
Udviklingen af inficerede (I(t)) stiger fra t = 0 til t ≈ 6,5, så modellen viser, at der er en epidemi.<br />
Efter t ≈ 6,5 hvor antallet af inficerede individer var nået op på knapt 600, er I(t) aftagende i resten<br />
af intervallet og nærmer sig langsomt 0.<br />
10
SIR modellen, eksempel 3<br />
Vi lader nu antallet af modtagelige individer til tiden 0 være det dobbelte af antallet i det første<br />
eksempel, dvs. S(0) = 7000. I(0) sættes igen til 50. Nu er altså en betydelig mindre andel af<br />
befolkningen inficerede til tiden 0. Forløbet af grafen viser imidlertid et noget mere drastisk forløb<br />
end i de to foregående eksempler. Udviklingen af inficerede stiger endnu hurtigere end før og når et<br />
maksimum på ca. 2750, hvorefter den falder igen. Antallet af resistente stiger tilsvarende kraftigt,<br />
og vil med tiden udgøre langt hovedparten af den samlede befolkning, og tilsvarende af<br />
modtagelige S(t) falde og stabilisere sig på ca. 200 individer. Der er altså i dette tilfælde tale om<br />
nærmest en total populationsudryddelse (hvis vi altså betragter R(t) som antallet af døde). Når S(0)<br />
er meget stor i forhold til den relative removalrate, og I(0) udgør en mindre del af den samlede<br />
population fås altså en ret drastisk udvikling af epidemien.<br />
Figur 3: Illustration af eksempel 3. De tre gruppers (S(t), I(t) og R(t)) størrelse afbilledet som funktion af tiden.<br />
S(0) = 7000, I(0) = 50, R(0) = 0, N = 7050, c/N = 0,0003 og ν = 0,55.<br />
SIR modellen, eksempel 4<br />
Lad igen S(0) = 7000 men lad I(0) = 100. De resterende parametre er som i eksempel 1. Figuren<br />
vises nogenlunde det samme som eksempel 3. Det ses altså igen, at det ikke har store betydning, om<br />
en lidt større del af befolkningen er smittet fra starten.<br />
11
Figur 4: Illustration af eksempel 4. De tre gruppers (S(t), I(t) og R(t)) størrelse afbilledet som funktion af tiden.<br />
S(0) = 7000, I(0) = 100, R(0) = 0, N = 7100, c/N = 0,0003 og ν = 0,55.<br />
SIR modellen, eksempel 5<br />
I forhold til det første eksempel, vil vi nu halvere antallet af modtagelige individer, så S(0) = 1750.<br />
I(0) = 50. Det ses at I(t) er svagt aftagende i hele forløbet, så der er altså ikke tale om en epidemi.<br />
R(t) er stigende, mens S(t) er aftagende, men i dette tilfælde krydser de ikke hinanden. Det vil sige<br />
at antallet af modtagelige forbliver betydeligt større (ca.1450 individer) end antallet af resistente<br />
eller døde (ca.350 individer).<br />
12
Figur 5: Illustration af eksempel 5. De tre gruppers (S(t), I(t) og R(t)) størrelse afbilledet som funktion af tiden.<br />
S(0) = 1750, I(0) = 50, R(0) = 0, N = 1800, c/N = 0,0003 og ν = 0,55.<br />
SIR modellen, eksempel 6<br />
Vi betragter nu tilfældet S(0) = 1750, I(0) = 100, R(0) = 0 og altså N = 1850. Removalraten, ν,<br />
sættes vi til 0,55, mens vi har bestemt os for en infektionsraten, c/N, sættes til 0,0003. Altså er den<br />
eneste forskel til eksempel 2 at S(0) er blevet halveret. Parametrene S(t), I(t) og R(t) vil nu udvikle<br />
sig som vist på Figur 6.<br />
13
Figur 6: Illustration af eksempel 6. De tre gruppers (S(t), I(t) og R(t)) størrelse afbilledet som funktion af tiden.<br />
S(0) = 1750, I(0) = 100, R(0) = 0, N = 1850, c/N = 0,0003 og ν = 0,55.<br />
S(t) er som i eksempel 2 aftagende gennem hele intervallet, mens R(t) er stigende gennem hele<br />
intervallet. Antallet af modtagelige individer S(t) stabiliserer sig med tiden ved ca. 1300, mens<br />
antallet af resistente/døde med tiden stabiliserer sig ved ca. 550 individer.<br />
I dette tilfælde ser vi, at antallet af smittede/smittende, I(t), falder gennem hele intervallet. Der er<br />
altså i dette tilfælde ikke tale om en epidemi. I(t) går dog som i de tidligere eksempler mod 0 med<br />
tiden.<br />
c<br />
I de sidste to eksempler vil vi se hvad der sker, når vi justerer på værdierne for infektionsraten<br />
N<br />
og removalraten v.<br />
SIR modellen, eksempel 7<br />
c<br />
Lad som i det første eksempel S(0) = 3500 og I(0) = 50. Vi sætter nu infektionsraten til = 0 og<br />
N<br />
removalraten til v=1. Figuren viser nu – hvilket også gerne skulle være tilfældet – at antallet af<br />
modtagelige ikke ændrer sig (forbliver på 3500 individer), og at de inficerede hurtigt bliver<br />
14
esistente. Når infektionsraten er 0, kan der naturligvis ikke ske nogen bevægelse fra gruppen af<br />
modtagelige over i gruppen af inficerede.<br />
Figur 7: Illustration af eksempel 7. De tre gruppers (S(t), I(t) og R(t)) størrelse afbilledet som funktion af tiden.<br />
S(0) = 3500, I(0) = 50, R(0) = 0, N = 3550, c/N = 0 og ν = 1.<br />
SIR modellen, eksempel 8<br />
c<br />
Vi sætter S(0) = 3500 og I(0) = 50. Infektionsraten sættes nu til = 1og<br />
removalraten til v = 0. Da<br />
N<br />
v = 0 vil der selvfølgelig ikke ske nogen bevægelse fra gruppen af inficerede over i gruppen af<br />
resistente. Grafen viser derfor også, at antallet af resistente forbliver konstant på 0. Samtidig ser vi,<br />
at alle fra gruppen af modtagelige individer på meget kort tid blive inficeret. Dvs. S(t) falder hurtigt<br />
og stabiliserer sig på 0, mens I(t) tilsvarende stiger og stabiliseres på 3550.<br />
15
Figur 8: Illustration af eksempel 8. De tre gruppers (S(t), I(t) og R(t)) størrelse afbilledet som funktion af tiden.<br />
S(0) = 3500, I(0) = 50, R(0) = 0, N = 3550, c/N = 1 og ν = 0.<br />
I de ovennævnte eksempler, har vi forsøgt at illustrere, hvorledes parametrene S(t), I(t) og R(t)<br />
påvirker hinanden. Vi bemærkede, at når c/N, ν, I(0) og R(0) blev holdt konstant, udviklede de tre<br />
parametre S(t), I(t) og R(t) sig meget forskelligt afhængigt af størrelsen af S(0).<br />
Som vi har kunnet se ud fra eksemplerne, tyder det på, at S(t) er en aftagende funktion, mens R(t) er<br />
en voksende funktion.<br />
Dette kan forklares ud fra differentialligningerne, hvorom der gælder, at når I(t), S(t), c/N og ν er<br />
positive:<br />
S'<br />
( t)<br />
R'(<br />
t)<br />
=<br />
=<br />
c<br />
− ⋅ S(<br />
t)<br />
⋅ I(<br />
t)<br />
N<br />
ν ⋅ I(<br />
t)<br />
16<br />
⇒<br />
⇒<br />
S'<br />
( t)<br />
< 0<br />
R'(<br />
t)<br />
> 0<br />
Men at det forholder sig således, er dog ikke specielt underligt, idet modellen er konstrueret, så der<br />
kun kan flyttes individer ud af S-gruppen, mens der kun kan flyttes individer ind i R-gruppen.<br />
Hvilken værdi, de to funktioner konvergerer mod, er lidt sværere at bestemme. Vi (eller man) har<br />
ikke kunnet løse differentialligningssystemet, men har kun kunnet finde sammenhængene:
ν<br />
ν<br />
S(<br />
t)<br />
+ I(<br />
t)<br />
− ln( S(<br />
t))<br />
= S(<br />
0)<br />
+ I ( 0)<br />
− ln( S(<br />
0))<br />
c N<br />
c N<br />
⎛ c N<br />
⎞<br />
S(<br />
t)<br />
= S(<br />
0)<br />
⋅ exp⎜−<br />
( R(<br />
t)<br />
− R(<br />
0))<br />
⎟ > 0<br />
⎝ ν<br />
⎠<br />
Opskrivningen af I(t) er, som vi kan se af ovenstående eksempler, noget kompliceret, men man kan<br />
med sikkerhed sige, at I(t) med tiden vil gå med nul, idet alle inficerede vil blive resistente med<br />
tiden (forudsat at ν > 0).<br />
I vores ovenstående eksempler er der tale om en epidemi, hvis S(0) = 3500 eller 7000, men ikke<br />
hvis S(0) = 1750. I tilfældene, hvor der ikke er tale om epidemier, er I(t) en aftagende funktion i<br />
hele intervallet, mens I(t) har et maksimum hvis der er tale om en epidemi. Vi er heldigvis i stand til<br />
at afgøre om givne betingelser vil føre til en epidemi, hvilket vi vil se på i det følgende.<br />
Betingelser for opståen af en epidemi<br />
En væsentlig begrundelse for at udvikle modeller er netop at skabe viden, der i sin optimale<br />
anvendelse hindrer udviklingen af en epidemi. At vi således kan handle i tide, hvis vi ser, at<br />
betingelserne for udviklingen af en epidemi er til stede. Modellen skal, om man så må sige, bibringe<br />
os en indsigtsfuld handleparathed.<br />
Hvis vi skal udtale os om de i virkeligheden ret komplicerede processer, som er involveret i<br />
sygdomsspredning, må vi i første omgang se nærmere på differentialligningerne:<br />
⎛ S(<br />
t)<br />
⋅ c ⎞<br />
Det følger af ligningen for tilvæksten i individantallet i gruppen I, at I ( t)<br />
⋅ ⎜ −ν<br />
⎟ > 0 hvis<br />
⎝ N ⎠<br />
⎛ S(<br />
t)<br />
⋅ c ⎞<br />
⋅ N<br />
sygdommen er i udvikling. Det vil sige ⎜ −ν<br />
⎟ > 0 og altså S t ><br />
⎝ N ⎠<br />
c<br />
ν ν ⋅ N<br />
( ) , hvor<br />
c<br />
udtryk for den relative removalrate, som er forholdet mellem removalrate og infektionsraten. Disse<br />
resultater giver os nemt den vigtige tærskelsætning:<br />
Tærskelsætningen: Der opstår en epidemi, hvis begyndelsesværdien for antal modtagelige, S(0),<br />
overstiger den relative removalrate.<br />
S<br />
0<br />
ν<br />
⋅ N<br />
><br />
c<br />
⇔<br />
17<br />
S0<br />
⋅ c<br />
T = > 1<br />
ν ⋅ N<br />
er et
hvor T er den såkaldte reproduktionsrate.<br />
Denne vigtige parameter udtrykker, hvor mange individer, den inficerende når at smitte, inden<br />
vedkommende selv bliver resistent og således ikke længere er smittefarlig, under antagelse af at alle<br />
i befolkningen er modtagelige.<br />
Hvis man kender sygdommens infektionsrate og removalrate, giver modellen altså et direkte<br />
anvendeligt udtryk for, om en given befolknings gruppe vil udvikle en epidemi, med mindre der<br />
sættes relevante tiltag i værk. (Med relevante tiltag menes handlinger, der har til hensigt at<br />
begrænse smittespredning, dvs. isolation af inficerende individer, sygdomsbehandling, styrkelse af<br />
immunforsvaret hos risikogrupper o. lign).<br />
Af udtrykket ses det også, at jo større en befolkning er, desto mere sårbar er den for epidemier. Det<br />
kan forklares med, at smittespredningen er større i en stor befolkning end i en lille, fordi<br />
sandsynligheden for kontakt mellem et inficerende og et modtageligt individ øges med<br />
befolkningstallet.<br />
Det giver altså mening, at isolere grupper af befolkningen og dermed undgå eller begrænse<br />
kontakten mellem individerne. Dette kan naturligvis være yderst problematisk i områder af verden,<br />
hvor de sociale og sanitære forhold er katastrofale, og hvor mennesker og dyr lever mellem<br />
hinanden uden tag over hovedet.<br />
Udtrykket viser desuden, at hvis man reducerer infektionsraten og/eller øger removalrate (der i<br />
modellen antages at være konstante), så mindskes risikoen for at en given befolkning overskrider<br />
tærsklen for epidemiens udvikling.<br />
Tærskelværdien er et begreb, der både indeholder information om sygdommens spredningsevne,<br />
men også om befolkningens sygdomshistorie. En forenkling af tærskelsætningen, hvor man antager<br />
at hele befolkningen er modtagelige ved epidemiens start, altså at S(0) = N, R(0) = 0 og I(0) 1.<br />
Det er et udtryk, der kun indeholder oplysninger om<br />
ν<br />
kontaktraten og removalraten.<br />
Epidemiens forløb<br />
Som sagt, er I(t) en noget kompliceret funktion, der opfører sig forskelligt under forskellige<br />
betingelser, dog altid til slut gående mod 0. Dette afsnit prøver vi yderligere at beskrive I(t). Nogle<br />
gange er I(t) en aftagende funktion i hele tidsintervallet, men det er hvis der ikke opstår en epidemi,<br />
18
altså hvis S(0) er mindre end tærskelfrekvensen. Det betyder at I(t) er en aftagende funktion hvis<br />
Hvis derimod<br />
ν<br />
S(<br />
0)<br />
< .<br />
c N<br />
ν<br />
S(<br />
0)<br />
> , altså S(0) er større end tærskelfrekvensen vil der opstå en epidemi. I(t)<br />
c N<br />
vil i dette tilfælde stige til en maksimumværdi, hvorefter den vil være aftagende. Denne<br />
maksimumværdi for I(t) vil indtræde til det tidspunkt t, hvor<br />
en epidemi ikke længere er til stede.<br />
19<br />
ν<br />
S(<br />
t)<br />
= , dvs. når betingelserne for<br />
c N<br />
Formen på I(t), specielt nær endepunkterne, kan i tilfælde af en epidemi yderligere beskrives på<br />
følgende måde. Vi må forvente, at S(t) er en konstant for t < 0. Da vi også ved, at c/N og ν er<br />
konstante, kan vi altså i ligningen<br />
⎛ S(<br />
t)<br />
⋅ c ⎞<br />
I´(<br />
t)<br />
= I(<br />
t)<br />
⋅⎜<br />
−ν<br />
⎟<br />
⎝ N ⎠<br />
⎛ S ( t)<br />
⋅ c ⎞<br />
betragte ⎜ −ν<br />
⎟ som en konstant k1. Dermed har vi altså, at I ′ ( t)<br />
= k1<br />
⋅ I(<br />
t)<br />
. Denne simple<br />
⎝ N ⎠<br />
differentialligning har som bekendt løsningen<br />
eksponentielt i starten af en epidemi.<br />
I ( t)<br />
⋅<br />
Omvendt vil det i slutningen af en epidemi gælde, at<br />
k1t<br />
= c1<br />
e . Det vil sige, at I(t) vil stige<br />
ν<br />
S(<br />
t)<br />
< og S(t) går mod en konstant. I<br />
c N<br />
⎛ S(<br />
t)<br />
⋅ c ⎞<br />
dette tilfælde vil vi få en ny konstant: k2<br />
= ⎜ −ν<br />
⎟ . Denne konstant vil være negativ, idet<br />
⎝ N ⎠<br />
c ν<br />
k 2 < ⋅ −ν<br />
= 0 og vi vil derfor få en eksponentielt aftagende funktion I ( t)<br />
⋅<br />
N c N<br />
k2t<br />
= c2<br />
e . Dette vil<br />
altså betyde, at antallet af inficerede og inficerende individer vil aftage eksponentielt i slutningen af<br />
en epidemi.<br />
Vaccination<br />
De antagelser, der blev gjort under gennemgangen af SIR-modellen gælder stadig her. Vi vil<br />
undersøge, hvordan epidemimodellen ser ud, når vi antager, at en vis procentdel af individerne er
vaccineret mod sygdommen, som det er tilfældet for børnesygdomme som for eksempel mæslinger,<br />
fåresyge og røde hunde (MFR-vaccinen).<br />
Vi antager at en brøkdel, p, af individerne vaccineres før sygdommen bryder ud. SIR-modellen kan<br />
anvendes med de samme antagelser som i det foregående, men med nye begyndelsesbetingelser.<br />
Således er begyndelsesværdien af antal modtagelige individer S(t0) = (1-p)S0. Antal inficerede og<br />
inficerende individer er ved sygdommens start stadig I(t0) = I0. Antallet af immune individer er R(t0)<br />
= R0 + pS0 ved starten af den mulige epidemi. Bemærk at det totale antal individer stadig er N, idet<br />
S(t0) + I(t0) + R(t0) = (1-p)S0 + I0 + R0 + pS0 = N.<br />
Tærskelværdien, der som nævnt, udtrykker hvor mange individer, der smittes af den inficerende,<br />
inden vedkommende bliver resistent, er med de nye begyndelsesværdier givet ved:<br />
c ⋅ ( 1−<br />
p)<br />
⋅ S0<br />
T =<br />
.<br />
ν ⋅ N<br />
Denne værdi er dermed reduceret med en faktor ( 1−<br />
p)<br />
i forhold til tærskelværdien for SIR-<br />
modellen uden vaccination. Da de inficerede individer, dermed smitter færre individer, før de bliver<br />
resistente, er vaccination, som forventet, et godt tiltag mod udviklingen af en epidemi.<br />
Med hensyn til den omstridte MFR-vaccine, er vurderingen fra Statens Serum Institut da også, at<br />
vaccinen har virket positivt på folkesundheden. Siden 2003 er der ikke konstateret nogen tilfælde af<br />
mæslinger, og siden samme år er der heller ikke registreret nogen tilfælde af røde hunde blandt<br />
gravide og nyfødte.<br />
KONKLUSION<br />
I opgaven har vi betragtet SIR-modellen og opstillet en række eksempler til at illustrere<br />
sammenhængen mellem de indgående parametre. Der er gjort en række antagelser for at kunne opnå<br />
en relativt simpel matematisk model til beskrivelse af en epidemis udvikling. En række af disse<br />
antagelser vil naturligvis ikke være opfyldt i de fleste virkeligt forekommende populationer, og<br />
modellen er dermed at betragte som en forsimpling af virkeligheden. Det at opstille modeller for<br />
fænomener, hvor komplicerede forhold som f.eks. menneskers adfærd spiller ind, må vi betragte<br />
som yderst vanskeligt. En adækvat matematisk beskrivelse af epidemiers udvikling vil nok aldrig<br />
20
helt kunne lade sig gøre. Ikke desto mindre mener vi, at modellen giver en udmærket forståelse af<br />
hvilke faktorer, der spiller ind i forhold til udviklingen af en epidemi.<br />
Vi har altså fundet, at S(t) er en aftagende funktion, der med tiden stabiliseres, og med tiden går<br />
mod en konstant værdi k.<br />
R(t) er omvendt en tiltagende funktion, der med tiden stabiliseres og med tiden går mod en anden<br />
funktion givet ved N-k.<br />
I(t), der beskriver forløbet af smittende/smittede, vil med tiden gå mod 0. Hvis S(0) er mindre end<br />
eller lig den relative removalrate, vil I(t) være aftagende i hele intervallet, og der opstår ingen<br />
epidemi. Hvis omvendt S(0) er større end den relative removalrate, vil I(t) først vokse, indtil S(t) er<br />
lig den relative removalrate, hvorefter den igen vil være aftagende. I det sidste tilfælde er der altså<br />
tale om en epidemi. I(t) vil i dette tilfælde i begyndelsen vokse ekspotentielt og til sidst aftage<br />
ekspotentielt.<br />
21