Aldringens molekylærbiologi - Viden (JP)
Aldringens molekylærbiologi - Viden (JP)
Aldringens molekylærbiologi - Viden (JP)
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
4<br />
A k t u e l N a t u r v i d e n s k a b | 1 | 2 0 0 4<br />
G E R O N T O L O G I<br />
<strong>Aldringens</strong><br />
<strong>molekylærbiologi</strong><br />
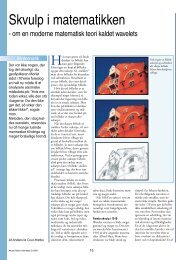
Skolepigen Nguyen Thi Ngoc på 13 år laver lektier. Hun lider af Hutchinson-Gilfords syndrom (progeria), og<br />
er Vietnams første kendte tilfælde med den dødelige sygdom, som skyldes en genetisk fejl.<br />
Foto: Nguyen Ha Minh, REUTERS / Scanpix.<br />
Af Tinna Stevnsner,<br />
Tina Thorslund og<br />
Vilhelm A. Bohr<br />
■ Det er et uundgåeligt faktum<br />
at vi alle ældes – og sidenhen<br />
dør! Nogle lever dog længere<br />
end andre – nogle er både psykisk<br />
og fysisk friske til det sidste,<br />
mens andre er svagelige allerede<br />
tidligt i alderdommen.<br />
Statistisk set er fremskreden<br />
alder dog forbundet med af en<br />
markant stigning i forekomsten<br />
af en lang række sygdomme, de<br />
såkaldt alderdoms-associerede<br />
sygdomme. Disse inkluderer<br />
bl.a. kræft, sukkersyge, hjertekar<br />
sygdomme og knogleskørhed.<br />
De basale <strong>molekylærbiologi</strong>ske<br />
processer, der fører til at vi<br />
ældes, kendes endnu ikke, men<br />
der er fl ere teorier, der forsøger<br />
at give en overordnet forklaring<br />
på aldrings-fænomenet.<br />
Forskning i de <strong>molekylærbiologi</strong>ske<br />
mekanismer, der fører<br />
til aldring, og de mange alderdoms-associerede<br />
sygdomme,<br />
kan på sigt nok ikke få os til at<br />
leve evigt – hvem har også lyst<br />
til det? Målet med den molekylære<br />
aldringsforskning er i stedet<br />
at øge livskvaliteten i den 3.<br />
alder. Dette kan bl.a. opnås ved<br />
forebyggende såvel som helbredende<br />
tiltag over for de alderdoms-associerede<br />
sygdomme.<br />
Telomerer<br />
– et biologisk urværk?<br />
Mennesket har 23 kromosompar,<br />
der som bekendt ofte afbilledes<br />
som langstrakte X’er. Hver<br />
af de fi re ender på et kromosompar<br />
beskyttes af en “hætte”<br />
– såkaldte telomerer, som er<br />
specifi kke DNA-strukturer, der
estår af en gentagen sekvens<br />
af nukleotider (DNA-byggesten),<br />
samt specifi kke telomerbindende<br />
proteiner. Telomererne<br />
har til funktion at hindre<br />
kromosom-enderne i at blive<br />
nedbrudt og dermed undgå, at<br />
DNA’et bliver ødelagt. Men,<br />
hver gang en celle deler sig, bliver<br />
telomerene kortere. Så jo<br />
ældre mennesker bliver – jo fl ere<br />
delinger cellerne i kroppen gennemgår<br />
– jo kortere bliver telomererne<br />
altså.<br />
Mange forskere har spekuleret<br />
over, om denne forkortelse<br />
af telomererne fungerer som et<br />
slags urværk, en slags nedtælling.<br />
Når telomerlængden når<br />
et bestemt kritisk niveau, så dør<br />
cellen simpelthen! En understøttelse<br />
af denne teori kommer<br />
fra viden om kræftceller. Kræftceller<br />
er i princippet udødelige<br />
celler, og i netop disse celler,<br />
forekommer der ikke telomerforkortelse.<br />
Manglen på telomerforkortelse<br />
i kræftceller skyldes<br />
tilstedeværelsen af enzymet<br />
telomerase, der kan forlænge<br />
telomerstrukturerne i takt med<br />
at cellerne deles. Man har vist,<br />
at hvis genet, der koder for<br />
enzymet telomerase, indsættes i<br />
normale celler, så udviser disse<br />
celler ikke længere tegn på aldring.<br />
Dette er en af de primære<br />
grunde til, at telomerlængden<br />
betragtes som en vigtig faktor i<br />
aldring.<br />
Der er dog også mange aspekter<br />
af aldring, som denne teori<br />
ikke kan forklare, såsom den<br />
betydelige variation i menneskers<br />
levetid. Det er ydermere<br />
blevet vist, at telomererne i<br />
ældre mennesker er så lange, at<br />
længden af dem ikke burde være<br />
kritisk før end ved gennemsnitslevealdre,<br />
der ligger 25-50 år<br />
over, hvad vi ser i dag.<br />
Ophobning af DNA skader<br />
og genomisk instabilitet<br />
Som nævnt så ofte før – er vi<br />
alle et produkt af arv og miljø.<br />
Miljøet menes i høj grad også<br />
at bidrage til aldringsprocessen,<br />
bl.a. ved at udsætte kroppen for<br />
en lang række ydre påvirkninger,<br />
der skader cellernes makromolekyler<br />
– det vil sige både<br />
proteiner, RNA og DNA.<br />
Solens ultraviolette stråler og<br />
mange former for forurening er<br />
A k t u e l N a t u r v i d e n s k a b | 1 | 2 0 0 4<br />
G E R O N T O L O G I<br />
Førtidige aldringssyndromer<br />
Aldrings-syndrom<br />
og hyppighed<br />
Hutchinson-Gilford<br />
1 pr. 4.000.000<br />
Werner<br />
1 pr. 1.000.000<br />
Cockayne<br />
(CS)<br />
1 pr. 1.000.000<br />
Trichothiodystrophy<br />
(TTD)<br />
1 pr. 1.000.000<br />
Ataxia Telangiectasia<br />
(AT)<br />
1 pr. 50.000<br />
Gennemsnitlig<br />
levetid<br />
13 år<br />
46 år<br />
12 år<br />
10 år<br />
20 år<br />
Typiske symptomer<br />
Sygdommen indtræder inden for barnets<br />
første 2 leveår. Meget tidligt bærer disse mennesker<br />
præg af tidligt udviklet alderdomssvaghed.<br />
De taber hår og øjenvipper. De har ofte<br />
åreforkalkning og udviser i høj grad mangel<br />
på underhudsfedt. Sygdommen rammer oftest<br />
hvide mennesker og lidt hyppigere drenge end<br />
piger. Dødsårsag er oftest hjertestop.<br />
Symptomerne for Werner syndrom indtræder,<br />
når børnene når puberteten. Kendetegnet<br />
er en slående misforhold mellem patientens<br />
faktiske alder og deres udseende. De får i en<br />
ung alder gråt hår og rynket hud. Desuden er<br />
der blandt disse patienter en overhyppighed<br />
af kræft, grå stær og knogleskørhed. Sygdommen<br />
er hyppigst forekommende i Japan.<br />
Der fi ndes to typer af CS. Den klassiske type<br />
indtræder inden for barnets første 10 leveår.<br />
I den anden type er symptomerne allerede<br />
tilstede fra barnets fødsel. Karakteristika<br />
for denne sygdom er en kraftig og hurtig<br />
nedbrydning af nerveceller, forekomst af grå<br />
stær, dværgvækst og oftest er patienterne<br />
følsomme over for sollys.<br />
Det mest i øjenfaldende karakteristika for TTD<br />
er patienternes skrøbelige hår og negle samt<br />
ekstremt tørre hud med tendens til skældannelse.<br />
De er ofte fysisk og mentalt underudviklede,<br />
og mange af patienterne er følsomme<br />
over for sollys.<br />
AT er en sygdom karakteriseret ved fremadskridende<br />
tab af evne til koordinering af<br />
bevægelser, udvidelse af de små kar i øjnene<br />
og gentagne infektioner af luftvejene. AT<br />
patienter er i høj grad præ-disponerede for<br />
kræft. Sygdommen kan diagnosticeres i den<br />
tidlige barndom.<br />
gode eksempler på udefrakommende<br />
faktorer, som kan trænge<br />
ind i vores celler og skade<br />
DNA’et. Hvis skaderne forbliver<br />
i DNA’et, kan det medføre det,<br />
der kaldes genomisk instabilitet.<br />
Det er ikke muligt fuldstændigt<br />
at undgå de påvirkninger,<br />
der skader vores DNA. Vi er<br />
bl.a. afhængige af den ilt, vi<br />
indånder, selvom netop ilt har<br />
vist sig at være særlig skadeligt<br />
for vores DNA. Ilt kan nemlig<br />
i kroppen forvandles til meget<br />
reaktive molekyler kaldet frie<br />
radikaler, og disse frie radikaler<br />
vil lynhurtigt reagere med<br />
Genetisk defekt<br />
Skyldes mutationer i Lamin<br />
A genet, der koder for et<br />
cellekerne protein.<br />
Skyldes mutationer i<br />
Werner-genet, som er et gen<br />
involveret i opretholdelsen<br />
af genomets stabilitet.<br />
Kan skyldes mutationer<br />
i enten CSA- eller CSB-<br />
generne. Disse gener koder<br />
for proteiner, som bl.a. er<br />
nødvendige for koblingen<br />
imellem DNA-reparation og<br />
transskription.<br />
Kan skyldes mutationer<br />
i enten XPB- eller XPD-<br />
generne. XPB- og XPDproteinerne<br />
er involverede<br />
i transskription og DNAreparation.<br />
Skyldes mutationer i ATM<br />
genet. ATM er et protein,<br />
der signalerer forekomsten<br />
af DNA skader til cellen<br />
DNA med en lang række skader<br />
til følge. Sådanne DNA-skader<br />
kaldes oxidative skader og disse<br />
har vist sig i særlig grad at blive<br />
ophobet med alderen.<br />
DNA-skader kan medføre en<br />
lang række cellulære forandringer,<br />
da informationen indkodet<br />
i DNA’et i første omgang kan<br />
blive misfortolket eller gå tabt.<br />
Forbliver skaderne i DNA’et,<br />
kan det på sigt medføre, at cellen<br />
enten udvikler sig til en<br />
kræftcelle eller også bliver cellen<br />
programmeret til at dø, hvilket<br />
kan have fatale konsekvenser,<br />
hvis cellen f.eks. er en nerve-<br />
5
6<br />
A k t u e l N a t u r v i d e n s k a b | 1 | 2 0 0 4<br />
G E R O N T O L O G I<br />
En japansk kvinde med Werner<br />
syndrom. På billedet til venstre er<br />
hun 14 år og på billedet til højre<br />
ses hun som 48 årig.<br />
celle der ikke kan erstattes af en<br />
ny celle. Det er derfor vigtigt,<br />
at cellens DNA holdes intakt<br />
og som følge deraf har cellerne<br />
udviklet en lang række reparations-systemer,<br />
der fjerner forskellige<br />
former for DNA-skader.<br />
DNA reparationssystemerne<br />
er dog ikke i stand til at fjerne<br />
100% af skaderne, og derfor<br />
ophobes fejl i DNA med alderen.<br />
På cellulært plan betyder<br />
det, at jo ældre organismen bliver<br />
jo fl ere skader vil der være<br />
ophobet i cellernes DNA – og<br />
jo dårligere vil cellerne fungere.<br />
Og jo dårligere cellerne fungerer,<br />
jo dårligere vil kroppen og<br />
dens organer, muskler, hjerne<br />
og knogler fungere. Således kan<br />
ophobning af DNA-skader altså<br />
Telomerteori<br />
Telomer<br />
Centromer<br />
Telomer<br />
DNA<br />
Kromatid<br />
Kromosom<br />
Basepar<br />
Der sidder telomerer for enden<br />
af alle vores kromosomer.<br />
Telomererne, der består af en<br />
bestemt repeteret DNA sekvens<br />
samt specifi kke proteiner,<br />
danner en struktur der beskytter<br />
vores genetiske materiale<br />
(kromosomerne) mod nedbryd-<br />
Telomer<br />
føre til at vi ældes.<br />
Til støtte for teorien, om at<br />
akkumulering af DNA-skader<br />
medfører aldring, har adskillige<br />
studier vist, at der er en sammenhæng<br />
mellem pattedyrs<br />
evne til at udføre DNA-reparation<br />
og deres gennemsnitslevealder.<br />
Førtidige<br />
aldringssyndromer<br />
Det er klart, at en regulering af<br />
aldringsprocessen må afhænge<br />
af mange og ikke bare et enkelt<br />
gen. Nogle få mennesker opnår<br />
en meget høj levealder på 120<br />
år eller derover. Vi kender<br />
endnu ikke til de særlige genetiske<br />
eller molekylære forhold,<br />
der gør sig gældende hos disse<br />
individer. Til gengæld kender vi<br />
en række genetiske sygdomme,<br />
hvor patienterne gennemgår<br />
en førtidig aldringsproces. Fællestrækkene<br />
for patienter med<br />
disse førtidige aldringssyndromer<br />
er, at de i en meget ung<br />
alder ser gamle ud med gråt hår<br />
og rynker, og de har i denne<br />
unge alder en stærkt forøget<br />
risiko for at udvikle en række<br />
sygdomme som kræft, hjertekar<br />
sygdomme, type II sukkersyge<br />
og grå stær, som vi nor-<br />
ning. Flere studier har vist, at telomerene<br />
bliver kortere med alderen.<br />
Til venstre er vist en skematisk tegning<br />
af, hvordan telomeren sidder<br />
i enden af kromosomet. Til højre<br />
er vist et computerprogram, som<br />
forskere i DCMG benytter sig af, til<br />
at bestemme længden af telome-<br />
malt forbinder med aldring.<br />
Forskere har længe interesseret<br />
sig for disse sygdomme,<br />
da disse førtidige aldringssyndromer<br />
kan bruges som modelsystemer<br />
for, hvad der sker ved<br />
normal aldring. Hvis man kan<br />
identifi cere, hvad det er for cellulære<br />
defekter i disse patienter,<br />
der fører til den førtidige aldring<br />
og de alderdoms-associerede<br />
sygdomme, så kan denne<br />
viden med stor sandsynlighed<br />
overføres til, hvad der sker i<br />
normal aldring.<br />
Eksempler på førtidige aldringssyndromer<br />
er: Hutchinson-Gilford<br />
progeria, Werner<br />
Syndrom, Cockayne syndrom,<br />
Trichothiodystrophy og Ataxia<br />
Telangiectasia (se boks). Et fællestræk<br />
for celler fra patienter<br />
med de forskellige førtidige aldringssyndromer<br />
er, at de alle har<br />
øget genomisk instabilitet, sammenlignet<br />
med celler fra raske<br />
mennesker.<br />
De defekte gener, der forårsager<br />
de nævnte førtidige aldringssyndromer,<br />
er nu alle blevet<br />
identifi ceret, hvilket gør det<br />
muligt at foretage detaljerede<br />
studier af proteinerne og de cellulære<br />
processer, som proteinerne<br />
er involverede i.<br />
rene på menneskets 23 kromosom-par.<br />
De 23 kromosom-par<br />
er vist i forskellige farver og<br />
baseret på intensiteten af de<br />
lysende prikker i enderne af<br />
kromosomerne kan længden af<br />
telomerene bestemmes.<br />
Werner syndrom er nok det<br />
førtidige aldringssyndrom, der<br />
har fl est ligheder med normal<br />
aldring. Sygdommen skyldes<br />
mutationer i Werner-genet.<br />
Dette gen koder for Wernerproteinet,<br />
som er et enzym, der<br />
både kan vikle DNA-strenge<br />
fra hinanden, og nedbryde<br />
enderne på DNA-strenge. Werner-proteinet<br />
har vist sig at<br />
være involveret i mange forskellige<br />
cellulære processer,<br />
såsom DNA-reparation, transskription<br />
(budbringning fra<br />
DNA’et), replikation (kopiering<br />
af DNA’et), rekombination<br />
(omrokering imellem<br />
DNA-strenge) samt vedligeholdelse<br />
af telomererne. Werner-proteinet<br />
synes dog ikke<br />
at være essentielt for nogle af<br />
disse processer, men den overordnede<br />
nedsatte effektivitet af<br />
disse mange forskellige processer<br />
giver tilsammen ophav til<br />
genomisk instabilitet.<br />
Mutationer i to forskellige<br />
gener kaldet CSA og CSB, kan<br />
give ophav til Cockayne syndrom.<br />
De proteiner, som disse<br />
gener koder for (CSA- og CSBproteinerne),<br />
er i lighed med<br />
Werner-proteinet involveret i en<br />
række vigtige cellulære processer<br />
som DNA-reparation, transskription<br />
og celledød. CSA- og<br />
CSB-proteinerne er dermed<br />
også vigtige for opretholdelsen<br />
af genomisk stabilitet.<br />
Først for ganske nyligt har<br />
man fundet ud af, at mutationer<br />
i Lamin A genet giver<br />
ophav til Hutchinson-Gilford<br />
progeria. Lamin A er et strukturelt<br />
protein i cellekernen uden<br />
enzymatisk aktivitet. Endnu<br />
er der ingen der rigtigt forstår,<br />
hvordan defekten i netop dette<br />
protein kan give ophav til det<br />
komplekse sygdomsbillede som<br />
Hutchinson-Gilford progeria<br />
har.<br />
Fremtidsperspektiver<br />
Mutationer i et enkelt, eller få,<br />
af de mange hundrede gener der<br />
er involverede i opretholdelsen<br />
af genomisk stabilitet kan altså<br />
føre til et sygdomsbillede, der<br />
på mange måder ligner normal<br />
aldring. Hvis defekter i opretholdelse<br />
af genomisk stabilitet<br />
fører til førtidige aldringssyn-
Radioaktivitet Rygning Stofskifte og energiproduktion<br />
i cellens mitokondrier<br />
Forurening<br />
Normal e<br />
baser<br />
G A G C T T C G T T G C G A T C C G C A<br />
C T U G A A G C A A T C G C T A G G C G T<br />
Ikke korrekt<br />
base<br />
I vores omgivelser er der mange kilder til DNA-skader. Nogle af disse kilder kan vi til dels beskytte os imod, såsom<br />
radioaktivitet, rygning, solens farlige stråler og forurening. Andre kilder til DNA-skader er helt uundgåelige, som dem<br />
der kommer fordi vi trækker vejret og spiser. Der kan opstå mange forskellige typer af DNA-skader, der hver især har<br />
deres særlige indfl ydelse på DNA’ets funktion. De forskellige typer af DNA-skader bliver repareret af et antal DNAreparations<br />
systemer, som hver især er specialiserede i at fjerne bestemte typer af skader.<br />
Dansk Center for<br />
Molekylær Gerontologi<br />
Der har på verdensplan været en markant stigning indenfor den molekylære aldringsforskning i de senere år. I<br />
Danmark blev ”Dansk Center for Molekylær Gerontologi” (DCMG) grundlagt som tværfagligt center i 1995, og<br />
det blev indlejret som Universitetscenter ved Aarhus Universitet i 2001. Forskningsgrupper i DCMG arbejder på<br />
at forstå forskellige aspekter af de generelle molekylære mekanismer, der ligger bag aldringsprocessen.<br />
På et af laboratorierne ved DCMG – Laboratorium for DNA Reparation – arbejder vi bl.a. med at opnå større<br />
indsigt i det såkaldte CSB-proteins rolle i aldringsprocessen. Mutationer i dette protein kan give ophav til<br />
Cockayne syndrom, som er et førtidigt aldringssyndrom.<br />
På laboratoriet er vi i tæt samarbejde med ”Laboratory of Molecular Gerontology” på National Institute on<br />
Aging, NIH i Baltimore, USA, i gang med at undersøge, hvilke proteiner CSB-proteinet vekselvirker med og sidder<br />
i kompleks med i cellen. Endvidere undersøger vi , hvorledes CSB’s aktivitet reguleres af forskellige biokemiske<br />
modifi ceringer, og hvorledes disse modifi ceringer påvirker CSB’s vekselvirkninger med andre proteiner og proteinets<br />
lokalisering i cellen.<br />
En anden del af aktiviteterne ved laboratoriets forskningsaktiviteter drejer sig om at belyse de processer, der<br />
er med til at vedligeholde cellernes energistationer, mitokondrierne, og hvordan mitokondriernes kapacitet for<br />
DNA- reparation ændres med alderen. En række studier tyder nemlig på, at især ophobning af oxidative skader i<br />
mitokondrierne, spiller en vigtig rolle i aldringsprocessen.<br />
dromer, er det så muligt, at normal<br />
aldring er delvis forårsaget<br />
af utilstrækkelig reparation af<br />
DNA-skader? Forhåbentlig vil<br />
yderligere forskning i DNAreparation<br />
og molekylær gerontologi<br />
kunne give os svar på<br />
dette spørgsmål ved at tilveje-<br />
DNA-skader<br />
6-4 foto<br />
produkt<br />
Pyrimidin<br />
dimer<br />
Brud på DNA strengen<br />
Manglende<br />
base<br />
Voluminøs skade<br />
bringe detaljeret viden om de<br />
basale mekanismer, der sørger<br />
for opretholdelsen af genomisk<br />
stabilitet.<br />
Samtidig vil denne forskning<br />
kunne stimulere udviklingen af<br />
nye medicinske behandlinger,<br />
som kan reducere DNA-skader<br />
Kovalent binding mellem baser<br />
på samme DNA streng<br />
A k t u e l N a t u r v i d e n s k a b | 1 | 2 0 0 4<br />
G E R O N T O L O G I<br />
Sol-lys<br />
Kovalent binding mellem baser<br />
på modsatte DNA strenge<br />
og/eller fremme DNA-reparation.<br />
Sådanne nye initiativer<br />
må forventes at kunne udsætte<br />
adskillige af de alderdomsassocierede<br />
sygdomme, og dermed<br />
øge produktiviteten og livskvaliteten<br />
i den ældre del af befolkningen.<br />
■<br />
Om forfatterne<br />
Tinna Stevnsner er lektor på<br />
Molekylærbiologisk Institut,<br />
Aarhus Universitet,<br />
og tilknyttet Dansk Center<br />
for Molekylær Gerontologi<br />
(DCMG)<br />
email: tvs@mb.au.dk<br />
Tina Thorslund er ph.d.-studerende<br />
ved Molekylærbiologisk<br />
Institut, Aarhus Universitet,<br />
med støtte fra DCMG.<br />
Vilhelm A. Bohr er<br />
adjungeret professor ved<br />
Molekylærbiologisk Institut,<br />
Aarhus Univeristet, Laboratorichef<br />
for Laboratory<br />
of Molecular Gerontology,<br />
National Institute on Aging,<br />
NIH, Baltimore, USA og er<br />
ligeledes tilknyttet DCMG.<br />
Adresse: Dansk Center for<br />
Molekylær Gerontologi,<br />
Molekylærbiologisk Institut,<br />
Aarhus Universitet, Byg. 130,<br />
8000 Århus C,<br />
Tlf.: 89422656<br />
email: molgeron@mb.au.dk,<br />
Hjemmeside: www.dcmg.dk<br />
Læs videre<br />
Hvorfor ældes vi forskelligt? Af<br />
Kaare Christensen; Gyldendal<br />
Uddannelse<br />
Livets kode: DNA. Af Vilhelm<br />
A. Bohr og Birgit L. Andersen;<br />
Fremad.<br />
Human premature aging<br />
syndromes and genomic<br />
instability; Bohr VA.;<br />
Mechanisms in Aging and<br />
Development 2002 Apr. 30,<br />
vol. 123(8) page 987-93<br />
Mitochondrial repair of 8oxoguanine<br />
and changes<br />
with aging; Stevnsner T.,<br />
Thorslund T., Souza-Pinto<br />
NC., Bohr VA.; Experimental<br />
Gerontology 2002 Oct-Nov:<br />
37 (10-11) page 1189-96<br />
7