kemi C-B - VUC Aarhus
kemi C-B - VUC Aarhus
kemi C-B - VUC Aarhus
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
<strong>VUC</strong> <strong>Aarhus</strong>. Kemi B. Laboratoriekursus.<br />
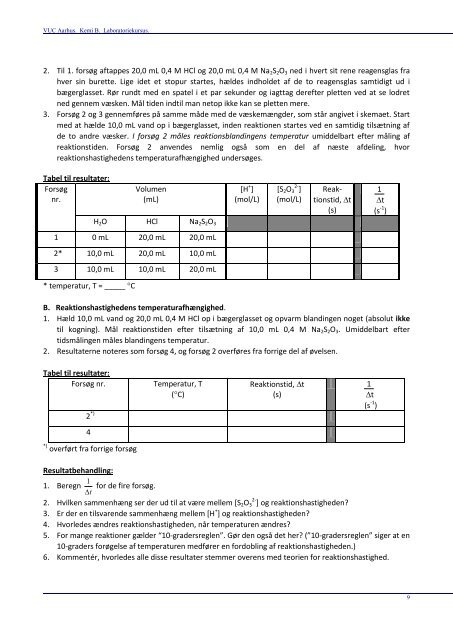
2. Til 1. forsøg aftappes 20,0 mL 0,4 M HCl og 20,0 mL 0,4 M Na 2 S 2 O 3 ned i hvert sit rene reagensglas fra<br />
hver sin burette. Lige idet et stopur startes, hældes indholdet af de to reagensglas samtidigt ud i<br />
bægerglasset. Rør rundt med en spatel i et par sekunder og iagttag derefter pletten ved at se lodret<br />
ned gennem væsken. Mål tiden indtil man netop ikke kan se pletten mere.<br />
3. Forsøg 2 og 3 gennemføres på samme måde med de væskemængder, som står angivet i skemaet. Start<br />
med at hælde 10,0 mL vand op i bægerglasset, inden reaktionen startes ved en samtidig tilsætning af<br />
de to andre væsker. I forsøg 2 måles reaktionsblandingens temperatur umiddelbart efter måling af<br />
reaktionstiden. Forsøg 2 anvendes nemlig også som en del af næste afdeling, hvor<br />
reaktionshastighedens temperaturafhængighed undersøges.<br />
Tabel til resultater:<br />
Forsøg<br />
nr.<br />
Volumen<br />
(mL)<br />
[H + ]<br />
(mol/L)<br />
[S 2 O 3 2- ]<br />
(mol/L)<br />
Reaktionstid,<br />
t<br />
(s)<br />
1<br />
t<br />
(s -1 )<br />
H 2 O HCl Na 2 S 2 O 3<br />
1 0 mL 20,0 mL 20,0 mL<br />
2* 10,0 mL 20,0 mL 10,0 mL<br />
3 10,0 mL 10,0 mL 20,0 mL<br />
* temperatur, T = _____ C<br />
B. Reaktionshastighedens temperaturafhængighed.<br />
1. Hæld 10,0 mL vand og 20,0 mL 0,4 M HCl op i bægerglasset og opvarm blandingen noget (absolut ikke<br />
til kogning). Mål reaktionstiden efter tilsætning af 10,0 mL 0,4 M Na 2 S 2 O 3 . Umiddelbart efter<br />
tidsmålingen måles blandingens temperatur.<br />
2. Resultaterne noteres som forsøg 4, og forsøg 2 overføres fra forrige del af øvelsen.<br />
Tabel til resultater:<br />
Forsøg nr.<br />
2 *)<br />
Temperatur, T<br />
(C)<br />
Reaktionstid, t<br />
(s)<br />
1<br />
t<br />
(s -1 )<br />
4<br />
*) overført fra forrige forsøg<br />
Resultatbehandling:<br />
1. Beregn 1 t<br />
for de fire forsøg.<br />
2. Hvilken sammenhæng ser der ud til at være mellem [S 2 O 3 2- ] og reaktionshastigheden?<br />
3. Er der en tilsvarende sammenhæng mellem [H + ] og reaktionshastigheden?<br />
4. Hvorledes ændres reaktionshastigheden, når temperaturen ændres?<br />
5. For mange reaktioner gælder “10-gradersreglen”. Gør den også det her? (”10-gradersreglen” siger at en<br />
10-graders forøgelse af temperaturen medfører en fordobling af reaktionshastigheden.)<br />
6. Kommentér, hvorledes alle disse resultater stemmer overens med teorien for reaktionshastighed.<br />
9