Intrauterine Wachstumsretardierung (IUWR)
Intrauterine Wachstumsretardierung (IUWR)
Intrauterine Wachstumsretardierung (IUWR)
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
<strong>Intrauterine</strong> <strong>Wachstumsretardierung</strong> (<strong>IUWR</strong>)<br />
1. Terminologie<br />
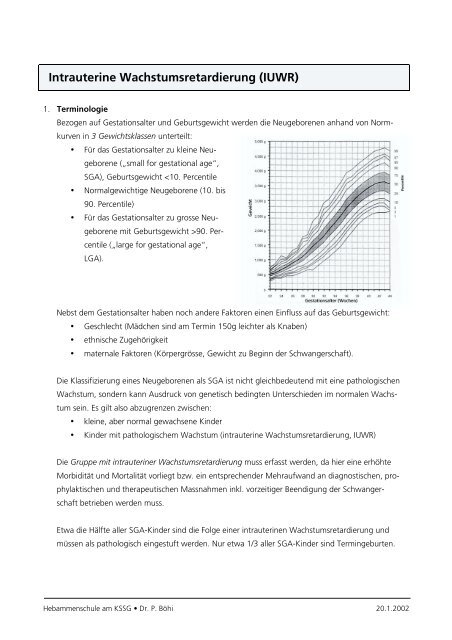
Bezogen auf Gestationsalter und Geburtsgewicht werden die Neugeborenen anhand von Normkurven<br />
in 3 Gewichtsklassen unterteilt:<br />
Für das Gestationsalter zu kleine Neugeborene<br />
(„small for gestational age“,<br />
SGA), Geburtsgewicht 90. Percentile<br />
(„large for gestational age“,<br />
LGA).<br />
Nebst dem Gestationsalter haben noch andere Faktoren einen Einfluss auf das Geburtsgewicht:<br />
Geschlecht (Mädchen sind am Termin 150g leichter als Knaben)<br />
ethnische Zugehörigkeit<br />
maternale Faktoren (Körpergrösse, Gewicht zu Beginn der Schwangerschaft).<br />
Die Klassifizierung eines Neugeborenen als SGA ist nicht gleichbedeutend mit eine pathologischen<br />
Wachstum, sondern kann Ausdruck von genetisch bedingten Unterschieden im normalen Wachstum<br />
sein. Es gilt also abzugrenzen zwischen:<br />
kleine, aber normal gewachsene Kinder<br />
Kinder mit pathologischem Wachstum (intrauterine <strong>Wachstumsretardierung</strong>, <strong>IUWR</strong>)<br />
Die Gruppe mit intrauteriner <strong>Wachstumsretardierung</strong> muss erfasst werden, da hier eine erhöhte<br />
Morbidität und Mortalität vorliegt bzw. ein entsprechender Mehraufwand an diagnostischen, prophylaktischen<br />
und therapeutischen Massnahmen inkl. vorzeitiger Beendigung der Schwangerschaft<br />
betrieben werden muss.<br />
Etwa die Hälfte aller SGA-Kinder sind die Folge einer intrauterinen <strong>Wachstumsretardierung</strong> und<br />
müssen als pathologisch eingestuft werden. Nur etwa 1/3 aller SGA-Kinder sind Termingeburten.<br />
Hebammenschule am KSSG Dr. P. Böhi 20.1.2002
<strong>Intrauterine</strong> <strong>Wachstumsretardierung</strong><br />
2. Ätiologie der intrauterinen <strong>Wachstumsretardierung</strong><br />
Es gibt eine Vielzahl von Ursachen einer <strong>IUWR</strong>, welche sich bezüglich Verlauf, Schweregrad und<br />
Prognose unterscheiden. Klinisch ist vor allem die Unterteilung sinnvoll in:<br />
Seite 2<br />
Formen, die primär auf fetaler Pathologie basieren bei weitgehend ungestörter Versorgung<br />
Formen mit einer Beeinträchtigung der Versorgung.<br />
Primär fetal (ungestörte Versorgung) Gestörte Versorgung<br />
Endogen<br />
- Fehlbildungen<br />
- Chromosomenanomalien: Trisomie<br />
13, 18, 21<br />
- Stoffwechselerkrankungen<br />
Exogen<br />
- <strong>Intrauterine</strong> Infektionen: Röteln, Zytomegalie,<br />
Toxoplasmose, Herpes<br />
- Strahlenexposition<br />
Präplazentar<br />
- O2-Mangel (Höhenexposition)<br />
- Hyperthermie<br />
- Mangelernährung<br />
- Toxische Einflüsse, Nikotin,<br />
Alkohol, Drogen<br />
Maternale Störungen/Erkrankungen<br />
- Anämie<br />
- Hypertonie/Präeklampsie<br />
- Chronische Nierenleiden<br />
- Zyanotische Herzvitien<br />
- Systemischer Lupus erythematodes<br />
- Diabetes mellitus<br />
Plazentar<br />
- Plazenta praevia<br />
- vorzeitige Plazentalösung<br />
- Chromosomen Mosaik<br />
- Gestörte Plazentation (mit/ohne<br />
Uteruspathologie)<br />
Der Anteil der endogenen, primär fetal bedingten Wachstumsstörungen beträgt 10-20%. Diese<br />
idR. symmetrischen <strong>Wachstumsretardierung</strong>en sind häufig mit Chromosomenstörungen und Fehlbildungen<br />
assoziiert.<br />
Die Unterteilung der Gruppe mit gestörter Versorgung in präplazentar, maternal und plazentar<br />
weist erheblich Überlappungen auf, allen gemeinsam ist jedoch die Beeinträchtigung der Zufuhr<br />
von Sauerstoff und Nahrungsstoffen mit dem mütterlichen Blut in das uteroplazentare Gefässgebiet.<br />
Hebammenschule am KSSG Dr. P. Böhi 20.1.2002
<strong>Intrauterine</strong> <strong>Wachstumsretardierung</strong><br />
Je nach Ursache können Zusammensetzung des Blutes, Durchblutung der Plazenta oder die Entwicklung<br />
der Plazenta gestört sein.<br />
In 40% aller Fälle mit <strong>IUWR</strong> lässt sich keine Ursache ermitteln (idiopathisch).<br />
Seite 3<br />
3. Pathophysiologie des fetalen Wachstums<br />
Das Gewebewachstum basiert auf Vermehrung der Zellzahl durch Teilung (Hyperplasie) und Zunahme<br />
des Zellvolumens (Hypertrophie). Das embryonale Wachstum im ersten Trimenon geschieht<br />
vor allem durch Zellvermehrung, während im letzten Trimenon das hypertrophische Zellwachstum<br />
im Vordergrund steht. Im mittleren Trimenon sind beide Formen gleich vertreten.<br />
Das intrauterine Wachstum wird von 2 Faktoren bestimmt:<br />
genetisch determiniertes Wachstumspotential<br />
Zufuhr von Sauerstoff, Nahrungsstoffen, Vitaminen, Mineralien, Spurenelementen<br />
Das intrauterine Wachstum ist vor allem von der Zufuhr von Nahrungsstoffen abhängig. Diese Versorgung<br />
wird durch die Mutter sichergestellt, diese hat einen grösseren Einfluss auf die Grösse des<br />
Kindes als der Vater. Postnatal ist das genetisch determinierte Wachstumspotential bestimmend.<br />
Das Wachstum der verschiedenen Körperteile des Fetus wird unterschiedlich reguliert, je nach<br />
Zeitpunkt einer Störung im Verlaufe der Schwangerschaft sind die Auswirkungen verschieden:<br />
frühe Form: Längenwachstum am meisten betroffen, enge Korrelation zu Kopfumfang und<br />
Körpergewicht. Klinisch ausgeprägteste Form der Retardierung mit schwerster perinataler<br />
Pathologie.<br />
spätere Form: Längenwachstum und Kopfumfang weniger betroffen, vor allem Verminderung<br />
an subkutanem Fettgewebe dh. vor allem Gewicht reduziert.<br />
Je nach Zeitpunkt der Störung tritt somit eine symmetrische <strong>IUWR</strong> auf mit gleichförmiger Beeinträchtigung<br />
von Längenwachstum, Kopfumfang und Körpergewicht bzw. eine asymmetrische<br />
Form mit vorwiegender Beeinträchtigung von Abdomenumfang und Gewicht.<br />
Die symmetrische <strong>IUWR</strong> findet sich gehäuft bei Karyotypanomalien, Nikotin- und Drogenabusus<br />
sowie viralen Infektionen. Auch eine früh einsetzende intrauterine Versorgungsstörung kann zu<br />
einer symmetrischen <strong>IUWR</strong> führen.<br />
Hebammenschule am KSSG Dr. P. Böhi 20.1.2002
<strong>Intrauterine</strong> <strong>Wachstumsretardierung</strong><br />
Eine intrauterine Mangelversorgung mit ungenügender Zufuhr von Sauerstoff, Nahrungsstoffen,<br />
Vitaminen, Mineralien und Spurenelementen führt zu einer Verlangsamung des Wachstums. Reguliert<br />
durch IFG-1 und Insulin findet eine Hemmung des Zellwachstums statt.<br />
Sowohl bei genetischen Ursachen wie Versorgungsstörungen sind die therapeutischen Interventionsmöglichkeiten<br />
sehr begrenzt. Die Schwangerschaftsbetreuung konzentriert sich darauf, Dauerschäden<br />
fetaler Organe infolge chronischem Mangel an Sauerstoff und anderen Substraten zu<br />
vermeiden (Zeitpunkt der drohenden Dekompensation erkennen) bzw. den optimalen Entbindungszeitpunkt<br />
festzulegen - möglichst unter Vermeidung einer Frühgeburt.<br />
Es gibt einen Zusammenhang zwischen <strong>IUWR</strong> mit Dauerschäden fetaler Organe und im Erwachsenenalter<br />
manifest werdenden Erkrankungen des Herz-Kreislauf-Systems und des Stoffwechsels<br />
(Diabetes mellitus Typ II, Hyperlipidämie).<br />
Da 2/3 alle Fälle mit <strong>IUWR</strong> durch chronische intrauterine Mangelversorgung bedingt sind, welche<br />
durch die optimale Wahl des Entbindungszeitpunkts bzw. eine intensive perinatale Betreuung beeinflusst<br />
werden können, soll diese Form der <strong>IUWR</strong> in der Folge weiter besprochen werden.<br />
Seite 4<br />
4. Screening und Untersuchungsmethoden<br />
Voraussetzung zur Erkennung des SGA-Fetus ist die exakte Kenntnis des Gestationsalters. Bei unsicherer<br />
letzter Periode ist die Messung der Scheitel-Steiss-Länge (SSL) in der 9.-12. SSW am zuverlässigsten<br />
zur Festlegung des Geburtstermins bzw. des Gestationsalters.<br />
Für die fetale Gewichtsschätzung führt die kombinierte Messung von Kopf- und Abdomenumfängen<br />
zu den besten Ergebnissen. Berücksichtigt werden müssen zusätzlich ethnische Herkunft, sozioökonomischer<br />
Status, Ausgangsgewicht und Körperlänge der Mutter sowie das Geschlecht des<br />
Kindes.<br />
Die Grenzziehung bei der 10. Percentile geschieht aufgrund epidemiologischer Faktoren und ist<br />
willkürlich. Damit ist noch keine Unterscheidung zwischen einem normal ernährten, aber konstitutionell<br />
kleinen Fetus und und einem <strong>IUWR</strong>-Fetus gemacht.<br />
Eine Hilfe bei der Diagnose einer <strong>IUWR</strong> ist der sog. Ponderal-Index: Geburtsgewicht (g) / Geburtslänge<br />
(cm) 3 x 100. Damit kann die Verdachtsdiagnose einer <strong>IUWR</strong> gestellt werden.<br />
Am aussagekräftigsten ist die Abnahme der Wachstumsrate als Hinweis auf eine <strong>IUWR</strong>, selbst<br />
wenn die Masse noch über der 10. Percentile liegen. Umgekehrt ist ein Fetus, welcher sich zwar<br />
Hebammenschule am KSSG Dr. P. Böhi 20.1.2002
<strong>Intrauterine</strong> <strong>Wachstumsretardierung</strong><br />
unterhalb der 10. Percentile, aber parallel zu den Percentilenkurven entwickelt, nicht besonders<br />
gefährdet.<br />
Wachstum bei <strong>IUWR</strong>: Gewicht und Abdomenumfang entwickeln sich nicht percentilengerecht,<br />
sondern entwickeln einen immer grösseren Wachstumsrückstand bis zum Wachstumsstillstand.<br />
Klinische Untersuchung: Die Messung des Symphysen-Fundus-Abstands ist eine wichtige Untersuchung<br />
und kann entweder als Screening-Untersuchung ab der 32. SSW oder seriell als Verlaufskontrolle<br />
eingesetzt werden.<br />
Besser mit dem Geburtsgewicht korreliert die sonographische Messung des fetalen Abdomenumfangs,<br />
hier kann ebenfalls mit einer Einzelmessung oder besser mittels serieller Messungen der<br />
Verdacht auf eine <strong>IUWR</strong> erhoben werden.<br />
Durch das kombinierte Vorgehen dh. wiederholte Symphysen-Fundus-Messungen mit Messung<br />
des fetalen Abdomenumfangs im Falle des Verdachts auf Retardierung können 93% aller Feten<br />
mit <strong>IUWR</strong> erfasst werden (PPV 85%).<br />
Seite 5<br />
Hebammenschule am KSSG Dr. P. Böhi 20.1.2002
<strong>Intrauterine</strong> <strong>Wachstumsretardierung</strong><br />
Ultraschallbiometrie: Die Erkennung eines SGA-Fetus gelingt am besten sonographisch durch<br />
eine Gewichtsschätzung basierend auf bestimmten Messdaten, wobei die Kenntnis des korrekten<br />
Termins natürlich eine Voraussetzung ist. Es werden die folgenden Masse bestimmt:<br />
Kopf: Biparietaler und fronto-okzipitaler Durchmesser, Kopfumfang<br />
Abdomen: Thoraxquer- und anterio-posteriorer Durchmesser, Abdomenumfang<br />
Lange Röhrenknochen: Femur, Humerus.<br />
(Oben) Messung des biparietalen Kopfdurchmessers (bezeichnet durch x- - - - - -x) und<br />
des Kopfumfangs. (Mitte) Messung des Abdomenumfangs. (Unten) Messung der Femurlänge<br />
(bezeichnet durch x- - - - - -x).<br />
Seite 6<br />
Hebammenschule am KSSG Dr. P. Böhi 20.1.2002
<strong>Intrauterine</strong> <strong>Wachstumsretardierung</strong><br />
Auf diese Weise können bis zu 89% aller SGA-Feten erfasst werden. Sensitivster Parameter ist der<br />
Abdomenumfang.<br />
Es gibt eine Reihe von prädiktiven klinischen und ultrasonographischen Hinweiszeichen, für die Erkennung<br />
eines <strong>IUWR</strong>-Feten:<br />
Klinische Hinweiszeichen:<br />
- Reduzierter Symphysen-Fundus-Abstand (serielle Messungen!)<br />
- „Kleiner Bauch“, geringe Gewichtszunahme<br />
- St.n. <strong>IUWR</strong><br />
- Hypertensive Schwangerschaftserkrankung<br />
- Nikotin- bzw. Drogenabusus<br />
Ultrasonographische und andere Hinweiszeichen:<br />
- Reduzierter fetaler Abdomenumfang (serielle Messungen!)<br />
- Oligohydramnion<br />
- Pathologische Dopplerflussmessung<br />
- Pathologisches CTG<br />
- Pathologisches Bewegungsprofil (Biophysikalisches Profil).<br />
Seite 7<br />
Ca. 75% aller Patientinnen mit SGA-Feten weisen solche prädisponierenden Risiken wie eine belastete<br />
Anamnese, eine SIH, einen fortgeschrittenen Diabetes mellitus, einen starken Nikotinabusus<br />
oder eine unzureichende Gewichtszunahme im 3. Trimenon auf.<br />
Dopplersonographie: Obwohl eine <strong>IUWR</strong> häufig mit pathologischen Flussmustern einhergeht ist<br />
die Dopplersonographie fetaler und maternaler Gefässe als Screening-Methode ungeeignet. Die<br />
Ultraschallbiometrie erfasst das fetale Wachstum viel direkter und ist dem Doppler somit überlegen.<br />
Plazentaassoziierte Risikofaktoren: Aus der Uberlegung, dass Störungen im Wachstum und der<br />
Entwicklung der Plazenta sowie der Anpassung der Durchblutung der klinischen Entwicklung einer<br />
<strong>IUWR</strong> vorausgehen, wurde nach plazentaren Screeningmöglichkeiten im frühen 2. Trimenon gesucht,<br />
um eine <strong>IUWR</strong> früh erfassen zu können.<br />
Sowohl die sonographische Bestimmung des Plazentavolumens, Dopplerflussmessungen fetaler<br />
und maternaler Gefässe, wie die Bestimmung von Proteinen fetalen oder plazentaren Ursprungs<br />
erwiesen sich als zu wenig sensitiv und spezfisch, um die frühzeitige Erkennung einer <strong>IUWR</strong> zu ermöglichen.<br />
Hebammenschule am KSSG Dr. P. Böhi 20.1.2002
<strong>Intrauterine</strong> <strong>Wachstumsretardierung</strong><br />
5. Diagnostik und Uberwachung<br />
Wie bereits erwähnt, reflektiert eine fetale Wachstumskurve, die unterhalb der Norm verläuft,<br />
nicht notwendigerweise eine fetale Pathologie.<br />
Bei Verdacht auf SGA muss als erstes eine Ursachenabklärung vorgenommen werden:<br />
fetaler Infekt<br />
Fehlbildungen (in 22% mit <strong>IUWR</strong> assoziiert)<br />
Karyotypisierung (Chromosomenanomalie bei <strong>IUWR</strong> in 2-8%)<br />
gefässrelevante maternale Erkrankungen.<br />
Als zweites ist die Uberwachung des eigentlichen hypoxiegefährdeten <strong>IUWR</strong>-Kollektivs zentraler<br />
Bestandteil des klinischen Managements, um den optimalen Entbindungszeitpunkt festlegen zu<br />
können.<br />
Chordozentese - Chromosomenanomalien, Infektion, Plazentarinsuffizienz: Die Nabelschnurpunktion<br />
erlaubt eine Fetalblutanalyse mit rascher<br />
Karyotypisierung innert 72h, eine Beurteilung der<br />
Blutgase mit Einblick in den fetalen Metabolismus und<br />
die Diagnostik wichtiger Infektionen (Zytomegalie, Toxoplasmose<br />
u.a.).<br />
Diese invasive Methode weist eine Abortrate von 0.3 -<br />
1.9% auf. Zur Diagnostik der fetalen Gefährdung bzw.<br />
Festlegung des Entbindungszeitpunkts sind nichtinvasive<br />
Untersuchungen wie die Dopplersonographie<br />
besser geeignet.<br />
Seite 8<br />
Dopplersonographie: Hier werden ebenfalls Percentilenkurven zur Einteilung in normale und pathologische<br />
Blutströmungsmuster eingesetzt. Als pathologisch gelten Gefässwiderstände >90. Percentile<br />
für die maternalen und fetalen Gefässe, bezogen auf das aktuelle Gestationsalter (Nabelschnurarterie,<br />
fetale Aorta, uteroplazentares Gefässbett).<br />
Bei den fetalen Gehirnarterien (A. cerebri media) gilt dagegen eine Abnahme des Gefässwiderstandes<br />
<strong>Intrauterine</strong> <strong>Wachstumsretardierung</strong><br />
Es gibt typische Flussmusterveränderungen, die eine weitere Einschränkung der fetalen Versorgung<br />
signalisieren:<br />
Sauerstoffsparschaltung zugunsten des Gehirns („brain sparing“) dh. Gefässwiderstand in<br />
der Nabelschnurarterie >90. Percentile, in der A. cerebri media des Feten
<strong>Intrauterine</strong> <strong>Wachstumsretardierung</strong><br />
Seite 10<br />
Die Dopplersonographie ist bei der Triage zwischen SGA und <strong>IUWR</strong>-Feten hilfreich und erlaubt bei<br />
unauffälligen Dopplerbefunden bei biometrisch kleinem Fetus - nach Ausschluss von Fehlbildungen<br />
- die ambulante Überwachung, was Kosten spart und die Belastung der Eltern reduziert.<br />
Fruchtwassermenge: Die Fruchtwassermenge wird sonographisch mit dem „amniotic fluid index“<br />
(AFI) bestimmt. Der Uterus wird in 4 Quadranten eingeteilt, in jedem Quadranten wird senkrecht<br />
zur Unterlage das grösste Fruchtwasserdepot ausgemessen, die summierten Werte ergeben<br />
den Fruchtwasserindex in cm.<br />
Bei einem AFI
<strong>Intrauterine</strong> <strong>Wachstumsretardierung</strong><br />
Seite 11<br />
verschiedener Organe mit Akut- sowie Langzeitmorbidität bei den Uberlebenden bis hin zum perinatalen<br />
Tod infolge schwerer Hypoxie.<br />
Die Zustandsbeurteilung des Feten hat insbesondere das Ziel, Hirnschäden mit neuromotorischen<br />
Entwicklungsstörungen zu vermeiden. Die Entbindung muss somit vor dem Auftreten entsprechender<br />
Organschäden vorgenommen werden.<br />
Bei früh im Verlaufe der Schwangerschaft auftretender Dekompensation der fetalen Versorgung<br />
stellt das Abwägen des Risikos bleibender hypoxischer Organschäden gegenüber der Problemen<br />
der Unreife eine besondere Herausforderung dar.<br />
Die Adaptation des Feten an die chronische Mangelversorgung läuft in einer Sequenz an Veränderungen<br />
ab, welche sich mittels Ultraschall bzw. Doppler verfolgen lassen. Hierbei gilt die Zentralisation<br />
des arteriellen Kreislaufs des Feten mit bevorzugter Blutzufuhr zum Gehirn, zum Herzen und<br />
zu den Nebennieren als frühe Adaptation, welche später von zunehmenden Einschränkungen der<br />
fetalen Körperbewegungen gefolgt wird.<br />
Veränderungen der Doppler-Blutflussmuster gehen Veränderungen des Bewegungsmusters und<br />
auch des CTGs voraus und stellen somit den frühesten und sensitivsten Prädiktor der fetalen Gefährdung<br />
dar, weshalb der Doppler die Uberwachungsmethode der Wahl bei <strong>IUWR</strong> darstellt.<br />
Im CTG ist die Abnahme der Variabilität ein<br />
frühes Zeichen, während in der Endphase<br />
der Dekompensation dopplersonographisch<br />
ein negativer enddiastolischer Fluss und im<br />
CTG ein silentes Muster mit angedeuteten<br />
späten Dezelerationen auftritt.<br />
Das Zeitintervall von Beginn der Zentralisierung des fetalen Kreislaufs bis zur präterminalen Phase<br />
der Dekompensation - welche eine rasche Beendigung der Schwangerschaft notwendig macht -<br />
variieren individuell beträchtlich und hängen auch vom Gestationsalter ab. Je frühzeitiger in der<br />
Schwangerschaft pathologische Flussveränderungen auftreten, desto grösser ist das Zeitintervall<br />
bis zur Dekompensation.<br />
Bei einem GA >32 SSW und entsprechender Dopplerpathologie ist die Schwangerschaft zu beenden,<br />
bei Präeklampsie ist diese Grenze bei 28 SSW anzusetzen. Bei zu geringem Schwangerschaftsalter<br />
oder Notwendigkeit einer Lungenreifungsinduktion kann die Zusatzinformation aus<br />
Hebammenschule am KSSG Dr. P. Böhi 20.1.2002
<strong>Intrauterine</strong> <strong>Wachstumsretardierung</strong><br />
Seite 12<br />
dem venösen Doppler hinzugezogen werden, um den zeitlichen Spielraum bzw. das Vorliegen einer<br />
Hypoxie und Azidose abzuschätzen.<br />
Bei schlechter Prognose ist eine Chromosomenanalyse (Plazentabiopsie) notwendig, um das Procedere<br />
festlegen zu können.<br />
In der Regel werden diese Schwangerschaften per Kaiserschnitt beendet, da der Wehenstress vom<br />
Kind nicht toleriert wird bzw. rasches Handeln notwendig ist. In ausgewählten Fällen kann auch<br />
eine vaginale Geburt stattfinden.<br />
7. Langzeitentwicklung<br />
Nebst den akuten Problemen der perinatalen Phase bei <strong>IUWR</strong> ist die spätere Entwicklung des Kindes<br />
von grösstem Interesse. Besonders folgenschwer sind neuromotorische Bewegungsstörungen<br />
(Zerebralparese), welche gehäuft mit <strong>IUWR</strong> assoziiert sind. Im Kindes- und Adoleszentenalter manifestieren<br />
sich vermehrt Verzögerungen der sprachlichen Entwicklung, Lernschwierigkeiten sowie<br />
Verhaltensstörungen.<br />
Viele Kinder mit <strong>IUWR</strong> zeigen auch im Kindes- und Adoleszentenalter einen Gewichts- und Grössenrückstand.<br />
Es zeigen sich immer mehr Zusammenhänge zwischen einer Pathologie des intrauterinen Wachstums<br />
und der Morbidität im Erwachsenenalter wie Hypertonie, Herz-Kreislauf-Erkrankungen, Hyperlipidämie<br />
und Diabetes mellitus Typ II.<br />
Hebammenschule am KSSG Dr. P. Böhi 20.1.2002