Klasse 9 - Schiller - Gymnasium Witten
Klasse 9 - Schiller - Gymnasium Witten
Klasse 9 - Schiller - Gymnasium Witten
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
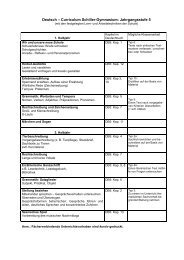
- Vergleich mit einer schwachen Säure<br />
(z.B. Essigsäure) um Reaktivitätsunterschiede<br />
aufzuzeigen<br />
Übertragung der Eigenschaften der exemplarisch<br />
gewählten (Magen)Säure auf weitere<br />
Säuren:<br />
- Um welche Restanionen (Säurerestionen)<br />
handelt es sich?<br />
- Struktur der Essigsäure, Schwefelsäure,<br />
Phosphorsäure als Beispiel für Säuren,<br />
die mehrere Protonen enthalten<br />
können.<br />
Begriff der Konzentration<br />
sowie Definition des pH-Wertes als Maß für<br />
die H + -Ionen-Konzentration, Veranschaulichung<br />
z.B. an Hand von Verdünnungsreihen<br />
Das Phänomen des Sodbrennens und die<br />
Wirkungsweise von Antazida als Übergang zu<br />
den Basen):<br />
- Welche Stoffe sind in Antazida enthalten<br />
(z.B. Beipackzettel von Rennie® ,<br />
CR I/II. 6<br />
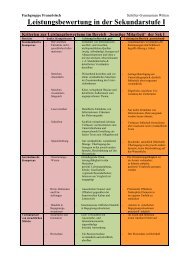
chemische Reaktionen zum Nachweis chemischer Stoffe<br />
benutzen (Knallgasprobe, Kalkwasserprobe).<br />
CR II.4<br />
Möglichkeiten der Steuerung chemischer Reaktionen durch<br />
Variation von Reaktionsbedingungen beschreiben.<br />
M II.4<br />
Zusammensetzung und Strukturen verschiedener Stoffe<br />
mit Hilfe von Formelschreibweisen darstellen (Summen-/<br />
Strukturformeln, (Isomere)).<br />
M II.5 a<br />
Kräfte zwischen Molekülen und Ionen beschreiben und<br />
erklären.<br />
M II.6<br />
den Zusammenhang zwischen Stoffeigenschaften und<br />
Bindungsverhältnissen (Ionenbindung, Elektronpaarbindung)<br />
erklären<br />
CR.II.5<br />
Stoffe durch Formeln und Reaktionen durch Reaktionsgleichungen<br />
beschreiben und dabei in quantitativen Aussagen<br />
die Stoffmenge benutzen (und einfache stöchiometrische<br />
Berechnungen durchführen)<br />
CR II.9 b<br />
die alkalische Reaktion von Lösungen auf das Vorhandensein<br />
von Hydroxidionen zurückführen.<br />
CR II.9 c<br />
den Austausch von Protonen als Donator-Akzeptor-Prinzip<br />
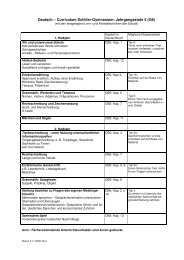
Stärke von Säuren<br />
Ionen in sauren Lösungen:<br />
Säurerest-Ion<br />
Schwefelsäure/ Phosphorsäure<br />
einprotonig / mehrprotonig<br />
Lernerfolgskontrolle: z.B.<br />
- Steckbrief von Säuren<br />
erstellen<br />
- Schriftliche Übung<br />
zur Dissoziation<br />
pH-Wert-Definition<br />
Indikatorenverdünnungsreihe<br />
Neutralisation<br />
Base<br />
6