ORGANISCHE CHEMIE
ORGANISCHE CHEMIE
ORGANISCHE CHEMIE
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
NTB Druckdatum: 31.03.13 MWC I<br />
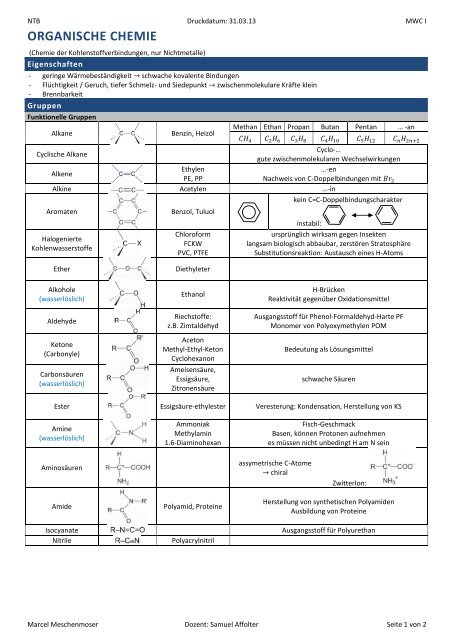
<strong>ORGANISCHE</strong> <strong>CHEMIE</strong><br />
(Chemie der Kohlenstoffverbindungen, nur Nichtmetalle)<br />
Eigenschaften<br />
- geringe Wärmebeständigkeit schwache kovalente Bindungen<br />
- Flüchtigkeit / Geruch, tiefer Schmelz- und Siedepunkt zwischenmolekulare Kräfte klein<br />
- Brennbarkeit<br />
Gruppen<br />
Funktionelle Gruppen<br />
Alkane<br />
Benzin, Heizöl<br />
Methan Ethan Propan Butan Pentan … -an<br />
Cyclische Alkane<br />
Cyclo-…<br />
gute zwischenmolekularen Wechselwirkungen<br />
Alkene<br />
Ethylen<br />
…-en<br />
PE, PP<br />
Nachweis von C-Doppelbindungen mit<br />
Alkine Acetylen …-in<br />
kein C=C-Doppelbindungscharakter<br />
Aromaten<br />
Halogenierte<br />
Kohlenwasserstoffe<br />
Benzol, Tuluol<br />
Chloroform<br />
FCKW<br />
PVC, PTFE<br />
instabil:<br />
ursprünglich wirksam gegen Insekten<br />
langsam biologisch abbaubar, zerstören Stratosphäre<br />
Substitutionsreaktion: Austausch eines H-Atoms<br />
Ether<br />
Alkohole<br />
(wasserlöslich)<br />
Aldehyde<br />
Ketone<br />
(Carbonyle)<br />
Carbonsäuren<br />
(wasserlöslich)<br />
Diethyleter<br />
Ethanol<br />
Riechstoffe:<br />
z.B. Zimtaldehyd<br />
Aceton<br />
Methyl-Ethyl-Keton<br />
Cyclohexanon<br />
Ameisensäure,<br />
Essigsäure,<br />
Zitronensäure<br />
H-Brücken<br />
Reaktivität gegenüber Oxidationsmittel<br />
Ausgangsstoff für Phenol-Formaldehyd-Harte PF<br />
Monomer von Polyoxymethylen POM<br />
Bedeutung als Lösungsmittel<br />
schwache Säuren<br />
Ester Essigsäure-ethylester Veresterung: Kondensation, Herstellung von KS<br />
Amine<br />
(wasserlöslich)<br />
Ammoniak<br />
Methylamin<br />
1.6-Diaminohexan<br />
Fisch-Geschmack<br />
Basen, können Protonen aufnehmen<br />
es müssen nicht unbedingt H am N sein<br />
Aminosäuren<br />
assymetrische C-Atome<br />
chiral<br />
ZwitterIon:<br />
Amide<br />
Isocyanate<br />
Nitrile<br />
Polyamid, Proteine<br />
Polyacrylnitril<br />
Herstellung von synthetischen Polyamiden<br />
Ausbildung von Proteine<br />
Ausgangsstoff für Polyurethan<br />
Marcel Meschenmoser Dozent: Samuel Affolter Seite 1 von 2
NTB Druckdatum: 31.03.13 MWC I<br />
Modelle<br />
Molekülformel<br />
Summenformel<br />
Isomere<br />
Konformations-Isomere<br />
Konstitutionsformel<br />
Strukturformel<br />
Valenzstrichformel<br />
Konstitutions-Isomere<br />
1-Buten<br />
H H H<br />
C C H<br />
H C C<br />
Sesselform<br />
H H H<br />
2-Buten<br />
Wanneform<br />
H H H<br />
H C C<br />
C C H<br />
H H H<br />
Chiralität (optische Aktivität)<br />
=Molekül, das mit seinem Spiegelbild nicht zur Deckung gebracht werden kann.<br />
C-Atom mit 4 unterschiedlichen Substitutionen<br />
H<br />
H<br />
C<br />
H<br />
H<br />
C<br />
H<br />
H<br />
C<br />
H<br />
H<br />
C<br />
H<br />
H<br />
Strukturformel räumlich<br />
Keilstrichformel<br />
H H H H<br />
H C C<br />
C C H<br />
H H<br />
H H<br />
Konfigurations-Isomere<br />
cis-trans Isomere<br />
cis-2-Buten<br />
trans-2-Buten<br />
Kurzschreibweise<br />
C als Punkt<br />
ohne H<br />
Reaktionstypen<br />
Addition<br />
Substitution<br />
Elimination<br />
Kondensation<br />
2 Stoffe reagieren zu einem neuen Stoff<br />
Austausch eines Substituenten<br />
Abspaltung eines Moleküls<br />
2 Stoffe reagieren unter Bildung eines leichtflüssigen<br />
Stoffes, meist Wasser<br />
Marcel Meschenmoser Dozent: Samuel Affolter Seite 2 von 2