Thalidomid (α-Phthalimidoglutarimid) ist der Wirkstoff des Schlaf ...
Thalidomid (α-Phthalimidoglutarimid) ist der Wirkstoff des Schlaf ...
Thalidomid (α-Phthalimidoglutarimid) ist der Wirkstoff des Schlaf ...
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
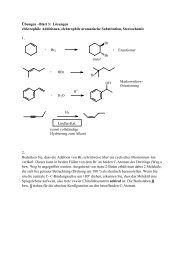
Bei <strong>Thalidomid</strong> handelt es sich um eine stereochemisch aktive Verbindung, die als (R)- und<br />
(S)-Enantiomer enantiomerenrein hergestellt werden kann. Die Verbindung wurde als<br />
Racemat verkauft und führte zu schweren Fehlbildungen am ungeborenen Leben. Man<br />
vermutete zunächst eine teratogene Wirkung <strong>der</strong> (S)-Verbindung. Da jedoch beide<br />
Enantiomere im Körper nach wenigen Stunden racemisieren, wenn auch unvollständig, lässt<br />
sich keinem <strong>der</strong> Enantiomere eine teratogene bzw. beruhigende Wirkung zuschreiben. Dabei<br />
wandeln sich die Enantiomere ineinan<strong>der</strong> um, und zwar unabhängig davon, ob reines R- o<strong>der</strong><br />
S-Enantiomer verabreicht wird; es stellt sich ein R/S-Verhältnis von ca. 1:1,7 ein. Die<br />
Geschichte vom „guten“ und „bösen“ <strong>Thalidomid</strong>-Enantiomer hat jedoch noch immer sehr<br />
viele Anhänger und <strong>ist</strong> in vielen renommierten Lehrbüchern und Journalen zu finden. Sogar<br />
das Nobel-Komitee macht davor nicht Halt. [2] Es gibt zwar Hinweise darauf, dass bei<br />
ähnlichen Verbindungen das (S)-Enantiomer dennoch das wirksamere, d. h. das<br />
fruchtschädigende Enantiomer sein könnte, das in das Immunsystem eingreift. Aber selbst<br />
wenn man wüsste, dass nur eines <strong>der</strong> Enantiomere schädlich <strong>ist</strong>, würde das wenig nützen, da<br />
im Körper durch die Racemisierung immer beide Formen präsent sind<br />
<strong>Thalidomid</strong> blockiert den Wachstumsfaktor VEGF (vascular endothelial growth factor),<br />
wodurch es zu einer fehlenden Vaskularisierung (Blutgefäßbildung) in den Extremitäten <strong>des</strong><br />
Embryos kommt. Dies führt zu einer verkürzten o<strong>der</strong> fehlenden Anlage <strong>der</strong> Arme und Beine.<br />
Obwohl <strong>der</strong> Stolberger Herstellerfirma 1961 bereits 1.600 Warnungen über beobachtete<br />
Fehlbildungen an Neugeborenen vorlagen, wurde Contergan nach wie vor vertrieben. Zu<br />
jenem Zeitpunkt hatte es 46 % <strong>des</strong> Marktes für barbituratfreie <strong>Schlaf</strong>mittel erobert. In <strong>der</strong> Zeit<br />
nach 1961, nachdem Contergan vom Markt zurückgezogen wurde, wurde es weiterhin an<br />
verschiedenen Tierarten getestet. Die Resultate waren größtenteils negativ o<strong>der</strong> zeigten keine<br />
vergleichbaren Fehlbildungen am Nachwuchs. Obwohl Ratten und Mäuse durch die Substanz<br />
sediert wurden (<strong>der</strong> Grund, weshalb man überhaupt auf die sedierende Wirkung <strong>des</strong><br />
<strong>Thalidomid</strong> gekommen war, lag darin, dass bei einem Versuch, bei dem eine völlig an<strong>der</strong>e<br />
Wirkung <strong>des</strong> <strong>Wirkstoff</strong>es untersucht werden sollte, die Nagetiere, die <strong>Thalidomid</strong> erhielten,<br />
wi<strong>der</strong> Erwarten einschliefen), konnte auch in klassischen Tierversuchen mit hoher<br />
Konzentration keine fruchtschädigende Wirkung <strong>des</strong> Präparates nachgewiesen werden. Erst<br />
viel später nach <strong>der</strong> Contergankatastrophe zeigten sich bei einer bestimmten Kaninchenart,<br />
die als Versuchstier vor Markteinführung überhaupt nicht als Tiermodell üblich war, eine<br />
teratogene Wirkung. Diese dadurch nachgewiesene Artspezifität einer teratogenen Wirkung<br />
war bis dato unbekannt und stellt bis heute ein Dilemma bei <strong>der</strong> Übertragbarkeit von<br />
Tierversuchsergebnissen auf den Menschen dar.