Analytische HPLC
Analytische HPLC
Analytische HPLC
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
Probenvorbereitung<br />
Informationen zu unseren Produkten erhalten Sie bei Ihrem lokalen VWR-Ansprechpartner,<br />
senden Sie uns eine E-Mail an:<br />
chromjournal@eu.vwr.com<br />
oder besuchen Sie unsere Website www.vwr.com<br />
Flüssig-Flüssig Extraktion in seiner effektivsten Form:<br />
Probenvorbereitung mittels EXtrelut ® NT<br />
EXtrelut ® NT1 1.15094.0001<br />
EXtrelut ® NT3 1.15095.0001<br />
EXtrelut ® NT20 1.15096.0001<br />
EXtrelut ® NT Säulen sind mit einer chemisch<br />
inerten Festphase (Kieselgur) gefüllt. Das Prinzip<br />
der Anwendung ist folgende: die wässrige<br />
Probenlösung wird auf die trockene Säule<br />
aufgetragen und verteilt sich über die<br />
Oberfläche des Kieselgurs als dünner Film.<br />
Eluiert wird mit Hilfe eines organischen<br />
Lösungsmittels, das mit Wasser nicht mischbar<br />
ist. Während die organische Phase durch die<br />
Säule sickert, werden lipohile Substanzen aus der<br />
wässerigen Phase extrahiert. Die im Eluat gelösten<br />
Substanzen können direkt oder nach Eindampfen<br />
des Lösungsmittels analysiert werden.<br />
EXtrelut ® NT kann für die routinemäßig<br />
durchgeführte flüssig-flüssig Extraktion eingesetzt<br />
werden und gewährleistet:<br />
• einen sparsamen Umgang mit Lösungsmittel,<br />
Probenmaterial und Zeit<br />
• eine einfache und reproduzierbare<br />
Durchführung der Extraktion<br />
• hohe Ausbeuten und reine, emulsionsfreie Eluate<br />
Anwendungsbeispiel<br />
Schnelle und effiziente Extraktion von<br />
krebserregenden Aminen mittels<br />
EXtrelut ® NT<br />
Das Interesse an heterozyklischen, aromatischen<br />
Aminen hat in den vergangenen Jahren durch die<br />
sich häufenden Hinweise auf ihre potentiell<br />
krebserregenden Eigenschaften stark<br />
zugenommen. Diese Amine werden in vielen<br />
Probenmaterialien wie gebratenes Fleisch, Fisch<br />
und anderen Nahrungsmitteln sowie als Derivate<br />
in Textilien nachgewiesen. Der Nachweis und die<br />
Analyse lipophiler Substanzen in solchen<br />
komplexen Probenmaterialien bedarf einer<br />
effektiven Probenvorbereitung. Im<br />
Anwendungsbeispiel wird dies für Azo-Farbstoffe<br />
in Textilien gezeigt.<br />
Probenvorbereitung<br />
2 g des Textilgewebes wird mit 25 mL 1N NaOH<br />
für 30 Minuten gekocht. Nach Zugabe von 1 g<br />
Na 2 S 2 O 4 wird die Probe für weitere 30 Minuten<br />
gekocht. Nach Abkühlen werden 20 mL der<br />
wässrigen Lösung auf eine EXtrelut ® NT20 Säule<br />
aufgetragen. Weitere 15 Minuten reichen für eine<br />
homogene Verteilung der wässrigen Probe auf<br />
der Oberfläche des Säulenmaterials aus. Der<br />
schrittweise Auftrag von 40 mL Ethylacetat<br />
eluiert die lipophilen Amine der Probe. Das Eluat<br />
wird auf 0,5 mL Volumen eingeengt, in 15 mL<br />
Acetonitril aufgenommen und nochmals auf 0,5<br />
mL eingeengt. Diese Probe wird mit 1 ml<br />
Acetonitril verdünnt und chromatographisch<br />
analysiert.<br />
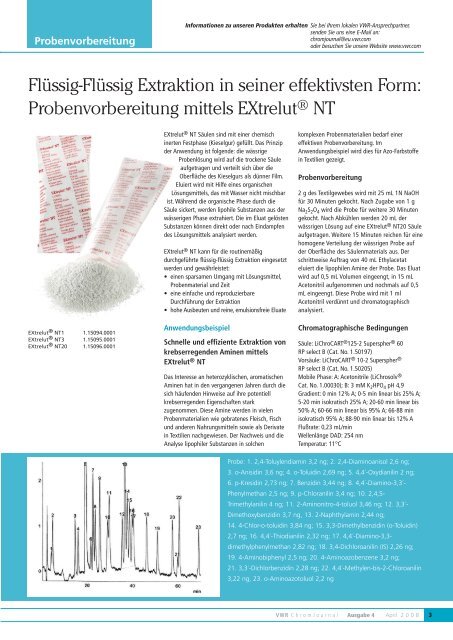
Chromatographische Bedingungen<br />
Säule: LiChroCART ® 125-2 Superspher ® 60<br />
RP select B (Cat. No. 1.50197)<br />
Vorsäule: LiChroCART ® 10-2 Superspher ®<br />
RP select B (Cat. No. 1.50205)<br />
Mobile Phase: A: Acetonitrile (LiChrosolv ®<br />
Cat. No. 1.00030); B: 3 mM K 2 HPO 4 pH 4,9<br />
Gradient: 0 min 12% A; 0-5 min linear bis 25% A;<br />
5-20 min isokratisch 25% A; 20-60 min linear bis<br />
50% A; 60-66 min linear bis 95% A; 66-88 min<br />
isokratisch 95% A; 88-90 min linear bis 12% A<br />
Flußrate: 0,23 mL/min<br />
Wellenlänge DAD: 254 nm<br />
Temperatur: 11°C<br />
Probe: 1. 2,4-Toluylendiamin 3,2 ng; 2. 2,4-Diaminoanisol 2,6 ng;<br />
3. o-Anisidin 3,6 ng; 4. o-Toluidin 2,69 ng; 5. 4,4´-Oxydianilin 2 ng;<br />
6. p-Kresidin 2,73 ng; 7. Benzidin 3,44 ng; 8. 4,4´-Diamino-3,3´-<br />
Phenylmethan 2,5 ng; 9. p-Chloranilin 3,4 ng; 10. 2,4,5-<br />
Trimethylanilin 4 ng; 11. 2-Aminonitro-4-toluol 3,46 ng; 12. 3,3´-<br />
Dimethoxybenzidin 3,7 ng, 13. 2-Naphthylamin 2,44 ng;<br />
14. 4-Chlor-o-toluidin 3,84 ng; 15. 3,3-Dimethylbenzidin (o-Toluidin)<br />
2,7 ng; 16. 4,4´-Thiodianilin 2,32 ng; 17. 4,4´-Diamino-3,3-<br />
dimethylphenylmethan 2,82 ng; 18. 3,4-Dichloroanilin (IS) 2,26 ng;<br />
19. 4-Aminobiphenyl 2,5 ng; 20. 4-Aminoazobenzene 3,2 ng;<br />
21. 3,3´-Dichlorbenzidin 2,28 ng; 22. 4,4´-Methylen-bis-2-Chloroanilin<br />
3,22 ng, 23. o-Aminoazotoluol 2,2 ng<br />
VWR ChromJournal Ausgabe 4 April 2008 3