06 Fortschritte im Erregernachweis
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
<strong>Erregernachweis</strong><br />
<strong>Fortschritte</strong> <strong>im</strong> <strong>Erregernachweis</strong>?<br />
Was kulturunabhängige Verfahren dem Kliniker bringen<br />
Mit mehr als 250.000 Erkrankungsfällen<br />
pro Jahr und einer Sterblichkeitsrate<br />
von ca. 25% zählt die Sepsis zu den<br />
häufigsten Todesursachen in Deutschland.<br />
Die hohe Letalität wird zum einen<br />
durch das größtenteils schwer kranke<br />
Patientenkollektiv bedingt, andererseits<br />
führen bereits geringe Verzögerungen<br />
bei der Therapieeinleitung oder die falsche<br />
Antibiotikawahl zu einer deutlichen<br />
Prognoseverschlechterung bei einer<br />
Sepsis.<br />
Leider liegt zum Zeitpunkt der Diagnosestellung<br />
für gewöhnlich kein mikrobiologischer<br />
Befund mit <strong>Erregernachweis</strong><br />
und Resistenztestung vor, weshalb<br />
die antibiotische Therapie zunächst empirisch<br />
geführt werden muss. Die Idealvorstellung<br />
einer schnellen mikrobiologischen<br />
Diagnostik, die womöglich direkt<br />
am Patientenbett stattfindet und<br />
innerhalb von wenigen Minuten einen<br />
endgültigen Befund erbringt, könnte <strong>im</strong><br />
Fall einer Sepsis wesentlich zum Therapieerfolg<br />
beitragen, lässt sich derzeit<br />
aber noch nicht verwirklichen.<br />
Im Gegensatz dazu erscheint die konventionelle,<br />
kulturabhängige Blutkulturdiagnostik,<br />
die für den <strong>Erregernachweis</strong><br />
und eine erste, orientierende Resistenztestung<br />
mindestens sechzehn<br />
bis vierundzwanzig Stunden benötigt,<br />
Transportzeiten in das Labor nicht eingerechnet,<br />
viel zu langsam. Neue kulturunabhängige<br />
Verfahren werden daher<br />
als vielversprechende, schnelle Alternative<br />
zur vermeintlich altmodischen, kulturabhängigen<br />
Diagnostik gehandelt.<br />
Wie läuft die konventionelle<br />
Blutkulturdiagnostik ab?<br />
Der Zeitaufwand für die kulturbasierte<br />
Erregerdiagnostik ergibt sich aus den<br />
Abb. 1: Bebrütung der Blutkulturflaschen<br />
langen Bebrütungszeiten. Zunächst<br />
werden die be<strong>im</strong>pften Blutkulturflaschen<br />
in speziellen Inkubationsautomaten<br />
bebrütet (Abbildung 1), die bakterielles<br />
Wachstum automatisch registrieren<br />
und anzeigen können. Die benötigte<br />
Bebrütungsdauer hängt hierbei vor allem<br />
von der einge<strong>im</strong>pften Ke<strong>im</strong>zahl,<br />
also der Erregerkonzentration <strong>im</strong> Patientenblut,<br />
ab und beträgt <strong>im</strong> Fall einer<br />
schweren Sepsis üblicherweise weniger<br />
als zehn, eher zwei bis sechs Stunden.<br />
Nach der initialen Bebrütung in Blutkulturflaschen<br />
müssen die positiven<br />
Blutkulturen auf feste Nährmedien ausgestrichen<br />
und für weitere zwölf Stunden<br />
inkubiert werden (Abbildung 2).<br />
So können letztlich Reinkulturen gewonnen<br />
werden, die für die abschließenden<br />
Tests zur Erregeridentifizierung<br />
und Resistenztestung verwendet<br />
werden können.<br />
Um die Diagnose von Blutstrominfektionen<br />
zu beschleunigen, werden seit der<br />
Jahrtausendwende zunehmend neue,<br />
kulturunabhängige Methoden, wie die<br />
Massenspektrometrie oder verschiedene<br />
molekularbiologische Verfahren, in<br />
der Sepsisdiagnostik eingeführt und erprobt<br />
(Abbildung 4). Die Vorteile einer<br />
schnellen Diagnose liegen auf der<br />
Hand: Die Therapie kann zeitnah gezielt<br />
auf besondere Resistenzen ausgerichtet<br />
werden, während gleichzeitig<br />
der Verbrauch von Reserveantibiotika<br />
vermindert und die Entwicklung neuer<br />
Antibiotikaresistenzen verhindert werden<br />
können. Die Einsatzmöglichkeiten<br />
der einzelnen Methoden sowie ihre<br />
Vor- und Nachteile sollen <strong>im</strong> Folgenden<br />
vorgestellt werden.<br />
Molekularbiologische Verfahren<br />
Kommerzielle molekularbiologische Systeme<br />
sind mittlerweile zu einem festen<br />
Bestandteil des mikrobiologisch-diagnostischen<br />
Labors geworden. Die Syste-<br />
Nr. 4, 2017 25
<strong>Erregernachweis</strong><br />
Abb. 2: Ausstreichen der Blutkulturflaschen auf Agarplatten<br />
Abb. 3: Automatisierung der Kulturanlage<br />
me sind in den letzten zwei Jahrzehnten<br />
wesentlich kostengünstiger und benutzerfreundlicher<br />
geworden, sodass einige<br />
Hersteller bereits Geräte zur pointof-care-Diagnostik<br />
anbieten können.<br />
Nicht nur die auf klassischen PCR-Verfahren<br />
basierenden Systeme konnten<br />
opt<strong>im</strong>iert werden, auch neue Methoden<br />
wie die isothermale Amplifikation oder<br />
die Fluoreszenz-in-situ-Hybridisierung<br />
ermöglichen inzwischen eine schnelle<br />
und einfache Diagnostik. Sogenannte<br />
Multiplex-Systeme erlauben die s<strong>im</strong>ultane<br />
Suche nach mehreren Erregern<br />
und Resistenzgenen in einem einzelnen<br />
Untersuchungsgang.<br />
Grundsätzlich können die Verfahren<br />
zur Untersuchung von Nativblut, bebrüteter<br />
Blutkulturen oder auch zur<br />
Analyse von bakteriellen Einzelkolonien<br />
nach Anzucht eingesetzt werden.<br />
Aufgrund der kurzen Untersuchungsdauer<br />
von Minuten bis wenigen Stunden<br />
wird die Diagnostik erheblich beschleunigt.<br />
Noch sind es vor allem die<br />
vergleichsweise hohen Kosten pro Untersuchungsgang,<br />
die einem häufigeren<br />
Einsatz <strong>im</strong> Weg stehen. Zukünftig ist<br />
jedoch ein weiterer Preisrückgang zu erwarten,<br />
sodass bereits diskutiert wird,<br />
ob molekularbiologische Methoden die<br />
konventionelle Blutkulturdiagnostik in<br />
Zukunft gänzlich ersetzen können.<br />
Um jedoch hier keinem Trugschluss zu<br />
unterliegen, müssen sich klinisch und<br />
diagnostisch tätige Ärzte der Grenzen<br />
dieser molekularbiologischer Verfahren<br />
bewusst sein. Im Gegensatz zur klassischen<br />
Blutkulturdiagnostik mit der<br />
prinzipiell alle kultivierbaren Erreger<br />
26<br />
nachgewiesen werden können, werden<br />
durch molekularbiologische Untersuchung<br />
nur zuvor definierte Erreger und<br />
Resistenzgene erfasst. Die Wahrscheinlichkeit<br />
falsch negativer Befunde bleibt<br />
daher groß und eine Ausschlussdiagnostik<br />
ist nicht möglich. Außerdem fehlen<br />
be<strong>im</strong> alleinigen Nukleinsäurenachweis<br />
wichtige Begleitparameter der konventionellen<br />
Blutkulturdiagnostik, wie die<br />
Bebrütungs dauer (t<strong>im</strong>e-to-positivity)<br />
oder die Anzahl positiver Blutkulturen,<br />
die helfen können, die klinische Relevanz<br />
des Befundes als tatsächliche Blutstrominfektion<br />
oder wahrscheinliche Hautkontamination<br />
einzuordnen.<br />
Darüber hinaus kann be<strong>im</strong> Nachweis<br />
mehrerer Erreger ein zusätzlich gefundenes<br />
Resistenzgen nicht sicher einem<br />
best<strong>im</strong>mten Ke<strong>im</strong> zugeordnet werden.<br />
So kann zum Beispiel bei gleichzeitigem<br />
Vorliegen von Staphylococcus aureus und<br />
Methicillin-resistenten Koagulase-negativen<br />
Staphylokokken nicht zwischen<br />
einer meldepflichtigen MRSA-Blutstrominfektion<br />
und einem MSSA-Befund<br />
mit zusätzlicher Hautkontamination<br />
unterschieden werden.<br />
Neue molekularbiologische Hochdurchsatzverfahren,<br />
die unter dem<br />
Schlagwort next-generation-sequencing<br />
(NGS) zusammengefasst werden, stellen<br />
ein vielversprechendes Werkzeug<br />
für die mikrobiologische Diagnostik<br />
der Zukunft dar. Diese Methoden erlauben<br />
es in wenigen Stunden die Basenpaarabfolge<br />
eines kompletten Bakteriengenoms<br />
zu beschreiben.<br />
Bioinformatische Analysen erlauben<br />
anschließend die Erregeridentifizierung<br />
oder die Best<strong>im</strong>mung von Resistenzgenen.<br />
So handelt es sich dabei um<br />
ein universelles Verfahren – das heißt,<br />
es können theoretisch sämtliche bakteriellen<br />
und viralen Erreger sowie Pilze<br />
mit einem Untersuchungsschritt ermittelt<br />
werden.<br />
Eine erste Durchführbarkeitsstudie bei<br />
wenigen Patienten konnte bereits zeigen,<br />
dass die Methode in der Diagnostik<br />
von Blutstrominfektionen funktionieren<br />
kann und dabei sowohl quantitative<br />
Aussagen zur vermeintlichen Erregerlast<br />
als auch Aussagen zu Antibiotikaresistenzen<br />
erlaubt (Grumaz; Genome<br />
Med 2016; 8:73). Bisher bleibt der Ansatz<br />
jedoch rein exper<strong>im</strong>entell und es<br />
fehlen aussagekräftige, klinische Studien,<br />
die den Einsatz der Systeme in der<br />
Routinediagnostik evaluieren.<br />
Massenspektrometrie – MALDI-TOF<br />
Neben molekularbiologischen Methoden<br />
hat in den letzten zwei Jahrzehnten<br />
vor allem die Massenspektrometrie,<br />
genauer die Matrix-assistierte Laser-<br />
Desorption-Ionisierung mit Flugzeitanalyse<br />
(engl. t<strong>im</strong>e of flight) oder kurz<br />
MALDI-TOF, die mikrobiologische<br />
Diagnostik revolutioniert. Aktuell werden<br />
mit diesem Verfahren Erreger sehr<br />
rasch identifiziert, jedoch keine Resistenztestungen<br />
durchgeführt.<br />
Das Verfahren beruht auf der Ionisierung<br />
bakterieller Proteine mittels Laserbestrahlung<br />
und Beschleunigung der ionisierten<br />
Partikel in einem elektrischen<br />
Feld. Abhängig von Ladung und molekularer<br />
Masse ergeben sich charakte-<br />
Nr. 4, 2017
<strong>Erregernachweis</strong><br />
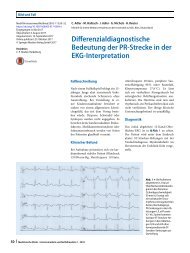
20<br />
15<br />
10<br />
5<br />
0<br />
1990 1995 2000 2005 2010 2015<br />
Abb. 4: Anzahl der Publikationen zu den Stichworten „rapid detection“ und „blood culture“<br />
in der Datenbank PubMed 1990-2016<br />
ristische Flugzeitspektren, die mit einer<br />
Datenbank abgeglichen werden,<br />
die eine Vielzahl von Erregern enthält.<br />
Diese Methode eignet sich zuverlässig<br />
zur Erregeridentifizierung und hat seit<br />
ihrer Einführung zeitaufwendige biochemische<br />
Verfahren, wie die „bunte<br />
Reihe“, weitestgehend aus der Routinediagnostik<br />
verdrängt. Die Stärke des<br />
MALDI-TOF-Verfahrens liegt in den<br />
kurzen Bedienungs- und Analysezeiten<br />
von nur wenigen Minuten und dem geringen<br />
Kostenaufwand pro Probe.<br />
Standardmäßig kommt das Verfahren<br />
bisher zur Identifizierung von auf Festmedien<br />
angezüchteten Bakterienkolonien<br />
zum Einsatz. Mit entsprechenden<br />
Aufarbeitungsprotokollen kann aber<br />
auch eine Untersuchung direkt aus zuvor<br />
bebrüteten Blutkulturen erfolgen.<br />
Dieser Untersuchungsansatz funktioniert<br />
bereits stabil und ermöglicht in<br />
den meisten Fällen die Ke<strong>im</strong>detektion,<br />
noch bevor Reinkulturen des Erregers<br />
vorliegen.<br />
Zur Detektion von Antibiotikaresistenzen<br />
wird die Massenspektrometrie<br />
bisher nur exper<strong>im</strong>entell angewandt.<br />
Zwar wurde bereits beschrieben, wie best<strong>im</strong>mte<br />
Einzelresistenzen direkt oder<br />
indirekt mittels MALDI-TOF nachgewiesen<br />
werden können, bisher ist aber<br />
nicht absehbar, dass sich hieraus eine<br />
universell einsetzbare Methode für die<br />
Routinediagnostik ergibt, die der kulturbasierten<br />
Resistenztestung ebenbürtig<br />
ist. Nachteile der Massenspektrometrie<br />
sind die aufwendige technische<br />
Installation sowie die hohen Anschaffungskosten,<br />
die den wirtschaftlichen<br />
Einsatz eines MALDI-TOF-Systems<br />
nur in einem Großlabor mit entsprechend<br />
hohem Probenaufkommen ermöglichen<br />
und keine point-of-care-Diagnostik<br />
zulassen.<br />
Die Möglichkeit, die Massenspektrometrie<br />
mit Nukleinsäureamplifikationsverfahren<br />
zu kombinieren, soll an dieser<br />
Stelle nicht unerwähnt bleiben. Bei diesem<br />
Vorgehen werden universelle bakterielle<br />
Pr<strong>im</strong>er eingesetzt, um möglichst<br />
viele kurze Amplifikationsprodukte zu<br />
erhalten. Anschließend werden in einem<br />
zweiten Untersuchungsschritt die<br />
erzeugten Nukleinsäurestränge mittels<br />
Massenspektrometrie analysiert.<br />
Das Verfahren vereint die Vorteile beider<br />
Methoden, da es einerseits kulturunabhängig<br />
arbeitet, dabei aber ein<br />
wesentlich größeres Ke<strong>im</strong>spektrum<br />
erfassen kann als handelsübliche Multiplex-PCRs.<br />
Ein erstes kommerzielles<br />
System, das auf diesem Untersuchungsprinzip<br />
beruhte, war jedoch nicht zuletzt<br />
aufgrund der sehr hohen Anschaffungskosten<br />
sowie hoher Kosten pro Untersuchung<br />
wenig attraktiv und wurde bereits<br />
kurze Zeit nach seiner Einführung wieder<br />
in Europa vom Markt genommen.<br />
Der Stellenwert neuer Methoden<br />
in der Sepsisdiagnostik<br />
Nach wie vor stellt die kulturbasierte<br />
Erreger- und Resistenzdiagnostik in<br />
der Medizinischen Mikrobiologie den<br />
Goldstandard dar, an dem sich andere<br />
Methoden messen lassen müssen.<br />
Darüber hinaus konnte in der letzten<br />
Zeit die kulturabhängige Diagnostik<br />
durch neue Verfahren zur automatisierten<br />
Probenverarbeitung entscheidend<br />
verbessert und auch beschleunigt<br />
werden (Abbildung. 3). Die konventionelle<br />
Blutkultur ist daher aktuell das<br />
Mittel der Wahl zur kostengünstigen<br />
und universellen Diagnostik von Blutstrominfektionen.<br />
Die konventionelle Blutkulturdiagnostik<br />
konnte in der jüngsten Zeit durch<br />
Massenspektrometrie und molekularbiologische<br />
Verfahren sinnvoll ergänzt<br />
werden. Während die Massenspektrometrie<br />
bereits ein Routineverfahren<br />
darstellt, werden molekularbiologische<br />
Methoden aufgrund der vergleichsweise<br />
hohen Kosten bisher nur optional eingesetzt.<br />
Gerade molekularbiologische<br />
Verfahren können jedoch Abkürzungen<br />
innerhalb des diagnostischen Pfades<br />
ermöglichen und zeitnah eine erste<br />
Aussage zu wichtigen Erregern und<br />
Resistenzen erlauben.<br />
Der Einsatz kulturunabhängiger Methoden<br />
sollte stets eingebettet in die<br />
klassische Blutkulturdiagnostik <strong>im</strong> Rahmen<br />
einer Stufendiagnostik erfolgen.<br />
Ausschlaggebende Parameter, die dem<br />
Diagnostiker Anlass zum Einsatz neuer<br />
Methoden geben können, sind beispielsweise<br />
die t<strong>im</strong>e-to-positivity, die<br />
Anzahl positiver Blutkulturen oder auch<br />
der mikroskopische Befund. Wichtig<br />
für die Indikationsstellung sind vor allem<br />
aber klinische Informationen, weshalb<br />
die Kommunikation zwischen behandelnden<br />
Ärzten und dem diagnostischen<br />
Labor entscheidend ist. Nur so<br />
kann eine fokussierte, schnelle Diagnostik<br />
und die korrekte Befundinterpretation<br />
bei kritisch kranken Patienten gewährleistet<br />
werden.<br />
Interessenkonflikte: Keine<br />
Prof. Dr. Bettina Löffler<br />
Dr. Steffen Höring<br />
Institut für Med. Mikrobiologie<br />
Universitätsklinikum Jena<br />
bettina.loeffler@med.uni-jena.de<br />
Nr. 4, 2017 27