Módulo 4. Concepto de Exergía Introducción La importancia ... - C.I.E.
Módulo 4. Concepto de Exergía Introducción La importancia ... - C.I.E.
Módulo 4. Concepto de Exergía Introducción La importancia ... - C.I.E.
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
<strong>Módulo</strong> <strong>4.</strong> <strong>Concepto</strong> <strong>de</strong> <strong>Exergía</strong><br />
<strong>Introducción</strong><br />
<strong>La</strong> <strong>importancia</strong> <strong>de</strong>l <strong>de</strong>sarrollo <strong>de</strong> los sistemas térmicos que utilicen eficazmente<br />
los recursos energéticos, como el petróleo, la gasolina, el gas natural y el carbón,<br />
ha cobrado gran <strong>importancia</strong>, tanto por las razones <strong>de</strong> disminución <strong>de</strong> recursos,<br />
al ser los principales combustibles <strong>de</strong> fuentes no renovables, como sobre <strong>de</strong>l<br />
impacto que se causan sobre el medio ambiente al utilizarlos. <strong>La</strong> eficacia <strong>de</strong><br />
su uso, en un sistema específico, se <strong>de</strong>termina con los dos principios<br />
fundamentales <strong>de</strong> la Termodinámica.<br />
<strong>La</strong> energía que entra en un sistema con el combustible, electricidad flujos <strong>de</strong><br />
materia, y otros, está presente en los productos finales que produce el sistema y<br />
por cada subproducto que genera dicho sistema ya que la energía no se <strong>de</strong>struye,<br />
conforme al primer principio <strong>de</strong> la Termodinámica.<br />
Actualmente existe un gran interés para analizar <strong>de</strong> forma más cerrada los<br />
dispositivos <strong>de</strong> conversión <strong>de</strong> energía para <strong>de</strong>sarrollar nuevas técnicas que<br />
empleen mejor los recursos naturales actuales y mitiguen el impacto sobre el<br />
medio ambiente que ocasiona su uso.<br />
El objetivo <strong>de</strong> este módulo es examinar el <strong>de</strong>sempeño <strong>de</strong> dispositivos técnicos<br />
conforme a las dos leyes fundamentales <strong>de</strong> la Termodinámica, introduciendo el<br />
concepto <strong>de</strong> exergía o trabajo útil máximo que pue<strong>de</strong> obtenerse, conforme a la<br />
reversibilidad <strong>de</strong> los procesos y la forma en que las irreversibilida<strong>de</strong>s <strong>de</strong>struyen<br />
dicha exergía.<br />
Como es sabido, existen diversas formas <strong>de</strong> energía, cada una <strong>de</strong> ellas con<br />
características peculiares. En las aplicaciones técnicas <strong>de</strong> la energía es frecuente<br />
limitarse a la realización <strong>de</strong> balances energéticos, basados en el empleo <strong>de</strong>l<br />
Primer Principio <strong>de</strong> la Termodinámica, consi<strong>de</strong>rando como equivalentes todas<br />
las formas <strong>de</strong> energía. Ahora bien, la capacidad <strong>de</strong> obtención <strong>de</strong> trabajo útil a<br />
partir <strong>de</strong> una misma cantidad <strong>de</strong> energía <strong>de</strong>pen<strong>de</strong> en la forma en que ésta se<br />
presente.<br />
Aparece así la i<strong>de</strong>a <strong>de</strong> calidad <strong>de</strong> la energía, que pue<strong>de</strong> <strong>de</strong>finirse como la<br />
capacidad <strong>de</strong> originar una transformación. Consi<strong>de</strong>remos, por ejemplo, la<br />
capacidad <strong>de</strong> producción <strong>de</strong> un cierto efecto (calentar un local, comprimir un gas,<br />
hacer progresar una reacción endotérmica, ...) con una cantidad dada <strong>de</strong> energía.<br />
Con 100 J <strong>de</strong> energía calorífica disponible a 1000 k se pue<strong>de</strong> producir un efecto<br />
menor que con 100 J <strong>de</strong> energía eléctrica. Si el ambiente se encuentra, por
ejemplo, a 300 k, el efecto posible con 100 J disponibles a 400 k es mucho menor<br />
que a 1000 k.<br />
Si comparamos 1 KJ <strong>de</strong> electricidad generada por una planta <strong>de</strong> potencia,<br />
contra 1 KJ <strong>de</strong> energía <strong>de</strong> un flujo <strong>de</strong> agua en una planta <strong>de</strong> enfriamiento,<br />
claramente se ve que la electricidad tiene la mejor calidad, y no por<br />
casualidad, el mayor valor económico.<br />
Cuando se analiza termodinámicamente un proceso, es indispensable tener en<br />
consi<strong>de</strong>ración las diferencias en la calidad <strong>de</strong> la energía. Esta característica<br />
<strong>de</strong>pen<strong>de</strong> <strong>de</strong>l modo en que se almacena la forma <strong>de</strong> energía consi<strong>de</strong>rada. El<br />
almacenamiento pue<strong>de</strong> ser or<strong>de</strong>nado o <strong>de</strong>sor<strong>de</strong>nado (aleatorio) en mayor o menor<br />
grado. Dado que la entropía refleja el <strong>de</strong>sor<strong>de</strong>n <strong>de</strong> un sistema, es <strong>de</strong> esperar que<br />
sirva también para <strong>de</strong>terminar la medida en que se presenta una forma <strong>de</strong> energía<br />
or<strong>de</strong>nada y por lo tanto evalué la cantidad <strong>de</strong> energía utilizable que se pue<strong>de</strong><br />
obtener. Precisamente es éste el campo <strong>de</strong> acción <strong>de</strong>l Segundo Principio <strong>de</strong> la<br />
Termodinámica.<br />
<strong>La</strong> exergía es un parámetro que mi<strong>de</strong> la calidad <strong>de</strong> la energía. Este parámetro<br />
pue<strong>de</strong> emplearse para analizar la eficiencia energética <strong>de</strong> los procesos<br />
industriales. Con un análisis <strong>de</strong> exergía pue<strong>de</strong>n compararse diferentes<br />
alternativas para comprobar cuál tiene el mayor rendimiento energético. Sin<br />
embargo, <strong>de</strong>be quedar lo suficientemente claro que dichos análisis no<br />
proporcionan soluciones por sí mismos.<br />
Con lo que po<strong>de</strong>mos concluir que la exergía es el máximo trabajo útil que<br />
po<strong>de</strong>mos obtener <strong>de</strong> un flujo <strong>de</strong> energía dado, en cualquiera <strong>de</strong> sus formas que<br />
sea almacenado o transferido; pero también lo po<strong>de</strong>mos ver como la mínima<br />
energía necesaria que se requiera para obtener un producto final.<br />
<strong>4.</strong>1 Primera y Segunda Ley Combinadas<br />
Consi<strong>de</strong>rando el caso genérico <strong>de</strong> un volumen <strong>de</strong> control en el que se producen<br />
cualquier tipo <strong>de</strong> procesos físicos o químicos (sin consi<strong>de</strong>rar los nucleares), en el<br />
que existen varios flujos <strong>de</strong> materia entrando y saliendo <strong>de</strong>l sistema, transferencia<br />
<strong>de</strong> calor con varios reservorios a diferentes temperaturas y una producción <strong>de</strong> un<br />
trabajo útil. Consi<strong>de</strong>rando que en el intervalo tiempo elemental dt entra al sistema<br />
la masa dme por la entrada genérica e y sale la masa dms por la salida genérica s,<br />
entra el calor dQ a la temperatura genérica T y se el trabajo útil dWu.<br />
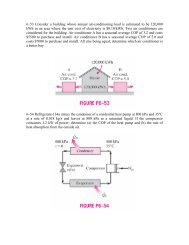
El diagrama <strong>de</strong> energías <strong>de</strong>l volumen <strong>de</strong> control se presenta en la Figura 1, en<br />
don<strong>de</strong> quedan representados todos los flujos <strong>de</strong> masa y energía conforme a la<br />
<strong>de</strong>scripción <strong>de</strong>l párrafo anterior.
e<br />
Para nuestro caso, como suce<strong>de</strong> en la gran mayoría <strong>de</strong> los procesos reales <strong>de</strong><br />
ingeniería, <strong>de</strong>spreciemos la energía cinética y potencial <strong>de</strong> las corrientes <strong>de</strong><br />
materias entrantes y salientes y consi<strong>de</strong>ramos estado estacionario.<br />
dme<br />
T0 T1 T2 Tn<br />
DQ0 DQ1 DQ2 dQn<br />
VOLUMEN DE<br />
CONTROL<br />
dWu<br />
Figura 1. Balance termodinámico <strong>de</strong> un volumen <strong>de</strong> control.<br />
El primer balance que formulamos es el <strong>de</strong> masa, <strong>de</strong> acuerdo con el principio <strong>de</strong><br />
conservación <strong>de</strong> masa, que al consi<strong>de</strong>rar estado estacionario no existe<br />
acumulación <strong>de</strong> masa en el sistema.<br />
Σdme = Σdms BALANCE DE MASA (1)<br />
El balance <strong>de</strong> Primera Ley o balance <strong>de</strong> energía queda como:<br />
Σhe dme + ΣdQ = Σhs dms + Wu BALANCE DE ENERGÍA (2)<br />
En don<strong>de</strong> he y hs correspon<strong>de</strong>n a las entalpías específicas <strong>de</strong> cada flujo <strong>de</strong><br />
entrada y salida respectivamente.<br />
El balance <strong>de</strong> Segunda Ley o balance entrópico queda como:<br />
dms<br />
s
dQ<br />
∑ =<br />
n<br />
i<br />
sedme + ∑ + dS ∑ g<br />
i = 0 Ti<br />
s<br />
s<br />
dm<br />
s<br />
(3)<br />
BALANCE DE ENTOPÍA<br />
En don<strong>de</strong> se y ss son las entropías <strong>de</strong> los flujos entrantes y salientes<br />
respectivamente y dSg es la entropía generada por el sistema en el intervalo <strong>de</strong><br />
tiempo dt.<br />
Si <strong>de</strong> las ecuaciones <strong>de</strong> balance <strong>de</strong> energía y entropía <strong>de</strong>spejamos Q 1 0 nos queda:<br />
Q = ∑(<br />
hdm)<br />
+ W ( ∑(<br />
hdm)<br />
+ ∑dQ<br />
)<br />
(4)<br />
0<br />
s<br />
s<br />
u<br />
e<br />
(En don<strong>de</strong> la sumatoria <strong>de</strong> los calores es <strong>de</strong>s<strong>de</strong> i=1 hasta n, <strong>de</strong>scontando el Q0.)<br />
e<br />
dQ<br />
= ∑ ) T (5)<br />
n<br />
i=<br />
1<br />
n<br />
i<br />
Q0 ( ( s dm)<br />
∑(<br />
sdm)<br />
+ ∑<br />
s<br />
e + dSg<br />
s<br />
e<br />
i = 1 Ti<br />
igualando ambas ecuaciones y <strong>de</strong>spejando el trabajo útil nos queda<br />
n<br />
0<br />
( h T s ) dm ∑(<br />
h T s ) dm + 1 dQ T S<br />
0<br />
0<br />
i<br />
g<br />
∑ (6)<br />
= ∑<br />
Wu e<br />
e e<br />
s<br />
s s<br />
0<br />
i = 1 Ti<br />
Si <strong>de</strong>finimos como el Ambiente Estable <strong>de</strong> Referencia (AER) las condiciones <strong>de</strong><br />
T=T0 y P=P0, po<strong>de</strong>mos ver <strong>de</strong> la ecuación anterior que los dos primeros términos<br />
<strong>de</strong> la <strong>de</strong>recha correspon<strong>de</strong>n a la diferencia <strong>de</strong> exergías <strong>de</strong> los flujos <strong>de</strong> masa, el<br />
siguiente es la sumatoria <strong>de</strong> las exergías asociadas a los flujos calor y el último<br />
término es la <strong>de</strong>strucción <strong>de</strong> exergía.<br />
Por lo que el balance <strong>de</strong> exergía queda expresado como:<br />
Wu = Σbe dme - Σbs dms + ΣBQ- Bd BALANCE DE EXERGÍA (7)<br />
De esta ecuación po<strong>de</strong>mos concluir que el trabajo útil máximo suce<strong>de</strong> cuando el<br />
proceso es reversible Sg = 0, por lo que en un proceso real (irreversible) se pier<strong>de</strong><br />
capacidad <strong>de</strong> hacer trabajo a una razón <strong>de</strong><br />
.<br />
T S 0<br />
1 Consi<strong>de</strong>rando el subíndice 0 el flujo <strong>de</strong> energía o materia que conecta con el medio <strong>de</strong> referencia<br />
g<br />
.<br />
i<br />
T<br />
0
El trabajo real es entonces igual al trabajo reversible menos el trabajo<br />
perdido<br />
Wu = Wr - Wl (8)<br />
En don<strong>de</strong> Wl = T0 Sg que se conoce como el Teorema <strong>de</strong> Gouy-Stodola<br />
Con este juego <strong>de</strong> ecuaciones <strong>de</strong> balance, masa, energía y exergía, queda<br />
<strong>de</strong>finido termodinámicamente cualquier proceso, evaluando no solamente las<br />
características energéticas, si no también la operación <strong>de</strong>l sistema cuantificando<br />
las irreversibilida<strong>de</strong>s internas <strong>de</strong> operación y las externas.<br />
Una <strong>de</strong> las gran<strong>de</strong>s utilida<strong>de</strong>s que nos brinda el análisis exergético es po<strong>de</strong>r<br />
evaluar la capacidad <strong>de</strong> producir trabajo que se pier<strong>de</strong> en cada proceso <strong>de</strong>ntro <strong>de</strong><br />
una planta <strong>de</strong> fuerza o cualquier otro proceso y con esta visión <strong>de</strong>finir en que<br />
partes es más conveniente actuar <strong>de</strong> una manera priorizada para ir corrigiendo los<br />
incrementos <strong>de</strong> irreversibilida<strong>de</strong>s que se presentan durante la operación <strong>de</strong> la<br />
planta.<br />
Como conclusión <strong>de</strong> este análisis es que el análisis <strong>de</strong> exergía es equivalente a<br />
realizar los análisis <strong>de</strong> primera y segunda ley <strong>de</strong> una manera conjunta.<br />
<strong>4.</strong>2 Energía y <strong>Exergía</strong><br />
Los diferentes tipos <strong>de</strong> energía presentan también diferentes calida<strong>de</strong>s,<br />
entendiendo por calidad la cantidad <strong>de</strong> trabajo útil que se pue<strong>de</strong> obtener. Estas<br />
diferencias radican en la posibilidad <strong>de</strong> producir trabajo o <strong>de</strong> transformar un tipo <strong>de</strong><br />
energía en otro. Por ejemplo, la calidad <strong>de</strong> un flujo <strong>de</strong> calor <strong>de</strong>pen<strong>de</strong> <strong>de</strong> la<br />
temperatura a la que está la fuente <strong>de</strong> don<strong>de</strong> sale; a mayor temperatura, una<br />
fuente <strong>de</strong> calor pue<strong>de</strong> transferir su energía con más posibilida<strong>de</strong>s que a menor<br />
temperatura 2 .<br />
<strong>La</strong> energía or<strong>de</strong>nada (o <strong>de</strong> alta calidad) pue<strong>de</strong> presentarse <strong>de</strong> las formas<br />
siguientes:<br />
(A) Energía potencial, tal como la almacenada en un campo<br />
gravitatorio, eléctrico o magnético, o en la <strong>de</strong>formación <strong>de</strong> un muelle<br />
perfectamente elástico, etc.<br />
(B) Energía cinética no aleatoria, como la almacenada en un volante<br />
en rotación, o en un chorro no turbulento <strong>de</strong> un fluido i<strong>de</strong>al.<br />
2 El mar es una inmensa fuente <strong>de</strong> energía (sólo hay que calcular la entalpía <strong>de</strong>l agua salada, y multiplicarla por toda la<br />
masa <strong>de</strong>l mar), pero como su temperatura es similar a la <strong>de</strong>l medio que la ro<strong>de</strong>a, no pue<strong>de</strong> transferir toda esta energía en<br />
forma <strong>de</strong> calor.
En la figura <strong>4.</strong>2 se presenta un conjunto <strong>de</strong> aparatos que producen la<br />
transformación entre diversos tipos <strong>de</strong> energía or<strong>de</strong>nada. Si no existen<br />
efectos disipativos, tales como rozamientos mecánicos, viscosidad,<br />
resistencia eléctrica, etc., cada uno <strong>de</strong> los aparatos actúa <strong>de</strong> una forma<br />
reversible por lo que su rendimiento es <strong>de</strong>l 100%. Por lo tanto, la energía<br />
potencial ganada por la pesa es igual a la cinética aportada por el chorro <strong>de</strong><br />
agua que entra en la turbina. Con este ejemplo se ilustra el hecho <strong>de</strong> que la<br />
energía or<strong>de</strong>nada goza <strong>de</strong> las siguientes propieda<strong>de</strong>s:<br />
Figura <strong>4.</strong>2 Transformaciones reversibles <strong>de</strong> energía.<br />
Pue<strong>de</strong> transformarse totalmente en otra forma or<strong>de</strong>nada, si se realiza el<br />
proceso reversiblemente.<br />
El intercambio <strong>de</strong> energía or<strong>de</strong>nada entre dos sistemas se produce en<br />
forma <strong>de</strong> trabajo.<br />
El intercambio reversible <strong>de</strong> energía or<strong>de</strong>nada se produce sin cambios en<br />
las entropías <strong>de</strong> los sistemas afectados y pue<strong>de</strong> analizarse sólo con la ayuda<br />
<strong>de</strong>l Primer Principio.<br />
<strong>La</strong>s propieda<strong>de</strong>s termodinámicas <strong>de</strong>l ambiente no intervienen en la<br />
<strong>de</strong>terminación <strong>de</strong> los intercambios <strong>de</strong> energía or<strong>de</strong>nada.
Pasemos ahora a la energía <strong>de</strong>sor<strong>de</strong>nada. Pertenece a esta clase la energía<br />
interna, tanto <strong>de</strong> naturaleza física como química, asociada con movimientos<br />
aleatorios <strong>de</strong> átomos o moléculas.<br />
Analicemos algunos procesos <strong>de</strong> conversión <strong>de</strong> energía <strong>de</strong>sor<strong>de</strong>nada en<br />
or<strong>de</strong>nada. Consi<strong>de</strong>remos en primer lugar un reservorio calorífico a la<br />
temperatura T. Si el ambiente se encuentra a una temperatura To , el<br />
segundo principio nos indica que la manera más eficaz <strong>de</strong> transformar<br />
energía calorífica (<strong>de</strong>sor<strong>de</strong>nada) en trabajo mecánico (or<strong>de</strong>nado) es<br />
mediante una máquina reversible que funcione entre las temperaturas T y To.<br />
El trabajo W realizado verifica η cQ<br />
, en don<strong>de</strong> η c es la eficiencia <strong>de</strong> Carnot 1-<br />
To/T. Por tanto, la calidad <strong>de</strong> Q, que viene medida por η c , <strong>de</strong>pen<strong>de</strong> <strong>de</strong> la<br />
temperatura T a que está disponible y <strong>de</strong> la To <strong>de</strong>l ambiente. Por otra parte,<br />
el manantial calorífico pier<strong>de</strong> una entropía Q/T, igual a la Qo/To ganada por el<br />
ambiente. No hay creación <strong>de</strong> entropía, por ser el proceso reversible.<br />
Otro proceso simple es la expansión isoterma <strong>de</strong> una gas i<strong>de</strong>al <strong>de</strong>s<strong>de</strong> el<br />
estado (p, To) al (po , To), siendo po la presión <strong>de</strong>l ambiente. El trabajo<br />
realizado será W = nrto Ln (p/po). <strong>La</strong> entropía <strong>de</strong>l gas experimentará un<br />
aumento ∆ S gas = n R Ln (p/p ), que coinci<strong>de</strong> con la entropía perdida por el<br />
ambiente − ∆S<br />
amb = Q/To<br />
= W/To<br />
.<br />
o<br />
Consi<strong>de</strong>remos finalmente un sistema que experimenta un proceso reversible<br />
en las condiciones (po, To) <strong>de</strong>l ambiente. Pue<strong>de</strong> ser, por ejemplo, una<br />
reacción química en una pila galvánica reversible. El trabajo útil producido<br />
es Wu=- ∆ G = −∆H<br />
+ To∆S<br />
, que <strong>de</strong>pen<strong>de</strong> <strong>de</strong> ∆H y ∆S.<br />
<strong>La</strong> entropía <strong>de</strong>l ambiente<br />
experimenta un cambio ∆S amb = Q / To<br />
= - To∆S<br />
/ To<br />
= - ∆S<br />
.<br />
<strong>La</strong>s consi<strong>de</strong>raciones anteriores ponen <strong>de</strong> manifiesto las siguientes peculiarida<strong>de</strong>s<br />
<strong>de</strong> los procesos que preten<strong>de</strong>n obtener la conversión más eficaz <strong>de</strong> energía<br />
<strong>de</strong>sor<strong>de</strong>nada en energía or<strong>de</strong>nada:<br />
− Los procesos han <strong>de</strong> ser reversibles.<br />
− <strong>La</strong> eficacia <strong>de</strong> la conversión <strong>de</strong>pen<strong>de</strong> <strong>de</strong> las propieda<strong>de</strong>s<br />
termodinámicas <strong>de</strong>l sistema y <strong>de</strong>l ambiente.<br />
− Hay que aplicar el Segundo Principio en el análisis.<br />
− El proceso origina, en general, cambios entrópicos en los sistemas<br />
que intervienen.
Vemos, por tanto, que la calidad (o capacidad <strong>de</strong> producir un efecto útil) <strong>de</strong> las<br />
formas <strong>de</strong>sor<strong>de</strong>nadas <strong>de</strong> energía <strong>de</strong>pen<strong>de</strong> <strong>de</strong> la entropía, <strong>de</strong>l tipo <strong>de</strong> energía y<br />
<strong>de</strong> las funciones termodinámicas <strong>de</strong>l sistema y <strong>de</strong>l ambiente; las formas<br />
or<strong>de</strong>nadas, por el contrario, no <strong>de</strong>pen<strong>de</strong>n <strong>de</strong> la entropía, tienen una calidad<br />
máxima e invariable y son totalmente convertibles en otras formas <strong>de</strong> energía.<br />
En general, se acepta como medida <strong>de</strong> la calidad <strong>de</strong> la energía, su capacidad para<br />
producir trabajo. El problema con esta <strong>de</strong>finición es elegir el nivel <strong>de</strong> referencia<br />
a<strong>de</strong>cuado. Hay que tener en cuenta, que para que una máquina térmica realice<br />
trabajo, <strong>de</strong>be tomar calor <strong>de</strong>s<strong>de</strong> una fuente a alta temperatura, y ce<strong>de</strong>r parte <strong>de</strong><br />
ese calor a un sumi<strong>de</strong>ro a baja temperatura 3 .<br />
Si la temperatura (fría) <strong>de</strong>l sumi<strong>de</strong>ro es muy alta, muy pocas fuentes tendrán la<br />
temperatura necesaria como para que una máquina térmica pue<strong>de</strong> transformar el<br />
calor <strong>de</strong> esta fuente en trabajo. Por tanto el nivel <strong>de</strong> referencia (es <strong>de</strong>cir, el valor<br />
<strong>de</strong> la temperatura fría) es muy importante a la hora <strong>de</strong> <strong>de</strong>finir la exergía. Como es<br />
habitual que las máquinas térmicas trabajen con el medio que las ro<strong>de</strong>a como foco<br />
frío, se suele tomar el nivel <strong>de</strong> referencia en la temperatura ambiente.<br />
En los procesos reales T no se pue<strong>de</strong> incrementar infinitamente. Su valor<br />
esta <strong>de</strong>finido por las condiciones metalúrgicas <strong>de</strong> los materiales y la T0<br />
<strong>de</strong>pen<strong>de</strong> <strong>de</strong> las condiciones ambientales.<br />
Por tanto, a la hora <strong>de</strong> calcular la exergía es necesario especificar cuál es el<br />
entorno en el que trabaja la máquina térmica. Debido a la falta <strong>de</strong> un equilibrio<br />
termodinámico en la naturaleza, no se pue<strong>de</strong> especificar completamente cuál es<br />
el estado <strong>de</strong> referencia (<strong>de</strong>bido a que, como ya se ha dicho, las condiciones <strong>de</strong>l<br />
medio son cambiantes). Normalmente, es suficiente con <strong>de</strong>finir el estado <strong>de</strong><br />
equilibrio mediante la temperatura.<br />
<strong>La</strong> capacidad <strong>de</strong> un medio energético para realizar trabajo expresa su potencial<br />
para transformarse en otros tipos <strong>de</strong> energía, y por tanto la exergía pue<strong>de</strong><br />
aplicarse al estudio <strong>de</strong> procesos tecnológicos como son plantas <strong>de</strong> energía, ciclos<br />
termodinámicos, máquinas, etc.<br />
A diferencia <strong>de</strong> la energía, no existe una ley <strong>de</strong> conservación para la exergía.<br />
Cualquier fenómeno irreversible causa una pérdida <strong>de</strong> exergía, lo que significa una<br />
reducción <strong>de</strong>l potencial <strong>de</strong> los efectos útiles <strong>de</strong> la energía, o por el contrario a un<br />
aumento <strong>de</strong>l consumo <strong>de</strong> energía proporcionado por el reservorio o foco caliente,<br />
para lograr una generación <strong>de</strong> trabajo igual.<br />
Si excluimos los efectos nucleares, magnéticos y eléctricos, la exergía, B, <strong>de</strong> una<br />
sustancia se pue<strong>de</strong> dividir en cuatro componentes: exergía cinética Bk, exergía<br />
potencial Bp, exergía física Bf y exergía química B0. <strong>La</strong> exergía cinética es igual<br />
a la energía cinética cuando la velocidad tiene como nivel <strong>de</strong> referencia la<br />
3 Según el Segundo Principio <strong>de</strong> la Termodinámica
superficie <strong>de</strong> la Tierra. Lo mismo ocurre con la exergía potencial. En la Figura <strong>4.</strong>3<br />
se muestran los diferentes tipos <strong>de</strong> exergía.<br />
<strong>Exergía</strong> <strong>Exergía</strong><br />
Pot. cinética<br />
p<br />
Figura <strong>4.</strong>3. Formas <strong>de</strong> exergía.<br />
B B + B + B + B = B + B + B<br />
= 0 (9)<br />
k<br />
f<br />
<strong>La</strong> exergía física es el trabajo que se pue<strong>de</strong> obtener sometiendo a la sustancia a<br />
procesos físicos 4 reversibles <strong>de</strong>s<strong>de</strong> la temperatura y presión iniciales, hasta el<br />
estado <strong>de</strong>terminado por la presión y la temperatura <strong>de</strong>l entorno.<br />
<strong>La</strong> exergía química es el trabajo que se pue<strong>de</strong> obtener <strong>de</strong> una sustancia que se<br />
encuentra a la presión y temperatura <strong>de</strong>l entorno, si alcanza un estado <strong>de</strong><br />
equilibrio termodinámico mediante reacciones químicas.<br />
En ocasiones, a la suma <strong>de</strong> la exergía física y química se le <strong>de</strong>nomina exergía<br />
térmica, Bt.<br />
Bt = Bf<br />
+ B0<br />
(10)<br />
Ambiente y estado muerto<br />
<strong>Exergía</strong><br />
<strong>Exergía</strong> térmica<br />
<strong>Exergía</strong> <strong>Exergía</strong><br />
física química<br />
Para el análisis exergetico hay que referirse constantemente a un ambiente<br />
estable <strong>de</strong> referencia (AER), que se supone en un estado <strong>de</strong> equilibrio<br />
termodinámico completo. Si alguna propiedad intensiva <strong>de</strong> un sistema (presión,<br />
temperatura, potencial químico, etc.) difiere <strong>de</strong> la correspondiente <strong>de</strong>l ambiente,<br />
existe una posibilidad <strong>de</strong> realización <strong>de</strong> un trabajo. El ambiente proporciona, por<br />
tanto, un nivel <strong>de</strong> referencia natural para la <strong>de</strong>terminación <strong>de</strong> la energía utilizable.<br />
4 Entendiendo por tal aquél dón<strong>de</strong> no hay cambio en la composición <strong>de</strong> la sustancia.<br />
Bf<br />
Bp Bk Bt<br />
B<br />
p<br />
k<br />
B0<br />
t
El ambiente pue<strong>de</strong> actuar sobre un sistema <strong>de</strong> las tres formas siguientes:<br />
a) Transferencia <strong>de</strong> calor, como manantial a la temperatura To . Dada la<br />
enorme capacidad calorífica <strong>de</strong>l ambiente, los intercambios <strong>de</strong> calor<br />
afectarán <strong>de</strong>spreciablemente a su temperatura.<br />
b) Intercambio <strong>de</strong> trabajo <strong>de</strong> expansión o compresión, como almacén <strong>de</strong><br />
energía utilizable. Se produce sólo cuando el sistema experimenta un<br />
cambio <strong>de</strong> volumen. Cuando éste cambia en ∆V cuasi-estáticamente, el<br />
sistema realiza un trabajo po ∆V sobre el ambiente. Está claro que este<br />
trabajo no es útil, aunque pue<strong>de</strong> ser recuperado si el sistema vuelve cuasiestáticamente<br />
al volumen inicial.<br />
c) Intercambio <strong>de</strong> materia, como <strong>de</strong>pósito <strong>de</strong> sustancias <strong>de</strong> trabajo potencial<br />
químico, en equilibrio estable. Pue<strong>de</strong> producirse en sistemas abiertos.<br />
A consecuencia <strong>de</strong> estas interacciones, el ambiente <strong>de</strong>termina los niveles <strong>de</strong><br />
temperatura, presión y potenciales químicos que han <strong>de</strong> tomarse como<br />
referencia para los cálculos <strong>de</strong> energía utilizable. Cuando el sistema llega al<br />
equilibrio termodinámico completo con el ambiente, se dice que se<br />
encuentra en el estado muerto. En dicho estado, la presión, la temperatura y<br />
los potenciales químicos <strong>de</strong>l sistema son iguales a los <strong>de</strong>l ambiente.<br />
En aplicaciones éste se produce cuando existe una pared física que impi<strong>de</strong> el<br />
intercambio <strong>de</strong> material entre sistema y ambiente. Lo <strong>de</strong>signaremos estado<br />
ambiental.<br />
<strong>Exergía</strong> <strong>de</strong> un flujo <strong>de</strong> materia.<br />
Consi<strong>de</strong>remos en primer lugar un proceso <strong>de</strong> flujo <strong>de</strong> materia en forma <strong>de</strong><br />
corriente <strong>de</strong> un fluido cualquiera en régimen estacionario. Se trata <strong>de</strong> investigar el<br />
trabajo útil máximo que pue<strong>de</strong> obtenerse al llevar dicha corriente <strong>de</strong>s<strong>de</strong> un<br />
estado inicial genérico, en el que se encuentra, hasta el estado muerto, con la sola<br />
intervención <strong>de</strong> la corriente y la <strong>de</strong>l ambiente.<br />
<strong>La</strong> energía mecánica obtenida por unidad <strong>de</strong> masa que circula entre el estado<br />
inicial genérico y el estado muerto verifica.<br />
1 2<br />
e o<br />
2<br />
= wu<br />
+ ( co<br />
− c ) + g(<br />
z − z),<br />
(11)<br />
2<br />
en don<strong>de</strong> wu representa el trabajo útil, c la velocidad que lleva el fluido y z la<br />
altura o cota. Hay que recordar que tanto la energía cinética ½ c 2 como la<br />
potencial gz son transformables íntegramente en trabajo útil con los dispositivos<br />
a<strong>de</strong>cuados.
Al aplicar el Primer Principio resulta:<br />
q = ho – h + e (12)<br />
en don<strong>de</strong> h es la entalpía específica <strong>de</strong>l fluido.<br />
<strong>La</strong> energía mecánica e obtenida será máxima cuando el proceso sea reversible.<br />
En particular se tomará el calor q reversiblemente, a la temperatura To <strong>de</strong>l<br />
ambiente. Entonces aplicando la Segunda Ley<br />
qrev = To (so – s) (13)<br />
en don<strong>de</strong> s es la entropía específica <strong>de</strong>l fluido.<br />
Igualando ambas ecuaciones nos queda:<br />
Despejando se obtiene<br />
T0 (s0 –s) = h0 – h + emax (14)<br />
e o<br />
o o o<br />
= ( h.<br />
−T<br />
s)<br />
− ( h −T<br />
s ) = b<br />
max (15)<br />
en don<strong>de</strong> b representa la función <strong>de</strong> estado exergía específica.<br />
Si <strong>de</strong>finimos una nueva función, <strong>de</strong>nominada la función <strong>de</strong> Darrieus, como:<br />
y ≡ h - Tos (16)<br />
Entonces la función <strong>de</strong> exergía toma la forma<br />
b = y – y0 (17)<br />
Este resultado expresa que la energía mecánica máxima que pue<strong>de</strong> obtenerse al<br />
llevar la corriente <strong>de</strong>l fluido <strong>de</strong>s<strong>de</strong> un estado genérico hasta el estado muerto,<br />
<strong>de</strong>nominada exergía, es igual a la disminución <strong>de</strong> la función <strong>de</strong> Darrieus.<br />
<strong>La</strong> función <strong>de</strong> Darrieus se presta a una representación gráfica muy simple en<br />
el diagrama <strong>de</strong> Mollier (h,s). De acuerdo con emax = ( h.<br />
− To<br />
s)<br />
− ( ho<br />
− Tos<br />
o ) = b , las<br />
líneas <strong>de</strong> igual exergía vendrán representadas por rectas h – Tos = cte (ver<br />
Figura <strong>4.</strong>4).
Cuando h = ho y T = To , resulta b = 0 y la recta correspondiente se llama<br />
recta <strong>de</strong>l estado muerto, lugar geométrico <strong>de</strong> los estados <strong>de</strong> exergía nula<br />
Figura <strong>4.</strong><strong>4.</strong> Representación <strong>de</strong> la exergía en el plano h-s.<br />
Si representamos por 1 y 0 respectivamente el estado genérico y el muerto,<br />
la exergía b <strong>de</strong> 1, viene dada por el segmento vertical 1B trazado entre 1 y la<br />
línea <strong>de</strong>l estado muerto. En la misma figura se dibuja la sencilla<br />
construcción gráfica que relaciona h – ho con b.<br />
Como (∂H/∂S)p = T, la línea <strong>de</strong>l estado muerto es tangente en 0 a la isobara po<br />
.<br />
<strong>Exergía</strong> <strong>de</strong> un flujo <strong>de</strong> calor<br />
Pasemos ahora a un proceso <strong>de</strong> flujo <strong>de</strong> calor. Si un reservorio a la temperatura<br />
T ce<strong>de</strong> un calor q, se trata <strong>de</strong> investigar el trabajo útil máximo que pue<strong>de</strong><br />
obtenerse con la sola intervención <strong>de</strong>l reservorio y <strong>de</strong>l ambiente, reservorio a T0.<br />
De acuerdo con el Segundo Principio el rendimiento máximo <strong>de</strong> dicha conversión<br />
energética es 1 – To /T, luego la cantidad <strong>de</strong> calor q posee la exergía bq siguiente:<br />
bq = q (1 – T0/T ) (18)<br />
Vemos por tanto, que el contenido exergético <strong>de</strong> un flujo <strong>de</strong> calor es tanto menor<br />
cuanto más se aproxima T a To .<br />
<strong>Exergía</strong> química<br />
Consi<strong>de</strong>remos un proceso en el cual tiene lugar una reacción química, es <strong>de</strong>cir,<br />
un proceso en el cual un flujo <strong>de</strong> reactivos R en unas condiciones <strong>de</strong> temperatura
y presión To y Po , sufre una reacción química para transformarse en un flujo <strong>de</strong><br />
producto P a las mismas To y Po , según se ilustra en la Figura <strong>4.</strong>5.<br />
T0 P0<br />
Reactivos<br />
Figura <strong>4.</strong>5 Análisis <strong>de</strong> un proceso en el que hay reacción química.<br />
Suponiendo que el reactor es el espacio en don<strong>de</strong> se realiza esta reacción y opera<br />
reversiblemente, <strong>de</strong>seamos conocer el valor <strong>de</strong>l trabajo máximo utilizable wu, que<br />
coincidirá con la exergía asociada a ese cambio químico.<br />
En este sistema conforme a la Primera Ley:<br />
wu = q + hR – hp (19)<br />
Como el proceso en el reactor se realiza reversiblemente, tenemos conforme a la<br />
Segunda Ley:<br />
q = To (sp – sR) (20)<br />
En don<strong>de</strong> los subíndices R y P se refieren a las propieda<strong>de</strong>s <strong>de</strong> los reactivos y<br />
productos respectivamente.<br />
Combinando ambas ecuaciones nos queda:<br />
wu = (hR – To sR) – (hp – To sp) (21)<br />
Si recordamos a <strong>de</strong>finición <strong>de</strong> la función entalpía libre <strong>de</strong> Gibbs g que está dada<br />
por:<br />
g = h – Ts (22)<br />
y la sustituimos en nuestra ecuación <strong>de</strong> trabajo útil se convierte en:<br />
Q<br />
Reactor<br />
Wu<br />
T0 P0<br />
Productos
wu = gR – qp = - ∆ g = b0 (23)<br />
con sólo tomar como temperatura T la <strong>de</strong>l AER, To.<br />
Vemos, por tanto, que en un proceso con reacción química, el trabajo útil máximo<br />
que pue<strong>de</strong> obtenerse coinci<strong>de</strong> con la disminución <strong>de</strong> energía libre <strong>de</strong> Gibbs que<br />
tiene lugar en el mismo.<br />
En un proceso <strong>de</strong> flujo <strong>de</strong> materia, pue<strong>de</strong> llegarse al estado ambiental (To, po) en<br />
estado metastable. Mediante un proceso químico, como el acabado <strong>de</strong> escribir,<br />
podría llevarse la materia a su estado <strong>de</strong> equilibrio, que sería el estado muerto. El<br />
cálculo <strong>de</strong> exergías en general se apoya en este hecho, distinguiendo la exergía<br />
física y la química.<br />
Para una sustancia que se encuentra en un estado termodinámico genérico<br />
(T, p), su exergía física se <strong>de</strong>termina respecto <strong>de</strong>l estado ambiental (To , po),<br />
que pue<strong>de</strong> ser <strong>de</strong> equilibrio metastable, conforme a las diferencias <strong>de</strong> las<br />
funciones <strong>de</strong> Darrieus (y-y0).<br />
<strong>La</strong> exergía química se calcula mediante expresiones <strong>de</strong> la diferencia <strong>de</strong> las<br />
funciones <strong>de</strong> Gibbs, para las reacciones a To y Po que llevan las sustancias<br />
al equilibrio final con el AER.<br />
<strong>4.</strong>3 Cambios <strong>de</strong> exergía térmica entre dos estados<br />
<strong>La</strong> diferencia <strong>de</strong> la exergía térmica <strong>de</strong> dos estados pue<strong>de</strong> calcularse a partir <strong>de</strong>l<br />
mo<strong>de</strong>lo mostrado en la Figura <strong>4.</strong>6.
Figura <strong>4.</strong>6. Cambio <strong>de</strong> exergía en un sistema abierto.<br />
<strong>La</strong> fuente <strong>de</strong> energía con entalpía H1 y entropía S1 entra en la máquina<br />
reversible. Después <strong>de</strong> someterse a cambios físicos y/o químicos, el efluente tiene<br />
una entalpía H2 y una entropía S2. Sólo vamos a consi<strong>de</strong>rar la exergía térmica; por<br />
tanto, suponemos que las velocida<strong>de</strong>s <strong>de</strong> los dos efluentes son similares, e igual<br />
pasa con la altura, por lo que los cambios <strong>de</strong> energía cinética y potencial son<br />
<strong>de</strong>spreciables.<br />
<strong>La</strong> máquina pue<strong>de</strong> intercambiar calor con su entorno, <strong>de</strong> manera reversible. El<br />
máximo trabajo que pue<strong>de</strong> realizar esta máquina viene dado por la diferencia entre<br />
la exergía <strong>de</strong> la corriente <strong>de</strong> entrada y la exergía <strong>de</strong> la corriente <strong>de</strong> salida. Esta<br />
diferencia vendrá dada por:<br />
∆Bt Bt<br />
− Bt<br />
= −(<br />
H1<br />
− H2<br />
+ Q0<br />
)<br />
= (24)<br />
<strong>La</strong> condición <strong>de</strong> reversibilidad conduce a:<br />
2<br />
1<br />
Q0<br />
S 2 − S1<br />
− = 0<br />
(25)<br />
T<br />
Con lo que sustituyendo nos queda:<br />
B BT<br />
0<br />
H<br />
1<br />
H<br />
2<br />
T<br />
0 ( S1<br />
S2<br />
T 2 = − − −<br />
1<br />
− (26)<br />
)
Si consi<strong>de</strong>ramos que en el proceso no hay variación <strong>de</strong> masa, la masa <strong>de</strong>l flujo<br />
entrante es igual a la que sale, po<strong>de</strong>mos trabajarla con las propieda<strong>de</strong>s<br />
específicas con lo que se tiene que:<br />
bt1 – bt2 = h1 – h2 – T0(s1 – s2) (27)<br />
Si durante el proceso no existen reacciones químicas y no existe ningún cambio<br />
en la composición molar <strong>de</strong> la sustancia, la exergía química no interviene y se<br />
anula al ser igual en ambos estados.<br />
El cambio <strong>de</strong> estado <strong>de</strong> la corriente que atraviesa la máquina pue<strong>de</strong><br />
representarse <strong>de</strong> varias formas. Una <strong>de</strong> ellas es la mostrada en la Figura <strong>4.</strong>7. El<br />
proceso que origina el cambio <strong>de</strong> estado 1→ B es isentrópico, y conduce a la<br />
sustancia hasta la temperatura <strong>de</strong>l entorno. El proceso C→2 es también<br />
isentrópico, y conduce a la sustancia hasta la temperatura <strong>de</strong> la corriente <strong>de</strong><br />
salida. El proceso B→C es isotérmico, y lleva a cabo la transferencia <strong>de</strong> calor<br />
reversible con el entorno. El punto A, que se encuentra sobre la misma<br />
isentálpica que el punto 2 y permite calcular la entalpía <strong>de</strong> la corriente <strong>de</strong> salida, y<br />
por tanto la diferencia <strong>de</strong> entalpía entre la entrada y la salida, H1 – H2.<br />
Figura <strong>4.</strong>7. Representación <strong>de</strong>l cambio <strong>de</strong> exergía en el diagrama T-s.<br />
En el caso <strong>de</strong> gases i<strong>de</strong>ales, y suponiendo que su calor específico es constante,<br />
po<strong>de</strong>mos <strong>de</strong>sarrollar la siguiente ecuación, utilizando las relaciones<br />
termodinámicas vistas anteriormente para el cambio <strong>de</strong> entalpía y <strong>de</strong> entropía.
⎡<br />
T ⎤ P<br />
= c ⎢(<br />
T −T<br />
) −T<br />
ln + RT ln<br />
0 0<br />
0<br />
T<br />
⎥<br />
(28)<br />
⎣<br />
P<br />
0 ⎦<br />
0<br />
bf p<br />
Ejercicio 1. (Se <strong>de</strong>ja como ejercicio al alumno esta <strong>de</strong>mostración)<br />
<strong>La</strong> exergía física específica consta <strong>de</strong> dos términos: uno que <strong>de</strong>pen<strong>de</strong> <strong>de</strong> la<br />
temperatura y otro que <strong>de</strong>pen<strong>de</strong> <strong>de</strong> la presión.<br />
Graficando esta ecuación en coor<strong>de</strong>nadas adimensionales nos queda tal como<br />
se muestra en la siguiente Figura <strong>4.</strong>8. El componente que <strong>de</strong>pen<strong>de</strong> <strong>de</strong> la<br />
temperatura es siempre no negativo. El componente que <strong>de</strong>pen<strong>de</strong> <strong>de</strong> la presión<br />
sólo es negativo si la presión es inferior a la presión <strong>de</strong>l entorno. Esto es así<br />
porque se necesita trabajo para comprimir el gas, <strong>de</strong> manera que pueda ser<br />
expulsado al entorno a una presión superior.<br />
Figura <strong>4.</strong>8. Variación <strong>de</strong> la exergía física en forma adimensional.
<strong>4.</strong>4 Irreversibilida<strong>de</strong>s<br />
<strong>La</strong> causa <strong>de</strong> la <strong>de</strong>strucción <strong>de</strong> exergía son las irreversibilida<strong>de</strong>s <strong>de</strong> los sistemas,<br />
<strong>de</strong> esta forma la exergía <strong>de</strong>struida cuantifica en unida<strong>de</strong>s <strong>de</strong> energía las<br />
irreversibilida<strong>de</strong>s presentadas en los procesos.<br />
Un proceso se dice que es reversible si es posible que regresando cada paso <strong>de</strong>l<br />
mismo se reestablezcan exactamente a su estado inicial respectivo el sistema y el<br />
medio circundante.<br />
Un proceso irreversible es cuando no hay forma <strong>de</strong> regresarlo, esto es, que no<br />
hay medios por los cuales el sistema y sus alre<strong>de</strong>dores pue<strong>de</strong>n ser exactamente<br />
restaurados a sus respectivos estados iníciales.<br />
Los procesos reversibles son una i<strong>de</strong>alización ya que cualquier sistema real<br />
siempre es irreversible.<br />
En la Figura <strong>4.</strong>9 se presenta gráficamente este concepto, recordando que la<br />
termodinámica clásica solo analiza estados <strong>de</strong> equilibrio.<br />
Figura <strong>4.</strong>9.<br />
Un sistema que ha pasado por un proceso irreversible no necesariamente es<br />
excluido para ser restaurado a su estado inicial, sin embargo, aunque el sistema<br />
fuera restaurado a su estado inicial, no será posible regresar el entorno al estado<br />
en el que estaba inicialmente.
Hay varios efectos en los que su presencia durante un proceso le causa<br />
irreversibilida<strong>de</strong>s, entre estos se incluyen los siguientes, aunque no son limitativos:<br />
• <strong>La</strong> transferencia <strong>de</strong> calor a través <strong>de</strong> una diferencia <strong>de</strong> temperatura finita<br />
• <strong>La</strong> expansión <strong>de</strong> un gas o un líquido a una presión menor como la mostrada<br />
en la Figura <strong>4.</strong>10<br />
P1<br />
P1 > P2<br />
P2<br />
Figura <strong>4.</strong>10 Válvula <strong>de</strong> expansión adiabática.<br />
• <strong>La</strong> reacción química espontánea<br />
• <strong>La</strong> combustión<br />
• Fricción - la fricción <strong>de</strong> <strong>de</strong>slizamiento como la <strong>de</strong>l flujo <strong>de</strong> fluidos<br />
• <strong>La</strong> corriente eléctrica fluye a través <strong>de</strong> una resistencia<br />
• <strong>La</strong> magnetización o polarización con histéresis<br />
• <strong>La</strong> <strong>de</strong>formación inelástica<br />
• Cualquier proceso que no se lleve a cabo <strong>de</strong> manera cuasiestática<br />
• Cualquier proceso que provoque diferencias <strong>de</strong> temperaturas <strong>de</strong>ntro <strong>de</strong>l mismo<br />
sistema como la producida por el efecto <strong>de</strong> Seebeck o efecto termopar,<br />
mostrado en la Figura <strong>4.</strong>11
Figura <strong>4.</strong>11. Efecto <strong>de</strong> Seebeck.<br />
• <strong>La</strong> mezcla <strong>de</strong> materia <strong>de</strong> diferentes composiciones o estados, como la<br />
mostrada en la Figura <strong>4.</strong>12 en que se ve una mezcla <strong>de</strong> diferentes estados <strong>de</strong><br />
la materia o en la Figura <strong>4.</strong>13, que muestra un mezclador <strong>de</strong> dos flujos.<br />
m1<br />
m2<br />
Figura <strong>4.</strong>12. Mezclado <strong>de</strong> diferentes estados <strong>de</strong> la materia.<br />
m3 = m1 + m2
Figura <strong>4.</strong>13 Mezclado <strong>de</strong> dos fluidos.<br />
<strong>La</strong>s irreversibilida<strong>de</strong>s pue<strong>de</strong>n ser divididas en dos tipos, internas y externas.<br />
<strong>La</strong>s irreversibilida<strong>de</strong>s internas son aquellas que ocurren <strong>de</strong>ntro <strong>de</strong>l sistema,<br />
mientras que las externas son las que ocurren <strong>de</strong>ntro <strong>de</strong>l entorno, normalmente<br />
en el entorno inmediato. Como esta clasificación <strong>de</strong>pen<strong>de</strong> <strong>de</strong> el lugar don<strong>de</strong> el<br />
analista establezca la frontera <strong>de</strong>l sistema y el entorno inmediato, es arbitraria y no<br />
se pue<strong>de</strong> generalizar.<br />
Cuando en un proceso dado no existen irreversibilida<strong>de</strong>s internas se<br />
<strong>de</strong>nomina Proceso internamente reversible<br />
Los ingenieros <strong>de</strong>ben ser capaces <strong>de</strong> reconocer irreversibilida<strong>de</strong>s, evaluando su<br />
influencia y estimando su impacto en los costos monetarios que implican, para<br />
po<strong>de</strong>r reducirlos. Sin embargo, la necesidad <strong>de</strong> alcanzar ritmos <strong>de</strong> producción<br />
rentables, la transferencia <strong>de</strong> calor rápida que se requiere en varios procesos<br />
industriales, la aceleración rápida y otras circunstancias <strong>de</strong> la operación <strong>de</strong> los<br />
procesos, invariablemente implica la presencia <strong>de</strong> irreversibilida<strong>de</strong>s importantes.<br />
Por esta razón las irreversibilida<strong>de</strong>s son aceptadas <strong>de</strong>ntro <strong>de</strong> ciertos rangos en<br />
todos los sistemas <strong>de</strong>bido a que los cambios en diseño y operación que se<br />
requieren para reducirlas normalmente son muy costosos.<br />
Sin embargo, las mejoras en el comportamiento termodinámico <strong>de</strong> los procesos<br />
normalmente originan la reducción <strong>de</strong> las irreversibilida<strong>de</strong>s, las acciones<br />
llevadas a cabo en esta dirección normalmente están restringidas por un número<br />
<strong>de</strong> factores prácticos a menudo relacionados con los costos.<br />
Es por estas razones que en cualquier caso práctico es muy importante evaluar<br />
técnica y económicamente el efecto <strong>de</strong> las irreversibilida<strong>de</strong>s y las acciones<br />
requeridas para disminuirlas, con la finalidad <strong>de</strong> <strong>de</strong>cidir cuales son convenientes<br />
llevar a cabo.<br />
A manera <strong>de</strong> ejemplo, consi<strong>de</strong>re dos cuerpos a diferentes temperaturas y<br />
capaces <strong>de</strong> comunicarse térmicamente. Con una diferencia finita <strong>de</strong><br />
temperaturas entre ellos, se presenta una transferencia <strong>de</strong> calor espontánea y,<br />
como se había mencionado antes, esta constituirá una fuente <strong>de</strong> irreversibilidad.<br />
Se pue<strong>de</strong> esperar que la <strong>importancia</strong> <strong>de</strong> las irreversibilida<strong>de</strong>s disminuya conforme<br />
la diferencia <strong>de</strong> la temperatura va disminuyendo.<br />
Mientras la diferencia entre las temperaturas <strong>de</strong> los cuerpos se va acercando a<br />
cero, la transferencia <strong>de</strong> calor se acercará a la i<strong>de</strong>alizada. Del estudio <strong>de</strong><br />
transferencia <strong>de</strong> calor sabemos que la transferencia <strong>de</strong> una cantidad finita <strong>de</strong>
energía entre los cuerpos, cuando sus temperaturas difieren por muy poco,<br />
requiere <strong>de</strong> una cantidad consi<strong>de</strong>rable <strong>de</strong> tiempo o una gran área <strong>de</strong> transferencia<br />
<strong>de</strong> calor, o las dos. Para aproximarse al la transferencia <strong>de</strong> calor i<strong>de</strong>alizada o<br />
reversible, se requiere <strong>de</strong> una cantidad infinita <strong>de</strong> tiempo y/o un área infinita. Cada<br />
una <strong>de</strong> estas opciones claramente tiene implicaciones <strong>de</strong> costos.<br />
Conclusiones<br />
En el presente capítulo se <strong>de</strong>fine el concepto <strong>de</strong> exergía como el <strong>de</strong> la energía<br />
útil o la calidad <strong>de</strong> la energía, mediante el análisis combinado <strong>de</strong> las dos leyes<br />
fundamentales <strong>de</strong> la termodinámica. Así mismo se vieron las formas <strong>de</strong> evaluar<br />
la exergía para un flujo <strong>de</strong> materia y para un flujo <strong>de</strong> calor; tomando en cuenta<br />
que para un flujo <strong>de</strong> trabajo es la misma cantidad, ya que el trabajo es exergía<br />
pura.<br />
Ejercicios <strong>de</strong>l <strong>Módulo</strong> 4<br />
1. Ejemplo: <strong>Exergía</strong> <strong>de</strong>l vapor saturado<br />
Hallar la exergía específica <strong>de</strong>l vapor <strong>de</strong> agua saturado a una presión <strong>de</strong> 2 MPa,<br />
tomando como referencia el agua líquida a 25 ° C y 1 atm.<br />
Mediante unas tablas <strong>de</strong> vapor <strong>de</strong> agua obtenemos los datos que siguen:<br />
Estado P (MPa) t (°C) h(kJ kg -1 ) s (kJ k -1 kg -1 )<br />
1 2 212.374 2797.225 6.3366<br />
0 0.1 25.0 10<strong>4.</strong>856 0.3698<br />
Hay que observar que los valores <strong>de</strong> h y s para el agua líquida a 25°C y 1 atm<br />
(100 kPa) son prácticamente los mismos que a 25°C y la presión <strong>de</strong> vapor <strong>de</strong>l<br />
agua a 25°C (3.165 kPa).<br />
Se aplica la fórmula 15, en la que separamos el término entrópico <strong>de</strong>l entálpico:<br />
b1 = h1-ho-To (s1-so) = (2797.225 –10<strong>4.</strong>856)-298(6.3366-0.3698) = 2692.3686-<br />
1778.9615=913.407 kJ/kg<br />
En este resultado se aprecia que, <strong>de</strong>l salto entálpico total 2692.3638 kJ kg -1 , una<br />
parte importante,<br />
1778.9615 kJ kj -1 no es transformable en trabajo, ni tan siquiera en las<br />
condiciones más favorables concebibles (proceso totalmente reversible).
<strong>La</strong> exergía <strong>de</strong>l vapor <strong>de</strong> agua varía más fuertemente que la entalpía con la<br />
temperatura y la presión. Ejercicio para entregar: Se <strong>de</strong>ja como Tarea, que el<br />
participante elabore una tabla con los datos <strong>de</strong> entalpía y exergía (calculada)<br />
específicas <strong>de</strong>l vapor saturado en un intervalo <strong>de</strong> presiones que se extienda<br />
<strong>de</strong>s<strong>de</strong> 100 a 7000 kPa para ver la variación <strong>de</strong> la entalpía y <strong>de</strong> la exergía, (ver<br />
envió <strong>de</strong> trabajos).