Révisions cristallographie corrigé
Révisions cristallographie corrigé
Révisions cristallographie corrigé
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
Les Eucalyptus, Nice <strong>Révisions</strong> de chimie<br />
PT* Cristallographie<br />
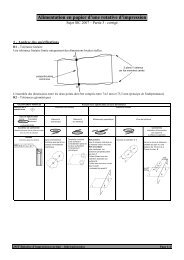
CR1 Structure de la blende<br />
1. Les anions S 2- forment un réseau cubique à faces centrées. Les cations Zn 2+ occupent la moitié des sites<br />
tétraédriques de ce réseau. Ils forment donc aussi un réseau cubique à faces centrées, décalé par rapport à<br />
celui des anions de telle sorte que les nœuds de l’un coïncident avec les sites tétraédriques de l’autre et<br />
réciproquement.<br />
La coordinence est le nombre de premiers voisins d’un atome donc le nombre de sphères qui touchent une<br />
sphère donnée. Chaque ion Zn 2+ est tangent à quatre ions S 2- . La coordinence est quatre pour cette<br />
structure.<br />
2. Les ions S 2- et Zn 2+ sont tangents suivant la diagonale du cube<br />
de coté<br />
a<br />
qui enveloppe le site tétraédrique, donc :<br />
2<br />
a<br />
2 r =<br />
( r )<br />
+ + −<br />
3<br />
2<br />
Les ions S 2- ne sont pas tangents suivant la diagonale d’une<br />
face de la maille : 4r− a 2 <<br />
On en déduit en divisant membre à membre :<br />
S 2-<br />
Zn 2+<br />
r<br />
r<br />
+<br />
−<br />
><br />
3<br />
2<br />
−1<br />
=<br />
Structure C.F.C. de la blende :<br />
S 2- aux nœuds ; Zn 2+ aux sites<br />
0,<br />
224<br />
3. Les anions Cl - forment un réseau cubique à faces centrées. Les cations Na + sont placés dans les sites<br />
octaédriques de ce réseau c’est à dire au centre du cube et au milieu de chaque arête. Ils forment donc<br />
aussi un réseau cubique à faces centrées, décalé par rapport à celui des anions de a<br />
de telle sorte que les<br />
2<br />
nœuds de l’un coïncident avec les sites octaédriques de l’autre et réciproquement. La coordinence est six<br />
pour cette structure.<br />
Les ions Cl - et Na + sont tangents suivant l’arête de la maille : 2 ( r r ) = a<br />
+ + −<br />
Les ions Cl - ne sont pas tangents suivant la diagonale d’une face de la maille : 4r < a 2<br />
r+<br />
On en déduit en divisant membre à membre : > 2 −1<br />
= 0,<br />
414<br />
r<br />
−<br />
Zn 2+<br />
Zn 2+<br />
S 2-<br />
Structure C.F.C. de la blende :<br />
Zn 2+ aux nœuds ; S 2- aux sites<br />
−
Les Eucalyptus, Nice <strong>Révisions</strong> de chimie<br />
PT* Cristallographie<br />
3 r+<br />
Finalement pour une maille de type blende : 0 , 224 = −1<br />
≤ ≤ 2 −1<br />
= 0,<br />
414<br />
2 r<br />
r+<br />
0,<br />
074<br />
4. x = = = 0,<br />
402 : La condition précédente est bien satisfaite.<br />
r 0,<br />
184<br />
−<br />
La compacité C est le rapport entre le volume occupé par les atomes et le volume total (nombre sans<br />
dimension compris entre 0 et 1). Il faut dénombrer le nombre d’atomes appartenant en propre à la maille.<br />
S 2- 1 1<br />
: 8 × + 6 × = 4 ; Zn<br />
8 2<br />
2+ : 4 (normal pour assurer la neutralité électrique)<br />
4<br />
4×<br />
π<br />
C =<br />
3<br />
a<br />
3 3 ( r + r )<br />
3<br />
+<br />
−<br />
=<br />
0,<br />
525<br />
CR2 Etude de la Würtzite<br />
( M + M ) 3<br />
4 + −<br />
−<br />
μ = = 3056kg.<br />
m<br />
3<br />
Na<br />
1. La maille usuelle est un prisme droit à base hexagonale qui reproduit le cristal à l’échelle microscopique.<br />
π<br />
3<br />
Cependant cette maille n’est pas une maille élémentaire. On raisonne habituellement sur le tiers de la<br />
maille précédente constituée d’un prisme droit à base losange. Les paramètres c et a sont liés. Dans le<br />
triangle rectangle ABC :<br />
2<br />
2<br />
⎛ c ⎞ ⎛ a 3 ⎞ 2<br />
+ = a ⇒<br />
⎜ ⎟ ⎜ ⎟<br />
⎝ 2 ⎠<br />
⎜ 3 ⎟<br />
⎝ ⎠<br />
a 3<br />
3<br />
S 2-<br />
2<br />
c = 2a = 0,624 nm<br />
3<br />
2. Il faut dénombrer le nombre d’atomes appartenant en propre à la<br />
maille : S 2- 1<br />
: 8 × + 1 = 2 . Donc deux ions Zn<br />
8<br />
2+ appartiennent en<br />
propre à la maille et la moitié des sites tétraédriques est donc<br />
occupée.<br />
a<br />
3.<br />
2<br />
Le volume de la maille est le produit de la surface du losange a<br />
3<br />
2<br />
par la hauteur c :<br />
4 3 3<br />
2× π ( r+ + r−<br />
)<br />
C<br />
3<br />
2 M + M<br />
= = 0,705 ; μ =<br />
2 3<br />
2 3<br />
c a<br />
Nc<br />
a<br />
2<br />
2<br />
= 4103 kg. m<br />
−<br />
S 2-<br />
c<br />
a<br />
C<br />
S 2-<br />
( + − ) −3<br />
a<br />
a<br />
c<br />
2<br />
B<br />
A<br />
Zn 2+
Les Eucalyptus, Nice <strong>Révisions</strong> de chimie<br />
PT* Cristallographie<br />
La structure de la würtzite est donc plus compacte que celle de la blende.<br />
4. blende ZnS wurtzite<br />
ZnS → . Cet équilibre est monovariant, en effet le calcul de la variance donne :<br />
V = C + 2 − Φ = 1+<br />
2 − 2 = 1<br />
A pression imposée (1 bar), les deux variétés allotropiques ne peuvent donc être en équilibre qu’à une<br />
température donnée soit 900°C. Si on augmente la pression à cette température l’équilibre est alors<br />
rompu. Cherchons la forme stable. Initialement (équilibre) l’affinité était nulle. Sa variation s’écrit :<br />
dA T −d<br />
r<br />
( Δ G)<br />
T = − ( μw − μb<br />
) T<br />
= d<br />
Or : dμ = Vmdp<br />
− SmdT<br />
Donc : dA T = ( Vmb<br />
− Vmw<br />
)dp<br />
Puisque mb mw V V > , l’affinité devient positive par augmentation isotherme de pression. La forme stable<br />
est alors la variété la plus dense donc la würtzite. Le problème est identique à celui ,classique, de<br />
l’équilibre entre le carbone graphite et le carbone diamant, la forme stable sous forte pression étant le<br />
diamant. Inversement, une augmentation isobare de température entraînerait une transformation en<br />
blende.<br />
CR3 Etude structurale de la galène<br />
1. Voir la figure 1.<br />
2. Un atome de plomb pour un atome de soufre donc PbS.<br />
3. Chaque ion<br />
Pb 2+<br />
2<br />
S − ou<br />
2<br />
Pb + est entouré de six plus proches voisins, la coordinence est donc 6/6.<br />
En appelant respectivement r + et r − les rayons ioniques de<br />
2<br />
Pb + et<br />
+ −<br />
• Le contact entre les ions de signes opposés impose a = 2 ( r + r )<br />
• Les ions<br />
Figure 1<br />
S 2-<br />
2−<br />
2<br />
S − (figure 2) :<br />
S ne doivent pas être au contact et donc à la limite 4r ≤ a 2 .<br />
+<br />
r<br />
On en déduit : ≥ 2 −1<br />
= 0,<br />
414<br />
r −<br />
Pour la coordinence supérieure 8/8, structure cubique centrée (figure 3 et 4) :<br />
+ −<br />
• Le contact entre les ions de signes opposés impose a = 2(<br />
r + r )<br />
−<br />
Pb 2+<br />
S 2-<br />
Figure 2<br />
3 ,<br />
a
Les Eucalyptus, Nice <strong>Révisions</strong> de chimie<br />
PT* Cristallographie<br />
4.<br />
• Les ions<br />
2−<br />
S ne doivent pas être au contact et donc à la limite 2 r ≤ a .<br />
r<br />
On en déduit : ≥ 3 −1<br />
= 0,<br />
732<br />
r −<br />
+<br />
r<br />
Donc une structure de type cubique F impose : 0, 414 ≤ ≤ 0,<br />
732<br />
r −<br />
r<br />
Ce qui est bien le cas ici puisque = 0,<br />
652 .<br />
r −<br />
+ − a<br />
⎫ +<br />
r + r = = 0,297 nm⎪<br />
⎧ ⎪r<br />
= 0,117 nm<br />
2<br />
⎬ ⇒ ⎨ −<br />
+ −<br />
r r = 0,652 ⎪ ⎪⎩ r = 0,180 nm<br />
⎭<br />
1 1<br />
5. Une maille contient en propre : 8× + 6×<br />
= 4 ions<br />
8 2<br />
+<br />
+<br />
−<br />
a<br />
anion<br />
2<br />
Figure 4<br />
a<br />
cation<br />
2+<br />
1<br />
2−<br />
Pb et 12× + 1 = 4 ions S .<br />
4<br />
( )<br />
4 207,19 + 32,06 10<br />
D’où une masse volumique pour la galène : ρ =<br />
23 −9<br />
6,02.10 0,594.10<br />
CR4 Sites de structures CFC<br />
1. = 0,<br />
128 nm<br />
r Fe<br />
2. = 0,<br />
1374 nm ; = 0,<br />
3886 nm<br />
r Pd<br />
Figure 3<br />
a Pd<br />
−3<br />
( )<br />
3<br />
ρ = 7,59.10 kg. m<br />
3 −3<br />
3. 4 atomes de Palladium et 8 sites tétraédriques appartiennent en propre à la maille donc 1 site sur quatre<br />
occupé par H dans Pd2H.<br />
4. La petite taille des atomes d’hydrogène explique la très faible augmentation du paramètre de maille lors<br />
de l’insertion de ces atomes dans les sites tétraédriques.<br />
5. 4 sites octaédriques appartiennent en propre à la maille donc la proportion est 4Fe pour 4 12 = 1 3 C d’où<br />
la formule de l’austénite Fe12 C .<br />
6. ( 2 −1)<br />
r = 0,<br />
053 nm<br />
rocta ≤ Fe . Le rayon de l’atome de carbone est nettement supérieur donc l’insertion ne<br />
peut se faire qu’en petite proportion.
Les Eucalyptus, Nice <strong>Révisions</strong> de chimie<br />
PT* Cristallographie<br />
CR5 Cristaux d'oxyde de Nickel<br />
r ≤ 2 − 1 r = 0,0592 nm<br />
1. ( )<br />
2.<br />
2+ 2−<br />
Ni O<br />
ρ = 7,<br />
50 g.<br />
cm<br />
3. 2+ = 0,125<br />
Ni<br />
−3<br />
r nm<br />
CR6 Le tungstène<br />
1.<br />
M =<br />
0,13× 180 + 26,3 × 182 + 14,3 × 183 + 30,67 × 184 + 28,6 × 186<br />
100<br />
M 183,9 g. mol −<br />
=<br />
2. Pour déterminer la configuration électronique d’un élément on applique (voir cours de première année) :<br />
• le principe d’exclusion de Pauli,<br />
• la règle de Klechkowski,<br />
• la règle de Hund.<br />
3.<br />
Pour Z = 74 la configuration électronique qui découle des règles précédentes est :<br />
1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 4d 10 5p 6 6s 2 4f 14 5d 4<br />
Mais une sous couche 5d à moitié remplie devenant plus stable, la configuration est en fait :<br />
1s 2 …...6s 1 4f 14 5d 5<br />
1<br />
4. Une maille cubique centrée contient deux atomes : un au centre et 8× = 1 aux sommets. La coordinence<br />
8<br />
des atomes est de huit.<br />
5. La compacité C est le rapport entre le volume occupé par les atomes et le volume total (nombre sans<br />
dimension compris entre 0 et 1). Le nombre d’atomes appartenant en propre à la maille est de deux et les<br />
atomes sont tangents, sur la diagonale du cube donc 4r = a 3 :<br />
4 3<br />
2×<br />
π r<br />
3 π 3<br />
C = = = 0,68<br />
3<br />
a 8<br />
−3<br />
2 × M atome 2× 183,9 × 10<br />
Masse volumique : ρ = =<br />
−<br />
V 316.10 × 6,02.10<br />
maille<br />
( )<br />
12 23<br />
ρ =<br />
19,36.10 kg. m<br />
3 −3<br />
1