Le frottis conventionnel est source de faux négatifs etson usage exclusif comme outil de ces programmes adémontré ses limites.Dès lors, des technologies nouvelles ont été proposéespour l’amélioration de l’efficacité de ce dépistage. Elles sontappliquées de routine depuis 1997 à l’<strong>Institut</strong> J. <strong>Bordet</strong>.Ce sont : -la cytologie en milieu liquide ;-la détection du virus du papillome humain(HPV).LA CYTOLOGIE EN MILIEU LIQUIDELe frottis traditionnel était un étalement sur une lame(plaquette en verre), des cellules recueillies dans leurmucus par la rotation d’une spatule en bois sur le relief ducol utérin.La préservation des cellules après étalement se faisaitpar un spray fixateur.L’usage d’une brosse en plastique, dessinée de façon àépouser la forme du col, a rangé la spatule dans les objets dupassé.Les cellules ne s’incrustent pas dans la brosse etl’étalement se fait comme avec un pinceau.Néanmoins, il est facile d’imaginer qu’une partiesubstantielle du prélèvement reste sur la brosse et est jetéeavec elle.La performance des nouvelles techniques en milieuliquide repose sur 5 modifications majeures :• l’étalement par frottis et la fixation sont abandonnés ;• la brosse directement plongée dans un flacon deliquide conservateur est adressée au laboratoire ;• le liquide contenant les cellules en suspension estfiltré au travers d’un gradient de densité qui leconcentre et l’enrichit proportionnellement encellules analysables au laboratoire ;• le culot cellulaire est étalé de façon homogène encouche mince sur la lame ;• la technique d’étalement et de coloration eststandardisée par un automate.Les avantages attendus sont :• la récupération immédiate de la brosse et de soncontenu dans le liquide fixateur assure le transfertd’un maximum de cellules sur la lame ;• l’étalement disperse les cellules de façon homogène,offrant une meilleure visibilité à l’observateur aumicroscope ;• la standardisation depuis le prélèvement jusqu’à lalame colorée à analyser, assure une qualité constanted’échantillonnage.Grâce à cette technique, le nombre de frottisinsatisfaisants, c’est-à-dire trop épais, hémorragiques outrop inflammatoires a été significativement diminué.La qualité accrue de la préparation a aussi permis dediminuer le pourcentage de cas aux atypies de significationindéterminée, réduisant d’autant les rappels de patientes etles frottis de contrôle dans des délais rapprochés.L’accroissement de la sensibilité et de la spécificitépermet donc de donner des résultats plus précis auxfemmes, orientant plus rapidement les unes vers lacolposcopie et la biopsie de contrôle, tout en évitant auxautres des contrôles inutiles.Par ailleurs, les cas ambigus, grâce au milieu liquide,peuvent faire l’objet d’une analyse simultanée enbiologie moléculaire pour rechercher la présence depapillomavirus.LA DETECTION DU VIRUS HPVNos connaissances sur l’étiopathogénie du cancer ducol et les progrès rapides de nos connaissances de biologiemoléculaire ont permis de réaliser qu’il n’y a pas dedéveloppement du cancer du col et de ses phasesprécoces, sans infection persistante par le virus HPV.L’identification par la biologie moléculaire de séquencesd’ADN oncogène viral à l’aide de sondes appropriées,permet donc d’isoler les patientes à risque de cellesporteuses de sous-types non oncogènes de ce virus, ouencore exemptes de toute infection des cellules du col.Le reliquat de suspension cellulaire est utilisé pourdétecter la présence de séquences d’ADN, des virus HPVdits «à haut risque» dans le culot résiduel.Les cas cytologiquement douteux, dont le test restenégatif, ont une valeur prédictive négative affleurant les100%, qui permet de reclasser comme normaux ces frottisatypiques et d’éviter l’angoisse d’examens superflus à despersonnes pouvant rentrer dans un cycle de dépistageclassiqueEN CONCLUSIONLa cytologie reste la pierre angulaire du dépistage ducancer du col de l’utérus.Notre but a été d’en optimiser la performance, parl’adoption d’une technique de prélèvement validée par laFood & Drug Administration américaine.Le prélèvement en milieu liquide permet d’obtenir deslames de qualité supérieure au frottis conventionnel. Lalecture plus sûre assure une réduction de la zone de gris dufrottis jugé suspect et affine la perception exacte desanomalies précancéreuses.L’adjonction du test HPV en biologie moléculaire dansles cas douteux et d’une double lecture des frottis intégrantle résultat du test HPV nous permet d’obtenir une parfaitecorrélation entre le diagnostic cytologique et le résultat dela biologie moléculaire. Ce double contrôle a une valeur detest d’assurance-qualité.La cytologie en milieu liquide a permis de diminuersignificativement le pourcentage de frottis inadéquats; letypage HPV des cas ambigus, pratiqué simultanément àl’examen cytologique ajoute un tri essentiel entre patientesà risque élevé de développer un cancer, et celles dontl’absence de détection du virus autorise à adopter uneattitude plus conservatrice.La sensibilité d’un seul test de Papanicolaou estextrêmement variable, allant de 30 à 85% ; il est évidentque cette sensibilité est tributaire du volume d’activité dulaboratoire et il est admis que l’expérience soutenue, doncun nombre annuel élevé de cas, est le garant d’un dépistagede qualité.Sous une apparence simpliste, le dépistage du cancer ducol nécessite une qualité irréprochable de prélèvement, depréparation, de lecture et d’interprétation par une équipemotivée bénéficiant d’une <strong>format</strong>ion continue et d’uncontrôle de qualité constant.8 BN 73 • 2ème trimestre 2005
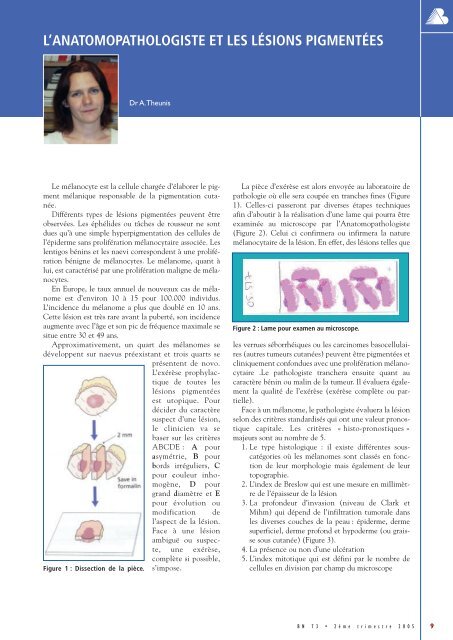
L’ANATOMOPATHOLOGISTE ET LES LÉSIONS PIGMENTÉESDr A.TheunisLe mélanocyte est la cellule chargée d’élaborer le pigmentmélanique responsable de la pigmentation cutanée.Différents types de lésions pigmentées peuvent êtreobservées. Les éphélides ou tâches de rousseur ne sontdues qu’à une simple hyperpigmentation des cellules del’épiderme sans prolifération mélanocytaire associée. Leslentigos bénins et les naevi correspondent à une proliférationbénigne de mélanocytes. Le mélanome, quant àlui, est caractérisé par une prolifération maligne de mélanocytes.En Europe, le taux annuel de nouveaux cas de mélanomeest d’environ 10 à 15 pour 100.000 individus.L’incidence du mélanome a plus que doublé en 10 ans.Cette lésion est très rare avant la puberté, son incidenceaugmente avec l’âge et son pic de fréquence maximale sesitue entre 30 et 49 ans.Approximativement, un quart des mélanomes sedéveloppent sur naevus préexistant et trois quarts seprésentent de novo.L’exérèse prophylactiquede toutes leslésions pigmentéesest utopique. Pourdécider du caractèresuspect d’une lésion,le clinicien va sebaser sur les critèresABCDE : A pourasymétrie, B pourbords irréguliers, Cpour couleur inhomogène,D pourgrand diamètre et Epour évolution oumodification del’aspect de la lésion.Face à une lésionambiguë ou suspecte,une exérèse,complète si possible,Figure 1: Dissection de la pièce. s’impose.La pièce d’exérèse est alors envoyée au laboratoire depathologie où elle sera coupée en tranches fines (Figure1). Celles-ci passeront par diverses étapes techniquesafin d’aboutir à la réalisation d’une lame qui pourra êtreexaminée au microscope par l’Anatomopathologiste(Figure 2). Celui ci confirmera ou infirmera la naturemélanocytaire de la lésion. En effet, des lésions telles queFigure 2:Lame pour examen au microscope.les verrues séborrhéiques ou les carcinomes basocellulaires(autres tumeurs cutanées) peuvent être pigmentées etcliniquement confondues avec une prolifération mélanocytaire.Le pathologiste tranchera ensuite quant aucaractère bénin ou malin de la tumeur. Il évaluera égalementla qualité de l’exérèse (exérèse complète ou partielle).Face à un mélanome, le pathologiste évaluera la lésionselon des critères standardisés qui ont une valeur pronostiquecapitale. Les critères « histo-pronostiques »majeurs sont au nombre de 5.1. Le type histologique : il existe différentes souscatégoriesoù les mélanomes sont classés en fonctionde leur morphologie mais également de leurtopographie.2. L’index de Breslow qui est une mesure en millimètrede l’épaisseur de la lésion3. La profondeur d’invasion (niveau de Clark etMihm) qui dépend de l’infiltration tumorale dansles diverses couches de la peau : épiderme, dermesuperficiel, derme profond et hypoderme (ou graissesous cutanée) (Figure 3).4. La présence ou non d’une ulcération5. L’index mitotique qui est défini par le nombre decellules en division par champ du microscopeBN 73 • 2ème trimestre 2005 9