Tópico 5 - Editora Saraiva
Tópico 5 - Editora Saraiva
Tópico 5 - Editora Saraiva
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
Determine:<br />
a) o trabalho, em joules, realizado pelo gás no ciclo ABCDA;<br />
b) o ponto do ciclo em que a energia interna do sistema é máxima e o<br />
ponto onde é mínima.<br />
Resolução:<br />
a) τ = ciclo N [área interna]<br />
τ = (6 – 2) · (3 – 1) (J)<br />
ABCDA<br />
τ ABCDA = 8 J<br />
b) A energia interna é máxima no ponto de temperatura máxima. Nesse<br />
ponto, o produto pressão × volume é máximo.<br />
U máx → C<br />
Da mesma forma, a energia interna é mínima onde o produto p V é<br />
mímino:<br />
U mín → A<br />
Respostas: a) 8 J; b) C; A<br />
49 Um recipiente de volume ajustável contém n mols de moléculas<br />
de um gás ideal. Inicialmente, o gás está no estado A, ocupando um<br />
volume V à pressão p. Em seguida, o gás é submetido à transformação<br />
indicada na f igura.<br />
p<br />
2p<br />
p<br />
0<br />
A<br />
B<br />
Calcule o calor absorvido pelo gás na transformação cíclica ABCA.<br />
V<br />
Resolução:<br />
Numa transformação cíclica, a variação de energia interna ΔU é nula<br />
(ΔU = 0).<br />
Usando-se a 1 a Lei da Termodinâmica:<br />
Q = τ + ΔU<br />
Q = τ<br />
Assim:<br />
Q = τ = [área do triângulo ABC]<br />
(2V – V) · (2p – p)<br />
Q =<br />
2<br />
p V<br />
Q =<br />
2<br />
Resposta:<br />
p V<br />
2<br />
C<br />
2V<br />
V<br />
<strong>Tópico</strong> 5 – Termodinâmica<br />
99<br />
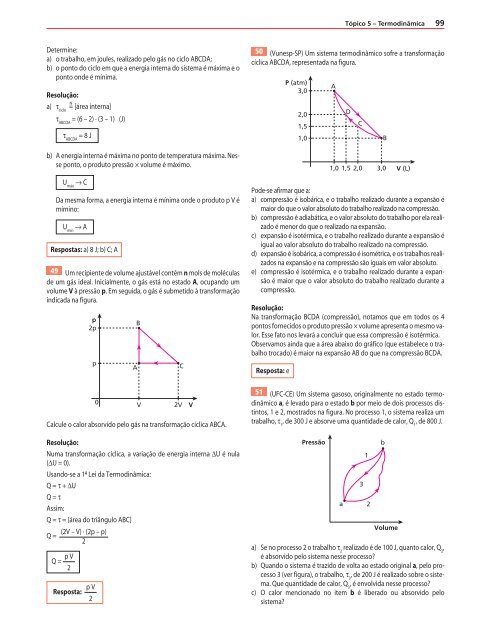
50 (Vunesp-SP) Um sistema termodinâmico sofre a transformação<br />
cíclica ABCDA, representada na f igura.<br />
P (atm)<br />
3,0<br />
2,0<br />
1,5<br />
1,0<br />
A<br />
D<br />
C<br />
1,0 1,5 2,0 3,0 V (L)<br />
Pode-se af irmar que a:<br />
a) compressão é isobárica, e o trabalho realizado durante a expansão é<br />
maior do que o valor absoluto do trabalho realizado na compressão.<br />
b) compressão é adiabática, e o valor absoluto do trabalho por ela realizado<br />
é menor do que o realizado na expansão.<br />
c) expansão é isotérmica, e o trabalho realizado durante a expansão é<br />
igual ao valor absoluto do trabalho realizado na compressão.<br />
d) expansão é isobárica, a compressão é isométrica, e os trabalhos realizados<br />
na expansão e na compressão são iguais em valor absoluto.<br />
e) compressão é isotérmica, e o trabalho realizado durante a expansão<br />
é maior que o valor absoluto do trabalho realizado durante a<br />
compressão.<br />
Resolução:<br />
Na transformação BCDA (compressão), notamos que em todos os 4<br />
pontos fornecidos o produto pressão × volume apresenta o mesmo valor.<br />
Esse fato nos levará a concluir que essa compressão é isotérmica.<br />
Observamos ainda que a área abaixo do gráf ico (que estabelece o trabalho<br />
trocado) é maior na expansão AB do que na compressão BCDA.<br />
Resposta: e<br />
51 (UFC-CE) Um sistema gasoso, originalmente no estado termodinâmico<br />
a, é levado para o estado b por meio de dois processos distintos,<br />
1 e 2, mostrados na f igura. No processo 1, o sistema realiza um<br />
trabalho, τ 1 , de 300 J e absorve uma quantidade de calor, Q 1 , de 800 J.<br />
Pressão<br />
a<br />
3<br />
1<br />
2<br />
b<br />
B<br />
Volume<br />
a) Se no processo 2 o trabalho τ 2 realizado é de 100 J, quanto calor, Q 2 ,<br />
é absorvido pelo sistema nesse processo?<br />
b) Quando o sistema é trazido de volta ao estado original a, pelo processo<br />
3 (ver f igura), o trabalho, τ 3 , de 200 J é realizado sobre o sistema.<br />
Que quantidade de calor, Q 3 , é envolvida nesse processo?<br />
c) O calor mencionado no item b é liberado ou absorvido pelo<br />
sistema?